BAB 2
TINJAUAN PUSTAKA
2.1 Tanaman Mangga (Mangifera indica L.)
Mangga yang berkembang di Indonesia diperkirakan berasal dari India, yang
dipercaya pemeliharaannya telah ada seiring peradaban India. Sejarah pun mencatat
bahwa mangga pertama kali ditemukan oleh Alexander Agung di lembah Indus, India.
Kata mangga sendiri berasal dari bahasa Tamil, yaitu mangas atau man-kay.
Dalam bahasa botani, mangga disebut Mangifera indica L. yang berarti tanaman
mangga berasal dari India.
Dari India, sekitar abad ke-4 SM, tanaman mangga menyebar ke berbagai
negara, yakni melalui pedagang India yang berkelana ke timur sampai ke
Semenanjung Malaysia. Pada tahun 1400 dan 1450, mangga mulai ditanam di
kepulauan Sulu dan Mindanau, Filipina, di pulau Lizon sekitar tahun 1600, dan di
kepulauan Maluku pada tahun 1665 (Pracaya, 2011).
2.1.1 Taksonomi dan Morfologi Tanaman Mangga
Dalam tatanama sistematika (taksonomi) tumbuhan, tanaman mangga diklasifikasikan
sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Sapindales
Famili : Anacardiaceae
Genus : Mangifera
Tanaman mangga tumbuh dalam bentuk pohon berbatang tegak, bercabang
banyak, serta rindang dan hijau sepanjang tahun. Tinggi tanaman dewasanya bisa
mencapai 10-40 m dengan umur bisa mencapai lebih dari 100 tahun. Morfologi
tanaman mangga terdiri atas akar, batang, daun, dan bunga. Bunga menghasilkan buah
dan biji yang secara generatif dapat tumbuh menjadi tanaman baru (Pracaya, 2011).
Mangga rata-rata berbunga satu kali sehingga panen buah dapat dilakukan
beberapa kali dalam satu periode karena buah tidak masak bersamaan. Mangga
cangkokan mulai berbuah pada umur 4 tahun sedangkan mangga okulasi pada umur
5-6 tahun. Buah panen pertama hanya mencapai 10-15 buah, pada tahun ke-10 jumlah
buah dapat mencapai 300-500 buah/pohon, pada umur 15 tahun mencapai 1000
buah/pohon, dan produksi maksimum tercapai pada umur 20 tahun dengan potensi
produksi mencapai 2000 buah/pohon/tahun (Tafajani, 2011).
Buah mangga memiliki keanekaragaman bentuk antara lain bulat,
bulat-pendek dengan ujung pipih, dan bulat-panjang agak pipih. Susunan tubuh buah terdiri
dari beberapa lapisan, yaitu sebagai berikut :
a. Kulit buah
Buah mangga yang muda memiliki kulit berwarna hijau, namun menjelang matang
berubah warna menurut jenis dan varietasnya.
b. Daging buah
Buah mangga yang masih muda pada umumnya memiliki daging buah yang
berwarna kuning keputih-putihan. Menjelang tua daging buah berubah menjadi
kekuning-kuningan sampai kejingga-jinggan. Rasa daging buah mangga bervariasi,
yaitu asam sampai manis dengan aroma yang khas pada setiap varietas mangga.
c. Biji
Biji mangga berkeping dua dan memiliki sifat poliembrional, karena dari satu biji
dapat tumbuh lebih dari satu bakal tanaman (Rukmana, 1997).
2.1.2 Komposisi Kimia Buah Mangga
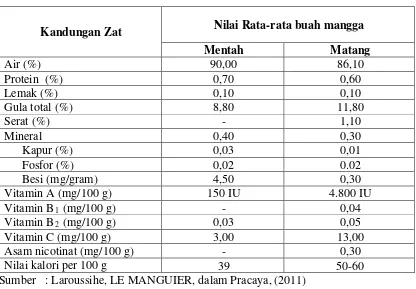
Tabel 2.1 Komposisi Kimia dan Nilai Gizi Buah Mangga
Kandungan Zat Nilai Rata-rata buah mangga
Mentah Matang
Sumber : Laroussihe, LE MANGUIER, dalam Pracaya, (2011)
Komponen daging buah mangga yang paling banyak adalah air dan
karbohidrat. Selain itu juga mengandung protein, lemak, macam-macam asam,
vitamin, mineral, tanin, zat warna, dan zat yang mudah menguap sehingga
menciptakan aroma harum khas buah mangga.
Karbohidrat daging buah mangga terdiri dari gula sederhana, tepung, dan
selulosa. Gula sederhananya berupa sukrosa, glukosa, dan fruktosa yang memberikan
rasa manis dan bermanfaat bagi pemulihan tenaga pada tubuh manusia. Selain gula,
rasa dan karakteristik buah mangga juga dipengaruhi oleh tanin dan campuran asam.
Tanin pada buah mangga menyebabkan rasa kelat dan terkadang pahit. Tanin juga
menyebabkan buah mangga menjadi hitam setelah diiris. Sementara itu, rasa asam
pada buah mangga disebabkan oleh adanya asam sitrat (0,13-0,17%) dan vitamin C
(Pracaya, 2011).
2.1.3 Jenis dan Varietas Tanaman Mangga
Pengembangan varietas mangga dapat dilakukan secara generatif maupun vegetatif.
Masing-masing varietas mangga dapat dibedakan berdasarkan ukuran, warna daging,
pohon, ukuran, dan bentuk daun. Di Indonesia ada beberapa jenis dan varietas mangga
komersial yang sudah terkenal bagus mutunya, antara lain :
a. Mangga Golek
Dalam bahasa Jawa, golek berarti ”mencari”. Berdasarkan kata itu pulalah penamaan
jenis mangga ini karena setelah menikmati rasanya orang akan mencari lagi buah
mangga yang baru saja dimakan. Daging buah tebal, lunak dengan warna kuning tua.
Daging buahnya boleh dikatakan tidak berserat, tidak berair (kalau diiris tidak banyak
mengeluarkan air). Aromanya cukup harum dengan rasa yang manis.
b. Mangga Arumanis
Disebut mangga arumanis karena rasanya manis dan aromanya harum (arum). Daging
buah tebal, lunak berwarna kuning, dan tidak berserat (serat sedikit). Aroma harum,
tidak begitu berair, dengan rasa yang manis, tapi bagian ujung kadang-kadang masih
ada rasa asam.
c. Mangga Manalagi
Disebut manalagi karena sekali makan orang akan mencarinya lagi. Rasa mangga
manalagi seperti perpaduan rasa antara golek dan arumanis. Kemungkinan pohon
mangga manalagi merupakan hasil persilangan alami antara golek dengan arumanis.
Buah ini sering dimakan dalam keadaan masih keras, tetapi daging buah sudah
kelihatan kuning.
d. Mangga Madu
Mangga ini disebut madu karena rasanya manis seperti madu lebah. Daging buah yang
sudah masak berwarna kuning. Bagian dalam kuningnya makin ke dalam makin tua
seperti warna madu. Serat daging buah sedikit. Kadar air buah sedang dengan rasanya
yang manis seperti madu dan aromanya harum (Pracaya, 2011).
e. Mangga Udang
Mangga ini berasal dari Desa Hutanagonang, Kecamatan Muara, Kabupaten Tapanuli
Utara. Panjang rata-rata mangga ini hanya sekitar 6 cm. Dikenal dua jenis mangga
udang, yaitu yang berukuran kecil dan berukuran besar. Buahnya berbentuk lonjong.
Kulitnya tipis dan berwarna hijau muda pada waktu muda, lalu berubah menjadi
kuning keemasan setelah tua. Daging buahnya berwarna kuning, lunak berair, rasanya
f. Kuini
Dalam taksonomi tumbuhan, kuini merupakan tanaman mangga dengan spesies
Mangifera odorata Griffith yang masih berkerabat dekat dengan bacang.
Gambar 2.1 Perbandingan Buah Kuini dan Bacang
Warna kulit buah muda hijau dan setelah masak hijau kekuningan pada
pangkalnya, dengan permukaan kulit licin. Warna daging buah kuning-orange.
Tekstur daging buah agak berserat. Bagi orang yang tidak tahan akan terasa gatal
apabila makan buah kuini ini. Rasa daging buah manis, kadang ada yang agak masam.
Bentuk buah lonjong dengan nisbah P/L sebesar 1,21-1,52. Ukuran buah sedang,
bobot buah sekitar 162-470 g. Bagian buah yang dapat dimakan sekitar 44,62-64,47%
(Antarlina, 2003).
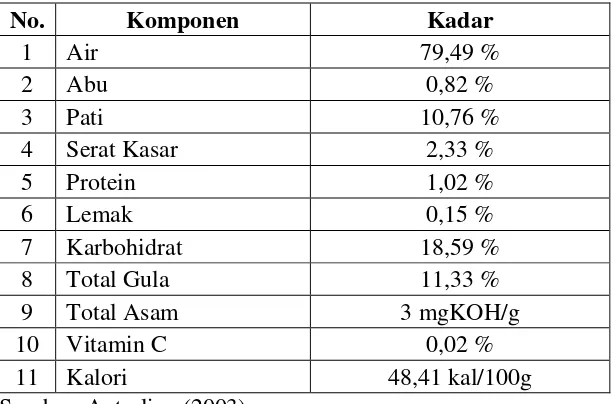
Tabel 2.2 Karakteristik Kimia Buah Kuini
No. Komponen Kadar
1 Air 79,49 %
2 Abu 0,82 %
3 Pati 10,76 %
4 Serat Kasar 2,33 %
5 Protein 1,02 %
6 Lemak 0,15 %
7 Karbohidrat 18,59 %
8 Total Gula 11,33 %
9 Total Asam 3 mgKOH/g
10 Vitamin C 0,02 %
11 Kalori 48,41 kal/100g
Sumber: Antarlina (2003)
2.2 Karbohidrat
Istilah karbohidrat timbul karena rumus molekul senyawa ini dapat dinyatakan sebagai
hidrat dari karbon. Definisi karbohidrat ialah polihidroksialdehida, polihidroksiketon,
atau zat yang memberikan senyawa seperti ini jika dihidrolisis dengan asam berair,
dimana gugus hidroksil dan gugus karbonil merupakan gugus fungsi utama dalam
karbohidrat.
Karbohidrat biasanya digolongkan menurut strukturnya sebagai monosakarida,
oligosakarida, atau polisakarida. Istilah sakarida berasal dari kata Latin (sakarum,
gula) dan merujuk pada rasa manis dari beberapa karbohidrat sederhana (Hart, 2003).
2.2.1 Monosakarida
Monosakarida ialah karbohidrat yang tidak dapat dihidrolisis menjadi senyawa yang
lebih sederhana lagi. Monosakarida digolongkan berdasarkan jumlah atom karbon
yang ada (triosa, tetrosa, pentosa, heksosa, dan seterusnya) dan berdasarkan apakah
gugus karbonil yang ada sebagai aldehida atau sebagai keton (Hart, 2003).
Glukosa, monosakarida yang paling umum, kadang-kadang disebut gula darah,
gula anggur, atau dekstrosa. Binatang menyusui dapat mengubah sukrosa, laktosa,
maltosa, dan pati menjadi glukosa, yang kemudian dapat digunakan sebagai energi
oleh organisme itu, atau disimpan sebagai glikogen (Fessenden, 1986).
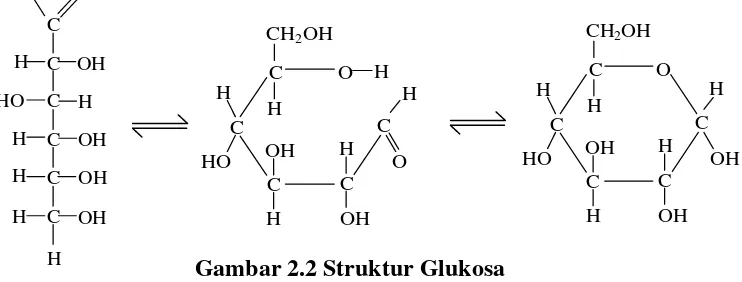
Gambar 2.2 Struktur Glukosa
Glukosa merupakan heksosa yang paling penting secara nutrisi dan paling
melimpah di alam. Glukosa terdapat dalam madu dan buah seperti anggur, ara, dan
kurma. Anggur yang matang, sebagai contoh, terdiri dari 20-30% glukosa. Glukosa
juga dikenal sebagai gula darah karena gula diangkut oleh darah menuju jaringan
tubuh untuk memenuhi kebutuhan energi. Gula lainnya yang diserap dalam tubuh
harus dimetabolisme oleh liver menjadi glukosa. Glukosa pada umumnya digunakan
sebagai pemanis dalam manisan dan makanan lainnya, termasuk beberapa makanan
bayi (Seager, 2008).
2.2.2 Oligosakarida
Oligosakarida adalah polimer dengan derajat polimerisasi 2 sampai 10 yang biasanya
bersifat larut dalam air. Oligosakarida yang terdiri dari dua monosakarida disebut
disakarida, dan bila tiga molekul disebut triosa (Winarno, 1995).
Oligosakarida yang paling sering dijumpai ialah disakarida. Dalam disakarida,
dua monosakarida ditautkan oleh ikatan glikosidik antara karbon anomerik dari satu
unit monosakarida dan gugus hidroksil dari unit lainnya. Beberapa contoh disakarida :
a. Maltosa
Maltosa ialah disakarida yang diperoleh lewat hidrolisis parsial dari pati. Hidrolisis
lanjutan dari maltosa hanya menghasilkan D-glukosa. Jadi, maltosa terdiri atas dua
unit glukosa yang bertautan.
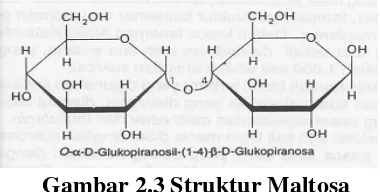
Gambar 2.3 Struktur Maltosa
Karbon anomerik di unit glukosa sebelah kanan pada maltosa ialah suatu
hemiasetal. Secara alami, bila maltosa berada dalam larutan, fungsi hemiasetal ini
akan berkesetimbangan dengan bentuk aldehida rantai terbuka. Dengan begitu,
maltosa menghasilkan uji Tollens positif dan reaksi lain yang serupa seperti pada
karbon anomerik glukosa.
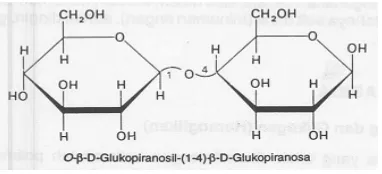
b. Selobiosa
Selobiosa ialah disakarida yang diperoleh dari hidrolisis parsial selulosa. Hidrolisis
selobiosa lebih lanjut hanya menghasilkan D-glukosa. Jadi, selobiosa merupakan
isomer maltosa. Pada kenyataannya, selobiosa berbeda dari maltosa hanya karena
struktur lainnya identik termasuk tautan antara C-1 dari unit di kiri dan gugus
hidroksil pada C-4 di unit kanan.
Gambar 2.4 Struktur Selobiosa c. Sukrosa
Disakarida komersial yang paling penting ialah sukrosa, atau gula pasir. Sukrosa
terjadi dalam semua tumbuhan fotosintetik, yang berfungsi sebagai sumber energi.
Sukrosa diperoleh secara komersial dari batang tebu dan bit gula, yang kadarnya
14-20% dari cairan tumbuhan tersebut.
Hidrolisis sukrosa memberikan D-glukosa dan ketosa D-fruktosa dengan
jumlah mol yang ekuivalen. Sukrosa tidak mempunyai gugus aldehida bebas yang
berpotensi sehingga tidak dapat mereduksi reagen Tollens, Fehling, atau Benedict.
Oleh karena itu sukrosa disebut sebagai gula non-pereduksi (Hart, 2003).
Gambar 2.5 Struktur Sukrosa 2.2.3 Polisakarida
Polisakarida dalam bahan makanan berfungsi sebagai penguat tekstur (selulosa,
hemiselulosa, pektin, lignin) dan sebagai sumber energi (pati, dekstrin, glikogen,
fruktan). Polisakarida merupakan polimer molekul-molekul monosakarida yang dapat
berantai lurus atau bercabang dan dapat dihidrolisis. Hasil hidrolisis sebagian akan
menghasilkan oligosakarida dan dapat dipakai untuk menentukan struktur molekul
polisakarida (Winarno, 1995).
Sebagai contoh, pati ialah karbohidrat penyimpan energi bagi tumbuhan yang
tersusun dari unit-unit glukosa yang bergabung lewat ikatan 1,4-α-glikosidik,
1,6-α-glikosidik. Hidrolisis parsial dari pati menghasilkan maltosa dan hidrolisis
sempurna hanya menghasilkan D-glukosa.
2.2.3.1 Selulosa
Selain pati, polisakarida yang banyak ditemukan di alam adalah selulosa. Selulosa
merupakan polimer tak bercabang dari sejumlah glukosa yang bergabung lewat ikatan
1,4-β-glikosidik. Pemeriksaan selulosa dengan sinar X menunjukkan bahwa selulosa
terdiri atas rantai linear dari unit selobiosa. Walaupun manusia dan beberapa hewan
dapat mencerna pati, tidak sama halnya dengan selulosa. Hal ini disebabkan oleh
perbedaan ikatan glikosidiknya (Hart, 2003).
Berat molekul selulosa berkisar antara 100.000 hingga 1.000.000. Kapas
merupakan salah satu sumber yang kaya akan selulosa, mengandung lebih dari 90%
selulosa per satuan berat. Kebanyakan tanaman lain juga mengandung persentase
selulosa yang tinggi secara relatif, pada umumnya berkisar antara 10-15%. Selulosa
sangat penting dalam industri kimia. Sebagai contoh, digunakan dalam industri pabrik
barang-barang kertas, cat, bahan peledak, dan rayon. Selulosa merupakan satu dari
senyawa yang paling berlimpah di bumi (Wingrove, 1939).
Gambar 2.6 Struktur Selulosa 2.2.3.2 Sifat-Sifat Selulosa
Selulosa tidak memiliki rasa, tidak berbau, tidak larut dalam
organik. Selulosa dapat dipecah menjadi unit-unit kimia glukosa dengan
mereaksikannya dengan asam pekat pada suhu tinggi.
Dibandingkan dengan pati, selulosa jauh lebih bersifat kristal. Dimana pati
mengalami transisi kristal menjadi amorf ketika dipanaskan dalam air pada suhu
mencapai 60-70ºC. Sedangkan selulosa membutuhkan suhu 320ºC dan tekanan 25
Kebanyakan sifat selulosa tergantung pada panjang rantai atau derajat
polimerisasi unit glukosa. Selulosa dari pulp kayu memiliki panjang rantai khas antara
300-1700 unit. Kapas dan serat tanaman lainnya sama seperti selulosa bakteri
memiliki panjang rantai berkisar antara 800-10.000 unit (Klemm, 2005).
Selulosa yang diturunkan dari tanaman biasanya ditemukan dalam suatu
campuran dengan hemiselulosa, lignin, pektin, dan zat-zat lain. Sementara selulosa
mikroba cukup murni, memiliki kadar air cukup tinggi dan terdiri dari rantai panjang.
Selulosa larut dalam kuprietilendiamin (CED), kadmiumetilendiamin (Cadoxen),
N-metilmorfolina N-oksida, dan litium klorida atau dimetilformamida. Pelarut-pelarut ini
digunakan dalam produksi selulosa diregenerasi dari pelarutan pulp (Stenius, 2000).
2.2.3.3 Hidrolisis Selulosa
Hidrolisis selulosa lengkap dengan HCl 30%, hanya menghasilkan D-glukosa.
Disakarida yang terisolasi dari selulosa yang terhidrolisis sebagian adalah selobiosa,
yang dapat dihidrolisis lebih lanjut menjadi D-glukosa dengan suatu katalis asam atau
dengan emulsin enzim. Selulosa sendiri tidak mempunyai karbon hemiasetal-selulosa
sehingga tidak dapat mengalami mutarotasi atau dioksidasi oleh reagensia seperti
Tollens (Fessenden, 1986).
Selulosa Selobiosa Glukosa
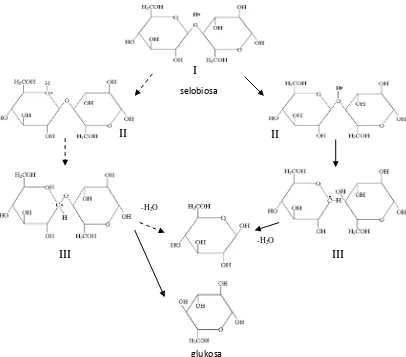
Hidrolisis dalam suasana asam, yang menghasilkan pemecahan ikatan
glikosidik berlangsung dalam tiga tahap. Tahap pertama, proton yang bertindak
sebagai katalisator asam berinteraksi cepat dengan oksigen glikosida yang
menghubungkan dua unit gula (I), membentuk asam konjugat (II). Langkah ini diikuti
dengan pemecahan yang lambat dari ikatan C-O, yang menghasilkan zat antara kation
karbonium siklik (III). Protonasi dapat juga terjadi pada oksigen cincin (II),
menghasilkan pembukaan cincin dan kation karbonium nonsiklik (III). Tidak ada
kepastian ion karbonium mana yang paling mungkin terbesar pada kation siklik.
Akhirnya kation karbonium mulai mengadisi molekul air dengan cepat, membentuk
-H2O
-H2O
I
Gambar 2.7 Mekanisme Dasar Hidrolisis Selobiosa 2.3 Sirup Glukosa
Sirup glukosa merupakan salah satu bahan pemanis makanan dan minuman yang
berbentuk cairan dan dihasilkan melalui proses hidrolisis. Pembuatan sirup glukosa
pertama kali dilakukan pada tahun 1811 oleh ilmuwan Jerman bernama Gottlieb
Sigismund Constantin Krichhoff. Bahan baku utama produksi sirup glukosa di dunia
adalah pati berupa tepung tapioka, dan ada beberapa macam bahan lainnya seperti
tepung maizena, beras, kentang, akar-akaran dan sagu. Beberapa macam proses
pembuatan sirup glukosa melalui hidrolisis pati antara lain dengan katalis asam,
enzim, dan gabungan keduanya (http://letshare17.blogspot.com).
Proses pembuatan sirup glukosa dengan hidrolisis enzim dilakukan dengan
menghidrolisis pati dengan enzim α-amilase yang berfungsi memutuskan ikatan α-1,4
secara acak di bagian dalam molekul baik amilosa maupun amilopektin. Untuk sirup
-H2O
II II
III III
glukosa yang dihasilkan melalui hidrolisis pati dengan asam, katalis asam yang biasa
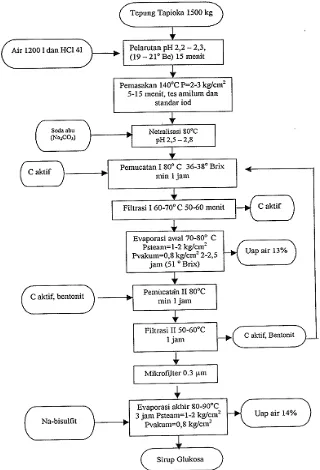
digunakan adalah asam klorida. Secara umum, pembuatan sirup glukosa dengan
hidrolisis asam (PT Indonesian Maltose Industry) adalah sebagai berikut:
Gambar 2.8 Diagram Alir Pembuatan Sirup Glukosa
Proses hidrolisis asam lebih mudah dilakukan dari pada hidrolisis enzim
karena peralatan yang digunakan pada hidrolisis asam cukup sederhana dan prosesnya
tidak rumit. Lain halnya dengan proses hidrolisis enzim yang membutuhkan peralatan
cukup banyak dengan proses yang rumit karena melibatkan kerja enzim dengan
Tabel 2.3 Standar Mutu Sirup Glukosa
No Komponen Spesifikasi
1. Air Maksimum 20%
2. Gula reduksi dihitung sebagai D-glukosa Maksimum 1%
3. Sulfur dioksida (SO2 Untuk kembang gula sekitar 400
ppm, yang lain maksimum 40 ppm.
)
4. Pemanis buatan Negatif
5. Logam berbahaya (Pb,Cu, Zn dan As) Negatif
6. Natrium Benzoat Maksimum 250 ppm
7. Warna Tidak berwarna sampai
kekuningan
8. Jumlah bakteri Maksimum 500 koloni/gram
9. Kapang Negatif
10. Khamir Negatif
Sumber : SII.0418-81
2.4 Analisis Karbohidrat 2.4.1 Analisis Kualitatif
Beberapa cara untuk mengetahui adanya karbohidrat dalam suatu bahan antara lain:
a. Uji Molisch
Karbohidrat oleh asam sulfat pekat akan dihidrolisis menjadi monosakarida dan
selanjutnya monosakarida mengalami dehidrasi oleh asam sulfat menjadi furfural atau
hidroksi metil furfural. Senyawa-senyawa ini dengan alfa naftol akan berkondensasi
membentuk senyawa kompleks yang berwarna ungu.
b. Uji Iodin
Karbohidrat golongan polisakarida akan memberikan reaksi dengan larutan iodin dan
memberikan warna spesifik bergantung pada jenis karbohidratnya. Amilosa dengan
iodin akan berwarna biru, amilopektin dengan iodin akan berwarna merah violet,
glikogen maupun dextrin dengan iodin akan berwarna merah coklat.
c. Uji Pembentukan Osason
Aldosa ataupun ketosa dengan fenilhidrasin dan dipanaskan akan membentuk
hidrason atau osason. Reaksi antar senyawaan tersebut merupakan reaksi
oksido-reduksi, atom C yang mengalami reaksi adalah atom C nomor satu dan dua dari aldosa
d. Uji Fehling
Larutan fehling yang terdiri dari campuran kupri sulfat, Na-K-tartrat dan natrium
hidroksida dengan gula reduksi dan dipanaskan akan terbentuk endapan berwarna
hijau, kuning orange atau merah bergantung dari macam gula reduksinya (Sudarmadji,
1987).
e. Uji Benedict
Pereaksi benedict berupa larutan yang mengandung kupri sulfat, natrium karbonat,
dan natrium sitrat. Glukosa dapat mereduksi ion Cu++ dari kupri sulfat menjadi ion Cu+ yang kemudian mengendap sebagai Cu2
2.4.2 Analisis Kuantitatif
O. Adanya natrium karbonat dan natrium
sitrat membuat pereaksi benedict bersifat basa lemah. Endapan yang terbentuk dapat
berwarna hijau, kuning, atau merah bata. Warna endapan ini tergantung pada
konsentrasi karbohidrat yang diperiksa (Poedjiadi, 1994).
Penentuan karbohidrat yang termasuk polisakarida maupun oligosakarida memerlukan
perlakuan pendahuluan yaitu hidrolisis terlebih dahulu sehingga diperoleh
monosakarida. Untuk keperluan ini, bahan dihidrolisis dengan asam atau enzim pada
suatu keadaan tertentu. Beberapa cara analisis kuantitatif monosakarida antara lain:
a. Metode Luff Schoorl
Pada penentuan gula secara Luff Schoorl, yang ditentukan adalah kuprioksida dalam
larutan sebelum direaksikan dengan gula reduksi (titrasi blanko) dan sesudah
direaksikan dengan sampel gula reduksi (titrasi sampel). Penentuannya dengan titrasi
menggunakan Na-tiosulfat. Selisih titrasi blanko dengan titrasi sampel ekuivalen
dengan kuprooksida yang terbentuk dan juga ekuivalen dengan jumlah gula reduksi
yang ada dalam bahan/larutan.
b. Metode Munson-Walker
Penentuan gula cara ini adalah dengan menentukan banyaknya kuprooksida yang
terbentuk dengan cara penimbangan atau dengan melarutkan kembali dengan asam
nitrat kemudian menitrasi dengan tiosulfat. Jumlah kuprooksida yang terbentuk
ekuivalen dengan banyaknya gula reduksi yang ada dalam larutan dan telah
disediakan dalam bentuk tabel Hammond, yakni hubungan antara banyaknya
c. Metode Lane-Eynon
Penentuan gula cara ini dengan menitrasi reagen Soxhlet (larutan CuSO4
d. Metode Nelson-Somogyi
, K-N-tartrat)
dengan larutan gula yang diselidiki. Banyaknya larutan sampel yang dibutuhkan untuk
menitrasi reagen Soxhlet dapat diketahui banyaknya gula yang ada dengan melihat
pada tabel Lane-Eynon (Sudarmadji, 1987).
Metode ini dapat digunakan untuk mengukur kadar gula reduksi dengan menggunakan
pereaksi tembaga arsenomolibdat. Kupri mula-mula direduksi menjadi bentuk kupro
dengan pemanasan larutan gula. Kupro yang terbentuk berupa endapan selanjutnya
dilarutkan dengan arsenomolibdat menjadi molibdenum berwarna biru yang
menunjukkan ukuran konsentrasi gula. Dengan membandingkannya terhadap larutan
standar, konsentrasi gula dalam sampel dapat ditentukan. Reaksi warna yang terbentuk
dapat menentukan konsentrasi gula dalam sampel dengan mengukur absorbansinya
(Sudarmadji, 1989).
Warna biru yang dihasilkan kemudian diukur absorbansinya dengan cara
spektrofotometri UV-Visible. Cara ini merupakan anggota teknik analisis
spektroskopik yang memakai sumber radiasi elektromagnetik ultra violet dekat
(190-380 nm) dan sinar tampak ((190-380-780 nm) dengan memakai instrumen
spektrofotometer.
Analisis dengan spektrofotometri UV-Visible selalu melibatkan pembacaan
absorban radiasi elektromagnetik oleh molekul atau radiasi elektromagnetik yang
diteruskan. Keduanya dikenal sebagai absorban (A) tanpa satuan dan transmitan
dengan satuan persen (%T) (Mulja, 1995).
Istilah log (P0
2.6 Manisan Buah
/P) disebut absorban dan diberi lambang A. Istilah lain yang
telah digunakan secara sinonim dengan absorban dan yang mungkin dijumpai dalam
literatur adalah ekstingsi (extinction), rapatan optik (optical density) dan absorbansi
(absorbancy) (Underwood, 1986).
Manisan buah adalah buah-buahan yang direndam dalam larutan gula selama beberapa
nafsu makan. Teknologi membuat manisan merupakan salah satu cara
membuat kadar gula dalam buah meningkat dan kadar airnya berkurang. Keadaan ini
akan menghambat pertumbuha
lama (Muaris, 2003).
Ada dua jenis manisan, antara lain manisan basah dan manisan kering.
Manisan basah adalah manisan yang diperoleh setelah penirisan buah dari larutan
gula. Manisan basah mempunyai kandungan air yang lebih banyak dan penampakan
yang lebih menarik karena mirip dengan buah aslinya. Manisan ini biasanya dibuat
dari buah yang keras. Sedangkan manisan kering adalah manisan yang diperoleh
setelah buah ditiriskan kemudian dijemur hingga kering. Manisan kering memiliki
daya simpan yang lebih lama, kadar air yang lebih rendah, dan kadar gula yang lebih
tinggi. Manisan kering biasanya dibuat dari buah yang teksturnya lunak (Fatah, 2004).
2.7 Uji Organoleptik
Uji organoleptik merupakan hasil reaksi fisikologik berupa tanggapan atau kesan mutu
oleh panelis. Panelis adalah sekelompok orang yang bertugas menilai sifat atau
kualitas bahan berdasarkan kesan subyektif. Panelis dapat dibagi menjadi enam
kelompok yaitu panelis pencicipan perorangan, panelis pencicipan terbatas, panelis
terlatih, panelis agak terlatih, dan panelis konsumen. Pengujian bahan pangan dengan
panelis agak terlatih sering dilakukan karena tidak memerlukan panelis yang memiliki
kepekaan tinggi. Panelis agak terlatih biasanya merupakan sekelompok mahasiswa
atau staf peneliti (15 sampai 25 orang) yang mengetahui sifat-sifat sensorik dari
contoh yang dinilai melalui penjelasan atau latihan sekedarnya (Soekarto, 1985).
Tes yang paling umum digunakan untuk mengukur tingkat kesukaan sampel
adalah skala hedonik. Istilah "hedonik" didefinisikan sebagai "yang berkaitan dengan
kesenangan". Skala mencakup serangkaian pernyataan atau titik dimana panelis
menyatakan tingkat suka atau tidak suka untuk sampel. Skala yang paling umum
adalah skala hedonik 9 poin, mulai dari "amat sangat suka (like extremely)", “sangat
suka (like very much)”, “suka (like moderately)”, “kurang suka (like slightly)”, “antara
“tidak suka (dislike moderately)”, “sangat tidak suka (dislike very much)”, dan “amat
sangat tidak suka (dislike extremely)”.
Sampel dikodekan dan disajikan dalam gaya presentasi identik. Urutan
presentasi sampel secara acak untuk masing-masing panelis dan dapat disajikan secara