VALIDASI METODE SPEKTROFOTOMETRI VISIBEL UNTUK
PENETAPAN KADAR AMPISILIN MENGGUNAKAN
PEREAKSI ASETILASETON DAN FORMALIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : ARNIE ROOSITA
NIM : 038114006
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
Penelitian untuk Skripsi
VALIDASI METODE SPEKTROFOTOMETRI VISIBEL UNTUK PENETAPAN KADAR AMPISILIN MENGGUNAKAN PEREAKSI
ASETILASETON DAN FORMALIN
Oleh : ARNIE ROOSITA
NIM : 038114006
telah disetujui oleh :
Pembimbing
iii
Pengesahan Skripsi
VALIDASI METODE SPEKTROFOTOMETRI VISIBEL UNTUK PENETAPAN KADAR AMPISILIN MENGGUNAKAN PEREAKSI
ASETILASETON DAN FORMALIN
Oleh : ARNIE ROOSITA
NIM : 038114006
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal : 31 Januari 2007
Mengetahui
Fakultas Farmasi
Universitas Sanata Dharma
Dekan
Rita Suhadi, M. Si., Apt.
Pembimbing :
Prof. Dr. Sudibyo Martono, M. S., Apt. ...
Panitia Penguji : Tanda tangan
1. Prof. Dr. Sudibyo Martono, M. S., Apt. ...
2. Drs. Sulasmono, Apt. ...
Semalam aku bermimpi sedang berjalan menyisir pantai bersama TUHAN. Di cakrawala terbentang adegan kehidupanku.
Pada setiap adegan aku melihat dua pasang jejak kaki di pasir, sepasang jejak kakiku dan sepasang lagi jejak kaki TUHAN.
Setelah adegan terakhir dari kehidupanku terhampar di hadapanku, aku menoleh ke belakang melihat jejak kaki di pasir.
Aku memperhatikan bahwa berkali-kali di sepanjang jalan hidupku, terutama pada saat-saat paling gawat dan mencekam,
hanya terdapat sepasang jejak kaki saja.
“TUHAN, di manakah Engkau?
Engkau mengatakan bila aku memutuskan untuk mengikuti Engkau, Engkau akan berjalan bersama aku sepanjang jalan hidupku. Namun aku memperhatikan
bahwa pada saat-saat paling gawat dan beban menindas hidupku, hanya terdapat sepasang jejak kaki saja,
dan aku tidak mengerti
mengapa pada waktu aku sangat membutuhkan Engkau, justru Engkau meninggalkan aku”.
“AnakKu, engkau sangat berharga di mataKu, Aku sangat mengasihi engkau
dan Aku tidak akan meninggalkan engkau.
Pada waktu engkau dalam bahaya dan dalam penderitaan, Engkau hanya melihat sepasang jejak kaki saja,
karena pada waktu itu Aku menggendongmu”.
Karya kecilku ini kupersembahkan untuk :
Hati Kudus Yesus dan Bunda Maria sebagai ungkapan syukurku,
Bapak dan ibu sebagai tanda hormat dan baktiku,
Kakakku yang kukasihi,
Diriku sendiri,
dan untuk almamaterku.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa atas
limpahan kasih dan kemurahan-Nya sehingga penelitian dan penyusunan skripsi
yang berjudul “Validasi Metode Spektrofotometri Visibel untuk Penetapan Kadar
Ampisilin Menggunakan Pereaksi Asetilaseton dan Formalin” dapat diselesaikan.
Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
(S. Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Dalam pelaksanaan penelitian hingga selesainya penyusunan skripsi ini,
penulis banyak mendapat bantuan dari berbagai pihak. Oleh karena itu, dengan
segala kerendahan hati pada kesempatan ini penulis ingin mengucapkan terima kasih
kepada :
1. Rita Suhadi, M. Si., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta.
2. Prof. Dr. Sudibyo Martono, M. S., Apt., selaku Dosen Pembimbing yang telah
meluangkan waktu untuk membimbing, mengarahkan, memberi saran dan
koreksi selama penelitian sampai penyusunan skripsi ini.
3. Drs. Sulasmono, Apt., selaku Dosen Penguji atas diskusi, saran dan koreksinya.
4. Dra. A. Nora Iska Harnita, M. Si., Apt., selaku Dosen Penguji atas diskusi, saran
dan koreksinya.
5. Bapak dan ibu yang telah dengan penuh kesabaran dan susah payah mendidik
dan membesarkan aku. Terima kasih juga atas kasih sayang, doa yang
menguatkan aku dalam setiap cobaan, pengorbanan dan dukungannya di
sepanjang hidupku hingga aku mampu menyelesaikan tugas belajar di
Universitas Sanata Dharma.
6. Pak Bambang dan Bu Kis (Laboran Laboratorium Analisis Obat dan Makanan
Fakultas Farmasi Universitas Gadjah Mada Yogyakarta) atas bantuan, arahan
dan kerjasamanya selama penelitian. Juga untuk seluruh laboran Fakultas
Farmasi UGM yang telah membantu selama penelitian.
7. Mas Ottok yang sudah membantu dalam penyediaan bahan penelitian.
8. Teman seperjuanganku, Marga dan Eta, untuk kerjasama dan kebersamaan
dalam kegagalan dan keberhasilan kita. Gagal itu biasa. Berhasil, itu baru luar
biasa.
9. Mas Fahrul yang mau meluangkan waktu untuk berdiskusi.
10. Mas Anang dan Mbak Wiek yang sudah memberi dorongan semangat, mau
mendengar keluh kesahku, menjadi teman ngobrol sepanjang hari. Terima kasih
juga sudah banyak membantu dalam penyusunan naskah skripsi ini. Thanka lot!
Tanpa kalian aku akan kesepian.
11. Lilik yang senantiasa memberiku dorongan semangat, penghiburan, perhatian,
doa, cinta, dan menjadi tempat untuk menumpahkan segala kebahagiaan dan
kesedihanku.
12. Mas Koko yang sudah membantu menerjemahkan. Teman-teman “Silvester I”
dan “de Bronth” untuk hari-hari yang penuh tawa dan kebersamaan kalian
selama ini.
13. Teman-teman praktikum kelompok A untuk canda tawa, masukan, curhat,
obrolan kita, kebersamaan, dan hari-hari yang menyenangkan selama ini. Nanda
(untuk pinjaman laptopnya), dan juga untuk kelas A angkatan 2003 atas
kebersamaan kita.
Penulis menyadari bahwa penyusunan skripsi ini masih jauh dari sempurna
dan masih banyak kekurangan. Oleh karena itu, penulis mengharapkan kritik dan
saran yang membangun. Harapan penulis semoga skripsi ini memberi sedikit
tambahan pengetahuan khususnya di bidang kefarmasian dan dapat dimanfaatkan
sebagaimana mestinya.
Yogyakarta, Januari 2007
Penulis
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, Januari 2007 Penulis
Arnie Roosita
INTISARI
Ampisilin termasuk antibiotik golongan β-laktam yang sampai saat ini masih digunakan untuk pengobatan penyakit infeksi seperti infeksi saluran kemih dan saluran nafas. Pada penelitian ini dilakukan pengembangan metode analisis untuk penetapan kadar ampisilin yang berpedoman pada penelitian Patel et al. (1992) tentang penetapan kadar sefaleksin dengan pereaksi asetilaseton dan formalin secara spektrofotometri visibel, karena ampisilin memiliki kemiripan struktur dengan sefaleksin. Penelitian ini bertujuan untuk mengetahui apakah metode analisis tersebut memiliki validitas yang baik dan dapat diaplikasikan untuk penetapan kadar ampisilin dalam kapsul.
Penelitian ini termasuk penelitian non eksperimental deskriptif. Penetapan kadar ampisilin didasarkan pada reaksi antara ampisilin dengan hasil kondensasi asetilaseton dan formalin yang menghasilkan senyawa kuning. Kadar ampisilin ditetapkan dengan mengolah data serapan larutan kuning tersebut pada panjang gelombang serapan maksimum 398,0 nm dengan persamaan garis regresi linier. Validasi metode analisis ditentukan berdasarkan akurasi, presisi, dan linearitas yang diperoleh berturut-turut dari nilai % perolehan kembali, koefisien variasi (KV), dan koefisien korelasi (r).
Hasil yang diperoleh adalah % perolehan kembali = 99,85-102,37 %; KV = 1,05 %; r = 0,9992; dan rata-rata kadar ampisilin dalam kapsul = 567,16 mg/kapsul atau 113,43 %. Hasil penelitian menunjukkan bahwa metode analisis tersebut memiliki validitas yang baik, meliputi: akurasi, presisi, dan linearitas untuk penetapan kadar ampisilin dan dapat diaplikasikan untuk penetapan kadar ampisilin dalam kapsul.
Kata kunci : validasi metode analisis, spektrofotometri visibel, ampisilin, asetilaseton, formalin.
ABSTRACT
Ampicillin is one of β-lactam antibiotic which in recent still used for treatment the infection, such as urinary tract infection and respiratory tract infection. This research focuses on developing methods for ampicillin determination based on Patel et al. (1992) about visible spectrophotometry method with acetylaceton and formalin reagent for determination of cephalexin because ampicillin has structure similarity with cephalexin. This research intends to find out whether that method shows good validity and able to be applied to determine the rate ampicillin in the capsule.
This research can be categorized as descriptive non experimental one. The determination of ampicillin is based on the reaction between ampicillin with acetylaceton and formalin that yields yellow compound. The rate of ampicillin is determined by analyzing the data of yellow solution absorption within maximum wavelength 398,0 nm using linear regression equation The validation of the method is determined by its continuous accuracy, precision, and linearity from the percentage of the recovery, variation coefficient, and correlation coefficient..
It is found out that the result of the recovery = 99.85-102.37 %; variation coefficient = 1.05 %; correlation coefficient = 0.9992; and the average rate of ampicillin in the capsule = 567.16 mg/capsule or 113.43 %. The result shows that visible spectrophotometry method with acetylaceton and formalin reagent shows good validity in terms of accuracy, precision, and linearity for ampicillin determination and can be applied to determine the rate of ampicillin in the capsule.
Keyword : validation of method, visible spectrophotometry, ampicillin, acetylaceton, formalin.
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
KATA PENGANTAR ... v
PERNYATAAN KEASLIAN KARYA ... viii
INTISARI ... ix
ABSTRACT... x
DAFTAR ISI ... xi
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Perumusan masalah ... 3
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 5
B. Tujuan Penelitian ... 5
BAB II PENELAAHAN PUSTAKA ... 6
A. Ampisilin ... 6
B. Asetilaseton ... 10
C. Formalin ... 10
D. Spektrofotometri UV-Vis ... 11
1. Definisi spektrofotometri UV-Vis ... 11
2. Interaksi molekul dengan radiasi elektromagnetik ... 11
3. Konsep dasar radiasi elektromagnetik ... 12
4. Tipe-tipe transisi elektron ... 13
5. Pembacaan serapan dan transmitan ... 15
6. Hukum Lambert-Beer ... 17
7. Kesalahan fotometrik ... 18
8. Analisis kualitatif ... 19
9. Analisis kuantitatif... 20
10. Reaksi pembentukan warna ... 21
E. Parameter Validasi, Kategori Metode Analisis, dan Kesalahan dalam Analisis 23 1. Parameter validasi metode analisis ... 23
2. Kategori metode analisis ... 25
3. Kesalahan dalam analisis ... 26
F. Landasan Teori ... 27
G. Hipotesis ... 28
BAB III METODOLOGI PENELITIAN ... 29
A. Jenis dan Rancangan Penelitian ... 29
B. Definisi Operasional ... 29
C. Bahan-Bahan Penelitian ... 29
D. Alat-Alat Penelitian ... 30
E. Tata Cara Penelitian ... 30
1. Pembuatan larutan ... 30
2. Optimasi penetapan kadar ampisilin ... 31
3. Pembuatan kurva baku ... 33
4. Aplikasi metode spektrofotometri visibel untuk penetapan kadar ampisilin dalam kapsul “X” menggunakan pereaksi asetilaseton dan formalin... 33
5. Validasi metode spektrofotometri visibel untuk penetapan kadar ampisilin menggunakan pereaksi asetilaseton dan formalin ... 34
F. Analisis Hasil ... 35
BAB IV HASIL DAN PEMBAHASAN ... 37
A. Penetapan Operating Time ... 37
B. Penetapan pH Optimum ... 42
C. Penetapan Volume Pereaksi Optimum ... 44
D. Penetapan Panjang Gelombang Serapan Maksimum (λmaks)... 45
E. Penetapan Kurva Baku Ampisilin ... 47
F. Penetapan Kadar Ampisilin dalam Kapsul “X” ... 50
G. Analisis Validasi Metode Analisis ... 52
BAB V KESIMPULAN DAN SARAN ... 56
A. Kesimpulan ... 56
B. Saran ... 56
DAFTAR PUSTAKA ... 57
LAMPIRAN ... 60
BIOGRAFI ... 71
DAFTAR TABEL
Halaman
Tabel I. Kriteria penerimaan akurasi pada konsentrasi analit yang berbeda .... 23
Tabel II. Kriteria penerimaan presisi pada konsentrasi analit yang berbeda ... 24
Tabel III. Parameter validasi yang dipersyaratkan untuk validasi metode analisis... 26
Tabel IV. Hasil penetapan operating time reaksi antara ampisilin dengan asetilaseton dan formalin ... 41
Tabel V. Hasil penetapan pH optimum reaksi antara ampisilin dengan asetilaseton dan formalin ... 44
Tabel VI. Hasil penetapan volume pereaksi optimum ... 45
Tabel VII. Hasil penetapan kurva baku ampisilin sesudah direaksikan dengan asetilaseton dan formalin ... 48
Tabel VIII. Hasil modifikasi data penetapan kurva baku ampisilin sesudah direaksikan dengan asetilaseton dan formalin ... 49
Tabel IX. Hasil penetapan kadar ampisilin dalam kapsul “X” dengan metode spektrofotometri visibel menggunakan pereaksi asetilaseton dan formalin ... 51
Tabel X. Hasil penetapan % perolehan kembali sampel ampisilin ... 52
Tabel XI. Hasil penetapan % perolehan kembali ampisilin baku ... 53
Tabel XII. Hasil penetapan nilai KV ... 54
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur sefaleksin ... 2
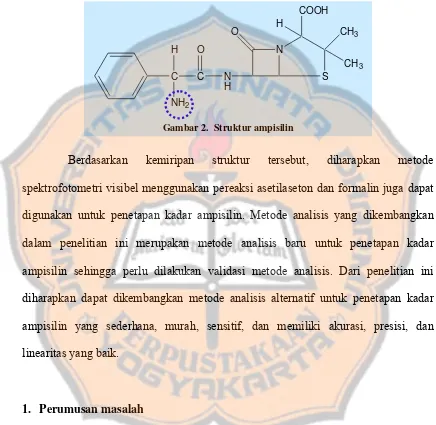
Gambar 2. Struktur ampisilin ... 3
Gambar 3. Struktur asetilaseton ... 10
Gambar 4. Struktur formalin ... 10
Gambar 5. Diagram tingkat energi elektronik ... 15
Gambar 6. Reaksi antara asetilaseton dan formalin ... 38
Gambar 7. Usulan reaksi antara ampisilin dengan senyawa hasil kondensasi asetilaseton dan formalin ... 40
Gambar 8. Spektrum hasil pengukuran stabilitas reaksi antara ampisilin dengan asetilaseton dan formalin ... 41
Gambar 9. Spektra hasil penetapan λmaks ampisilin pada konsentrasi 0,081; 0,113; 0,145 mg/ml yang bereaksi dengan asetilaseton dan formalin ... 46
Gambar 10. Hubungan antara konsentrasi ampisilin dengan serapan senyawa hasil reaksi ampisilin dengan asetilaseton dan formalin ... 50
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan konsentrasi larutan ampisilin baku pada penetapan
kurva baku ... 60
Lampiran 2. Spektrum ampisilin baku dan sampel ampisilin pada konsentrasi 0,145 mg/ml ... 61
Lampiran 3. Perhitungan kadar ampisilin dalam kapsul “X” ... 62
Lampiran 4. Perhitungan % perolehan kembali ampisilin ... 65
Lampiran 5. Perhitungan nilai koefisien variasi fungsi (Vx0) ... 68
Lampiran 6. Sertifikat analisis ampisilin ... 70
BAB I PENGANTAR
A. Latar Belakang
Sampai saat ini penyakit infeksi masih banyak terjadi di Indonesia. Oleh
karena itu, ketersediaan obat-obat untuk terapi penyakit infeksi masih sangat
dibutuhkan. Antibiotik merupakan salah satu obat yang dapat digunakan untuk terapi
penyakit infeksi, khususnya infeksi oleh bakteri. Ampisilin adalah salah satu contoh
antibiotik yang termasuk dalam golongan β-laktam turunan penisilin yang
mempunyai masalah pada resistensi. Walaupun demikian, sampai saat ini ampisilin
masih digunakan untuk mengobati infeksi saluran kemih dan infeksi saluran
pernapasan seperti sinusitis, otitis media, bronchitis kronik, dan epiglotis (Petri,
2001).
Seperti halnya obat-obat pada umumnya, penggunaan ampisilin selain
memberikan efek terapeutik juga dapat menghasilkan efek toksik bila dosisnya
berlebih atau malah tidak berefek bila dosisnya kurang. Oleh karena itu,
pemberiannya harus dilakukan dengan benar agar kerja obat tersebut efektif dan
aman. Tercapainya keefektifan dan keamanan obat tersebut juga didukung oleh
kualitas dan mutu obat yang baik. Oleh karenanya, kontrol kualitas dan mutu obat
sangat penting untuk dilakukan. Salah satu langkah dalam kontrol kualitas dan mutu
obat adalah dengan analisis kimia terhadap zat aktif yang meliputi analisis kualitatif
dan kuantitatif (penetapan kadar). Untuk antibiotik perlu juga dilakukan uji potensi
antibiotik secara mikrobiologi.
2
Penetapan kadar ampisilin menurut Farmakope Indonesia IV (1995) dapat
dilakukan dengan metode kromatografi cair kinerja tinggi (KCKT). Metode analisis
ini memiliki sensitivitas dan daya pisah yang baik, cepat, dan dapat digunakan untuk
penetapan kadar senyawa dalam campuran tanpa perlu pemisahan terlebih dahulu.
Namun, operasionalnya mahal. Ampisilin juga dapat ditetapkan kadarnya
berdasarkan penetapan kadar antibiotik secara iodometri (Anonim, 1995). Metode
analisis ini spesifik untuk penetapan kadar ampisilin utuh sehingga sekaligus dapat
menggambarkan potensi ampisilin. Namun, metode ini kurang sensitif untuk
penetapan kadar ampisilin dalam kadar kecil.
Pengembangan metode analisis untuk penetapan kadar obat perlu untuk
dilakukan. Tujuannya adalah untuk mencari metode analisis alternatif dan untuk
perkembangan ilmu. Metode analisis yang dikembangkan tersebut harus memenuhi
persyaratan validasi metode analisis.
Patel et al. (1992) melakukan penelitian tentang penetapan kadar sefaleksin
menggunakan pereaksi asetilaseton dan formalin dengan metode spektrofotometri
visibel.
C H
NH2 C O
N
H N
O
S
CH3 COOH
Gugus fungsi pada sefaleksin yang berperan dalam reaksi dengan asetilaseton dan
formalin adalah gugus amin primer. Dilihat dari strukturnya, ampisilin mirip dengan
sefaleksin. Ampisilin juga memiliki gugus amin primer seperti halnya sefaleksin.
C
Gambar 2. Struktur ampisilin
Berdasarkan kemiripan struktur tersebut, diharapkan metode
spektrofotometri visibel menggunakan pereaksi asetilaseton dan formalin juga dapat
digunakan untuk penetapan kadar ampisilin. Metode analisis yang dikembangkan
dalam penelitian ini merupakan metode analisis baru untuk penetapan kadar
ampisilin sehingga perlu dilakukan validasi metode analisis. Dari penelitian ini
diharapkan dapat dikembangkan metode analisis alternatif untuk penetapan kadar
ampisilin yang sederhana, murah, sensitif, dan memiliki akurasi, presisi, dan
linearitas yang baik.
1. Perumusan masalah
Berdasarkan latar belakang di atas maka dapat disusun permasalahan
sebagai berikut :
a. apakah metode spektrofotometri visibel menggunakan pereaksi asetilaseton dan
formalin memenuhi parameter validasi metode analisis yang meliputi akurasi,
4
b. apakah metode spektrofotometri visibel menggunakan pereaksi asetilaseton dan
formalin dapat diaplikasikan untuk penetapan kadar ampisilin dalam kapsul?
2. Keaslian penelitian
Sejauh pengetahuan penulis, penelitian tentang validasi metode
spektrofotometri visibel untuk penetapan kadar ampisilin menggunakan pereaksi
asetilaseton dan formalin belum pernah dilakukan. Penelitian tentang ampisilin yang
pernah dilakukan dan dipublikasikan antara lain penetapan kadar ampisilin utuh
secara spektrofotometri UV dengan reagen imidazole (Bundgaard, 1974), penetapan
kadarampisilin dalam tablet dengan nama generik dan dagang menggunakan KCKT
fase terbalik (Putra, 2002), perbandingan metode spektrofotometri UV dengan
menggunakan reagen imidazole dan iodometri pada penetapan kadar ampisilin utuh
dalam suspensi ampisilin terdegradasi (Hermanto, 2004), dan pengaruh suhu dan
lama penyimpanan terhadap kadar ampisilin utuh dalam suspensi oral ampisilin
(Nyoman, 2004).
Penelitian tentang antibiotik golongan β-laktam yang lain menggunakan
metode analisis yang sejenis juga pernah dilakukan, yaitu penelitian tentang
penetapan kadar sefaleksin dalam berbagai bentuk sediaan dengan pereaksi
asetilaseton dan formalin secara spektrofotometri visibel oleh Patel et al. (1992),
penetapan kadar sefadroksil secara spektrofotometri visibel dengan pereaksi etil
asetoasetat dan formalin (Rianti, 2005), penetapan kadar sefadroksil dalam kapsul
menggunakan metode spektrofotometri UV dengan pereaksi etil asetoasetat dan
kadar sefadroksil menggunakan pereaksi asetilaseton dan formalin (Mirmayanti,
2007), dan validasi metode spektrofotometri visibel untuk penetapan kadar
amoksisilin menggunakan pereaksi asetilaseton dan formalin (Sunarto, 2007).
3. Manfaat penelitian
Hasil penelitian nantinya diharapkan memberikan manfaat sebagai berikut :
a. manfaat teoritis dari penelitian ini adalah memberikan informasi tentang
validasi metode spektrofotometri visibel menggunakan pereaksi asetilaseton dan
formalin untuk penetapan kadar ampisilin.
b. manfaat metodologis dari penelitian ini adalah memberikan informasi
tentang pengembangan metode analisis untuk penetapan kadar ampisilin agar
nantinya dapat digunakan sebagai metode analisis alternatif untuk penetapan kadar
ampisilin.
B. Tujuan Penelitian
1. Untuk mengetahui apakah metode spektrofotometri visibel menggunakan
pereaksi asetilaseton dan formalin memenuhi parameter validasi metode analisis
yang meliputi akurasi, presisi, dan linearitas jika digunakan untuk penetapan
kadar ampisilin.
2. Untuk mengetahui apakah metode spektrofotometri visibel menggunakan
pereaksi asetilaseton dan formalin dapat diaplikasikan untuk penetapan kadar
BAB II
PENELAAHAN PUSTAKA
A. Ampisilin
Ampisilin berbentuk anhidrat dengan bobot molekul (BM) 349,40 atau
trihidrat dengan BM 403,45. Ampisilin mengandung tidak kurang dari 900 µg dan
tidak lebih dari 1050 µg per mg C16H19N3O4S, dihitung terhadap zat anhidrat. pH
ampisilin antara 3,5 sampai 6,0. Ampisilin berupa serbuk hablur, putih, dan praktis
tidak berbau. Kelarutan ampisilin adalah sukar larut dalam air dan metanol; tidak
larut dalam benzena, dalam karbon tetraklorida, dan dalam kloroform. Kapsul
ampisilin mengandung sejumlah ampisilin (anhidrat atau trihidrat) setara dengan
tidak kurang dari 90,0% dan tidak lebih dari 120,0% C16H19N3O4S jumlah yang
tertera pada etiket (Anonim, 1995).
Ampisilin termasuk dalam antibiotik golongan β-laktam karena memiliki
struktur dasar cincin β-laktam. Perubahan pada cincin β-laktam dapat mengubah
aktivitasnya sebagai anti bakteri. Ampisilin adalah salah satu antibiotik golongan β
-laktam turunan penisilin yang digolongkan dalam aminopenisilin karena di dalam
strukturnya terdapat gugus amino. Aminopenisilin memiliki aktivitas anti bakteri
yang hampir sama dengan penisilin G namun spektrum kerjanya lebih luas daripada
penisilin G (Petri, 2001). Mekanisme kerja ampisilin sebagai anti bakteri adalah
menghambat pembentukan dinding sel bakteri dengan cara berikatan dengan
penicillin binding proteins (PBPs) sehingga akan menghambat fase transpeptidase
akhir dari sintesis peptidoglikan pada dinding sel bakteri (Lacy et al., 2003).
Ampisilin bersifat bakterisida terhadap beberapa bakteri gram positif dan
bakteri gram negatif (Petri, 2001) tetapi ampisilin tidak tahan terhadap penisilinase.
Oleh karena itu, ampisilin resisten terhadap bakteri pembentuk penisilinase
(Mutschler, 1991). Ampisilin menunjukkan stabilitas yang baik dalam suasana asam,
efektif pada konsentrasi hambat minimum, diabsorpsi dengan baik dalam usus
sehingga dapat diberikan secara oral (Hou and Poole, 1969). Namun, penggunaan
ampisilin setelah mengkonsumsi makanan akan menurunkan absorpsi obat (Petri,
2001). Oleh karena itu, ampisilin harus diminum dalam keadaan perut kosong yaitu 1
jam sebelum makan atau 2 jam setelah makan (Lacy et al., 2003).
Beberapa metode analisis yang dapat digunakan untuk penetapan kadar
ampisilin adalah :
1. metode iodometri
Penetapan kadar ampisilin secara iodometri didasarkan pada reduksi iodium
oleh penisilamin yang terbentuk melalui inaktivasi ampisilin oleh alkali atau enzim
penisilinase dan diikuti dengan penambahan asam. Larutan alkali atau enzim
penisilinase akan menghidrolisis ampisilin sehingga terjadi pemecahan cincin β
-laktam dan terbentuk asam α-aminobenzilpenisiloat. Senyawa ini dengan
penambahan asam akan membentuk penisilamin. Ampisilin tidak dapat bereaksi
8
Kadar ampisilin ditetapkan dengan menambahkan iodium berlebih ke
dalam larutan yang mengandung penisilamin. Kelebihan iodium dititrasi kembali
dengan natrium tiosulfat. Perbedaan volume iodium yang dikonsumsi larutan sampel
dengan blangko menggambarkan kadar ampisilin dalam larutan (Ivashkiv, 1973).
2. metode spektrofotometri UV
Metode ini didasarkan pada pengikatan merkurium oleh α-asetamido
benzilpenisilin yang merupakan hasil asetilasi ampisilin dengan asetat anhidrat dalam
larutan pada pH 9. Hasil reaksi antara merkurium dengan α-asetamido benzilpenisilin
adalah asam α-asetamido benzilpenisilinat yang mengikat merkurium. Kadar
ampisilin ditentukan dengan mengukur asam α-asetamido benzilpenisilinat yang
mengikat merkurium dengan spektrofotometri UV (Ivashkiv, 1973).
3. metode KCKT
Menurut Farmakope Indonesia IV (1995) penetapan kadar ampisilin dapat
dilakukan dengan KCKT dengan fase gerak air : asetonitril : KH2PO4 1 M : asam
asetat 1 M (909 : 80 : 10 : 1) dan fase diam berupa kolom analisis 4 mm x 30 cm
dengan bahan pengisi L1 yaitu oktadesil silana terikat secara kimiawi pada partikel
mikrosilika berpori dengan ukuran partikel 5-10 µm. Sistem KCKT ini juga
menggunakan pra kolom dengan ukuran 4 mm x 5 cm. Laju aliran fase gerak lebih
kurang 2 ml/ menit. Detektor yang digunakan adalah detektor UV 254 nm. Pelarut
yang digunakan berupa campuran KH2PO4 1 M dan asam asetat 1 M (10 : 1). Selain
itu, juga dapat digunakan fase gerak lain yaitu 0,067 M KH2PO4 pH 4,6 : methanol
4. metode fluorometri
Ampisilin dapat ditetapkan kadarnya dengan fluorometri karena ampisilin
dalam larutan asam pada suhu yang dinaikkan akan memendarkan warna kuning
(Ivashkiv, 1973).
5. metode penetapan kadar ampisilin yang lainnya adalah titrasi dengan basa,
biasanya menggunakan NaOH (Auterhoff and Kovar, 1987), metode polarigrafi,
kromatografi lapis tipis, kromatografi kertas, dan metode mikrobiologi (Ivashkiv,
1973).
Ampisilin memiliki kemiripan struktur dengan sefaleksin yaitu keduanya
sama-sama memiliki cincin β-laktam dan gugus amin primer. Patel et al. (1992)
melakukan penelitian tentang penetapan kadar sefaleksin dengan pereaksi
asetilaseton dan formalin secara spektrofotometri visibel. Pada penelitian tersebut
terlebih dahulu dilakukan optimasi kondisi reaksi yang meliputi konsentrasi pereaksi,
pH pereaksi, waktu reaksi, suhu reaksi, dan pelarut. Selektivitas reaksi juga
ditentukan dengan cara mengamati pengaruh penambahan berbagai macam eksipien
ke dalam sefaleksin terhadap nilai % perolehan kembali.
Penetapan kadar sefaleksin didasarkan pada reaksi antara sefaleksin
dengan hasil kondensasi asetilaseton dan formalin dalam bufer asetat. Gugus fungsi
pada sefaleksin yang bertanggung jawab dalam reaksi tersebut adalah gugus amin
primer. Hasil reaksi antara gugus amin primer pada sefaleksin dengan hasil
kondensasi asetilaseton dan formalin adalah larutan berwarna kuning yang memiliki
10
gelombang 400,0 nm. Kadar sefaleksin ditentukan dengan mengolah data
pengukuran serapan larutan tersebut menggunakan persamaan garis regresi linier.
Hasil penelitian Patel et al. (1992) menunjukkan bahwa metode tersebut sederhana,
cepat, akurat, dan selektif untuk penetapan kadar sefaleksin baik dalam bentuk murni
(senyawa baku) maupun dalam berbagai macam sediaan obat.
B. Asetilaseton
Asetilaseton P (gambar 3) mengandung tidak kurang dari 98% C5H8O2 dan
memiliki bobot molekul 100,11. Senyawa ini berupa cairan jernih, tidak berwarna
hingga kuning lemah, dan mudah terbakar. Kelarutan asetilaseton P adalah larut
dalam air dan dapat bercampur dengan etanol, dengan kloroform, dengan aseton,
dengan eter, dan dengan asam asetat glasial. Asetilaseton P memiliki indeks bias
1,4505 dan 14525 pada suhu 20o (Anonim, 1995).
H3C C
O
CH2 C
O
CH3
Gambar 3. Struktur asetilaseton
C. Formalin
C O
H H
Formalin (larutan formaldehid) adalah larutan yang mengandung 37 %
formaldehid dalam air, biasanya ditambahkan 10-15 % metanol untuk mencegah
polimerisasi. Larutan formalin 100 % atau larutan formalin 40 adalah larutan yang
mengandung 40 gram formaldehid dalam 100 ml pelarut. Formalin berupa cairan
tidak berwarna dan berbau sangat tajam. Formaldehid berupa gas yang mudah
terbakar, berbau sangat tajam, sangat larut air; larut dalam alkohol dan dalam eter,
sangat reaktif, dan mudah mengalami polimerisasi (Anonim, 1989).
D. Spektrofotometri UV-Vis 1. Definisi spektrofotometri UV-Vis
Spektrofotometri UV-Vis adalah salah satu teknik analisis fisiko-kimia
yang mengamati interaksi atom atau molekul dari suatu zat kimia dengan radiasi
elektromagnetik ultraviolet dekat (190-380 nm) dan sinar tampak (380-780 nm)
dengan menggunakan spektrofotometer (Mulja dan Suharman, 1995).
2. Interaksi molekul dengan radiasi elektromagnetik
Suatu berkas radiasi elektromagnetik bila dilewatkan melalui suatu zat
kimia maka sebagian dari radiasi elektromagnetik tersebut akan diserap (Khopkar,
1990). Molekul dalam zat tersebut akan menyerap radiasi elektromagnetik pada
daerah panjang gelombang yang energinya sesuai dengan beda energi antara keadaan
dasar dan keadaan eksitasi dalam molekul (Roth and Blaschke, 1981). Molekul dapat
12
mengalami transisi elektron dari tingkat energi rendah ke tingkat energi tinggi yaitu
tingkat eksitasi (Khopkar, 1990). Elektron molekul organik yang menyerap meliputi
elektron yang digunakan pada ikatan antara atom-atom dan elektron nonbonding atau
elektron tak berpasangan yang pada umumnya terlokalisasi (Skoog, 1985).
Gugus fungsi pada suatu molekul organik yang bertanggung jawab terhadap
serapan radiasi ultraviolet dekat dan sinar tampak adalah kromofor. Molekul organik
yang mengandung gugus kromofor disebut kromogen (Christian, 2004). Pada
senyawa organik dikenal pula gugus auksokrom, yaitu gugus fungsi heteroatom yang
mempunyai elektron valensi nonbonding seperti –OH, -NH2 dan -OCH3 yang tidak
menyerap radiasi pada panjang gelombang >200 nm (Pecsok et al., 1976).
Terikatnya gugus auksokrom pada gugus kromofor akan mengakibatkan pergeseran
pita serapan menuju ke panjang gelombang yang lebih panjang dan disertai
perubahan intensitas serapan (Mulja dan Suharman, 1995).
3. Konsep dasar radiasi elektromagnetik
Energi radiasi elektromagnetik yang diserap menyebabkan perubahan
energi elektronik suatu molekul sehingga menyebabkan terjadinya transisi elektron
valensi molekul tersebut. Hubungan antara energi yang diserap untuk transisi
elektron dengan frekuensi, panjang gelombang, dan bilangan gelombang adalah :
………... (1)
∆E = h x v = h x
λ
c
dengan :
E = energi (Joule)
h = konstante Planck (6,63 x 10-34 Joule. detik) v = frekuensi radiasi (Hertz)
c = kecepatan radiasi (3 x 1010 cm. detik-1)
λ = panjang gelombang (cm)
v = bilangan gelombang (cm-1)
(Silverstein etal., 1991)
Berdasar persamaan di atas, energi yang dibutuhkan suatu molekul untuk
bertransisi berbanding terbalik dengan panjang gelombang. Molekul yang
membutuhkan energi transisi lebih besar akan menyerap radiasi elektromagnetik
pada panjang gelombang yang lebih pendek, sebaliknya molekul yang membutuhkan
energi transisi lebih kecil akan menyerap pada panjang gelombang yang lebih
panjang.
4. Tipe-tipe transisi elektron
Radiasi ultraviolet dan cahaya tampak akan meningkatkan energi elektronik
sebuah molekul. Artinya energi yang disumbangkan oleh foton-foton memungkinkan
elektron-elektron mengatasi kekangan inti dan pindah ke orbital baru yang lebih
tinggi energinya (Day and Underwood, 2002). Oleh karena itu, serapan radiasi
ultraviolet dan sinar tampak dapat menyebabkan terjadinya transisi elektron σ→σ*,
n→σ*, n→π *, dan π→π * (gambar 5). σ* dan π * adalah orbital atom antibonding,
sedangkan n adalah orbital atom nonbonding yang mempunyai energi diantara orbital
atom bonding dan antibonding (Khopkar, 1990). Transisi elektron yang dapat terjadi
14
a. transisi elektron σ→σ*. Pada tipe transisi ini elektron di orbital σ bonding
akan tereksitasi ke orbital antibonding. Transisi ini tidak terjadi pada daerah radiasi
ultraviolet dekat, tetapi terjadi pada daerah radiasi ultraviolet jauh (Khopkar, 1990).
Transisi ini membutuhkan energi yang terbesar dan terjadi pada molekul dengan
ikatan tunggal, misalnya alkana (Mulja dan Suharman, 1995).
b. transisi elektron n→σ*. Pada transisi ini terjadi eksitasi elektron dari
orbital nonbonding ke orbital antibonding.Transisi ini terjadi pada senyawa-senyawa
jenuh dengan elektron nonbonding, membutuhkan energi yang lebih rendah daripada
transisi elektron σ→σ* dan terjadi karena radiasi pada daerah 150-250 nm (Khopkar,
1990).
c. transisi elektron n→π* dan transisi elektron π→π*. Kebanyakan
penerapan spektrofotometri UV-Vis pada senyawa organik didasarkan pada transisi
n→π* ataupun π→π*. Energi yang diperlukan untuk transisi menghasilkan serapan
maksimum pada daerah 200-700 nm (Khopkar, 1990). Transisi n→π* terjadi pada
senyawa yang memiliki elektron nonbonding yang tereksitasi ke orbital antibonding,
contohnya senyawa-senyawa yang mengandung gugus C=O, C=S, C=N, dan N=O
(Daglish,1969). Transisi π→π* dihasilkan oleh senyawa dengan ikatan rangkap dua
dan tiga (alkena dan alkuna) bila menyerap energi yang sesuai dan terjadi di daerah
σ* antibonding
π* antibonding
E n nonbonding
π bonding
σ bonding
Gambar 5. Diagram tingkat energi elektronik
(Mulja dan Suharman, 1995)
5. Pembacaan serapan dan transmitan
Jika suatu radiasi elektromagnetik dilewatkan pada suatu larutan dengan
intensitas radiasi semula (Io), maka sebagian radiasi tersebut akan diteruskan (It),
dipantulkan (Ir), dan diserap (Ia), sehingga :
Io = It + Ir + Ia
……… (2)
Pada prakteknya nilai Ir sangat kecil(~ 4%) sehingga dapat diabaikan. Maka
persamaan di atas menjadi :
………... (3) Io = It + Ia
16
Analisis dengan spektrofotometri UV-Vis selalu melibatkan pembacaan
serapan radiasi elektromagnetik oleh molekul atau radiasi elektromagnetik yang
teruskan. Keduanya dikenal sebagai serapan (A) tanpa satuan dan transmitan dengan
satuan persen (%T) (Mulja dan Suharman, 1995). Serapan (A) adalah logaritma
perbandingan intensitas cahaya yang dipancarkan (Io) terhadap intensitas cahaya
yang diteruskan (It) (Roth and Blaschke, 1981). Serapan dirumuskan:
……….. (4)
A = log
t o I I
(Skoog, 1985)
Transmitan (%T) adalah perbandingan intensitas dari sinar yang diteruskan (It)
terhadap sinar yang dipancarkan (Io) dalam persen (Roth dan Blaschke, 1981).
Transmitan dirumuskan:
……… (5)
T =
o t I I
(Skoog, 1985)
Panjang gelombang terjadinya serapan bergantung pada kekuatan elektron
terikat dalam molekul (Day and Underwood, 2002). Panjang gelombang yang
digunakan untuk dalam pengukuran serapan adalah panjang gelombang serapan
maksimum (λmaks), karena perubahan serapan untuk setiap satuan konsentrasi adalah
paling besar pada λmaks, sehingga akan diperoleh kepekaan analisis yang maksimum.
Selain itu, pita serapan di sekitar λmaks datar sehingga mengurangi kesalahan pada
6. Hukum Lambert-Beer
Serapan radiasi elektromagnetik oleh suatu zat penyerap pada panjang
gelombang monokromatis digambarkan oleh 2 hukum. Kedua hukum tersebut
adalah:
a. hukum Lambert yaitu intensitas radiasi yang diteruskan (I) menurun
secara eksponensial dengan meningkatnya tebal larutan (b).
b. hukum Beer yaitu intensitas radiasi yang diteruskan (I) menurun secara
eksponensial dengan meningkatnya konsentrasi larutan (c).
Kombinasi kedua hukum tersebut menghasilkan hukum Lambert-Beer yang
dirumuskan :
...……….. (6)
log
I Io
= A = k x b x c
dengan Io adalah intensitas radiasi yang terjadi, A adalah serapan dan k adalah daya
serap (liter/g/cm) (Fell, 1986).
Daya serap adalah serapan larutan 1 gram/liter pada kuvet setebal 1 cm.
Daya serap disebut daya serap molar (ε) bila satuannya liter/mol/cm. Daya serap
molar adalah serapan 1 molar larutan pada kuvet setebal 1 cm (Fell, 1986). Daya
serap molar dirumuskan :
ε = A11%cmx 0,1 x BM
..………... (7)
dengan A11%cm adalah serapan jenis dan BM adalah bobot molekul.
18
Nilai daya serap molar tergantung pada area molekul sasaran (a) dan
probabilitas transisi elektron (p) yang dirumuskan :
..………... (8)
ε = 0,87 x 1020 x p x a
(Skoog, 1985)
Nilai p antara 0,1 – 1 memberikan serapan yang kuat (ε = 104 - 105). Puncak
spektrum yang memiliki nilai ε kurang dari 103 (nilai p kurang dari 0,01) dikatakan
intensitas serapannya lemah (Skoog, 1985).
Bila konsentrasi dinyatakan dalam gram/100 ml maka k dideskripsikan
sebagai serapan jenis yang dilambangkan dengan (Fell, 1986). Serapan jenis
adalah serapan dari larutan 1% b/v zat terlarut dalam kuvet setebal 1 cm. Harga
serapan jenis pada panjang gelombang tertentu dalam suatu pelarut merupakan sifat
dari zat terlarut (Anonim, 1995).
% 1
cm 1 A
7. Kesalahan fotometrik
Ketepatan prosedur fotometrik dibatasi oleh nilai serapan. Pada nilai
serapan rendah, intensitas radiasi yang terjadi dan yang diteruskan hampir sama
sehingga kesalahan dalam pembacaan serapan relatif besar karena yang dibaca oleh
alat adalah perbedaan antara intensitas radiasi yang terjadi dan yang diteruskan. Pada
nilai serapan tinggi, intensitas radiasi yang diteruskan terlalu kecil sehingga tidak
Untuk pembacaan serapan (A) atau transmitan (T) pada daerah yang
terbatas, kesalahan penentuan kadar hasil analisis dinyatakan :
……… ……… (9)
C C
∆
= T log 0,4343
x T
T
∆
∆T adalah harga rentang skala transmitan terkecil dari alat yang masih dapat terbaca
pada analisis dengan metode spektrofotometri UV-Vis. Dari rumus di atas dapat
diperhitungkan kesalahan pembacaan A atau T pada analisis dengan spektrofotometri
UV-Vis. Pembacaan A (0,2-0,8) atau %T (15-65%) akan memberikan persentase
kesalahan analisis yang dapat diterima (0,5-1%) untuk ∆T = 1% (Mulja dan
Suharman, 1995). Apabila pembacaan serapan di luar rentang tersebut maka dapat
dilakukan hal-hal berikut : pengenceran larutan, penggunaan kuvet yang lebih tepat,
atau pemilihan panjang gelombang yang lebih tepat (Pecsok et al., 1976).
8. Analisis kualitatif
Analisis kualitatif dengan metode spektrofotometri UV-Vis hanya dipakai
untuk data pendukung. Analisisnya dapat dilakukan dengan :
a. pemeriksaan kemiripan spektrum UV-Vis
b. penentuan panjang gelombang serapan maksimum (λmaks).
20
9. Analisis kuantitatif
Analisis kuantitatif dengan metode spektrofotometri UV-Vis (Mulja dan
Suharman, 1995) dapat digolongkan menjadi :
a. analisis kuantitatif zat tunggal dengan metode spektrofotometri UV-Vis
dapat dilakukan dengan berbagai cara yaitu :
1) dengan membandingkan serapan atau persen transmitan zat yang dianalisis
dengan senyawa baku pada λmaks. Persyaratannya pembacaan nilai serapan antara
sampel dan senyawa baku tidak jauh berbeda.
………. (10)
dengan :
A(S) = serapan larutan sampel
C(S) = konsentrasi larutan sampel
A(R.S) = serapan senyawa baku
C(R.S) = konsentrasi senyawa baku
A(S) x C(S) = A(R.S) x C(R.S)
2) dengan menggunakan kurva baku larutan senyawa baku dengan pelarut tertentu
pada λmaks. Dibuat grafik dengan ordinat adalah serapan dan sebagai absis adalah
konsentrasi.
3) dengan menghitung nilai larutan sampel pada pelarut tertentu dan
dibandingkan dengan zat yang dianalisis yang tertera pada buku resmi.
%
4) dengan menghitung nilai ε sampel dan dibandingkan dengan nilai ε zat yang
b. analisis kuantitatif campuran dua macam zat. Prinsip pelaksanaannya
adalah mencari serapan atau beda serapan tiap-tiap komponen yang memberikan
korelasi yang linier terhadap konsentrasi, sehingga akan dihitung masing-masing
kadar campurannya secara serentak atau salah satu komponen dalam campuran.
c. analisis kuantitatif campuran tiga macam zat atau lebih (multi
komponen). Prinsipnya adalah kalibrasi tiap-tiap komponen dengan memakai larutan
baku.
10.Reaksi pembentukan warna
Ruang lingkup spektrofotometri serapan dapat diperluas dengan reaksi
pembentukan warna yang akan meningkatkan sensitivitas dan selektivitas suatu
senyawa bila dibandingkan penetapannya secara spektrofotometri UV. Reaksi warna
digunakan untuk memodifikasi spektrum suatu molekul penyerap sehingga dapat
dideteksi pada daerah sinar tampak dan terpisah dari komponen pengganggu lain
yang dapat terdeteksi bila diukur pada daerah ultraviolet (Fell, 1986). Pada reaksi
warna, perubahan senyawa tidak berwarna menjadi senyawa berwarna terjadi karena
adanya perpanjangan gugus kromofor oleh penambahan zat lain ke dalam larutan
tersebut atau karena terjadi pembentukan kompleks warna (Roth and Blaschke,
1981). Selain itu, senyawa yang dari asalnya berwarna juga dapat dideteksi pada
daerah sinar tampak.
Beberapa hal yang perlu diperhatikan dalam reaksi warna (Vogel, 1994)
22
a. kespesifikan reaksi warna. Sangat sedikit reaksi yang khas untuk
suatu zat tertentu, tetapi banyak reaksi menghasilkan warna untuk sekelompok kecil
zat yang sehubungan saja, artinya reaksi-reaksi itu selektif.
b. kesebandingan antara warna dan konsentrasi. Intensitas warna
hendaknya meningkat secara linier dengan naiknya konsentrasi zat yang akan
ditetapkan. Jika tidak dinyatakan lain, diharapkan bahwa korelasi tersebut memenuhi
hukum Lambert-Beer.
c. kestabilan warna. Warna yang dihasilkan hendaknya cukup stabil
untuk memungkinkan pembacaan yang tepat. Periode warna optimum harus cukup
panjang untuk membuat pengukuran yang cermat.
d. reprodusibilitas. Prosedur reaksi warna harus memberi hasil yang
dapat diulang pada kondisi eksperimen yang khas.
e. kejernihan larutan. Larutan harus bebas dari endapan karena endapan
dapat menghamburkan maupun menyerap cahaya.
f. kepekaan tinggi. Diharapkan reaksi warna sangat peka terutama bila
yang ditetapkan adalah zat berkuantitas kecil dan diharapkan pula produk reaksi
E. Parameter Validasi, Kategori Metode Analisis dan Kesalahan dalam Analisis
1. Parameter validasi metode analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa
parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Parameter-parameter yang digunakan sebagai pedoman validasi metode
analisis adalah :
a. akurasi adalah kedekatan hasil analisis yang diperoleh dengan memakai
metode tersebut dengan nilai yang sebenarnya. Akurasi metode analisis biasanya
dinyatakan dengan persen perolehan kembali analit dalam sampel yang kadarnya
telah diketahui dengan pasti (Anonim, 2005). Berikut adalah kriteria penerimaan
akurasi berdasarkan kadar analit (Yuwono dan Indrayanto, 2005) :
Tabel I. Kriteria penerimaan akurasi pada konsentrasi analit yang berbeda
Kadar analit (%) Rata-rata % perolehan kembali (%)
100 98-102
≥ 10 98-102
≥ 1 97-103
≥ 0,1 95-105
0,01 90-107
Akurasi untuk kadar obat yang besar adalah 95-105 % sedangkan untuk bioanalisis
rentang 80-120% masih bisa diterima (Mulja dan Hanwar, 2003).
b. presisi adalah derajat kesesuaian di antara hasil uji individual ketika
24
sampel yang homogen. Presisi dinyatakan dalan simpangan baku atau simpangan
baku relatif (koefisien variasi) (Anonim, 2005).
Presisi terdiri dari 3 macam, yaitu (Anonim, 2005) :
1) Reproducibility adalah keseksamaan metode bila analisis dikerjakan di
laboratorium yang berbeda.
2) Intermediate precision adalah keseksamaan metode jika analisis dikerjakan di
laboratorium yang sama pada hari yang berbeda atau analis yang berbeda atau
peralatan yang berbeda.
3) Repeatability adalah keseksamaan metode jika analisis dilakukan oleh analis
yang sama dengan peralatan yang sama pada interval waktu yang pendek.
Berikut adalah kriteria penerimaan presisi berdasarkan kadar analit (Yuwono dan
Indrayanto, 2005) :
Tabel II. Kriteria penerimaan presisi pada konsentrasi analit yang berbeda
Kadar analit (%) Koefisien variasi/ KV (%)
100 1,3
≥ 10 2,7
≥ 1 2,8
≥ 0,1 3,7
0,01 5,3
Unttuk bioanalisis nilai KV 15-20% masih dapat diterima (Mulja dan Hanwar, 2003).
c. spesifisitas suatu metode adalah kemampuan suatu metode untuk
mengukur dengan akurat respon analit dalam sampel dengan adanya komponen lain
yang mungkin ada dalam sampel seperti pengotor dan produk degradasi (Anonim,
d. detection limit adalah konsentrasi analit terkecil yang dapat terdeteksi,
tetapi tidak perlu kuantitatif, di bawah kondisi percobaan yang ditentukan.
Pengukuran detection limit digambarkan sebagai rasio signal-to-noise dengan
membandingkan hasil uji sampel dengan analit yang diketahui konsentrasinya dan
blangko serta menetapkan konsentrasi terendah analit yang dapat terdeteksi untuk
metode instrumental. Rasio signal-to-noise untuk detection limit adalah 2:1 atau 3:1.
Selain itu, penentuan detection limit dapat juga didasarkan pada slope kurva baku
dan standar deviasi (simpangan baku) (Anonim, 2005).
e. quantitation limit menyatakan jumlah terendah analit dalam sampel
yang dapat ditentukan dengan akurasi dan presisi yang dapat diterima di bawah
kondisi percobaan yang ditentukan. Rasio signal-to-noise untuk quantitation limit
adalah 10:1. Penentuan quantitation limit dapat juga didasarkan pada slope kurva
baku dan standar deviasi (simpangan baku) (Anonim, 2005).
f. linearitas dan range. Linearitas adalah kemampuan metode analisis
untuk memberikan respon secara langsung atau dengan bantuan transformasi
matematik yang baik, proporsional terhadap konsentrasi analit dalam sampel pada
rentang yang diberikan (Anonim, 2005). Range adalah interval level analit terendah
dan tertinggi yang sudah ditunjukkan dapat ditetapkan dengan akurasi, presisi, dan
linearitas yang dapat diterima (Anonim, 2005).
2. Kategori metode analisis
26
a. kategori I, mencakup metode analisis untuk kuantifikasi komponen
terbesar dalam obat atau bahan aktif (termasuk bahan pengawet) dari suatu sediaan.
b. kategori II, mencakup metode analisis untuk penentuan impurities
bahan obat dan degradasi produk sediaan farmasi, termasuk penentuan kuantitatif
dan uji batas.
c. kategori III, mencakup metode analisis yang digunakan untuk
menentukan karakteristik sediaan farmasi (seperti disolusi, pelepasan obat).
d. kategori IV, mencakup uji identifikasi.
Setiap kategori metode analisis memiliki persyaratan validasi yang
berbeda-beda, seperti yang tercantum pada tabel III.
Tabel III. Parameter validasi yang dipersyaratkan untuk validasi metode analisis Kategori II
Parameter Kategori I
Kualitatif Uji batas
Kategori III Kategori IV
Akurasi Ya Ya * * Tidak
Presisi Ya Ya Tidak Ya Tidak
Spesifisitas Ya Ya Ya * Ya
Detection Limit Tidak Tidak Ya * Tidak
Quantitation Limit Tidak Ya Tidak * Tidak
Linearitas Ya Ya Tidak * Tidak
Range Ya Ya * * Tidak
* Mungkin dibutuhkan, tergantung pada sifat tes yang spesifik.
(Anonim, 2005)
3. Kesalahan dalam analisis
a. kesalahan sistematik merupakan hasil analisis yang menyimpang secara
tetap dari nilai sebenarnya karena proses pelaksanaan prosedur analisis. Kesalahan
sistematik ada 2 macam, yaitu:
1) kesalahan pada metode analisis, agak sulit dideteksi karena kesalahan metode
analisis ini antara lain disebabkan sifat fisika kimia pereaksi yang dipakai tidak
memadai.
2) kesalahan individual adalah kesalahan yang timbul karena kesalahan individu
dalam pengamatan atau pembacaan instrumen yang dihadapi.
Kesalahan ini dapat dicari sebabnya dan dapat dikendalikan dengan kalibrasi
instrumen secara berkala, pemilihan metode dan prosedur standar dari badan resmi,
pemakaian bahan kimia dengan derajat untuk analisis, dan peningkatan pengetahuan
peneliti.
b. kesalahan tidak sistematik adalah penyimpangan tidak tetap dari hasil
penentuan kadar dengan instrumentasi yang disebabkan oleh fluktuasi instrumen
yang dipakai. Meningkatnya kesalahan tidak sistematik disebabkan tiap bagian
instrumen memberikan noise yang kecil yang kemudian ada kemungkinan menjadi
semakin besar sebagai nilai noise kumulatif. Penyebab kesalahan ini tidak diketahui.
Pemakaian instrumen dengan kualitas baik akan menekan nilai kesalahan ini.
F. Landasan Teori
Ampisilin merupakan antibiotik golongan β-laktam turunan penisilin, yang
28
golongan β-laktam turunan sefalosporin. Kemiripan struktur tersebut bukan hanya
terletak pada keberadaan cincin β-laktam tetapi kedua senyawa tersebut juga
memiliki gugus amin primer. Penetapan kadar sefaleksin dapat dilakukan dengan
metode spektrofotometri visibel dengan pereaksi asetilaseton dan formalin.
Penetapan kadar sefaleksin tersebut didasarkan pada pembentukan senyawa
berwarna kuning hasil reaksi sefaleksin dengan hasil kondensasi asetilaseton dan
formalin. Gugus fungsi pada sefaleksin yang bereaksi dengan asetilaseton dan
formalin adalah gugus amin primer. Metode spektrofotometri visibeldengan pereaksi
asetilaseton dan formalin tersebut mempunyai tingkat selektivitas dan akurasi yang
baik untuk penetapan kadar sefaleksin baik dalam senyawa murni maupun dalam
berbagai macam sediaan obat.
G. Hipotesis
1. Metode spektrofotometri visibelmenggunakan pereaksi asetilaseton dan formalin
memiliki validitas yang baik untuk penetapan kadar ampisilin.
2. Metode spektrofotometri visibelmenggunakan pereaksi asetilaseton dan formalin
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian non eksperimental dengan
rancangan penelitian deskriptif, sebab pada penelitian ini tidak dilakukan manipulasi
terhadap subjek uji. Penelitian hanya mendeskripsikan keadaan yang ada.
B. Definisi Operasional
1. Parameter validasi metode analisis yang diamati dalam penelitian ini adalah
akurasi, presisi, dan linearitas.
2. Sampel ampisilin yang digunakan adalah kapsul ampisilin merek “X” yang
mengandung ampisilin 500 mg.
3. Kadar ampisilin dinyatakan dalam mg/ kapsul.
C. Bahan-Bahan Penelitian
Bahan yang digunakan dalam penelitian ini meliputi ampisilin baku
(Brataco Chemika), kapsul ampisilin 500 mg (buatan pabrik tertentu dengan kode
“X”), asetilaseton, formalin, asam asetat 96%, natrium asetat, natrium hidroksida,
asam klorida, dan akuades (Laboratorium Analisis Obat dan Makanan Fakultas
Farmasi UGM). Kecuali dinyatakan lain, bahan-bahan penelitian yang digunakan ada
penelitian ini memiliki kualitas p. a. produksi E. Merck.
30
D. Alat-Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah spektrofotometer
ultraviolet–visibel (Spectronic Genesys 5, MILTON ROY), pH meter (Hanna
Instrument pH 209), neraca analitik (Precisa 125 A. SCS Swiss Quality), mikropipet
Gilson 1000 µl, penangas air, termometer, kertas saring, dan alat-alat gelas yang
lazim.
E. Tatacara Penelitian 1. Pembuatan larutan
a. Pembuatan larutan natrium asetat 0,2 M.
Sebanyak 8,2 g natrium asetat ditimbang seksama, dimasukkan ke dalam labu
ukur 500 ml kemudian dilarutkan dengan akuades sampai tanda.
b. Pembuatan larutan asam asetat 0,2 M.
Sebanyak 11,8 ml asam asetat 96 % dipipet, kemudian diencerkan dengan
akuades sampai volume 1 liter.
c. Pembuatan larutan NaOH 2 M.
Ditimbang seksama 4,0 g NaOH kemudian dilarutkan dalam akuades bebas
CO2 sampai volume 50 ml.
d. Pembuatan larutan HCl 2 M.
Dilarutkan 17 ml HCl pekat dalam 100 ml akuades.
e. Pembuatan larutan pereaksi (Patel et al., 1992).
Sebanyak 16,0 ml natrium asetat 0,2 M dan 34,0 ml asam asetat 0,2 M
menit di atas penangas air dengan suhu 80oC, didinginkan, pH diatur dengan
penambahan larutan NaOH 2 M atau HCl 2 M sampai mencapai pH yang
diinginkan, kemudian diencerkan dengan akuades sampai 100 ml.
f. Pembuatan larutan baku.
Ditimbang seksama 201,7mg baku ampisilin, dilarutkan dengan akuades dan
diencerkan dalam labu ukur 100 ml. Konsentrasi yang diperoleh adalah
0,005M.
2. Optimasi penetapan kadar ampisilin
Oleh karena senyawa yang dianalisis pada penelitian ini berbeda dengan
senyawa yang dianalisis dalam penelitian Patel et al. (1992) maka dilakukan
optimasi yang meliputi :
a. Penetapan operating time.
Sebanyak 4 ml pereaksi pH 4 dimasukkan ke dalam labu ukur 25 ml,
ditambahkan 2,0 ml larutan baku ampisilin 0,005 M. Dipanaskan di dalam penangas
air dengan suhu 35oC, diencerkan dengan akuades sampai tanda. Diukur serapannya
pada panjang gelombang 400 nm sampai diperoleh serapan yang stabil pada rentang
waktu tertentu. Dilakukan penetapan blangko. Operating time adalah rentang waktu
saat larutan menghasilkan serapan yang stabil.
b. Penetapan pH optimum.
pH pereaksi dibuat bervariasi, yaitu pH 3, 4, 5, 6, dan 7 dengan
menambahkan larutan NaOH 2 M atau HCl 2 M. Untuk masing-masing nilai pH
32
larutan baku ampisilin 0,005 M, didiamkan selama operating time di dalam penangas
air dengan suhu 35oC, diencerkan dengan akuades sampai tanda. Diukur serapan
larutan pada panjang gelombang 400 nm. Dilakukan penetapan blangko. Nilai pH
optimum adalah pH pereaksi yang menghasilkan serapan paling besar.
c. Penetapan volume pereaksi optimum.
Larutan pereaksi dengan pH optimum dipipet 1, 2, 3, 4, 5, 6, 7, 8, 9, dan 10
ml, dimasukkan ke dalam labu ukur 25 ml. Pada masing-masing labu ukur tersebut
ditambahkan 2,0 ml larutan baku ampisilin 0,005 M, didiamkan selama operating
time di dalam penangas air dengan suhu 35oC, diencerkan dengan akuades sampai
tanda. Diukur serapan larutan pada panjang gelombang 400 nm, Dilakukan
penetapan blangko. Volume pereaksi optimum adalah volume pereaksi yang
menghasilkan serapan paling besar dan stabil.
d. Penetapan panjang gelombang serapan maksimum.
Sebanyak 1,0; 1,4; dan 1,8 ml larutan baku ampisilin 0,005 M dipipet dan
dimasukkan ke dalam labu ukur 25 ml. Masing-masing labu ukur ditambah dengan
pereaksi pada pH dan volume hasil optimasi. Didiamkan selama operating time di
dalam penangas air dengan suhu 35oC, diencerkan dengan akuades sampai tanda.
Serapan dibaca pada panjang gelombang 300-500 nm. Dilakukan penetapan blangko.
Panjang gelombang serapan maksimum adalah panjang gelombang yang
3. Penetapan kurva baku
Larutan baku ampisilin 0,005 M dipipet sebanyak 0,8; 1,0; 1,2; 1,4; dan 1,6
ml dan dimasukkan ke dalam labu ukur 25 ml. Masing-masing labu ukur ditambah
dengan pereaksi pada pH dan volume hasil optimasi. Didiamkan selama operating
time di dalam penangas air dengan suhu 35oC, diencerkan dengan akuades sampai
tanda. Diukur serapannya pada panjang gelombang serapan maksimum. Dilakukan
penetapan blangko. Dibuat kurva hubungan konsentrasi ampisilin vs serapan
senyawa hasil reaksi antara ampisilin dengan asetilaseton dan formalin dan
ditentukan persamaan garis regresi linier serta koefisien korelasinya.
4. Aplikasi metode spektrofotometri visibel untuk penetapan kadar ampisilin dalam kapsul “X” menggunakan pereaksi asetilaseton dan formalin
a. Pengambilan sampel.
Sampel yang digunakan terdiri dari 1 merek kapsul yang mengandung
ampisilin 500 mg yang beredar di pasaran. Kapsul ampisilin yang dipilih
adalah kapsul dengan nomor batch yang sama sebanyak 20 kapsul.
b. Penetapan kadar ampisilin dalam kapsul ”X”.
Ditimbang seksama sejumlah serbuk dari 20 kapsul yang setara dengan 100,9
mg ampisilin. Dimasukkan ke dalam labu ukur 50 ml, dilarutkan dengan
akuades kemudian diencerkan sampai tanda. Dipipet 1,0 ml, dimasukkan ke
dalam labu ukur 25 ml, ditambah dengan pereaksi pada pH dan volume hasil
optimasi. Didiamkan selama operating time di dalam penangas air dengan
suhu 35oC, diencerkan dengan akuades sampai tanda, diukur serapannya pada
34
ampisilin dalam kapsul “X” dihitung menggunakan persamaan garis regresi
linier yang diperoleh dari penetapan kurva baku ampisilin.
5. Validasi metode spektrofotometri visibel untuk penetapan kadar ampisilin menggunakan pereaksi asetilaseton dan formalin
a. Akurasi.
Ditimbang seksama sejumlah serbuk dari 20 kapsul yang setara dengan 100,9
mg ampisilin. Ditambahkan 100,9 mg baku ampisilin. Dimasukkan ke dalam
labu ukur 100 ml, dilarutkan kemudian diencerkan dengan akuades sampai
tanda. Dipipet 1,0 ml, dimasukkan ke dalam labu ukur 25 ml, ditambah
dengan pereaksi pada pH dan volume hasil optimasi. Didiamkan selama
operating time di dalam penangas air dengan suhu 35oC, diencerkan dengan
akuades sampai tanda. Diukur serapannya pada panjang gelombang
maksimum. Dilakukan penetapan blangko. Akurasi dinyatakan dengan %
perolehan kembali. Dihitung nilai % perolehan kembali (recovery), yaitu
perbandingan kadar ampisilin yang didapat dengan kadar ampisilin
sebenarnya.
b. Presisi.
Presisi dinyatakan dengan koefisien variasi (KV). Dari data hasil penetapan
kadar ampisilin dalam kapsul “X” dihitung nilai KV dari % kadar ampisilin
dalam kapsul untuk tiap replikasi dengan menggunakan kalkulator.
c. Linearitas.
Linearitas ditentukan dari nilai koefisien korelasi (r) yang diperoleh dari
penetapan kurva baku ampisilin. Nilai r hitung tersebut dibandingkan dengan
nilai r tabel dengan derajat bebas (df) = 3 dan taraf kepercayaan 99 %. Selain
itu, linearitas ditentukan juga dari nilai koefisien variasi fungsi (Vx0) yang
diperoleh dengan cara mengolah data hasil penetapan kurva baku ampisilin.
F. Analisis Hasil
Validasi metode analisis yang digunakan dalam penetapan kadar ampisilin
pada penelitian ini dapat ditentukan berdasarkan parameter berikut :
1. akurasi
Akurasi metode analisis dinyatakan dengan % perolehan kembali
(recovery) yang dihitung dengan cara sebagai berikut :
...(11)
% perolehan kembali (recovery) = x 100% sebenarnya
ampisilin kadar
didapat yang
ampisilin kadar
Metode analisis dikatakan memiliki akurasi yang baik bila % perolehan kembali
ampisilin baku berada pada rentang 98-102 % (Yuwono dan Indrayanto, 2005) dan
% perolehan kembali sampel ampisilin berada pada rentang 95-105 % (Mulja dan
Hanwar, 2003).
2. presisi
Presisi metode analisis dinilai berdasarkan KV yang dihitung dengan cara
36
KV = x 100% x
SD
……… (12)
Kadar analit dalam sampel pada penelitian ini adalah 75,96 % sehingga metode
analisis dikatakan memiliki presisi yang baik jika nilai KV kurang dari 2,7 %
(Yuwono dan Indrayanto, 2005).
3. linearitas
Linearitas metode analisis ditentukan berdasarkan nilai r hitung yang
diperoleh dari penetapan kurva baku ampisilin dan berdasarkan nilai Vx0. Jika r
hitung lebih besar dari r tabel dengan df = 3 dan taraf kepercayaan 99 % yaitu 0,959
(Cann, 2003) dan nilai Vx0 ≤ 2 % (Mulja dan Hanwar, 2003) maka metode analisis
BAB IV
HASIL DAN PEMBAHASAN
A. Penetapan Operating Time
Operating time adalah rentang waktu saat suatu larutan menghasilkan
serapan yang stabil. Pada rentang waktu tersebut reaksi antara ampisilin dengan
pereaksi yang menghasilkan senyawa berwarna kuning telah optimum sehingga pada
pengukuran serapan yang terbaca adalah semua ampisilin yang telah bereaksi dengan
pereaksi. Reaksi yang terjadi pada penetapan kadar ampisilin dalam penelitian ini
diawali dengan reaksi antara asetilaseton dan formalin pada pembuatan larutan
pereaksi yang membentuk senyawa 3,5-diasetil-2,6-heptanadion (gambar 6).
Reaksinya adalah :
1. pembentukan enol asetilaseton
H3C C
2. kondensasi enol asetilaseton dengan formalin
38
karbonil tak jenuh a,ß enol asetilaseton H
Gambar 6. Reaksi antara asetilaseton dan formalin
Tahap selanjutnya adalah reaksi antara ampisilin dan
3,5-diasetil-2,6-heptanadion (gambar 7). Hasil reaksi kedua senyawa tersebut adalah senyawa
berwarna kuning. Gugus fungsi pada ampisilin yang bertanggung jawab dalam
pembentukan senyawa berwarna kuning tersebut adalah gugus amin primer. Reaksi
antara ampisilin dan 3,5-diasetil-2,6-heptanadion adalah sebagai berikut :
C
Gugus amin primer ampisilin
40
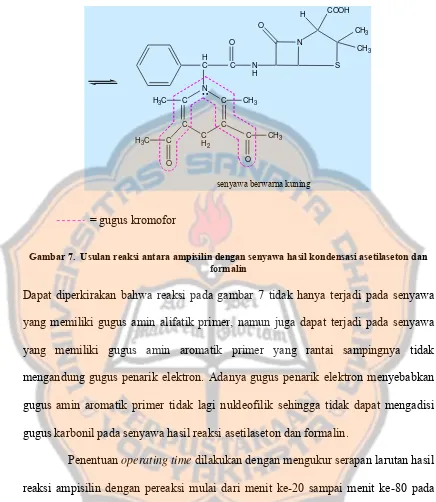
Gambar 7. Usulan reaksi antara ampisilin dengan senyawa hasil kondensasi asetilaseton dan formalin
Dapat diperkirakan bahwa reaksi pada gambar 7 tidak hanya terjadi pada senyawa
yang memiliki gugus amin alifatik primer, namun juga dapat terjadi pada senyawa
yang memiliki gugus amin aromatik primer yang rantai sampingnya tidak
mengandung gugus penarik elektron. Adanya gugus penarik elektron menyebabkan
gugus amin aromatik primer tidak lagi nukleofilik sehingga tidak dapat mengadisi
gugus karbonil pada senyawa hasil reaksi asetilaseton dan formalin.
Penentuan operating time dilakukan dengan mengukur serapan larutan hasil
reaksi ampisilin dengan pereaksi mulai dari menit ke-20 sampai menit ke-80 pada
Tabel IV. Hasil penetapan operating time reaksi antara ampisilin dengan asetilaseton dan formalin
Serapan senyawa hasil reaksi antara ampisilin dengan asetilaseton dan formalin pada λ 400 nm
Waktu inkubasi (menit)
Replikasi I Replikasi II Replikasi III
20 0,438 0,492 0,429
25 0,494 0,544 0,533
30 0,526 0,596 0,555
35 0,549 0,633 0,584
40 0,568 0,653 0,593
45 0,599 0,668 0,610
50 0,600 0,680 0,628
55 0,613 0,687 0,632
60 0,621 0,691 0,645
65 0,649 0,690 0,655
70 0,653 0,702 0,638
75 0,657 0,705 0,639
80 0,661 0,715 0,653
Dari data pada tabel IV diketahui bahwa reaksi ampisilin dengan pereaksi
stabil mulai menit ke-70. Untuk mengetahui stabilitas reaksinya, dilakukan
pengukuran serapan selama 30 menit terhadap larutan hasil reaksi ampisilin dengan
pereaksi yang sudah dipanaskan pada suhu 35oC selama 70 menit. Hasil pengukuran
serapan tersebut tersaji pada gambar 8.
42
Pada gambar 8 terlihat bahwa selama 30 menit serapan larutan tersebut
tetap stabil. Hal tersebut menunjukkan bahwa reaksi ampisilin dengan pereaksi
optimum mulai dari menit ke-70 sampai menit ke-100. Dengan demikian,
pengukuran serapan larutan dapat dilakukan pada menit ke-70 sampai menit ke-100.
Untuk keseragaman, pengukuran serapan selanjutnya dilakukan pada menit ke-70.
B. Penetapan pH Optimum
Reaksi penentu pada penetapan kadar ampisilin dengan pereaksi
asetilaseton dan formalin adalah tahap reaksi adisi nukleofilik dan eliminasi H2O.
Kedua tahap reaksi tersebut tergantung pH sehingga pH memegang peranan penting
agar reaksi antara ampisilin dengan pereaksi dapat berjalan optimum. Menurut
Fessenden and Fessenden (1994), reaksi tersebut optimum pada pH 3 sampai 4. Bila
pH terlalu asam (di bawah pH optimum) maka konsentrasi amin primer bebas
menjadi sangat kecil bahkan dapat diabaikan karena gugus amin primer bebas pada
ampisilin akan bereaksi dengan asam membentuk RNH3+. Reaksinya adalah :
RNH2 + H+ RNH3+
Amin primer pada ampisilin
RNH3+ tidak nukleofilik sedangkan konsentrasi amin primer bebas yang
bersifat nukleofilik sangat kecil sehingga reaksi adisi nukleofilik yang seharusnya
berjalan cepat menjadi lebih lambat. Di sisi lain, pH yang terlalu asam menyebabkan
konsentrasi H+ menjadi besar sehingga gugus OH- akan sangat mudah terprotonkan
menjadi H2O. H2O merupakan gugus pergi yang lebih baik dibanding OH-. Hal ini