SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Gayatri Kusuma Wardani NIM : 068114010
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
VALIDASI METODE PENETAPAN KADAR ASAM URSOLAT DALAM EKSTRAK DAUN BINAHONG (Anredera cordifolia (Ten.) Steenis) DENGAN
METODE KROMATOGRAFI CAIR KINERJA TINGGI
Yang diajukan oleh : Gayatri Kusuma Wardani
068114010
telah disetujui oleh : Pembimbing I
Saat
saat
saat
dan
t aku tak
aku mem t keadaan aku mem t rencana aku mem saat putu aku mem paham ma milih untu mengecew milih untu hidupku milih untu
us asa me
Nama : Gayatri Kusuma Wardani Nomor Mahasiswa : 068114010
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
“Validasi Metode Penetapan Kadar Asam Ursolat dalam Ekstrak Daun Binahong (Anredera cordifolia (Ten.) Steenis) Dengan Metode Kromatografi Cair Kinerja Tinggi”
Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal 21 Juni 2010 Yang menyatakan
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 21 Juni 2010
Penulis
berkat, rahmat, dan bimbingan-Nya sehingga Penulis dapat menyelesaikan skripsi
yang berjudul “Validasi Metode Penetapan Kadar Asam Ursolat dalam Ekstrak Daun Binahong (Anredera cordifolia (Ten.) Steenis) Dengan Metode Kromatografi Cair Kinerja Tinggi”. Skripsi ini disusun untuk memenuhi persyaratan dalam penyelesaian studi untuk meraih gelar Sarjana Farmasi di
Universitas Sanata Dharma Yogyakarta.
Keberhasilan penelitian ini tidak lepas dari bantuan dan perhatian
orang-orang di sekitar Penulis, baik secara materi maupun emosional. Untuk itu pada
kesempatan ini Penulis ingin menyampaikan terima kasih kepada beberapa pihak
yang telah member dukungan di dalam penyelesaian skripsi ini, antara lain :
1. Ipang Djunarko, M. Sc., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta yang telah membantu dalam proses penyusunan
skripsi ini.
2. Lucia Wiwid Wijayanti, M. Si, selaku dosen pembimbing yang dengan sabar
telah membimbing, memberi dukungan, gagasan, dan kritik yang sangat berarti
dalam proses penyusunan skripsi ini.
3. Yohanes Dwiatmaka, M. Si., selaku dosen penguji yang telah memberi bantuan
memberi bantuan dan dukungan yang sangat berarti bagi Penulis.
6. Bapak dan Ibuku, Cosmas Bambang Subiyanto dan Gayatri Gunartin, atas
segala kasih sayang, doa, perhatian, perjuangan, dan dukungan dalam setiap
langkah hidupku.
7. Mas Ottok, Mas Bimo, Mas Parlan, Mas Kunto, Mas Sigit, Mas Wagiran, dan
Pak Timbul yang telah banyak membantu terselesainya penelitian.
8. B. Kris Mantoro, atas kehadirannya yang telah mewarnai hidupku, juga atas
dukungan dan semangat yang diberikan selama ini.
9. Robertus Satrio Wibisono, atas dukungan, kebersamaan, dan perjuangan yang
menyenangkan, menyedihkan, dan mengharukan selama penelitian dan
penyusunan skripsi ini.
10. Saudara-saudaraku di kost Pasadena, Maria Laksmi Parahita, Anastasia
Aprilistyawati, Maria Evangeli, Dewi Prasetyaningrum, Widya
Kusumawardani, dan Swastika Maharani atas keceriaan, kebersamaan, dan
dukungan yang telah diberikan selama ini.
11. Sahabat-sahabatku, Maria Yolanda, Veronika Yuni Candra Sari, Laurensia
Utami Susanti, Rr. Kusumowardani, Adhitya Eka Prasetya, Efrinita Nur
dapat disebutkan satu per satu atas doa dan dukungannya.
Dengan segala kerendahan hati Penulis menyadari bahwa skripsi ini tidak
sempurna, oleh karena itu Penulis akan menerima kritik, koreksi, dan saran dari
berbagai pihak guna menjadikan skripsi ini lebih baik. Pada akhirnya, Penulis
untuk mengetahui apakah metode kromatografi cair kinerja tinggi fase terbalik memenuhi parameter validasi metode analisis yang meliputi akurasi, presisi, linearitas, LOD, dan LOQ jika digunakan untuk penetapan kadar asam ursolat dan untuk mengetahui apakah metode kromatografi cair kinerja tinggi fase terbalik dapat diaplikasikan untuk penetapan kadar asam ursolat dalam ekstrak daun binahong.
Penelitian ini merupakan penelitian non eksperimental deskriptif. Analisis menggunakan metode kromatografi cair kinerja tinggi fase terbalik dengan menggunakan fase diam kolom C18 dan fase gerak campuran metanol:ortophosphoric acid 1% (90:10) dengan kecepatan alir 0.6 ml/menit. Kesahihan metode diukur dengan nilai akurasi, presisi, linearitas, LOD, dan LOQ.
Hasil dari penelitian menunjukkan bahwa metode kromatografi cair kinerja tinggi fase terbalik merupakan metode yang valid untuk menentukan kadar asam ursolat. Hasil penelitian menunjukkan bahwa metode memiliki linearitas yang baik dengan nilai r sebesar 0.999995. Recovery dan CV untuk volume injek 2,0; 6,0; dan 10,0 µl berturut-turut adalah 104.413%, 0.05%; 105.931%, 0.01%; dan 107.909%, 0.02%. Nilai LOD dan LOQ berturut-turut adalah 3.117x10-3 dan 0.0104.
using the high performance liquid chromatography method. The purposes of this research are to know whether the reverse phase high performance liquid chromatography method accomplishes the validation parameters of the analytical method including accuration, precision, linearity, LOD, and LOQ if it is used for the establisment of ursolic acid content and to know whether the reverse phase high performance liquid chromatography method can be applied to the establisment of ursolic acid content in the extract of binahong leaves.
This research is a non-experimental descriptif research. The analysis uses the reverse phase high performance liquid chromatography method using the C18 column stationary phase and the mobile phase of mixed methanol: ortophosphoric acid 1% (90:10) with the flow rate 0,6 ml/second. The validity of method is measured using the rate of accuration, precision, linearity, LOD, and LOQ.
The result of this research shows that the reverse phase high performance liquid chromatography method is the valid method to determine the ursolic acid content. The result of this research shows that the method has good linearity with the rate r in the amount of 0,999995. Recovery and CV for the inject volume 2,0; 6,0; and 10,0 µl in sequence are 104,413 %, 0,05%; 105,931%, 0,01%; and 107,909%, 0,02%. The LOD and LOQ rates in sequence are 3,117x10-3 and 0,0104.
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PULIKASI ... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA ... vii
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xvii
BAB I. PENDAHULUAN A.Latar Belakang ... 1
B.Rumusan Masalah ... 3
C.Keaslian penelitian ... 3
D.Manfaat penelitian ... 4
a. Manfaat Praktis ... 4
A.Binahong ... 5
B.Asam Ursolat ... 6
C.Ekstraksi Simplisia ... 7
a. Simplisia ... 7
b. Ekstrak ... 7
c. Ekstraksi ... 7
D.Kromatografi Cair Kinerja Tinggi ... 8
E. Parameter Validasi Metode Analisis ... 18
a. Parameter Metode Analisis ... 18
b. Kategori Metode Analisis ... 22
c. Kesalahan Dalam Analisis ... 23
F. Landasan Teori ... 24
G.Hipotesis ... 25
BAB III. METODOLOGI PENELITIAN A.Jenis Penelitian ... 26
B.Variabel Operasional ... 26
C.Alat-alat Penelitian ... 27
D.Bahan-bahan Penelitian ... 27
B.Penetapan Kurva Baku ... 37
C.Penyiapan Sampel ... 39
D.Analisis Kualitatif ... 41
E. Validitas Metode ... 46
a. Akurasi ... 46
b. Presisi ... 47
c. Linearitas ... 48
d. Limit of Detection (LOD) dan Limit of Quantitation (LOQ) ... 48
BAB V. KESIMPULAN DAN SARAN A.Kesimpulan ... 50
B.Saran ... 50
DAFTAR PUSTAKA ... 51
LAMPIRAN ... 55
Tabel II. Kriteria Penerimaan Akurasi Pada Konsentrasi Analit Yang
Berbeda ... 19
Tabel III. Kriteria Penerimaan Presisi Pada Konsentrasi Analit Yang
Berbeda ... 20
Tabel IV. Parameter Validasi Yang Dipersyaratkan Untuk Validasi
Metode Analisis ... 23
Tabel V. Hasil Penetapan Kurva Baku Asam Ursolat ... 38
Tabel VI. Hasil Perhitungan Recovery ... 47
Tabel VII. Hasil Perhitungan Kesalahan Sistemik dan Kesalahan Acak ... 47
Tabel VIII. Penimbangan Baku Asam Ursolat 90% ... 55
Gambar 2. Struktur Kimia Asam Ursolat ... 6
Gambar 3. Skema Alat Kromatografi Cair Kinerja Tinggi ... 8
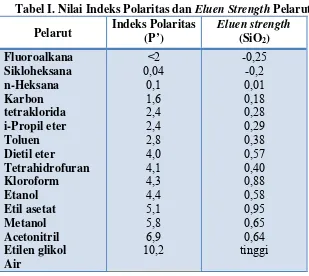
Gambar 4. Difusi Eddy ... 13
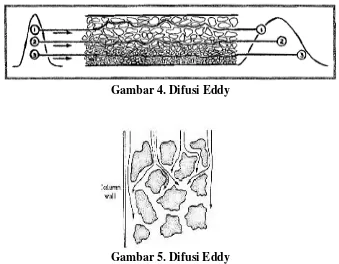
Gambar 5. Difusi Eddy ... 13
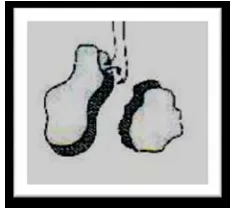
Gambar 6. Transfer Massa Fase Diam ... 14
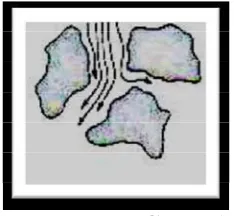
Gambar 7. Transfer Massa Fase Gerak ... 15
Gambar 8. Gugus Polar Asam Ursolat ... 36
Gambar 9. Gugus Non Polar Asam Ursolat ... 36
Gambar 10. Interaksi Hidrogen Antara Asam Ursolat Dengan Fase Gerak Metanol Dalam Fase Gerak ... 37
Gambar 11. Kurva Hubungan Antara Massa Baku Asam Ursolat Dengan AUC ... 39
Gambar 12. Kromatogram Standar Asam Ursolat ... 43
Gambar 13. Kromatogarm Sampel ... 44
Ursolat ... 55
Lampiran 2. Hasil Perhitungan Recovery, Kesalahan Sistemik, dan
Kesalahan Acak ...
Lampiran 3. Perhitungan LOD dan LOQ ... 63
Lampiran 4. Penimbangan daun binahong (Anredera cordifolia (Ten.)
Steenis) ... 64
Lampiran 5. Penimbangan rendemen ekstrak daun binahong (Anredera
cordifolia (Ten.) Steenis) ... 64
A. Latar Belakang Penelitian
Tanaman binahong (Anredera cordifolia (Ten.) Steenis) dikenal memiliki
khasiat dalam pengobatan. Binahong disebutkan mempunyai kandungan kimia seperti
asam oleanolat, asam askorbat, dan ancordin (Lazuardhi, 2009). Penelitian-penelitian
sebelumnya lebih banyak membahas kandungan asam oleanolat dalam tanaman
binahong dan belum membuktikan adanya kandungan asam ursolat dalam ekstrak
daun binahong. Asam oleanolat dan asam ursolat merupakan senyawa golongan
triterpen pentasiklik, yang membedakan keduanya hanyalah posisi gugus metil pada
atom karbon nomor 19 dan 20 (Olszewska, 2008). Posisi gugus metil pada asam
oleanolat terletak pada atom karbon nomor 19, sedangkan pada asam ursolat, gugus
metil terletak pada atom karbon nomor 20. Inilah yang menyebabkan kepolaran di
antara kedua senyawa tersebut tidak jauh berbeda. Aktivitas antara kedua senyawa
tersebut juga tidak jauh berbeda, seperti antiinflamasi, antioksidan, dsb.
Menurut Wojciak dan Korsior (2007), asam oleanolat, asam ursolat, dan
asam betulinat dapat dijumpai pada folium Salviae, folium Plantaginis lanceolatae,
dan flos Lamii albi. Berdasarkan hal tersebut, dapat diperkirakan bahwa tanaman
yang mengandung senyawa asam oleanolat dimungkinkan mengandung pula asam
ursolat. Hal ini dikarenakan asam oleanolat merupakan isomer dari asam ursolat,
Pada penelitian sebelumnya, asam ursolat biasa dijumpai pada tanaman ceri
hitam (Prunus serotina Ehrh.), Eriobotrya japonica, Rosmarinus officinalis, dan
Glechoma hederaceae (Cha, 1996). Beberapa penelitian menunjukkan bahwa asam
ursolat memiliki aktivitas yang berguna dalam bidang pengobatan, seperti
antiinflamasi, antitumor, antikanker, anti HIV, antioksidan, antiinvasif, antiulcer,
antiarterosklerosis, hepatoprotektif, gastroprotektif, antihiperlipidemia, dsb (Liao,
2005). Bahkan saat ini sedang dikembangkan sediaan kosmetik anti aging yang
menggunakan garam asam ursolat sebagai bahan aktifnya (Anonim, 2009).
Metode kromatografi cair kinerja tinggi adalah metode yang dipilih untuk
digunakan dalam analisis asam ursolat. Namun belum diketahui apakah metode ini
memiliki validitas yang baik atau tidak apabila diaplikasikan pada penetapan kadar
asam ursolat dalam ekstrak daun binahong. Dari penelitian ini diharapkan dapat
diperoleh metode penetapan kadar asam ursolat menggunakan kromatografi cair
B. Rumusan Masalah
Berdasarkan latar belakang dapat dirumuskan permasalahan sebagai
berikut :
a. Apakah metode kromatografi cair kinerja tinggi fase terbalik memenuhi
parameter validasi metode analisis yang meliputi akurasi, presisi, linearitas,
LOD, dan LOQ jika digunakan dalam penetapan kadar asam ursolat?
b. Apakah metode kromatografi cair kinerja tinggi fase terbalik dapat
diaplikasikan untuk menetapkan kadar asam ursolat dalam ekstrak daun
binahong?
C. Keaslian Karya
Sejauh pengetahuan penulis, penelitian dengan menggunakan tanaman binahong
sudah cukup banyak dilakukan di Indonesia, antara lain :
1. Formulasi Gel Antiluka Ekstrak Daun Binahong (Anredera baselloides
(Ten.) Steenis) dengan Basis Carbopol (Setyaningretry, 2007).
2. Optimasi Formula Span 80 dan Tween 80 dalam cold cream Obat Luka
Ekstrak Daun Binahong (Anredera cordifolia (Ten.) Steenis) dengan Metode
Simplex Lattice Design (Paramita, 2008).
Namun penelitian terkait kandungan asam ursolat dalam ekstrak daun binahong
D. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat sebagai
berikut:
a. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi
apakah metode kromatografi cair kinerja tinggi fase terbalik valid untuk
menentukan kadar asam ursolat dalam ekstrak daun tanaman binahong
(Anredera cordifolia (Ten,) Steenis).
b. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan informasi
tentang validasi metode kromatografi cair kinerja tinggi fase terbalik untuk
penetapan kadar asam ursolat.
E. Tujuan Penelitian
1. Untuk mengetahui apakah metode kromatografi cair kinerja tinggi fase terbalik
memenuhi parameter validasi metode analisis yang meliputi akurasi, presisi,
linearitas, LOD, dan LOQ jika digunakan untuk penetapan kadar asam ursolat.
2. Untuk mengetahui apakah metode kromatografi cair kinerja tinggi fase terbalik
dapat diaplikasikan untuk penetapan kadar asam ursolat dalam ekstrak daun
BAB II
TINJAUAN PUSTAKA
A. Binahong
Tanaman binahong (Anredera cordifolia (Ten.) Steenis) yang termasuk
dalam famili Basellaceae berupa tumbuhan menjalar, berumur panjang (perenial), dan
bisa mencapai panjang ± 5 m. Batangnya lunak, berbentuk silindris, saling membelit,
dan berwarna merah. Daun tanaman ini bertangkai sangat pendek (subsessile),
susunannya berseling, berwarna hijau, dan berbentuk jantung (cordata). Bunganya
majemuk berbentuk tandan, bertangkai panjang, muncul di ketiak daun. Akarnya
berbentuk rimpang, berdaging lunak. Binahong merupakan tanaman asli daerah
Amerika Selatan. Tanaman ini tumbuh baik di cuaca tropis dan sub-tropis.
Berkembang secara generatif (biji), namun lebih sering dikembangbiakkan secara
vegetatif melalui akar rimpangnya. (Hidayati, 2009).
Gambar 1. Binahong
Tanaman binahong (Anredera cordifolia (Ten.) Steenis) memiliki beberapa
nama lain, antara lain Boussingaultia gracilis Miers, Boussingaultia cordifolia,
Boussingaultia baselloides (Hidayati, 2009).
Dalam tanaman binahong terdapat beberapa kandungan kimia, seperti asam
oleanolat, asam askorbat, fenol, minyak atsiri, ancordin, dsb (Lazuardhi, 2009).
B. Asam Ursolat
O
CH3 CH3
CH3 C CH3 CH3 O OH H H CH3 H3C
H
H
C30H48O3
Gambar 2. Struktur Kimia Asam Ursolat
Asam ursolat merupakan golongan senyawa triterpen pentasiklik (Wojciak
dan Korsior, 2007). Senyawa ini dapat ditemui pada tumbuhan apel, basil, bilberries,
cranberries, elder flower, peppermint, rosemary, lavender, oregano, thyme, hawthorn,
prunes, Prunus serotina Ehrh., dsb (Olszewska, 2008). Senyawa ini mempunyai berat
Asam ursolat dikenal mempunyai berbagai macam khasiat, seperti
antiinvasif, antiinflamasi. antiulcer, antiaterosklerosis, dan hepatoprotektif (Liao,
2005). Selain itu, asam ursolat juga mempunyai khasiat sebagai antitumor, anti-HIV,
antimikroba, antifungi, gastroprotektif, dan antihiperlipidemia (Wojciak dan Korsior,
2007). Selain dalam bidang pengobatan, asam ursolat juga sering digunakan dalam
kosmetik sebagai anti(photo)aging dalam bentuk garam (Anonim, 2010).
C. Ekstraksi Simplisia 1. Simplisia
Simplisia adalah bahan alam yang digunakan sebagai obat yang belum
mengalami pengolahan apapun kecuali pengeringan. Ada 3 macam simplisia yaitu
simplisia nabati, simplisia hewani, dan simplisia mineral. Simplisia nabati adalah
simplisia yang berupa tanaman utuh, bagian tanaman,dan eksudat tanaman (Anonim,
1979).
2. Ekstrak
Ekstrak adalah sediaan kering, kental, atau cair dibuat dengan menyari
simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya
matahari langsung (Anonim, 1979). Ekstrak cair adalah sediaan dari simplisia nabati
yang mengandung etanol sebagai pelarut atau sebagai pengawet (Hidayati, 2009).
3. Ekstraksi
Ekstraksi atau penyarian merupakan pemindahan massa zat aktif yang
pelarutan zat aktif dalam cairan penyari (Hidayati, 2009). Metode penyarian dipilih
berdasarkan zat aktif yang terkandung dalam simplisia dan stabilitas zat aktif tersebut
dalam cairan penyari (Anonim, 1986).
D. Kromatografi Cair Kinerja Tinggi
Kromatografi cair kinerja tinggi adalah suatu sistem kromatografi yang fase
geraknya dialirkan dengan cepat dengan bantuan pompa dan hasilnya dideteksi
dengan detektor (Gritter et al., 1985). Tujuan analisis dengan KCKT yaitu
didapatkannya pemisahan yang baik dalam waktu yang relatif singkat (Mulja, 1995).
Gambar 3. Skema Alat Kromatografi Cair Kinerja Tinggi
(Kazakevich dan Mc Nair, 1996)
Berdasarkan sistem peralatannya maka KCKT termasuk kromatografi kolom
karena dipakai fase diam yang ter-packing di dalam kolom, sedangkan berdasarkan
proses pemisahannya KCKT digolongkan sebagai kromatografi partisi dan
antara dua pelarut yang tidak bercampur yang ada pada fase diam dan fase gerak.
Fase diam (polar atau non polar) disalutkan pada penyangga dan dikemas ke dalam
kolom. Jika linarut ditambahkan ke dalam sistem yang terdiri atas dua pelarut yang
tidak bercampur dan keseluruhan sistem dibiarkan setimbang, linarut akan tersebar
antara dua fase menurut persamaan : K =
Cm Cs
K adalah koefisien distribusi dan Cs dan Cm adalah konsentrasi linarut berturut-turut
dalam fase diam dan fase gerak (Johnson dan Stevenson, 1978).
Pada kromatografi fase terbalik, fase diamnya bersifat non polar, biasanya
digunakan hidrokarbon dan fase geraknya relatif bersifat polar seperti air, metanol
atau asetonitril (Skoog et al., 1994).
Kolom yang biasa digunakan pada kromatografi partisi fase terbalik adalah
kolom dengan kemasan fase terikat, yang bersifat stabil karena fase diamnya terikat
secara kimia pada penyangga, sehingga tidak mudah terbawa oleh fase gerak.
Penyangga pada kemasan fase terikat biasanya terbuat dari silika yang sudah
diseragamkan, berpori, dan umumnya partikel mempunyai diameter 3,5 atau 10 µm
(Skoog et al., 1998).
KCKT fase terbalik menggunakan fase diam yang berupa senyawa organik,
dimana senyawa organik ini terikat secara kimia dengan gugus silanol pada
permukaan silika. Hal ini yang menyebabkan permukaan silika menjadi bersifat non
polar. Dalam kromatografi jenis ini, senyawa lebih polar terelusi lebih dahulu,
Fase diam yang biasa digunakan pada kromatografi partisi fase terbalik
adalah oktadesilsilan (ODS). Selain ODS, dikenal pula silika dengan substitusi oktil
(C8). Panjang pendeknya rantai karbon mempengaruhi tertambatnya senyawa pada
fase diam. Kolom dengan rantai panjang bersifat retensif, sehingga senyawa yang
mempunyai sifat mirip dengan kolom akan tertambat lebih lama (Munson, 1991).
Fase gerak merupakan salah satu faktor yang mempengaruhi pemisahan.
Berbagai macam pelarut atau fase gerak digunakan dalam sistem KCKT, tetapi ada
beberapa sifat yang perlu diperhatikan yaitu, fase gerak yang digunakan harus murni
tanpa cemaran, sesuai dengan detektor, dapat melarutkan cuplikan, memiliki
viskositas yang rendah dan memungkinkan memperoleh kembali cuplikan dengan
mudah jika diperlukan (Johnson and Stevenson, 1991).
Kepolaran pelarut merupakan ukuran kekuatan pelarut atau kemampuan
pelarut untuk mengelusi suatu senyawa. Kandungan utama fase gerak pada
kromatografi fase terbalik adalah air. Pelarut yang dapat campur dengan air seperti
metanol, etanol, asetonitril, dioksan, tetrahidrofuran, dan dimetilformamida
ditambahkan untuk mengatur kepolaran fase gerak (Munson, 1991).
Polaritas fase gerak dalam KCKT sangat mempengaruhi kromatogram yang
dihasilkan, sehingga perlu diperhitungkan komposisi campuran pelarut yang akan
digunakan. Berdasarkan nilai P’(indeks polaritas), maka besarnya polaritas campuran
pelarut dapat dihitung dengan persamaan berikut :
Nilai Pcampuran adalah polaritas campuran, P’ menyatakan indeks polaritas,
merupakan fraksi pelarut dalam campuran dan n adalah jenis pelarut yang digunakan
(Skoog, 1985).
Berikut ini adalah daftar pelarut berikut nilai indeks polaritas dan eluen
strength dari beberapa pelarut (Skoog et al.., 1985).
Tabel I. Nilai Indeks Polaritas dan Eluen Strength Pelarut
Eluen strength merupakan ukuran kemampuan fase gerak menarik analit dari
fase diam. Waktu retensi analit akan turun jika digunakan fase gerak dengan eluen
strength rendah, sebaliknya waktu retensi analit akan meningkat jika digunakan fase
gerak dengan eluen strength tinggi (Snyder et al.., 1997).
Keberhasilan atau kegagalan analisis tergantung pada pemilihan kolom dan
kondisi kerja yang tepat. Ukuran kinerja kolom dapat dilihat dari kemampuan kolom Pelarut Indeks Polaritas (P’) Eluen strength (SiO
N L HETP
H = =
dalam memisahkan senyawa (Johnson dan Stevenson, 1978). Batasan yang paling
sering digunakan yaitu bilangan lempeng teoritik dan faktor resolusi (Munson, 1991).
1. Teori Lempeng (Plate Theory)
Salah satu ukuran kinerja kolom adalah jumlah lempeng teoritik yang
dihitung dengan persamaan:
16 5,54
Nilai w adalah lebar alas, w1/2 adalah lebar alas puncak pada setengah tinggi
puncak, dan tR adalah waktu retensi (Sastrohamidjojo, 2001).
Jumlah pelat teori berbanding lurus dengan panjang kolom. Karena
panjang kolom bermacam-macam, maka diperlukan ukuran efisiensi kolom yang
tidak bergantung pada panjang kolom. Tinggi atau jarak yang setara dengan pelat,
H atau Height Equivalent to a Theoritical Plate (HETP), merupakan ukuran
efisiensi kolom yang lebih disukai karena memungkinkan perbandingan antara
kolom yang panjangnya berlainan. H berkaitan dengan jumlah pelat teori menurut
persamaan berikut:
L menunjukkan panjang kolom biasanya dalam mm, dan N menunjukkan jumlah
2. Teori Laju (Rate Theory)
Pada waktu migrasi, analit mengalami transfer antara fase diam dan fase
gerak berkali-kali. Waktu tinggal pada fase diam maupun fase gerak tidak teratur
dan tergantung pada tersedianya energy termal dari lingkungannya yang
memungkinkan transfer tersebut. Analit hanya dapat bergerak bila berada dalam
fase gerak, sehingga migrasi di dalam kolom tidak teratur. Hal ini mengakibatkan
laju rata-rata analit relatif terhadap fase gerak bervariasi sehingga terjadi pelebaran
puncak analit. Faktor-faktor utama penyebab terjadinya pelebaran puncak yaitu:
a. Difusi Eddy, merupakan aliran tidak teratur yang menyebabkan
terjadinya pencampuran konvektif. Difusi Eddy disebabkan oleh banyak
kemungkinan pada kemasan kolom yang kurang baik.
Gambar 4. Difusi Eddy
Gambar 4 dan 5 menunjukkan proses terjadinya difusi Eddy. Nomor 1
menunjukkan analit yang keluar lebih dahulu karena melewati kolom dengan
partikel berukuran besar dan kurang kompak. Nomor 2 menunjukkan analit keluar
lebih lambat dari nomor 1 karena ukuran partikel yang lebih kecil dan lebih
kompak daripada nomor 1. Nomor 3, analit keluar paling akhir, hal ini terjadi
karena melewati bagian kolom dengan ukuran partikel halus dan kompak.
b. Difusi Longitudinal, merupakan efek dari gerakan random molekul
analit dalam fase gerak karena adanya perbedaan konsentrasi.
c. Transfer massa non-ekuillibrium, merupakan efek laju ekuilibrasi
analit di antara fase gerak dan fase diam yang terbatas. Hal ini terjadi karena pada
umumnya aliran fase gerak terlalu cepat untuk mendapatkan ekuilibrium antara
kedua fase (Noegrohati, 1994).
Transfer massa dinyatakan dengan nilai Cstasionery dan Cmobile. Cstasionery merupakan
hasil dari ditahannya solut karena adanya fase diam. Suatu molekul bergerak
lambat dalam fase diam, sementara molekul lainnya melaju melalui kolom
bersama dengan fase gerak. Untuk mengatasi hal ini diperlukan fase diam yang
lebih encer (tidak terlalu kental). Peristiwa ini dapat digambarkan sebagai berikut :
Cmobile menggambarkan adanya peristiwa di mana solut dalam fase diam bertemu
dengan fase gerak yang masih baru. Hal ini dapat digambarkan sebagai berikut :
Gambar 7. Transfer Massa Fase Gerak (Willard et al., 1988) Hubungan antara ketiga faktor dapat digambarkan dengan persamaan Van
Deemter :
. .
A = difusi Eddy
B = difusi longitudinal
C = transfer massa non-ekuilibrium
= rata-rata flow rate linear fase gerak
H = HETP (Noegrohati,1994)
Faktor resolusi adalah ukuran pemisahan dari dua puncak. Daya pisah
(Rs) dapat diukur dengan persamaan:
2 1 2 1 1 2 2 ) )( 2 / 1 ( ) ( w w t w w t t
Rs R R
Nilai tR2 dan tR1 adalah waktu retensi senyawa, diukur pada titik maksimum
puncak dan Δt adalah selisih antara tR2 dan tR1. Nilai w2 dan w1 adalah lebar alas
puncak dinyatakan dalam satuan waktu.
Untuk memperbaiki resolusi dapat dinyatakan dengan parameter-parameter
sebagai berikut:
Berdasarkan rumus tersebut terlihat bahwa resolusi merupakan fungsi dari 3
faktor, yaitu selektivitas kolom yang tergantung pada α, faktor kapasitas yang
tergantung pada nilai k’ dan faktor efisiensi yang tergantung pada nilai N
(Noegrohati, 1994).
Hasil pemisahan ditunjukkan pada kromatogram dan selanjutnya dapat
ditentukan waktu retensi atau waktu tambat (tr) yang dapat digunakan untuk
mengidentifikasi senyawa. Tr adalah selang waktu yang diperlukan oleh linarut mulai
pada saat injeksi sampai keluar dari kolom dan sinyalnya ditangkap oleh detektor.
Waktu retensi ini bersifat khas untuk senyawa tertentu. Beberapa mungkin
mempunyai waktu retensi yang berdekatan, tetapi setiap senyawa hanya memiliki
satu waktu retensi saja, karena setiap senyawa memiliki harga K (koefisien distribusi)
yang spesifik (Mulja, 1995).
Kualitas pemisahan KCKT dapat ditentukan dengan resolusi dan waktu
dua dan waktu pemisahannya singkat. Resolusi dapat ditentukan dengan tiga
parameter yang secara langsung berhubungan dengan kondisi percobaan, yaitu faktor
pemisahan, jumlah lempeng teoritis, dan rata-rata faktor retensi antara dua peak yang
berdekatan (faktor kapasitas).
Parameter faktor pemisahan dan faktor kapasitas ditentukan dengan
beberapa kondisi yang mempengaruhi waktu retensi atau kesetimbangan distribusi
antara sampel dengan fase diam dan sampel dengan fase gerak, yaitu :
1. Komposisi fase diam
2. Komposisi fase gerak
3. Temperatur
Jumlah lempeng teoritis dapat ditingkatkan dengan beberapa faktor, yaitu :
1. Kualitas kolom yang baik (ter-packing dengan baik)
2. Kolom yang lebih panjang
3. Kecepatan alir yang lebih lambat
4. Makin kecil partikel dalam kolom
5. Viskositas fase gerak yang lebih rendah dan temperatur yang lebih tinggi
6. Molekul sampel yang lebih kecil
7. Efek ekstra kolom yang minimum.
Bentuk peak sama pentingnya dalam perkembangan metode KCKT. Kolom
dan kondisi percobaan yang menghasilkan peak yang simetris selalu dipilih. Peak
yang asimetris dapat terjadi karena antara lain jumlah sampel yang berlebihan,
menyebabkan pengekoran atau peak yang asimetris harus dihindari, karena dapat
menyebabkan pemisahan yang buruk dan menurunkan presisi, serta menurunkan
kemampuan untuk pengukuran setiap peak secara akurat.
Detektor yang paling sering digunakan selama perkembangan metode KCKT
adalah detektor UV. Pemilihan detektor yang tepat dapat meningkatkan selektivitas
dan sensitivitas serta mengurangi baseline noise (Snyder, 1997).
E. Parameter Validasi, Kategori Metode, dan Kesalahan dalam Analisis 1. Parameter Validasi Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter
tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis antara lain:
a. Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat
kedekatan hasil analisis dengan kadar analit yang sebenarnya. Akurasi dinyatakan
dengan persen perolehan kembali (recovery) analit yang ditambahkan (Harmita,
2004).
Kriteria % perolehan kembali yang diijinkan pada setiap konsentrasi
Tabel II. Kriteria Penerimaan Akurasi Pada Konsentrasi Analit Yang Berbeda
Analit pada sampel (%)
Rata-rata yang diperoleh (%) 100 98-102 >10 98-102 >1 97-103 >0.1 95-105 0.01 90-107 0.001 90-107
0.0001 (1 ppm) 80-110
0.00001 (100 ppb) 80-110
0.000001 (10 ppb) 60-115
0.0000001 (1 ppb) 40-120
(Harmita, 2004)
Akurasi untuk kadar obat yang besar adalah 95-105%, sedangkan untuk bioanalisis
rentang 80-120% masih bisa diterima (Mulja dan Hanwar, 2003).
b. Presisi
Presisi adalah ukuran yang menunjukkan derajat kesesuaian antara hasil
uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
prosedur diterapkan secara berulang-ulang pada sampel-sampel yang diambil dari
campuran yang homogen (Harmita, 2004).
Presisi dinyatakan dalam koefisien variasi (KV). Suatu metode dapat
dikatakan baik apabila memiliki KV < 2% (Harmita, 2004).
Presisi terdiri dari 3 macam, yaitu (Anonim, 1995) :
1) Reproducibility, adalah keseksamaan metode bila analisis dikerjakan
2) Intermediate precision, adalah keseksamaan metode bila analisis
dikerjakan di laboratorium yang sama pada hari yang berbeda atau analis yang
berbeda atau peralatan yang berbeda.
3) Repeatibility, adalah keseksamaan metode jika analisis dilakukan oleh
analis yang sama dengan peralatan yang sama pada interval waktu yang pendek.
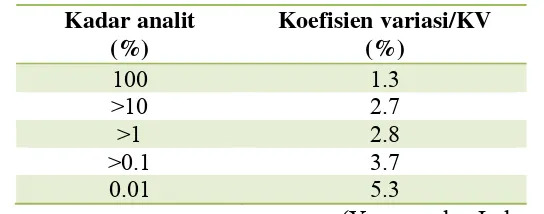
Tabel III. Kriteria Penerimaan Presisi Pada Konsentrasi Analit Yang Berbeda
Kadar analit (%)
Koefisien variasi/KV (%)
100 1.3
>10 2.7
>1 2.8
>0.1 3.7
0.01 5.3
(Yuwono dan Indrayanto, 2005)
Untuk bioanalisis, nilai KV 15-20% masih dapat diterima (Mulja dan Hanwar,
2003).
c. Linearitas dan rentang
Linearitas merupakan kemampuan suatu metode (pada rentang tertentu)
untuk mendapatkan hasil uji yang secara langsung proposional dengan konsentrasi
analit di dalam sampel. Rentang adalah jarak antara level terbawah dan teratas dari
metode analisis yang telah dipakai untuk mendapatkan presisi, akurasi dan
linieritas yang bisa diterima (Anonim, 2007).
d. Spesifitas
Spesifitas merupakan karakteristik terpenting dari suatu metode dan harus
kemampuan suatu metode untuk mengukur dengan akurat respon analit di antara
seluruh komponen sampel potensial yang mungkin ada dalam matriks sampel
(Mulja dan Hanwar, 2003).
e. Limit of Detection (LOD)
LOD adalah konsentrasi analit terendah dalam sampel yang masih dapat
diukur pada kondisi percobaan tertentu tetapi tidak perlu secara kuantitatif.
Penentuan LOD pada metode instrumental dapat didasarkan pada signal to noise
ratio yaitu dengan cara membandingkan hasil pengukuran analit yang telah
diketahui konsentrasinya terhadap respon blangko. Konsentrasi analit yang mampu
memberikan respon 2-3 kali respon blangko inilah yang kemudian ditetapkan
sebagai LOD. Penentuan LOD dapat pula didasarkan pada standar deviasi yang
diperoleh dari pengukuran sejumlah blangko yang kemudian dikalikan dengan
faktor sebesar 2 atau 3 (Anonim, 1995).
f. Limit of Quantitation (LOQ)
LOQ adalah konsentrasi terendah dari analit dalam sampel yang masih
dapat dianalisis dengan presisi dan akurasi yang baik pada kondisi percobaan
tertentu dari suatu metode. LOQ merupakan parameter uji kuantitatif untuk
senyawa berkadar rendah dalam sampel yang mengandung bahan-bahan lainnya
seperti bahan pengotor dalam serbuk obat dan hasil degradasi dari suatu produk
obat jadi. Penentuan LOQ pada metode instrumental biasanya didasarkan pada
standar deviasi yang diperoleh dari pengukuran sejumlah blangko yang kemudian
g. Sensitivitas
Sensitivitas merupakan kemampuan metode untuk mengidentifikasi
perbedaan yang kecil antar konsentrasi analit. Faktor yang mempengaruhi
sensitivitas ini adalah kemiringan dari kurva baku dan presisi, misalkan terdapat
dua metode analisis dengan tingkat presisi yang sama akan tetapi kemiringan
kurva baku keduanya berbeda maka metode yang lebih sensitif adalah metode
yang mempunyai kemiringan kurva baku yang lebih curam, begitu juga sebaliknya
(Skoog, 1985).
h. Range
Range adalah interval antara konsentrasi terendah sampai konsentrasi
tertinggi dari analit yang dapat diukur secara kuantitatif menggunakan metode
analisis tertentu dan menghasilkan akurasi serta presisi yang memadai. Biasanya
range mempunyai satuan yang sama dengan satuan yang digunakan pada hasil
analisis (Anonim, 1995).
2. Kategori Metode Analisis
Metode analisis dapat dibedakan menjadi 4, yaitu :
a. Kategori I, mencakup metode analisis untuk kuantifikasi komponen terbesar
dalam obat atau bahan aktif (termasuk bahan pengawet) dari suatu sediaan.
b. Kategori II, mencakup metode analisis untuk penentuan impurities bahan obat
dan degradasi produk sediaan farmasi, termasuk penentuan kuantitatif dan uji
c. Kategori III, mencakup metode analisis yang digunakan untuk menentukan
karakteristik sediaan farmasi (seperti disolusi, pelepasan obat).
d. Kategori IV, mencakup uji identifikasi.
Setiap kategori metode analisis memiliki persyaratan validasi yang berbeda-beda
seperti yang tercantum pada tabel IV.
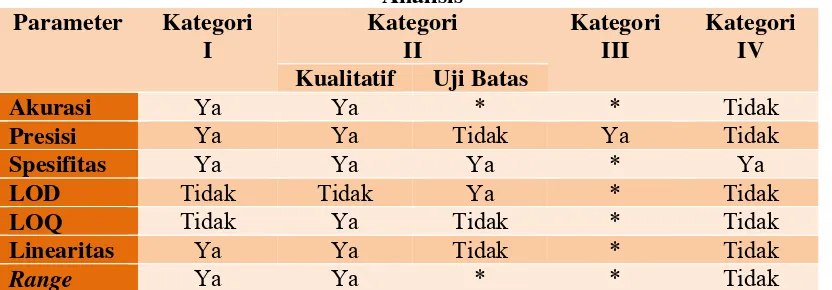
Tabel IV. Parameter Validasi Yang Dipersyaratkan Untuk Validasi Metode Analisis
Parameter Kategori I Kategori II Kategori III Kategori IV Kualitatif Uji Batas
Akurasi Ya Ya * * Tidak
Presisi Ya Ya Tidak Ya Tidak
Spesifitas Ya Ya Ya * Ya
LOD Tidak Tidak Ya * Tidak
LOQ Tidak Ya Tidak * Tidak
Linearitas Ya Ya Tidak * Tidak
Range Ya Ya * * Tidak
* Mungkin dibutuhkan, tergantung pada sifat test yang spesifik.
(Anonim, 2005).
3. Kesalahan Dalam Analisis
Kesalahan pada metode analisis kimia, yaitu :
a. Kesalahan sistematik, merupakan hasil analisis yang menyimpang secara tetap
dari nilai sebenarnya karena proses pelaksanaan prosedur analisis. Kesalahan
sistematik ada 2 macam, yaitu :
1) Kesalahan pada metode analisis, agak sulit dideteksi karena kesalahan
metode analisis ini disebabkan sifat fisika kimia pereaksi yang dipakai tidak
2) Kesalahan individual, adalah kesalahan yang timbul karena kesalahan
individu dalam pengamatan atau pembacaan instrumen yang dihadapi.
Kesalahan ini dapat dicari sebabnya dan dapat dikendalikan dengan kalibrasi
instrumen secara berkala, pemilihan metode dan prosedur standar dari badan
resmi, pemakaian bahan kimia dengan derajat untuk analisis, dan peningkatan
pengetahuan peneliti.
b. Kesalahan tidak sistematik, adalah penyimpangan tidak tetap dari hasil
penentuan kadar dengan instrumenasi yang disebabkan oleh fluktuasi instrumen
yang dipakai. Meningkatnya kesalahan tidak sistematik disebabkan tiap bagian
instrumen memberikan noise yang kecil yang kemudian ada kemungkinan
menjadi semakin besar sebagai nilai noise kumulatif. Penyebab kesalahan ini
tidak diketahui. Pemakaian instrumen dengan kualitas baik akan menekan nilai
kesalahan ini.
F. Landasan Teori
Tanaman binahong (Anredera cordifolia (Ten.) Steenis) diketahui memiliki
beberapa kandungan kimia, salah satunya adalah asam ursolat. Asam ursolat yang
ingin diteliti dalam penelitian ini merupakan isomer dari asam oleanolat. Metode
KCKT dapat digunakan dalam penetapan kadar asam ursolat dalam ekstrak daun
binahong karena adanya perbedaan interaksi asam ursolat dan senyawa lain dalam
ekstrak daun binahong terhadap fase diam dan fase gerak yang digunakan. Pada
terbalik karena asam ursolat merupakan senyawa organik yang mempunyai gugus
polar yang relatif larut dalam metanol sehingga sulit dipisahkan menggunakan
kromatogafi cair kinerja tinggi fase normal yang menggunakan kolom polar dan fase
gerak yang bersifat non polar karena analit akan cenderung terikat kuat pada fase
diam dan pemisahannya akan relatif lama dan tidak efisien.
G. Hipotesis
Dari rumusan permasalahan, dapat disusun hipotesis sebagai berikut :
1. Metode kromatografi cair kinerja tingi fase terbalik memenuhi parameter
validasi metode analisis yang meliputi akurasi, presisi, linearitas, LOD, dan
LOQ jika digunakan dalam penetapan kadar asam ursolat.
2. Metode kromatografi cair kinerja tinggi fase terbalik dapat diaplikasikan untuk
BAB III
METODOLOGI PENELITIAN
A. Jenis Penelitian
Penelitian yang dilakukan termasuk penelitian non eksperimental deskriptif.
Penelitian ini dilakukan di Laboratorium Kimia Analisis Instrumental Universitas
Sanata Dharma Yogyakarta.
B. Variabel Operasional 1. Variabel bebas
Variabel bebas dari penelitian ini adalah jenis dan perbandingan fase gerak,
yaitu metanol:ortophosphoric acid 1% (90:10), serta flow rate sebesar 0,6
ml/menit.
2. Variabel tergantung
Variabel tergantung pada penelitian ini adalah nilai akurasi, presisi, linearitas,
Limit Of Detection (LOD), dan Limit Of Quatitative (LOQ).
3. Variabel terkendali
Variabel terkendali dalam penelitian kali ini adalah kemurnian pelarut yang
digunakan. Untuk mengatasinya digunakan pelarut yang mempunyai kemurnian
C. Alat-alat Penelitian
Seperangkat KCKT yang terdiri dari pompa merk Shimadzu LC-10AD C21 2547
06757, detektor UV Vis merk Shimadzu SPD 10 AV, CBM 101 merk Shimadzu,
seperangkat komputer merk ACER, printer merk Hewlett Packard Deskjet 670C,
injektor jenis katup injek model 77251, kolom C18 merk Knauer 4.6 mm x 25 cm,
syringe merk Hamilton Part, alat degassing ultrasonik merk Retsch tipe T640,
penyaring Whatmann anorganik dan organik, membran filter merk Whatman,
evaporator, neraca analitik merk Scaltec SBC 22, vakum merk Gast model
DOA-P104-BN, millipore dengan ukuran pori 0,45 µm, waterbath, evaporator, pipet tetes,
pipet volume (1 ml, 5 ml, 10 ml), labu ukur (10 ml, 50 ml, 100 ml), Erlenmeyer, dan
alat-alat gelas lain.
D. Bahan-bahan Penelitian
Kloroform [p.a. Merck], metanol [p.a. Merck], orthophosphoric acid [p.a. Merck],
aquabidest (PT. Ikapharmindo Putramas), asam ursolat standar [Sigma], dan daun
E. Tata Cara Penelitian 1. Penyiapan Sampel
a. Pemilihan sampel
Sampel yang dipilih adalah daun tanaman binahong yang dikeringkan. Sampel
yang digunakan direplikasi sebanyak 3 kali dan dibuat triplo di setiap
replikasinya.
b. Determinasi tanaman
Determinasi tanaman binahong dilakukan dengan panduan buku “Flora of Java”
sehingga diketahui tanaman binahong termasuk dalam famili Basellaceae.
Kemudian tanaman binahong (Anredera cordifolia (Ten.) Steenis) dibuat
herbariumnya dalam bentuk kering meliputi akar, batang, dan daun.
c. Pengeringan sampel
Lebih kurang 100,0 gram daun segar tanaman binahong dicuci sampai bersih
dengan air mengalir. Daun segar tersebut kemudian dipotong-potong dan
dikeringkan dengan menggunakan oven pada suhu 60⁰C.
d. Ekstraksi sampel
Lima gram daun binahong kering ditimbang kemudian diekstraksi
menggunakan digesti selama 30 menit dengan pelarut kloroform sebanyak 30,0
ml (ekstraksi I). Ekstrak kental yang didapatkan kemudian disaring dengan
menggunakan kertas saring. Residu ekstraksi pertama kemudian diekstraksi
(1:1 v/v) sebanyak 30,0 ml selama 30 menit (ekstraksi II). Ekstrak dari hasil
ekstraksi II kemudian disaring menggunakan kertas saring dan dicampur
dengan hasil ekstraksi I yang kemudian dilakukan evaporasi hasil ekstraksi
sampai pelarut teruapkan sempurna pada suhu 70⁰C. Rendemen hasil evaporasi
kemudian dilarutkan dengan metanol sampai 25,0 ml.
2. Validasi Metode Kromatografi Cair Kinerja Tinggi a. Pembuatan larutan stok asam ursolat
Larutan stok asam ursolat dibuat dengan cara menimbang seksama sebanyak
0,01 g baku asam ursolat, kemudian dilarutkan dalam campuran
kloroform-metanol 1:4 (v/v) hingga volume 10,0 ml.
b. Pembuatan larutan intermediet asam ursolat
Larutan intermediet asam ursolat dibuat dengan cara memipet 1,0 ml larutan
baku asam ursolat, kemudian ditambah dengan campuran kloroform-metanol
1:4 (v/v) hingga 10,0 ml. Asam ursolat dengan konsentrasi 94,4 µg/ml ini
kemudian disaring dengan millipore dan di-degassing dengan menggunakan
ultrasonicator selama 15 menit.
c. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian ini adalah campuran metanol dan
orthophosphoric acid 1% dengan perbandingan 90:10 (v/v). Orthophosphoric
aquabidest. Campuran metanol:orthophosphoric acid 1% 90:10 (v/v) ini
kemudian disaring dengan penyaring Whatman anorganik dengan bantuan
pompa vakum lalu di-degassing dengan menggunakan ultrasonicator selama 15
menit.
d. Pembuatan kurva baku
Larutan intermediet asam ursolat yang dibuat dengan konsentrasi 94,4 µg/ml
yang sudah disaring dengan millipore dan di-degassing dengan ultrasonicator
selama 15 menit dimasukkan ke dalam tray dan dibuat seri volume injek
dengan volume 2,0; 4,0; 6,0; 8,0; dan 10,0 µl, kemudian diinjek dengan
kecepatan alir fase gerak yang optimum dan dideteksi pada panjang gelombang
maksimum asam ursolat. Dari kromatogram dilihat AUC pada waktu retensi
yang sesuai dengan waktu retensi asam ursolat. Dibuat kurva regresi linier yang
menyatakan hubungan antara kadar asam ursolat vs harga AUC, kemudian
ditentukan nilai koefisien korelasinya.
e. Recovery kurva baku
Satu mililiter larutan intermediet asam ursolat yang dibuat dengan konsentrasi
94,4 µg/ml ditambah dengan sampel ekstrak daun binahong hingga 10,0 ml,
kemudian disaring dengan millipore dan di-degassing dengan ultrasonicator
selama 15 menit dimasukkan ke dalam tray dan dibuat seri volume injek
dengan volume 2,0; 6,0; dan 10,0 µl, kemudian diinjek dengan 3 kali replikasi
dengan kecepatan alir fase gerak yang optimum dan dideteksi pada panjang
sehingga diperoleh 9 data. Dari kromatogram dilihat AUC pada waktu retensi
sesuai dengan dengan waktu retensi asam ursolat. Kadar asam ursolat dihitung
dengan memasukkan harga AUC ke persamaan kurva baku yang diperoleh.
f. Analisis validitas metode KCKT
Parameter-parameter yang digunakan sebagai pedoman kesahihan suatu metode
analisis antara lain:
(1)Akurasi
Akurasi metode analisis dinyatakan dengan % perolehan kembali
(recovery) yang dihitung dengan cara sebagai berikut :
% recovery = x100%
sebenarnya ursolat asam kadar didapat yang ursolat asam kadar
metode analisis dikatakan memiliki akurasi yang baik apabila %
perolehan kembali baku asam oleanolat berada pada rentang 98-102%
(Yuwono dan Indrayanto, 2005).
(2)Presisi
Presisi metode analisis dinilai berdasarkan Koefisien Variasi yang
dihitung dengan cara sebagai berikut :
x100% kadar rata rata SD − = KV
metode analisis dikatakan baik jika nilai KV < 2% (Yuwanto dan
(3)Linearitas
Linearitas dilihat dari harga r (koefisien korelasi) hasil pengukuran seri
baku asam ursolat. Suatu metode dikatakan memiliki linearitas yang baik
jika nilai r > 0,99 atau r2 > 0,997 (Chan et al.., 2004). Rentang ditentukan
dari kadar asam ursolat yang digunakan dalam analisis, mulai dari kadar
terkecil hingga terbesar.
(4)Limit Of Detection (LOD) dan Limit Of Quantitation (LOQ)
LOD dan LOQ dapat dihitung menggunakan rumus :
LOD = b x Sy 3 LOQ = b x Sy 10
Dimana Sy merupakan simpangan baku residual yang diperoleh melalui
akar dari jumlah (y-y’)2 dibagi (n-2), sedang b merupakan slope dari
persamaan kurva baku.
3. Uji Kualitatif
Sebanyak 0,5 ml ekstrak daun binahong ditambah 0,5 ml baku asam ursolat
dengan konsentrasi 94,4 µg/ml, kemudian ditambah dengan pelarut
kloroform:metanol (1:4) v/v hingga volume 10,0 ml. Campuran ini kemudian
ultrasonicator selama 15 menit, lalu diinjeksikan dalam sistem kromatografi cair
BAB IV
HASIL DAN PEMBAHASAN
A.Penyiapan fase gerak metanol:ortophosphoric acid 1% (90:10)
Fase gerak yang digunakan adalah campuran metanol dan ortophosphoric
acid 1% dengan perbandingan 90:10. Pemilihan fase gerak didasarkan pada sistem
kromatografi yang dipilih. Senyawa yang akan dianalisis mempunyai bobot molekul
kurang dari 2000 dan larut dalam alkohol tetapi tidak larut dalam air. Oleh karena itu,
dipilih sistem kromatografi partisi dalam KCKT. Pada sistem kromatografi partisi,
fase diam dapat bersifat polar maupun non polar. Jika fase diam yang digunakan
bersifat polar dan fase diam yang digunakan bersifat non polar, maka disebut
kromatografi fase normal. Demikian sebaliknya, apabila digunakan fase diam bersifat
non polar dan fase gerak yang digunakan bersifat polar, maka disebut kromatografi
fase terbalik. Pada penelitian ini digunakan sistem kromatografi fase terbalik karena
jika dilihat dari struktur senyawa asam ursolat merupakan senyawa yang mempunyai
gugus polar, sehingga dapat digunakan kolom oktadesilsilan (ODS) yang bersifat non
polar dan fase gerak yang bersifat polar. Pemilihan fase gerak yang akan digunakan
ini sangat penting karena akan mempengaruhi waktu retensi dan pemisahan
komponen yang akan dianalisis.
Pembuatan fase gerak terlebih dahulu dengan membuat larutan
orthophosphoric acid 1%, karena ortophosphoric acid yang tersedia di laboratorium
dengan ortophosphoric acid 1% tersebut dengan perbandingan yang diinginkan
(90:10). Campuran tersebut kemudian disaring dengan menggunakan penyaring
Whatman anorganik dengan bantuan pompa vakum. Digunakan penyaring Whatman
anorganik karena fase gerak yang digunakan bersifat polar, sehingga penyaring dapat
menahan kotoran yang ada. Namun apabila digunakan penyaring yang bersifat
organik, maka fase gerak yang digunakan dapat melarutkan atau melewati penyaring
sehingga pori-pori penyaring menjadi besar dan akibatnya akan ada kotoran tidak
dapat tersaring. Setelah disaring, fase gerak kemudian di-degassing dengan
menggunakan ultrasonicator selama 15 menit. Hal ini bertujuan agar gelembung gas
yang terjebak di dalam fase gerak dapat terbebas dan tidak mengganggu saat
pembacaan dengan membentuk sinyal palsu.
Gugus polar asam ursolat akan berinteraksi dengan fase gerak melalui ikatan
hidrogen. Semakin banyak gugus polar yang dimiliki oleh suatu senyawa, maka akan
semakin banyak ikatan hidrogen yang terbentuk sehingga afinitas antara fase gerak
dengan gugus polar suatu senyawa semakin besar dan akan semakin cepat terelusi
O
CH3 CH3
CH3 C CH3 CH3 O OH H H CH3 H3C
H
H
Gambar 8. Gugus Polar Asam Ursolat
O
CH3 CH3
CH3 C CH3 CH3 O OH H H CH3 H3C
H
H
O
CH3 H
CH3 C CH3 H H CH3 CH3 CH3 O O H H H OCH3 O H H OCH3 O O H CH3 H CH3 CH3 CH3 Gambar 10. Interaksi Hidrogen Antara Asam Ursolat Dengan Metanol Dalam
Fase Gerak
B.Penetapan kurva baku
Hasil penetapan kurva baku asam ursolat adalah suatu persamaan regresi
linear yang dapat digunakan untuk menghitung kadar asam ursolat dalam sampel.
Bila serapan sampel diketahui maka kadar asam ursolat dalam sampel dapat dihitung
dengan cara memasukkan serapan sampel ke dalam persamaan regresi linear.
Persamaan regresi linear tersebut menggambarkan hubungan antara konsentrasi asam
ursolat dengan serapan asam ursolat. Penetapan kurva baku pada penelitian ini
menggunakan larutan intermediet asam ursolat dengan volume injek 2,0; 4,0; 6,0;
ini tidak digunakan variasi seri konsentrasi, tetapi menggunakan variasi volume injek,
sebab dengan menggunakan variasi volume injek sudah dapat menggambarkan
variasi seri konsentrasi, sehingga dapat dikonversi ke massa. Penetapan kurva baku
diukur pada panjang gelombang maksimum teoritis, yaitu 210 nm. Hasil penetapan
kurva baku asam ursolat dapat dilihat pada tabel V.
Tabel V. Hasil Penetapan Kurva Baku Asam Ursolat
Volume Injek
(µl)
Repetisi I Repetisi II Repetisi III Massa
Baku (µg)
AUC Massa Baku
(µg)
AUC Massa Baku
(µg)
AUC
2.0 0.1888 124308 0.1998 129600 0.1930 124712
4.0 0.3776 250582 0.3996 265904 0.3860 253685
6.0 0.5664 378897 0.5994 396144 0.5790 382119
8.0 0.7552 506832 0.7992 531983 0.7720 510732
10.0 0.9440 635246 0.9990 664154 0.9650 637376
A = -4264.8 B = 676973.5169 r = 0.999995
A = -2999.1 B = 668261.7618 r = 0.999979
A = -2987.7 B = 664443.0052 r = 0.999994 Persamaan
Kurva Baku
y = 676973.5169x - 4264.8
y = 668261.7618x - 2999.1
y = 664443.0052x - 2987.7 Keterangan : A = intercept
B = slope
r = corr coeff.
y = Bx + A
Dari data di atas diperoleh 3 persamaan regresi linear dengan nilai α yang
lebih baik dan semuanya memiliki nilai koefisien korelasi (r) hitung yang lebih besar
dari pada nilai koefisien korelasi (r) tabel dengan df = 3 dan taraf kepercayaan 99%
antara konsentrasi asam ursolat dengan serapan asam ursolat. Dari 3 persamaan
regresi di atas dapat dilihat persamaan regresi linear yang paling baik adalah y =
676973,5169x – 4264,8 karena persamaan regresi linear tersebut memiliki nilai r
hitung yang paling mendekati 1 yaitu 0,999995. Oleh karena itu, persamaan regresi
linear inilah yang nantinya digunakan untuk menetapkan kadar asam ursolat dalam
sampel. Berikut ini adalah kurva hubungan antara massa baku asam ursolat dengan
serapan yang diberikan.
Gambar 11. Kurva Hubungan Antara Massa Baku Asam Ursolat Dengan AUC
C.Penyiapan Sampel
Penyiapan sampel dimulai dari pemilihan daun segar binahong, kemudian
dipotong-potong dan dikeringkan dalam oven pada temperatur 60ºC. Pengeringan 0
100000 200000 300000 400000 500000 600000 700000
0 0,2 0,4 0,6 0,8 1
AUC
daun binahong merupakan proses penting yang bertujuan untuk menghilangkan air
yang terkandung sehingga membran sel rusak dan asam ursolat lebih mudah diambil.
Daun binahong diekstraksi dengan digesti. Digesti merupakan salah satu
metode ekstraksi dengan maserasi yang disertai dengan pemanasan suhu rendah
(40-50OC). Bahan yang diekstraksi direndam dalam cairan penyari di dalam labu alas
bulat yang dilengkapi dengan alat pendingin tegak, kemudian dipanaskan sampai
mendidih. Cairan penyari akan menguap, yang kemudian uap tersebut akan
mengembun dalam pendingin tegak dan akan kembali menyari zat aktif dalam
simplisia tersebut.
Kandungan asam ursolat pada daun binahong diambil dengan menggunakan
sistem 2 kali ekstraksi. Ekstraksi pertama menggunakan pelarut kloroform sebanyak
30,0 ml selama 30 menit pada suhu 70ºC. Residu dari ekstraksi pertama kemudian
diekstraksi kembali dengan menggunakan pelarut campuran antara metanol dan
kloroform sebanyak 30,0 ml dengan perbandingan 1:1 (v/v) selama 30 menit pada
suhu 70ºC. Hasil ekstraksi pertama dan kedua dicampur untuk kemudian dievaporasi
menggunakan rotari evaporator. Digunakan pelarut kloroform pada ekstraksi pertama
karena asam ursolat lebih bersifat non polar dan kloroform juga bersifat non polar,
seperti pada prinsip like dissolve like di mana kepolaran dari kloroform menarik zat
yang mempunyai kepolaran yang hampir sama pada daun binahong salah satunya
yaitu asam ursolat. Kemudian residu dari ekstraksi pertama diekstraksi kembali
dengan menggunakan pelarut koroform-metanol (1:1) v/v untuk memastikan bahwa
Evaporasi dilakukan dengan tujuan untuk mengeringkan ekstrak daun
binahong. Prinsip evaporasi adalah dengan menarik pelarut sehingga didapatkan
rendemen. Rendemen ini kemudian dilarutkan dengan pelarut metanol sampai
mencapai volume 25,0 ml. Kemudian sebanyak 1,0 ml ekstrak daun binahong
ditambah dengan metanol sampai volume 10,0 ml. Setelah itu, sampel disaring
dengan menggunakan millipore (sebagai membran filter) untuk menghilangkan
semua partikel yang tak larut dalam fase gerak. Semakin kecil ukuran pori membran
filter, maka filtrat yang dihasilkan akan semakin jernih. Pada penelitian digunakan
millipore dengan ukuran pori 0,45 µm, karena partikel yang akan dihilangkan adalah
partikel yang berukuran lebih dari 0,45 µm. Partikel harus dihilangkan sebab partikel
akan dapat menyumbat inlet kolom, sehingga dapat merusak kolom yang pada
akhirnya akan mengurangi umur normal kolom. Filtrat yang didapatkan selanjutnya
di-degassing selama 15 menit untuk menghilangkan gelembung gas yang terdapat
dalam larutan. Gelembung gas dalam sampel harus dihilangkan agar tidak
menyumbat kolom instrumen dan tidak memberikan sinyal palsu sehingga tidak
mengganggu pembacaan.
D.Analisis kualitatif
Uji kualitatif menunjukkan adanya puncak yang mempunyai waktu retensi
yang sama dengan puncak kromatogram standar asam ursolat. Waktu retensi asam
ursolat pada kromatogram standar menunjukkan bahwa puncak terjadi pada menit
yang berdekatan antara standar asam ursolat dengan sampel menunjukkan bahwa
dalam ekstrak daun binahong terdapat senyawa asam ursolat. Hal ini diperkuat
dengan analisis menggunakan teknik spiking. Dengan menggunakan teknik ini dapat
diketahui pada kromatogram, pada sekitar menit ke-23, AUC yang didapat lebih besar
dari pada AUC sampel maupun AUC standar. Dari kromatogram dapat dilihat bahwa
AUC untuk baku asam ursolat sebesar 378897, AUC untuk sampel ekstrak daun
binahong sebesar 132084, dan AUC untuk spiking sebesar 734811. Diketahuinya
waktu retensi asam ursolat di sekitar menit ke-23, maka proses analisis dengan
menggunakan metode kromatografi cair kinerja tinggi fase terbalik ini berlangsung
selama 60 menit untuk setiap penginjeksian. Kromatogram hasil uji kualitatif
Keberhasilan pemisahan ditunjukkan dengan nilai resolusi dimana nilai
resolusi dihitung dengan persamaan berikut :
Rs =
(Noegrohati, 1994).
Dari hasil perhitungan diperoleh nilai resolusi sebesar 2,1. Nilai ini
menunjukkan nilai resolusi yang baik, karena nilai resolusi yang baik adalah lebih
dari 2 dan dengan didapatkannya nilai resolusi yang baik maka dapat dikatakan
bahwa telah terjadi pemisahan senyawa dengan baik.
E.Validitas metode 1. Akurasi
Akurasi dimaksudkan untuk mengetahui seberapa dekat antara hasil yang
diukur dengan menggunakan suatu metode analisis dengan hasil yang sebenarnya.
Akurasi dinyatakan dalam % perolehan kembali (recovery). Semakin sedikit
selisih antara keduanya maka akurasi metode analisis semakin baik. Menurut
Harmita (2004), akurasi yang baik untuk analisis bahan obat dengan kadar lebih
dari 10% adalah dinyatakan dalam recovery 90-110%. Serapan hasil pengukuran
diolah dengan persamaan regresi linear y = 676973,5169x – 4264,8 sehingga
Tabel VI. Hasil Perhitungan Recovery Volume injek (µl) Massa teoritis (µg) AUC Massa terukur (µg) Recovery (%)
2.0 0.094
132084 0.1007 106.673
104.413% 133101 0.1014 107.944
121793 0.0931 98.622
6.0 0.094
395495 0.0984 104.237
105.931% 400792 0.0997 105.614
409706 0.1019 107.944
10.0 0.094
691068 0.1027 108.792
107.909% 673256 0.1000 105.932
692868 0.1029 109.004
Rentang yang diperoleh adalah antara 104,413-107,909%. Hasil ini sudah masuk
dalam range 90-110%, sehingga dapat dikatakan bahwa metode analisis asam
ursolat secara kromatografi cair kinerja tinggi telah memenuhi syarat akurasi.
2. Presisi
Presisi menunjukkan keterulangan dan ketertiruan hasil yang diperoleh.
Presisi dinyatakan dalam KV (koefisien variasi). Menurut Harmita, presisi suatu
metode analisis untuk kadar analit lebih dari 10% dikatakan baik apabila KV
kurang dari 2,7%. Semakin kecil KV yang diperoleh, maka semakin baik presisi
metode yang digunakan.
Tabel VII. Hasil Perhitungan Kesalahan Sistemik dan Kesalahan Acak
Nilai Volume Injek (µl)
2.0 6.0 10.0
SD 5.055 1.873 1.716
Berdasarkan pengukuran yang dilakukan, diperoleh KV ≤ 2,7%. Hasil ini
menunjukkan bahwa presisi dari metode analisis asam ursolat secara kromatografi
cair kinerja tinggi telah memenuhi syarat presisi.
3. Linearitas
Linearitas menyatakan hubungan korelasi antara kadar dengan serapan.
Linearitas dinyatakan sebagai koefisien korelasi (r). Semakin baik nilai r maka
semakin baik korelasi antara kadar dengan serapan, yaitu dengan adanya
peningkatan kadar maka akan meningkatkan serapannya secara proporsional.
Berdasarkan pengukuran yang dilakukan diperoleh nilai r masing-masing
sebesar 0,999995; 0,999979; dan 0,999994. Nilai r ini sudah memenuhi
persyaratan APVMA tahun 2004 yaitu > 0,99% dan lebih besar dari rtabel, yaitu
0,959 (taraf kepercayaan 95% dan derajat bebas 3). Menurut Chan et al., linearitas
yang baik tercapai apabila nilai r2 ≥ 0,997. Dari ketiga nilai r tersebut semua
memenuhi persyaratan tersebut. Hasil ini menunjukkan bahwa linearitas dari
metode analisis asam ursolat secara kromatografi cair kinerja tinggi telah
memenuhi syarat linearitas.
4. Limit of Detection (LOD) dan Limit of Quantitation (LOQ)
LOD atau batas deteksi adalah jumlah terkecil analit dalam sampel yang
dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan
analit yang masih dapat dianalisis oleh suatu metode analisis dengan hasil yang
tetap memenuhi syarat akurasi dan presisi. LOD dan LOQ dapat ditentukan dari
persamaan regresi linear kurva baku. Semakin kecil nilai LOD dan LOQ maka
dapat dikatakan bahwa sensitivitas dari metode tersebut semakin baik.
Berdasarkan hasil pengukuran dan perhitungan, nilai LOD yang diperoleh
sebesar 3,117x10-3 µg/ml. Sedangkan nilai LOD yang diperoleh sebesar 0,0104
µg/ml. Konsentrasi terkecil dari seri kurva baku harus lebih besar dari nilai LOQ
agar analisis senyawa dapat memenuhi persyaratan akurasi dan presisi yang baik.
Dalam penelitian ini, konsentrasi seri kurva baku yang paling kecil adalah 94,4
µg/ml. Dengan demikian, kurva baku dapat digunakan dalam penetapan kadar
BAB V
KESIMPULAN DAN SARAN
A.Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa metode kromatografi cair
kinerja tinggi fase terbalik dengan detektor ultraviolet yang dikembangkan dalam
penelitian ini merupakan metode yang valid dalam penetapan kadar asam ursolat
dalam ekstrak daun binahong (Anredera cordifolia (Ten.) Steenis), dengan
memenuhi parameter metode analisis yang meliputi akurasi, presisi, linearitas,
LOD, dan LOQ.
B.Saran
Perlu dilakukan penetapan kadar asam ursolat dalam ekstrak daun
binahong (Anredera cordifolia (Ten.) Steenis) dengan metode kromatografi cair
DAFTAR PUSTAKA
Anonim, 1979, Farmakope Indonesia, edisi III, 8-9, 28, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1986, Sediaan Galenik, 8-51, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1989, The Merck Index an Encyclopedia of Chemicals, Drugs, and Biologicals, 11th Ed., 9801, Merck & Co., Inc., Rahway N. J., USA
Anonim, 1995, Farmakope Indonesia, edisi IV, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 2005, The United States Pharmacopeia, 28th Ed., 1982-1984, United States Pharmacopeia Convention, Inc., Rockville
Anonim, 2007, The United State Pharmacopeia, edisi 30 (monograph on CD-ROM), United States Pharmacopeia Convention, Inc.
Anonim, 2009, Ursolic Acid Na-salt,
http://www.kinetiktech.com/brochures/pdf/gfn/Ursolic_Acid_Leaflet.pdf, diakses tanggal 28 April 2010
Backer, C. A., dan Van de Brink, R., C., 1963, Flora of Java, volume I, Wolters Noordhoff, N. N., Groningen, the Nedherlands
Cha, Hee-Jae, Bae, Soo-Kyung, Lee, Ho-Young, Lee, Ok-Hee, Sato, H., Seiki, M., et al., Anti-Invasive Activity of Ursolic Acid Correlates with the Reduced Expression of Matrix Metalloproteinase-9 (MMP-9) in HT1080 Human
Fibrosarcoma Cells1,
http://cancerres.aacrjournals.org/cgi/reprint/56/10/2281.pdf, diakses tanggal 28 April 2010
Chann, A. J., 2003, Maths from Scratch for Biologist, 213, John Wiley and sons LTD, England
Gnoatto, Simone C. B., Schenkel, E. P., dan Bassani Y.L., 2005, HPLC Method to
Assay Total Saponins in Ilex paraguariensis Aqueous Extract,
Gritter, R. J., Bobbit, J. M., and Schwarting, A. E., 1985, Introduction to Chromatography, diterjemahkan oleh Kosasih Padmawinata, Edisi II, 205-219, Penerbit ITB, Bandung
Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya,
Majalah Ilmu Kefarmasian, 3 (1), 177, 129, Departemen Farmasi FMIPA UI, Jakarta
Hidayati, I. W., 2009, Uji Aktifitas Salep Ekstrak Daun Binahong (Anredera
cordifolia (Ten.) Steenis) sebagai Penyembuh Luka Bakar Pada Kulit
Punggung Kelinci, Skripsi, Universitas Muhammadiyah Surakarta Press, Surakarta
Johnson, E. L., and Stevenson R., 1978, Basic Liquid Chromatography, diterjemahkan oleh Kosasih Padmawinata, 6-9, 17-25, 90-91, 99-103, ITB Press, Bandung
Kanade, Shrinivas, 2010, Anti Aging Creams Ingedients,
http://www.buzzle.com/articles/anti-aging-cream-ingredients.html, diakses tanggal 12 Mei 2010
Kazakevich, Y., dan Mc Nair, H., 1996, Basic Liquid Chromatography, diterjemahkan oleh Padmawinata, 1-27, 90-117, , Institut Teknologi Bandung Press, Bandung
Lazuardhi, 2009, Binahong, http://www.lazuardhi.blogspot/binahong/ diakses tanggal 12 Mei 2010
Liao, Qiongfeng, Yang, W., Jia, Y., Chen, X., Gao, Q., and Bi., K., 2005, LC-MS Determination and Pharmacokinetic Studies of Ursolic Acid in Rat Plasma after Administration of The Traditional Chinese Medicinal Preparation Lu-Ying Extract, http://yakushi.pharm.or.jp/FULL_TEXT/125_6/pdf/509.pdf, diakses tanggal 28 April 2010
Li, Jie, Wei-Jian Guo, Qing-Yao Yang, 2002, Effects of Ursolic Acid and Oleanolic
Acid on Human Colon Carcinoma Cell Line HCT15,
http://www.wjgnet.com/1007-9327/8/493.pdf, diakses tanggal 28 April 2010
Mulja, M., dan Hanwar, D., 2003, Prinsip-Prinsip Cara Berlaboratorium yang Baik (Good Laboratory Practice), Majalah Farmasi Indonesia Airlangga, Vol. III,
Mulja, M. dan Suharman, 1995, Analisis Instrumental, 188, Institut Teknologi Bandung Press, Bandung
Munson, J. W., 1991, Pharmaceutical Analysis Modern Methods, diterjemahkan oleh Harjana, Parwa, B., 15, 33-34, Universitas Airlangga Press, Surabaya
Noegrohati, S., 1994, Pengantar Kromatografi, 16-17, Universitas Gajah Mada Press, Yogyakarta
Olszewska, M., 2008, Optimization and Validation of an HPLC-UV Method for Analysis of Corosolic, Oleanolic, and Ursolic Acids in Plant Material:Application to Prunus serotina Ehrh., Acta Chromatographica, Department of Pharmacognosy, Faculty of Pharmacy, Medical University of Lodz, Poland
Paramita, A., 2008, Optimasi Formula Span 80 dan Tween 80 Dalam Cold Cream Obat Luka Ekstrak Daun Binahong (Anredera cordifolia (Ten.) Steenis) dengan Metode Simplex Lattice Design, Skripsi, Universitas Sanata Dharma, Yogyakarta Raihan, 2007, http://www.google.co.id/imglanding?q=binahong&imgurl=http://raihan07.files. wordpress.com/2009/11/binahong.jpg&imgrefurl=http://raihan07.wordpress.co m/2009/11/21/khasiat-tanaman-binahong/&usg=__bMfRWyt8-orrUOZf6ZkedmIU47U=&h=359&w=336&am