BAB II
TINJAUAN PUSTAKA
2.1 Pengertian Obat
Surat Keputusan Menteri Kesehatan Republik Indonesia No 193/KabB/.
VII/71 mendefinisikan bahwa obat adalah suatu bahan atau paduan bahan-bahan
yang digunakan dalam menetapkan diagnosis, mencegah, mengurangkan,
menghilangkan, menyembuhkan penyakit atau gejala penyakit, luka atau kelainan
badaniah dan rohaniah pada manusia atau hewan serta memperindah badan atau
bagian badan manusia (Joenoes, 2001).
Batas antara obat dan racun sangat pendek, hal ini tergantung pada dosis
dan cara pemakaian. Oleh karena itu, obat dapat bersifat sebagai obat dan dapat
bersifat sebagai racun. Obat akan bersifat sebagai obat apabila tepat digunakan
pada suatu penyakit dengan dosis dan waktu yang tepat. Jadi, apabila digunakan
tidak tepat dalam pengobatan atau dengan dosis yang berlebihan akan
menimbulkan keracunan, sedangkan apabila dosisnya lebih kecil, maka pasien
tidak akan memperoleh kesembuhan (Widjajanti, 1988).
Efek farmakologi atau efek terapi obat harus mencapai tempat aksinya
dalam konsentrasi yang cukup untuk menimbulkan respon. Tercapainya
konsentrasi obat tergantung pada keadaan dan kecepatan obat diabsorpsi dari
tempat pemberian dan distribusinya oleh aliran darah ke bagian yang lain dari
badan. Kecepatan absorpsi obat akan dipengaruhi oleh laju disolusi, semakin
2.2 Tablet
Tablet adalah bentuk sediaan padat mengandung bahan obat dengan atau
tanpa bahan pengisi. Berdasarkan metode pembuatan, tablet dapat digolongkan
sebagai tablet cetak dan tablet kempa. Tablet cetak dibuat dengan cara menekan
massa serbuk lembab dengan tekanan rendah kedalam lubang cetakan. Tablet
kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul
menggunakan cetakan baja. Tablet dapat dibuat dalam berbagai ukuran, bentuk
dan penandaan permukaan tergantung pada desain cetakan (Ditjen POM, 1995).
Tablet didefenisikan sebagai bentuk sediaan solid yang mengandung satu
atau lebih zat aktif dengan atau tanpa berbagai eksipien (yang meningkatkan mutu
sediaan tablet) dan dibuat dengan mengempa campuran serbuk dalam mesin tablet
(Siregar dan Wikarsa, 2012).
Tablet dapat berbeda-beda dalam ukuran, bentuk, berat, kekerasan,
ketebalan, daya hancurnya, dan dalam aspek lainnya tergantung pada cara
pemakaian tablet dan metode pembuatannya. Kebanyakan tablet digunakan pada
pemberian obat-obat secara oral, dan kebanyakan dari tablet ini dibuat dengan
penambahan zat warna, zat pemberi rasa, dan lapisan-lapisan dalam berbagai
jenis. Tablet lain yang penggunaanya dengan cara sublingual, bukal, atau melalui
vagina, tidak boleh mengandung bahan tambahan seperti pada tablet yang
digunakan secara oral (Ansel, 1989).
Komposisi utama dari tablet adalah zat berkhasiat yang terkandung
tablet yaitu bahan penghancur, bahan penyalut, bahan pengikat, bahan pemberi
rasa dan bahan tambahan lainnya (Ansel, 1989).
2.2.1 Jenis-jenis tablet
Jenis-jenis tablet adalah sebagai berikut :
1. Tablet kompresi
Yaitu tablet kompresi dibuat dengan sekali tekanan menjadi berbagai
bentuk tablet dan ukuran, biasanya kedalam bahan obatnya diberi
tambahan sejumlah bahan pembantu antara lain :
a) Pengencer atau pengisi yang ditambahakan jika perlu kedalam
formulasi supaya membentuk ukuran tablet yang diinginkan.
b) Pengikat atau perekat, yang membantu pelekatan partikel dalam
formulasi, memungkinkan granul dibuat dan dijaga keterpaduan
hasil tabletnya.
c) Penghancur atau bahan yang dapat membantu penghancuran, akan
membantu memecah atau menghancurkan tablet setelah pemberian
sampai menjadi partikel-partikel yang lebih kecil, sehingga lebih
mudah diabsorpsi.
d) Antirekat pelincir atau zat pelincir yaitu zat yang meningkatkan
aliran bahan memasuki cetakan tablet dan mencegah melekatnya
bahan ini pada punch dan dieserta membuat tablet-tablet menjadi
bagus dan berkilat.
e) Bahan tambahan lain seperti zat warna dan zat pemberi rasa
2. Tablet kunyah
Pada tablet kunyah sebagai bahan pengisi dapat berupa mannitol, sorbitol,
laktosa atau dekstrosa ditambah bahan pemanis dan bahan pembau (Anief,
1987).
3. Tablet salut
Tablet sering disalut agar dapat menghilangkan rasa tak enak dari obat,
menaikkan stabilitas obat terhadap pengaruhuap, air, cahaya, dan terlihat
lebih baik (Anief, 1987).
a) Tablet salut gula
Tablet ini sering disebut dragee. Penyalutan dilakukan dengan
larutan gula dalam panci untuk penyalutan dan panci untuk
mengkilapkan tablet diputar dengan motor penggerak dan
dilengkapi dengan alat penghisap dan sistem penghembus dengan
udara panas (blower) (Anief, 2008).
b) Tablet salut selaput
Tablet kompresi ini disalut dengan selaput tipis dari polimer yang
larut atau tidak larut dalam air maupun membentuk lapisan yang
meliputi tablet. Biasanya lapisan ini bewarna, kelebihannya dari
penyalutan dengan gula adalah lebih tahan lama, lebih sedikit
bahan, waktu yang lebih sedikit untuk penggunaanya (Ansel,
c) Tablet salut enterik
Tablet salut enterik adalah tablet yang disalut dengan zat penyalut
yang relatif tidak larut dalam asam lambung, tetapi larut dalam
usus halus.
Penyalut enterik dimaksudkan:
a) Agar obat tidak mengiritir perut
b) Dikehendaki agar obat berkhasiat dalam usus seperti antelmintika
c) Menghindari obat menjadi inaktif dalam cairan lambung, yaitu
karena pH rendah atau dirusak enzim digostif dalam perut (Anief,
2008).
4. Tablet effervescent
Yaitu tablet berbuih dibuat dengan cara kompresi granul yang
mengandung garam effervescent atau bahan-bahan lain yang mampu
melepaskan gas ketika bercampur dengan air (Ansel, 1989).
2.2.2 Syarat-syarat tablet
Syarat-syarat tablet adalah sebagai berikut:
1. Keseragaman bobot
Keseragaman bobot ditetapkan sebagai berikut :
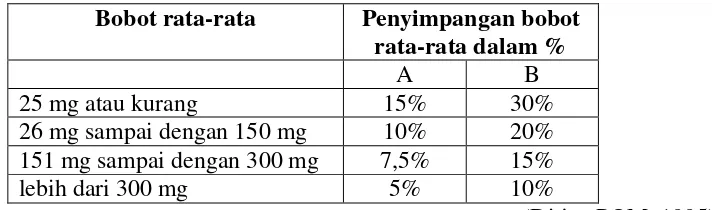
Ditimbang 20 tablet, dihitung bobot rata-rata tiap tablet. Jika
ditimbang satu-persatu, tidak boleh lebih dari 2 tablet yang menyimpang
dari bobot rata-rata lebih besar dari harga yang ditetapkan dalam kolom A
dan tidak boleh satu tablet pun yang bobotnya menyimpang dari bobot
10 tablet dan tidak satu tablet yang bobotnya menyimpang lebih besar dari
bobot rata- rata yang ditetapkan dalam kolom A maupun kolom B (Anief,
2008).
Tabel 2.1. Penyimpangan bobot rata-rata
Bobot rata-rata Penyimpangan bobot rata-rata dalam %
Kekerasan tablet dan ketebalannya berhubungan dengan isi die dan
gaya kompresi yang diberikan. Bila tekanan ditambahkan, maka kekerasan
tablet meningkat sedangkan ketebalan tablet berkurang. Selain itu metode
granulasi juga menentukan kekerasan tablet. Umumnya kekuatan tablet
berkisar 4-8 kg, bobot tersebut dianggap sebagai batas minimum untuk
menghasilkan tablet yang memuaskan. Alat yang digunakan untuk uji ini
adalah hardness tester, alat ini diharapkan dapat mengukur berat yang
diperlukan untuk memecahkan tablet (Ansel, 1989).
3. Friabilitas
Cara lain untuk menentukan kekuatan tablet ialah dengan
mengukur keregasannya (friabilitas). Gesekan dan goncangan merupakan
penyebab tablet menjadi hancur. Untuk menguji keregasan tablet
digunakan alat Roche friabilator. Sebelum tablet dimasukkan ke alat
kedalam alat, lalu alat dioperasikan selama empat menit atau 100 kali
putaran. Tablet ditimbang kembali dan dibandingkan dengan berat
mula-mula. Selisih berat dihitung sebagai keregasan tablet. Persyaratan
keregasan harus lebih kecil dari 0,8% (Ansel, 1989).
4. Waktu hancur (Disintegration Test)
Uji waktu hancur tablet dilakukan untuk tablet yang tidak bersalut,
tablet bersalut bukan enterik, tablet salut enterik, tablet bukal, dan tablet
sublingual. Uji waktu hancur dilakukan dengan menggunakan alat uji
waktu hancur. Masing-masing sediaan tablet tersebut mempunyai prosedur
uji waktu hancur dan persyaratan tertentu (Siregar dan Wikarsa, 2010).
Uji waktu hancur tidak dilakukan pada etiket jika dinyatakan
“tablet kunyah, tablet isap, tablet yang pelepasan zat aktif bertahap dalam
jangka waktu tertentu, atau tablet melepaskan zat aktif dalam dua periode
berbeda atau lebih dengan jarak waktu yang jelas diantara periode
pelepasan tersebut (Siregar dan Wikarsa, 2010).
5. Disolusi (Dissolution Test)
Disolusi adalah suatu proses perpindahan molekul obat dari bentuk
padat ke dalam larutan suatu media. Uji ini dimaksudkan untuk
mengetahui banyaknya zat aktif yang terlarut dan memberikan efek terapi
di dalam tubuh. Kecepatan absorbsi obat tergantung pada pemberian yang
dikehendaki dan juga harus dipertimbangkan frekuensi pemberian obat
6. Penetapan kadar zat aktif
Penetapan kadar zat aktif bertujuan untuk mengetahui apakah
kadar zat aktif yang terkandung didalam suatu sediaan sesuai dengan yang
tertera pada etiket dan memenuhi syarat seperti yang tertera pada
masing-masing monografi. Bila zat aktif obat tidak memenuhi syarat maka obat
tersebut tidak akan memberikan efek terapi dan juga tidak layak untuk
dikonsumsi (Syamsuni, 2007).
2.3 Paraseta
mol
Rumus Bangun : Acetamenophen; Paracetamol; p-acetamidophenol; N-
acetyl-p-amino-phenol
Gambar 2.1. Struktur parasetamol Rumus Struktur : C8H9NO2
Berat Molekul : 151,16
Nama Kimia : 4’- Hidroksiasetanilida
Pemerian : Serbuk hablur, putih; tidak berbau; rasa sedikit pahit.
Kelarutan : Larut dalam air mendidih dan dalam natrium
hidroksida1N; mudah larut dalam etanol; tidak larut dalam
2.3.1 Mekanisme kerja
Mekanisme kerja yang berhubungan dengan sistem biosintesis
prostaglandin (PG) ini memperlihatkan secara in vitro bahwa dosis rendah aspirin
dan indometasin Anti-Inflamasi Non-Steroid (AINS) diketahui menghambat
berbagai reaksi biokimiawi, hubungan dengan efek analgesik, antipiretik dan
anti-inflamasinya belum jelas. Selain itu obat Anti Inflamasi Non-Steroid (AINS)
secara umum tidak menghambat biosintesis leukotrien, yang diketahui ikut
berperan dalam inflamasi (Nafrialdi dan Setiawati, 2007).
Golongan obat ini menghambat enzim siklo-oksigenase sehingga konversi
asam arakidonat menjadi PGG2 terganggu. Setiap obat menghambat
siklo-oksigenase dengan cara yang berbeda. Khusus parasetamol, hambatan biosintesis
prostaglandin (PG) hanya terjadi bila lingkungannya rendah kadar peroksid
seperti di hipotalamus. Lokasi inflamasi biasanya mengandung banyak peroksid
yang dihasilkan oleh leukosit. Ini menjelaskan mengapa efek anti-inflamasi
parasetamol praktis tidak ada (Nafrialdi dan Setiawati, 2007).
2.3.2 Farmakokinetik
Parasetamol diserap cepat dan sempurna melalui saluran cerna.
Konsentrasi tertinggi dalam plasma dicapai dalam waktu setengah jam, masa
paruh dalam plasma antara 1-3 jam.Obat ini tarsebar ke seluruh cairan tubuh.
Dalam plasma sebagian terikat oleh protein plasma, 25%. Obat ini mengalami
metabolisme oleh anzim-anzim mikrosom dalam hati. 80% asetaminofen
dikonjugasi dengan asam glukuronat dan sebagian kecil dengan asam sulfat dalam
hidroksilasi ini dapat menimbulkan methemoglobinemia dan hemolisis eritrosit.
Obat ini diekskresi melalui ginjal, sebagian kecil sebagai asetaminofen (3%) dan
sebagian besar dalam bentuk terkonjugasi (Nafrialdi dan Setiawati, 2007).
2.3.3 Farmakodinamik
Efek analgesik parasetamol serupa dengan salisilat yaitu menghilangkan
atau mengurangi nyeri ringan sampai sedang. Keduanya menurunkan suhu tubuh
dengan mekanisme yang diduga juga berdasarkan efek sentral seperti salisilat
(Nafrialdi dan Setiawati, 2007).
Efek anti-inflamasinya sangat lemah, oleh karena itu parasetamol tidak
digunakan sebagaai antireumatik. Parasetamol merupakan penghambat biosintesis
prostaglandin (PG) yang lemah. Efek iritasi, erosi, dan perdarahan lambung tidak
terlihat pada obat ini, demikian juga gangguan pernafasan dan keseimbangan
asam basa (Nafrialdi dan Setiawati, 2007).
2.3.4 Efek samping
Reaksi alergi terhadap derivat para-aminofenol jarang terjadi.
Manifestasinya berupa eritema atau urtikaria dan gejala yang lebih berat berupa
demam dan lesi pada mukosa (Nafrialdi dan Setiawati, 2007).
Methemoglobinemia dan sulfhemoglobinemia jarang menimbulkan
masalah pada dosis terapi, karena hanya kira-kira 1-3% hemoglobin (Hb) diubah
menjadi met-Hb. Penggunaan semua jenis analgesik dosis besar secara menahun
terutama dalam kombinasi berpotensi menyebabkan nefropati analgesik (Nafrialdi
2.3.5 Indikasi
Penggunaan asetaminofen sebagai analgetik dan antipiretik adalah sama
dengan penggunaan salisilat. Analgesik, penggunaan asetaminofen dapat
diberikan tiap 3-4 jam untuk keadaan seperti sakit kepala, migren, serta nyeri
haid. Tetapi sebaiknya terapi jangan diberikan terlalu lama. Jika dosis terapeutik
biasa tidak memberi manfaat, dosisi yang lebih besar biasanya juga tidak
menolong. Antipiretik, penggunaan asetaminofen untuk meredakan demam telah
terdesak oleh penggunaannya untuk menimbulkan analgesia.Untuk dewasa dosis
325 mg-1000 mg, diberikan secara oral tiap 3 atau 4 jam. Untuk anak 20 mg/kg
BB diberikan tiap 4-6 jam, dosis total perhari jangan melebihi 3,6 g (Tanu, 1972).
2.3.6 Sediaan dan dosis
Untuk nyeri dan demam oral 2-3 dd 0,5-1 g, maksimum 4 g/hari, pada
penggunaan kronis maksimum 2,5 g/hari. Anak-anak: 4-6 dd 10 mg/kg, yakni
rata-rata usia 3-12 bulan 60 mg, 1-4 tahun 120-180 mg, 4-6 tahun 180 mg, 7-12
tahun 240-360 mg, 4-6 x sehari. Rektal 20 mg/kg setiap kali, dewasa 4 dd 0,5-1 g,
anak-anak usia 3-12 bulan 2-3 dd 120 mg, 1-4 tahun 2-3 dd 240 mg, 4-6 tahun 4
dd 240 mg, dan 7-12 tahun 2-3 dd 0,5 g (Tjay dan Kirana, 2002).
2.3.7 Sindrom toksik yang umum
Asetaminofen jika dikonsusmsi secara akut lebih dari 150-200 mg/kg
(pada anak-anak) atau 7 gr (pada orang dewasa) dianggap sebagai potensi toksik.
Metabolit yang sangat toksik diproduksi didalam hati (Katzung, 2004).
Awalnya pasien mengalami gangguan gastrointernal ringan (mual,
kadar aminotransferase dan hipoprotrombinemia. Pada kasus berat, terjadi gagal
hati fulminan, sehingga menyebabkan ensefalopati hepatis dan kematian. Kadar
keparahan keracunan ditentukan oleh kadar asetaminofen serum. Jika kadarnya
kira-kira 4 jam setelah mengonsumsi lebih dari 150-200 mg/L, maka pasien
tersebut beresiko mengalami kerusakan hati (Katzung, 2004).
2.4 Uji Disolusi
Uji Disolusi didefenisikan sebagai proses suatu zat padat masuk ke dalam
pelarut menghasilkan suatu larutan. Secara sederhana, disolusi adalah proses zat
padat melarut. Secara prinsip, proses ini dikendalikan oleh afinitas antara zat
padat dan pelarut. Secara singkat, alat untuk menguji karakteristik disolusi dan
sediaan padat kapsul atau tablet terdiri dari :
1) Motor pengaduk dengan kecepatan yang dapat diubah,
2) Keranjang baja stainless berbentuk silinder atau dayung untuk ditempelkan
keujung batang pengaduk,
3) Bejana dari gelas, atau bahan lain yang inert dan transparan dengan
volume 1000 ml, bertutup sesuai dengan di tengah-tengahnya ada tempat
untuk menempelkan pengaduk, dan ada lubang tempat masuk pada 3
tempat, dua untuk memindahkan contoh dan satu untuk menempatkan
termometer, dan
4) Penangas air yang sesuai untuk menjaga temperatur pada media disolusi
(seperti yang dicantumkan dalam masing-masing monografi) ditempatkan
dalam bejana dan biarkan mencapai temperatur 37°C ± 0,5°C. Kemudian
ditempatkan dalam keranjang dan pengaduk diputar dengan kecepatan
seperti yang ditetapkan dalam monografi. Pada waktu-waktu tertentu
contoh dari mesin diambil untuk analisis kimia dari bagian obat yang
terlarut. Tablet atau kapsul harus memenuhi persyaratan seperti yang
tertera dalam monografi untuk kecepatan disolusi (Ansel, 1989).
Laju disolusi dapat menjadi tahap pembatasan kecepatan sebelum zat aktif
berada dalam darah. Akan tetapi jika bentuk sediaan (tablet) yang diberikan secara
per oral masuk dan berada di saluran cerna dalam bentuk sediaan solid, ada dua
kemungkinan yang dapat terjadi untuk tahap pembatasan kecepatan zat aktif
berada dalam sirkulasi. Pertama, bentuk sediaan solid harus terdisintegrasi dan zat
aktif larut dalam media cair dan kemudian harus melewati membran saluran
cerna. Zat aktif yang mudah larut akan cenderung cepat melarut, membuat tahap
pembatasan kecepatan, yakni difusi pasif atau transpor aktif zat aktif, untuk
absorpsi melalui membran saluran cerna. Sebaliknya kecepatan absorpsi zat aktif
yang sukar larut akan dibatasi oleh laju disolusi zat aktif yang tidak larut, atau
juga dapat dibatasi oleh kecepatan disintegrasi bentuk sediaan (Siregar dan
Wikarsa, 2010).
2.4.1 Metode uji disolusi
Menurut Ditjen POM (1995), ada dua metode alat uji disolusi sesuai
dengan yang tertera dalam masing-masing monografi:
a) Alat 1 (Tipe Keranjang)
Alat terdiri dari wadah bertutup yang terbuat dari kaca, suatu motor,
(keranjang) berbentuk silinder dengan dasar setengah bola, tinggi 160
mm−175 mm, diameter 98 mm−106 mm dan kapasitas nominal 1000 ml.
Batang logam berada pada posisi sedemikian sehingga sumbunya tidak lebih
dari 2 mm pada setiap titik dari sumbu vertikal wadah dan berputar dengan
halus dan tanpa goyangan. Sebuah tablet diletakkan dalam keranjang saringan
kawat kecil yang diikatkan pada bagian bawah batang logam yang digerakkan
oleh motor yang kecepatannya dapat diatur. Wadah dicelupkan sebagian di
dalam suatu tangas air yang sesuai sehingga dapat mempertahankan suhu
dalam wadah pada 37o ± 0,5oC selama pengujian dan menjaga agar gerakan air
halus dan tetap. Pada bagian atas wadah ujungnya melebar, untuk mencegah
penguapan digunakan suatu penutup yang pas.
b) Alat 2 (Tipe Dayung)
Alat ini sama dengan alat 1, bedanya pada alat ini digunakan dayung
yang terdiri dari daun dan batang logam sebagai pengaduk. Daun melewati
diameter batang sehingga dasar daun dan batang rata. Dayung memenuhi
spesifikasi dengan jarak 25 mm ± 2 mm antara daun dan bagian dasar wadah
yang dipertahankan selama pengujian berlangsung. Sediaan obat dibiarkan
tenggelam ke bagian dasar wadah sebelum dayung mulai berputar. Gulungan
kawat berbentuk spiral dapat digunakan untuk mencegah mengapungnya
sediaan.
2.4.2 Pengaruh bentuk sediaan terhadap laju disolusi
Faktor-faktor yang mempengaruhi laju disolusi dari bentuk sediaan
1. Faktor yang berkaitan dengan sifat fisikokimia obat
Sifat-sifat fisikokimia dari obat yang mempengaruhi laju disolusi meliputi
kelarutan, bentuk kristal, bentuk hidrat solvasi dan kompleksasi serta
ukuran-ukuran partikel. Sifat-sifat fisikokimia lain seperti kekentalan berperan terhadap
munculnya permasalahan dalam disolusi seperti terbentuknya flokulasi, flotasi
dan aglomerasi (Syukri, 2002).
2. Faktor yang berkaitan dengan formulasi sediaan
Formulasi sediaan berkaitan dengan bentuk sediaan, bahan pembantu dan
cara pengolahan. Pengaruh bentuk sediaan pada laju disolusi tergantung pada
kecepatan pelepasan bahan aktif yang terkandung pada kecepatan pelepasan bahan
aktif yang terkandung di dalamnya. Secara umum laju disolusi akan menurun
menurut urutan sebagai berikut: suspensi, kapsul, tablet, dan tablet salut. Secara
teoritis disolusi bermacam sediaan padat tidak selalu urutan dan masalahnya
sama, karena diantara masing-masing bentuk sediaan padat tersebut akan ada
perbedaan baik ditinjau dari segi teori maupun peralatan uji disolusi, seperti pada
sediaan berbentuk serbuk, kapsul, tablet-kaplet, suppositoria, suspensi, topikal dan
transdermal. Penggunaan bahan pembantu sebagai bahan pengisi, pengikat,
penghancur, dan pelicin dalam proses formulasi mungkin akan menghambat atau
mempercepat laju disolusi tergantung pada bahan pembantu yang dipakai. Cara
pengolahan dari bahan baku, bahan pembantu dan prosedur yang dilaksanakan
dalam formulasi sediaan padat peroral juga akan berpengaruh pada laju disolusi.
Perubahan lama waktu pengadukan pada granulasi basah dapat menghasilkan
tablet dengan waktu hancur dan disolusi yang lama.Faktor formulasi yang dapat
mempengaruhi laju disolusi diantaranya kecepatan disintegrasi, interaksi obat
dengan eksipien, kekerasan dan porositas (Siregar dan Wikarsa, 2010).
3. Faktor yang berkaitan dengan alat uji disolusi dan parameter uji Faktor ini sangat dipengaruhi oleh lingkungan selama percobaan yang
meliputi kecepatan pengadukan, suhu medium, pH medium dan metode uji yang
dipakai. Pengadukan mempengaruhi penyebaran partikel-partikel dan tebal
lapisan difusi sehingga memperluas permukaan partikel yang berkontak dengan
pelarut. Suhu medium berpengaruh terhadap kelarutan zat aktif. Untuk zat yang
kelarutannya tidak tergantung pH, perubahan pH medium disolusi tidak akan
mempengaruhi laju disolusi. Pemilihan kondisi pH pada percobaan in vitro
penting karena kondisi pH akan berbeda pada lokasi obat di sepanjang saluran
cerna sehingga akan mempengaruhi kelarutan dan laju disolusi obat (Syukri,
2002).
2.4.3 Syarat penerimaan hasil disolusi
Pada interval waktu yang ditetapkan dari media diambil cuplikan pada
daerah pertengahan antara permukaan media disolusi dan bagian atas dari
keranjang berputar atau daun dari alat dayung tidak kurang 1 cm dari dinding
wadah untuk analisis penetapan kadar dari bagian obat yang terlarut. Tablet harus
memenuhi syarat seperti yang terdapat dalam monografi untuk kecepatan disolusi
(Ditjen POM, 1995).
Pengujian dengan tiga tahap, Pada tahap 1 (S1), 6 tablet diuji. Bila pada
tahap 2 (S2). Pada tahap ini 6 tablet tambahan diuji lagi. Bila tetap tidak
memenuhi syarat, maka pengujian dilanjutkan lagi ke tahap 3 (S3). Pada tahap ini
12 tablet tambahan diuji lagi (Siregar dan Wikarsa, 2010).
Tabel 2.2. Tabel penerimaan hasil uji disolusi
Tahap Jumlah sediaan yang diuji Syarat penerimaan
S1 6 Tiap unit sediaan tidak kurang dari Q+
5%
S2 6 Rata-rata dari12 unit (S1+S2) adalah
sama dengan atau lebih besar dari Q dan tidak satu unit sediaan yang lebih kecil dari Q–15%
S3 12 Rata-rata dari 24 unit (S1+S2+S3 )
adalah sama dengan atau lebih besar dari Q, tidak lebih dari 2 unit sediaan yang lebih kecildari Q–15% dan tidak satupun unit yang lebih kecil dari Q–25%
Keterangan:
S1 : Tahap pertama S2 : Tahap kedua S3 : Tahap ketiga
Q : Jumlah zat aktif yang terlarut yang tertera dalam masing-masing monografi
Harga Q adalah jumlah zat aktif yang terlarut, seperti yang tertera dalam
masing-masing monografi, dinyatakan dalam persen dari jumlah yang tertera pada
etiket. Angka 5% dan 15% adalah persen dari jumlah yang tertera pada etiket
sehingga mempunyai arti yang sama dengan Q. Kecuali ditetapkan lain dalam
masing-masing monografi, persyaratan umum untuk penetapan satu titik tunggal
ialah terdisolusi 75% dalam 45 menit dengan menggunakan Alat 1 pada 100 rpm
2.5 Metode Penetapan Kadar Secara Spektrofotometri Ultraviolet (UV) 2.5.1 Defenisi
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum
dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas
cahaya yang ditransmisikan atau yang diabsorpsi. Jadi, spektrofotometer
digunakan untuk mengukur energi secara relatif jika energi tersebut
ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang
gelombang. Kelebihan spektrofotometer dibandingkan fotometer adalah panjang
gelombang dari sinar putih dapat lebih terseleksi dan ini diperoleh dengan alat
penguat seperti prisma ataupun celah optis (Gandjar dan Rohman, 2007).
Metode spektrofotometri UV-Vis adalah pengukuran intensitas sinar
ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar ultraviolet dan
cahaya tampak memiliki energi yang cukup untuk mempromosikan elektron pada
kulit terluar ke tingkat energi yang lebih tinggi. Spektrofotometri UV-Vis
biasanya digunakan untuk molekul organik di dalam larutan. Spektrumnya
mempunyai daerah yang lebar dan sedikit informasi yang bisa didapatkan dari
spektrum ini, tetapi spektrum ini sangat berguna untuk pengukuran secara
kuantitatif. Sinar ultraviolet berada pada panjang gelombang 200-400 nm,
sedangkan visible berada pada panjang gelombang 400-800 nm (Dachriyanus,
2.5.2 Instrumen
Komponen- komponen suatu spektrofotometer meliputi sebagai berikut:
- Sumber cahaya
Lampu deuterium digunakan untuk daerah UV pada panjang gelombang
dari 190-350 nm, sementara lampu halogen kuarsa atau lampu tungsten digunakan
untuk daerah visible (pada panjang gelombang antara 350-900 nm) (Gandjar dan
Rohman, 2007).
- Monokromator
Digunakan untuk mendispersikan sinar kedalam komponen-komponen
panjang gelombangnya yang selanjutnya akan dipilih oleh celah (slit).
Monokromator berputar sedemikian rupa sehingga kisaran panjang gelombang
dilewatkan pada sampel sebagai scan instrumen melewati spektrum (Gandjar dan
Rohman, 2007).
- Optik-optik
Dapat didesain untuk memecah sumber sinar, sehingga sumber sinar
melewati 2 kompartemen, dan sebagaimana dalam spektrofotometer berkas ganda
(double beam), suatu larutan blanko dapat digunakan dalam suatu kompartemen
untuk mengkoreksi pembacaan atau spektrum sampel. Yang paling sering
digunakan sebagai blanko dalam spektrofotometri adalah semua pelarut yang
digunakan untuk melarutkan sampel atau pereaksi (Gandjar dan Rohman, 2007).
- Detektor
Kebanyakan detektor menghasilkan sinyal listrik yang dapat mengaktifkan
kuantitatif berkaitan dengan tenaga cahaya yang mengenainya.
Persyaratan-persyaratan penting untuk detektor meliputi:
1) Sensitivitas tinggi hingga dapat mendeteksi tenaga cahaya yang
mempunyai tingkatan rendah sekalipun.
2) Waktu respon yang pendek (Sastrohamidjojo, 1991).
Menurut Gandjar dan Rohman (2007), hal-hal yang harus diperhatikan
dalam analisis spektofotometri ultraviolet adalah:
a. Pemilihan panjang gelombang maksimum
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah
panjang gelombang yang mempunyai absorbansi maksimal. Untuk memilih
panjang gelombang maksimal, dilakukan dengan membuat kurva hubungan antara
absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi
tertentu.
b. Pembuatan kurva baku
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai
konsentrasi. Masing-masing absorbansi larutan dengan berbagai konsentrasi
diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi
dengan konsentrasi.
c. Pembacaan absorbansi sampel atau cuplikan
Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2-0,6.
Anjuran ini berdasarkan anggapan bahwa pada kisaran nilai absorbansi tersebut