I. PENDAHULUAN
A. Latar Belakang
Karakteristik penting hasil pertanian salah satunya masih melakukan aktivitas respirasi. Akan tetapi respirasi yang terjadi tidak sama dengan tanaman induknya yang tumbuh dengan lingkungan aslinya, karena bahan hasil pertanian mengalami berbagai bentuk kejutan seperti hilangnya suplai nutrisi, proses panen, pengemasan dan transportasi dapat menimbulkan kerusakan mekanis. Hal ini akan mengakibatkan menurunnya kualitas bahkan kuantitas produk tersebut.
Aktivitas metabolisme pada buah dan sayuran segar dicirikan dengan adanya proses respirasi. Laju respirasi produk hortikultura selain dipengaruhi oleh suhu dan kelembaban, juga dipengaruhi oleh komposisi gas, terutama O2dan CO2 di sekitar produk. Laju respirasi dapat ditekan dengan menurunkan konsentrasi O2 dan menaikkan CO2 di sekitar produk. Komposisi gas di sekitar produk tersebut dikendalikan melalui pencampuran dari dua atau lebih gas-gas seperti udara, N2, O2 dan CO2 (Rokhani, 2007). Respirasi menghasilkan panas yang menyebabkan terjadinya peningkatan panas. Sehingga proses kemunduran seperti kehilangan air, pelayuan, dan pertumbuhan mikroorganisme akan semakin meningkat.
B. Tujuan
Tujuan dari penelitian ini adalah:
1. Mengkaji pengaruh suhu penyimpanan terhadap laju respirasi brokoli. 2. Mengkaji karakteristik respirasi brokoli selama penyimpanan.
3 II. TINJAUAN PUSTAKA
A. Brokoli (Brassica oleraceaL. var. italic)
Brokoli merupakan sayuran subtropik yang termasuk dalam golongan tanaman kubis-kubisan dan sering dikenal dengan nama kubis bunga hijau. Pemanenan brokoli dilakukan pada saat bunga mencapai ukuran maksimal dan telah padat (kompak), tetapi kuncup bunganya belum mekar. Umur panen adalah 47 - 67 hari setelah tanam. Waktu panen yang paling tepat adalah pagi dan sore hari, dengan cara memotong tangkai bunga bersama sebagian batang dan daun-daunnya sepanjang 25 cm dengan menggunakan pisau. Untuk pemasaran jarak jauh sebaiknya disertakan enam helai daun. Sedangkan untuk tujuan pemasaran dekat, hanya disertakan 3 - 4 helai daun, dan ujung-ujung daunnya dipotong (Rukmana, 1994). Brokoli mempunyai tingkat taksonomi sebagai berikut:
Divisi : Spermatophyta
Sub divisi : Dycotyledonae
Famili : Cruciferae
Genus : Brassica
Spesies : Brassica oleraceaL. var italic
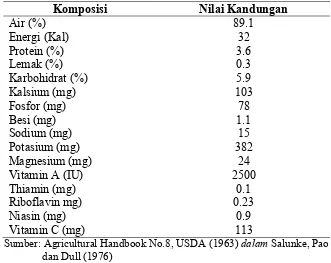
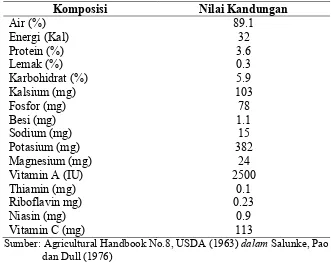
Tabel 1. Nilai nutrisi brokoli per 100 g bagian yang dapat dimakan
Sumber: Agricultural Handbook No.8, USDA (1963) dalam Salunke, Pao dan Dull (1976)
Rukmana (1994) menyebutkan kualitas brokoli dapat dilihat dari kekompakan bunga (curd density), kehijauannya, cacatnya, serta diameter bunganya. Menurut Susila (2006) pengelompokkan (grading) brokoli dilihat dari ukuran bunganya, yaitu:
- Grade 1 : diameter bunga 30 cm - Grade 2 : diameter bunga 25 - 30 cm - Grade 3 : diameter bunga 20 - 25 cm - Grade 4 : diameter 15 - 20 cm
5 dan pembusukan (Rokhani, 1995). Pra pendinginan dapat dilakukan dengan cara
hydrocooling atau dengan menggunakan es, jika kondisinya baik dan sirkulasi udara pada ruang penyimpanan sesuai maka brokoli dapat bertahan 10 - 14 hari pada suhu 0oC (Rokhani, 1995).
Brokoli memiliki umur simpan yang pendek, yaitu 1 - 2 hari pada kondisi suhu 20 oC, RH 60 – 70%; 2 - 6 hari pada kondisi suhu 4oC, RH 80 – 90 %; 1 - 2 minggu pada kondisi suhu 0 oC, RH 90 – 95 % dan dikemas dalam kotak
polystyrene yang diberi es (Tan, 2005 dalam Bafdal, et al., 2007). Menurut Bafdal, et al., (2007) bahwa jika 15 kg brokoli yang setelah dipanen diberi perlakuan hydrocoolingkemudian dimuat dalam kontainer yang diberi bongkahan es (ice crushed) sebanyak 3 kg dapat menjaga suhu di dalam kontainer 8.5 – 10.3 o
C selama 22 jam.
B. Karakteristik Respirasi
Menurut Winarno dan Kartakusuma (1981), respirasi adalah suatu proses metabolisme dengan cara menggunakan oksigen dalam pembakaran senyawa yang lebih kompleks seperti pati, gula, protein, lemak, dan asam organik, sehingga menghasilkan molekul yang sederhana seperti CO2, air serta energi dan molekul lain yang dapat digunakan oleh sel untuk reaksi sintesa.
Energi yang dikeluarkan berupa panas akibat respirasi (dikenal sebagai panas vital atau vital heat) mempengaruhi penerapan teknologi pasca panen, seperti memperkirakan kebutuhan sistem pendingin dan ventilasi (Kader, 1993). Menurut (Hardenburg, Watada dan Wang, 1968), reaksi kimia sederhana untuk proses respirasi dapat dituliskan sebagai berikut:
C6H12O6+ 6O2 6CO2+ 6H2O + 673 kcal
Menurut Phan et al., 1986 dalam Ananta, 1997 laju respirasi buah dan sayuran dipengaruhi oleh faktor luar dan faktor dalam. Faktor dalam yang mempengaruhi respirasi adalah tingkat perkembangan organ tanaman, ukuran produk, lapisan alamiah dan jenis jaringan. Faktor luar yang mempengaruhi adalah suhu, konsentrasi gas O2 dan CO2 yang tersedia, zat-zat pengatur tumbuh dan kerusakan yang ada pada buah dan sayuran.
Laju respirasi brokoli termasuk sangat tinggi (Kader, 1987; Hardenburg, Walada dan Wang, 1968). Semakin cepat laju respirasi maka semakin besar jumlah panas yang dilepaskan per satuan waktu. Laju respirasi besarnya bervariasi tergantung jenis komoditi, akan tetapi terutama dipengaruhi oleh suhu dan komposisi gas di sekitar komoditi tersebut (Kader, 1989; Saltveit, 1989; Manapperuma and Singh, 1987 dalam Rokhani, 1995).
B.1. Pengaruh Suhu
Laju respirasi brokoli dipengaruhi secara nyata oleh suhu penyimpanan, yaitu semakin tinggi suhu penyimpanan, laju respirasinya semakin besar; juga sebaliknya, laju respirasi semakin menurun dengan semakin rendahnya suhu penyimpanan; melalui pengaturan suhu dan kelembaban serta komposisi gas ruang penyimpanan, mutu produk hortikultura yang disimpan dapat dipertahankan (Rokhani, 1995). Laju respirasi brokoli yang digambarkan sebagai laju produksi CO2 (mg/kg jam) pada suhu penyimpanan 0 oC, 4 - 5 oC, 10 oC, 15 - 16 oC, dan 20 - 21 oC adalah berturut-turut (mg/kg jam) 19 - 21, 32 – 37, 75 - 87, 161 – 186, dan 278 – 320 (Hardenburg, Watada dan Wang, 1986). Laju respirasi brokoli juga dipengaruhi oleh ukuran floret (Tian, et al. dalamFinger, et al., 1999) dan jenis kultivarnya (Finger, et al., 1999).
7 respirasi telah berlangsung, dan sejauh mana proses itu bersifat aerobik atau anaerobik (Phanet al.,1986).
Tabel 2. Sifat-sifat respirasi berdasarkan tipe substrat yang digunakan
Tipe menunjukkan bahwa yang digunakan dalam respirasi itu suatu substrat yang mengandung oksigen, yaitu asam-asam organik. Bila kuosien respirasi kurang dari satu, maka ada beberapa kemungkinan, yaitu (a) substrat mempunyai perbandingan oksigen terhadap karbon yang lebih kecil daripada heksosa, (b) oksidasi belum tuntas, misalnya terhenti pada pembentukan asam suksinat atau zat antara lain; (c) CO2 yang dikeluarkan digunakan dalam proses-proses sintesis, misalnya pembentukan asam oksalat dan asam malat dari piruvat.
cenderung terhambat dikarenakan denaturasi enzim. Sedangkan suhu buah atau sayuran umumnya lebih tinggi dari ruang penyimpanan akibat panas respirasi. Perbedaan suhu tersebut cukup kritis dalam penentuan laju metabolisme produk.
Penjelasan tentang penurunan Q10 pada suhu yang tinggi adalah bahwa laju penetrasi O2 ke dalam sel lewat kutikula atau periderma mulai menghambat respirasi saat reaksi kimia berlangsung dengan cepat. Difusi O2 dan CO2 juga dipercepat dengan peningkatan suhu, tapi Q10 untuk proses fisika ini hanya 1.1 ; jadi suhu tidak mempercepat secara nyata difusi larutan lewat air. Peningkatan suhu sampai 40 °C atau lebih, laju respirasi malahan menurun, khususnya bila tumbuhan berada pada keadaan ini dalam jangka waktu yang lama. Enzim yang diperlukan mulai mengalami denaturasi dengan cepat pada suhu yang tinggi, mencegah peningkatan metabolik yang semestinya terjadi. Pada kecambah kacang kapri, peningkatan suhu dari 25 menjadi 45 °C mula-mula meningkatkan respirasi dengan cepat, tapi setelah dua jam laju respirasinya mulai berkurang. Kemungkinan penjelasannya ialah jangka waktu dua jam sudah cukup lama untuk merusak sebagian enzim respirasi (Salisbury & Ross, 1995).
B.2. Pengaruh Komposisi Gas
Komposisi gas yang utama dalam mempengaruhi respirasi adalah oksigen, karbondioksida, dan etilen (Kays, 1991). Beberapa penelitian telah menunjukkan bahwa komposisi O2 rendah dan CO2 tinggi akan menghambat laju respirasi. Pantastico et al., 1986 menyatakan bahwa etilen dapat mempercepat proses respirasi dan pembentukannya sekaligus didorong oleh laju respirasi. Dengan mengubah konsentrasi gas O2 menjadi 3 % dari 22 % dan meningkatkan konsentrasi CO2 menjadi 4 % dari keadaan normal, buah dan sayuran tidak mengalami efek kerusakan dan memperlambat proses pematangan selama beberapa hari (Liyod Ryall et al., 1982dalamTubagus, 1993).
9 komoditas. Penyimpanan dengan atmosfir termodifikasi dapat dilakukan dengan penyimpanan atmosfer terkendali (controlled atmosphere, CA) atau atmosfir modifikasi (modified atmosphere, MA)
Rokhani (1996) mengemukakan bahwa pada sistem CA komposisi gas dalam ruang penyimpanan diukur secara terus menerus dan perlu menginjeksikan gas atau campuran gas tertentu untuk mempertahankan komposisi gas yang diinginkan. Sedangkan sistem MA merupakan sistem statis tanpa melakukan monitoring komposisi gas selama penyimpanan. Komposisi gas pada penyimpanan sistem MA ditentukan dari komposisi gas awal yang terdapat dalam kemasan, laju konsumsi oksigen dan laju produksi karbondioksida oleh komoditas, sifatnya permeabelitas dari kemasan dan suhu penyimpanan.
Komposisi gas yang diinginkan pada sistem CA lebih teliti dibandingkan MA. Dalam praktiknya sistem CA memerlukan gas-gas pengendali seperti oksigen, karbondioksida dan nitrogen serta sejumlah peralatan untuk pengaturan dan pengendalian komposisi gas yang secara praktis diterapkan untuk penyimpanan dalam bentuk curah.
Menurut Wang dan Hruscha (1977) dalam Tubagus (1993) bahwa pada suhu penyimpanan 10 oC dengan modified atmosphere, brokoli yang tidak dikemas dapat bertahan selama 3 hari dan setelah hari ketujuh bahan akan menguning. Selanjutnya brokoli yang dikemas dengan film tertutup dapat dipertahankan mutunya sampai 14 hari. Pada penyimpanan 20 oC brokoli yang tidak dikemas hanya bertahan selama 2 hari dengan kemasan tertutup sampai hari kedua warna dapat dipertahankan tetapi mengalami kerusakan fisik.
penyimpanan. Pada kondisi ini kerusakan dan pembusukan akan tejadi setelah 10 hari penyimpanan.
B.3. Pola Respirasi
Buah-buahan dan sayuran dapat diklasifikasikan berdasarkan pola respirasi selama pematangan sebagi klimakterik dan non klimakterik. Istilah klimakterik dicetuskan oleh Kidd dan West (1925) dalam Pantastico (1986), yang pertama kali menguraikan gejala tersebut pada saat meneliti fisiologi pasca panen apel
Bramley Seedling (diukur dengan produksi CO2) pada suhu 12.2 oC adalah lambat dan konstan pada waktu tertentu, lalu sesudah itu meningkat sampai puncak (klimaks). Oleh karena itu mereka menamakan fenomena tersebut dengan kenaikan klimakterik. Hal ini menyimpulkan bahwa ciri dari proses klimakterik adalah kenaikan produksi CO2yang mendadak.
Menurut Biale (1954) dalam Kays (1991), buah non klimakterik akan bereaksi terhadap pemberian C2H4 pada tingkat manapun dengan kenaikan laju konsumsi O2 yang tergantung pada konsentrasi etilen sedangkan pada buah klimakterik, peningkatan konsentrasi C2H4 hanya akan menggeser pola respirasi secara horizontal. Buah klimakterik mengadakan reaksi respiratik bila C2H4 diberikan dalam keadaan pra klimakterik, dan tidak lagi peka terhadap C2H4 setelah masa kenaikan klimakterik terlampaui.
C. Teknik Pengukuran Laju Respirasi
Dalam proses respirasi beberapa senyawa penting yang dapat digunakan untuk mengukur laju respirasi adalah perubahan kandungan glukosa, jumlah ATP, CO2 yang diproduksi dan O2 yang dikonsumsi. Dari keempat cara tersebut, pengukuran dengan menghitung produksi CO2 lebih sederhana dan lebih praktis. Sedangkan menentukan jumlah O2 yang dikonsumsi dapat dilakukan dengan alat yang mempunyai kepekaan tinggi seperti kromatografi gas karena jumlahnya relatif sedikit (Winarno dan Kartakusuma, 1981).
11 jaringan (internal) atau dari gas yang ditimbulkan oleh jaringan (eksternal). Pengukuran laju respirasi dengan mengambil sampel gas secara internal telah dilakukan oleh Saltveit (1982). Dibandingkan cara internal, pengambilan sampel gas secara eksternal lebih sederhana dan tidak merusak bahan. Terdapat dua metode dalam pengambilan sampel gas secara eksternal, yaitu metode statis atau sistem tertutup (closed system) dan metode dinamis atau sistem terbuka (open system).
Dalam metode sistem tertutup bahan ditempatkan dalam suatu wadah tertutup dimana gas CO2 yang dihasilkan terakumulasi dan gas O2 yang dikonsumsi menjadi berkurang konsentrasinya. Laju respirasi dihitung dengan mengetahui berat bahan, volume bebas wadah, dan perbedaan konsentrasi setelah waktu tertentu (Rokhani, 1996). Mannapperuma dan Singh (1990) menyatakan persamaan laju respirasi sistem tertutup pada suhu tertentu dengan satuan ml/kg-jam seperti pada persamaan (1) dan (2).
R1 (1)
R2 (2)
dimana
R = laju respirasi (ml/kg jam)
x = konsentrasi gas (desimal)
t = waktu (jam)
V = volume bebas (ml)
W = berat produk (kg)
subskrip 1, 2 = masing-masing menyatakan gas O2dan CO2.
outlet gas pada “respiration chamber”. Mannapperuma dan Singh (1990) menentukan laju respirasi pada sistem terbuka berdasarkan kesetimbangan massa oksigen dan karbondioksida. Sedangkan kesetimbangan massa nitrogen digunakan untuk menghitung laju aliran gas masuk. Persamaan kesetimbangan untuk oksigen, karbondioksida, dan nitrogen ditunjukkan dalam persamaan berikut:
Kesetimbangan O2 : R1 = (Gx1– Qy1) /W (3)
Kesetimbangan CO2 : R2 = (Gx2– Qy2) /W (4)
Kesetimbangan N2 : G = Q(y3/x3) (5)
dimana
R = laju respirasi (ml/kg jam)
G = laju respirasi gas masuk (ml/jam)
Q = laju aliran gas keluar (ml/jam)
W = berat produk (kg)
x = konsentrasi gas masuk (desimal)
y = konsentrasi gas keluar (desimal)
subskrip 1, 2, dan 3 masing-masing menyatakan gas O2, CO2, dan N2.
D. Model Pendugaan
13 optimalisasi dalam objek dan untuk mengadakan pendugaan atau prediksi untuk memperbaiki keadaan objek. Dari model matematika dapat diperoleh gambaran yang lebih jelas mengenai objek tanpa harus mengganggu keberadaan objek. Pengembangan model matematika merupakan suatu siklus fenomena yang berdasarkan konsep model verbal.
Metode pengkorelasian yang akan digunakan adalah metode regresi linear yaitu:
Linear sederhana : R = a + bT (6)
Eksponensial : R = aebT (7)
Logaritmik : R = aTb (8)
Untuk menyatakan laju respirasi sebagai fungsi suhu dapat digunakan persamaan Arrhenius:
R = Ro e–E/RT (9)
dimana
R = konstanta penurunan konsentrasi
Ro= konstanta E = energi aktivasi T = suhu mutlak (C+273)
III.METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Maret 2010 di Laboratorium Teknologi Pengolahan Hasil Pertanian (TPPHP) Departemen Teknik Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
B. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah brokoli (Brassica oleracea L. var. italic) yang didapat di daerah sekitar Bogor. Sedangkan peralatan yang digunakan adalah unit pencampur gas, stoples, inkubator, gas analyzer IRA-107 untuk mengukur konsentrasi CO2 dan portable oxygen tester POT-101 untuk mengukur konsentrasi O2, timbangan dan alat penunjang lainnya.
C. Metode Penelitian
C.1. Pengukuran laju respirasi
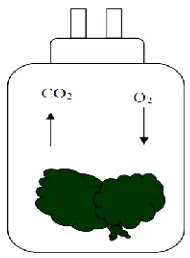
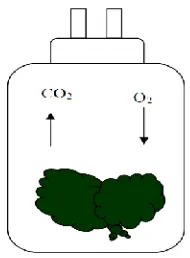
Pengukuran laju respirasi dengan menggunakan sistem tertutup, yaitu: tutup stoples yang digunakan dilubangi dengan diameter 1 cm sebanyak dua buah dan pada lubang tersebut dimasukkan selang plastik sepanjang 30 cm. Pada pertemuan selang plastik dengan penutup stoples diberi lem dan lilin malam untuk menghindari kebocoran gas.
15 Brokoli segar dibersihkan dan dipilih bunga (floret) yang memiliki bentuk fisik yang baik dan seragam, kemudian ditimbang dan dimasukkan ke dalam stoples dan ditutup rapat. Untuk menghindari kebocoran gas, antara penutup dan leher stoples diberi lilin malam dan selang plastiknya ditekuk dan dijepit.
Pengukuran kandungan gas dilakukan tiap 24 jam, dan diukur dengan 3 kali ulangan masing-masing berjarak 3 jam. Pengukuran dilakukan setiap hari sampai brokoli busuk. Setelah dilakukan pengukuran, stoples dibuka untuk mengembalikan udara ke kondisi normal.
Gambar 3. Skema kegiatan pengukuran laju respirasi
C.2. Rancangan percobaan
dihitung berdasarkan konsentrasi gas O2 atau CO2, volume bebas, interval waktu dan berat sampel seperti pada persamaan (1) dan (2). Berikut perlakuan-perlakuan dalam penelitian (Tabel 2).
Tabel 3. Perlakuan-perlakuan penelitian
Perlakuan Suhu (oC) Ulangan Berat per sampel (g)
Model aditif RAL yang digunakan adalah:
(10) dimana
Yij = nilai pengamatan dari perlakuan ke-i dan ulangan ke-j µ = nilai tengah umum
= tambahan akibat perlakuan ke-i
= tambahan akibat acak galat percobaan dari percobaan dari perlakuan ke-i pada ulangan ke-j
Analisis data yang digunakan adalah uji GLM untuk menguji keragaman dan dilanjutkan dengan uji Duncan.
C.3. Model pendugaan respirasi
Setelah dilakukan pengukuran konsentrasi gas O2 dan gas CO2 kemudian dilakukan perhitungan untuk menentukan laju respirasi dari brokoli. Kemudian langkah selanjutnya adalah memprediksi laju respirasi brokoli terhadap suhu. Digunakan empat model matematika yaitu berdasarkan persamaan (6), (7), (8), (9). Dari keempat model tersebut dipilih model yang terbaik berdasarkan koefisien determinasi masing-masing model.
17
lnR = ln a + b T (11)
atau
ln R = α+ βT (12)
Persamaan (8) ditransformasi menjadi:
log R = log a + blog T (13)
atau
log R = α + βlog T (14)
Persamaan (10) ditransformasi menjadi:
ln R = ln Ro – (E/R)(1/T) (15)
atau
ln R = α–β(1/T) (16)
dimana
α = peubah intersep
β = kemiringan
IV. HASIL DAN PEMBAHASAN
A. Pengaruh Suhu pada Respirasi Brokoli
Pada hasil penelitian menunjukkan bahwa brokoli mempunyai respirasi yang tinggi. Namun pada suhu yang rendah, hasil pengamatan menunjukkan bahwa konsentrasi O2 yang dikonsumsi dan produksi CO2 semakin sedikit (Lampiran 1) yang menunjukkan bahwa respirasi brokoli pada suhu rendah lebih lambat dibandingkan dengan suhu ruang. Lampiran 2 menunjukkan laju respirasi (konsumsi O2 dan produksi CO2) pada suhu 5 oC, 10 oC, 15 oC, 20 oC, dan 27 oC (suhu ruang).
19 menghasilkan molekul yang sederhana seperti CO2, sehingga pada suhu penyimpaan yang lebih tinggi konsentrasi CO2yang semakin besar dan konsumsi O2yang semakin besar pula.
B. Karakteristik Respirasi B.1. Pola Respirasi Brokoli
Laju respirasi petunjuk yang baik untuk daya simpan buah dan sayuran sesudah dipanen. Intensitas respirasi dianggap sebagai ukuran laju jalannya metabolisme, oleh karena itu sering dianggap sebagai petunjuk mengenai potensi daya simpan buah.
Menurut Soesarsono (1988) dalam Nugroho (1997) buah dan sayuran dapat digolongkan atas dasar laju pemasakan yaitu golongan klimakterik dan non klimakterik. Golongan klimakterik ditandai dengan proses yang cepat pada fase pemasakan (ripening) dan peningkatan respirasi yang mencolok. Sebaliknya golongan non klimakterik tidak terlihat nyata perubahan pada fase pemasakannya karena proses respirasi berjalan lambat. Penurunan laju respirasi merupakan petunjuk terjadinya kerusakan enzim (Pantastico, 1989).
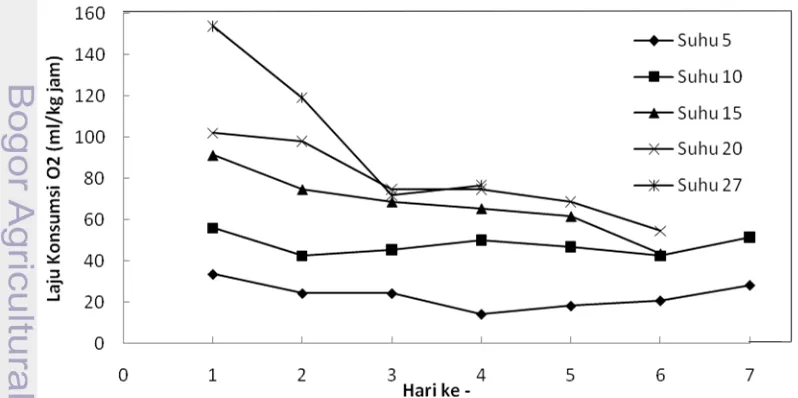
Gambar 4. Grafik laju konsumsi O2pada 7 hari penyimpanan
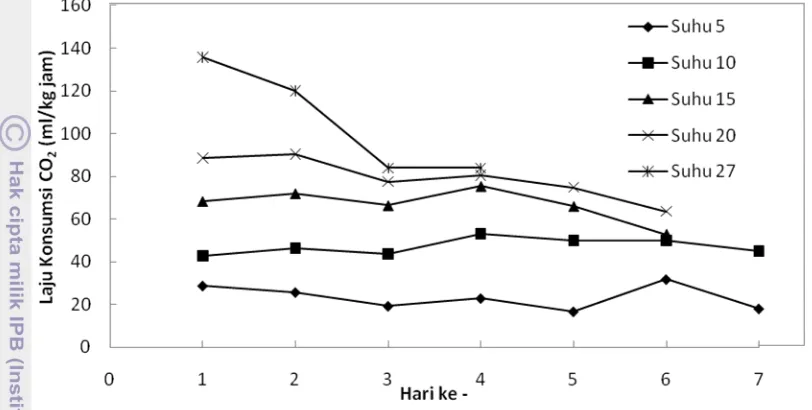
Gambar 5. Grafik laju produksi CO2pada 7 hari penyimpanan
Jika dilihat posisi grafik untuk masing-masing perlakuan suhu, Gambar 4 dan Gambar 5 menunjukkan bahwa laju respirasi brokoli sangat dipengaruhi oleh suhu penyimpanan. Pada suhu penyimpanan 5oC posisi grafik berada pada paling bawah yang menunjukkan bahwa pada suhu 5 oC brokoli mengkonsumsi O2 dan memproduksi CO2 paling sedikit diantara suhu penyimpanan lainnya. Sedangkan pada suhu penyimpanan 27 oC posisi grafik berada paling atas dan menunjukkan bahwa pada suhu 27oC (suhu ruang) memiliki laju respirasi yang paling tinggi.
21 enzim respiratoris (Solomos, 1983 dalam Asrofi, 1986). Kondisi demikian menyebabkan terjadinya peningkatan proses metabolisme dalam jaringan, sehingga sayuran dapat membusuk.
Menurunnya jumlah CO2 yang dihasilkan dapat disebabkan karena menurunnya konsentrasi ADP yang bersifat sebagai akseptor fosfat dan terjadinya kerusakan mitokondria (Winarno dan Kartakusuma, 1981). Konsentrasi ADP yang menurun dan kerusakan mitokondria menyebabkan ATP yang dihasilkan juga menurun. ATP yang berfungsi sebagi penyuplai energi dalam bentuk fosfat berenergi tinggi dengan cara memecah ikatan fosfatnya (Wills et al., 1981 dalam
Asrofi, 1986). Karena ATP menurun, maka energi yang dapat digunakan untuk melangsungkan reaksi metabolik selanjutnya juga menurun. Keadaan demikian menyebabkan jumlah CO2yang dihasilkan semakin menurun.
Pada penelitian ini pola respirasi brokoli menunjukkan kecenderungan yang terus menurun dan tidak terjadi kenaikan produksi CO2 yang mendadak. Dengan demikian dapat disimpulkan bahwa brokoli termasuk sayuran non klimakterik.
B.2. Respiratory Quotient(RQ)
Respirasi membutuhkan O2dan menghasilkan zat sisa metabolisme berupa uap air, CO2, dan panas sebagai entropi (energi panas yang tidak termanfaatkan). Kuosien respirasi (respiratory quotient) merupakan perbandingan CO2 terhadap O2. Nilai RQ brokoli ditunjukkan pada Tabel 4.
Tabel 4. Hasil uji Duncan laju respirasi dan respiratory quotient(RQ) brokoli
Suhu (oC) Laju respirasi (ml/kg jam)
Hasil uji Duncan (Lampiran 3 dan 4) menunjukkan bahwa laju konsumsi O2 berbeda nyata untuk suhu 15 oC, 20 oC, dan 27 oC berbeda nyata. Hasil uji pada suhu 5 oC dan 10 oC tidak berbeda nyata yang berarti laju konsumsi O2 hampir sama. Sedangkan laju produksi CO2berbeda nyata untuk suhu 5oC, 10oC, dan 27 oC. Hasil uji pada suhu 15 oC dan 20 oC tidak berbeda nyata. Laju konsumsi O2 dan laju produksi CO2pada suhu 5 oC dan 10 oC (Gambar 4 dan 5) merupakan laju terkecil diantara suhu penyimpanan lainnya. Sehingga dalam penelitian ini, suhu tersebut merupakan suhu terbaik untuk penyimpanan brokoli.
Pada Tabel 3 menunjukkan nilai RQ brokoli yang disimpan pada lima suhu penyimpanan yang berbeda. Nilai RQ brokoli hampir seluruhnya bernilai 1.0, hal ini menunjukkan bahwa proses metabolisme berlangsung secara normal menggunakan substrat karbohidrat, protein atau lemak dengan ketersediaan oksigen yang cukup. Komponen terbesar pada brokoli setelah air adalah karbohidrat. Dengan demikian dapat dikatakan bahwa substrat yang digunakan untuk proses respirasi sebagian besar adalah karbohidrat. Pada kondisi respirasi anaerobik umumnya nilai RQ lebih besar dari satu.
B.3. Q10 (Kuosien Suhu)
Karakter perubahan pada laju reaksi akibat suhu tersebut biasanya ditentukan dengan kuosien suhu (Q10), yaitu rasio laju reaksi tertentu pada suatu tingkat suhu (T1) terhadap laju reaksi tersebut saat suhu naik 10 oC (T1+ 10 oC). Nilai Q10brokoli ditunjukkan pada Tabel 5.
23 diperlukan mulai mengalami denaturasi dengan cepat pada suhu yang tinggi, mencegah peningkatan metabolik yang semestinya terjadi.
Tabel 5. Nilai Q10berdasarkan perhitungan model
Model nilai Q10 dengan Kays (1991) yang menyatakan pada kebanyakan produk, nilai Q10 berkisar antara 2.0 – 2.5 saat suhu 5 oC hingga 25 oC hal ini dimungkinkan karena brokoli mempunyai laju respirasi yang terlalu tinggi sehingga suhu dalam stoples lebih tinggi dari ruang penyimpanan akibat panas respirasi yang mengakibatkan enzim terdenaturasi lebih cepat.
Tabel 6. Nilai Q10pada 3 skala suhu
C. Model Pendugaan Respirasi
Pengukuran laju respirasi dilakukan karena laju respirasi merupakan salah satu parameter yang dibutuhkan untuk menduga konsentrasi O2 dan CO2. Penurunan konsentrasi O2dan peningkatan konsentrasi gas CO2merupakan suatu tanda bahwa sayuran mengalami proses respirasi.
Laju respirasi ditentukan berdasarkan konsentrasi gas sebelum dan setelah melewati sampel bahan. Komposisi gas dianalisis menggunakan gas analyzer. Dengan menggunakan persamaan (1) dan (2) maka diperoleh laju respirasi yang menyatakan konsumsi O2dan laju produksi CO2.
Model digunakan untuk menghitung estimasi laju respirasi brokoli pada waktu tertentu untuk mengoptimalkan waktu penyimpanan. Untuk menyusun sebuah persamaan terlebih dahulu harus mendapatkan pasangan data yang akan dianalisis. Data yang akan diambil untuk dijadikan bahan penyusunan persamaan adalah data hari pertama sampai keempat, karena setelah hari keempat data suhu yang didapatkan tidak lengkap karena brokoli pada suhu ruangan telah busuk, sehingga tidak dimungkinkan untuk pengambilan sampel gas (Lampiran 1).
Dari data eksperimen laju respirasi brokoli pada berbagai suhu selama 4 hari ditunjukkan pada Lampiran 2. Pendugaan laju respirasi dilakukan dengan analisis regresi untuk menentukan model persamaan dan akan dipilih empat kemungkinan model regresi, yatu model regresi linear sederhana, eksponensial, logaritmik, dan Arrhenius. Laju respirasi adalalah peubah tak bebas, sedangkan peubah bebas yang digunakan adalah suhu. Suhu merupakan faktor yang sangat berpengaruh terhadap kecepatan reaksi, kecepatan reaksi meningkat seiring dengan peningkatan suhu. Hasil dari penyususunan model akan dibandingkan dengan hasil pengukuran respirasi dan akan ditentukan model terbaik dari model yang telah disusun. Pemilihan model terbaik berdasarkan nilai R2yang terbesar.
Dalam analisis regresi, koefisien determinasi adalah ukuran dari
25 antara X dan Y dalam persamaan tersebut. Koefisien determinasi, adalah sebuah besaran yang mengukur ketepatan garis regresi. Nilai R2 ini menunjukkan persentase besarnya variabilitas dalam data yang dijelaskan oleh model regresi. Maksimum nilai R2 adalah 100% dan minimal 0. Jika nilai R2= 100 %, misalnya untuk regresi linier sederhana semua titik data akan menempel ke garis regresi, semakin kecil R2maka data makin menyebar jauh dari garis. Oleh karena itu jika R2 kecil maka keeratan hubungan antara X dan Y lemah dan jika R2 = 0 menunjukkan bahwa X tidak memiliki hubungan dengan Y.
Tabel 7. Model perhitungan hasil transformasi untuk konsumsi O2
Model Parameter model (rata-rata)
α β R2
1. Regresi linear sederhana 11.12 3.69 0.9663
2. Eksponensial 3.11 0.06 0.8705
3. Logaritmik 0.78 0.90 0.9848
4. Arrhenius 22.80 5404.00 0.8854
Tabel 8. Model perhitungan hasil transformasi produksi CO2
Model Parameter model (rata-rata)
α β R2
1. Regresi linear sederhana 9.36 3.70 0.9861
2. Eksponensial 3.09 0.06 0.9028
3. Logaritmik 0.78 0.88 0.9943
4. Arrhenius 22.80 5411.07 0.9155
Keterangan: R2= Koefisien determinasi
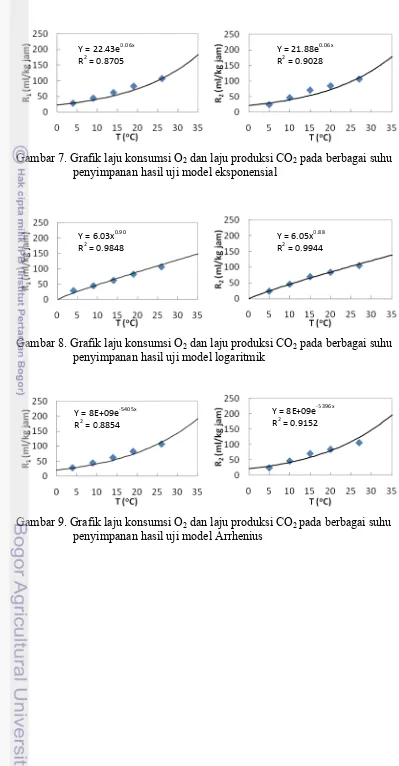
Tabel 7 dan 8 menyajikan transformasi persamaan dari empat model yang digunakan untuk pendugaan laju respirasi rata-rata, sedangkan untuk hasil ulangan dapat dilihat pada Lampiran 3 dan 4. Gambar 6, 7, 8, dan 9 menyajikan grafik dari keempat model persamaan respirasi rata-rata brokoli, sedangkan untuk hasil ulangan dapat dilihat pada Lampiran 5, 6, 7, dan 8 .
model eksponensial, 0.9848 untuk model logaritmik, dan 0.8854 untuk model Arrhenius. Koefisien determinasi terbesar untuk pendugaan konsumsi O2 adalah dengan model logaritmik.
Untuk produksi CO2 juga mempunyai koefisien determinasi yang bervariasi yaitu diantara 0.9861 untuk model linear sederhana, 0.9028 untuk model eksponensial, 0.9943 untuk model logaritmik dan 0.9155 untuk model Arrhenius. Koefisien determinasi terbesar untuk pendugaan produksi CO2 adalah dengan linear sederhana dan model logaritmik.
Gambar 6, 7, 8, dan 9 menyajikan grafik laju respirasi brokoli pada berbagai suhu penyimpanan keempat model matematika. Data laju respirasi brokoli pada berbagai suhu penyimpanan empat model dapat dilihat pada Lampiran 11. Laju konsumsi O2pada hasil percobaan pada suhu 5 oC adalah 24.0 ml/kg jam, model regresi linear 29.57 ml/kg jam, model eksponensial 30.28 ml/kg jam, model logaritmik 25.67 ml/kg jam, dan model Arrhenius 28.90 ml/kg jam. Laju produksi CO2pada hasil percobaan pada suhu 5 oC adalah 24.3 ml/kg jam, model regresi linear 27.86 ml/kg jam, model eksponensial 29.53 ml/kg jam, model logaritmik 24.94 ml/kg jam, dan model Arrhenius 29.74 ml/kg jam. Dari keempat model tersebut model logaritmik yang paling mendekati nilai laju respirasi hasil percobaan.
Gambar 6. Grafik laju konsumsi O2 dan laju produksi CO2pada berbagai suhu penyimpanan hasil uji model linear sederhana
Y = 3.69x + 11.12 R2= 0.9663
27 Gambar 7. Grafik laju konsumsi O2dan laju produksi CO2pada berbagai suhu
penyimpanan hasil uji model eksponensial
Gambar 8. Grafik laju konsumsi O2dan laju produksi CO2pada berbagai suhu penyimpanan hasil uji model logaritmik
Gambar 9. Grafik laju konsumsi O2dan laju produksi CO2 pada berbagai suhu penyimpanan hasil uji model Arrhenius
Y = 22.43e0.06x R2= 0.8705
Y = 21.88e0.06x R2= 0.9028
Y = 6.03x0.90 R2= 0.9848
Y = 6.05x0.88 R2= 0.9944
Y = 8E+09e-5405x R2= 0.8854
V. KESIMPULAN DAN SARAN
A. Kesimpulan
1. Laju respirasi brokoli dipengaruhi oleh suhu penyimpanan. Pada suhu penyimpanan rendah laju respirasi brokoli rendah dan sebaliknya, yaitu laju respirasi semakin tinggi dengan semakin tingginya suhu penyimpanan.
2. Pola respirasi brokoli menunjukkan kecenderungan yang terus menurun dan tidak terjadi kenaikan produksi CO2 yang mendadak. Pola ini menunjukkan bahwa brokoli termasuk sayuran non klimakterik.
3. Nilai RQ brokoli hampir seluruhnya bernilai 1.0, hal ini menunjukkan bahwa proses metabolisme berlangsung secara normal (aerobik).
4. Nilai Q10 brokoli hasil pendugaan laju respirasi dengan menggunakan model berkisar antara 1.72 – 1.88 yang berarti bahwa setiap kenaikan suhu sebesar 10oC laju respirasi akan meningkat sebanyak 1.72 - 1.88 kali.
5. Untuk menduga laju respirasi pada brokoli di berbagai suhu penyimpanan dapat digambarkan dengan model logaritmik karena lebih baik diantara keempat model matematika.
B. Saran
SKRIPSI
MODEL PENDUGAAN LAJU RESPIRASI BROKOLI
(
Brassica oleracea
L. var. italic)
PADA BERBAGAI SUHU PENYIMPANAN
Oleh:
DWI JAYANTI AGUSTINA F14062586
2010
DEPARTEMEN TEKNIK PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
DAFTAR PUSTAKA
Asrofi, Yamis. 1986. Mempelajari Pola Respirasi dengan Cara Pengeringan dari Buah Salak (Salacca edolis, Reinw).(Skripsi). Departemen Teknik Pertanian, Fakultas Teknologi Peranian, IPB. Bogor.
Hardenburg RE, AE Watada, CY Wang. 1986. The Commercial Storage of Fruits, Vegetables, and Florits and Nursery Stocks. Departement of Agricultural, Agricultural Handbook No. 66 (Revised), 13p. USA.
Hardenburg RE. 1997. Dasar-dasar Pengemasan. Di dalam: Pantastico EB, editor. Fisiologi Pascapanen Penanganan dan Pemanfaatan Buah-buahan dan Sayur-sayuran Tropika dan Subtropika.Ed ke-4.Kamariyani, penerjemah; Tjitrosoepomo, editor.Gadjah Mada University Press.Yogyakarta.
http//en.wikipedia.org/wiki/Category:Brassica_oleraca.
Kader AA. 1993. Postharvest Biology and Technology : An Overview. Di dalam Kumpulan Materi Pelatihan Pascapanen Buah-buahan dan Sayur-sayuran; PAU Pangan dan Gizi Institut Pertanian Bogor, 10 – 15 Mei 1993.
Kitinoja L, AA Kader. 2002. Praktik-praktik Penanganan Pascapanen Skala Kecil : Manual untuk Produk Hortikultura (Edisi ke 4). Terjemahan. Postharvest Horticulture Series No.8 (Juli 2002), University of California, Davis, Postharvest Technology Research and Information Center. USA.
Koh et al. Content of Ascorbic Acid, Quercetin, Kaempferol and Total Phenolics in Commercial Broccoli. Journal of Food Composition and Analysis 22 (2009) 637-643. http://www.elsevier.co./locate/jfca.
La Rianda et al. Pengkajian Karakteristik dan Pendugaan Umur Simpan Jambu Mete Segar (Anacardium occidentale L.) pada Sistem Penyimpanan Atmosfir Termodifikasi. Buletin Keteknikan Pertanian Vol. 14, No. 1, April 2000.http://www.google.co.id/LaaRianda_PengkajianKarakteristikdanPend ugaan.pdf-Adobe Reader. [5 Pebruari 2010].
30 Muchtadi, Deddy. 1992. Fisiologi Pasca Panen Sayuran dan Buah-Buahan. Pusat
antar Unversitas Pangan dan Gizi. IPB. Bogor.
Nugroho, Ananta Puji. 1997. Mempelajari Laju Respirasi Buah Nenas Iris dalam Keadaan Terolah Minimal.(Skripsi). Departemen Teknik Pertanian, Fakultas Teknologi Peranian, IPB. Bogor.
Pantastico, E.R.B. 1986. Fisiologi Pasca Panen, Penanganan dan Pemanfaatan Buah-Buahan dan Sayuran Tropika dan Subtropika. Terjemahan. Gajah Mada University Press.Yogyakarta.
Rahardi, F., R. Pulungkun, A. Budiarti. 1994. Agribisnis Tanaman Sayur. Penebar Swadaya. Jakarta.
Rokhani, H dan E Darmawati.1995. Mempelajari Laju Transpirasi dan Pengaruh Komposisi Gas pada Penyimpanan Brokoli secara Controlled Atmosphere
[Laporan Penelitian]. Bogor: Jurusan Mekanisasi Pertanian FATETA Institut Pertanian Bogor.
Rokhani, H. 1996. Rancang Bangun Sistem Pencampuran Gas dan Pengukuran Laju Respirasi pada Penyimpanan Hortikultura secara Atmosfir Terkendali. Bogor: Jurusan Mekanisasi Pertanian FATETA Institut Pertanian Bogor.
Rokhani, H. 2007. Teknik Pengukuran Laju Transpirasi Produk Hortikultura pada Kondisi Atmosfir Terkendali, Bagian I: Metode Sistem Tertutup. Jurnal Keteknikan Pertanian Vol. 21 No. 4, Desember 2007.
Roosmani. A. B. 1975. Percobaan Pendahuluan Terhadap Buah-Buahan dan Sayuran Indonesia.Buletin Penelitian Hortikultura LPH Pasar Minggu. Jakarta.
Rukmana, M. R. 1994.Kubis Bunga dan Brokol, edisi I. Kanisius Yogyakarta. Winarno, F.G dan M. Aman Kartakusuma. 1981. Fisiologi Lepas Panen. Sentra
Hudaya. Jakarta.
Salisbury, Frank and Ross, Cleon. 1995. Fisiologi Tumbuhan Jilid 2. Penerbit ITB.Bandung.
Sutrisno.2007. Pengendalian Respirasi untuk Mempertahankan Mutu Pasca Panen Produk Segar Hortikultura. Jurnal Keteknikan Pertanian Vol. 21 No. 3, September 2007.
Tubagus, mulyadi. 1993. Mempelajari Penyimpanan Brokoli (Brasica oleraceaL. var. italica) dan Kembang Kol (Brasica oleracea L . var . botrytis) dengan "Modified Atmosphere". (Skripsi). Departemen Teknik Pertanian, Fakultas Teknologi Peranian, IPB. Bogor.
SKRIPSI
MODEL PENDUGAAN LAJU RESPIRASI BROKOLI
(
Brassica oleracea
L. var. italic)
PADA BERBAGAI SUHU PENYIMPANAN
Oleh:
DWI JAYANTI AGUSTINA F14062586
2010
DEPARTEMEN TEKNIK PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
MODEL PENDUGAAN LAJU RESPIRASI BROKOLI
(
Brassica oleracea
L. var. italic)
PADA BERBAGAI SUHU PENYIMPANAN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada jurusan Teknik Pertanian, Fakultas Teknologi Pertanian,
Institut Pertanian Bogor.
Oleh:
DWI JAYANTI AGUSTINA F14062586
2010
DEPARTEMEN TEKNIK PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
ii Judul Skripsi : Model Pendugaan Laju Respirasi Brokoli (Brassica oleraceaL.
var. italic) pada Berbagai Suhu Penyimpanan Nama : Dwi Jayanti Agustina
NIM : F14062586
Menyetujui Bogor, Oktober 2010
Dosen Pembimbing,
Dr. Ir. Rokhani Hasbullah, M.Si NIP: 19640813 199102 1 001
Mengetahui:
Ketua Departemen,
Dr. Ir. Desrial, M.Eng NIP: 19661201 199103 1 004
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 1 September 1988 di Kabupaten Cirebon, Jawa Barat. Orang tua penulis adalah Yanto Sunarto dan Sopiyah. Penulis memulai pendidikan formalnya pada tahun 1994 - 2000 di SDN III Kertawinangun, tahun 2000 - 2003 di SLTPN 1 Cirebon Barat, tahun 2003 - 2006 di SMAN 2 Cirebon, tahun 2006 - 2010 di Institut Pertanian Bogor.
iv Dwi Jayanti Agustina. F14062586. Model Pendugaan Laju Respirasi Brokoli (Brassica oleracea L. var. italic) di Berbagai Suhu Penyimpanan. Dosen Pembimbing: Dr. Ir. Rokhani Hasbullah,M.Si
RINGKASAN
Karakteristik penting hasil pertanian salah satunya masih melakukan aktivitas respirasi. Respirasi adalah suatu proses metabolisme dengan cara menggunakan oksigen dalam pembakaran senyawa yang lebih kompleks seperti pati, gula, protein, lemak, dan asam organik, sehingga menghasilkan molekul yang sederhana seperti CO2, air serta energi dan molekul lain yang dapat digunakan oleh sel untuk reaksi sintesa. Laju respirasi buah dan sayuran dipengaruhi oleh faktor luar dan faktor dalam. Faktor dalam yang mempengaruhi respirasi adalah tingkat perkembangan, ukuran produk, lapisan alamiah dan jenis jaringan. Faktor-faktor luar yang mempengaruhi adalah suhu, konsentrasi gas O2 dan CO2 yang tersedia, zat-zat pengatur tumbuh dan kerusakan yang ada pada buah dan sayuran.
Tujuan dari penelitian ini adalah mengkaji pengaruh suhu penyimpanan terhadap laju respirasi brokoli, mengkaji pola respirasi brokoli selama penyimpanan, membuat model pendugaan respirasi brokoli pada berbagai suhu penyimpanan.
Bahan yang digunakan dalam penelitian ini adalah brokoli (Brassica oleracea L. var. italic) yang didapat di daerah sekitar Bogor. Sedangkan peralatan yang digunakan adalah unit pencampur gas, stoples, inkubator, gas analyzer IRA-107 untuk mengukur konsentrisi CO2 dan portable oxygen tester POT-101 untuk mengukur konsentrasi O2, timbangan dan alat penunjang lainnya. Metode penelitian ini terdiri dari pengukuran laju respirasi (konsumsi O2 dan produksi CO2) diukur pada suhu 5 oC, 10 oC, 15oC, 20 oC, dan 27 oC serta pendugaan laju respirasi dengan empat model.
kenaikan suhu sebesar 10 oC laju respirasi akan meningkat sebanyak 1.72 - 1.88 kali.
vi KATA PENGANTAR
Puji syukur penulis ucapkan kehadirat Allah SWT atas berkat, rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi “Model Pendugaan Laju Respirasi Brokoli (Brassica oleracea L. var. italic) pada Berbagai Suhu Penyimpanan” sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian di Institut Pertanian Bogor.
Model pendugaan digunakan untuk mengenali perilaku suatu objek dengan cara mencari keterkaitan antara unsur-unsurnya untuk mengadakan optimalisasi dalam objek dan untuk mengadakan pendugaan atau prediksi untuk memperbaiki keadaan objek. Dari model matematika dapat diperoleh gambaran mengenai jumlah dari gas O2 dan CO2 dari suatu produk pertanian untuk menentukan penanganan pasca panen.
Pada kesempatan kali ini penulis menyampaikan ucapan terima kasih antara lain kepada:
1. Dr. Ir. Rokhani Hasbullah, M.Si. selaku dosen pembimbing akademik yang telah memberikan bimbingan kepada penulis, sehingga dapat menyelesaikan skripsi ini.
2. Dr. Ir. Lilik Pujantoro, M. Agr. dan Ir. Susilo Sarwono selaku dosen penguji yang telah memberikan masukan dalam penyelesaian skripsi ini.
3. Ayahanda dan Ibunda serta kakak dan adik tercinta yang selalu memberikan dorongan motivasi dan do’a selama ini.
4. Teman – teman etoser, etoser 43, pendamping etos, keluarga wisma nurul fitri, segenap pengurus Dompet Dhuafa Republika, LPI (Lembaga Pengembangan Insani), dan pengurus beasiswa KSE.
5. Pak Aminudin dan Pak Sulyaden yang banyak membantu selama penelitian. 6. Rachmat Aditya, Azzah Khairunnisa dan Herina yang telah memberikan
motivasi dan seluruh teman TEP 43.
Akhirnya penulis mengharapkan saran dan kritik dari semua pihak untuk penyempurnaan tulisan ini agar penelitian ini lebih bermanfat bagi pengguna.
Bogor, Oktober 2010
DAFTAR ISI
A. Brokoli (Brassica oleraceaL. var. italic) ...3 B. Karakteristik Respirasi ...5 C. Teknik Pengukuran Laju Respirasi ...10 D. Model Pendugaan...12 III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian ...14 B. Bahan dan Alat ...14 C. Metode Penelitian...14 IV. HASIL DAN PEMBAHASAN
viii DAFTAR TABEL
1. Nilai nutrisi brokoli per 100 g bagian yang dapat dimakan...4 2. Sifat-sifat respirasi berdasarkan tipe substrat yang digunakan ...7 3. Perlakuan-perlakuan penelitian...16 4. Hasil uji Duncan laju respirasi dan respiratory quotient(RQ) brokoli ...21 5. Nilai Q10berdasarkan perhitungan model...23 6. Nilai Q10pada 3 skala suhu...23 7. Model perhitungan hasil transformasi untuk konsumsi O2...23 8. Model perhitungan hasil transformasi untuk konsumsi CO2...23
DAFTAR GAMBAR
1. Brokoli (Brasicca oleraceaL.var. italic) ...3 2. Visualisasi susunan dalam stoples ...14 3. Skema kegiatan pengukuran laju respirasi...15 4. Grafik laju konsumsi O2pada 7 hari penyimpanan ...14 5. Grafik laju produksi CO2pada 7 hari penyimpanan ...20 6. Grafik laju konsumsi O2dan laju produksi CO2pada berbagai suhu
penyimpanan hasil uji model linear sederhana ...26 7. Grafik laju konsumsi O2 dan laju produksi CO2pada berbagai suhu
penyimpanan hasil uji model eksponensial ...27 8. Grafik laju konsumsi O2 dan laju produksi CO2pada berbagai suhu
penyimpanan hasil uji model logaritmik...27 9. Grafik laju konsumsi O2dan laju produksi CO2 pada berbagai suhu
penyimpanan hasil uji model Arrhenius...27
x DAFTAR LAMPIRAN
1. Tabel perubahan konsentrasi O2dan CO2 brokoli selama 7 hari ...33 2. Laju respirasi brokoli selama 7 hari...37 3. Hasil analisis sidik ragam dan uji lanjut Duncan laju konsumsi O2...38 4. Hasil analisis sidik ragam dan uji lanjut Duncan laju konsumsi CO2...40 5. Grafik laju respirasi brokoli metode regresi linear sederhana ...42 6. Grafik laju respirasi brokoli metode regresi eksponensial...43 7. Grafik laju respirasi brokoli metode regresi logaritmik...44 8. Grafik laju respirasi brokoli metode Arrhenius ...45 9. Grafik Laju respirasi brokoli rata-rata empat model...45 10. Tabel hasil perhitungan 4 model analisis regresi konsumsi O2...48 11. Tabel hasil perhitungan 4 model analisis regresi konsumsi CO2...49 12. Laju respirasi brokoli pada berbagai suhu penyimpanan hasil uji 4 model
matematika ...50 13. Data perhitungan laju respirasi brokoli...50
I. PENDAHULUAN
A. Latar Belakang
Karakteristik penting hasil pertanian salah satunya masih melakukan aktivitas respirasi. Akan tetapi respirasi yang terjadi tidak sama dengan tanaman induknya yang tumbuh dengan lingkungan aslinya, karena bahan hasil pertanian mengalami berbagai bentuk kejutan seperti hilangnya suplai nutrisi, proses panen, pengemasan dan transportasi dapat menimbulkan kerusakan mekanis. Hal ini akan mengakibatkan menurunnya kualitas bahkan kuantitas produk tersebut.
Aktivitas metabolisme pada buah dan sayuran segar dicirikan dengan adanya proses respirasi. Laju respirasi produk hortikultura selain dipengaruhi oleh suhu dan kelembaban, juga dipengaruhi oleh komposisi gas, terutama O2dan CO2 di sekitar produk. Laju respirasi dapat ditekan dengan menurunkan konsentrasi O2 dan menaikkan CO2 di sekitar produk. Komposisi gas di sekitar produk tersebut dikendalikan melalui pencampuran dari dua atau lebih gas-gas seperti udara, N2, O2 dan CO2 (Rokhani, 2007). Respirasi menghasilkan panas yang menyebabkan terjadinya peningkatan panas. Sehingga proses kemunduran seperti kehilangan air, pelayuan, dan pertumbuhan mikroorganisme akan semakin meningkat.
2 B. Tujuan
Tujuan dari penelitian ini adalah:
1. Mengkaji pengaruh suhu penyimpanan terhadap laju respirasi brokoli. 2. Mengkaji karakteristik respirasi brokoli selama penyimpanan.
II. TINJAUAN PUSTAKA
A. Brokoli (Brassica oleraceaL. var. italic)
Brokoli merupakan sayuran subtropik yang termasuk dalam golongan tanaman kubis-kubisan dan sering dikenal dengan nama kubis bunga hijau. Pemanenan brokoli dilakukan pada saat bunga mencapai ukuran maksimal dan telah padat (kompak), tetapi kuncup bunganya belum mekar. Umur panen adalah 47 - 67 hari setelah tanam. Waktu panen yang paling tepat adalah pagi dan sore hari, dengan cara memotong tangkai bunga bersama sebagian batang dan daun-daunnya sepanjang 25 cm dengan menggunakan pisau. Untuk pemasaran jarak jauh sebaiknya disertakan enam helai daun. Sedangkan untuk tujuan pemasaran dekat, hanya disertakan 3 - 4 helai daun, dan ujung-ujung daunnya dipotong (Rukmana, 1994). Brokoli mempunyai tingkat taksonomi sebagai berikut:
Divisi : Spermatophyta
Sub divisi : Dycotyledonae
Famili : Cruciferae
Genus : Brassica
Spesies : Brassica oleraceaL. var italic
4 Tabel 1. Nilai nutrisi brokoli per 100 g bagian yang dapat dimakan
Komposisi Nilai Kandungan
Sumber: Agricultural Handbook No.8, USDA (1963) dalam Salunke, Pao dan Dull (1976)
Rukmana (1994) menyebutkan kualitas brokoli dapat dilihat dari kekompakan bunga (curd density), kehijauannya, cacatnya, serta diameter bunganya. Menurut Susila (2006) pengelompokkan (grading) brokoli dilihat dari ukuran bunganya, yaitu:
- Grade 1 : diameter bunga 30 cm - Grade 2 : diameter bunga 25 - 30 cm - Grade 3 : diameter bunga 20 - 25 cm - Grade 4 : diameter 15 - 20 cm
dan pembusukan (Rokhani, 1995). Pra pendinginan dapat dilakukan dengan cara
hydrocooling atau dengan menggunakan es, jika kondisinya baik dan sirkulasi udara pada ruang penyimpanan sesuai maka brokoli dapat bertahan 10 - 14 hari pada suhu 0oC (Rokhani, 1995).
Brokoli memiliki umur simpan yang pendek, yaitu 1 - 2 hari pada kondisi suhu 20 oC, RH 60 – 70%; 2 - 6 hari pada kondisi suhu 4oC, RH 80 – 90 %; 1 - 2 minggu pada kondisi suhu 0 oC, RH 90 – 95 % dan dikemas dalam kotak
polystyrene yang diberi es (Tan, 2005 dalam Bafdal, et al., 2007). Menurut Bafdal, et al., (2007) bahwa jika 15 kg brokoli yang setelah dipanen diberi perlakuan hydrocoolingkemudian dimuat dalam kontainer yang diberi bongkahan es (ice crushed) sebanyak 3 kg dapat menjaga suhu di dalam kontainer 8.5 – 10.3 o
C selama 22 jam.
B. Karakteristik Respirasi
Menurut Winarno dan Kartakusuma (1981), respirasi adalah suatu proses metabolisme dengan cara menggunakan oksigen dalam pembakaran senyawa yang lebih kompleks seperti pati, gula, protein, lemak, dan asam organik, sehingga menghasilkan molekul yang sederhana seperti CO2, air serta energi dan molekul lain yang dapat digunakan oleh sel untuk reaksi sintesa.
Energi yang dikeluarkan berupa panas akibat respirasi (dikenal sebagai panas vital atau vital heat) mempengaruhi penerapan teknologi pasca panen, seperti memperkirakan kebutuhan sistem pendingin dan ventilasi (Kader, 1993). Menurut (Hardenburg, Watada dan Wang, 1968), reaksi kimia sederhana untuk proses respirasi dapat dituliskan sebagai berikut:
C6H12O6+ 6O2 6CO2+ 6H2O + 673 kcal
6 Menurut Phan et al., 1986 dalam Ananta, 1997 laju respirasi buah dan sayuran dipengaruhi oleh faktor luar dan faktor dalam. Faktor dalam yang mempengaruhi respirasi adalah tingkat perkembangan organ tanaman, ukuran produk, lapisan alamiah dan jenis jaringan. Faktor luar yang mempengaruhi adalah suhu, konsentrasi gas O2 dan CO2 yang tersedia, zat-zat pengatur tumbuh dan kerusakan yang ada pada buah dan sayuran.
Laju respirasi brokoli termasuk sangat tinggi (Kader, 1987; Hardenburg, Walada dan Wang, 1968). Semakin cepat laju respirasi maka semakin besar jumlah panas yang dilepaskan per satuan waktu. Laju respirasi besarnya bervariasi tergantung jenis komoditi, akan tetapi terutama dipengaruhi oleh suhu dan komposisi gas di sekitar komoditi tersebut (Kader, 1989; Saltveit, 1989; Manapperuma and Singh, 1987 dalam Rokhani, 1995).
B.1. Pengaruh Suhu
Laju respirasi brokoli dipengaruhi secara nyata oleh suhu penyimpanan, yaitu semakin tinggi suhu penyimpanan, laju respirasinya semakin besar; juga sebaliknya, laju respirasi semakin menurun dengan semakin rendahnya suhu penyimpanan; melalui pengaturan suhu dan kelembaban serta komposisi gas ruang penyimpanan, mutu produk hortikultura yang disimpan dapat dipertahankan (Rokhani, 1995). Laju respirasi brokoli yang digambarkan sebagai laju produksi CO2 (mg/kg jam) pada suhu penyimpanan 0 oC, 4 - 5 oC, 10 oC, 15 - 16 oC, dan 20 - 21 oC adalah berturut-turut (mg/kg jam) 19 - 21, 32 – 37, 75 - 87, 161 – 186, dan 278 – 320 (Hardenburg, Watada dan Wang, 1986). Laju respirasi brokoli juga dipengaruhi oleh ukuran floret (Tian, et al. dalamFinger, et al., 1999) dan jenis kultivarnya (Finger, et al., 1999).
respirasi telah berlangsung, dan sejauh mana proses itu bersifat aerobik atau anaerobik (Phanet al.,1986).
Tabel 2. Sifat-sifat respirasi berdasarkan tipe substrat yang digunakan
Tipe menunjukkan bahwa yang digunakan dalam respirasi itu suatu substrat yang mengandung oksigen, yaitu asam-asam organik. Bila kuosien respirasi kurang dari satu, maka ada beberapa kemungkinan, yaitu (a) substrat mempunyai perbandingan oksigen terhadap karbon yang lebih kecil daripada heksosa, (b) oksidasi belum tuntas, misalnya terhenti pada pembentukan asam suksinat atau zat antara lain; (c) CO2 yang dikeluarkan digunakan dalam proses-proses sintesis, misalnya pembentukan asam oksalat dan asam malat dari piruvat.
8 cenderung terhambat dikarenakan denaturasi enzim. Sedangkan suhu buah atau sayuran umumnya lebih tinggi dari ruang penyimpanan akibat panas respirasi. Perbedaan suhu tersebut cukup kritis dalam penentuan laju metabolisme produk.
Penjelasan tentang penurunan Q10 pada suhu yang tinggi adalah bahwa laju penetrasi O2 ke dalam sel lewat kutikula atau periderma mulai menghambat respirasi saat reaksi kimia berlangsung dengan cepat. Difusi O2 dan CO2 juga dipercepat dengan peningkatan suhu, tapi Q10 untuk proses fisika ini hanya 1.1 ; jadi suhu tidak mempercepat secara nyata difusi larutan lewat air. Peningkatan suhu sampai 40 °C atau lebih, laju respirasi malahan menurun, khususnya bila tumbuhan berada pada keadaan ini dalam jangka waktu yang lama. Enzim yang diperlukan mulai mengalami denaturasi dengan cepat pada suhu yang tinggi, mencegah peningkatan metabolik yang semestinya terjadi. Pada kecambah kacang kapri, peningkatan suhu dari 25 menjadi 45 °C mula-mula meningkatkan respirasi dengan cepat, tapi setelah dua jam laju respirasinya mulai berkurang. Kemungkinan penjelasannya ialah jangka waktu dua jam sudah cukup lama untuk merusak sebagian enzim respirasi (Salisbury & Ross, 1995).
B.2. Pengaruh Komposisi Gas
Komposisi gas yang utama dalam mempengaruhi respirasi adalah oksigen, karbondioksida, dan etilen (Kays, 1991). Beberapa penelitian telah menunjukkan bahwa komposisi O2 rendah dan CO2 tinggi akan menghambat laju respirasi. Pantastico et al., 1986 menyatakan bahwa etilen dapat mempercepat proses respirasi dan pembentukannya sekaligus didorong oleh laju respirasi. Dengan mengubah konsentrasi gas O2 menjadi 3 % dari 22 % dan meningkatkan konsentrasi CO2 menjadi 4 % dari keadaan normal, buah dan sayuran tidak mengalami efek kerusakan dan memperlambat proses pematangan selama beberapa hari (Liyod Ryall et al., 1982dalamTubagus, 1993).
komoditas. Penyimpanan dengan atmosfir termodifikasi dapat dilakukan dengan penyimpanan atmosfer terkendali (controlled atmosphere, CA) atau atmosfir modifikasi (modified atmosphere, MA)
Rokhani (1996) mengemukakan bahwa pada sistem CA komposisi gas dalam ruang penyimpanan diukur secara terus menerus dan perlu menginjeksikan gas atau campuran gas tertentu untuk mempertahankan komposisi gas yang diinginkan. Sedangkan sistem MA merupakan sistem statis tanpa melakukan monitoring komposisi gas selama penyimpanan. Komposisi gas pada penyimpanan sistem MA ditentukan dari komposisi gas awal yang terdapat dalam kemasan, laju konsumsi oksigen dan laju produksi karbondioksida oleh komoditas, sifatnya permeabelitas dari kemasan dan suhu penyimpanan.
Komposisi gas yang diinginkan pada sistem CA lebih teliti dibandingkan MA. Dalam praktiknya sistem CA memerlukan gas-gas pengendali seperti oksigen, karbondioksida dan nitrogen serta sejumlah peralatan untuk pengaturan dan pengendalian komposisi gas yang secara praktis diterapkan untuk penyimpanan dalam bentuk curah.
Menurut Wang dan Hruscha (1977) dalam Tubagus (1993) bahwa pada suhu penyimpanan 10 oC dengan modified atmosphere, brokoli yang tidak dikemas dapat bertahan selama 3 hari dan setelah hari ketujuh bahan akan menguning. Selanjutnya brokoli yang dikemas dengan film tertutup dapat dipertahankan mutunya sampai 14 hari. Pada penyimpanan 20 oC brokoli yang tidak dikemas hanya bertahan selama 2 hari dengan kemasan tertutup sampai hari kedua warna dapat dipertahankan tetapi mengalami kerusakan fisik.
10 penyimpanan. Pada kondisi ini kerusakan dan pembusukan akan tejadi setelah 10 hari penyimpanan.
B.3. Pola Respirasi
Buah-buahan dan sayuran dapat diklasifikasikan berdasarkan pola respirasi selama pematangan sebagi klimakterik dan non klimakterik. Istilah klimakterik dicetuskan oleh Kidd dan West (1925) dalam Pantastico (1986), yang pertama kali menguraikan gejala tersebut pada saat meneliti fisiologi pasca panen apel
Bramley Seedling (diukur dengan produksi CO2) pada suhu 12.2 oC adalah lambat dan konstan pada waktu tertentu, lalu sesudah itu meningkat sampai puncak (klimaks). Oleh karena itu mereka menamakan fenomena tersebut dengan kenaikan klimakterik. Hal ini menyimpulkan bahwa ciri dari proses klimakterik adalah kenaikan produksi CO2yang mendadak.
Menurut Biale (1954) dalam Kays (1991), buah non klimakterik akan bereaksi terhadap pemberian C2H4 pada tingkat manapun dengan kenaikan laju konsumsi O2 yang tergantung pada konsentrasi etilen sedangkan pada buah klimakterik, peningkatan konsentrasi C2H4 hanya akan menggeser pola respirasi secara horizontal. Buah klimakterik mengadakan reaksi respiratik bila C2H4 diberikan dalam keadaan pra klimakterik, dan tidak lagi peka terhadap C2H4 setelah masa kenaikan klimakterik terlampaui.
C. Teknik Pengukuran Laju Respirasi
Dalam proses respirasi beberapa senyawa penting yang dapat digunakan untuk mengukur laju respirasi adalah perubahan kandungan glukosa, jumlah ATP, CO2 yang diproduksi dan O2 yang dikonsumsi. Dari keempat cara tersebut, pengukuran dengan menghitung produksi CO2 lebih sederhana dan lebih praktis. Sedangkan menentukan jumlah O2 yang dikonsumsi dapat dilakukan dengan alat yang mempunyai kepekaan tinggi seperti kromatografi gas karena jumlahnya relatif sedikit (Winarno dan Kartakusuma, 1981).
jaringan (internal) atau dari gas yang ditimbulkan oleh jaringan (eksternal). Pengukuran laju respirasi dengan mengambil sampel gas secara internal telah dilakukan oleh Saltveit (1982). Dibandingkan cara internal, pengambilan sampel gas secara eksternal lebih sederhana dan tidak merusak bahan. Terdapat dua metode dalam pengambilan sampel gas secara eksternal, yaitu metode statis atau sistem tertutup (closed system) dan metode dinamis atau sistem terbuka (open system).
Dalam metode sistem tertutup bahan ditempatkan dalam suatu wadah tertutup dimana gas CO2 yang dihasilkan terakumulasi dan gas O2 yang dikonsumsi menjadi berkurang konsentrasinya. Laju respirasi dihitung dengan mengetahui berat bahan, volume bebas wadah, dan perbedaan konsentrasi setelah waktu tertentu (Rokhani, 1996). Mannapperuma dan Singh (1990) menyatakan persamaan laju respirasi sistem tertutup pada suhu tertentu dengan satuan ml/kg-jam seperti pada persamaan (1) dan (2).
R1 (1)
R2 (2)
dimana
R = laju respirasi (ml/kg jam)
x = konsentrasi gas (desimal)
t = waktu (jam)
V = volume bebas (ml)
W = berat produk (kg)
subskrip 1, 2 = masing-masing menyatakan gas O2dan CO2.
12 outlet gas pada “respiration chamber”. Mannapperuma dan Singh (1990) menentukan laju respirasi pada sistem terbuka berdasarkan kesetimbangan massa oksigen dan karbondioksida. Sedangkan kesetimbangan massa nitrogen digunakan untuk menghitung laju aliran gas masuk. Persamaan kesetimbangan untuk oksigen, karbondioksida, dan nitrogen ditunjukkan dalam persamaan berikut:
Kesetimbangan O2 : R1 = (Gx1– Qy1) /W (3)
Kesetimbangan CO2 : R2 = (Gx2– Qy2) /W (4)
Kesetimbangan N2 : G = Q(y3/x3) (5)
dimana
R = laju respirasi (ml/kg jam)
G = laju respirasi gas masuk (ml/jam)
Q = laju aliran gas keluar (ml/jam)
W = berat produk (kg)
x = konsentrasi gas masuk (desimal)
y = konsentrasi gas keluar (desimal)
subskrip 1, 2, dan 3 masing-masing menyatakan gas O2, CO2, dan N2.
D. Model Pendugaan
optimalisasi dalam objek dan untuk mengadakan pendugaan atau prediksi untuk memperbaiki keadaan objek. Dari model matematika dapat diperoleh gambaran yang lebih jelas mengenai objek tanpa harus mengganggu keberadaan objek. Pengembangan model matematika merupakan suatu siklus fenomena yang berdasarkan konsep model verbal.
Metode pengkorelasian yang akan digunakan adalah metode regresi linear yaitu:
Linear sederhana : R = a + bT (6)
Eksponensial : R = aebT (7)
Logaritmik : R = aTb (8)
Untuk menyatakan laju respirasi sebagai fungsi suhu dapat digunakan persamaan Arrhenius:
R = Ro e–E/RT (9)
dimana
R = konstanta penurunan konsentrasi
Ro= konstanta E = energi aktivasi T = suhu mutlak (C+273)
14 III.METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Maret 2010 di Laboratorium Teknologi Pengolahan Hasil Pertanian (TPPHP) Departemen Teknik Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
B. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah brokoli (Brassica oleracea L. var. italic) yang didapat di daerah sekitar Bogor. Sedangkan peralatan yang digunakan adalah unit pencampur gas, stoples, inkubator, gas analyzer IRA-107 untuk mengukur konsentrasi CO2 dan portable oxygen tester POT-101 untuk mengukur konsentrasi O2, timbangan dan alat penunjang lainnya.
C. Metode Penelitian
C.1. Pengukuran laju respirasi
Pengukuran laju respirasi dengan menggunakan sistem tertutup, yaitu: tutup stoples yang digunakan dilubangi dengan diameter 1 cm sebanyak dua buah dan pada lubang tersebut dimasukkan selang plastik sepanjang 30 cm. Pada pertemuan selang plastik dengan penutup stoples diberi lem dan lilin malam untuk menghindari kebocoran gas.
Brokoli segar dibersihkan dan dipilih bunga (floret) yang memiliki bentuk fisik yang baik dan seragam, kemudian ditimbang dan dimasukkan ke dalam stoples dan ditutup rapat. Untuk menghindari kebocoran gas, antara penutup dan leher stoples diberi lilin malam dan selang plastiknya ditekuk dan dijepit.
Pengukuran kandungan gas dilakukan tiap 24 jam, dan diukur dengan 3 kali ulangan masing-masing berjarak 3 jam. Pengukuran dilakukan setiap hari sampai brokoli busuk. Setelah dilakukan pengukuran, stoples dibuka untuk mengembalikan udara ke kondisi normal.
Gambar 3. Skema kegiatan pengukuran laju respirasi
C.2. Rancangan percobaan
16 dihitung berdasarkan konsentrasi gas O2 atau CO2, volume bebas, interval waktu dan berat sampel seperti pada persamaan (1) dan (2). Berikut perlakuan-perlakuan dalam penelitian (Tabel 2).
Tabel 3. Perlakuan-perlakuan penelitian
Perlakuan Suhu (oC) Ulangan Berat per sampel (g)
Model aditif RAL yang digunakan adalah:
(10) dimana
Yij = nilai pengamatan dari perlakuan ke-i dan ulangan ke-j µ = nilai tengah umum
= tambahan akibat perlakuan ke-i
= tambahan akibat acak galat percobaan dari percobaan dari perlakuan ke-i pada ulangan ke-j
Analisis data yang digunakan adalah uji GLM untuk menguji keragaman dan dilanjutkan dengan uji Duncan.
C.3. Model pendugaan respirasi
Setelah dilakukan pengukuran konsentrasi gas O2 dan gas CO2 kemudian dilakukan perhitungan untuk menentukan laju respirasi dari brokoli. Kemudian langkah selanjutnya adalah memprediksi laju respirasi brokoli terhadap suhu. Digunakan empat model matematika yaitu berdasarkan persamaan (6), (7), (8), (9). Dari keempat model tersebut dipilih model yang terbaik berdasarkan koefisien determinasi masing-masing model.
lnR = ln a + b T (11)
atau
ln R = α+ βT (12)
Persamaan (8) ditransformasi menjadi:
log R = log a + blog T (13)
atau
log R = α + βlog T (14)
Persamaan (10) ditransformasi menjadi:
ln R = ln Ro – (E/R)(1/T) (15)
atau
ln R = α–β(1/T) (16)
dimana
α = peubah intersep
β = kemiringan
18 IV. HASIL DAN PEMBAHASAN
A. Pengaruh Suhu pada Respirasi Brokoli
Pada hasil penelitian menunjukkan bahwa brokoli mempunyai respirasi yang tinggi. Namun pada suhu yang rendah, hasil pengamatan menunjukkan bahwa konsentrasi O2 yang dikonsumsi dan produksi CO2 semakin sedikit (Lampiran 1) yang menunjukkan bahwa respirasi brokoli pada suhu rendah lebih lambat dibandingkan dengan suhu ruang. Lampiran 2 menunjukkan laju respirasi (konsumsi O2 dan produksi CO2) pada suhu 5 oC, 10 oC, 15 oC, 20 oC, dan 27 oC (suhu ruang).
menghasilkan molekul yang sederhana seperti CO2, sehingga pada suhu penyimpaan yang lebih tinggi konsentrasi CO2yang semakin besar dan konsumsi O2yang semakin besar pula.
B. Karakteristik Respirasi B.1. Pola Respirasi Brokoli
Laju respirasi petunjuk yang baik untuk daya simpan buah dan sayuran sesudah dipanen. Intensitas respirasi dianggap sebagai ukuran laju jalannya metabolisme, oleh karena itu sering dianggap sebagai petunjuk mengenai potensi daya simpan buah.
Menurut Soesarsono (1988) dalam Nugroho (1997) buah dan sayuran dapat digolongkan atas dasar laju pemasakan yaitu golongan klimakterik dan non klimakterik. Golongan klimakterik ditandai dengan proses yang cepat pada fase pemasakan (ripening) dan peningkatan respirasi yang mencolok. Sebaliknya golongan non klimakterik tidak terlihat nyata perubahan pada fase pemasakannya karena proses respirasi berjalan lambat. Penurunan laju respirasi merupakan petunjuk terjadinya kerusakan enzim (Pantastico, 1989).
20 Gambar 4. Grafik laju konsumsi O2pada 7 hari penyimpanan
Gambar 5. Grafik laju produksi CO2pada 7 hari penyimpanan
Jika dilihat posisi grafik untuk masing-masing perlakuan suhu, Gambar 4 dan Gambar 5 menunjukkan bahwa laju respirasi brokoli sangat dipengaruhi oleh suhu penyimpanan. Pada suhu penyimpanan 5oC posisi grafik berada pada paling bawah yang menunjukkan bahwa pada suhu 5 oC brokoli mengkonsumsi O2 dan memproduksi CO2 paling sedikit diantara suhu penyimpanan lainnya. Sedangkan pada suhu penyimpanan 27 oC posisi grafik berada paling atas dan menunjukkan bahwa pada suhu 27oC (suhu ruang) memiliki laju respirasi yang paling tinggi.
enzim respiratoris (Solomos, 1983 dalam Asrofi, 1986). Kondisi demikian menyebabkan terjadinya peningkatan proses metabolisme dalam jaringan, sehingga sayuran dapat membusuk.
Menurunnya jumlah CO2 yang dihasilkan dapat disebabkan karena menurunnya konsentrasi ADP yang bersifat sebagai akseptor fosfat dan terjadinya kerusakan mitokondria (Winarno dan Kartakusuma, 1981). Konsentrasi ADP yang menurun dan kerusakan mitokondria menyebabkan ATP yang dihasilkan juga menurun. ATP yang berfungsi sebagi penyuplai energi dalam bentuk fosfat berenergi tinggi dengan cara memecah ikatan fosfatnya (Wills et al., 1981 dalam
Asrofi, 1986). Karena ATP menurun, maka energi yang dapat digunakan untuk melangsungkan reaksi metabolik selanjutnya juga menurun. Keadaan demikian menyebabkan jumlah CO2yang dihasilkan semakin menurun.
Pada penelitian ini pola respirasi brokoli menunjukkan kecenderungan yang terus menurun dan tidak terjadi kenaikan produksi CO2 yang mendadak. Dengan demikian dapat disimpulkan bahwa brokoli termasuk sayuran non klimakterik.
B.2. Respiratory Quotient(RQ)
Respirasi membutuhkan O2dan menghasilkan zat sisa metabolisme berupa uap air, CO2, dan panas sebagai entropi (energi panas yang tidak termanfaatkan). Kuosien respirasi (respiratory quotient) merupakan perbandingan CO2 terhadap O2. Nilai RQ brokoli ditunjukkan pada Tabel 4.
Tabel 4. Hasil uji Duncan laju respirasi dan respiratory quotient(RQ) brokoli
Suhu (oC) Laju respirasi (ml/kg jam)
22 Hasil uji Duncan (Lampiran 3 dan 4) menunjukkan bahwa laju konsumsi O2 berbeda nyata untuk suhu 15 oC, 20 oC, dan 27 oC berbeda nyata. Hasil uji pada suhu 5 oC dan 10 oC tidak berbeda nyata yang berarti laju konsumsi O2 hampir sama. Sedangkan laju produksi CO2berbeda nyata untuk suhu 5oC, 10oC, dan 27 oC. Hasil uji pada suhu 15 oC dan 20 oC tidak berbeda nyata. Laju konsumsi O2 dan laju produksi CO2pada suhu 5 oC dan 10 oC (Gambar 4 dan 5) merupakan laju terkecil diantara suhu penyimpanan lainnya. Sehingga dalam penelitian ini, suhu tersebut merupakan suhu terbaik untuk penyimpanan brokoli.
Pada Tabel 3 menunjukkan nilai RQ brokoli yang disimpan pada lima suhu penyimpanan yang berbeda. Nilai RQ brokoli hampir seluruhnya bernilai 1.0, hal ini menunjukkan bahwa proses metabolisme berlangsung secara normal menggunakan substrat karbohidrat, protein atau lemak dengan ketersediaan oksigen yang cukup. Komponen terbesar pada brokoli setelah air adalah karbohidrat. Dengan demikian dapat dikatakan bahwa substrat yang digunakan untuk proses respirasi sebagian besar adalah karbohidrat. Pada kondisi respirasi anaerobik umumnya nilai RQ lebih besar dari satu.
B.3. Q10 (Kuosien Suhu)
Karakter perubahan pada laju reaksi akibat suhu tersebut biasanya ditentukan dengan kuosien suhu (Q10), yaitu rasio laju reaksi tertentu pada suatu tingkat suhu (T1) terhadap laju reaksi tersebut saat suhu naik 10 oC (T1+ 10 oC). Nilai Q10brokoli ditunjukkan pada Tabel 5.