SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN
EKSTRAK ETANOL SERTA FRAKSI n-HEKSANA
ETILASETAT DAN AIR HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
SKRIPSI
OLEH:
YANI PUTRI SIMBOLON
NIM 101501121
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN
EKSTRAK ETANOL SERTA FRAKSI n-HEKSANA
ETILASETAT DAN AIR HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
SKRIPSI
Diajukan sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
YANI PUTRI SIMBOLON
NIM 101501121
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN
EKSTRAK ETANOL SERTA FRAKSI n-HEKSANA
ETILASETAT DAN AIR HERBA KURMAK MBELIN
(Enydra fluctuans Lour.)
OLEH:
YANI PUTRI SIMBOLON
NIM 101501121
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 16 Agustus 2014
Pembimbing I, Panitia Penguji,
NIP 195112231980032002 NIP 195103261978022001
Dra. Herawaty Ginting, M.Si., Apt.
Pembimbing II, NIP 195112231980032002
Dr. M. Pandapotan Nasution, M.P.S., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 194908111976031001 NIP 195709091985112001
Drs. Suryadi Achmad, M.Sc., Apt. NIP 195109081985031002
Medan, 9 Oktober 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
iv
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul “Skrining Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Etanol serta
Fraksi n-Heksana Etilasetat dan Air Herba Kurmak Mbelin (Enydra fluctuans
Lour.)”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar
sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
USU Medan yang telah memberikan fasilitas selama masa pendidikan. I
Apt., selaku pembimbing yang telah memberikan waktu, bimbingan dan nasehat
selama penelitian hingga selesainya penyusunan skripsi ini. Bapak Dr. Edy
Suwarso, S.U., Apt., selaku penasehat akademik yang telah memberikan
bimbingan kepada penulis selama masa perkuliahan. Bapak dan Ibu staf pengajar
Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik selama masa
perkuliahan. Bapak dan Ibu Kepala Laboratorium Penelitian dan Farmakognosi
yang telah memberikan fasilitas, petunjuk dan membantu selama penelitian. Ibu
Prof. Dr. Rosidah, M.Si., Apt., Ibu Dr. Marline Nainggolan, M.S., Apt., dan
Bapak Drs. Suryadi Achmad, M.Sc., Apt., selaku dosen penguji yang telah
memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi
v
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
kepada Ayahanda Tombor Simbolon, S.H., M.M., dan Ibunda Mindo Napitupulu,
S.Pd., atas doa dan pengorbanannya dengan tulus dan ikhlas bagi kesuksesan
penulis, juga untuk abang dan adik tersayang Dharma Yoga Putra Simbolon,
Sharon Tara Simbolon, Grace Auditia Simbolon serta teman-teman penulis Meity
Mardiana Nainggolan, Nona Juwita Christiana Marbun, Grace Kyara Rotua
Nababan, Arta Maria Hutagaol, Friska Rani Sarah Purba, Melisa Anriani
Sitanggang, Ria Mintan Sihotang, Satia Cristenson Devina Sirait, Maya Natalina
Hutapea, Yemima Kasih Oriza Silalahi, Novia Christin Nainggolan dan Presty
Sipayung yang selalu setia memberi doa, bantuan dan semangat.
Penulis menyadari bahwa penulisan skripsi ini masih banyak kekurangan,
oleh karena itu penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan
dan ilmu kefarmasian khususnya.
Medan, Oktober 2014
Penulis
Yani Putri Simbolon
vi
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL SERTA FRAKSI n-HEKSANA
ETILASETAT DAN AIR HERBA KURMAK MBELIN (Enydra fluctuans Lour.)
ABSTRAK
Kurmak mbelin (Enydra fluctuans Lour.) adalah tumbuhan yang telah dikenal sejak dahulu kala, berasal dari wilayah Indo-China, yang tumbuh di daerah tropis di Asia dan Afrika. Kurmak mbelin, terutama bagian pucuk muda, digunakan sebagai sayur di Asia Tenggara (Indo-China dan Thailand), baik mentah maupun direbus. Di Kabupaten Karo kurmak mbelin dikonsumsi sebagai sayuran. Tumbuhan ini memiliki rasa yang agak pahit. Bagian herba memiliki aktivitas antimikroba dan antioksidan. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, golongan kandungan senyawa kimia dan aktivitas antioksidan ekstrak herba kurmak mbelin.
Serbuk simplisia herba kurmak mbelin diekstraksi secara perkolasi dengan pelarut etanol 96%. Ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental, kemudian difraksinasi dengan pelarut n-heksana dan etilasetat, diuji aktivitas antioksidannya terhadap DPPH (1,1-diphenyl-2-picrylhydrazil) sebagai radikal bebas dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-60 setelah penambahan pelarut metanol. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil karakterisasi simplisia diperoleh kadar air 5,2%, kadar sari yang larut dalam air 20,63%, kadar sari yang larut dalam etanol 17,24%, kadar abu total 14,28% dan kadar abu yang tidak larut dalam asam 0,54%. Hasil skrining fitokimia herba kurmak mbelin mengandung senyawa kimia golongan flavonoida, glikosida, saponin, steroida/triterpenoida dan tanin. Hasil pengujian aktivitas antioksidan dengan metode DPPH menunjukkan bahwa ekstrak etanol, fraksi n -heksana, fraksi etilasetat dan fraksi air dari herba kurmak mbelin memiliki aktivitas antioksidan yang sangat kuat dengan nilai inhibitory concentration (IC50) yang diperoleh dari ekstrak etanol, fraksi n-heksana, fraksi etilasetat dan fraksi air sebesar 25,93, 19,51, 17,14 dan 35,18 ppm.
vii
PHYTOCHEMICAL SCREENING AND ANTIOXIDANT ACTIVITY OF ETHANOL EXTRACT AND n-HEXANE ETHYLACETATE AND AQUEOUS FRACTIONS OF KURMAK MBELIN HERB
(Enydra fluctuans Lour.)
ABSTRACT
Kurmak Mbelin (Enydra fluctuans Lour.) is a plant of the old world, originated from the Indo-China region, which grows in tropical regions of Asia and Africa. Kurmak mbelin, especially young shoots, are consumed as vegetable or spice in Southeast Asia (Indo-China and Thailand), either raw or boiled. In Karo kurmak mbelin is consumed as a vegetable. This plant tastes rather bitter. The herb also has antimicrobial and antioxidant activities. The purpose of this study was to determine the characteristics of simplex, to determine the chemical compounds contained and to measure the antioxidant activity of extracts of the kurmak mbelin herb.
The ethanolic extract was prepared by percolation with 96% ethanol. Percolate was concentrated in vacuo and by freeze dryer. The simplex of kurmak mbelin herb was also fractionated with n-hexane and ethylacetate. Then, the antioxidant activity of extracts were tested using DPPH as free radical. Absorbance of DPPH was measured at 516 nm, at 60th minute after the addition of methanol solvent. Antioxidant activity was measured as a decrease in absorbance of DPPH solution after the addition of extract.
The result of simplex characterization gave the water content value 5.2%, the water soluble extract 20.63%, the ethanol soluble extract 17.24%, the total ash 14.28% and the acid insoluble ash 0.54%. The result of phytochemical screening showed that kurmak mbelin herb contains flavonoid, glycoside, saponin, steroid/triterpenoid and tannin. The results of antioxidant activity testing showed that ethanolic extract, n-hexane fraction, ethylacetate fraction and aqueous fraction of kurmak mbelin exhibited strong antioxidant activity with inhibitory concentration (IC50) of ethanolic extract, n-hexane fraction, ethylacetate fraction and aqueous fraction 25.93, 19.51, 17.14 and 35.18 ppm consecutively.
viii
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan ... 4
1.5 Manfaat ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Daerah tumbuh ... 5
2.1.2 Nama daerah ... 5
ix
2.1.4 Sistematika tumbuhan ... 6
2.1.5 Morfologi tumbuhan ... 7
2.1.6 Kandungan kimia ... 7
2.1.7 Kegunaan ... 7
2.2 Simplisia dan Ekstrak ... 8
2.2.1 Simplisia ... 8
2.2.2 Ekstrak ... 8
2.3 Radikal Bebas ... 11
2.4 Antioksidan ... 12
2.4.1 Antioksidan alami ... 13
2.4.2 Betakaroten ... 13
2.4.3 Polifenol ... 14
2.5 Spektrofotometri UV–Visibel ... 16
2.6 Penentuan Aktivitas Antioksidan dengan Metode DPPH .... 16
2.6.1 Pelarut ... 19
2.6.2 Pengukuran absorbansi–panjang gelombang ... 19
2.6.3 Waktu reaksi ... 19
BAB III METODE PENELITIAN ... 20
3.1 Alat-Alat ... 20
3.2 Bahan-Bahan ... 20
3.3 Penyiapan Tumbuhan ... 21
3.3.1 Pengambilan tumbuhan ... 21
3.3.2 Identifikasi tumbuhan ... 21
x
3.4 Pembuatan larutan pereaksi ... 21
3.4.1 Larutan pereaksi Bouchardat ... 21
3.4.2 Larutan pereaksi Mayer ... 22
3.4.3 Larutan pereaksi Dragendorff ... 22
3.4.4 Larutan pereaksi Molish ... 22
3.4.5 Larutan pereaksi asam klorida 2 N ... 22
3.4.6 Larutan pereaksi asam sulfat 2 N ... 22
3.4.7 Larutan pereaksi asam nitrat 0,5 N ... 22
3.4.8 Larutan pereaksi timbal (II) asetat 0,4 M ... 23
3.4.9 Larutan pereaksi besi (III) klorida 1% ... 23
3.4.10 Larutan pereaksi kloralhidrat 70% b/b ... 23
3.4.11 Larutan pereaksi DPPH 0,5 mM ... 23
3.5 Pemeriksaan Mikroskopik Herba Kurmak Mbelin ... 23
3.6 Pemeriksaan Karakteristik Simplisia ... 23
3.6.1 Pemeriksaan makroskopik ... 24
3.6.2 Pemeriksaan mikroskopik ... 24
3.6.3 Penetapan kadar air ... 24
3.6.4 Penetapan kadar sari larut dalam air ... 25
3.6.5 Penetapan kadar sari larut dalam etanol ... 25
3.6.6 Penetapan kadar abu total ... 25
3.6.7 Penetapan kadar abu tidak larut dalam asam ... 26
3.7 Skrining Fitokimia ... 26
3.7.1 Pemeriksaan alkaloida ... 26
xi
3.7.3 Pemeriksaan saponin ... 27
3.7.4 Pemeriksaan flavonoida ... 27
3.7.5 Pemeriksaan antrakinon ... 28
3.7.6 Pemeriksaan tanin ... 28
3.7.7 Pemeriksaan steroida/triterpenoida ... 28
3.8 Pembuatan Ekstrak ... 29
3.8.1 Pembuatan ekstrak etanol ... 29
3.8.2 Pembuatan fraksi ekstrak ... 29
3.9 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel ... 30
3.9.1 Prinsip metode penangkapan radikal bebas DPPH ... 30
3.9.2 Pengukuran larutan DPPH ... 30
3.9.3 Pembuatan larutan induk ... 30
3.9.4 Pengukuran aktivitas antioksidan sampel uji ... 30
3.9.5 Penentuan persen peredaman ... 31
3.9.6 Penentuan nilai IC50 ... 31
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Hasil Identifikasi Tumbuhan ... 32
4.2 Hasil Pemeriksaan Mikroskopik Herba Kurmak Mbelin .... 32
4.3 Hasil Pemeriksaan Karakteristik Simplisia ... 32
4.3.1 Hasil pemeriksaan makroskopik ... 32
4.3.2 Hasil pemeriksaan mikroskopik ... 33
4.3.3 Hasil pemeriksaan karakteristik serbuk simplisia ... 33
xii
4.4.1 Hasil skrining fitokimia serbuk simplisia ... 34
4.4.2 Hasil skrining fitokimia ekstrak ... 35
4.5 Hasil Penentuan Panjang Gelombang Serapan Maksimum ... 36
4.6 Hasil Analisis Aktivitas Antioksidan ... 37
4.7 Hasil Analisis Peredaman Radikal Bebas DPPH oleh Sampel Uji ... 38
4.8 Hasil Analisis Nilai IC50 (Inhibitory Concentration) Sampel Uji ... 39
BAB V KESIMPULAN DAN SARAN ... 42
5.1 Kesimpulan ... 42
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
xiii
DAFTAR TABEL
Tabel Halaman
4.1 Hasil pemeriksaan karakteristik serbuk simplisia herba
kurmak mbelin ... 33
4.2 Hasil skrining fitokimia serbuk simplisia herba kurmak
mbelin ... 34
4.3 Hasil skrining fitokimia ekstrak herba kurmak mbelin ... 35
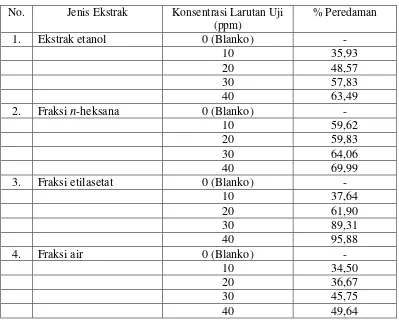
4.4 Hasil analisis peredaman radikal bebas oleh ekstrak herba
kurmak mbelin ... 39
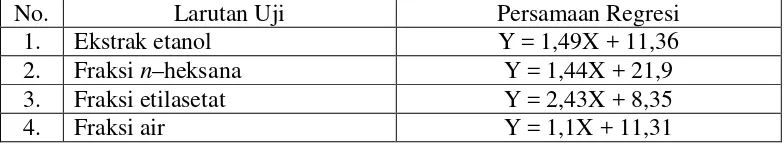
4.5 Hasil persamaan regresi linier dari ekstrak herba kurmak
mbelin ... 40
xiv
DAFTAR GAMBAR
Gambar Halaman
2.1 Rumus bangun betakaroten ... 14
2.2 Struktur dasar polifenol ... 14
2.3 Rumus bangun DPPH ... 17
2.4 Resonansi DPPH ... 18
2.5 Reaksi antara DPPH dengan atom H netral yang berasal dari antioksidan ... 18
4.1 Kurva serapan maksimum larutan DPPH 40 ppm dalam metanol secara spektrofotometri visibel ... 36
xv
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil identifikasi tumbuhan ... 46
2 Tumbuhan dan herba kurmak mbelin (Enydra fluctuans Lour.) ... 47
3 Simplisia dan serbuk simplisia herba kurmak mbelin (Enydrae fluctuansis) ... 48
4 Gambar mikroskopik dari herba kurmak mbelin (Enydra fluctuans Lour.) ... 49
5 Bagan pembuatan serbuk simplisia herba kurmak mbelin (Enydra fluctuans Lour.) ... 52
6 Bagan pembuatan ekstrak etanol herba kurmak mbelin (Enydra fluctuans Lour.) ... 53
7 Bagan pembuatan fraksi ekstrak dari herba kurmak mbelin (Enydra fluctuans Lour.) ... 54
8 Perhitungan pemeriksaan karakteristik serbuk simplisia herba kurmak mbelin (Enydra fluctuans Lour.) ... 55
9 Hasil uji antioksidan ... 59
10 Perhitungan nilai IC50 ... 79
vi
SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL SERTA FRAKSI n-HEKSANA
ETILASETAT DAN AIR HERBA KURMAK MBELIN (Enydra fluctuans Lour.)
ABSTRAK
Kurmak mbelin (Enydra fluctuans Lour.) adalah tumbuhan yang telah dikenal sejak dahulu kala, berasal dari wilayah Indo-China, yang tumbuh di daerah tropis di Asia dan Afrika. Kurmak mbelin, terutama bagian pucuk muda, digunakan sebagai sayur di Asia Tenggara (Indo-China dan Thailand), baik mentah maupun direbus. Di Kabupaten Karo kurmak mbelin dikonsumsi sebagai sayuran. Tumbuhan ini memiliki rasa yang agak pahit. Bagian herba memiliki aktivitas antimikroba dan antioksidan. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, golongan kandungan senyawa kimia dan aktivitas antioksidan ekstrak herba kurmak mbelin.
Serbuk simplisia herba kurmak mbelin diekstraksi secara perkolasi dengan pelarut etanol 96%. Ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental, kemudian difraksinasi dengan pelarut n-heksana dan etilasetat, diuji aktivitas antioksidannya terhadap DPPH (1,1-diphenyl-2-picrylhydrazil) sebagai radikal bebas dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-60 setelah penambahan pelarut metanol. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil karakterisasi simplisia diperoleh kadar air 5,2%, kadar sari yang larut dalam air 20,63%, kadar sari yang larut dalam etanol 17,24%, kadar abu total 14,28% dan kadar abu yang tidak larut dalam asam 0,54%. Hasil skrining fitokimia herba kurmak mbelin mengandung senyawa kimia golongan flavonoida, glikosida, saponin, steroida/triterpenoida dan tanin. Hasil pengujian aktivitas antioksidan dengan metode DPPH menunjukkan bahwa ekstrak etanol, fraksi n -heksana, fraksi etilasetat dan fraksi air dari herba kurmak mbelin memiliki aktivitas antioksidan yang sangat kuat dengan nilai inhibitory concentration (IC50) yang diperoleh dari ekstrak etanol, fraksi n-heksana, fraksi etilasetat dan fraksi air sebesar 25,93, 19,51, 17,14 dan 35,18 ppm.
vii
PHYTOCHEMICAL SCREENING AND ANTIOXIDANT ACTIVITY OF ETHANOL EXTRACT AND n-HEXANE ETHYLACETATE AND AQUEOUS FRACTIONS OF KURMAK MBELIN HERB
(Enydra fluctuans Lour.)
ABSTRACT
Kurmak Mbelin (Enydra fluctuans Lour.) is a plant of the old world, originated from the Indo-China region, which grows in tropical regions of Asia and Africa. Kurmak mbelin, especially young shoots, are consumed as vegetable or spice in Southeast Asia (Indo-China and Thailand), either raw or boiled. In Karo kurmak mbelin is consumed as a vegetable. This plant tastes rather bitter. The herb also has antimicrobial and antioxidant activities. The purpose of this study was to determine the characteristics of simplex, to determine the chemical compounds contained and to measure the antioxidant activity of extracts of the kurmak mbelin herb.
The ethanolic extract was prepared by percolation with 96% ethanol. Percolate was concentrated in vacuo and by freeze dryer. The simplex of kurmak mbelin herb was also fractionated with n-hexane and ethylacetate. Then, the antioxidant activity of extracts were tested using DPPH as free radical. Absorbance of DPPH was measured at 516 nm, at 60th minute after the addition of methanol solvent. Antioxidant activity was measured as a decrease in absorbance of DPPH solution after the addition of extract.
The result of simplex characterization gave the water content value 5.2%, the water soluble extract 20.63%, the ethanol soluble extract 17.24%, the total ash 14.28% and the acid insoluble ash 0.54%. The result of phytochemical screening showed that kurmak mbelin herb contains flavonoid, glycoside, saponin, steroid/triterpenoid and tannin. The results of antioxidant activity testing showed that ethanolic extract, n-hexane fraction, ethylacetate fraction and aqueous fraction of kurmak mbelin exhibited strong antioxidant activity with inhibitory concentration (IC50) of ethanolic extract, n-hexane fraction, ethylacetate fraction and aqueous fraction 25.93, 19.51, 17.14 and 35.18 ppm consecutively.
1
BAB I PENDAHULUAN
1.1Latar Belakang
Kemajuan teknologi dan ilmu pengetahuan modern yang semakin pesat
dan canggih di zaman sekarang ini ternyata hidup berdampingan dan saling
melengkapi dengan obat tradisional. Hal ini terbukti dari banyaknya peminat
pengobatan tradisional (Dalimartha, 2000). Masyarakat semakin sadar akan
pentingnya kembali ke alam dengan memanfaatkan obat–obat alami. Minat
terhadap obat tradisional terutama yang berasal dari tumbuhan tetap tinggi
disebabkan obat tradisional dapat diperoleh tanpa resep dokter, dapat diramu
sendiri, bahan baku tidak perlu diimpor dan tanaman obat dapat ditanam sendiri
oleh pemakainya (Djauhariya dan Hernani, 2004).
Radikal bebas adalah salah satu hasil samping metabolisme tubuh yang
paling merusak, diproduksi secara alami oleh tubuh dalam jumlah kecil, tetapi
akan timbul masalah bila diproduksi terlalu banyak. Berbagai penyakit seperti
kanker, arthritis, diabetes mellitus, katarak dan penyakit jantung disebabkan oleh
radikal bebas. Banyak bukti menunjukkan bahwa radikal bebas tidak hanya
menimbulkan penyakit tetapi juga mempercepat proses penuaan (Kramer, 2004).
Antioksidan adalah senyawa yang dalam kadar rendah dapat
memperlambat atau menghambat oksidasi. Radikal bebas dilumpuhkan oleh
antioksidan dengan memberikan elektron kepadanya sehingga tidak lagi mudah
bereaksi dengan bagian-bagian dari tubuh (Kosasih, dkk., 2004). Ada tiga cara
2
energi radikal bebas, menghentikan pembentukannya dan menghambat reaksi
berantai sehingga meminimalkan kerusakan sel (Kramer, 2004).
Ekstraksi dengan cara partisi cair-cair merupakan metode pemisahan yang
sangat baik dan populer karena dapat dilakukan untuk sampel dalam jumlah besar
ataupun jumlah kecil serta sangat berguna untuk memisahkan suatu zat dari zat
lain dengan cara melakukan partisi sampel antar 2 pelarut yang tidak saling
campur (Khopkar, 2008). Salah satu fasenya seringkali berupa air dan fase lain
berupa pelarut organik seperti kloroform. Ekstraksi pelarut juga digunakan untuk
memekatkan suatu zat yang ada dalam sampel dengan jumlah kecil sehingga
memungkinkan untuk deteksi atau kuantifikasinya. Kebanyakan prosedur
ekstraksi cair–cair merupakan ekstraksi sampel dari fase air ke dalam pelarut non
polar atau agak polar seperti heksana, diklorometan, atau sebaliknya. Ekstraksi
dilakukan dengan menggunakan corong pisah dalam waktu beberapa menit.
Pelarut organik yang dipilih mempunyai kelarutan yang rendah dalam air (<10%),
dapat menguap dan mempunyai kemurnian yang tinggi untuk meminimalkan
adanya kontaminasi sampel (Rohman, 2007).
Kurmak mbelin (Enydra fluctuans Lour.) suku Asteraceae merupakan
salah satu sayuran yang sering dikonsumsi oleh masyarakat di Kabupaten Karo,
mudah didapat dengan harga yang relatif murah serta menjadi sangat bermanfaat
sebagai obat jika dikaitkan dengan kandungan kimianya terutama golongan
3
Berdasarkan hal di atas, penulis tertarik untuk mengetahui aktivitas
antioksidan dari herba kurmak mbelin dengan cara ekstraksi cair–cair
menggunakan pelarut polar (air), semi polar (etanol dan etilasetat) dan non polar
(n-heksana) (Houghton dan Raman, 1998).
1.2Perumusan Masalah
a. Apakah karakteristik simplisia herba kurmak mbelin dapat ditentukan?
b. Apakah terdapat perbedaan golongan senyawa kimia yang terkandung
dalam ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air
herba kurmak mbelin?
c. Apakah ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air
herba kurmak mbelin memiliki aktivitas antioksidan?
1.3Hipotesis
a. Karakteristik simplisia herba kurmak mbelin dapat ditentukan sesuai
dengan cara karakterisasi yang terdapat dalam Materia Medika
Indonesia.
b. Terdapat perbedaan golongan senyawa kimia yang terkandung dalam
ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air herba
kurmak mbelin berdasarkan pelarut yang digunakan.
c. Ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air herba
4
1.4Tujuan
Tujuan penelitian ini adalah untuk:
a. mengetahui karakteristik simplisia dari herba kurmak mbelin.
b. mengetahui perbedaan golongan senyawa kimia yang terkandung dalam
ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air herba
kurmak mbelin.
c. mengetahui aktivitas antioksidan dari ekstrak etanol, fraksi n–heksana,
fraksi etilasetat dan fraksi air herba kurmak mbelin.
1.5Manfaat
Manfaat dari penelitian ini adalah sebagai informasi tentang karakteristik
simplisia, golongan kandungan senyawa kimia dan aktivitas antioksidan dari
ekstrak etanol, fraksi n–heksana, fraksi etilasetat dan fraksi air herba kurmak
5
BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, nama daerah, nama asing,
sistematika tumbuhan, morfologi tumbuhan serta kandungan kimia dan kegunaan
dari tumbuhan.
2.1.1 Daerah tumbuh
Kurmak mbelin (Enydra fluctuans Lour.) tumbuh di daerah tropis dan
subtropis (Patil, et al., 2008). Tumbuhan ini tumbuh di tanah rawa di India,
Bangladesh, Burma, Srilanka dan beberapa tempat di Asia Tenggara; di sepanjang
tepi sungai kecil di Manila dan pada daerah tropis di Afrika; di kolam dan danau
di daerah Bengal (Anonima, 2009). Di Bangladesh, kurmak mbelin tumbuh di
kolam, rawa-rawa dan sungai (Uddin, 2011). Di Filipina, kurmak mbelin tumbuh
di Provinsi Rizal di Luzon dan di sepanjang tepi sungai kecil (Anonimb, 2012).
Kurmak mbelin tumbuh liar dan kadang-kadang dibudidayakan. Di
dataran tinggi Karo, tumbuhan ini dapat tumbuh pada ketinggian 1800 m dari
permukaan laut. Di Jawa, kurmak mbelin tumbuh pada ketinggian 5-1600 m dari
permukaan laut (Anonimc, 1995).
2.1.2 Nama daerah
Kurmak mbelin disebut juga Ombur (Banten), sedangkan dalam bahasa
6
2.1.3 Nama asing
Nama asing kurmak mbelin menurut Anonimb (2012) adalah sebagai
berikut:
Inggris : Buffalo spinach, air cress, marsh herb
Malaysia : Chengkeru, Kangkong kerbau
Filipina : Kangkong kelabaw
Kamboja : Kanting ring
Laos : Bungz ping
India : Helencha, harkuch
China : Zhao ju
Thailand : Phak bung ruem
Vietnam : Cay rau ngo, Rau ngo, ngo Trau, ngo đất, ngo Huong
2.1.4 Sistematika tumbuhan
Sistematika tumbuhan kurmak mbelin menurut Gupta (2011) adalah
sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Asterales
Famili : Asteraceae
Genus : Enydra
7
2.1.5 Morfologi tumbuhan
Kurmak mbelin (Enydra fluctuans Lour.) tumbuh sepanjang tahun dan
termasuk tumbuhan menjalar yang tumbuh berkelompok (Anonima, 2009). Batang
agak berdaging, memiliki rongga, panjangnya 30 cm atau lebih, bercabang,
perakaran pada nodul yang lebih rendah dan agak berbulu. Diameter batang
0,3 – 0,6 m (Patil, et al., 2008). Daun berbentuk lanset dengan panjang
2,5 - 7,5 cm, runcing atau tumpul di ujung daun dan agak bergerigi pada tepi
daun. Daun hanya terdiri atas helaian saja (daun duduk), posisi daun berhadapan
dan menyilang. Bunganya berwarna putih, krem atau putih-kehijauan
(Tjitrosoepomo, 2007; Uddin, 2011).
2.1.6 Kandungan kimia
Kurmak mbelin (Enydra fluctuans Lour.) merupakan sumber yang baik
dari β-karoten. Tumbuhan ini mengandung saponin, myricyl alkohol, kaurol,
kolesterol, sitosterol, lakton seskuiterpen termasuk germacranolide, enhydrin,
fluctuanin dan fluctuandin, sejumlah asam diterpenoid dan isovalerate serta
turunan angelate, stigmasterol, steroid lain dan giberelin A9 dan A13 telah
diisolasi dari tumbuhan ini (Uddin, 2011). Kurmak mbelin juga mengandung
alkaloid, flavonoid, triterpenoid/steroid, tanin, glikosida dan klorin. Studi
menunjukkan kadar abu rendah dan sumber yang baik dari β-karoten
(3,7 - 4,2 mg/100 g secara bobot segar (Anonimb, 2012; Eneh, et al., 2013). Pada
konsentrasi 0,21% dari berat kering terkandung minyak esensial (Anonima, 2009).
2.1.7 Kegunaan
Daun kurmak mbelin digunakan oleh masyarakat Melayu sebagai obat
8
sebagai tambahan untuk tonik, penawar rasa sakit pada gonore, neuralgia dan
penyakit saraf lainnya (Patil, et al., 2008). Daunnya juga dapat menyembuhkan
peradangan dan cacar serta memiliki aktivitas analgesik, antidiare dan
antihipotensi (Sannigrahi, et al., 2010). Tumbuhan ini juga digunakan untuk
mengobati rheumatoid arthritis dan ascites. Bagian herba memiliki aktivitas
anthelmintik, antimikroba dan antioksidan (Akter, et al., 2012; Swain, et al.,
2012). Kurmak mbelin biasanya dimasak dengan kari ikan dan sebagai penambah
nafsu makan setelah mengalami demam atau tifus. Daunnya juga dapat
menyembuhkan leucoderma, bronchitis. Daun yang telah dihaluskan diletakkan di
atas kepala sebagai penurun panas (Eneh, et al., 2013; Uddin, 2011). Bagian muda
tumbuhan dikonsumsi sebagai salad di beberapa negara, termasuk Malaya. Di
Filipina, kadang-kadang daunnya dikukus sebelum dimakan dengan nasi dan
kentang rebus, juga digunakan pada kulit sebagai obat herpes. (Anonima, 2009).
2.2Simplisia dan Ekstrak 2.2.1 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang
belum mengalami pengolahan apapun juga dan kecuali dikatakan lain, berupa
bahan yang telah dikeringkan. Simplisia dibedakan simplisia nabati, simplisia
hewani dan simplisia pelikan (mineral). Simplisia nabati adalah simplisia yang
berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan (Depkes, 2000).
2.2.2 Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
9
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian sehingga memenuhi baku yang telah ditetapkan
(Depkes, 2000).
Pembuatan sediaan ekstrak dimaksudkan agar zat berkhasiat yang terdapat
di simplisia terdapat dalam bentuk yang mempunyai kadar yang tinggi dan hal ini
memudahkan zat berkhasiat dapat diatur dosisnya (Anief, 2000).
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut
cair yang sesuai. Senyawa aktif yang terdapat dalam berbagai simplisia dapat
digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan lain-lain.
Diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah
pemilihan pelarut dan cara ekstraksi yang tepat (Depkes, 2000).
Beberapa metode ekstraksi yang sering digunakan dalam berbagai
penelitian antara lain Depkes (2000) yaitu:
a. Cara dingin
1. Maserasi
Maserasi adalah proses pengekstraksi simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
ruangan (kamar). Secara teknologi termasuk ekstraksi dengan prinsip metode
pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan
pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan
pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama
10
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umunya dilakukan pada temperatur
ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap perendaman
antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus
menerus sampai diperoleh ekstrak (perkolat) yang tidak bereaksi ketika
ditambahkan serbuk Mg dan asam klorida pekat.
b. Cara panas
1. Refluks
Refluks adalah ektraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan
adanya pendingin balik. Umunya dilakukan pengulangan proses pada residu
pertama sampai 3 - 5 kali sehingga dapat termasuk proses ekstraksi sempurna.
2. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru
yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu
dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada
temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum
dilakukan pada temperatur 40 - 50oC.
4. Infundasi
11
(bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96 - 98oC)
selama waktu tertentu (15 - 20 menit).
5. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥30 menit) dan
temperatur sampai titik didih air.
2.3 Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih
elektron yang tidak berpasangan. Radikal bebas bertendensi kuat memperoleh
elektron dari atom lain, sehingga atom lain yang kekurangan satu elektron ini
berubah menjadi radikal bebas pula yang disebut radikal bebas sekunder (Kosasih,
dkk., 2004).
Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang
tidak terkontrol menghasilkan ikatan silang (cross-link) pada DNA, protein, lipida
atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul.
Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan
berperan dalam patologi dari berbagai penyakit degeneratif, yakni kanker,
aterosklerosis, rematik, jantung koroner, katarak dan penyakit degenerasi saraf
seperti parkinson (Silalahi, 2006).
Mekanisme reaksi radikal bebas merupakan suatu deret reaksi-reaksi
bertahap yaitu: (1) permulaan (inisiasi, initiation) suatu radikal bebas, (2)
perambatan (propagasi, propagation) reaksi radikal bebas; (3) pengakhiran
(terminasi, termination) reaksi radikal bebas. Tahapan mekanisme reaksi radikal
12
Tahap 1 (Inisiasi):
Cl-Cl �⎯⎯⎯⎯⎯⎯⎯��� 2 Cl•(Radikal bebas)
Tahap 2 (Propagasi):
CH4 + Cl• CH3• + HCl
CH3• + Cl2 CH3Cl + Cl•(dapat bereaksi dengan CH4)
Tahap 3 (Terminasi):
CH3• + Cl• CH3Cl
CH3• + CH3• CH3CH3
2.4 Antioksidan
Antioksidan atau reduktor berfungsi untuk mencegah terjadinya oksidasi
atau menetralkan senyawa yang telah teroksidasi dengan cara menyumbangkan
hidrogen dan atau elektron (Silalahi, 2006).
Atas dasar fungsinya antioksidan dapat dibedakan menjadi 5 (lima)
sebagai berikut.
a. Antioksidan primer
Antioksidan ini berfungsi untuk mencegah terbentuknya radikal bebas
yang baru karena dapat merubah radikal bebas yang ada menjadi molekul yang
berkurang dampak negatifnya.
b. Antioksidan sekunder
Antioksidan sekunder merupakan senyawa yang berfungsi menangkap
radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi
kerusakan yang lebih besar. Contoh yang populer, antioksidan sekunder adalah
13
c. Antioksidan tersier
Antioksidan tersier merupakan senyawa yang memperbaiki sel-sel dan
jaringan yang rusak karena serangan radikal bebas, biasanya yang termasuk
kelompok ini adalah jenis enzim misalnya metionin sulfoksidan reduktase yang
dapat memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk
perbaikan DNA pada penderita kanker.
d. Oxygen scavenger
Antioksidan yang termasuk oxygen scavenger mengikat oksigen sehingga
tidak mendukung reaksi oksidasi, misalnya vitamin C.
e. Chelators atau sequesstrants
Mengikat logam yang mampu mengkatalisis reaksi oksidasi misalnya
asam sitrat dan asam amino (Kumalaningsih, 2006).
2.4.1 Antioksidan alami
Sayur-sayuran dan buah-buahan kaya akan zat gizi (vitamin, mineral, serat
pangan) serta berbagai kelompok zat bioaktif lain yang disebut zat fitokimia. Zat
bioaktif ini bekerja secara sinergis, meliputi mekanisme enzim detoksifikasi,
peningkatan sistem kekebalan, pengurangan agregasi platelet, pengaturan sintesis
kolesterol dan metabolisme hormon, penurunan tekanan darah, antioksidan,
antibakteri serta efek antivirus (Silalahi, 2006).
2.4.2 β-karoten
β-karoten dipercaya dapat menurunkan resiko penyakit jantung dan
kanker. β-karoten berperan sebagai antioksidan. β-karoten terdapat pada aprikot,
14
menu makanan dapat mengurangi risiko terkena penyakit jantung (Kosasih, dkk.,
2004).
Sebagai antioksidan β-karoten bekerja dengan cara memperlambat fase
inisiasi. β-karoten merupakan salah satu provitamin A. Pemberian vitamin A
dalam dosis tinggi dapat bersifat toksis. Akan tetapi, β-karoten dalam jumlah
banyak mampu memenuhi kebutuhan vitamin A, dan selebihnya tetap sebagai β
-karoten yang berfungsi sebagai antioksidan (Silalahi, 2006).
Gambar 2.1 Rumus bangun β-karoten
2.4.3 Polifenol
Gambar 2.2 Struktur dasar polifenol
Senyawa fenol dapat di definisikan secara kimiawi oleh adanya satu cincin
aromatik yang membawa satu (fenol) atau lebih (polifenol) gugus hidroksil,
termasuk derifat fungsionalnya. Polifenol adalah kelompok zat kimia yang
ditemukan pada tumbuhan. Zat ini memiliki tanda khas yakni memiliki banyak
gugus fenol dalam molekulnya. Polifenol memiliki sifat kelarutan yang
berbeda-beda pada suatu pelarut. Hal ini disebabkan oleh gugus hidroksil pada senyawa
15
dapat menstabilkan radikal bebas dengan melengkapi kekurangan elektron yang
dimiliki radikal bebas dan menghambat terjadinya reaksi berantai dari
pembentukan radikal bebas. Polifenol merupakan komponen yang bertanggung
jawab terhadap aktivitas antioksidan dalam buah dan sayuran (Hattenschwiller
dan Vitousek, 2000).
Polifenol sebagai antioksidan primer menonaktifkan radikal bebas sesuai
dengan mekanisme transfer atom hidrogen (HAT) (1) dan transfer elektron
tunggal (SET) (2). Dalam mekanisme HAT (1), antioksidan ArOH bereaksi
dengan radikal bebas R dengan mentransfer sebuah atom hidrogen, melalui
pecahan homolisis ikatan O-H:
ArOH + R• ArO• + RH
Produk reaksi adalah spesies RH berbahaya dan radikal ArO• yang teroksidasi.
Bahkan jika reaksi mengarah pada pembentukan radikal lain, kurang reaktif
terhadap R•. Karena distabilkan oleh beberapa faktor. Mekanisme SET (2)
memberikan elektron untuk disumbangkan ke R•:
ArOH + R• ArOH+• + R
-Anion R- adalah spesies stabil secara energetik dengan jumlah elektron genap,
sedangkan radikal kation ArOH+• juga dalam kasus ini merupakan spesies radikal
kurang reaktif. Secara khusus, ArO• dan ArOH+• adalah struktur aromatik dimana
elektron ganjil berasal dari reaksi dengan radikal bebas, memiliki kemungkinan
tersebar di seluruh molekul, sehingga menjadi stabilisasi radikal (Leopoldini, et
16
2.5 Spektrofotometri UV-Visibel
Ahli kimia telah lama menggunakan warna sebagai bantuan dalam
mengenali zat-zat kimia. Spektrofotometri dapat dianggap sebagai perluasan
pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur absorpsi
energi radiasi macam-macam zat kimia dan memungkinkan dilakukannya
pengukuran kualitatif dari suatu zat dengan ketelitian yang lebih besar (Day dan
Underwood, 1986).
Spektrofotometer pada dasarnya terdiri atas sumber sinar monokromator,
tempat sel untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau
pencatat (Ditjen POM, 1979). Spektrofotometer yang sering digunakan dalam
dunia industri farmasi salah satu adalah spektrofotometer ultraviolet dengan
panjang gelombang 200 - 400 nm dan visibel (cahaya tampak) dengan panjang
gelombang 400 - 800 nm (Rohman, 2007).
2.6 Penentuan Aktivitas Antioksidan Dengan Metode DPPH
Pada tahun 1922, Goldschmidt dan Renn menemukan senyawa berwarna
ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen
kolorimetri untuk proses redoks. DPPH sangat berguna dalam berbagai
penyelidikan seperti inhibisi atau radikal polimerisasi kimia, penentuan sifat
antioksidan amina, fenol atau senyawa alami (vitamin, ekstrak tumbuh-tumbuhan,
obat obat-obatan) dan untuk menghambat reaksi homolitik. DPPH berwarna
sangat ungu seperti KMnO4 dan bentuk tereduksinya yaitu
1,1-difenil-2-picrylhydrazine (DPPH-H) yang berwarna oranye-kuning. DPPH tidak larut
17
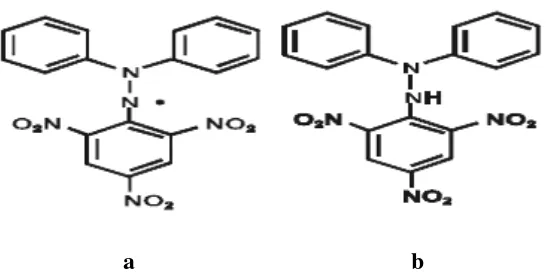
[image:34.595.172.446.103.242.2]a b
Gambar 2.3 Rumus bangun DPPH Keterangan:
a. bentuk radikal DPPH
b. bentuk nonradikal (DPPH-H)
DPPH merupakan radikal bebas yang stabil pada suhu kamar dan sering
digunakan untuk mengevaluasi aktivitas antioksidan beberapa senyawa atau
ekstrak bahan alam. DPPH menerima elektron atau radikal hidrogen akan
membentuk molekul diamagnetik yang stabil. Interaksi antioksidan dengan DPPH
baik secara transfer elektron atau radikal hidrogen pada DPPH, akan menetralkan
radikal bebas dari DPPH dan membentuk DPPH tereduksi. Warna larutan berubah
dari ungu tua menjadi kuning terang dan absorbansi pada panjang gelombang 517
nm akan hilang jika semua elektron pada radikal bebas DPPH menjadi
berpasangan. Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom
hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat reduktor. Suatu
zat mempunyai sifat antioksidan bila nilai IC50 kurang dari 200 ppm. Bila nilai
IC50 yang diperoleh berkisar antara 200 - 1000 ppm, maka zat tersebut kurang
aktif namun masih berpotensi sebagai zat antioksidan (Molyneux, 2004).
Senyawa antioksidan mempunyai sifat yang relatif stabil dalam bentuk
18
diprediksi dari golongan fenolat, flavonoida dan alkaloida, yang merupakan
senyawa-senyawa polar. Aktivitas antioksidan merupakan kemampuan suatu
senyawa atau ekstrak untuk menghambat reaksi oksidasi yang dapat dinyatakan
dengan persen penghambatan (Brand, 1995).
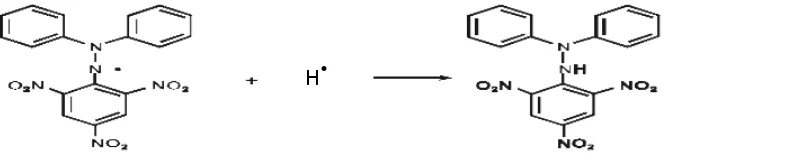
[image:35.595.116.519.403.483.2]Gambar 2.4 Resonansi DPPH (1,1- diphenyl-2-picrylhydrazyl)
Gambar 2.5 Reaksi antara DPPH dengan atom H netral yang berasal dari antioksidan
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah
harga konsentrasi efisien atau Effective Concentration (EC50) atau Inhibitory
Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat
antioksidan yang memberikan % penghambatan 50%. Harga EC50 atau IC50 yang
rendah berarti aktivitas antioksidan tinggi (Brand, 1995).
19
2.6.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut metanol atau
etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji
sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.6.2 Pengukuran absorbansi-panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
uji sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang
maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm
dan 520 nm. Pada prakteknya hasil pengukuran yang memberikan peak
maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang yang
disebutkan diatas. Nilai absorbansi yang mutlak tidaklah penting, karena panjang
gelombang dapat diatur untuk memberikan absorbansi maksimum sesuai dengan
alat yang digunakan (Molyneux, 2004).
2.6.3 Waktu reaksi
Pada metode sebelumnya waktu reaksi yang direkomendasikan adalah 30
menit dan sudah sering dilakukan. Waktu yang paling cepat yang pernah
digunakan, 5 menit atau 10 menit. Kenyataannya waktu reaksi yang benar adalah
ketika reaksi sudah mencapai kesetimbangan. Kecepatan reaksi dipengaruhi oleh
20
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian laboratorium.
Penelitian meliputi pengambilan tumbuhan, identifikasi tumbuhan, karakterisasi
simplisia, skrining fitokimia, pembuatan ekstrak etanol, fraksi n-heksana, fraksi
etilasetat, fraksi air dan uji aktivitas antioksidan dengan metode DPPH sebagai
sumber radikal bebas dan absorbansi DPPH diukur menggunakan alat
spektrofotometer visibel pada panjang gelombang 516 nm.
3.1Alat-Alat
Alat-alat yang digunakan terdiri dari alat-alat gelas laboratorium,
desikator, freeze dryer (Virtis), krus porselin, lemari pengering, mikroskop, neraca
analitis (Vibra), neraca kasar (O’haus), oven listrik (Stork), penangas air
(Yenaco), rotary evaporator (Stuart), spektofotometer UV/Vis (Shimadzu
UV-1800) dan tanur (Gallenkamp).
3.2 Bahan-Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah herba kurmak
mbelin dan air suling. Bahan-bahan kimia yang digunakan, kecuali dinyatakan
lain adalah berkualitas pro analisis: produksi Sigma: 1,1-diphenyl
-2-picrylhydrazyl (DPPH). Produksi Merck: etanol, metanol, kloroform, n-heksana,
etilasetat, isopropanol, eter, benzen, asam asetat anhidrida, natrium hidroksida,
alfa naftol, asam nitrat pekat, asam sulfat pekat, asam klorida pekat, toluena,
21
(III) nitrat, besi (III) klorida, amil alkohol.Bahan kimia berkualitas teknis: etanol
96%, n-heksana dan etilasetat.
3.3Penyiapan Tumbuhan 3.3.1 Pengambilan tumbuhan
Pengambilan tumbuhan dilakukan secara purposif yaitu tanpa
membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang
digunakan adalah herba kurmak mbelin yang diperoleh dari Desa Singa,
Kabanjahe, Kabupaten Karo, Provinsi Sumatera Utara.
3.3.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan oleh Pusat Penelitian dan Pengembangan
Biologi LIPI di Bogor. Tumbuhan yang digunakan untuk penelitian adalah sama
dengan tumbuhan yang digunakan oleh Silalahi. Hasil identifikasi tumbuhan dapat
dilihat pada Lampiran 1, halaman 46.
3.3.3 Pengolahan tumbuhan
Pengolahan herba kurmak mbelin dilakukan terhadap tumbuhan segar,
yaitu herba dibersihkan dari kotoran-kotoran, dicuci dengan air sampai bersih,
ditiriskan, ditimbang (5 kg), lalu dikeringkan di lemari pengering pada suhu
40 - 50oC sampai menjadi simplisia, kemudian ditimbang (430 g).
3.4Pembuatan Larutan Pereaksi 3.4.1 Larutan pereaksi bouchardat
Sebanyak 4 g kalium iodida ditimbang, kemudian dilarutkan dalam air
suling, ditambahkan iodium sebanyak 2 g dan dicukupkan dengan air suling
22
3.4.2 Larutan pereaksi mayer
Sebanyak 1,4 g raksa (II) klorida ditimbang, kemudian dilarutkan dalam
air suling hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida
lalu dilarutkan dalam 10 ml air suling. Kedua larutan dicampurkan dan
ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes, 1995).
3.4.3 Larutan pereaksi dragendorff
Sebanyak 0,8 g bismuth (III) nitrat ditimbang, kemudian dilarutkan dalam
20 ml asam nitrat pekat. Pada wadah lain ditimbang sebanyak 27,2 g kalium
iodida lalu dilarutkan dalam 50 ml air suling. Kedua larutan dicampurkan dan
didiamkan sampai memisah sempurna. Larutan yang jernih diambil dan
diencerkan dengan air suling hingga 100 ml (Depkes, 1995).
3.4.4 Larutan pereaksi molish
Sebanyak 3 g alfa naftol ditimbang, kemudian dilarutkan dalam asam
nitrat 0,5 N hingga volume 100 ml (Depkes, 1995).
3.4.5 Larutan pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat dilarutkan dalam air suling hingga
volume 100 ml (Depkes, 1995).
3.4.6 Larutan pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat dilarutkan dalam air suling hingga
volume 100 ml (Depkes, 1995).
3.4.7 Larutan pereaksi asam nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga
23
3.4.8 Larutan pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal asetat ditimbang, kemudian dilarutkan dalam air
suling bebas karbondioksida hingga volume 100 ml (Depkes, 1995).
3.4.9 Larutan pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air
suling hingga volume 100 ml (Depkes, 1995).
3.4.10 Larutan pereaksi kloralhidrat 70% b/b
Sebanyak 70 g kristal kloralhidrat ditimbang, kemudian dilarutkan dalam
30 ml air suling (Depkes, 1995).
3.4.11 Larutan pereaksi DPPH 0,5 mM
Sebanyak 20 mg DPPH ditimbang, kemudian dilarutkan dalam metanol
hingga volume 100 ml (Marinova, 2011).
3.5Pemeriksaan Mikroskopik Herba Kurmak Mbelin
Pemeriksaan mikroskopik dilakukan terhadap penampang melintang dari
daun dan batang kurmak mbelin. Caranya: 2 - 3 tetes larutan kloralhidrat
diteteskan di atas kaca objek, lalu sayatan daun dan batang kurmak mbelin
diletakkan di atasnya, dipanaskan, kemudian ditutup dengan kaca penutup, lalu
diamati di bawah mikroskop.
3.6Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air,
penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan
24
3.6.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap herba kurmak mbelin
dengan mengamati bentuk, warna, bau, rasa dan ukuran simplisia.
3.6.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia herba
kurmak mbelin. Sedikit serbuk simplisia ditaburkan di atas kaca objek yang telah
ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian
diamati di bawah mikroskop.
3.6.3 Penetapan kadar air
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu
alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume
air dalam tabung penerima dibaca dengan ketelitian 0,05 ml. Dimasukkan 5 g
serbuk simplisia yang telah ditimbang seksama ke dalam labu tersebut, kemudian
dipanaskan hati-hati selama 15 menit. Kecepatan tetesan diatur 2 tetes per detik
setelah toluen mendidih, sampai sebagian besar air terdestilasi, kemudian
kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Bagian dalam
pendingin dibilas dengan toluen setelah semua air terdestilasi. Destilasi
dilanjutkan selama 5 menit kemudian tabung penerima dibiarkan mendingin pada
suhu kamar. Volume air dibaca dengan ketelitian 0,05 ml setelah air dan toluen
memisah sempurna. Selisih kedua volume air yang dibaca sesuai dengan
kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung
25
3.6.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama
24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling sampai 1
liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama
kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat
pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang
telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap.
Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah
dikeringkan di udara (Depkes, 1995).
3.6.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama
24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali
selama 6 jam pertama lalu dibiarkan selama 18 jam kemudian disaring cepat
untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai
kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan
ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen
sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan
di udara (Depkes, 1995).
3.6.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang dengan seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara kemudian diratakan.
Krus dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu
26
tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara
(Depkes, 1995).
3.6.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25
ml asam klorida encer selama 5 menit, lalu bagian yang tidak larut dalam asam
dikumpulkan dan disaring melalui kertas saring yang dipijarkan sampai bobot
tetap kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam
asam dihitung terhadap bahan yang dikeringkan di udara (Depkes, 1995).
3.7Skrining Fitokimia
Skrining fitokimia serbuk simplisia herba kurmak mbelin meliputi:
pemeriksaan senyawa alkaloida, glikosida, saponin, flavonoida, antrakinon, tanin
dan steroida/triterpenoida.
3.7.1 Pemeriksaan alkaloida
Sebanyak 0,5 g serbuk simplisia ditimbang, kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2
menit, didinginkan dan disaring. Filtrat dipakai untuk tes alkaloida. Diambil 3
tabung reaksi lalu ke dalam masing-masing tabung reaksi dimasukkan 0,5 ml
filtrat. Pada tabung:
a. Ditambahkan 2 tetes pereaksi Bouchardat
b. Ditambahkan 2 tetes pereaksi Dragendorff
c. Ditambahkan 2 tetes pereaksi Mayer
Alkaloida disebut positif jika terjadi endapan atau kekeruhan pada paling sedikit 2
27
3.7.2 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml
campuran 7 bagian volume etanol 96% dan 3 bagian volum air suling ditambah
dengan 10 ml asam klorida 2 N. Direfluks selama 30 menit, didinginkan dan
disaring. Diambil 20 ml filtrat, ditambahkan 25 ml air suling dan 25 ml timbal (II)
asetat 0,4 M lalu dikocok selama 5 menit dan disaring. Filtrat disari dengan 20 ml
campuran 3 bagian kloroform dan 2 isopropanol dilakukan berulang sebanyak tiga
kali. Kumpulan sari air diuapkan pada temperatur tidak lebih dari 50oC. Sisanya
dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut,
yaitu 0,1 ml larutan percobaan dimasukkan ke dalam tabung reaksi, diuapkan di
penangas air. Sisa dilarutkan dalam 2 ml air suling dan 5 tetes pereaksi Molish
kemudian secara perlahan ditambahkan 2 ml asam sulfat pekat. Glikosida positif
jika terbentuk cincin ungu (Depkes, 1995).
3.7.3 Pemeriksaan saponin
Sebanyak 0,5 g sampel dimasukkan ke dalam tabung reaksi dan
ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat
selama 10 detik, timbul busa yang mantap tidak kurang dari 10 menit setinggi
1 - 10 cm. Ditambahkan 1 tetes larutan asam klorida 2 N, bila buih tidak hilang
menunjukkan adanya saponin (Depkes, 1995).
3.7.4 Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia kemudian ditambahkan 100 ml air panas,
dididihkan selama 5 menit dan disaring dalam keadaan panas, filtrat yang
diperoleh kemudian diambil 5 ml lalu di tambahkan 0,1 g serbuk Mg dan 1 ml
28
Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil
alkohol (Farnsworth, 1966).
3.7.5 Pemeriksaan glikosida antrakinon
Sebanyak 0,2 g serbuk simplisia ditambahkan 5 ml asam sulfat 2 N,
dididihkan 5 menit, didinginkan, ditambahkan 10 ml benzen, dikocok lalu
didiamkan. Lapisan benzen dipisahkan dengan cara disaring, filtrat yang berwarna
kuning menunjukkan adanya glikosida antrakinon. Lapisan benzen dikocok
dengan 1 - 2 ml natrium hidroksida 2 N lalu didiamkan. Lapisan air berwarna
merah dan lapisan benzen tidak berwarna menunjukkan adanya glikosida
antrakinon (Depkes, 1995).
3.7.6 Pemeriksaan tanin
Sebanyak 0,5 g sampel disari dengan 10 ml air suling, disaring lalu
filtratnya diencerkan dengan air suling sampai tidak berwarna. Dua ml larutan
ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau
hijau kehitaman menunjukkan adanya tanin (Depkes, 1995).
3.7.7 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g sampel dimaserasi dengan n-heksana selama 2 jam, lalu
disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan 2 tetes
asam asetat anhidrida dan 1 tetes asam sulfat pekat. Timbul warna biru atau hijau
menunjukkan adanya steroida dan timbul warna merah, pink atau ungu
29
3.8Pembuatan Ekstrak
3.8.1Pembuatan ekstrak etanol
Pembuatan ekstrak etanol herba kurmak mbelin dilakukan secara perkolasi
menggunakan pelarut etanol. Prosedur pembuatan ekstrak: sebanyak 250 g serbuk
simplisia dibasahi dengan etanol 96% dan dibiarkan selama 3 jam, kemudian
dimasukkan ke dalam alat perkolator, lalu cairan penyari etanol dituang sampai
semua simplisia terendam dan terdapat selapis cairan penyari di atasnya. Mulut
tabung perkolator ditutup dengan alumunium foil dan dibiarkan selama 24 jam,
kemudian kran dibuka dan perkolat dibiarkan menetes dengan kecepatan 20 tetes
/menit, perkolat ditampung. Perkolasi dihentikan pada saat beberapa tetes perkolat
tidak bereaksi ketika ditambahkan serbuk Mg dan asam klorida pekat, kemudian
dipekatkan dengan alat penguap vakum putar (suhu 50oC) setelah itu dikeringkan
dengan freeze dryer hingga diperoleh ekstrak kental.
3.8.2Pembuatan ekstrak dan fraksi
Sebanyak 10 g ekstrak etanol herba kurmak mbelin ditambahkan dengan
40 ml etanol dan 100 ml air panas, dihomogenkan lalu dimasukkan ke corong
pisah kemudian diekstraksi dengan 100 ml n-heksana sebanyak 3 kali sehingga
dihasilkan fraksi n-heksana dan fraksi air. Fraksi n-heksana dipekatkan. Fraksi air
diekstraksi dengan 100 ml etilasetat sebanyak 3 kali sehingga dihasilkan fraksi
etilasetat dan fraksi air. Fraksi etilasetat dipekatkan dengan rotary evaporator
30
3.9Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel 3.9.1Prinsip metode penangkapan radikal bebas DPPH
Kemampuan sampel uji dalam meredam proses oksidasi DPPH (1,1–
diphenyl–2-picrylhydrazil) sebagai radikal bebas dalam larutan metanol (sehingga
terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50
(konsentrasi sampel uji yang mampu meredam radikal bebas 50%) digunakan
sebagai parameter untuk menentukan aktivitas antioksidan sampel uji.
3.9.2Pengukuran larutan DPPH
Sebanyak 20 mg DPPH dilarutkan dalam metanol hingga volume 100 ml
untuk mendapatkan larutan DPPH 0,5 mM (konsentrasi 200 ppm). Dipipet
sebanyak 5 ml kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan
dengan metanol sampai garis tanda (konsentrasi 40 ppm). Pengukuran dilakukan
pada panjang gelombang 400 - 800 nm (Rohman, 2007).
3.9.3Pembuatan larutan induk
Sebanyak 25 mg ekstrak kurmak mbelin ditimbang, dimasukkan ke dalam
labu tentukur 25 ml, dilarutkan dengan metanol lalu volumenya dicukupkan
dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
3.9.4Pengukuran aktivitas antioksidan sampel uji
Larutan induk dipipet sebanyak 0,25 ml; 0,5 ml; 0,75 ml; dan 1 ml ke
dalam labu tentukur 25 ml untuk mendapatkan konsentrasi larutan uji 10 ppm, 20
ppm, 30 ppm, dan 40 ppm. Ditambahkan 5 ml larutan DPPH 0,5 mM (200 ppm)
ke dalam masing-masing labu tentukur lalu volumenya dicukupkan dengan
metanol sampai garis tanda. Pengukuran dilakukan setelah didiamkan selama 60
31
3.9.5Penentuan persen peredaman
Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH
(peredaman warna ungu DPPH) akibat adanya penambahan sampel. Nilai serapan
larutan DPPH sebelum dan sesudah penambahan ekstrak tersebut dihitung sebagai
persen peredaman (% peredaman) dengan rumus sebagai berikut:
% peredaman = Akontrol - Asampel Akontrol
x 100%
Keterangan: Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Selanjutnya hasil perhitungan dimasukkan ke dalam persamaan regresi
dengan konsentrasi ekstrak (ppm) sebagai absis (sumbu X) dan nilai % peredaman
(antioksidan) sebagai ordinatnya (sumbu Y).
3.9.6Penentuan nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji
(ppm) yang memberikan peredaman DPPH sebesar 50% (mampu meredam proses
oksidasi DPPH sebesar 50%). Nilai 0% berarti tidak mempunyai aktivitas
antioksidan, sedangkan nilai 100% berarti peredaman total dan pengujian perlu
dilanjutkan dengan pengenceran larutan uji untuk melihat batas konsentrasi
aktivitasnya. Hasil perhitungan dimasukkan ke dalam persamaan regresi dengan
konsentrasi ekstrak (ppm) sebagai absis (sumbu X) dan nilai % peredaman
(antioksidan) sebagai ordinatnya (sumbu Y). Secara spesifik, suatu senyawa
dikatakan sebagai antioksidan sangat kuat jika nilai IC50 kurang dari 50 ppm, kuat
untuk IC50 bernilai 50 - 100 ppm, sedang jika IC50 bernilai 100 - 150 ppm dan
32
BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense,
Bidang Botani Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia
(LIPI), Bogor, menunjukkan bahwa sampel termasuk ke dalam suku Asteraceae,
spesies Enydra fluctuans Lour.
4.2Hasil Pemeriksaan Mikroskopik Herba Kurmak Mbelin
Hasil pemeriksaan mikroskopik dari penampang melintang daun kurmak
mbelin memperlihatkan adanya rambut penutup, kutikula, berkas pengangkut,
stomata, jaringan epidermis atas dan epidermis bawah serta jaringan mesofil yang
terdiri dari jaringan pagar dan jaringan bunga karang. Pada penampang melintang
batang tampak adanya sel epidermis, jaringan korteks dengan rongga udara yang
besar (rexogen), berkas pembuluh tipe kolateral terbuka dan jaringan parenkim.
4.3Hasil Pemeriksaan Karakteristik Simplisia 4.3.1Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik dari simplisia menunjukkan bahwa
simplisia berupa daun kering menggulung tidak beraturan dan keriput, memiliki
warna hijau tua, bau aromatik, rasa agak pahit, ukuran panjang 4,5 – 6 cm dan
33
4.3.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik dari serbuk simplisia terdapat fragmen
mesofil, stomata tipe anomositik, xilem dengan dinding berpenebalan spiral, dan
rambut penutup.
4.3.3 Hasil pemeriksaan karakteristik serbuk simplisia
Hasil penetapan kadar air serbuk simplisia herba kurmak mbelin
memenuhi persyaratan dari buku Materia Medika Indonesia yaitu tidak lebih dari
10%. Kadar air yang melebihi persyaratan memungkinkan terjadinya
pertumbuhan jamur. Penetapan kadar sari larut air untuk mengetahui kadar sari
yang larut dalam air. Senyawa-senyawa yang dapat larut dalam air adalah
glikosida, gula, gom, protein, enzim, zat warna, dan asam organik. Penetapan
kadar sari larut etanol untuk mengetahui kadar sari yang larut dalam pelarut polar.
Senyawa-senyawa yang dapat larut dalam etanol adalah glikosida, antrakinon,
steroid terikat, klorofil, dan dalam jumlah sedikit yang larut yaitu lemak dan
saponin (Depkes, 1986). Penetapan kadar abu total untuk mengetahui kadar zat
anorganik yang terdapat pada simplisia, sedangkan penetapan kadar abu tidak
larut asam untuk mengetahui kadar zat anorganik yang tidak larut dalam asam
[image:50.595.118.508.623.744.2](Depkes, 1995). Hasilnya dapat dilihat pada Tabel 4.1 berikut ini.
Tabel 4.1 Hasil pemeriksaan karakteristik serbuk simplisia herba kurmak mbelin
No. Parameter Hasil Pemeriksaan (%)
1. 2. 3. 4. 5. Kadar air
Kadar sari larut air
Kadar sari larut etanol
Kadar abu total
Kadar abu tidak larut asam
5,2
20,63
17,24
14,28
34
4.4 Hasil Skrining Fitokimia
4.4.1 Hasil skrining fitokimia serbuk simplisia
Hasil skrining fitokimia terhadap serbuk simplisia diketahui bahwa serbuk
simplisia herba kurmak mbelin mengandung golongan senyawa-senyawa kimia
[image:51.595.118.512.263.380.2]seperti yang terlihat pada Tabel 4.2 berikut ini.
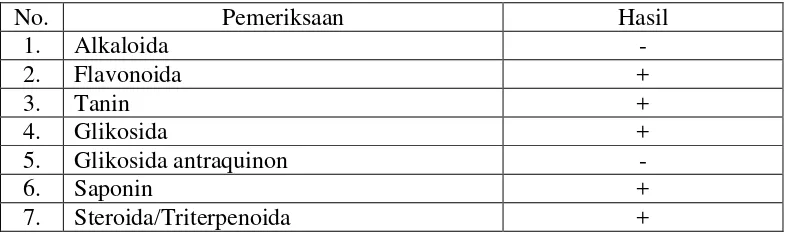
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia herba kurmak mbelin
No. Pemeriksaan Hasil
1. Alkaloida -
2. Flavonoida +
3. Tanin +
4. Glikosida +
5. Glikosida antraquinon -
6. Saponin +
7. Steroida/Triterpenoida +
Keterangan: ( + ) positif : mengandung golongan senyawa ( - ) negatif: tidak mengandung golongan senyawa
Penentuan golongan senyawa kimia terhadap serbuk simplisia herba
kurmak mbelin dilakukan untuk mendapatkan informasi golongan senyawa
metabolit sekunder yang terdapat di dalamnya. Skrining flavonoid dengan
penambahan serbuk Mg, HCl pekat dan amil alkohol memberikan warna jingga
pada lapisan amil alkohol. Ini dianggap bahwa flavonoid positif pada herba
kurmak mbelin. Sedangkan skrining tanin dengan penambahan FeCl3 memberikan
warna biru kehitaman yang menunjukan adanya tanin yaitu pirogalol (Farnsworth,
1966).
Skrining glikosida dengan penambahan pereaksi Molish dan asam sulfat
pekat akan terbentuk cincin ungu. Pereaksi Molish merupakan pereaksi umum
yang digunakan untuk identifikasi karbohidrat, dalam hal ini adalah gula.
35
cm dan tidak hilang dengan penambahan HCl 2 N (Depkes, 1995). Skrining
steroid dengan penambahan Liebermann-Burchard memberikan warna merah
ungu (Harborne, 1987).
Hasil di atas menunjukkan bahwa kurmak mbelin memiliki potensi
sebagai antioksidan dengan adanya senyawa yang mempunyai potensi sebagai
antioksidan yaitu flavonoida dan tanin (Rahman dan Choudhary, 2001).
4.4.2Hasil skirining fitokimia ekstrak dan fraksi
Hasil skrining fitokimia terhadap ekstrak dan fraksi herba kurmak mbelin
mengandung golongan senyawa-senyawa kimia seperti yang terlihat pada Tabel
[image:52.595.113.511.402.548.2]4.3 berikut ini.
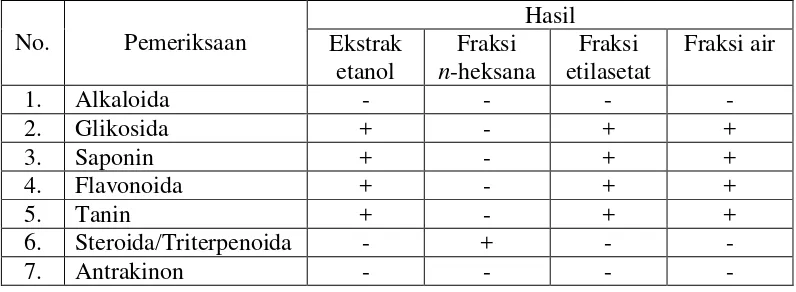
Tabel 4.3 Hasil skrining fitokimia ekstrak dan fraksi herba kurmak mbelin
No. Pemeriksaan
Hasil Ekstrak etanol Fraksi n-heksana Fraksi etilasetat Fraksi air
1. Alkaloida - - - -
2. Glikosida + - + +
3. Saponin + - + +
4. Flavonoida + - + +
5. Tanin + - + +
6. Steroida/Triterpenoida - + - -
7. Antrakinon - - - -
Keterangan: (+) positif: mengandung golongan senyawa (-) negatif: tidak mengandung golongan senyawa
Skrining fitokimia terhadap ekstrak etanol, fraksi n-heksana, etilasetat dan
air menunjukkan adanya distribusi golongan senyawa kimia berdasarkan
kepolaran pelarut yang digunakan. Dalam proses fraksinasi, senyawa yang
bersifat polar yaitu glikosida, flavonoid, saponin dan tanin terdapat dalam ekstrak
etanol, fraksi etilasetat dan air, sedangkan steroid terdapat dalam fraksi n-heksana
36
herba kurmak mbelin memiliki potensi sebagai antioksidan, yaitu dengan adanya
senyawa-senyawa yang mempunyai potensi sebagai antioksidan antara lain tanin
dan flavonoida (Rahman dan Choudhary, 2001).
4.5 Hasil Penentuan Panjang Gelombang Serapan Maksimum
Hasil pengukuran serapan maksimum larutan DPPH 40 ppm dalam
metanol dengan menggunakan spektrofotometer UV-Visibel. Hasil pengukuran
menunjukkan bahwa larutan DPPH dalam metanol menghasilkan serapan
maksimum sebesar 0,991 ppm pada panjang gelombang 516 nm dan termasuk
dalam kisaran panjang gelombang sinar tampak (400 nm - 800 nm) (Rohman,
[image:53.595.118.503.390.709.2]2007). Data hasil pengukuran dapat dilihat pada Gambar 4.1.
Gambar 4.1 Kurva serapan maksimum larutan DPPH 40 ppm dalam metanol secara
37
4.6 Hasil Analisis Aktivitas Antioksidan
Aktivitas antioksidan ekstrak etanol, fraksi n-heksana, etilasetat dan air
dari herba kurmak mbelin diperoleh dari hasil pengukuran absorbansi DPPH pada
menit ke-60 dengan adanya penambahan larutan uji dengan konsentrasi 10 ppm,
20 ppm, 30 ppm, dan 40 ppm yang dibandingkan dengan kontrol DPPH (tanpa
penambahan larutan uji). Untuk melihat hubungan absorbansi DPPH terhadap
pertambahan konsentrasi larutan uji dalam menganalisis aktivitas antioksidan
[image:54.595.115.480.317.667.2]dapat dilihat pada Gambar 4.2.
Gambar 4.2 Hasil analisis aktivitas antioksidan ekstrak etanol, fraksi n-heksana, etilasetat dan air dari herba kurmak mbelin pada menit ke-60.
0 0.2 0.4 0.6 0.8 1 1.2
0 10 20 30 40
A
b
so
rb
a
n
si