KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK
ETANOL PUCUK DAUN LABU KUNING (Cucurbita moschata
Duch.) DAN HERBA PELENG (Spinacia oleracea L.)
SERTA
HERBA SABI (Brassica rapa L.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH :
LORAETTA BRETY SEBAYANG NIM 081501032
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK
ETANOL PUCUK DAUN LABU KUNING (Cucurbita moschata
Duch.) DAN HERBA PELENG (Spinacia oleracea L.)
SERTA
HERBA SABI (Brassica rapa L.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
LORAETTA BRETY SEBAYANG NIM 081501032
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK
ETANOL PUCUK DAUN LABU KUNING (Cucurbita moschata
Duch.) DAN HERBA PELENG (Spinacia oleracea L.)
SERTA
HERBA SABI (Brassica rapa L.)
OLEH :
LORAETTA BRETY SEBAYANG NIM 081501032
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Juli 2012 Pembimbing I, Panitia Penguji,
Dra. Herawaty Ginting, M.Si., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195112231980032002 NIP 195709091985112001
Pembimbing II, Dra. Herawaty Ginting M.Si., Apt. NIP 195108161980031002
Dr. M.Pandapotan Nasution, MPS., Apt. Dra. Erly Sitompul, M.Si., Apt. NIP 194908111976031001 NIP 195006121980032001
Drs. Suryadi Achmad, M.Sc., Apt. NIP 195109081985031002
Medan, Juli 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat, kasih dan karunianNya, sehingga penulis dapat menyelesaikan skripsi ini. Penelitian ini bertujuan untuk melakukan karakterisasi simplisia dan skrining fitokimia serta uji aktivitas antioksidan ekstrak etanol pucuk daun labu kuning (Cucurbita moschata Duch.) dan herba peleng (Spinacia oleracea L.) serta herba sabi (Brassica rapa L.). Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda dan Ibunda tercinta, Ir. Edy Perin Sebayang dan Ibunda D. Tarigan, yang tiada hentinya berkorban dengan tulus ikhlas bagi kesuksesan penulis, juga kepada adikku yang selalu setia memberi doa, dorongan, dan motivasi selama penulis melakukan penelitian.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna, sehingga penulis mengharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
Medan, Juli 2012 Penulis
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL PUCUK DAUN
LABU KUNING (Cucurbita moschata Duch.) DAN HERBA PELENG (Spinacia oleracea L.) SERTA HERBA SABI (Brassica rapa L.)
ABSTRAK
Pucuk daun labu kuning, herba peleng dan herba sabi merupakan tumbuhan yang digunakan sebagai sayur-sayuran yang terkenal pada masyarakat Tanah Karo, Sumatera Utara. Akhir-akhir ini sayur-sayuran ini juga disebut-sebut memiliki khasiat antioksidan yang dapat menangkal radikal bebas sehingga dapat mencegah berbagai macam penyakit. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia dan kekuatan aktivitas antioksidan dari ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi.
Karakterisasi dan skrining fitokimia dilakukan terhadap serbuk simplisia, selanjutnya serbuk simplisia diekstraksi secara perkolasi etanol 96%. Masing-masing ekstrak dipekatkan dengan bantuan rotary evaporator dan dikeringkan menggunakan freeze dryer sehingga diperoleh ekstrak kental. Terhadap masing-masing ekstrak diuji aktivitas antioksidan dengan menggunakan metode penangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil), dilakukan dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-60. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil pemeriksaan karakteristik simplisia pucuk daun labu kuning, herba peleng dan herba sabi, diperoleh kadar air 7,29%, 8,24%, dan 7,98%, kadar sari yang larut dalam air diperoleh 13,55%, 9,75% dan 22,19%, kadar sari yang larut dalam etanol 8,99%, 16,05%, 11,35%, kadar abu total diperoleh 6,67%, 6,62% dan 4,43% dan kadar abu yang tidak larut dalam asam diperoleh 0,48%, 0,30% dan 0,26%. Hasil skrining fitokimia diperoleh pucuk daun labu kuning mengandung senyawa kimia golongan glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Herba peleng mengandung golongan alkaloida, glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Herba sabi mengandung golongan alkaloida, glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Hasil pengujian aktivitas antioksidan dalam meredam radikal bebas DPPH menunjukkan bahwa ekstrak etanol herba sabi memiliki aktivitas antioksidan kuat, ekstrak etanol pucuk daun labu kuning dengan aktivitas antioksidan sedang dan ekstrak etanol peleng dengan aktivitas antioksidan sangat lemah, dengan nilai Inhibitory Concentration (IC50) yang diperoleh dari ekstrak ekstrak etanol masing-masing sebesar 94,40 ppm, 101,47 ppm dan 421,04 ppm.
Kata kunci: antioksidan, pucuk daun labu kuning (Cucurbita moschata Duch.),
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING THEN ANTIOXIDANT ACTIVITIES TEST OF ETHANOL
EXTRACT FROM PUMPKIN LEAVE (Cucurbita moschata Duch.), PELENG HERBAL (Spinacia oleracea L.) AND SABI HERBAL
(Brassica rapa L.) ABSTRACT
Pumpkin leave, peleng herbal and sabi herbal are kind of spice among wild plants by the public Karo of North Sumatera. Lately, vegetables also touted to have antioxidant properties that can counteract the free radicals thus preventing various disease. The purpose of this study was to determine the characteristics of simplex, chemical compounds content and to know the strength of antioxidant activity of ethanol extracts of pumpkin leave, peleng herbal and sabi herbal
Characterization and phytochemical screening was done toward powder of simplex, furthermore the powder of simplex was extracted by gradually percolation used solvents ethanol 96%.. Each of extract concentrated using rotary evaporatory and dried using a freeze dryer to obtain viscous extract. Toward each of extract was assayed the antioxidant activity used scavenging of free radical DPPH (1,1-diphenyl-2-picrylhydrazil) method, by measured the DPPH absorbance at a wavelength of 516 nm in the 60th minutes. Antioxidant capability was measured as a decrease in absorbance of DPPH solution after addition of extract.
Test results of simplex characteristic pumpkin leave, peleng herbal and sabi herbal obtained level of water content 7.29%, 8.24%, and 7.98%, level of water-soluble extract 13.55%, 9.75% and 22.19%, level of ethanol-soluble extract 8.99%, 16.05%, and 11.35%, level of total ash 6.67%, 6.62% and 4.43%, and level of ash does not soluble in acid 0.48%, 0.30% and 0.26%. Based on phytochemical screening, it was obtained that pumpkin leave contains glycosides, flavonoides, saponins, tannins and steroides/triterpenoides. Peleng herbal contains alkaloides, glycosides, flavonoides, saponin, tannins and steroides/triterpenoides. Sabi herbal contains alkaloides, glycosides, flavonoides, saponins, tannins and steroides/triterpenoides. Results of testing the antioxidant activities in scavenging free radical DPPH showed that ethanol extract of sabi herbal have strong antioxidant activity, ethanol extract of pumpkin leave have medium antioxidant activity and ethanol extract of peleng herbal have very weak antioxidant activity, with a value of Inhibitory Concentration (IC50) obtained from ethanol extract amounted to 94.40 ppm, 101.47 ppm and 421.04 ppm.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan ... 4
1.5 Manfaat ... 4
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian tumbuhan ... 6
2.1.1 Daerah tumbuh ... 6
2.1.1.1 Labu kuning ... 6
2.1.1.3 Sabi ... 7
2.1.2 Nama daerah ... 7
2.1.2.1 Labu kuning ... 7
2.1.2.2 Peleng ... 7
2.1.2.3 Sabi ... 7
2.1.3 Nama asing ... 7
2.1.3.1 Labu kuning ... 7
2.1.3.2 Peleng ... 8
2.1.3.3 Sabi ... 8
2.1.4 Sistematika tumbuhan ... 8
2.1.4.1 Labu kuning ... 8
2.1.4.2 Peleng ... 9
2.1.4.3 Sabi ... 9
2.1.5 Morfologi tumbuhan ... 9
2.1.5.1 Labu kuning ... 9
2.1.5.2 Peleng ... 9
2.1.5.3 Sabi ... 10
2.1.6 Kandungan kimia ... 10
2.1.6.1 Labu kuning ... 10
2.1.6.2 Peleng ... 10
2.1.6.3 Sabi ... 10
2.1.7 Kegunaan ... 10
2.1.7.1 Labu kuning ... 10
2.1.7.3 Sabi ... 11
2.2 Ekstraksi ... 11
2.3 Radikal bebas ... 13
2.4 Antioksidan ... 14
2.4.1 Antioksidan alami ... 15
2.4.2 Vitamin C ... 16
2.4.3 Betakaroten ... 17
2.4.4 Vitamin E ... 18
2.4.5 Polifenol ... 18
2.5 Spektrofotometri UV-VIS ... 19
2.6 Penentuan aktivitas antioksidan dengan metode DPPH ... 20
2.6.1 Pelarut ... 23
2.6.2 Pengukuran absorbansi-panjang gelombang ... 23
2.6.3 Waktu pengukuran ... 23
BAB III METODE PENELITIAN ... 24
3.1 Alat dan Bahan ... 24
3.1.1 Alat-alat ... 24
3.1.2 Bahan-bahan ... 24
3.2 Pengumpulan dan Pengolahan Bahan Tumbuhan ... 25
3.2.1 Pengumpulan tumbuhan ... 25
3.2.2 Identifikasi tumbuhan ... 25
3.2.3 Pengolahan tumbuhan ... 25
3.3 Pembuatan Pereaksi ... 26
3.3.2 Pereaksi natrium hidroksida 2N ... 26
3.3.3 Pereaksi Bouchardat ... 26
3.3.4 PereaksiMayer ... 26
3.3.5 Pereaksi Dragendorff ... 26
3.3.6 Pereaksi besi (III) klorida 1% ... 26
3.3.7 Pereaksi Liebermann-Burchard ... 27
3.3.8 Pereaksi Molish ... 27
3.3.9 Pereaksi timbal (II) asetat 0,4 N ... 27
3.3.10 Larutan pereaksi asam sulfat 2 N ... 27
3.3.11 Larutan pereaksi DPPH 0,5 mM ... 27
3.4 Karakterisasi simplisia ... 27
3.4.1 Pemeriksaan makroskopik ... 27
3.4.2 Pemeriksaan mikroskopik ... 28
3.4.3 Penetapan kadar air ... 28
3.4.4 Penetapan kadar sari larut air ... 29
3.4.5 Penetapan kadar sari larut etanol ... 29
3.4.6 Penetapan kadar abu total ... 30
3.4.7 Penetapan kadar abu tidak larut asam ... 30
3.5 Skrining fitokimia ... 30
3.5.1 Pemeriksaan alkaloida ... 31
3.5.2 Pemeriksaan flavanoida ... 31
3.5.3 Pemeriksaan glikosida ... 31
3.5.4 Pemeriksaan Antrakuinon ... 32
3.5.6 Pemeriksaan tanin ... 32
3.5.7 Pemeriksaan steroida/triterpenoida ... 33
3.6 Pembuatan ekstrak etanol ... 33
3.7 Pengujian kemampuan antioksidan dengan apektrofotometer visibel ... 34
3.7.1 Prinsip metode penangkapan radikal bebas DPPH ... 34
3.7.2 Pembuatan larutan blanko ... 34
3.7.3 Penentuan panjang gelombang serapan Maksimum ... 34
3.7.4 Pembuatan larutan induk ... 34
3.7.5 Pembuatan larutan uji ... 34
3.7.6 Penentuan persen peredaman ... 35
3.7.7 Penentuan nilai IC50 ... 35
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1 Hasil identifikasi tumbuhan ... 37
4.2 Hasil karakterisasi sampel ... 37
4.3 Hasil skrining fitokimia ... 38
4.4 Hasil pengujian antioksidan ... 38
4.4.1 Hasil panjang gelombang serapan maksimum ... 40
4.5 Hasil analisis aktivitas antioksidan ... 40
4.6 Hasil analisis peredaman radikal bebas DPPH oleh sampel uji ... 43
4.7 Analisis nilai IC50 (Inhibitory concentration) Sampel uji ... 44
DAFTAR TABEL
Tabel Halaman 4.1 Hasil skrining fitokimia serbuk simplisia ... 39 4.2 Hasil analisis peredaman radikal bebas DPPH
oleh sampel uji ... 43 4.3 Hasil persamaan regresi linier yang diperoleh dari ekstrak
Pucuk daun labu kuning, herba peleng dan herba sabi ... 44 4.4 Nilai IC50 ekstrak etanol pucuk daun labu kuning,
DAFTAR GAMBAR
Gambar Halaman
2.1 Rumus Bangun Vitamin C ... 16
2.2 Rumus Bangun Betakaroten ... 18
2.3 Rumus Bangun Vitamin E ... 18
2.4 Struktur Dasar Polifenol ... 19
2.5 Rumus Bangun DPPH ... 22
2.6 Resonansi DPPH (1,1- diphenyl-2-picrylhydrazyl) ... 22
2.7 Reaksi antara DPPH dengan atom H netral yang berasal dari antioksidan ... 23
4.1 Kurva serapan maksimum larutan DPPH 40 ppm dalam metanol secara spektrofotometri visible ... 41
4.2 Hasil analisis aktivitas antioksidan ekstrak etanol pucuk labu kuning ... 42
4.3 Hasil analisis aktivitas antioksidan ekstrak etanol herba peleng ... 42
DAFTAR LAMPIRAN
Lampiran Halaman
1 Surat hasil identifikasi tumbuhan ... 51
2 Gambar makroskopik tumbuhan segar dan simplisa pucuk daun labu kuning ... 53
3 Gambar makroskopik tumbuhan segar dan simplisa Herba peleng ... 54
4 Gambar makroskopik tumbuhan segar dan simplisa Herba sabi ... 57
5 Gambar mikroskopik serbuk simplisa pucuk daun labu kuning ... 59
6 Gambar mikroskopik serbuk simplisa Herba peleng ... 59
7 Gambar mikroskopik serbuk simplisia Herba sabi ... 60
8 Gambar spektrofotometer UV-Vis (Shimadzu UV-1800) ... 61
9 Bagan pembuatan serbuk simplisia dan ekstrak Etanol ... 62
10 Hasil pemeriksaan karakteristik serbuk simplisia ... 66
11 Perhitungan penetapan kadar air serbuk simplisia ... 67
12 Perhitungan penetapan kadar sari larut air ... 70
13 Perhitungan penetapan kadar sari larut etanol ... 72
14 Perhitungan penetapan kadar abu total ... 74
15 Perhitungan penetapan kadar abu tidak larut asam ... 76
18 Hasil uji antioksidan ekstrak etanol herba sabi ... 82 19 Perhitungan nilai IC50 ekstrak etanol pucuk daun
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL PUCUK DAUN
LABU KUNING (Cucurbita moschata Duch.) DAN HERBA PELENG (Spinacia oleracea L.) SERTA HERBA SABI (Brassica rapa L.)
ABSTRAK
Pucuk daun labu kuning, herba peleng dan herba sabi merupakan tumbuhan yang digunakan sebagai sayur-sayuran yang terkenal pada masyarakat Tanah Karo, Sumatera Utara. Akhir-akhir ini sayur-sayuran ini juga disebut-sebut memiliki khasiat antioksidan yang dapat menangkal radikal bebas sehingga dapat mencegah berbagai macam penyakit. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia dan kekuatan aktivitas antioksidan dari ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi.
Karakterisasi dan skrining fitokimia dilakukan terhadap serbuk simplisia, selanjutnya serbuk simplisia diekstraksi secara perkolasi etanol 96%. Masing-masing ekstrak dipekatkan dengan bantuan rotary evaporator dan dikeringkan menggunakan freeze dryer sehingga diperoleh ekstrak kental. Terhadap masing-masing ekstrak diuji aktivitas antioksidan dengan menggunakan metode penangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil), dilakukan dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-60. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil pemeriksaan karakteristik simplisia pucuk daun labu kuning, herba peleng dan herba sabi, diperoleh kadar air 7,29%, 8,24%, dan 7,98%, kadar sari yang larut dalam air diperoleh 13,55%, 9,75% dan 22,19%, kadar sari yang larut dalam etanol 8,99%, 16,05%, 11,35%, kadar abu total diperoleh 6,67%, 6,62% dan 4,43% dan kadar abu yang tidak larut dalam asam diperoleh 0,48%, 0,30% dan 0,26%. Hasil skrining fitokimia diperoleh pucuk daun labu kuning mengandung senyawa kimia golongan glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Herba peleng mengandung golongan alkaloida, glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Herba sabi mengandung golongan alkaloida, glikosida, flavonoida, saponin, tanin dan steroida/triterpenoida. Hasil pengujian aktivitas antioksidan dalam meredam radikal bebas DPPH menunjukkan bahwa ekstrak etanol herba sabi memiliki aktivitas antioksidan kuat, ekstrak etanol pucuk daun labu kuning dengan aktivitas antioksidan sedang dan ekstrak etanol peleng dengan aktivitas antioksidan sangat lemah, dengan nilai Inhibitory Concentration (IC50) yang diperoleh dari ekstrak ekstrak etanol masing-masing sebesar 94,40 ppm, 101,47 ppm dan 421,04 ppm.
Kata kunci: antioksidan, pucuk daun labu kuning (Cucurbita moschata Duch.),
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING THEN ANTIOXIDANT ACTIVITIES TEST OF ETHANOL
EXTRACT FROM PUMPKIN LEAVE (Cucurbita moschata Duch.), PELENG HERBAL (Spinacia oleracea L.) AND SABI HERBAL
(Brassica rapa L.) ABSTRACT
Pumpkin leave, peleng herbal and sabi herbal are kind of spice among wild plants by the public Karo of North Sumatera. Lately, vegetables also touted to have antioxidant properties that can counteract the free radicals thus preventing various disease. The purpose of this study was to determine the characteristics of simplex, chemical compounds content and to know the strength of antioxidant activity of ethanol extracts of pumpkin leave, peleng herbal and sabi herbal
Characterization and phytochemical screening was done toward powder of simplex, furthermore the powder of simplex was extracted by gradually percolation used solvents ethanol 96%.. Each of extract concentrated using rotary evaporatory and dried using a freeze dryer to obtain viscous extract. Toward each of extract was assayed the antioxidant activity used scavenging of free radical DPPH (1,1-diphenyl-2-picrylhydrazil) method, by measured the DPPH absorbance at a wavelength of 516 nm in the 60th minutes. Antioxidant capability was measured as a decrease in absorbance of DPPH solution after addition of extract.
Test results of simplex characteristic pumpkin leave, peleng herbal and sabi herbal obtained level of water content 7.29%, 8.24%, and 7.98%, level of water-soluble extract 13.55%, 9.75% and 22.19%, level of ethanol-soluble extract 8.99%, 16.05%, and 11.35%, level of total ash 6.67%, 6.62% and 4.43%, and level of ash does not soluble in acid 0.48%, 0.30% and 0.26%. Based on phytochemical screening, it was obtained that pumpkin leave contains glycosides, flavonoides, saponins, tannins and steroides/triterpenoides. Peleng herbal contains alkaloides, glycosides, flavonoides, saponin, tannins and steroides/triterpenoides. Sabi herbal contains alkaloides, glycosides, flavonoides, saponins, tannins and steroides/triterpenoides. Results of testing the antioxidant activities in scavenging free radical DPPH showed that ethanol extract of sabi herbal have strong antioxidant activity, ethanol extract of pumpkin leave have medium antioxidant activity and ethanol extract of peleng herbal have very weak antioxidant activity, with a value of Inhibitory Concentration (IC50) obtained from ethanol extract amounted to 94.40 ppm, 101.47 ppm and 421.04 ppm.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Dewasa ini dunia kesehatan banyak membicarakan radikal bebas (free radical) dan antioksidan. Hal ini terjadi karena sebagian besar penyakit diawali oleh karena oksidasi yang berlebihan dalam tubuh (Winarsi, 2007). Radikal bebas selain terdapat di luar tubuh, radikal bebas juga terjadi dalam tubuh. Pembentukan radikal bebas dalam tubuh dan reaksi oksidasi pada biomolekul akan berlangsung sepanjang hidup. Radikal bebas dalam jumlah kecil masih dapat ditolerir oleh tubuh, namun berbahaya apabila dalam jumlah yang berlebih. Inilah penyebab utama dari proses penuaan dan berbagai penyakit degeneratif (Silalahi, 2006).
Tubuh manusia sebenarnya memproduksi beberapa jenis enzim antioksidan yaitu superoksida dismutase (SOD), katalase dan glutation peroksidase. Antioksidan yang diproduksi alami oleh tubuh akan menjadi lebih optimal bila kita mengkonsumsi makanan-makanan sehat seperti buah-buahan dan sayuran (Siagian, 2012).
Tanaman labu kuning (Cucurbita moschata Duch.) merupakan suatu jenis tanaman yang merambat dari suku Cucurbitaceae yang terdistribusi di seluruh dunia. Bagian tumbuhan yang digunakan adalah biji, buah, bunga dan daun. Tanaman ini mengandung karotenoid dan merupakan penghasil provitamin A yang cukup banyak. Daun tanaman ini menghasilkan asam lemak tak jenuh dan dibeberapa negara daunnya digunakan untuk mengobati sakit maag dan sakit kuning (Anonim, 2010).
Peleng (Spinacia oleracea L.) merupakan tumbuhan yang dijadikan makanan. Peleng mengandung vitamin seperti vitamin C, vitamin A dan vitamin E serta mineral seperti magnesium, mangan, kalsium, besi dan asam folat. Peleng juga mengandung flavonoid yang sangat kaya. Beberapa contohnya adalah kuersetin, mirisetin, kampeferol dan lain-lain (Subhash, 2010).
Sawi merupakan tumbuhan yang juga tersebar di seluruh dunia dan salah satu jenis sawi adalah sabi (Brassica rapa L.), yang mengandung polifenol yang cukup tinggi terutama flavonoid. Polifenol utama pada sayur ini adalah kuersetin, kaempferol dan isoramnetin (Cartea, et al., 2010).
1.2 Perumusan Masalah
1. Apakah karakteristik pucuk daun labu kuning (Cucurbita moschata
Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa
L.) dapat ditentukan?
2. Apakah kandungan golongan senyawa kimia dari pucuk daun labu kuning
(Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.) dapat ditentukan?
3. Apakah pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.) memiliki aktivitas antioksidan dan berapa kekuatan aktivitas antioksidan dari masing-masing tumbuhan?
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis dari penelitian ini adalah:
1. Dengan mengikuti cara pembuatan simplisia yang benar, maka dapat diketahui karakteristik simplisia pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.).
2. Kandungan golongan senyawa kimia dari pucuk daun labu kuning
3. Pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.) memiliki aktivitas antioksidan.
1.4Tujuan
Tujuan penelitian ini adalah :
1. Untuk menentukan karakteristik simplisia pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.).
2. Untuk mengetahui golongan senyawa kimia yang terkandung dalam pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.).
3. Untuk mengetahui kekuatan aktivitas antioksidan dari pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.).
1.5Manfaat
Manfaat penelitian ini adalah :
1. Dapat digunakan sebagai acuan tentang karakteristik simplisia pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea
2. Dapat memberikan informasi mengenai golongan senyawa-senyawa kimia yang terkandung dalam pucuk daun labu kuning (Cucurbita moschata
Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa
L.).
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh (habitat), morfologi tumbuhan, sistematika tumbuhan, nama daerah, nama asing, kandungan kimia dan kegunaan tumbuhan.
2.1.1 Daerah tumbuh 2.1.1.1 Labu kuning
Tanaman labu kuning banyak dibudidayakan di negara-negara Afrika, Amerika, India dan Cina, dapat tumbuh didataran rendah maupun dataran tinggi. Labu kuning adalah salah satu tanaman yang banyak tumbuh di Indonesia. Penanamannya tidak sulit, baik pembibitannya, perawatannya, hasilnyapun cukup memberikan nilai ekonomis untuk masyarakat. Tanaman ini dapat ditanam di lahan pertanian, halaman rumah atau tanah pekarangan yang kosong dapat kita manfaatkan (Sinaga, 2011).
2.1.1.2 Peleng
Peleng merupakan tanaman menahun, tumbuh subur di daerah dingin atau dataran tinggi yang beriklim sejuk, yaitu pada ketinggian 3000 kaki di atas permukaan laut dan lebih tinggi dapat tumbuh dengan baik. Tanah yang disenangi adalah tanah gembur yang mengandung tanah endapan (Heyne, 1987)
2.1.1.3 Sabi
dapat tumbuh pada iklim dingin dan merupakan tumbuhan dengan masa tumbuh yang singkat yaitu 45 hari. Sabi tumbuh dengan baik di tanah yang gembur dengan pH 5,5-6,8 (Duke, 1983).
2.1.2 Nama daerah 2.1.2.1 Labu kuning
Sumatera (Melayu) : Labu Parang Jawa Barat (Sunda) : Waluh
Jawa Tengah : Waluh
Tanah Karo : Tarok
2.1.2.2 Peleng
Karo : Peleng
Jawa : Bayam Jepang
2.1.2.3 Sabi
Jawa Barat : ansabi 2.1.3 Nama asing
2.1.3.1 Labu kuning
Inggris : pumpkin
2.1.3.2 Peleng
Inggris : Spinach
Cina : Bo cai
Jepang : Horenzo
Perancis : Epinard
India : Pinni
2.1.3.3 Sabi
Inggris : False pakchoi, Mock pakchoi
Thailand : Phakkat kheo kwangtung
Cina : Cai xin
2.1.4 Sistematika tumbuhan 2.1.4.1Labu kuning
Divisi : Spermatophyta Sub divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Cucurbitales
Familia : Cucurbitaceae
Genus : Cucurbita
Spesies : Cucurbita moschata Duch. (LIPI, 2012) 2.1.4.2Peleng
Divisi : Spermatophyta Sub Divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Caryophyllales
Famili : Chenopodiacea
Genus : Spinacia
2.1.4.3 Sabi
Divisi : Spermatophyta Sub Divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Capparales
Famili : Brassicaceae
Genus : Brassica
Spesies : Brassica rapa L. (LIPI, 2012) 2.1.5 Morfologi tumbuhan
2.1.5.1Labu kuning
Tumbuhan labu kuning merupakan jenis tanaman yang merambat. Batang berkayu lunak, segi lima, berambut, berbuku-buku panjang 25 cm hijau muda. Daunnya tunggal, bulat bertangkai, tangkai berlubang, ujung runcing tepi berombak, pangkal membulat, berbula panjang 7-35 cm, lebar 6-30 cm, beralur pertulangan menyirip, hjau. Buahnya bulat, berdaging tebal, diameter 25-35 cm, gundul dan berwarna kuning muda (Sinaga, 2011).
2.1.5.2Peleng
2.1.5.3Sabi
Sabi merupakan tumbuhan dengan bunga kuning, dengan batang berdaging 0.5-1 cm dan panjangnya 15-20 cm. Daun hijau terang atau gelap dan umumnya oval, dengan tepi daun sedikit bergerigi (Tenora, 2010).
2.1.6 Kandungan Kimia 2.1.6.1Labu Kuning
Bagian tumbuhan yang sering digunakan adalah buah, biji dan daun. Labu
kuning mengandung β-karoten, α-karoten dan lutein sedangkan daunnya
mengandung asam lemak tak jenuh (Anonim, 2010). 2.1.6.2Peleng
Peleng memiliki kandungan flavonoid yang tinggi seperti mirisetin, kuersetin dan kaempferol, senyawa fenol seperti asam ferulat, mengandung vitamin seperti vitamin A, C, E dan K, serta mineral seperti magnesium, mangan, kalsium, posfor dan besi (Subhash, 2010).
2.1.6.3Sabi
Sabi memiliki kandungan kimia seperti lemak, protein, karbohidrat, serat, kalsium, besi, posfor, natrium, kalsium, β-karoten, tiamin, riboflavin, niasin dan vitamin C (Duke, 1983).
2.1.7 Kegunaan 2.1.7.1Labu Kuning
2.1.7.2Peleng
Kegunaan secara tradisional, daun peleng dapat digunakan sebagai antipiretik, diuretik, obat cacing, laxantif, nyeri di persendian, radang paru-paru, demam, pilek, sakit tenggorokan, infeksi cacing, perut kembung dan mual (Subhash, 2010).
2.1.7.3Sabi
Sabi sering dikonsumsi sebagai sayuran. Daun nya juga dapat berkhasiat untuk terapi kanker, memiliki aktivitas antioksidan dan antimikroba (Tenore, 2012; Duke, 1983).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan lain-lain. Diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dan cara ekstraksi yang tepat (DepKes RI, 2000).
Menurut Departemen Kesehatan RI (2000), beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
A. Cara dingin 1. Maserasi
Remaserasi dilakukan dengan pengulangan penambahan pelarut setelah dilakukan penyarian maserat pertama dan seterusnya.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada suhu kamar. Proses perkolasi terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) yang terus-menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan. B. Cara panas
1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian simplisia dengan pengadukan secara terus-menerus pada temperatur yang lebih tinggi dari suhu kamar, yaitu secara umum dilakukan pada temperatur 40-50°C.
3. Sokletasi
4. Infundasi
Infundasi adalah proses penyarian simplisia dengan menggunakan pelarut air pada temperatur 90°C selama waktu 15 menit.
5. Dekoktasi
Dekoktasi adalah proses penyarian simplisia dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit.
2.3Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih elektron yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang tidak terkontrol menghasilkan ikatan silang dengan DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif, yakni kanker, aterosklerosis, jantung koroner, katarak dan penyakit degeneratif lainnya (Silalahi, 2006). Radikal bebas dapat masuk dan terbentuk dalam tubuh melalui pernafasan, kondisi lingkungan yang tidak sehat dan makanan berlemak (Kumalaningsih, 2006).
2.4 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas dan dapat memutus reaksi berantai dari radikal bebas (Kumalaningsih, 2006). Antioksidan atau reduktor berfungsi untuk mencegah terjadinya oksidasi atau menetralkan senyawa yang telah teroksidasi dengan cara menyumbangkan hidrogen dan atau elektron (Silalahi, 2006).
Menurut Kumalaningsih (2006), antioksidan dapat dikelompokkan menjadi 5 yakni:
a. Antioksidan primer
Antioksidan ini berfungsi untuk mencegah terbentuknya radikal bebas yang baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, yaitu sebelum sempat bereaksi. Contohnya adalah enzim superoksida dismutase (SOD) yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh karena radikal bebas.
b. Antioksidan sekunder
Antioksidan sekunder merupakan senyawa yang berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contohnya adalah vitamin E, vitamin C dan betakaroten yang dapat diperoleh dari buah-buahan.
c. Antioksidan tersier
reduktase yang dapat memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk perbaikan DNA pada penderita kanker.
d. Oxygen scavanger
Antioksidan yang termasuk oxygen scavanger mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya vitamin C.
e. Chelators atau sequesstrants
Mengikat logam yang mampu mengkatalisis reaksi oksidasi misalnya asam sitrat dan asam amino. Khasiat antioksidan untuk mencegah berbagai penyakit akibat pengaruh oksidatif akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan buah-buahan yang kaya akan antioksidan dari berbagai jenis daripada menggunakan antioksidan tunggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih efektif daripada suplemen antioksidan yang diisolasi (Silalahi, 2006).
Hasil penelitian menunjukkan bahwa buah-buahan, sayuran dan biji-bijian adalah sumber antioksidan yang baik dan bisa meredam reaksi berantai radikal bebas dalam tubuh, yang pada akhirnya dapat menekan proses penuaan dini (Kosasih, 2004).
2.4.1 Antioksidan alami
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik atau polifenolik yang dapat berupa golongan flavonoid, turunan asam sinamat, kumarin dan tokoferol. Golongan flavonoid yang memiliki aktivitas antioksidan meliputi flavon, flavonol, isoflavon, katekin, flavanon dan kalkon. Senyawa antioksidan alami polifenolik dapat bereaksi sebagai pereduksi, penangkap radikal bebas, pengkelat logam dan peredam terbentuknya singlet oksigen (Kumalaningsih, 2006).
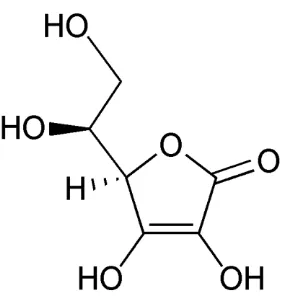
2.4.2 Vitamin C
Gambar 2.1 Rumus bangun vitamin C (Silalahi, 2006). 2.4.3 Betakaroten
Betakaroten merupakan salah satu provitamin A yang berperan sebagai antioksidan dan dipercaya dapat menurunkan resiko penyakit jantung dan kanker. Betakaroten terdapat pada aprikot, wortel dan mangga dan dengan mengkonsumsi 50 mg betakaroten tiap hari dalam menu makanan dapat mengurangi risiko terkena penyakit jantung (Kosasih, 2004).
Betakaroten bekerja sebagai antioksidan dengan cara memperlambat fase inisiasi. Pemberian vitamin A dalam dosis tinggi dapat bersifat toksis. Akan tetapi, betakaroten dalam jumlah banyak mampu memenuhi kebutuhan vitamin A dan selebihnya tetap sebagai betakaroten yang berfungsi sebagai antioksidan (Silalahi, 2006). Rumus bangun betakaroten dapat dilihat pada Gambar 2.2.
2.4.4 Vitamin E
Vitamin E terdiri dari struktur tokoferol, bersifat tidak larut dalam air tapi larut dalam lemak atau minyak.
Gambar 2.3 Rumus bangun vitamin E (Silalahi, 2006).
Struktur molekul vitamin E di atas menunjukkan bahwa vitamin E merupakan suatu antioksidan yang efektif, yang dengan mudah menyumbangkan atom hidrogen pada gugus hidroksil (OH) dari struktur cincin ke radikal bebas sehingga radikal bebas menjadi tidak reaktif. Dengan menyumbangkan hidrogen, vitamin E sendiri menjadi suatu radikal, tetapi lebih stabil karena elektron yang tidak berpasangan pada atom oksigen mengalami delokalisasi ke dalam struktur cincin aromatik (Silalahi, 2006).
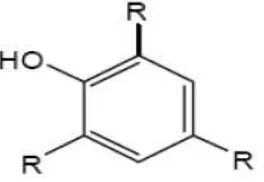
2.4.5 Polifenol
bertanggung jawab terhadap aktivitas antioksidan dalam buah dan sayuran (Hattenschwiler, 2000). Struktur dasar polifenol dapat dilihat pada Gambar 2.4.
Gambar 2.4 Struktur dasar polifenol (Hattenschwiler, 2000).
2.5Spektrofotometri UV-Visible
Prinsip kerja Spektrofotometer Visible adalah sinar/cahaya dilewatkan melewati sebuah wadah (kuvet) yang berisi larutan, dimana akan menghasilkan spektrum. Sebagian dari cahaya tersebut akan diserap dan sisanya akan dilewatkan. Nilai absorbansi dari cahaya yang dilewatkan akan sebanding dengan konsentrasi larutan di dalam kuvet. Alat ini menggunakan hukum Lambert Beer sebagai acuan (Ewing, 1975).
Ahli kimia telah lama menggunakan warna sebagai bantuan dalam mengenali zat-zat kimia. Spektrofotometri dapat dianggap sebagai perluasan suatu pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur absorpsi energi radiasi macam-macam zat kimia dan memungkinkan dilakukannya pengukuran kualitatif dari suatu zat dengan ketelitian yang lebih besar (Day, 1994).
nm sedangkan panjang gelombang untuk sinar tampak/visible antara 400-750 nm (Rohman, 2007).
2.6 Penentuan Aktivitas Antioksidan dengan Metode DPPH
Metode untuk menentukan aktivitas antioksidan ada beberapa cara, yaitu: (1). BCB Method (β-Carotene Bleaching Method) atau Metode Pemutihan β -karoten, (2). DPPH (1,1-difenil-2- picrylhydrazil) Radical Scavenging Method
(Metode Pemerangkapan Radikal Bebas DPPH), (3). Thiobarbituric Acid-Reactive Substance (TBARS) Assay, (4). ORAC Assay (Oxygen-Radical Absorbance Capacity), (5). CUPRAC Assay (Cupric Reducing Antioxidant Capacity), (6). FRAP Assay (Ferric Reducing Antioxidant Power), (7).
Determination of Conjugated Dienes, (8). Determination of Lipid Hydroperoxides (De la Rosa, 2010).
Pada tahun 1922, Goldschmidt dan Renn menemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen kolorimetri untuk proses redoks. DPPH berwarna sangat ungu seperti KMnO4 dan bentuk tereduksinya yaitu 1,1-difenil-2- picrylhydrazine (DPPH-H) yang berwarna oranye-kuning. DPPH bersifat tidak larut dalam air (Ionita, 2003).
kuning terang dan absorbansi pada panjang gelombang 517 nm akan hilang. Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat reduktor (Molyneux, 2004).
Metode DPPH merupakan suatu metode yang cepat, sederhana, dan murah yang dapat digunakan untuk mengukur kemampuan antioksidan yang terkandung dalam makanan. Metode DPPH dapat digunakan untuk sampel yang padat dan juga dalam bentuk larutan dan berlaku untuk keseluruhan kapasitas antioksidan sampel. Prinsipnya adalah elektron ganjil pada molekul DPPH memberikan serapan maksimum pada panjang gelombang tertentu yang berwarna ungu. Warna ini akan berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
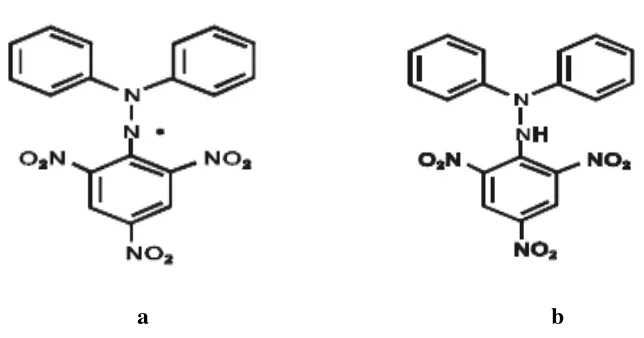
[image:40.595.117.439.551.720.2]Molyneux (2004), menyatakan bahwa suatu zat mempunyai sifat antioksidan bila nilai IC50 kurang dari 200 ppm. Bila nilai IC50 yang diperoleh berkisar antara 200-1000 ppm, maka zat tersebut kurang aktif namun masih berpotensi sebagai zat antioksidan. Rumus molekul DPPH dapat dilihat pada Gambar 2.5.
Keterangan:
a. bentuk radikal (DPPH) b. bentuk nonradikal (DPPH-H)
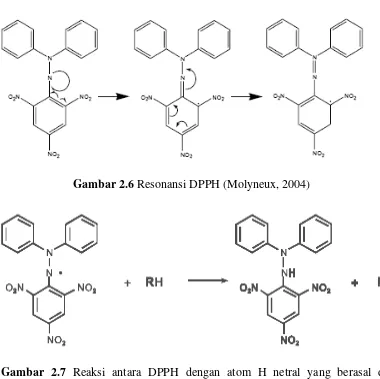
[image:41.595.113.493.238.617.2] [image:41.595.116.480.251.402.2]DPPH merupakan radikal bebas yang stabil karena resonansi yang dialaminya. Resonansi DPPH dan reaksi DPPH dengan atom H netral yang berasal dari senyawa-senyawa yang bersifat antioksidan dapat dilihat pada Gambar 2.6 dan Gambar 2.7.
Gambar 2.6 Resonansi DPPH (Molyneux, 2004)
Gambar 2.7 Reaksi antara DPPH dengan atom H netral yang berasal dari antioksidan (Molyneux, 2004).
antioksidan yang memberikan % penghambatan 50%. Zat yang mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah (Molyneux, 2004).
2.6.1 Pelarut
Metode ini akan memberikan hasil yang baik dengan menggunakan pelarut metanol atau etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.6.2 Pengukuran absorbansi – panjang gelombang
Panjang gelombang maksimum ( maks) yang digunakan dalam pengukuran sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm dan 520 nm. Pada prakteknya hasil pengukuran yang memberikan peak
maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan diatas (Molyneux, 2004).
2.6.3 Waktu pengukuran
BAB III
METODE PENELITIAN
Jenis penelitian yang dilakukan adalah penelitian eksperimental. Metodologi penelitian meliputi pengumpulan dan preparasi bahan, karakterisasi simplisia, pembuatan ekstrak etanol, skrining fitokimia dan uji aktivitas antioksidan dengan metode aktivitas antiradikal bebas DPPH dengan menggunakan alat spektrofotometer visibel.
3.1 Alat dan Bahan 3.1.1 Alat-alat
Alat-alat yang digunakan terdiri dari: Alat alat gelas laboratorium (Erlenmeyer, gelas beaker, gelas corong, gelas ukur, labu alas bulat, labu tentukur, pendingin Liebig, tabung reaksi), penguap vakum putar (Heidolph VV 2000), freeze dryer (Modulyo/Edwards), desikator, gelas penutup, mikroskop, krus porselin, krus tang, lemari pengering, neraca analitis (Vibra), object glass, penangas air (Yenaco), pisau, timbangan, spektofotometer UV/Vis (Shimadzu UV-1800) dan tanur (Gallenkamp)
3.1.2 Bahan-bahan
kalium iodida, besi (III) klorida, timbal (II) asetat, kloralhidrat, kloroform, isopropanol, natrium hidroksida dan amil alkohol.
3.2 Pengumpulan dan Pengolahan Bahan Tumbuhan 3.2.1 Pengumpulan sampel
Bahan tumbuhan yang digunakan dalam penelitian ini adalah pucuk daun labu kuning, herba peleng dan herba sabi, yang diambil dari Pasar sayur Berastagi, Tanah Karo. Pengambilan sampel dilakukan secara purposif tanpa membandingkan dengan tumbuhan serupa dari daerah lain.
3.2.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi-LIPI Bogor. Hasil determinasi dapat dilihat pada Lampiran 1, halaman 51-52.
3.2.3 Pengolahan tumbuhan
3.3 Pembuatan Pereaksi 3.3.1 Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga 100 ml (Ditjen POM, 1979).
3.3.2 Pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g natrium hidroksida dilarutkan dalam air suling bebas karbon dioksida hingga 100 ml (Ditjen POM, 1979).
3.3.3 Pereaksi Bouchardat
Sebanyak 2 g iodium dan 4 g kalium iodida dilarutkan dalam air suling hingga 100 ml (Ditjen POM, 1995).
3.3.4 Pereaksi Mayer
Sebanyak 1,569 g raksa (II) klorida dilarutkan dalam air suling hingga 60 ml. Pada wadah lain dilarutkan 5 g kalium iodida dalam 10 ml air suling. Kemudian keduanya dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml ( Ditjen POM,1995).
3.3.5 Pereaksi Dragendorff
Sebanyak 0,8 g bismut (III) nitrat dilarutkan dalam asam nitrat pekat 20 ml kemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam 50 ml air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih diambil dan diencerkan dengan air suling secukupnya hingga 100 ml (Ditjen POM, 1995).
3.3.6 Pereaksi besi (III) klorida 1%
3.3.7 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrida dengan 5 ml asam sulfat pekat tambahkan etanol hingga 50 ml (Merck, 1978).
3.3.8 Pereaksi Molish
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N secukupnya hingga diperoleh 100 ml larutan (Ditjen POM, 1979).
3.3.9 Pereaksi timbal (II) asetat 0,4 N
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam air suling bebas karbon dioksida secukupnya hingga 100 ml (Ditjen POM, 1995).
3.3.10 Larutan pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga diperoleh 100 ml (Ditjen POM, 1995).
3.3.11 Larutan Pereaksi DPPH 0,5 mM (Konsentrasi 200ppm)
Sebanyak 19,7 mg DPPH ditimbang, kemudian dilarutkan dalam metanol hingga volume 100 ml (Molyneux, 2004).
3.4 Karakterisasi Simplisia
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar dari simplisia pucuk daun labu kuning (Cucurbita moschata Duch.), herba peleng (Spinacia oleracea L.) dan herba sabi (Brassica rapa L.).
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia pucuk daun labu kuning, herba peleng dan herba sabi. Masing-masing serbuk simplisia diletakkan pada kaca objek yang berbeda yang telah ditetesi larutan kloralhidrat kemudian ditutup dengan kaca penutup, dipanaskan dan diamati di bawah mikroskop.
3.4.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Cara kerja :
terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1992).
Hal ini juga dilakukan terhadap serbuk simplisia herba peleng dan herba sabi.
3.4.4 Penetapan kadar sari larut air
Sebanyak 5 g serbuk simplisia pucuk daun labu kuning yang telah dikeringkan di udara dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air sampai 1 liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara, dan sisa dipanaskan pada suhu 105º C sampai bobot tetap. Kadar sari larut dalam air dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1989).
Hal ini juga dilakukan terhadap serbuk simplisia herba peleng dan herba sabi.
3.4.5 Penetapan kadar sari larut etanol
Hal ini juga dilakukan terhadap serbuk simplisia herba peleng dan herba sabi.
3.4.6 Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia pucuk daun labu kuning yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijarkan pada suhu 600ºC sampai arang habis, kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1989).
Hal ini juga dilakukan terhadap serbuk simplisia herba peleng dan herba sabi.
3.4.7 Penetapan kadar abu tidak larut asam
Abu yang telah diperoleh dalam penetapan kadar abu total dididihkan dalam 25 ml asam klorida 2 N selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu kemudian dicuci dengan air panas. Residu dan kertas saring dipijarkan pada suhu 600ºC sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu tidak larut dalam asam dihitung terhadap bahan yang dikeringkan (Ditjen POM, 1989).
Hal ini juga dilakukan terhadap serbuk simplisia herba peleng dan herba sabi.
3.5 Skrining Fitokimia
3.5.1 Pemeriksaan Alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g, ditambahkan 10 ml asam klorida 0,2 N, dipanaskan di atas penangas air selama 10 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloid. Ke dalam 4 tabung reaksi dimasukkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi : 1. ditambahkan 2 tetes pereaksi Mayer 2. ditambahkan 2 tetes larutan Iodium 3. ditambahkan 2 tetes pereaksi Dragendorff 4. ditambahkan 2 tetes pereaksi Bouchardat
Alkaloid positif jika terjadi endapan atau kekeruhan pada dua dari empat pereaksi di atas (Ditjen POM, 1989).
3.5.2 Pemeriksaan Flavonoida
Sebanyak 10 g serbuk ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.5.3 Pemeriksaan Glikosida
dilakukan berulang sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 50٥C. Sisanya dilarutkan dalam 2 ml metanol. Larutan metanol digunakan untuk percobaan berikut: 0,1 ml larutan percobaan dimasukan dalam tabung reaksi dan diuapkan diatas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan ikatan gula (Ditjen POM, 1989). 3.5.4 Pemeriksaan Antrakinon
Serbuk simplisia ditimbang sebanyak 0,2 g, ditambahkan 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzen, dikocok dan didiamkan. Lapisan benzen dipisahkan dan disaring. Kocok lapisan benzen dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzen tidak berwarna menunjukkan adanya antrakinon (Ditjen POM, 1989). 3.5.5 Pemeriksaan Saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukan ke dalam tabung reaksi, lalu ditambahkan 10 ml air panas, dinginkan kemudian dikocok kuat-kuat selama 10 detik. Terbentuk busa setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Ditjen POM, 1989).
3.5.6 Pemeriksaan Tanin
3.5.7 Pemeriksaan Steroida/Triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksan selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan beberapa tetes pereaksi Liebermann-Burchard. Timbulnya warna biru atau biru hijau menunjukan adanya steroida, sedangkan warna merah, merah muda atau ungu menunjukkan adanya triterpenoida (Harborne, 1987).
3.6 Pembuatan Ekstrak Etanol
3.7 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel 3.7.1 Prinsip Metode Penangkapan Radikal Bebas DPPH
Kemampuan sampel uji dalam meredam DPPH ( 1,1-Diphenyl-2-Picryl-hidrazyl) sebagai radikal bebas dalam larutan metanol (sehingga terjadi peredaman warna ungu DPPH) dengan nilai IC50 (konsentrasi sampel uji yang mampu meredam radikal bebas sebesar 50%) digunakan sebagai parameter untuk menentukan aktivitas antioksidan sampel uji tersebut.
3.7.2 Pembuatan Larutan Blanko
Larutan DPPH 0,5 mM (konsentrasi 200 ppm) dipipet sebanyak 5 ml, kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan volumenya dengan metanol sampai garis tanda (konsentrasi 40 ppm).
3.7.3 Penentuan Panjang Gelombang Serapan Maksimum
Larutan DPPH konsentrasi 40 ppm dihomogenkan dan diukur serapannya pada panjang gelombang 400-800 nm. Gambar spektrofotometer dapat dilihat pada Lampiran 8, halaman 62.
3.7.4 Pembuatan Larutan Induk
Sebanyak 25 mg ekstrak herba labu kuning, herba peleng dan herba sabi ditimbang kemudian dilarutkan dalam labu tentukur 25 ml dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
3.7.5 Pembuatan Larutan Uji
labu tentukur ditambahkan 5 ml larutan DPPH 0,5 mM (konsentrasi 40 ppm) lalu volume dicukupkan dengan metanol sampai garis tanda, didiamkan di tempat gelap, lalu diukur serapannya pada menit ke-60.
3.7.6 Penentuan Persen Peredaman
Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH (peredaman warna ungu DPPH) akibat adanya penambahan larutan uji. Nilai serapan larutan DPPH sebelum dan sesudah penambahan larutan uji tersebut dihitung sebagai persen peredaman.
Keterangan : A Kontrol = Absorbansi tidak mengandung sampel A Sampel = Absorbansi sampel
3.7.7 Penentuan Nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji ( g/ml) yang memberikan peredaman DPPH sebesar 50% (mampu meredam
proses oksidasi DPPH sebesar 50%). Nilai 0% berarti tidak mempunyai aktivitas antioksidan, sedangkan nilai 100% berarti peredaman total dan pengujian perlu dilanjutkan dengan pengenceran larutan uji untuk melihat batas konsentrasi aktivitasnya. Hasil perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak ( g/ml) sebagai absis (sumbu X) dan nilai % peredaman (antioksidan) sebagai ordinatnya (sumbu Y). Hasil pengujian dapat dilihat pada Lampiran 16-18, halaman 77-83 dan perhitungan IC50 dapat dilihat pada Lampiran 19-21, halaman 84-86.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi-LIPI Bogor menunjukkan bahwa sampel pucuk daun labu kuning termasuk suku Cucurbitacea, spesies Cucurbita moschata
Duch. Sampel herba peleng termasuk suku Chenopodiacea, spesies Spinacia oleracea Linn. Herba sabi termasuk suku Brassicacea, spesies Brassica rapa L.
4.2 Hasil Karakterisasi Simplisia a. Pemeriksaan Makroskopik
Hasil pemeriksaan makroskopik simplisia pucuk daun labu kuning adalah serbuk berwarna coklat, tidak memiliki bau dan rasa yang khas serta panjang sekitar 3-5 cm. Hasil pemeriksaan simplisia herba peleng adalah simplisia berwarna hijau kekuningan, panjang sekitar 3-7 cm, batang berwarna hijau dengan tekstur mudah rapuh. Hasil pemeriksaan herba sabi adalah simplisia berwarna hijau muda, tepi daun bergerigi, panjang sekitar 4-8 cm, tidak memiliki bau yang khas.
b. Pemeriksaan Mikroskopik
rambut penutup, berkas pengangkut dan hablur kristal kalsium oksalat. Hasil
pemeriksaan herba sabi terlihat jaringan gabus, stomata dan berkas pengangkut.
c. Hasil Pemeriksaan Karakterisasi Serbuk Simplisia
Hasil pemeriksaan karakterisasi serbuk simplisia pucuk daun labu kuning, herba peleng dan herba sabi diperoleh kadar air sebesar 7,29%, 8,62% dan 7,98%..Kadar sari yang larut dalam air sebesar 13,55%, 9,75%, 22,19%. Kadar sari yang larut dalam etanol sebesar 8,99%, 16,05% dan 11,35%. Kadar abu total sebesar 6,67%, 6,62% dan 4,43%. Kadar abu tidak larut dalam asam sebesar 0,48%, 0,30% dan 0,26%. Hasil penetapan kadar air simplisia herba memenuhi persyaratan Materia Medika Indonesia yaitu tidak melebihi 10%. Kadar air yang melebihi persyaratan memungkinkan terjadinya pertumbuhan jamur. Penetapan kadar sari yang larut dalam air untuk mengetahui kadar sari yang larut dalam air. Monografi dari serbuk simplisia pucuk daun labu kuning, herba peleng dan herba sabi tidak ditemukan di buku Materia Medika Indonesia. Penetapan kadar sari yang larut dalam etanol untuk mengetahui kadar sari yang larut dalam etanol. Penetapan kadar abu total untuk mengetahui kadar zat anorganik yang ada pada simplisia, sedangkan penetapan kadar abu yang tidak larut dalam asam untuk mengetahui kadar zat anorganik yang tidak larut dalam asam.
4.3 Hasil Skrining Fitokimia
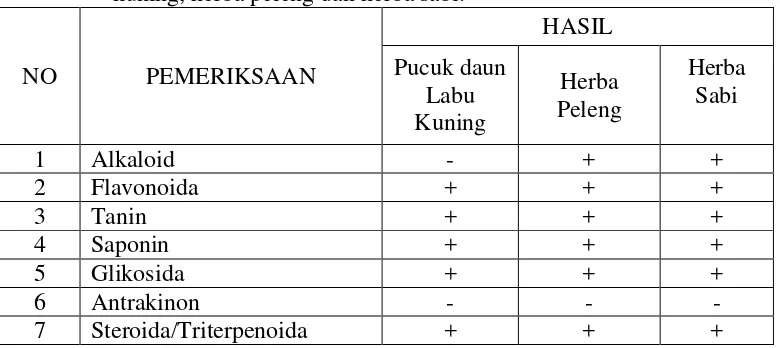
Tabel 4.1. Hasil skrining fitokimia simplisia dan ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi.
NO PEMERIKSAAN
HASIL Pucuk daun
Labu Kuning
Herba Peleng
Herba Sabi
1 Alkaloid - + +
2 Flavonoida + + +
3 Tanin + + +
4 Saponin + + +
5 Glikosida + + +
6 Antrakinon - - -
7 Steroida/Triterpenoida + + +
Keterangan: (+) positif : mengandung golongan senyawa (-) negatif: tidak mengandung golongan senyawa
Hasil yang diperoleh pada Tabel 4.1 di atas menunjukkan bahwa pucuk daun labu kuning, herba peleng, herba sabi memiliki potensi sebagai antioksidan, yaitu dengan adanya senyawa-senyawa yang mempunyai potensi sebagai antioksidan umumnya merupakan senyawa flavonoida (Kumalaningsih, 2006). Senyawa tersebut bertindak sebagai penangkap radikal bebas karena gugus hidroksil yang dikandungnya mendonorkan hidrogen kepada radikal bebas (Silalahi, 2006).
4.4 Hasil Analisis Aktivitas Antioksidan Sampel Uji
4.4.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum
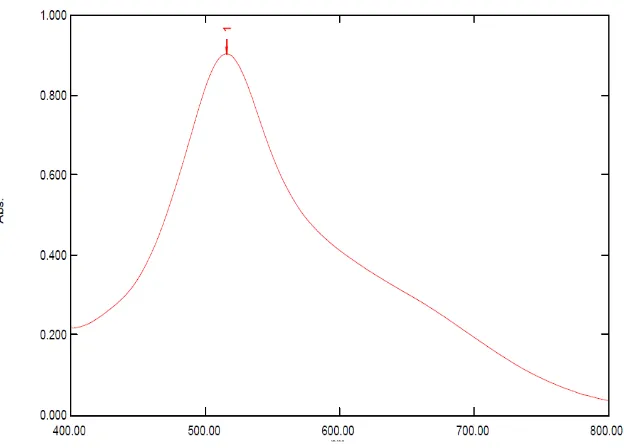
Hasil pengukuran serapan maksimum larutan DPPH 40 ppm dalam metanol dengan menggunakan spektrofotometer UV-Vis. Data hasil pengukuran dapat dilihat pada Gambar 3.1 berikut ini:
Gambar 3.1 Kurva serapan maksimum larutan DPPH 40 ppm dalam metanol secara spektrofotometri visibel.
Hasil pengukuran menunjukkan bahwa larutan DPPH dalam metanol menghasilkan serapan maksimum pada panjang gelombang 516 nm (Molyneux, 2003).
4.5 Hasil Analisis Aktivitas Antioksidan
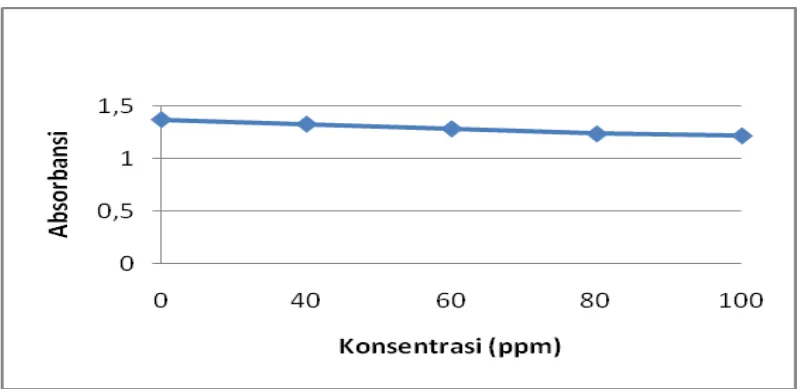
[image:59.595.151.463.189.413.2]Untuk melihat hubungan absorbansi DPPH terhadap pertambahan konsentrasi larutan uji dalam menganalisis aktivitas antioksidan dapat dilihat pada Gambar 4.2, 4.3 dan 4.4.
Gambar 4.2 Hasil analisis aktivitas antioksidan ekstrak etanol pucuk daun labu kuning (Cucurbita moschata Duch.)
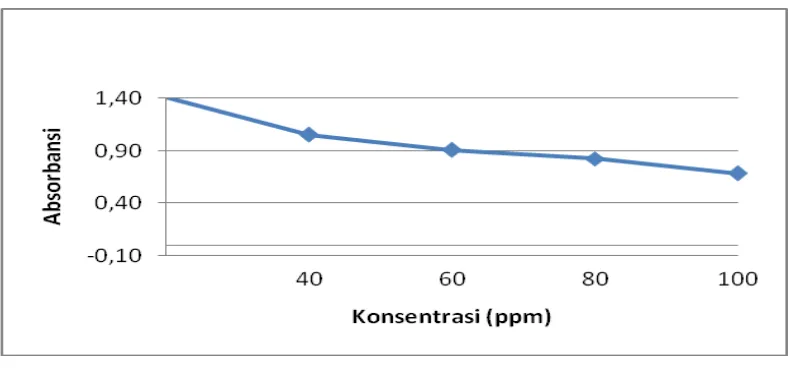
[image:60.595.112.508.141.341.2] [image:60.595.114.519.404.600.2]Gambar 4.4 Hasil analisis aktivitas antioksidan ekstrak etanol herba sabi (Brassica rapa L.).
Hasil analisis aktivitas antioksidan ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi dapat dilihat adanya penurunan nilai absorbansi DPPH yang diberi larutan uji dibandingkan terhadap kontrol pada setiap kenaikan konsentrasi. Penurunan absorbansi yang semakin besar menunjukkan aktivitas antioksidan yang semakin besar pula. Ekstrak etanol herba sabi memiliki penurunan yang paling besar, kemudian ekstrak pucuk daun labu kuning dan yang paling kecil adalah ekstrak herba peleng.
Ekstrak etanol herba sabi mengandung banyak senyawa fenol dan merupakan sumber polifenol yang cukup besar terutama flavonoid (Cartea, et al.,
2011).
[image:61.595.114.510.81.267.2]tua menjadi kuning terang dan absorbansi pada panjang gelombang maksimumnya akan hilang (Molyneux, 2004).
[image:62.595.112.506.402.559.2]4.6 Hasil Analisis Peredaman Radikal Bebas DPPH Oleh Sampel Uji Kemampuan antioksidan diukur pada menit ke-60 sebagai penurunan serapan larutan DPPH (peredaman radikal bebas DPPH) akibat adanya penambahan larutan uji. Nilai serapan larutan DPPH sebelum dan sesudah penambahan larutan uji tersebut dihitung sebagai persen peredaman. Hasil analisis yang telah dilakukan, diperoleh nilai persen peredaman pada setiap kenaikan konsentrasi sampel uji seperti yang terlihat pada Tabel 4.2 di bawah ini:
Tabel 4.2. Hasil analisis peredaman radikal bebas oleh ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi.
Menit ke-
Konsentrasi Sampel
%Peredaman Pucuk Daun
Labu kuning Herba Peleng Herba Sabi
60
DPPH 0 0 0
40 ppm 20,37 3,14 25,07
60 ppm 30,97 6,42 35,33
80 ppm 37,60 9,92 41,17
100 ppm 49,88 11,31 51,43
4.7 Analisis Nilai IC50 (Inhibitory Concentration) Sampel Uji
[image:63.595.129.491.320.398.2]Nilai IC50 diperoleh berdasarkan persamaan regresi linier yang didapatkan dengan cara memplot konsentrasi larutan uji dan persen peredaman DPPH sebagai parameter aktivitas antioksidan, dimana konsentrasi larutan uji (ppm) sebagai absis dan nilai persen peredaman sebagai ordinat. Hasil persamaan regresi linier yang diperoleh untuk ekstrak etanol dari pucuk daun labu kuning, herba peleng dan herba sabi dapat dilihat pada Tabel 4.3 berikut ini:
Tabel 4.3 Hasil persamaan regresi linier yang diperoleh dari ekstrak etanol dari pucuk daun labu kuning, herba peleng dan herba sabi
Larutan Uji Persamaan regresi
Ekstrak pucuk daun labu kuning Y = 0,4890 X + 0,3783 Ekstrak herba peleng Y = 0,1201 X- 0,5676
Ekstrak herba sabi Y = 0,5052 X + 2,3068
Hasil analisis nilai IC50 yang diperoleh berdasarkan perhitungan persamaan regresi dapat dilihat pada Tabel 4.4 berikut ini:
Tabel 4.4 Nilai IC50 ekstrak etanol dari pucuk daun labu kuning, herba peleng dan herba sabi.
Sampel IC50 (ppm)
Ekstrakpucuk daun labu kuning 101,47 ppm
Ekstrak herba peleng 421,04 ppm
Ekstrak herba sabi 94,40 ppm
[image:63.595.123.497.519.608.2]antioksidan kuat. Dimana nilai IC50 dari vitamin C adalah 26,16 ppm (Tessa, 2011). Secara keseluruhan aktivitas antioksidan ekstrak etanol pucuk daun labu kuning, herba peleng dan herba sabi masih di bawah aktivitas antioksidan vitamin C.
BAB V
KESIMPULAN DAN SARAN 5.1Kesimpulan
1. Hasil pemeriksaan karakteristik simplisia pucuk daun labu kuning diperoleh kadar air 7,29%, kadar sari larut dalam air 13,55%, kadar sari larut dalam etanol 8,99%, kadar abu total 6,67% dan kadar abu yang tidak larut dalam asam 0,48%. Hasil pemeriksaan karakteristik simplisia herba peleng diperoleh kadar air 8,62%, kadar sari yang larut dalam air 9,75%, kadar sari yang larut dalam etanol 16,05%, kadar abu total 6,62% dan kadar abu yang tidak larut dalam asam 0,30%. Hasil pemeriksaan karakteristik simplisia herba sabi diperoleh kadar air 7,98%, kadar sari yang larut dalam air 22,19%, kadar sari yang larut dalam etanol 11,35%, kadar abu total 4,43% dan kadar abu yang tidak larut dalam asam 0,26%.
2. Hasil uji skrining fitokimia pada serbuk simplisia pucuk daun labu kuning, herba peleng dan herba sabi diperoleh adanya kesamaan kandungan golongan senyawa flavonoida, tanin, saponin, glikosida dan steroid/triterpenoid; namun pada labu kuning, tidak adanya golongan senyawa alkaloid.
DAFTAR PUSTAKA
Anonim. (2010). Cucurbita moschata Duschene. Diakses pada tahun 2010. http://www.globinmed.com/index.php?option=com_content&view=article &id=79227:cucurbita-moschata-duchesne&catid=705:c
Bondet, V., Williams, W.B., dan Berset, C. (1997). Kinetics and Mechanisms of Antioxidant Activity Using the DPPH Free Radical Method. Lebensm.-Wiss. U.-Technol. 30(1): 609-615.
Cartea, M.E., Fransisco, M., Soengas, P., dan Velasco, P. (2010). Phenolic Compounds in Brassica Vegetables. Molecules., 2011, 16(1):251-280. Day, R.A., dan Underwood, A.L. (1986). Analisis Kimia Kualitatif. Edisi
Keenam. Penerjemah Iis Sopyan. Jakarta: Penerbit Erlangga. Hal. 382. De la Rosa, L., Emilio A., dan Gustavo, A. (2010). Fruit and Vegetable
Phytochemicals: Chemistry, Nutritional Value and Stability. New York: Wiley-Blackwell Publishing. Hal. 271-292.
Depkes. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Depkes RI. Hal. 1, 9-12, 17.
Ditjen POM. (1989). Materia Medika Indonesia. Jilid V. Jakarta: Depkes RI. Hal. 536-540.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Depkes RI. Hal. 33, 649, 696.
Ditjen POM. (1995). Farmakope Indonesia. Edisi empat. Jakarta: Depkes RI. Hal. 970, 1135, 1139, 1192.
Duke, J. (1983). Handbook of Energy Crops. Diakses pada Tanggal 4 Juli 2012. http://www.hort.purdue.edu/newcrop/duke_energy/brassica_rapa.html Ewing, G.W. (1975). Instrumental Methods of Chemical Analysis. Edisi empat.
Tokyo: McGraw-Hill Kogakusha. Hal. 34-40.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plants, Journal of Pharmaceutical Sciences. 55(3): 263.
Harbone, J.B. (1987). Metode Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan. Penerjemah Kosasih Padmawinata. Edisi II. Bandung: ITB Press. Hal. 147-148.
Heyne, K. (1987). Tanaman Berguna Indonesia. Jilid II. Cetakan pertama. Badan Litbang Kehutanan, Departemen Kehutanan Indonesia. Jakarta: Yayasan Sarana Wana Jaya. Hal. 733.
Ionita, P. (2005). Is DPPH Stable Free Radical a Good Scavenger for Oxygen Active Species?. Chem. Pap. 59(1): 11-16.
Kosasih, E.N., Tony, S., dan Hendro, H. (2004). Peran Antioksidan pada Lanjut Usia. Jakarta: Pusat Kajian Nasional Masalah Lanjut Usia. Hal. 56-57. Kumalaningsih, S. (2006). Antioksidan Alami. Cetakan Pertama. Surabaya:
Trubus Agrisarana. Hal. 4-5, 16.
Merck, E. (1978), Dyeing Reagents for Thin Layer and Paper Chromatography. Berlin: Federal Republic of Germany. Hal. 1.
Mardawati, E., Filianty, F., dan Marta, H. (2008). Kajian Aktivitas Antioksidan Ekstrak Kulit Manggis (Garcinia mangostana L.) dalam rangka Pemanfaatan Limbah Kulit Manggis di Kecamatan Pusphahiang di Kabupaten Tasikmalaya. Hal. 4.
Molyneux, P. (2004). The Use of The Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol., 2004, 26(2): 211-219.
Prakash, A. (2001). Antioxidant Activity. Medallion Laboratories-Analytical Progress. 19(2): 1-4.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 220-264.
Sembiring, S.A .(2005).