Lampiran 2. Gambar tanaman dan buah terong lalap ungu (Solanum melongenaL).
Tanaman terong lalap ungu
Buah terong lalap ungu
Lampiran 3.Gambar simplisia dan serbuk simplisia buah terong lalap ungu. (Solanum melongena L.)
Simplisia buah terong lalap ungu
Lampiran 4.Gambarmikroskopikdariserbuk simplisia buah terong lalap ungu (Solanum melongena L.)
1
2
3
Keterangan : perbesaran 10 X 40 1. Parenkim
Lampiran 5.Bagan pembuatan serbuk simplisia buah terong lalap ungu (Solanum melongena L.)
Dipisahkan dari tangkainya (5 kg) Dicuci
Ditiriskan
Dirajang ( 4,7 kg) Dikeringkan
Pemeriksaan makroskopik Dihaluskan
Simplisia (430 g)
Serbuk simplisia
Skrining fitokimia
Karakterisasi Pembuatan
ekstrak -Steroida/ triterpenoid -Alkaloid -Glikosida -Flavonoida -Saponin -Tanin -Steroida/
-Pemeriksaan mikroskopik -Penetapan kadar air -Penetapan kadar sari yang
larut dalam etanol
-Penetapan kadar sari yang larut dalam air
-Penetapan kadar abu total -Penetapan kadar abu yang
tidak larut dalamasam
Lampiran 6. Bagan pembuatan ekstrak etanol buah terong lalap ungu (Solanum melongena L.)
Dibasahi dengan etanol 96% dan didiamkan selama 3 jam
Dimasukkankedalamalatperkolator
Dituangkancairanpenyarietanolsecukupnyasa mpaisemuasimplisiaterendam dan terdapat selapis cairan penyri diatasnya.
Mulut perkolator ditutup denganalumunium foil
Perkolator didiamkanselama 24 jam Kran perkolator dibuka dandibiarkan
perkolat mengalir 1ml/menit
Dipekatkandenganrotary evaporatorpadasuhu 50°C
100 g serbuk simplisia
Perkolat Ampas
Lampiran 7.Perhitungan pemeriksaan karakteristik serbuk simplisia buah terong lalap ungu (Solanum melongena L.)
1. Penetapan kadar air
No. Berat sampel (g) Volume awal (ml) Volume akhir (ml)
1 5,003 1,8 2,1
2 5,006 2,1 2,4
3 5,022 2,4 2,7
1. Kadar air = 2,1-1,8
5,003 � %
= 5,99%
2. Kadar air = 2,4-2,1
5,006 � %
= 5,99%
3. Kadar air = 2,7-2,4
5,022 � %
= 5,97%
% rata-rata kadar air = 5,99+5,99+5,97 %
3 = 5,98%
2. Penetapankadar sari yang larutdalam air
No. Berat sampel (g) Berat sari (g)
1 5,012 0.2452
2 5,032 0,2325
3 5,019 0,2329
1. Kadar sari yang larut dalam air = ,
,
x
x
100% = 24,46%2. Kadar sari yang larut dalam air = ,
,
x
x
100% = 23,10% Kadar air= volume akhir-volume awalberat sampel
�
%Lampiran 7 (lanjutan)
3. Kadar sari yang larut dalam air = ,
,
x
x
100% = 26,19%% rata-rata kadar sari yang larut dalam air = , + , + , %= 24,58%
3. Penetapankadar sari yang larutdalametanol
No. Berat sampel (g) Berat sari (g)
1 5,036 0,2043
2 5,025 0,1971
3 5,032 0,1922
1. Kadar sari yang larut dalam etanol = ,
,
x
x
100% = 20,28%2. Kadar sari yang larut dalam etanol = ,
,
x
x
100% = 19,61%3. Kadar sari yang larut dalam etanol = ,
,
x
x
100% = 19,09%% rata-rata kadar sari yang larut dalam etanol = , + , + , %= 19,66%
4. Penetapankadarabu total
No. Berat sampel (g) Berat abu (g)
1 2,009 0,0903
2 2,005 0,0721
3 2,003 0,0806
Kadar sari =Berat Sampel x Berat sari × %
Kadar abu yang tidaklarutdalamasam
=
Berat AbuBerat Sampel
x 100%
Lampiran 7(lanjutan)1. Kadar abu total = ,
,
�
100% = 4,49%2. Kadar abu total = ,
,
�
100% = 3,59%3. Kadar abu total = ,
,
�
100% = 4,02%% rata-rata kadar abu total = , + , + , %
=
4,03%4. Penetapankadarabu yang tidaklarutdalamasam
No. Berat sampel (g) Berat abu (g)
1 2,002 0,0101
2 2,005 0,0072
3 2,008 0,0090
1. Kadarabu yang tidaklarutdalamasam = ,
,
�
100% = 0,50%2. Kadarabu yang tidaklarutdalamasam = ,
,
�
100% = 0,35%3. Kadarabu yang tidaklarutdalamasam = ,
,
�
100% = 0,48%Lampiran 8. Data absorbansi operating time larutan DPPH dalam metanol
No. ABS K*ABS
1 1,0076 1,0076
2 1,0168 1,0168
3 1,0314 1,0314
4 1,0411 1,0411
5 1,0560 1,0560
6 1,0664 1,0664
7 1,0739 1,0739
8 1,0898 1,0898
9 1,1018 1,1018
10 1,1359 1,1359
11 1,1366 1,1366
12 1,1366 1,1366
13 1,1366 1,1366
14 1,1366 1,1366
15 1,1366 1,1366
16 1,1366 1,1366
17 1,1366 1,1366
18 1,1366 1,1366
19 1,1366 1,1366
Lampiran 9.Perhitungan persen pemerangkapan DPPH Data absorbansi menit ke-60 pengukuran pertama
Konsentrasi Larutan Uji Absorbansi % Peredaman
DPPH 1,0620 -
15 ppm 0,9017 15,09
20 ppm 0,8629 18,74
25 ppm 0,7827 26,29
30 ppm 0,6791 36,05
% peredaman = � − � � �
�
x 100%
Keterangan: Akontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel
Perhitungan % peredaman ekstrak etanol buah terong lalap ungu - Konsentrasi 15 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 15,09% - Konsentrasi 20 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 18,74% - Konsentrasi 25 ppm
% peredaman = � − � � �
Lampiran 9(lanjutan)
=
, − ,, x 100%
= 26,29% - Konsentrasi 30 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 36,05%
Data absorbansi menit ke-60 pengukuran kedua
Konsentrasi Larutan Uji Absorbansi % Peredaman
DPPH 1,0964 -
15 ppm 0,9069 17,28
20 ppm 0,8755 20,14
25 ppm 0,7585 30,83
30 ppm 0,6982 36,31
% peredaman = � − � � �
�
x 100%
Keterangan: Akontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel
Perhitungan % peredaman ekstrak etanol buah terong lalap ungu - Konsentrasi 15 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
Lampiran 9 (lanjutan) - Konsentrasi 20 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 20,14% - Konsentrasi 25 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 30,83% - Konsentrasi 30 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
Data absorbansi menit ke-60 pengukuran ketiga
Konsentrasi Larutan Uji Absorbansi % Peredaman
DPPH 1,0173 -
15 ppm 0,8109 20,28
20 ppm 0,7744 23,87
25 ppm 0,6265 38,41
30 ppm 0,5959 41,42
% peredaman = � − � � �
�
x 100%
Keterangan: Akontrol = Absorbansi tidak mengandung sampel
Lampiran 9(lanjutan)
Perhitungan % peredaman ekstrak etanol buah terong lalap ungu - Konsentrasi 15 ppm
% peredaman = � − � � �
� x 100%
=
, − ,, x 100%
= 20,28% - Konsentrasi 20 ppm
% peredaman = � − � � �
� x 100%
= , − ,
, x 100%
= 23,87% - Konsentrasi 25 ppm
% peredaman = � − � � �
� x 100%
= , − ,
, x 100%
= 38,41% - Konsentrasi 30 ppm
% peredaman = � − � � �
� x 100%
= , − ,
, x 100%
Lampiran 9(lanjutan)
Data nilai rata-rata % peredaman ekstrak etanol Konsentrasi
Larutan Uji
% Peredaman 1
% Peredaman 2
% Peredaman 3
% Peredaman Rata-Rata
DPPH - - - -
15 ppm 15,09 17,28 20,28 17,55
20 ppm 18,74 20,14 23,87 20,91
25 ppm 26,29 30,83 38,41 31,84
Lampiran 10. Perhitungan nilai IC50
Ekstrak etanol buah terong lalap ungu
X Y XY X2
0 0 0 0
15 17,55 263,25 225
20 20,91 418,2 400
25 31,84 796 625
30 37,92 1137,6 900
ΣX= ΣY= , ΣXY= , ΣX2
= 2150
X=18 Y=21,64
X = Konsentrasi (ppm) Y = % Peredaman
a = ∑XY - ∑X ∑Y / n∑X - ∑X / n
a = , - - / , /
a = ,
a = 1,25
b = - a
b = (21,64) – (1,25) (18) b = -0,86
Jadi, persamaan garis regresi Y = 1,25X – 0,86 Nilai IC50 : Y = 1,25X – 0,86
DAFTAR PUSTAKA
Anonim. (2012). Terung (Solanum melongena L.). Tanggal akses : 10 Maret 2015. www.plantamor.com/index.php?plant=1167
Astawan, M., dan Kasih, A.L. (2008). Khasiat Warna-Warni Makanan. Jakarta: Penerbit Gramedia Pustaka Utama. Halaman 188.
Brand, W.W., Cuvelier, M.E., dan Berset, C. (1995). Use of a Free Radical Method to Evaluate Antioxidant Activity. Lebensmittel-wissenschaft und Technologie. 28(1): 25-30
Choundhary, B., dan Gaur, K. (2009). The Development and Regulation of Bt Brinjal in India (Eggplant/Aubergine). International Service For The Acquisition Of Agri-Biotech Applications.39: 1 - 119.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik secara Spektrofotometri. Padang: Andalas University Press. Halaman 1.
Depkes RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 33, 47.
Depkes RI. (1986). Sediaan Galenik. Jakarta: Departemen Kesehatan RI. Halaman 8 - 11.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI. Halaman 297 - 326. 333 - 340.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 1 - 11.
Ewing, G.W. (1975). Instrumental Methods of Chemical Analysis. Edisi Keempat. Tokyo: McGraw-Hill Kogakusha. Halaman 34 - 40.
Farnsworth, N. R. (1966). Biological and Phytochemical Screening of Plants. Journal of Pharmaceutical Sciences. 55(3): 263 - 264.
Fessenden, R.J., dan J.S. Fessenden. (1986). Kimia Organik. Diterjemahkan oleh A.H. Pudjaaymaka. Jakarta: Penerbit Erlangga. Halaman 223 - 226.
Fidrianny, I., Darmawati, A., dan Sukrasno. (2014). Antioxidant Capacities from Different Polarities Extract of Cucurbitaceae Leaves Using Frap, DPPH Assay and Correlation with Phenolic, Flavonoid, Carotenoid Content.
Hamid, A.A., Aiyelaagbe, O.O., Usman, L.A., Ameen, O.M., dan Lawal, A. (2010). Antioxidant: its Medicinal and Pharmacological Application. African Journal of Pure and Applied Chemistry. 4(8): 142-151.
Harborne, J.B. (1987). Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Terbitan Kedua. Bandung: Penerbit ITB. Halaman 147, 259.
Haryoto. ( 2009). Bertanam Terung dalam Pot. Yogyakarta: Penerbit Kanisius. Halaman 9 - 11.
Hastuti, L.D.S. (2007). Terung-Tinjauan Langsung Kebeberapa Pasar Di Kota Bogor. Tugas Akhir. Medan: Program Studi Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
Hattenschwiller, S., dan Vitousek, P.M. (2000). The Role of Polyphenols in Terrestrial Ecosystem Nutrient Cycling. TREE. 15(6): 238-243.
Heyne, K. (1987). Tumbuhan Berguna Indonesia III. Jakarta: Yayasan Sarana Wana Jaya. Halaman 1713.
Hutapea, J.R. (2001). Inventaris Tanaman Obat Indonesia (I). Jilid II. Jakarta: Bakti Husada. Halaman 315 - 316.
Ionita, P. (2005). Is DPPH Stable Free Radical A Good Scavenger for Oxygen Active Species?. Cem. Pap. 59(1): 11.
Jung, E.J., Bae, M.S., Jo, E.K., Jo, Y.H., dan Lee, S.C. (2011). Antioxidant Activity of Different Parts of Eggplant. Journal of Medicinal Plants Research. 5(18): 4610 - 4615.
Kandoliya, U.K., Bajaniya, V.K., Bhadja, N.K., Bodar, N.P., dan Golakiya, B.A. (2015). Antioxidant and Nutritional Components of Eggplant (Solanum melongena L.) Fruit Grown in Saurastra Region. International Journal of Current Microbiology and Applied Sciences. 4(2): 806 - 813.
Komisi Farmakope Eropa. (2005). European Pharmacopoeia 5.0. Uppsala: Dewan Eropa. Halaman 1084.
Kosasih, E.N., Setiabudhi, T., dan Heryanto, H. (2004). Peranan Antioksidan Pada Lanjut Usia. Jakarta: Pusat Kajian Nasional Masalah Lanjut Usia. Halaman 15, 56 – 60, 69.
Marinova, G., dan Batchvarov, V. (2011). Evaluation of the Methods for Determination of the Free Radical Scavenging Activity by DPPH. Bulg. J. Agric. Sci. 17: 13-14.
Markham, K.R. (1988). Cara Mengidentifikasi Flavonoid. Bandung: Penerbit ITB. Halaman 1.
Martiningsih, N.W., Sukarta, I.N., dan Yuniana, P.E. (2014). Skrining Fitokimia dan Uji Aktivitas Antioksidan dari Ekstrak Etanol Buah Terong Ungu (Solanum melongena L.). Jurnal Kimia. 8(2): 145 - 152.
Marxem, K., Vanselow, K.H., Lippemeier, S., Hintze, R., Ruser, A., dan Hansen, U.P. (2007). Determination of DPPH Radical Oxidation Caused by Methanolic Extracts of Some Microalgal Species by Linear Regression Analysis of Spectrophotometric Measurements. Sensor. 7: 2080 - 2095. Mashudi. (2007). Budi Daya Terong. Jakarta: Azka Press. Halaman 1 - 11.
Molyneux, P. (2004). The Use of the Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211 - 219.
Muchtadi, D. (2013). Antioksidan dan Kiat Sehat di Usia Produktif. Bandung: Alfabeta. Halaman 15
Persid, R., dan Verma, V.N. (2014). Photochemical Studies of Solanum melongena (Eggplant) Fruit by Flame Atomic Absorption Spectrometry. International Letters of Chemistry, Physics and Astronomy. 39: 211 - 218. Prakash, A. (2001). Antioxidant Activity. Medallion Laboratories-Analytical
Progress. 19(2): 1 - 4.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Penerjemah: Padmawinata, K. Bandung: Penerbit ITB. Halaman 191 - 193.
Rosidah, Yam, M.F., Sadikun, A., dan Asmawi, M.Z. (2008). Antioxidant Potential of Gynura procumbens. Pharmaceutical Biology. 46(9): 616 - 625.
Rukmana, R. (1994). Bertanam Terung. Yogyakarta: Penerbit Kanisius. Halaman 11 - 13.
Saparinto, C. (2013). Grow Your Own Vegetables: Panduan Praktis Menanam 14 Sayuran Konsumsi Populer di Pekarangan. Yogyakarta: Penerbit ANDI. Halaman 75.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Halaman 40 - 54.
Sunarjono, H. (2013). Bertanam 36 Jenis Sayur. Jakarta: Penerbit Penebar Swadaya. Halaman 54.
Supriati, Y., dan Herliana, E. (2010). Bertanam 15 Sayuran Organik dalam Pot. Jakarta: Penerbit Swadaya. Halaman 108.
Tiwari, A., Jadon, R.S., Tiwari, P., dan Nayak, S. (2009). Phytochemical Investigation of Crown of Solanum melongena Fruit. International Journal of Phytomedicine. 1: 9 - 11.
Vindayanti, O. (2012). Pemanfaatan Terung Ungu Dalam Pembuatan Dodol Yang Bermanfaat Sebagai Sumber Vitamin A. Tugas Akhir. Yogyakarta: Program Studi Teknik Boga, Jurusan Pendidikan Teknik Boga dan Busana, Fakultas Teknik, Universitas Negeri Yogyakarta.
Wijayakusuma, H. (2004). Penyembuhan dengan Terung. Jakarta: Penerbit Pustaka Populer Obor. Halaman7.
Winarsi, H. ( 2007). Antioksidan Alami dan Radikal Bebas. Yogyakarta: Penerbit Kanisius. Halaman 17, 20, 279.
World Health Organization. (1998). Quality Control Methods For Medicinal Plant Material. Switzerland: WHO. Halaman 35 - 39.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental. Metodologi penelitian meliputi pengambilan bahan tanaman, identifikasi bahan tanaman, pengolahan bahan tanaman, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak etanol dan uji aktivitas antioksidan dengan metode DPPH sebagai sumber radikal bebas dan absorbansi DPPH diukur menggunakan alat spektrofotometer visibel pada panjang gelombang 516 nm.
3.1Alat
Alat-alat yang digunakan terdiri dari alat-alat gelas laboratorium, aluminium foil, blender (National), cawan berdasar rata, desikator, kaca objek,
kaca penutup, kertas saring, krus porselin, mikroskop (Olympus), neraca analitis (Vibra), neraca kasar (O’haus), oven listrik (Stork), penangas air (Yenaco), rotary evaporator (Stuart), spektofotometer UV/Vis (Shimadzu), dan tanur (Gallenkamp).
3.2Bahan
(Mg), timbal (II) asetat, toluen, α-naftol. Bahan kimia berkualitas teknis: air suling dan etanol 96%.
3.3Penyiapan Bahan Tanaman
Penyiapan bahan tanaman meliputi pengumpulan bahan tanaman, identifikasi tanaman dan pembutan simplisia.
3.3.1 Pengumpulan bahan tanaman
Pengumpulan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan bahan tumbuhan yang sama dari daerah lain. Tumbuhan yang digunakan adalah buah terong lalap ungu yang diperoleh dari Desa Tandem Hulu, Kecamatan Hamparan Perak, Kabupaten Deli Serdang, Provinsi Sumatera Utara.
3.3.2 Identifikasi bahan tanaman
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian dan Pengembangan Biologi LIPI di Bogor. Hasil identifikasi tanaman dapat dilihat pada Lampiran 1, halaman 44.
Pembuatan simplisia
3.4Pembuatan Pereaksi
3.4.1 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air secukupnya hingga diperoleh larutan 100 ml (Depkes RI, 1995).
3.4.2 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan dalam air suling bebas karbon dioksida sebanyak 100 ml (Depkes RI, 1995).
3.4.3 Pereaksi natrium hidroksida 2 N
Sebanyak 8 g kristal natrium hidroksida dilarutkan dengan air suling sebanyak 100 ml (Depkes RI, 1995).
3.4.4 Pereaksi asam klorida 2 N
Sebanyak 17 ml larutan asam klorida pekat ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes RI, 1995).
3.4.5 Pereaksi asam sulfat 2 N
Sebanyak 5,5 ml larutan asam sulfat pekat ditambahkan air suling sampai 100 ml (Depkes RI, 1995).
3.4.6 Pereaksi kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air suling (Depkes RI, 1995).
3.4.7 Pereaksi Mayer
3.4.8 Pereaksi Molisch
Sebanyak 3 g α-naftol ditimbang, dilarutkan dalam asam nitrat 0,5 N hingga diperoleh larutan 100 ml (Depkes RI,1995).
3.4.9 Pereaksi Dragendorff
Sebanyak 0,8 g bismut (III) nitrat ditimbang, dilarutkan dalam 20 ml asam nitrat pekat, pada wadah lain ditimbang sebanyak 27,2 g kalium iodida, dilarutkan dalam 50 ml air suling, kemudian kedua larutan dicampurkan dan didiamkan sampai memisah sempurna. Larutan yang jernih diambil dan diencerkan dengan air suling hingga volume larutan 100 ml (Depkes RI, 1995).
3.4.10 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, dilarutkan dalam air suling secukupnya, lalu ditambahkan 2 g iodium kemudian ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes RI, 1995).
3.4.11 Pereaksi Liebermann-Burchard
Sebanyak 5 bagian volume asam sulfat pekat dicampurkan dengan 50 bagian volume etanol 95%. Kemudian ditambahkan dengan hati-hati 5 bagian volume asam asetat anhidrida ke dalam campuran tersebut dan dinginkan (Depkes RI, 1995).
3.5Pemeriksaan Karakteristik Simplisia
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap buah terong lalap ungu dengan mengamati bentuk, warna, bau, rasa dan ukuran simplisia. Gambar tanaman dan buah terong lalap ungu dapat dilihat pada Lampiran 2, halaman 46, dan gambar simplisia dan serbuk simplisia dapat dilihat pada Lampiran 3, halaman 47.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia buah terong lalap ungu. Serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop. Hasil pemeriksaan mikroskopik dapat dilihat pada Lampiran 4, halaman 48.
3.5.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung, tabung penerima 5 ml berskala 0,05 ml, alat penampung dan pemanas listrik.
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1998). Perhitungan kadar air dapat dilihat pada Lampiran 7, halaman 51. 3.5.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dengan 100 ml air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu bersumbat, dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105ºC sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995). Perhitungan kadar sari yang larut dalam air dapat dilihat pada Lampiran 7, halaman 51.
3.5.5 Penetapan kadar sari yang larut dalam etanol
etanol 96% dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995). Perhitungan kadar sari yang larut dalam etanol dapat dilihat pada Lampiran 7, halaman 52.
3.5.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada suhu 600 ºC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh
bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995). Perhitungan kadar abu total dapat dilihat pada Lampiran 7,
halaman 52.
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu total dididihkan dalam 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu, dicuci dengan air panas, lalu dipijar sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995). Perhitungan kadar abu yang tidak larut dalam asam dapat dilihat pada Lampiran 7, halaman 53.
3.6Skrining Fitokimia
3.6.1 Pemeriksaan steroida/triterpenoida
penguap. Pada sisa ditambahkan beberapa tetes pereaksi Liebermann-Burchard. Timbulnya warna biru atau biru hijau menunjukkan adanya steroida, sedangkan warna merah, merah muda atau ungu meunjukkan adanya triterpenoida (Harborne, 1987).
3.6.2 Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g, ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring, filtrat dipakai untuk uji alkaloida. Diambil 3 tabung reaksi, lalu ke dalam masing-masing tabung reaksi dimasukkan 0,5 ml filtrat. Pada tabung I : ditambahkan 2 tetes pereaksi Mayer, akan terbentuk endapan menggumpal berwarna putih atau kuning.
Pada tabung II : ditambahkan 2 tetes pereaksi Dragendorff, akan terbentuk endapan berwarna coklat atau jingga kecoklatan.
Pada tabung III : ditambahkan 2 tetes pereaksi Bourchardat, akan terbentuk endapan berwarna coklat sampai kehitaman.
Alkaloid disebut positif jika terjadi endapan atau kekeruhan pada dua atau tiga dari percobaan di atas (Depkes RI, 1995).
3.6.3 Pemeriksaan glikosida
kali. Kumpulan sari air diuapkan pada temperatur tidak lebih dari 50oC. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut, yaitu 0,1 ml larutan percobaan dimasukkan ke dalam tabung reaksi, diuapkan di penangas air. Sisa dilarutkan dalam 2 ml air suling dan 5 tetes pereaksi Molish kemudian secara perlahan ditambahkan 2 ml asam sulfat pekat. Glikosida positif jika terbentuk cincin ungu (Depkes, 1995).
3.6.4 Pemeriksaan flavonoid
Serbuk simplisia ditimbang sebanyak 10 g, ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966). 3.6.5 Pemeriksaan saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan ke dalam tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes RI, 1995).
3.6.6 Pemeriksaan tanin
3.7 Pembuatan Ekstrak
Pembuatan ekstrak etanol buah terong lalap ungu dilakukan dengan cara perkolasi. Prosedur pembuatan ekstrak sebanyak 100 g serbuk simplisia dibasahi dengan etanol 96% dan dibiarkan selama 3 jam. Kemudian dimasukkan ke dalam alat perkolator, lalu dituang cairan penyari etanol sampai semua simplisia terendam dan terdapat selapis cairan penyari diatasnya, mulut tabung perkolator ditutup dengan alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan dibiarkan tetesan ekstrak mengalir dengan kecepatan 1 ml/menit, perkolat ditampung. Cairan penyari ditambahkan berulang-ulang secukupnya sehingga selalu terdapat cairan penyari di atas simplisia. Perkolasi dihentikan jika cairan perkolat yang terakhir keluar tidak berwarna, lalu pekatkan dengan alat penguap vakum putar hingga diperoleh ekstrak kental (Depkes RI, 1979). Bagan kerja pembuatan ekstrak etanol dapat dilihat pada Lampiran 6, halaman 50.
3.8 Pengujian Aktivitas Antioksidan
3.8.1 Prinsip metode pemerangkapan radikal bebas DPPH
Kemampuan sampel uji dalam meredam proses oksidasi radikal bebas DPPH (1,1 diphenyl-2-picryl-hidrazyl) dalam larutan metanol (sehingga terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50 (konsentrasi
sampel uji yang mampu meredam radikal bebas 50%) digunakan sebagai parameter menentukan aktivitas antioksidan sampel uji (Molyneux, 2004).
3.8.2 Pembuatan larutan DPPH
sebanyak 5 ml kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan dengan metanol sampai garis tanda (konsentrasi 40 ppm).
3.8.3 Penentuan panjang gelombang serapan maksimum
Larutan DPPH konsentrasi 40 ppm dihomogenkan dan diukur serapannya pada panjang gelombang 400 - 800 nm. Gambar alat spektrofotometer dapat dilihat pada Lampiran 11, halaman 61.
3.8.4 Penentuan operating time
Larutan DPPH konsentrasi 40 ppm diukur serapannya pada panjang gelombang serapan maksimum yang telah diperoleh. Data absorbansi operating time dapat diliha pada Lampiran 8, halaman 54.
3.8.5 Pembuatan larutan induk
Sebanyak 25 mg ekstrak terong lalap ungu ditimbang, kemudian dilarutkan ke dalam labu tentukur 25 ml dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
3.8.6 Penentuan aktivitas antioksidan sampel uji
Larutan induk dipipet sebanyak 0,15 ml; 0,20 ml; 0,25 ml; dan 0,30 ml ke dalam labu tentukur 10 ml untuk mendapatkan konsentrasi larutan uji 15 ppm, 20 ppm, 25 ppm, dan 30 ppm. Ditambahkan 2 ml larutan DPPH 0,5 mM (200 ppm) ke dalam masing-masing labu tentukur lalu volumenya dicukupkan dengan metanol sampai garis tanda. Didiamkan selama 60 menit. Lalu diukur serapannya menggunakan spektrofotometer UV-visible pada panjang gelombang 516 nm. 3.8.7 Penentuan persen pemerangkapan
persen pemerangkapan radikal bebas dihitung dengan rumus sebagai berikut:
% pemerangkapan = Akontrol - Asampel
Akontrol x 100%
Keterangan: Akontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel
Perhitungan persen pemerangkapan DPPH dapat dilihat pada Lampiran 9, halaman 55 - 59.
3.8.8 Penentuan nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji
(g/ml) yang memberikan peredaman DPPH sebesar 50% (mampu menghambat / meredam proses oksidasi sebesar 50%). Hasil perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak (ppm) sebagai absis (sumbu X) dan
nilai % peredaman (antioksidan) sebagai ordinatnya (sumbu Y). Nilai IC50
( konsentrasi sample uji yang mampu memerangkap radikal bebas sebesar 50%) digunakan sebagai parameter untuk menentkan aktivitas antioksidan sample uji (Prakash, 2001). Perhitungan nilai IC50 dapat diliha pada Lampiran 10,
BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor, menunjukkan bahwa sampel termasuk ke dalam suku Solanaceae, spesies Solanum melongena L.
4.2Hasil Karakterisasi Simplisia 4.2.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik buah terong lalap ungu segar adalah bentuk buah bulat kecil dengan panjang ± 3cm dan lebar ± 2,5 cm - 3 cm.
Hasil pemeriksaan makroskopik simplisia buah terong lalap ungu adalah panjang ± 2 cm dan lebar ± 1,5 - 2 cm.
4.2.2 Hasil pemeriksaan organoleptis
Hasil pemeriksaan organoleptis buah terong lalap ungu adalah buah berwarna ungu dengan sedikit garis-garis putih, rasanya renyah, sedikit manis dan tidak getir.
Hasil pemeriksaan organoleptis simplisia buah terong lalap ungu adalah simplisia berupa irisan-irisan berwarna coklat dengan permukaan yang kasar. 4.2.3 Hasil pemeriksaan mikroskopik
4.2.4 Hasil pemeriksaan karakteristik serbuk simplisia
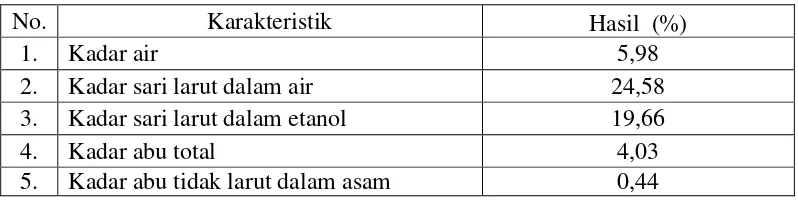
Monografi dari simplisia buah terong lalap ungu tidak terdapat dalam buku Materia Medika Indonesia (MMI), sehingga tidak ada acuan untuk menentukan parameter simplisia tersebut. Hasil pemeriksaan kadar air, kadar sari larut dalam air, kadar sari larut dalam etanol, kadar abu total, dan kadar abu tidak larut asam dapat dilihat pada Tabel 4.1 berikut ini :
Tabel 4.1 Hasil pemeriksaan karakteristik serbuk simplisia buah terong lalap ungu
No. Karakteristik Hasil (%)
1. Kadar air 5,98
2. Kadar sari larut dalam air 24,58
3. Kadar sari larut dalam etanol 19,66
4. Kadar abu total 4,03
5. Kadar abu tidak larut dalam asam 0,44
Penetapan kadar air dilakukan berhubungan dengan mutu simplisia agar tidak mudah ditumbuhi mikroorganisme. Berdasarkan Tabel 4.1 diperoleh kadar air simplisia buah terong lalap ungu sebesar 5,98%. Hal ini sesuai dengan persyaratan umum kadar air simplisia buah, yaitu ≤ 10%. Kadar air yang yang melebihi persyaratan memungkinkan terjadinya pertumbuhan jamur (Depkes RI, 1995).
[image:36.595.113.512.286.386.2]Penetapan kadar abu total dilakukan untuk mengetahui kadar senyawa anorganik dalam simplisia, misalnya logam K, Ca, Na, Pb dan Hg, sedangkan penetapan kadar abu tidak larut dalam asam dilakukan untuk mengetahui kadar senyawa abu yang tidak larut dalam asam, misalnya silika (WHO, 1998).
4.3 Hasil Skrining Fitokimia
[image:37.595.115.516.439.581.2]Pemeriksaan skrining fitokimia dilakukan secara kualitatif. Skrining fitokimia dilakukan untuk mengetahui golongan metabolit sekunder yang terkandung dalam simplisia dan ekstrak etanol. Hasil skrining fitokimia terhadap serbuk simplisia dan ekstrak etanol diketahui bahwa buah terong lalap ungu mengandung golongan senyawa-senyawa kimia seperti yang terlihat pada Tabel 4.2 berikut ini:
Tabel 4.2 Hasil skrining fitokimia
No. Pemeriksaan Simplisia Ekstrak
1. Steroida/triterpenoida + +
2. Alkaloida + +
3. Glikosida + +
4. Flavonoid + +
5. Saponin + +
6. Tanin + +
Keterangan: (+) Positif : mengandung golongan senyawa () Negatif : tidak mengandung golongan senyawa
yang mempunyai potensi antioksidan tersebut adalah antosianin yang merupakan
pigmen yang memberikan warna merah, merah senduduk dan ungu pada tanaman (Harbone, 1987). Antosianin bertindak sebagai penangkap radikal bebas karena
gugus hidroksil yang dikandungnya mendonorkan hidrogen kepada radikal bebas. Senyawa tersebut mampu menetralisir radikal bebas dengan memberikan elektron kepadanya sehingga atom dengan elektron yang tidak berpasangan mendapat paangan elektron dan menjadi stabil (Silalahi, 2006). Senyawa lain yang memiliki potensi sebagai antioksian adalah alkaloid, contohnya indol yang memiliki kemampuan untuk menghentikan reaksi rantai radikal bebas, quinolin dan kafein sebagai peredam radikal bebas dan melatonin yang berperan penting menjaga sel dari pengaruh radiasi (Yuhernita dan Juniarti, 2011). Senyawa turunan dari senyawa amin memiliki tahapan terminasi yang sangat lama, dengan demikian mampu menghentiksn reaksi berantai radikal bebas (Shahidi, 1997).
4.4 Hasil Pengujian Aktivitas Antioksidan
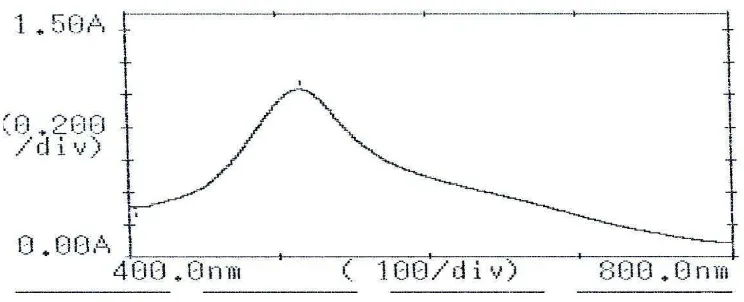
4.4.1Hasil penentuan panjang gelombang serapan maksimum
[image:38.595.125.497.577.728.2]Hasil pengukuran serapan maksimum larutan DPPH dengan menggunakan spektrofotometer UV-Visibel menghasilkan serapan maksimum pada panjang gelombang 516 nm termasuk dalam kisaran panjang gelombang sinar tampak (400 nm - 800 nm) (Dachriyanus, 2004), dan termasuk dalam rentang panjang gelombang DPPH yang berkisar antara 515 - 520 nm (Molyneux, 2004).
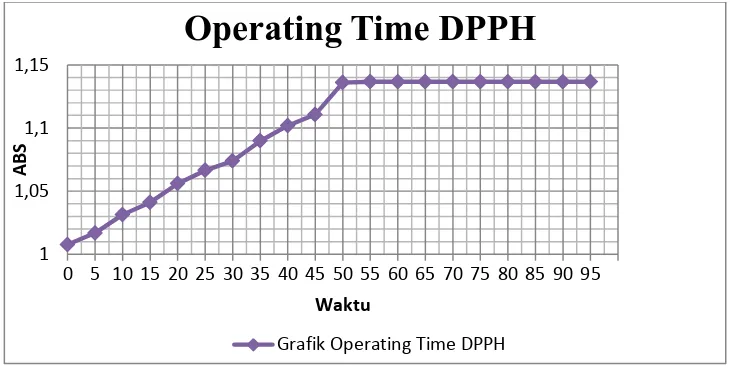
4.4.2 Hasil penentuan operating time larutan DPPH dalam metanol
Penentuan operating time bertujuan untuk mengetahui waktu pengukuran yang stabil. Hasil penentuan operating time diperoleh waktu kerja terbaik adalah pada menit ke 60 setelah penambahan pelarut metanol. Kurva absorbani untuk operating time larutan DPPH dalam metanol dapat dilihat pada gambar 4.2 berikut ini :
Gambar 4.2 Kurva absorbansi operating time larutan DPPH 4.4.3 Hasil analisis persen pemerangkapan DPPH oleh sample uji
Aktivitas antioksidan ekstrak etanol buah terong lalap ungu diperoleh dari hasil pengukuran absorbansi DPPH pada menit ke-60 dengan adanya penambahan larutan uji dengan konsentrasi 15 ppm, 20 ppm, 25 ppm, dan 30 ppm yang
1 1,05 1,1 1,15
0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95
A
B
S
Waktu
[image:39.595.141.506.415.600.2]Operating Time DPPH
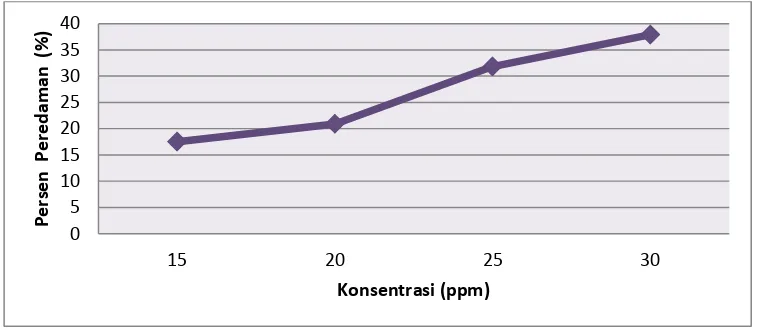
dibandingkan dengan kontrol DPPH (tanpa penambahan larutan uji). Pada hasil analisis aktivitas antioksidan ekstrak etanol buah terong lalap ungu dapat dilihat adanya penurunan nilai absorbansi DPPH yang diberi larutan uji terhadap kontrol pada setiap kenaikan konsentrasi. Penurunan absorbansi DPPH dan persen pemerangkapan dengan penambahan ekstrak etanol buah terong lalap ungu dapat dilihat pada Tabel 4.3 berikut ini :
Tabel 4.3 Hasil penurunan absorbansi dan persen pemerangkapan
Larutan uji Konsentrasi (ppm)
Absorbansi % Pemerangkapan
I II III I II III
Rata-rata
Ekstrak etanol terong lalap ungu
0 1,0620 1,0964 1,0173 0,00 0,00 0,00 0,00
15 0,9017 0,9069 0,8109 15,09 17,28 20,28 17,55
20 0,8629 0,8755 0,7744 18,74 20,14 23,87 20,91
25 0,7827 0,7585 0,6265 26,29 30,83 38,41 31,84
30 0,6791 0,6982 0,5959 36,05 36,31 41,42 37,92
[image:40.595.123.508.556.721.2]Hubungan antara konsentrasi dengan persen pemerangkapan radikal bebas DPPH oleh ekstrak etanol terong lalap ungu dapat dilihat pada Gambar 4.3 berikut ini:
Gambar 4.3 Hubungan konsentrasi dengan persen pemerangkapan
0 5 10 15 20 25 30 35 40
15 20 25 30
Penurunan nilai absorbansi menunjukkan aktivitas antioksidan yang semakin besar. Penurunan nilai absorbansi terjadi karena adanya pemerangkapan radikal bebas DPPH oleh larutan uji sehingga menunjukkan adanya aktivitas antioksidan. Pemerangkapan radikal bebas terjadi karena adanya transfer elektron atom hidrogen dari senyawa antioksidan kepada radikal bebas DPPH. Sehingga semua elektron pada senyawa radikal bebas DPPH menjadi berpasangan, yang ditandai dengan berubahnya warna larutan dari ungu tua menjadi kuning terang (Molyneux, 2004).
4.4.4 Hasil analisis nilai IC50
Nilai IC50 diperoleh berdasarkan perhitungan persamaan regresi linier
yang diperoleh dengan cara memplot konsentrasi larutan uji dan persen pemerangkapan DPPH sebagai parameter aktivitas antioksidan, dimana konsentrasi sampel (ppm) sebagai absis (sumbu X) dan nilai % pemerangkapan sebagai ordinat (sumbu Y). Nilai IC50 (konsentrasi sampel uji yang mampu
memerangkap radikal bebas sebesar 50%) digunakan sebagai parameter untuk menentukan aktivitas antioksidan sampel uji (Prakash, 2001).
Hasil persamaan regresi linier dan hasil analisis IC50 yang diperoleh dari
[image:41.595.113.510.604.655.2]ekstrak etanol buah terong lalap ungu dapat dilihat pada Tabel 4.4 berikut ini Tabel 4.4 Hasil persamaan regresi linier dan hasil analisis IC50
Larutan uji Persamaan regresi IC50 (ppm) Ekstrak etanol buah terong
lalap ungu Y = 1,25X - 0,86 40,68
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan: a. Hasil karakterisasi simplisia buah terong lalap ungu diperoleh kadar air 5,98%,
kadar sari larut air 24,58%, kadar sari larut etanol 19,66%, kadar abu total 4,03%, dan kadar abu tidak larut asam 0,44%.
b. Hasil skrining fitokimia simplisia dan ekstrak etanol buah terong lalap ungu menunjukkan adanya senyawa kimia golongan steroida, alkaloid, glikosida, flavonoid, saponin, dan tanin.
c. Nilai IC50 dari ekstrak etanol buah terong lalap ungu adalah sebesar 40,68 ppm
dan termasuk dalam kategori sangat kuat.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman
Uraian tanaman meliputi daerah tumbuh, nama daerah, nama asing, sistematika tanaman, morfologi tanaman, kandungan kimia dan kegunaan dari tanaman.
2.1.1 Daerah tumbuh
Terong (Solanum melongena L.) merupakan tanaman asli daerah tropis. Tanaman ini berasal dari benua Asia, terutama India, Birma, Indonesia dan Myanmar. Dari daerah-daerah ini kemudian dibawa ke Spanyol dan disebarluaskan ke negara-negara lain di Afrika Tengah, Afrika Timur, Afrika Barat, dan Amerika Selatan (Rukmana, 1994; Mashudi, 2007).
Tanaman terong sangat mudah dikembangbiakkan karena dapat tumbuh di daerah dataran rendah sampai dataran tinggi sekitar 1.200 m dari permukaan laut (Supriati dan Herliana, 2010).
2.1.2 Nama daerah
2.1.3 Nama asing
Tanaman terong banyak tersebar di berbagai negara dengan nama yang berbeda, misalnya eggplant (Eropa), aubergine (UK), brinjal (India), khatiri-kai (Srilanka), aikua (Katon), gie-zi (China), nasubi (Jepang), ca tim (Vietnam), dan makhua (Thailand) (Mashudi, 2007; Anonima, 2012).
2.1.4 Sistematika tanaman
Sistematika tanaman terong berdasarkan identifikasi oleh Herbarium Medanense (MEDA) adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Solanales Famili : Solanaceae Genus : Solanum
Spesies : Solanum melongena L.
Menurut Choudhary dan Gaur (2009) terdapat 3 varietas dibawah spesies Solanum melongena, yaitu :
1. Solanum melongena var. esculentum
Terong ini bentuk buahnya besar, bulat atau bulat telur. 2. Solanum melongena var. serpentinum
Terong ini bentuk buahnya panjang, ramping, bagian ujung biasanya membengkok.
3. Solanum melongena var. depressum
2.1.5 Morfologi tanaman
Terong (Solanum melongena L.) merupakan tanaman setahun jenis perdu yang dapat tumbuh hingga mencapai tinggi 50 - 150 cm. Batang bulat, bercabang, berkayu, berduri dan berbulu. Daun tunggal, bulat telur, ujung runcing, pangkal berlekuk, tepi berombak, panjang 3 - 15 cm, lebar 2 - 9 cm, pertulangan menyirip, warnanya hijau, letak daun berselang-seling dan bertangkai pendek. Bunga majemuk, berseling, terdiri dari 5 kelopak, bentuk lonceng, terdiri dari lima mahkota,berwarna putih lembayung sampai ungu, kepala sari kuning, (Hutapea, 2001; Haryoto, 2009). Buah terong merupakan buah sejati tunggal, berdaging tebal, bentuk buahnya beraneka ragam, diantaranya bulat kecil, silindris, lonjong, dan bulat panjang. Warna buahnya ungu, tetapi ada pula yang berwarna putih dan hijau bergaris putih (Sunarjono 2013; Mashudi, 2007). Biji pipih, kecil, kuning, dan licin. Akar tunggang dan berwarna cokelat muda (Hutapea, 2001).
2.1.6 Kandungan kimia
Kandungan zat aktif yang terkandung dalam terung yaitu alkaloid, saponin, flavonoid, polifenol, asam amino, alanina, arginina, asam askorbat, beta karoten, asam klorogenat, asam folat, saporin, dan nasunin (Hutapea, 2001; Wijayakusuma, 2004).
2.1.7 Kegunaan tanaman
manisan dan juga dodol ( Vindayanti, 2012; Hastuti, 2007). Tidak hanya sebagai bahan makanan, terong juga bermanfaat untuk mengobati berbagai penyakit, seperti seperti kanker, hipertensi, hepatitis, diabetes, arthritis, asma dan bronchitis (Persid dan Verma, 2014; Kandoliya, dkk., 2015).
2.2 Simplisia dan Ekstrak 2.2.1 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang belum mengalami pengolahan apapun juga dan kecuali dikatakan lain, berupa bahan yang telah dikeringkan. Simplisia dibedakan simplisia nabati, simplisia hewani dan simplisia pelikan (mineral). Simplisia nabati adalah simplisia yang
berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan (Depkes RI, 2000).
2.2.2 Ekstrak
Ekstrak yaitu sediaan kental atau cair yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes RI, 1995).
Menurut Depkes RI (2000), ada beberapa metode ekstraksi yang sering digunakan antara lain yaitu:
a. Cara dingin 1. Maserasi
Maserasi adalah proses pengekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar). Secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna (exhaustive extraction) yang umunya dilakukan pada temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus menerus sampai diperoleh ekstrak (perkolat) yang tidak bereaksi ketika ditambahkan serbuk Mg dan asam klorida pekat.
b. Cara panas 1. Refluks
2. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40 - 50oC.
4. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96 - 98oC) selama waktu tertentu (15 - 20 menit).
5. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥30 menit) dan temperatur sampai titik didih air.
2.3Radikal Bebas
menimbulkan berbagai penyakit seperti kanker, jantung koroner, katarak, serta penyakit degeneratif lainnya (Muchtadi, 2013).
Mekanisme reaksi radikal bebas terbentuk melalui 3 tahapan reaksi, yaitu : (1) permulaan (inisiasi, initiation) suatu radikal bebas, (2) perambatan (propagasi, propagation) reaksi radikal bebas; (3) pengakhiran (terminasi, termination) reaksi radikal bebas (Fessenden dan Fessenden, 1986).
Tahap inisiasi adalah tahap awal terbentuknya radikl bebas. tahap propagasi adalah tahap perpanjangan radikal berantai, dimana terjadi reaksi antara sutau radikal dengan senyawa lain dan menghasilkan radikal baru. Tahap terminasi adalah tahap akhir, terjadi pengikatan suatu radikal bebas dengan radikal bebas yang lain sehingga membentuk senyawa non radikal yang biasanya kurang reaktif dari radikal induknya (Kumalaningsih, 2006).
2.4Antioksidan
reaksi oksidasi, dengan cara mencegah terbentuknya radikal atau dengan mengikat radikal bebas dan molekul yang sangat reaktif (Winarsi, 2007).
Menurut Kosasih (2004) antioksidan dapat dibedakan menjadi 3 yaitu : a. Antioksidan primer
Antioksidan primer bekerja untuk mencegah terbentuknya senyawa radikal bebas baru dengan mengubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya sebelum radikal bebas bereaksi, contoh antioksidan ini adalah enzim SOD (superoxide dismutase) yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas.
b. Antioksidan sekunder
Antioksidan sekunder berfungsi menangkap senyawa radikal bebas serta mencegah terjadinya reaksi berantai, contoh antioksidan sekunder adalah vitamin E, vitamin C dan β-karoten, bilirubin, albumin.
c. Antioksidan tersier
Antioksidan tersier merupakan senyawa yang memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas, contoh enzim yang dapat memperbaiki DNA pada inti sel adalah metionin sulfoksidan reduktase.
Antioksidan alami yaitu antioksian yang dapat diperoleh dari tanaman atau hewan berupa tokoferol, vitamin C, betakaroten, flavonoid dan senyawa fenolik (Kumalaningsih, 2006).
2.4.1 Tokoferol
mudah menyumbangkan atom hidrogen pada gugus hidroksil ke radikal bebas sehingga radikal bebas menjadi tidak reaktif ( Silalahi, 2006).
[image:51.595.213.448.161.263.2]Rumus bangun tokoferol dapat dilihat pada gambar 2.1 berikut:
Gambar 2.1 Rumus bangun tokoferol 2.4.2 Vitamin C
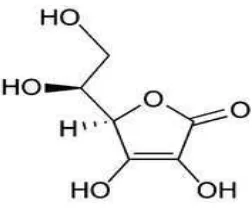
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan rumus molekul C6H8O6. Pemerian vitamin C adalah hablur atau serbuk berwarna
putih atau agak kekuningan. Pengaruh cahaya lambat laun menyebabkan berwarna gelap, dalam keadaan kering stabil di udara namun dalam larutan cepat teroksidasi. Vitamin C mudah larut dalam air, agak sukar larut dalam etanol,
praktis tidak larut dalam kloroform, dalam eter dan dalam benzen (Depkes RI, 1979). Rumus bangun vitamin C dapat dilihat pada gambar 2.2
berikut:
Gambar 2.2 Rumus bangun vitamin C
[image:51.595.267.393.541.645.2]askorbat adalah agen pereduksi sehingga dapat mengurangi oksigen reaktif ( Hamid, dkk., 2010).
2.4.3 Karotenoid
Karotenoid adalah suatu kelompok pigmen yang berwarna kuning, jingga atau merah jingga, mempunyai sifat larut dalam lemak atau pelarut organik tetapi tidak larut dalam air. Salah satu senyawa karotenoid adalah β-karoten, yaitu senyawa yang akan dikonversikan menjadi vitamin A oleh tubuh sehingga sering juga disebut sebagai pro-vitamin A (Kumalaningsih, 2006).
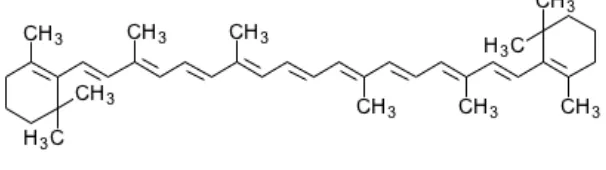
β-karoten mempunyai berat molekul 536,9 dengan rumus molekul C40H56.
[image:52.595.161.464.492.577.2]Karakteristik β-karoten adalah hablur atau serbuk berwarna coklat-merah atau merah kecoklatan, praktis tidak larut dalam air, sedikit larut dalam sikloheksana, kurang larut dalam etanol. β-karoten peka terhadap udara, panas dan cahaya, terutama ketika dalam bentuk larutan (Komisi Farmakope Eropa, 2005). Rumus bangun β-karoten dapat dilihat pada gambar 2.3 berikut:
Gambar 2.3 Rumus bangun β-karoten
2.4.4 Flavonoid
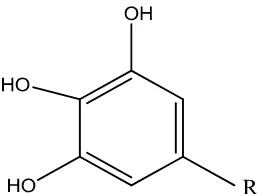
Flavonoid merupakan senyawa polifenol yang mengandung 15 atom karbon dalam inti dasarnya, yang tersusun dalam konfigurasi C6-C3-C6 (Markham,
[image:53.595.195.425.213.290.2]1998). Rumus bangun flavonoid dapat dilihat pada gambar 2.4 berikut :
Gambar 2.4 Rumus bangun flavonoid
Senyawa ini adalah senyawa pereduksi yang dapat menghambat reaksi oksidasi sehingga dapat dijadikan sebagai antioksidan (Robinson, 1995). Senyawa ini berperan sebagai penangkap radikal bebas karena mengandung gugus hidroksil (Silalahi, 2006).
2.4.5 Polifenol
Gambar 2.5 Rumus bangun polifenol
[image:53.595.247.379.475.572.2]radikal bebas dan menghambat terjadinya reaksi berantai dari pembentukan radikal bebas. Polifenol merupakan komponen yang bertanggung jawab terhadap aktivitas antioksidan dalam buah dan sayuran (Hattenschwiller dan Vitousek, 2000).
2.5 Spektrofotometer UV-Visibel
Spektrofotometer UV-Visibel adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan sinar tampak yang diabsorbsi oleh sampel. Spektrofotometer yang sering digunakan dalam dunia industri farmasi salah satu adalah spektrofotometer ultraviolet dengan panjang gelombang 200 - 400 nm dan
visibel (cahaya tampak) dengan panjang gelombang 400 - 800 nm ( Dachriyanus, 2004).
2.6 Metode Pemerangkapan Radikal Bebas DPPH
[image:55.595.260.369.250.359.2]DPPH (1,1-diphenyl-2-picrylhydrazil) pertama kali ditemukan pada tahun 1922 oleh Goldschmidt dan Renn. DPPH bersifat tidak larut dalam air, berwarna ungu pekat seperti KMnO4 dan bentuk tereduksinya (DPPH-H) berwarna jingga kekuningan (Ionita, 2005). Rumus bangun DPPH dapat dilihat pada gambar 2.5 berikut:
Gambar 2.6 Rumus bangun DPPH
Metode pemerangkapan radikal bebas DPPH merupakan metode yang paling banyak digunakan karena memiliki keunggulan, seperti cepat, sederhana, dan tidak mahal untuk mengukur kemampuan berbagai senyawa dalam memerangkap radikal bebas. (Marinova dan Batchvarov, 2011).
Metode uji antioksidan DPPH didasarkan pada reaksi penangkapan atom hidrogen oleh DPPH dari senyawa antioksidan. Selanjutnya DPPH akan diubah menjadi DPPH-H (bentuk tereduksi dari DPPH) oleh senyawa antioksidan. Warna ungu larutan DPPH akan berubah menjadi kuning lemah apabila elektron ganjil radikal bebas tersebut berpasangan dengan atom hidrogen dari senyawa antioksidan (Prakash, 2001).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah Inhibitory Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
antioksidan yang memberikan % penghambatan 50%. Nilai IC50 diperoleh
berdasarkan perhitungan persamaan regresi linier yang diperoleh dengan cara memplot konsentrasi larutan uji dan persen pemerangkapan DPPH (Brand, dkk., 1995). Secara spesifik, suatu senyawa dikatakan sebagai antioksidan sangat kuat jika nilai IC50 kurang dari 50 ppm, kuat untuk IC50 bernilai 50 - 100 ppm, sedang
jika IC50 bernilai 101 - 150 ppm dan lemah jika IC50 bernilai lebih dari 150 ppm
(Fidrianny, dkk., 2014). 2.6.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut metanol atau etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004). 2.6.2 Pengukuran absorbansi panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal. Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran sampel uji pada metode
pemerangkapan radikal bebas DPPH sangat bervariasi. Biasanya absorbansi DPPH diukur pada panjang gelombang 515 - 520 (Marxem, dkk., 2007).
2.6.3 Waktu pengukuran
BAB I PENDAHULUAN
1.1Latar Belakang
Dewasa ini telah banyak diungkapkan bahaya lingkungan yang tidak sehat anatara lain terbentuknya radikal bebas. Asap kendaraan bermotor, asap rokok dan asap dari industri menyumbang ratusan bahan kimia yang mengakibatkan pembentukan radikal bebas. Radikal bebas dapat masuk dan terbentuk dalam tubuh melalui pernafaan, kondisi lingkungan yang tidak sehat dan makanan yang berlemak (Kumalaningsih, 2006).
Radikal bebas adalah atom atau gugus atom yang memiliki satu atau lebih elektron tidak berpasangan, sehingga senyawa tersebut sangat reaktif mencari pasangan. (Fessenden dan Fessenden, 1986). Radikal bebas cenderung menangkap elektron dari molekul lain dan kemudian membuat senyawa baru yang tidak normal yang akan menyebabkan reaksi berantai. Radikal bebas dapat diatasi dengan adanya senyawa antioksidan (Kosasih, 2004).
akan menyerang komponen lipid, protein maupun DNA sehingga mengakibatkan kerusakan-kerusakan yang disebut dengan stress oksidatif. Proses perusakan oleh radikal bebas tersebut dapat dihambat dengan antioksidan tambahan yang berasal dari bahan makanan, terutama dari sayur-sayuran dan buah-buahan. Misalnya: vitamin C, vitamin E, β-karoten, dan flavonoid (Winarsi, 2007). Antioksidan alami yang berasal dari makanan seperti sayur-sayuran dan buah-buahan dapat memberikan manfaat yang baik dalam mempertahankan tubuh dari gangguan kesehatan dan menghambat proses penuaan (Kosasih, dkk., 2004).
Salah satu sayuran yang memiliki aktivitas antioksidan adalah terong. Terong termasuk sayuran yang banyak digemari berbagai kalangan. Terong biasanya dikonsumsi dengan cara dimasak, namum ada beberapa jenis terong yang dapat dimakan sebagai lalap segar. Selain sebagai bahan makanan, terong bermanfaat untuk mengobati berbagai penyakit, seperti kanker, hipertensi, hepatitis, diabetes, arthritis, asma dan bronchitis (Persid dan Verma, 2014; Kandoliya, dkk., 2015). Kandungan gizi pada terong cukup tinggi antara lain: protein, vitamin A, vitamin B, dan Vitamin C (Saparinto, 2013).
antosianinnya cukup tinggi (Astawan dan Kasih, 2008). Komponen fenolik utama dari kulit terong adalah antosianin. Antosianin merupakan pigmen berwarna merah atau ungu pada sayur-sayuran dan buah-buahan. Antosianin merupakan antioksidan yang memiliki potensi tinggi sebagai pemerangkap radikal bebas (Persid dan Verma, 2014; Jung, dkk., 2011).
Berdasarkan uraian di atas, maka penulis melakukan karakterisasi simplisia dan skrining fitokimia serta uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu dengan metode pemerangkapan radikal bebas 1,1-diphenyl-2-picryhydrazil (DPPH).
1.2Perumusan Masalah
Berdasarkan latar belakang diatas, maka perumusan masalah dalam penelitian ini adalah sebagai berikut:
a. apakah karakteristik simplisia buah terong lalap ungu dapat ditentukan?
b. apakah golongan senyawa kimia yang terkandung dalam buah terong lalap ungu ?
c. apakah nilai IC50 ekstrak etanol buah terong lalap ungu termasuk kedalam kategori sangat kuat?
1.3Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis dalam penelitian ini adalah sebagai berikut:
a. karakteristik simplisia buah terong lalap ungu dapat ditentukan.
lalap ungu adalah steroid/triterpenoid, alkaloid, glikosida, flavonoid, saponin, dan tanin.
c. nilai IC50 ekstrak etanol buah terong lalap ungu termasuk ke dalam kategori
sangat kuat.
1.4Tujuan
Berdasarkan hipotesis diatas, maka tujuan penelitian dalam penelitian ini adalah sebagai berikut:
a. untuk mengetahui karakterisasi simplisia buah terong lalap ungu.
b. untuk mengetahui kandungan golongan senyawa kimia yang terdapat pada simplisia buah terong lalap ungu.
c. untuk mengetahui nilai IC50 dan kategori kekuatan aktivitas antioksidan ekstrak
etanol buah terong lalap ungu.
1.5Manfaat
1.6Kerangka Pikir Penelitian
[image:61.595.109.517.138.605.2]Kerangka pikir penelitian ini dapat dilihat pada Gambar 1.1 dibawah ini: Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Skema kerangka pikir penelitian -Makroskopik -Mikroskopik -Kadar air
-Kadar sari yang larut dalam air
-Kadar sari yang larut dalam etanol
-Kadar abu total -Kadar abu yang tidak
larut dalam asam
-Steroida/triterpenoida -Alkaloid -Glikosida -Flavonoid -Saponin -Tanin Karakteritik simplisia Skrining fitokimia Serbuk simplisia
buah terong lalap ungu Aktivitas antioksidan dengan pemerangkapan radikal bebas DPPH
Nilai IC50
Eksrtak etanol buah terong lalap
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL BUAH
TERONG LALAP UNGU (Solanum melongena L.) ABSTRAK
Buah terong lalap ungu (Solanum melongena L.) yang termasuk suku Solanaceae merupakan salah satu sayuran yang banyak digemari oleh berbagai kalangan. Selain sebagai bahan makanan, secara empiris terong bermanfaat untuk mengobati berbagai penyakit, seperti seperti kanker, hipertensi, hepatitis, diabetes, arthritis, asma dan bronchitis. Kandungan gizi pada terong cukup tinggi, seperti protein, vitamin A, vitamin B, dan vitamin C. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia dan uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu.
Tahapan penelitian meliputi pengambilan bahan tanaman, identifikasi bahan tanaman, pembuatan simplisia, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak etanol dan uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu. Ekstraksi dibuat secara perkolasi dengan pelarut etanol 96%. Uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu diuji dengan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) pada panjang gelombang 516 nm setelah didiamkan selama 60 menit pada suhu kamar.
Hasil karakterisasi simplisia diperoleh kadar air 5,98%, kadar sari yang larut dalam air 24,58%, kadar sari yang larut dalam etanol 19,66%, kadar abu total 4,03%, dan kadar abu tidak larut asam 0,44%. Hasil skrining fitokimia buah terong lalap ungu mengandung senyawa kimia golongan steroida, alkaloid, glikosida, flavonoid, saponin dan tanin. Hasil pengujian aktivitas antioksidan dengan metode pemerangkapan radikal bebas DPPH menunjukkan bahwa ekstrak etanol buah terong lalap ungu memiliki aktivitas antioksidan yang sangat kuat dengan nilai IC50 (inhibitory concentration) yang diperoleh sebesar 40,68 ppm.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING
WITH ANTIOXIDANT ACTIVITY OF ETHANOL EXTRACT OF BUAH TERONG LALAP UNGU (Solanum melongena L.)
ABSTRACT
Buah terong lalap ungu (Solanum melongena L.) of the family Solanaceae is one of fruit vegetable favored by many people. Other than as functional foods, buah terong lalap ungu is usefull for treating several diseases, such us hypertension, hepatitis, diabetes, arthritis, asthma and bronchitis. The nutritional content is quite high content such as protein, vitamin A, vitamin B, and vitamin C. The purpose of the research was to determine the characteristics of simplex, phytochemical screening and to measure the antioxidant activity of extract ethanol of buah terong lalap ungu.
Stage of research include taking a plant, plant identification, making a simplex, simplex characterization, phytochemical screening, manufacture of ethanol extract and to measure the antioxidant activity of extract ethanol of purple eggplant fruit salad. . The extract was prepared by percolation of simplex with 96% ethanol. Then, the antioxidant activity test of extract ethanol of buah terong lalap ungu using DPPH (1,1-diphenyl-2-picrylhydrazil) free radical scavenging method at wave 516 nm after 60 minute of incubation at room temperature.
The results of simplex characterization gave the water content was 5.98%, water-soluble extract content was 24.58%, ethanol-soluble extract content was 19.66%, total ash content was 4.03%, and acid-insoluble ash content was 0.44%. The result of phytochemical screening showed that buah terong lalap ungu content was steroid, alkaloid, glycosides, flavonoid, saponin and tannin. The result of antioxidant activity test using DPPH free radical scavenging method showed that extract ethanol of buah terong lalap ungu exhibited strong antioxidant activity with inhibitory concentration (IC50) is 40.68 ppm.
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL
BUAH TERONG LALAP UNGU (Solanum melongena L.)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FADHILATURRAHMI S
NIM 101501128
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL
BUAH TERONG LALAP UNGU (Solanum melongena L.)
SKRIPSI
OLEH:
FADHILATURRAHMI S
NIM 101501128
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan
karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul Karakterisasi Simplisia dan Skrining Fitokimia serta Uji Aktivitas
Antioksidan Ekstrak Ekstrak Etanol Buah Terong Lalap Ungu (Solanum melongena L). Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Penulis juga mempersembahkan rasa terima kasih yang tak terhingga kepada keluarga tercinta, Ayahanda Surya Bakti dan Ibunda Nur Mawan Tambunan, adik-adikku Muhammad Ridho S dan Rinal Junanda S atas limpahan kasih sayang, doa dan semangat yang tak ternilai.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Juli 2015 Penulis,
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL BUAH
TERONG LALAP UNGU (Solanum melongena L.) ABSTRAK
Buah terong lalap ungu (Solanum melongena L.) yang termasuk suku Solanaceae merupakan salah satu sayuran yang banyak digemari oleh berbagai kalangan. Selain sebagai bahan makanan, secara empiris terong bermanfaat untuk mengobati berbagai penyakit, seperti seperti kanker, hipertensi, hepatitis, diabetes, arthritis, asma dan bronchitis. Kandungan gizi pada terong cukup tinggi, seperti protein, vitamin A, vitamin B, dan vitamin C. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia dan uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu.
Tahapan penelitian meliputi pengambilan bahan tanaman, identifikasi bahan tanaman, pembuatan simplisia, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak etanol dan uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu. Ekstraksi dibuat secara perkolasi dengan pelarut etanol 96%. Uji aktivitas antioksidan ekstrak etanol buah terong lalap ungu diuji dengan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) pada panjang gelombang 516 nm setelah didiamkan selama 60 menit pada suhu kamar.
Hasil karakterisasi simplisia diperoleh kadar air 5,98%, kadar sari yang larut dalam air 24,58%, kadar sari yang larut dalam etanol 19,66%, kadar abu total 4,03%, dan kadar abu tidak larut asam 0,44%. Hasil skrining fitokimia buah terong lalap ungu mengandung senyawa kimia golongan steroida, alkaloid, glikosida, flavonoid, saponin dan tanin. Hasil pengujian aktivitas antioksidan dengan metode pemerangkapan radikal bebas DPPH menunjukkan bahwa ekstrak etanol buah terong lalap ungu memiliki aktivitas antioksidan yang sangat kuat dengan nilai IC50 (inhibitory concentration) yang diperoleh sebesar 40,68 ppm.
Gambar

Dokumen terkait
Uji aktivitas antioksidan terhadap ekstrak etanol dan jus daging buah salak dilakukan dengan metode pemerangkapan radikal bebas 1,1 -diphenyl- 2 -picrylhydrazil (DPPH)
skrining fitokimia dan uji aktivitas antioksidan terhadap ekstrak etanol buah naga dan sari buah naga segar dengan metode penangkapan radikal bebas 1,1-diphenyl-
Pengujian aktivitas antioksidan ekstrak air dan ekstrak etanol hidrilla menggunakan metode pemerangkapan radikal bebas DPPH ( 1,1-diphenyl-2- picrylhydrazil ) setelah didiamkan
Hasil pengujian aktivitas antioksidan dengan metode pemerangkapan radikal bebas DPPH menunjukkan bahwa ekstrak etanol buah terong lalap ungu memiliki aktivitas antioksidan
Pengujian aktivitas antioksidan dari ekstrak daun kari menggunakan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) setelah pendiaman 60 menit pada suhu kamar
Manfaat dari penelitian ini adalah dapat memberikan informasi tentang karakteristik simplisia dan golongan senyawa kimia buah terong lalap ungu, serta dapat menambah
The Use of the Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity.. Antioksidan dan Kiat Sehat di Usia
Lampiran 7.Perhitungan pemeriksaan karakteristik serbuk simplisia buah terong lalap ungu ( Solanum melongena L.). Penetapan