LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. Kimia Farma (
Persero
) Tbk, Plant Jakarta
Jl. Rawagelam V No. 1 Kawasan Industri Pulogadung Jakarta Timur
05 Mei – 16 Mei 2008
Disusun oleh:
Ainul Mardiah (073202006)
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2008
Lembar Pengesahan
LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. Kimia Farma (
Persero
) Tbk
Plant Jakarta
Jl. Rawagelam V No. 1 Kawasan Industri Pulogadung Jakarta Timur
05 Mei – 16 Mei 2008
Laporan ini disusun untuk melengkapi salah satu syarat untuk memperoleh gelar
Apoteker pada Fakultas Farmasi Universitas Sumatera Utara Medan
Disusun oleh:
Ainul Mardiah, S. Si (073202006) Lady Balqis Ali, S. Farm (073202050) Rafiqoh Parinduri, S. Farm (073202073) Sri Wati, S. Farm (073202098)
PT. Kimia Farma (persero) Tbk Plant Jakarta
Disetujui oleh:
Drs. Herry Rustanto, Apt Dra. Tia Mutianingsih, Apt
Pembimbing PT. Kimia Farmasi Plant Jakarta Pembimbing PT. Kimia Farmasi Plant Jakarta
Fakultas Farmasi Universitas Sumatera Utara
Dekan
KATA PENGANTAR
Puji Syukur Alhamdulillah kami panjatkan kepada Tuhan Yang Maha
Esa, atas Berkat Rahmat-Nya sehingga Praktek Kerja Profesi Apoteker ( PKPA)
di PT. Kimia Farma (Persero) Tbk, Plant Jakarta pada tanggal 05 Mei 2008
sampai dengan 16 Mei 2008 telah dilaksanakan dengan baik.
Kerja Praktek Profesi Apoteker di PT. Kimia Farma (Persero) Tbk, Plant
Jakarta merupakan salah satu syarat yang harus dipenuhi untuk memperoleh gelar
apoteker di Fakultas Farmasi Universitas Sumatera Utara dengan harapan agar
setiap calon apoteker mendapatkan pengalaman dan pengetahuan tentang peran
apoteker di Industri Farmasi.
Pada kesempatan ini kami mengucapkan banyak terima kasih kepada
Bapak Drs. Herry Rustanto, Apt, dan Ibu Dra. Tia Mutianingsih, Apt, sebagai
pembimbing yang telah meluangkan waktu untuk memberikan bimbingan moril
dan pengatahuan kepada kami selama pelaksanaan PKPA di PT. Kimia Farma
(Persero) Tbk, Plant Jakarta. Dan kami turut mengucapkan banyak terima yang
sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara.
2. Bapak Drs. Wiryanto, M.Si, Apt., selaku Koordinator Program
Pendidikan Profesi Apoteker Universitas Sumatera Utara .
3. Bapak Drs. Abdul Manan, Apt., selaku Plant Manager Jakarta yang telah
memberikan tempat bagi kami dalam melaksanakan Praktek Kerja Profesi
4. Seluruh Staf dan Karyawan/ Karyawati PT. Kimia Farma (Persero) Tbk,
Plant Jakarta, yang telah banyak meluangkan waktunya untuk memberikan
bantuan informasi selama pelaksanaan PKPA ini.
5. Teman – teman Profesi Apoteker Stambuk 2007, terima kasih atas segala
bantuan dan motivasi yang telah diberikan
6. Semua pihak yang banyak memberikan bantuan baik moril maupun
materiil yang tidak dapat disebutkan satu persatu.
Kami berharap semoga pengetahuan dan pengalaman yang kami peroleh
selama kami menjalani PKPA ini dapat bermanfaat bagi rekan – rekan dan semua
pihak yang membutuhkan khususnya buat kalangan Profesi Apoteker.
Penulis menyadari bahwa laporan ini masih jauh dari sempurna, seperti
kata pepatah mengatakan Tak Ada Gading Yang Tak Retak oleh karena itu
penulis mengharapkan masukan , kritik dan saran dari pembaca bagi profesi
kefarmasian yang akan datang.
Jakarta, juli 2008
Penulis
DAFTAR ISI
2.3. Lokasi Industri Farmasi PT. Kimia Farma (Persero), Tbk ……….. 6
2.3.1. Lima Plant PT. Kimia Farma (Persero) Tbk …. 7 2.3.2. Struktur Organisasi ………... 8
2.4. Cara Pembuatan Obat yang Baik (CPOB) ……… 10
BAB III.KEGIATAN DIINDUSTRI FARMASI ……….. 22
3.1. Keterlibatan Dalam Produksi ……… 22
3.2. Bagian Penyimpanan ……… 25
3.3. Bagian Produksi ……… 28
3.4. Bagian Pengelolahan Mutu dan Validasi ………. 41
3.5. Keselamatan, Kesehatan Kerja dan Lingkungan …….. 46
BAB IV. PEMBAHASAN ……… 52
BAB V. KESIMPULAN DAN SARAN ……….. 57
5.1. Kesimpulan ……….. 57
5.2. Saran ……… 57
DAFTAR GAMBAR
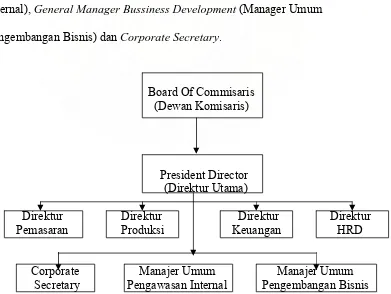
1. Struktur Organisasi PT. Kimia Farma (Persero) Tbk………..8
DAFTAR LAMPIRAN
1. Struktur Organisasi PPPI
(Perencanaan Pengendalian Produksi Dan Lingkungan…...……….59
2. Struktur Organisasi Bagian Produksi………60
3. Sruktur Organisasi Bagian Pengolahan Mutu………61
4. Struktur Organisasi Bagian Penyimpanan……….62
5. Alur Produksi Bagian Formulasi I……….63
6. Alur Proses Produksi Narkotika……….64
7. Alur Proses Produksi Bagian Formulasi II……….65
8. Alur Proses Sediaan Kapsul Bagian Formulasi III………66
9. Alur Proses Sediaan Injeksi Bagian Formulasi III………67
10.Alur Proses Sediaan Sirup Kering Bagian Formulasi III………..68
11..Alur Proses Sediaan Krim Bagian Formulasi III……….69
12.Alur Proses Produksi Tablet Dan Kapsul Betalaktam………..70
13.Bagan Proses Pengemasan………71
14.Alur Proses Produksi Sirup Kering Betalaktam………72
15.Skema Proses Pengolahan Air………..73
16.Alur Proses Produksi (Penerimaan Dan Penggunaan Bahan Baku Serta Bahan Pengemas)…..74
17.Alur Proses Produksi (Penerimaan Dan Penggunaan Bahan Baku Serta Bahan Pengemas, lanjutan)………..………..75
19.Upaya Pengolahan Limbah………77
20.Denah Bangunan PT. Kimia Farma (Persero) Tbk, Plant Jakarta……….78
21.Denah Bangunan PT. Kimia Farma (Persero) Tbk, Plant
BAB I
PENDAHULUAN
1.1. Latar Belakang
Kesehatan merupakan hak setiap warga Negara. Setiap orang mempunyai
hak untuk hidup layak, baik dalam kesehatan pribadi maupun keluarganya
termasuk didalamnya mendapatkan makanan, pakaian, perumahan dan pelayanan
sosial yang diperlukan.
Berdasarkan Undang – Undang Republik Indonesia No. 23 tahun 1992
tentang kesehatan, yang dimaksud dengan sehat adalah keadaan sejahtera dari
badan, jiwa dan sosial yang memungkinkan setiap orang hidup produktif secara
sosial dan ekonomi. Pembangunan kesehatan diarahkan guna mencapai kesadaran,
kemauan, dan kemampuan untuk hidup sehat bagi masyarakat agar dapat
mewujudkan derajat kesehatan yang optimal. Untuk dapat mencapai upaya, yaitu
peningkatan kesehatan (promotif), pencegahan penyakit (preventif),
penyembuhan penyakit (kuratif) dan pemulihan kesehatan (rehabilitatif).
Dalam menyelenggarakan upaya – upaya tersebut, maka diperlukan
sarana – sarana yang mendukung. Menurut Undang – Undang Republik Indonesia
No. 23 tahun 1992 pasal 56, salah satu sarana kesehatan adalah pabrik obat atau
industri farmasi. Industri farmasi sebagai salah satu sarana kesehatan adalah
tempat untuk melaksanakan pekerjaan kefarmasian, antara lain pembuatan obat,
pengendalian mutu, pengamanan pengadaan, penyimpanan dan distribusi obat.
Salah satu langkah utama yang dilakukan industri farmasi dalam upaya
dengan yang telah ditentukan serta sesuai dengan tujuan penggunaannya adalah
dengan menerapkan Pedoman Cara Pembuatan Obat Yang Baik (CPOB). Jaminan
mutu suatu produk obat jadi tidak hanya sekedar lulus dari serangkaian pengujian
akan tetapi mutu harus dibentuk atau dibangun pada seluruh tahapan proses
produksi dari awal sampai akhir. Oleh sebab itu, pelaksanaan CPOB harus
diterapkan pada seluruh aspek produksi dan pengendalian mutu.
Pengembangan produksi yang dilakukan PT. Kimia Farma (Persero) Tbk.
Plant Jakarta adalah dengan terus meningkatkan kualitas produk yang dihasilkan
dan meningkatkan jumlah produk yang memiliki sertifikat CPOB. PT. Kimia
Farma (Persero) Pant Jakarta selain mengupayakan pengembangan dan perbaikan
dalam aspek produksi juga dilakukan pada aspek sumber daya manusia.
Pengembangan aspek kualitas sumber daya manusia dilakukan dengan
memberikan kesempatan bagi personilnya untuk mengikuti pelatihan ataupun
seminar yang menunjang kemampuan dan keterampilan.
Industri farmasi merupakan institusi yang memiliki dwi fungsi yaitu unit
pelayanan kesehatan (non frofit oriented) dan sebagai institusi bisnis (profit
oriented). Industri farmasi merupakan tempat memproduksi obat jadi atau bahan
baku obat. Obat yang dibuat harus memiliki mutu tinggi dan kualitas yang baik.
Industri farmasi selain dapat sebagai unit usaha yang memproduksi obat
untukkebutuhan masyarakat, juga mempunyai peran yang sangat strategis dalam
menyediakan obat, karena obat merupakan salah satu komoditi dibidang
kesehatan yang sangat penting.
Praktek Kerja Profesi Apoteker di industri farmasi secara langsung dapat
dapat menilai sampai sejauh mana peran farmasis di industri obat. Kendala yang
biasa dihadapi oleh para farmasis selaku penanggung jawab dalam menegakan
profesionalismenya dalam lingkungan yang cenderung selalu berfikir tentang
profit oriented dan bukan patient oriented. Praktek kerja lapangan ini diharapkan
dapat memberikan gambaran dan wacana tentang atmosfer lingkungan industri
farmasi.
Universitas adalah sarana pencetak apoteker, sejak awal sudah harus
mempersiapkan lulusannya sehingga mempunyai wawasan dan pengetahuan yang
cukup untuk bisa berperan dan memberikan andil dalam menjalankan profesinya
diindustri farmasi. Aspek teoritis yang kuat dan ditunjang dengan aspek prakstis
yang diharapkan dapat mencetak lulusan tang berkualitas. Sehubungan dengan itu
maka Program Pendidikan Profesi Apoteker Universitas Sumatera Utara menjalin
kerja sama dengan PT. Kimia Farma (Persero) Tbk Plant Jakarta,
menyelenggarakan Praktek Kerja Profesi Apoteker yang dimulai dari tanggal 05
Mei 2008 sampai dengan tanggal 16 Mei 2008, dengan adanya Praktek Kerja
Profesi Apoteker di industri farmasi diharapkan mahasiswa Profesi Apoteker
mampu menerapkan ilmu yang diperoleh saat kuliah dan mendapatkan
pengetahuan praktis lainnya yang bermanfaat sebagai panduan dan tolak ukur
1.2. Tujuan
Tujuan Praktek Kerja Profesi Apoteker di Industri PT. Kimia Farma
(Persero) Tbk. Plant Jakarta adalah :
1. Mempersiapkan Apoteker untuk menjalani profesinya secara professional,
handal, dan mandiri serta mampu menghadapi tantangan dimasa yang akan
datang.
2. Memberikan gambaran tentang struktur organisasi, tugas dan fungsi
Apoteker, situasi dan kondisi di Industri PT. Kimia Farma (Persero) Tbk.
Plant Jakarta.
3. Mempelajari, memahami, mengetahui, tugas dan tangng jawab Apoteker
di Industri farmasi PT. Kimia Farma (Persero) Tbk. Plant Jakarta baik
BAB II
TINJAUAN UMUM INDUSTRI FARMASI
2.1. Sejarah
Industri adalah kegiatan memproses atau mengolahan barang dengan
menggunakan sarana dan peralatan, misalkan mesin, dalam pengertian bisnis,
Industri adalah himpunan perusahaan yang memproduksi barang-barang yang
bersifat substitusi dekat atau (closed substitute) yang memiliki nilai permintaan
silang yang relatif tinggi.
Industri farmasi menurut Surat Keputusan Mentri Kesehatan No.
245/MenKes/V/1990 adalah indutri obat jadi adalah industri yang menghasilkan
suatu produk yang telah melalui seluruh tahap proses pembuatan. Obat jadi
tersebut dapat berupa sediaan atau paduan bahan-bahan yang siap dipergunakan
untuk mempengaruhi atau menyelidiki sistem fisiologi atau keadaan patologi
dalam rangka penetapan diagnosis, pencegahan, penyembuhan, pemulihan,
peningkatan kesehatan dan kontrasepsi. Sedangkan industri bahan baku adalah
bahan yang diproduksi oleh suatu industri, diamana bahan baku tersebut adalah
semua bahan baik yang berkhasiat ataupun yang tidak berkhasiat yang digunakan
dalam proses penggunaan obat.
Menurut Surat Keputusan Mentri Kesehatan No. 245/MenKes/V/1990
usaha industri farmasi wajib memenuhi persyaratan sebagai berikut:
1. Didirikan oleh perusahaan umum (Perum), badan hukum berbentuk
perseroaan terbatas (PT) dan kopersai.
3. Memiliki Nomor Pokok Wajib Pajak (NPWP)
4. Memenuhi persyaratan Cara Pembuatan Obat Yang Baik (CPOB) sesuai
dengan SK MenKes No. 43/ MenKes/SK/II/1988 tentang pedoman CPOB.
5. Wajib mempekerjakan sekurang-kurangnya dua orang Apoteker Warga
Negara Indonesia (WNI), yang masing-masing sebagai penanggung jawab
pengawasan mutu dan penanggung jawab pengawasan produksi.
6. Obat jadi yang diproduksi oleh perusahaan Industri farmasi hanya boleh
diedarkan setelah mendapat persetujuan sesuai dengan ketentuan
perundang-undangan yang berlaku.
2.2 Visi dan Misi
A. Visi Industri Farmasi Indonesia menurut SK MenKes No. 47/SK/II/1983
adalah:
1. Upaya dibidang obat harus memperhatikan aspek sosial dan diarahkan
untuk mendukung peningkatan dan pemantapan upaya kesehatan.
2. Mengusahakan kemandirian dibidang obat, khususnya bahan baku obat
dengan jalan:
a. Mempercepat dan memperlancar transfer teknologi serta
meningkatkan kemampuan pengembangan teknologi.
b. Memberikan perlindungan yang wajar terhadap obat produksi
dalam negeri.
c. Penelitian dan pengembangan bahan baku dalam negeri dan
B. Misi Industri Farmasi Indonesia menurut SK MenKes No. 47/SK/II/1983
adalah:
1. Meningkatkan tersedianya dengan jenis dan jumlah yang cukup sesuai
dengan kebutuhan nyata masyarakat yang diperlukan dalam kesehatan.
2. Meningkatkan penyebaran obat secara merata dan teratur sehingga
mudah diperoleh pada saat yang diperlukan serta terjangkau oleh
masyarakat.
3. Menjamin kebenaran khasiat, keamanan, mutu dan keabsahan obat
yang beredar serta meningkatan ketepatan, kerasionalan dan efesiensi
penggunaan obat
4. Memanfaatkan potensi nasional deibidang obat menunjang
pembangunan ekonomi menuju tercapainya kemandirian dibidang
obat.
2.3. Lokasi Industri Farmasi PT. Kimia Farma (Persero) Tbk
PT. Kimia Farma (Persero) Tbk. Plant Jakarta berlokasi di JL.Rawagelam
V No. 1 Kawasan Industri Pulogadung Jakarta Timur. PT. Kimia Farma (Persero)
Tbk. Plant Jakarta mempunyai area seluas 35.000 m2, dengan area bangunan
untuk non betalaktam seluas 11,225 m2, sumber air yang digunakan berasal dari
perusahaan Air Minum (PAM)dan air artesis sedangkan sumber listrik yang
digunakan berasal dari Perusahaan Listrik Negara (PLN)dan sebagai cadangan
digunakan Generator Set. Sumber udara untuk setiap ruangan menggunakan Air
Bangunan pabrik PT. Kimia Farma (Persero) Tbk. Plant Jakarta yang
mencapai luas 35.000 m2 meliputi :
1. Gedung Perkantoran
Bangunan untuk perkantoran terletak di bagian depan yang terdiri dari dua
lantai. Pada lantai pertama terdapat lobi, masjid, koperasi, poliklinik, dapur
dan kantin. Pada lantai dua terdapat ruang Plant Manager, ruang Manager
Produksi, ruang Manager PPPI, ruang administrasi keuangan, ruang
personalia, ruang pembelian dan ruang rapat.
2. Gedung Produksi Non Betalaktam
Bangunan yang terletak dibelakang perkantoran dimana pada lantai satu
digunakan untuk produksi non betalaktam, produk steril, penyimpanan bahan
baku dan bahan pengemas. Lantaidua digunakan sebagai laboratorium
pengujian, dokumentasi, penyimpanan contoh pertinggal, teknologi
formulasi, pemastian mutu, dan perpustakaan.
3. Gedung Produksi Betalaktam
Bangunan untuk produksi betalaktam merupakan gedung yang terpisah yang
terdiri dari dua lantai. Lantai satu dipakai untuk produksi dan lantai dua
dipakai untuk ruang pengemasan sediaan.
4. Instalasi Pengolahan Air Limbah
Unit pengolahan limbah, terdiri dari dua bagian yaitu pengolahan limbah
betalaktam dan non betalaktam.
5. Bangunan Pelengkap
Bangunan ini terdiri dari generator diesel, penampungan air
2.3.1. Lima Plant PT. Kimia Farma (Persero) Tbk yaitu:
1. Plant Jakarta
Memproduksi obat dalam bentuk sediaan tablet, tablet salut, kapsul, granul,
sirup kering, suspensi/sirup, tetes mata, cream antibiotik dan injeksi. Unit ini
satu-satunya pabrik obat yang mendapat tugas oleh pemerintah untuk
memproduksi golongan narkotik di Indonesia. Unit produksi ini telah
memperoleh sertifikat CPOB dan ISO- 9001.
2. Plant Bandung
Memproduksi bahan baku Kina dan turunanya, dan Alat Kontrasepsi Dalam
Rahim (AKDR) serta obat asli Indonesia seperti Batugin Elixir dan
Enkasari. Unit ini juga memproduksi tablet, sirup, serbuk, dan produk
kontrasepsi Pil Keluarga Berencana. Unit produksi ini telah menerima
sertifikat CPOB dan ISO-9001.
3. Plant Semarang
. Unit Produksi ini mengkhususkan diri memproduksi minyak jarak,
pemurnian minyak nabati seperti minyak kelapa, minyak kelapa sawit,
minyak kedelai, minyak kacang serta kosmetika dalam bentuk serbuk/bedak.
Unit produksi ini menjamin kualitas hasil produksi dengan menerapkan
system manajemen mutu ISO-9001, serta telah mendapat sertifikat CPOB
4. Plant Watudakon (Jombang), Jawa Timur
Satu-satunya pabrik yang mengolah tambang yodium di Indonesia. Unit ini
memproduksi yodium dan garam-garamnya, bahan baku ferro sulfat sebagai
lunak “Yodiol” yang merupakan obat pilihan untuk pencegahan gondok.
Unit ini telah memproduksi sertifikat CPOB, ISO-9001 dan ISO-14001.
5. Plant Tanjung Morawa ( Medan), Sumatera Utara.
Unit ini khusus untuk memasok kebutuhan obat di wilayah Sumatera.
Produk yang dihasilkan pabrik berupa sediaan tablet, cream, dan kapsul
dalam skala kecil. Plant ini telah memperoleh sertifikat CPOB.
2.3.2 Struktur Organisasi
A. Struktur Organisasi PT. Kimia Farma (Persero) Tbk.
PT. Kimia Farma (Persero) Tbk, dipimpin oleh seorang Direktur Utama,
dibantu oleh 4 Direktur yaitu: Direktur Produksi, Direktur Pemasaran, Direktur
Keuangan, Direktur Umum. Selain direktur utama dibantu juga oleh beberapa
staff, yaitu: General Manager Internal Control (Manager Umum Pengawasan
Internal), General Manager Bussiness Development (Manager Umum
Pengembangan Bisnis) dan Corporate Secretary.
Board Of Commisaris
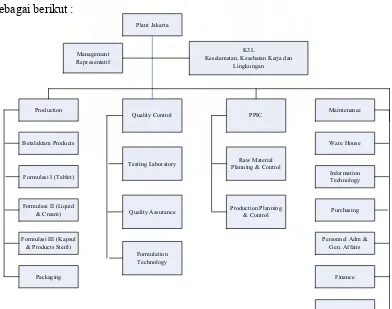
B. Struktur Organisasi PT. Kimia Farma (Persero)Tbk. Plant Jakarta
PT. Kimia Farma (Persero) Tbk. Plant Jakarta dipimpin oleh Plant
Manager yang langsung membawahi Bagian Produksi, Pengelolaan Mutu,
Perencanaan Pengendalian Produksi dan Inventori (PPPI), Bagian
Administrasi/Keuangan, Bagian Pembelian, Bagian Umum Personalia dan Bagian
Teknik Pemeliharaan.
Selain itu terdapat juga beberapa jabatan fungsionl seperti Management
Representative, bagian Kesehatan Keselamatan Kerja dan Lingkungan (K3L).
Jabatan-jabatan ini bekerja secara koordinatif, yang berada langsung dibawah
Plant Jakarta.
Plant Jakarta
Management Representatif
K3L
Keselamatan, Kesehatan Kerja dan Lingkungan
Bagan struktur organisasi PT. Kimia Farma (Persero) Tbk. Plant Jakarta adalah
sebagai berikut :
2.3 Cara Pembuatan Obat yang Baik (CPOB) a. Ketentuan Umum
Cara Pembuatan Obat Yang Baik (CPOB) menyangkut seluruh aspek
produksi dan pengendalian mutu, bertujuan untuk menjamin mutu yang telah
disesuaikan dengan tujuan penggunaannya.
Ketentuan umum memuat beberapa landasan yang penting diperhatikan
yaitu:
1. Pengawasan menyeluruh pada proses pembuatan obat untuk menjamin
bahwa konsumen obat yang bermutu tinggi. Pengawasan menyeluruh
merupakan salah satu kegiatan yang sangat esensial pada pembuatan obat.
2. Untuk menjamin mutu suatu obat jadi tidak boleh hanya mengandalkan pada
suatu pengujian tertentu saja. Mutu obat harus dibangun dalam produk obat
itu sendiri. Mutu obat tergantung mutu bangunan, peralatan dan personalia
yang terlibat.
3. CPOB merupakan pedoman yang dibuat untuk memastikan agar sifat dan
mutu obat yang dihasilkan sesuai dengan syarat bahwa standar mutu obat
yang telah ditentukan telah tercapai.
b. Personalia
Kualitas sediaan obat yang dihasilkan ditentukan oleh beberapa faktor
penunjang, salah satu faktor terpenting adalah faktor manusia. Oleh karena alur
produksi hanya bisa terjadi jika personil yang mengerjakannya mempunyai
kualitas yang sesuai dengan tingkat pendidikan dan pengalamannya.
Jumlah karyawan disemua tingkatan hendaklah cukup serta memiliki
kesehatan mental dan fisik yang baik sehingga mampu melaksanakan tugasnya
secara professional dan sebagaimana mestinya. Mereka hendaklah mempunyai
sikap dan kesadaran tinggi untuk mewujudkan CPOB. Hal-hal yang perlu
diperhatikan dalam aspek ini adalah:
1. Organisasi dan tanggung jawab
Dalam perusahaan, struktur organisasi disusun sedemikian rupa sehingga
bagian pengawasan mutu dipimpin oleh orang yang berbeda yang tidak saling
bertanggung jawab satu terhadap lain. Masing-masing hendaklah diberi
wewenang penuh dan sarana yang cukup yang diperlukan untuk melaksanakan
tugasnya secara efektif. Keduanya tidak dapat menghambat atau membatasi
tanggung jawabnya atau yang dapat menimbulkan pertentangan kepentingan
pribadi atau financial.
Manajer Produksi dan Pengawasan Mutu hendaklah seorang Apoteker
yang cakap, terlatih dan memiliki pengalaman praktis dan memadai di bidang
industri farmasi dan keterampilan dalam kepemimpinan sehingga memungkinkan
melaksanakan tugas secara professional.
Manajer Produksi hendaklah memiliki wewenang serta tanggung jawab
penuh untuk mengelola produksi obat. Manajer Produksi hendaklah memiliki
tanggung jawab bersama dalam menjaga mutu obat, baik dengan Manajer
Pengawasan Mutu maupun Manajer teknik.
Manajer Pengawasan Mutu hendaklah diberi wewenang dan tanggung
jawab penuh dalam seluruh tugas pengawasan mutu yaitu dalam penyusunan,
verifikasi dan pelaksanaan seluruh prosedur pengawasan mutu. Manajer
meluluskan bahan awal produk antara, produk ruahan dan obat jadi bila produk
sesuai dengan spesifikasinya, atau menolaknya bila tidak cocok dengan
spesifikasinya atau bila tidak dibuat dengan prosedur yang tidak disetujui kondisi
yang ditentukan.
2. Pelatihan
Seluruh karyawan yang berhubungan langsung dengan proses pembuatan
obat hendaklah dilatih mengenai kegiatan tertentu yang sesuai dengan tugasnya
maupun mengenai prinsip CPOB. Pelatihan hendaklah diberikan olah tenaga
kompoten. Pelatihan khusus hendaklah bagi mereka yang berkerja didaerah steril
dan daerah bersih atau bagi mereka yang bekerja menggunakan bahan yang
mempunyai resiko tinggi,toksik atau yang menimbulkan sensitifisasi.
Latihan mengenai CPOB harus dilakukan secara berkesinambungan dan
dengan frekuensi yang memadai untuk menjamin agar para karyawan terbiasa
dengan persyaratan dengan CPOB yang berkaitan dengan tugasnya. Pelatihan
mengenai CPOB dilaksanakan menurut program tertulis yang telah disetujui oleh
Manajer Produksi dan Manajer Pengawasan.
Catatan pelatihan karyawan mengenai CPOB hendaklah disimpan dan
efektifitas program pelatihan dinilai secara berkala. Setelah mengadakan
pelatihan, pelatihan karyawan hendaklah dinilai untuk menentukan apakah mereka
memilki kualifikasi yang memadai untuk melaksanakan tugas yang diberikan
3. Bangunan dan Fasilitas
Bangunan untuk produksi obat-obatan hendaklah memiliki ukuran,
rancangan konstruksi dan letak yang memadai untuk mencegah bahan yang dapat
meiliki kualitas dan hendaknya memberikan kondisi lingkunagan yang sesuai,
karena akan mempengaruhi kelancaran kerja. Letak bangunan dibuat cukup tinggi
agar terhindar dari banjir dan dilengkapi dengan saluran pembuangan air.
Beberap persyartan yang perlu diperhatikan pada bangunan industri
farmasi, antara lain:
1. Pabrik ditata sedemikian rupa untuk mencegah kekacauan dan kemungkinan
pencemaran silang serta tercampurnya obat, komponen , dan bahan
pengemas ysang berlainan.
2. Sekat ruangan hendaknya digunakan untuk mencegah pencemaran atau
kasalahan.
3. Diperlukan pemisahan ruangan untuk kegiatan tertentu sesuai dengan fungsi
kegiatan produksi.
4. Ruangan yang diperlukan untuk pembutan steril harus terpisah dari kegiatan
lainnya.
5. Untuk daerah produksi, permukaan bagian dalam ruangan (dinding, lantai,
dan langit-langit) harus licin, bebas dari keretakan dan sambungan terbuka,
mudah didesinfeksi dan dibersihkan. Lantai dibuat dari bahan kedap air,
permukaan rata, dan mudah dibersihkan.
6. Daerah penyimpanan hendaknya diatur sedemikian rupa, sehingga
memungkinkan penyimpanan bahan dan produk dalam keadaan kering,
bahan yang mudah terbakar, yang mudah meledak, yang sangat beracun,
narkotika dan bahan berbahaya lain serta untuk produk atau bahan yang
ditolak..
Berdasarkan kelompok kegiatan dan tingkat kebersihannya, maka tata
ruang bangunan industri farmasi terdiri atas:
1. White area (Daerah putih), termasuk kelas I dan II. Untuk kelas I, jumlah
partikel maksimum permeter kubik (m3) sebanyak 3.500 sedangkan untuk
kelas II jumlah partikel maksimum permeter kubik (m3) sebanyak 350.000.
Meliputi ruang penyaringan steril, pengolahan, pengisian salep mata,
pengisian injeksi, pengolahan aseptis, dan pengisian bubuk steril.
2. Grey area ( Daerah abu-abu), termasuk kelas III dimana, jumlah partikel
permeter kubik (m3) sebanyak 3.500.000. Meliputi ruang pengolahan dan
pengemasan obat nonsteril dan ruang pembuatan salep selain salep mata.
3. Black area (Daerah hitam) termasuk kelas IV yang meliputi ruang ganti
pakaian, ruang masuk, kantor penerimaan bahan awal, gudang bahan
awaldan obat jadi, ruang generator, ruang makan, ruang istirahat, dan toilet.
c. Peralatan
Peralatan yang digunakan dalam pembuatan obat hendaklah memiliki
rancangan bangunan dan konstruksi yang tepat, ukuran yang memadai, dan
ditempatkan dengan tepat, sehingga mutu setiap produk terjamin secara seragam
Rancangan bangunan dan konstruksi peralatan hendaklah memenuhi
persyaratan sebagai berikut:
1. Permukaan peralatan yang bersentuhan dengan bahan baku, produk antara,
produk jadi tidak boleh bereaksi. Mengadisi atau mengabsorbsi, yang dapat
mengubah identitas, mutu atau kemurniannya diluar batas yang ditentukan.
2. Peralatan tidak boleh menimbulkan akibat yang merugikan terhadap produk.
3. Bahan-bahan yang diperlukan untuk suatu tujuan khusus, seperti pelumas atau
pendingin tidak boleh bersentuhan langsung dengan bahan yang diolah.
4. Peralatan hendaknya dapat dibersihkan dengan mudah, baik bagian dalam
maupun bagian luar.
5. Peralatan yang digunakan untuk menimbang, mengukur, menguji, dan
mencatat hendaklah diperiksa ketelitiannya secara teratur serta dikalibrasi
menurut suatu program dan prosedur yang tepat.
6. Peralatan hendaknya dirawat sesuai dengan jadwal yang tepat.
7. Alat-alat harus dikalibrasi dan divalidasi untuk menjamin kelancaran kerja.
8. Daerah yang digunakan sebagai tempat penyimpanan bahan yang mudah
terbakar hendaklah dilengkapi dengan perlengkapan elektris yang eksploisasi
serta dibumikan dengan sempurna.
d. Sanitasi dan Higiene
Sanitasi dan Higiene mutlak diperlukan dalam setiap aspek pembuatan
obat Ruang lingkup sanitasi dan hygiene meliputi semua sumber pencemaran
produk seperti personalia, bangunan, peralatan, bahan awlal serta wadahnya.
Sumber pencemaran hendaklah dihilangkan dengan program sanitasi dan
1. Personalia
Seluruh karyawan hendaknya menjalani kesehatan baik sebelum maupun
setelah diterima sebagai karyawan selama bekerja. Higiene perorangan harus
dilatih dan diterapkan semua karyawan yang berhubungan dengan proses
produksi, dan semua karyawan hendaknya menghindari untuk bersentuhan
langsung dengan produksi, sehingga diperlukan pakaian pengaman yang
memadai dan sesuai dengan tugasnya.
2. Bangunan
Bangunan yang digunakan untuk pembuatan obat hendaknya dirancang dan
dibangun dengan tepat untuk memudahkan pelaksanaan sanitasi yang baik.
Bangunan hendaknya dilengkapi fasilitas sanitasi yang memadai seperti
toilet, loker, bak cuci, tempat penyimpanan bahan pembersih, insektisida,
bahan fungi dan lain-lain. Hendaknya disusun pula suatu prosedur yang
merupakan prosedur tetap untuk melaksanakan sanitasi dengan jadwal yang
teratur, serta diuraikan dengan cukup rinci.
3. Peralatan.
Peralatan harus dibersihkan sebelum dan sesudah digunakan sesuai prosedur
yang telah ditetapkan. Suatu prosedur yang dirinci untuk pembersihan dan
sanitasi peralatan sekurang-kurangnya meliputi penanggung jawab, jadwal,
metode, peralatan dan bahan yang dipakai dalam pembersihan, merupakan
prosedur tetap untuk melaksanakan sanitasi dengan jadwal yang teratur yang
tidak bersamaan dengan jadwal produksi. Selain itu prosedur sanitasi dengan
bahwa seluruh prosedur telah memenuhi syarat dan telah dilakukan secara
efektif.
e Produksi
Produksi obat-obatan hendaklah dilaksanakan sesuai dengan prosedur
yang telah ditetapkan agar senantiasa diperoleh obat jadi yang memenuhi
spesifikasi yang ditentukan. Aspek-aspek yang harus diperhatikan dalam kegiatan
produk meliputi:
1. Bahan awal
Pemeriksaan bahan awal dilakukan oleh bagian pemastian mutu berdasarkan
spesifikasi yang ditentukan dan dikarantina, sampai diluluskan untuk
dipakai. Bahan awal yang tidak memenuhi syarat disimpan terpisah untuk
dikembalikan kepada pemasok atau dimusnahkan.
2. Validasi proses
Semua prosedur produksi hendaklah divalidasi dengan tetap dan
dilaksanakan menurut prosedur yang telah ditentukan. Proses dan prosedur
tersebut hendaknya secara rutin dievaluasi ulang untuk memastikan bahwa
proses dan prosedur tetap mampu memberikan hasil yang diinginkan.
3. Pencemaran.
Pencemaran kimiawi atau mikroba terhadap suatu obat yang dapat
merugikan kesehatan atau mempengaruhi daya terapeutik serta
mempengaruhi kualitas produk tidak dapat diterima. Perhatian khusus
hendaklah diberikan pada masalah pencemaran silang, karena sekalipun sifat
dan tingkatanya tidak berpengaruh langsung pada kesehatan, hal ini
4. Sistem penomoran batch atau lot
Suatu system yang menjabarkan cara penomoran batch dan lot secara rinci
diperlukan untuk memastikan bahwa produk antara, produk ruahan atau
obat jadi suatu batch dan lot dapat dikenali dengan nomor batch dan lot
tertentu tidak digunakan secara berulang
5. Penimbangan dan penyerahan
Penimbangan atau perhitungan dan penyerhan bahan baku, bahan pengemas,
produk antara dan produk ruahan dianggap suatu bagian dari siklus produksi
dan memerlukan dokumentasi yang lengkap
6. Pengembalian
Semua bahan baku, bahan pengemas, produk antara dan produk ruahan yang
dikembalikan ketempat penyimpanan hendaklah didokumentasikan dan
dicek dengan baik. Bahan-bahan tersebut tidak boleh dikembalikan kecuali
memenuhi spesifikasi yang ditetapkan.
7. Pengelolaan
Pemeriksaan awal pada pengolahan baik bahan, kondisi daerah pengolahan,
wadah dan peralatan harus mengikuti prosedur tertulis yang telah ditetapkan.
Pencegahan pencemaran silang dalam seluruh tahap pengolahan.
8. Produk steril
Produk steril hendaklah dibuat dengan pengawasan khusus untuk
menghilangkan pencemaran mikroba dan partikel lain. Produksi steril dapat
digolongkan dalam dua kategori utama, yaitu yang harus diperoses dengan
cara aseptic pada semua tahap, dan yang disterilkan dalam wadah akhir yang
ruangan terpisah yang selalu bebas debu dan dialiri udara yang melewati
saringan bakteri. Tekanan udara dalam ruangan hendaklah lebih tinggi dari
ruangan disebelahnya.
9. Pengemasan
Produk ruahan menjadi obat jadi, yang dilaksanakan dengan pengawasan
yang tepat untuk menjaga identitas, keutuhan dan kualitas barang yang
sudah dikemas. Semua kegiatan pengemasan hendaklah dilaksanakan
dengan instruksi yang diberikan dan menggunakan bahan pengemas yang
tercantum dalam prosedur pengemasan induk.
10. Bahan atau produk pulihan
Bahan atau produk dapat diolah ulang atau dipulihkan asalkan bahan
tersebut layak untuk diolah ulang melalui prosedur tertentu yang telah
disahkan, serta hasilnya masih memenuhi persyaratan spesifikasi yang
ditentukan dan tidak terjadi perubahan yang berarti terhadap mutunya Sisa
produk yang tidak layak untuk diolah ulang atau bahan pulihan yang tidak
memiliki spesifikasi, mutu kemanjuran atau keamanan tidak boleh
ditambahkan kedalam batch berikutnya.
11. Obat kembalian
Obat jadi yang dikembalikan dari gudang pabrik jika, ditemukan adanya
kerusakan kualitas teknis obat atau adanya reaksi merugikan dari obat misal
karena label atau kemasan luar kotor atau rusak, dapat diberi label kembali
atau diolah ulang kebatch berikut asalkan tidak ada resiko terhadap mutu
produk dan pengerjaan pengolahan ulang hendaklah disahkan dan
dijual kembali, diberi label kembali atau diolah kembali jika telah dilakukan
evaluasi secara cermat dan hasil pemeriksaan ulang olah Bagian Pemastian
Mutu dinyatakan memenuhi syarat.
12. Karantina obat jadi dan penyerahan kegudang obat jadi
Karantina obat jadi merupakan titik akhir pengawasan sebelum obat jadi
diserahkan ke gudang dan siap didistribusikan.
13. Pengawasan distribusi obat jadi
Sistem distribusi hendaknya dirancang dengan tepat sehingga menjadi obat
jadi yang pertama masuk didistribusikan terlebih dahulu (First In First Out).
14. Penyimpanan bahan awal, Produk antara, produk ruahan dan obat jadi.
Bahan tersebut disimpan rapi dan teratur untuk mencegah resiko tercampur
baur atau pencemaran sera memudahkan pemeriksaan dan pemeliharaan.
f. Pengawasan Mutu
Pengendalian mutu obat dilaksanakan melalui sistem pengawasan yang
terencana dan terpadu. Pengawasan mutu merupakan bagian yang esensial dari
cara pembuatan obat yang baik untuk memastikan tiap obat yang dibuat senantiasa
memenuhi persyaratan mutu yang sesuai dengan penggunaannya. Pengawasan
mutu penting dalam penetapan spesifikasi, pengambilan contoh dan pengujian
beserta dukungan dan prosedur yang menjamin bahwa pengujian benar-benar
dilaksanakan, serta kelulusan bahan dan produk tidak akan diberikan sebelum
mtunya dinilai memuaskan. Keterlibatan dan rasa tanggung jawab semua unsur
yang berkepentingan dalam seluruh rangkaian pembuatan adalah mutlak untuk
mencapai sasaran mutu yang ditetapkan mulai dari saat obat dibuat sampai
Untuk keperluan tersebut harus ada suatu bagian pengawasan mutu yang
berdiri sendiri. Bagian pengawasan mutu bertanggung jawab untuk memastikan
bahwa:
1. Tahap produksi obat telah dilaksanakan sesuai prosedur yang telah
ditetapkan dan telah divalidasi sebelumnya, antara lain melalui evaluasi
dokumentasi produk terdahulu.
2. Semua pengawasan selama proses dan pemeriksaan laboratorium terhadap
suatu bets obat telah dilkasanakan dan bets tersebut telah memenuhi
spesifikasi yang ditetapkan sebelum didistribusi.
3. Suatu bets memenuhi persyaratan mutunya selama waktu peredaran yang
ditetapkan.
Bagian pengawasan mutu ini memiliki wewenang khusus untuk
memberikan keputusan akhir meluluskan atau menolak atas mutu bahan baku atau
produk obat ataupun hal lain yang mempengaruhi mutu obat.
g. Infeksi Diri
Tujuan infeksi diri adalah untuk melakukan penilaian apakah seluruh
aspek produksi dan pengendalian mutu dalam pabrik memenuhi ketentuan CPOB.
Program infeksi diri harus dirancang untuk mendeteksi kelemahan dan
pelaksanaan CPOB dan untuk menetapkan tindakan perbaikan. Infeksi diri ini
harus dilakukan secara teratur. Seluruh tindakan perbaikan yang disarankan untuk
melaksanakan infeksi diri ditunjuk tim infeksi diri yang mampu menilai secara
objektif pelaksanaan CPOB. Tim infeksi diri ditunjuk oleh manager perusahaan,
sekurang-kurangnya terdiri dari 3 orang yang ahli dibidang pekerjaan dan paham
dari perusahaan dengan atau tanpa bantuan tenaga ahli dari luar. Keseluruhan
prosedur dan pencatatan mengenai infeksi diri ini harus didokumentasikan.
h. Penanganan Ketentuan Terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian
Keluhan terhadap obat dan laporan keluhan dapat menyangkut mutu, efek
samping yang merugikan atau masalah efek terapeutik. Semua laporan dan
laporan keluhan hendaknya diteliti dan dievaluasi dibuatkan laporan.
Penarikan kembali obat dapat berupa penarikan kembali satu atau
beberapa bacth atau seluruh obat jadi tertentu dari suatu mata rantai distribusi.
Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak
memenuhi persyaratan mutu atau dasar pertimbangan adanya efek samping yang
tidak diperhitungkan yang merugikan kesehatan.
Obat kembalian adalah obat jadi yang telah beredar, yang kemudian
dikembalikan kepabrik karena adanya keluhan, kerusakan, kadarluarsa, masalah
keabsahan atau sebab lain mengenai kondisi obat, wadah atau kemasan sehingga
menimbulkan keraguan akan keamanan, identitas, mutu dan jumlah obat yang
bersangkutan.
Prosedur pengamanan obat kembalian hendaklah dengan
memperhatikan hal-hal berikut antara lain: Identifikasi dan pencatatan mutu dari
obat kembalian, dikarantina, dilakukaan penelitian, pemeriksaan dan pengujian.
Obat kembalian yang tidak dapat diolah ulang hendaklah dimusnahkan
dan hendaklah dibuat prosedur pemusnahan bahan atau produk yang ditolak
mencakup pencegahan pencemaran lingkungan dan mencegah kemungkinan
Pelaksanaan penanganan terhadap obat kembalian dan tindak lanjut
yang dilakukan hendaklah dicatat dan dilaporkan. Untuk tiap pemusnahan obat
kembalian hendaknya dibuat berita acara yang ditandatangani oleh pelaksana
pemusnahan dan saksi.
i .Dokumentasi
Dokumentasi pembuatan obat merupakan bagian dari sistem informasi
managemen yang meliputi spesifikasi prosedur, metode dan instruksi,
perencanaan, pelaksanaan, pengendalian, serta evaluasi seluruh rangkaian
pembuatan obat. Dokumentasi sangat penting untuk memastikan bahwa setiap
petugas dapat instruksi secara rinci dan jelas mengenai bidang tugas yang harus
dilakukan sehingga memperkecil resiko terjadinya salah tafsir dan kekeliruan
yang biasanya timbul karena hanya mengandalkan komunikasi lisan.
Sistem dokumentasi harus menggambarkan riwayat lengkap dari setiap
bacth atau lot suatu produk sehingga memungkinkan penyelidikan serta
penelusuran terhadap bacth atau lot produk yang bersangkutan. Sistem
BAB III
KEGIATAN DI INDUSTRI FARMASI
3.1. Keterlibatan Dalam Produksi
3.1.1. Bagian Perencanaan Pengendalian Produksi Dan Iventory ( PPPI )
PPPI merupakan bagian yang bertanggung jawab dalam perencanaan dan
pengendalian bahan produksi dan inventori serta menjadi penghubung antara
bagian marketing dan produksi.
Tugas dan fungsi dari PPPI adalah :
a. Mengevaluasi dan mengkonfirmasi pesanan dari pemasaran / unit lain.
b. Menghitung dan merencanakan kebutuhan bahan baku / kemasan.
c. Mengendalikan stok bahan baku / kemasan agar efektif dan efisien.
d. Merencanakan dan membuat jadwal produksi per triwulan untuk seluruh item.
e. Mengendalikan proses produksi agar efektif, efisien, dan sesuai jadwal.
f. Menyiapkan laporan Managerial per bulan.
Berdasarkan struktur organisasi, PPPI membawahi 2 bagian yaitu :
1) Bagian Perencanaan dan Pengendalian Bahan
a. Supervisor pengendalian bahan
b. Supervisor perencanaan bahan
2) Bagian Perencanaan dan Pengendalian Produksi
a. Supervisor pengendalian produksi
3.1.a. Bagian Perencanaan dan Pengendalian Bahan.
Tugas bagian ini merencanakan dan mengendalikan persediaan bahan
yang di butuhkan untuk proses produksi, bekerja sama dengan bagian pemasaran
yang mengacu pada Rencana Kerja dan Anggaran Perusahaan ( RKAP ). Dalam
hal perencanaan bahan PPPI berkoordinasi dengan 4 bagian lain yaitu bagian
produksi, bagian pengelolaan mutu, bagian penyimpanan dan bagian pembelian.
Perencanaan harus dilakukan secara efisien, beberapa strategi dalam
system perencanaan bahan baku dan bahan kemasan adalah sebagai berikut :
a. Penentuan kuantum stok ditetapkan berdasarkan hasil produksi tahun
sebelumnya dibagi 12 bulan dan stok minimum adalah persediaan untuk tiga
bulan.
b. Penentuan jumlah ditentukan dengan cara RE Order Level ( ROL ), yaitu
kuantum yang menyebutkan waktu dilakukan order kembali.
c. Jadwal penerimaan pesanan untuk bahan kemasan adalah 40 hari dari tanggal
SPPB ( Surat Permohonan Pemesanan Bahan ) dan untuk bahan baku adalah 3
bulan dari tanggal SPPB.
d. Jumlah yang di butuhkan termasuk untuk buffer stock, bila kurang akan
dibuatkan SPPB ( Surat Permohonan Pemesanan Bahan ).
Jumlah permintaan pemesanan barang dari pemasaran akan menjadi bahan
pertimbangan, sehingga akan ada beberapa kemungkinan yaitu :
a. Pesanan di penuhi 100 % karena bahan baku tersedia, SDM mencukupi dan
kapasitas mesin besar.
b. Pesanan tidak dipenuhi sama sekali karena bahan baku kosong atau mesin
c. Pesanan dipenuhi sebagian atau kurang dari 100 % karena keterbatasan bahan
dan kapasitas produksi.
d. Jumlah pesanan dapat ditambah atau dikurangi, hal tersebut terjadi karena
adanya beberapa factor, yaitu kapasitas produksi terbatas, stok obat di pasaran
masih banyak, serta bahan baku tidak lengkap.
Sesuai dengan pemesanan, maka bagian perencanaan dan pengendalian
bahan membuat surat permohonan pemesanan barang ( SPPB ) dengan
melampirkan spesifikasi bahan dan untuk bahan pengemas disertai contohnya
yang kemudian dikirim kebagian pembelian. Untuk pembelian produk local
dilakukan oleh bagian pembelian plant Jakarta, sedangkan untuk produk impor
dilakukan oleh bagian pembelian kantor pusat yang akan mengkoordinir bagian
pembelian ini di seluruh Indonesia. Untuk pengendalian stok bahan dilakukan
pengecekan jumlah pemakaian per hari perhitungan dengan cermat pada saat
pembuatan SPPB dan mengatur jadwal kedatangan bahan yang akan dipesan
sesuai jadwal.
3.1.b. Bagian Perencanaan dan Pengendalian Produksi
Tugas utama bagian perencanaan dan pengendalian produksi ( PP
Produksi ) adalah merencanakan dan mengendalikan proses produksi, agar
berjalan lancer dan berkesinambungan. Dilakukan berdasarkan konfirmasi dan
dibuat jadwal produksi per minggu dalam satu triwulan.
Bila bahan – bahan yang di perlukan untuk produksi telah di terima, maka langkah
– langkah selanjutnya adalah :
a. Mengevaluasi pesanan dengan mengkonfirmasi Bagian Perencanaan Bahan,
b. Mengkonfirmasi bagian pemasaran maksimal lima hari kerja.
c. Membuat rencana penurunan SPK ( Surat Perintah Kerja ), dimana rencana ini
harus di sesuaikan dengan kesiapan bahan dan mesin, SPK diturunkan ke
bagian produksi setiap minggu.
d. Mengevaluasi SPK apakah SPK tersebut belum, sedang atau sudah di
jalankan.
Supervisor PP Produksi memonitor perkembangan proses produksi, untuk
memudahkan monitoring, maka SPK yang di keluarkan harus diperiksa
kelengkapannya, antara lain :
1. Bon Penyerahan Bahan Baku ( BPBB ) dari penimbangan sentral ( PS ) ke
produksi.
2. Bon I sampai ke Bon IV adalah bon penyerahan produk setengah jadi
( BPPSJ ), yaitu :
• Bon I dari produksi ke KIP.
• Bon II dari KIP ke produksi.
• Bon III dari produksi ke KIP.
• Bon IV dari KIP ke pengemasan.
3. Bon V adalah bon penyerahan produk jadi ( BPPJ ) dari pengemasan ke
bagian penyimpanan.
4. Khusus untuk tablet salut terdapat :
• Bon IA dari proses massa ke KIP.
• Bon IIA dari KIP ke proses.
• Bon IB dari cetak ke KIP.
Setiap minggu dilakukan evaluasi kegiatan produksi dan setiap bulan
dibuat laporan evaluasi ke bagian pemasaran, apakah kegiatan produksi
memenuhi target atau tidak.
3.2. Bagian Penyimpanan
Bagian penyimpanan bertugas untuk mengelola penerimaan, penyimpan
dan pengeluaran baik bahan baku, bahan kemasan, serta produk jadi, bagian ini di
pimpin oleh seorang Asisten Manager Penyimpanan yang membawahi 4
supervisor, yaitu :
1. Supervisor Gudang Bahan Baku.
2. Supervisor Gudang Bahan Kemas.
3. Supervisor Gudang Bahan Jadi dan Ekspedisi.
4. Supervisor Penimbangan Sentral.
Alur proses pada bagian penyimpanan adalah sebagai berikut :
a. Penerimaan.
Barang yang dikirim oleh pemasok ke gudang penyimpanan disesuaikan
dengan surat pesanan ( SP ) dari bagian pembelian. Oleh petugas penyimpanan
setiap barang yang datang, harus diperiksa kesesuaiannya dengan SP dan
dilakukan pemeriksaan secara visual. Jika telah sesuai, bagian pembelian
membuat surat bukti titipan barang sementara ( BTBS ) dan di beri label kuning
sebagai tanda bahwa barang tersebut berstatus karantina. BTBS juga berfungsi
sebagai permohonan periksa yang di serahkan kepada bagian Laboratorium
Apabila hasil pemeriksaan laboratorium ( HPL ) tidak lulus, maka bahan
diberi label merah dan diberi tulisan DITOLAK kemudian dikembalikan kepada
pemasok disertai surat pengembalian. Untuk bahan baku yang DILULUSKAN
diberi label hijau oleh bagian Laboratorium Pengujian dan dibuat bon penerimaan
bahan baku ( BPBB ) dan bon penerimaan bahan kemas ( BPBK ). Apabila sudah
dinyatakan lulus, surat jalan ditanda tangani untuk penagihan pembayaran. Surat
jalan tersebut di serahkan kepada bagian Pembelian sebagai data stok barang.
Untuk bahan baku betalaktam penerimaan dilakukan dalam gudang tersendiri
yang terdapat di dalam area Beta Laktam.
Pada HPL terdapat jadwal uji ulang barang yang disimpan. Pemeriksaan
ulang bahan aktif dilakukan setiap 1 tahun sekali, sedangkan untuk bahan
tambahan di lakukan 2 tahun sekali. Jika hasil pemeriksaan ulang menyatakan
barang tersebut sudah tidak memenuhi syarat lagi, maka barang tersebut diberi
label DITOLAK kemudian dimusnahkan.
b. Penyimpanan.
Ruangan penyimpanan terbagi atas 4 ruang, di sesuaikan dengan sifat dan
jenisnya untuk menjaga stabilitas barang digudang penyimpanan, yaitu :
a. Ruang A
Terbagi atas 4 bagian, yaitu ; ruang penerimaan bahan baku, ruang
karantina bahan baku, produk jadi dan ekspedisi serta ruang sampling bahan baku.
Ruang sampling bahan baku merupakan zona abu – abu dan berada di bawah
tanggung jawab Laboratorium Pengujian. Suhu ruang A ini diatur tidak lebih dari
30ºC dan kelembaban ( Rh ) maksimal 75 % pengkondisian ruangan ini di
b. Ruang B
Merupakan gudang penyimpanan bahan baku ( umumnya untuk bahan –
bahan pembantu ). Suhu ruang ini di monitor tidak boleh lebih dari 30 ºC dan
kelembaban maksimal 75 % ± 5%. Pengkondisian ruangan ini dilakukan hanya
pada saat jam kerja.
c. Ruang C.
Merupakan ruang penyimpanan bahan pengemas primer (misal :
alumunium foil). Suhu ruang ini di monitor maksimal 25 ºC dan kelembaban
maksimal 70 % ± 5 %, dikondisikan selama 24 jam.
d. Ruang D.
Merupakan ruang penyimpanan bahan baku, terutama bahan aktif. Suhu
ruangan maksimal 25 ºC dan kelembaban maksimal 70 % ± 5 %, dikondisikan
selama 24 jam. Ruangan ini dibagi 4 bagian, yaitu :
• Untuk bahan aktif produk lisensi.
• Untuk bahan baku non lisensi.
• Bagian ruang bersuhu kurang dari 8-15 ºC ( cool storage ). Untuk
penyimpanan bahan aktif seperti dopamine HCL, ekstra kental saga, ekstra
pekat sirih, dll.
• Untuk penyimpanan bahan baku yang masih dalam status KIP jika memang
perlu kondisi penyimpanan khusus, bagian ini di batasi dengan garis kuning
pada lantai. Untuk produksi yang reject di dalam area di batasi garis merah.
Sistem penyimpanan yang digunakan dalam rak bawah merupakan bahan
– bahan yang sering di pakai, dan rak atas merupakan bahan – bahan yang jarang
suhu dan kelembaban gudang dilakukan 2x sehari, yaitu pada pukul 09.00 pagi
dan 14.00 siang. Pemeriksaan kebersihan gudang dilakukan 1x seminggu, seperti,
ventilasi, atap, lantai dan dinding, serta melindungi bahan dari gangguan binatang,
di lakukan pest control setiap 2 minggu sekali oleh pihak ketiga. Untuk barang –
barang yang mudah terbakar seperti aseton dan alcohol disimpan dalam gudang
terpisah dengan gudang terpisah dengan gudang lain “gudang api“.
c. Pengeluaran
Pengeluaran bahan baku dari penyimpanan melalui penimbangan sentral (
PS ) berdasarkan pada SPK dari PPPI kepada bagian produksi. Selanjutnya bagian
PS akan mengeluarkan BPBB ke bagian penyimpanan. Bagian penyimpanan akan
mengeluarkan barang sesuai dengan permintaan tersebut. System pengeluaran di
bagian penyimpanan menggunakan system FIFO ( First in First out ) dengan
melihat nomor hasil pemeriksaan laboratorium dan system FEFO ( First expire
First out ) untuk barang yang kadaluarsanya sangat pendek. Pengeluaran bahan
pengemas dari gudang kemasan berdasarkan BPBP ( Bon Permintaan Bahan
Pengemasan ) yang diserahkan oleh bagian produksi yang membutuhkan.
Bagian penyimpanan berkoordinasi dengan bagian PPPI, setiap akhir
bulan dilakukan stock opname barang yang dapat di lihat dari kartu stok bagian
penyimpanan. Jika terjadi kekeliruan karena penulisan atau kesalahan apapun,
maka harus dibuat berita acara.
d. Penimbangan Sentral.
Penimbangan sentral dipimpin oleh Supervisor Penimbangan Sentral (PS).
Setelah SPK di keluarkan oleh PPPI kepada bagian produksi, maka bagian
menyerahkan rencana produksi dan bahan baku, Catatan Pengolahan Batch ( CPB
) dan bon permintaan bahan baku ( BPBB ). Kemudian PS akan mengeluarkan
bon permintaan bahan baku intern ( BPBI ) pada gudang bahan baku. Bila
persediaan barang yang akan digunakan tidak tersedia atau tidak cukup maka
gudang bahan baku akan mengeluarkan barang permintaan.
PS memiliki 4 ruang penimbangan yaitu ruang 1, 2, 3 dan 4. ruang 1
digunakan untuk penimbangan zat aktif golongan narkotika. Ruang 4 digunakan
untuk penimbangan cairan dan gula dalam jumlah yang besar. Ruang 2 dan 3
digunakan untuk menimbang bahan baku lainnya.
3.3. Bagian Produksi
Bagian produksi PT. Kimia Farma ( Persero ) Tbk. Plant Jakarta dipimpin
oleh seorang Manager yang membawahi 5 ( Lima ) bagian yang masing – masing
dipimpin oleh seorang Asisten Manager yaitu Bagian Formulasi I, Formulasi II,
Formulasi III, Beta laktam dan Bagian Pengemasan.
1. Bagian Formulasi I dan Narkotika.
Bagian formulasi I dipimpin oleh seorang Asisten Manager yang
membawahi 3 Supervisor yaitu Supervisor Granulagsi,Pencetakan dan
Penyalutan. Alur proses produksi diawali dari bagian PPPI mengeluarkan SPK
(Surat Perintah Kerja) kepada Bagian Formulasi I untuk melakukan produksi
kemudian Bagian Formulasi I akan meminta bahan baku ke Penimbangan Sentral
dengan menyertakan rencana produksi dan penimbangan bahan baku,Catatan
Pengolahan Batch (CPB) yang dilampirkan dengan Berita Acara Produksi (BAP),
baku yang telah diterima dari Penimbangan Sentral akan dilanjutkan dengan
proses pencampuran.
Proses pembuatan tablet meliputi penimbangan bahan baku, pencampuran
dan pencetakan. Metode pembuatan tablet ada 3 macam yaitu granulasi basah,
granulasi kering dan kempa langsung. Pemilihan metode tergantung dari sifat zat
aktif yang akan dibuat tablet.
a. Granulasi Basah
Proses ini diawali dengan pembuatan larutan pengikat terlebih dahulu.
Bahan aktif, bahan pengisi dan bahan penghancur dicampur sampai homogen,
kemudian ditambahkan larutan pengikat dalam super mixer Diosna. Masa yang
didapat dilakukan pengayakan basah kemudian dikeringkan dalam ruang
pengering ( dehumidifier ) kurang lebih satu malam granul yang telah kering
tersebut dilakukan pengayakan kering, kemudian dilakukan final mixing dengan
menambahkan bahan pelicin didalam V-mixer selama 5 menit. Massa yang
dihasilkan kemudian dikirim ke KIP untuk diperiksa LOD nya ( bon I ), apabila
memenuhi syarat, bagian KIP akan menyerahkan Bon II, kemudian massa dicetak
dan dilakukan pemeriksaan meliputi bobot tablet setiap 30 menit. Setelah proses
pencetakan selesai kemudian produk dikirim ke KIP sebagai produk ruahan
disertakan Bon III dan akan diperiksa meliputi bobot tablet, diameter tablet, waktu
hancur, kekerasan dan uji disolusi. Apabila lulus maka produk diserahkan
kebagian pengemasan di sertakan Bon IV dan siap untuk dikemas.
b. Granulasi Kering.
Proses granulasi kering dilakukan dengan mengayak semua bahan
slugging dengan mesin roller compactor kemudian slug dihancurkan dan diayak
menjadi granul. Ukuran granul sesuai dengan ukuran mesh pada mesin pengayak.
Granul yang dihasilkan ditambahkan dengan fase luar dan dicampur dalam
V-mixer selama lima menit. Massa yang telah terbentuk dikirim ke KIP untuk
dilakukan pemeriksaan LOD granul, apabila diluluskan dilanjutkan ke proses
pencetakan. Produk yang telah dicetak dikirim lagi ke KIP untuk diperiksa
meliputi bobot tablet, diameter tablet, waktu hancur, kekerasan dan uji disolusi.
Apabila lulus maka produk diserahkan kebagian pengemasan untuk dikemas.
c. Cetak Langsung.
Proses pembuatan tablet dengan metode cetak langsung diawali dengan
proses pencampuran semua bahan pembantu, kemudian ditambahkan bahan aktif
dan dilakukan pencampuaran dengan V-mixer. Massa yang dihasilkan dikirim ke
KIP untuk diperiksa besarnya LOD di Laboratorium, setelah dinyatakan lulus
kemudian dilakukan pencetakan. Produk ruahan hasil pencetakan dikirim lagi ke
KIP untuk diperiksa meliputi bobot tablet, diameter tablet, waktu hancur,
kekerasan dan uji disolusi. Apabila lulus maka produk diserahkan kebagian
pengemasan untuk dikemas. Pada beberapa sediaan tablet dilakukan proses
penyalutan. Tablet salut yang diproduksi oleh PT. Kimia Farma (Pesero) Tbk.
Plant Jakarta ada 2 jenis yaitu: Tablet salut gula dan tablet selaput film.
Keutungan dari tablet salut antara lain:
a. Memperbaiki mutu estetika produk
b. Menutup rasa dan bau yang tidak enak.
c. Memungkinkan produk yang lebih mudah ditelan oleh penderita
e. Memudahkan penanganan terutama pada pengemasan.
f. Meningkatkan stabilitas produk.
g. Memodifikasi pelepasan zat aktif.
Macam – macam tablet salut antara lain :
a. tablet salut gula.
Proses pembuatan tablet salut gula adalah tablet yang akan disalut
dilakukan proteksi ( Protecting ) dengan melakukan larutan shellac atau polimer
organik, hal ini bertujuan untuk melindungi tablet inti terhadap pengaruh bahan
penyalut yang digunakan dalam penyalutan.
Tablet yang telah diproteksi kemudian diberi bentuk dan penambahan
bobot dengan proses sub coating yaitu melapisi tablet yang akan disalut untuk
mencegah masuknya air kedalam inti tablet, kemudian dikeringkan selama
semalam. Coating merupakan pelapisan yang dilakukan setelah inti tablet tertutup
sampai tablet inti tidak tampak lagi, setelah proses ini juga dilakukan pengeringan
selama semalam. Setelah tablet selesai di Coating, proses selanjutnya adalah
smoothing untuk membersihkan sisa Coating yang menempel pada tablet. Setelah
smoothing selesai maka dilakukan pemberian warna (Coloring) yang juga
merupakan salah satu identitas tablet tersebut, setelah pewarnaan selesai dan
sempurna langkah selanjutnya adalah polishing.
b. Salut Selaput Film
Proses yang dilakukan dalam proses penyalutan film adalah tahap
pertama pelarutan bahan salut film kemudian dimasukkan kedalam alat
berputar, sampai semua bahan penyalut habis. Seleksi juga dilakukan pada tablet
selaput namun tidak ada proses printing.
Selanjutnya ruahan tersebut dikirim keKIP, kemudian disampling oleh IPC
untuk dilakukan pemeriksaan oleh Laboratorium Pengujian. Bila hasilnya
diluluskan dapat dilanjutkan untuk dikemas.
d. Narkotika
PT. Kimia Farma ( Persero ) Tbk. Plant Jakarta diberi hak khusus untuk
memproduksi obat-obatan narkotika dan psikotropika. Berdasarkan Kep Men kes
RI No. HK 00.65.6.01986 tanggal 26 juni 1994 tentang penunjukan PT. Kimia
Farma ( Persero) Tbk. Sebagai perusahaan yang diberi izin untuk melaksanakan
produksi dan distribusi narkotika di Indonesia. Kep Men Kes RI No. 199/Men
Kes/SK/III/1996 tentang penunjukkan PBF PT. Kimia Farma (Persero) Tbk.
Depot sentral sebagai importir tunggal narkotika di Indonesia. Dalam
pelaksanaannya, pemesanan narkotika dengan tujuan pendistribusian ke
apotek-apotek seluruh Indonesia hanya bisa lewat PBF PT.Kimia Farma ( Persero ) Tbk.
Jakarta.
Berbeda sedikit dengan alur proses produksi lainnya, untuk obat golongan
narkotika terdapat perlakukan khusus. Mulai dari pembelian bahan baku oleh
bagian impor harus mendapatka izin dari BPOM mengenai jumlah dan jenisnya
berdasarkan kuota tiap tahun untuk Indonesia.
Tugas penanggung jawaban narkotika adalah menerima dan menyimpan
bahan baku narkotika dalam gudang tersendiri kemudian dilakukan pemeriksaan,
jika lulus bahan baku siap dipakai. Bagian produksi akan menyerahkan BPBB dan
selanjutnya sama dengan produk lainnya dan pada setiap tahap produksi dibuatkan
berita acara yang dilaporkan ke Badan Pengawasan Obat dan Makanan (BPOM).
Pengiriman produk jadi ke Unit Logistik Sentral dilakukan oleh Penanggung
Jawab Narkotika dan atau Asisten Apoteker Penanggung Jawab Gudang Narkotik.
Bagian Pengemasan memilki tempat khusus yang digunakan untuk
pengemasan produk narkotika. Gudang narkotika maupun ruangan karantina
dipisahkan dengan gudang lain dengan perlindungan khusus seperti tertutup rapat
tanpa jendela, atap bertralis dan memilki dua lapis pintu besi dengan kunci yang
berbeda.
2. Bagian Formulasi II
Bagian Formulasi II dipimpin oleh Asisten Manajer dan membawahi
beberapa Supervisor yaitu Supervisor Cairan, Supervisor Krim.
a. Produksi Cairan
Alur produksi cairan dimulai dari diturunkannya SPK oleh PPPI kepada
Bagian Formulasi II. Selanjutnya Bagian Formulasi II akan menyerahkan CPB
(Catatan Pengolahan Batch) dan BPBB kepada Penimbangan Sentral. Bahan baku
yang telah ditimbang dilarutkan dan dicampur dalam suatu tangki, setelah
homogen cairan dimasukkan dalam Colloid Mill untuk menghaluskan
partikel-partikel. Campuran yang dihasilkan disaring dengan saringan yang berukuran 200
mesh. Untuk cairan dalam bentuk suspensi, proses selanjutnya adalah
pencampuran dengan suspending agent CMC Na. Massa yang terbentuk dikirim
ke ruang karantina dan melewati proses pemeriksaan pH, viskositas dan kadar zat
(ditandai dengan menempelkan label berwarna hijau), bagian formulasi II akan
mengajukan BPBK (Bon Permintaan Bahan Kemas) untuk dilakukannya
pengemasan primer atau sering disebut juga pengisian massa dalam botol. Massa
yang telah dimasukkan kedalam botol, kemudian dikirim keruang karantina
sebagai produk ruahan. Setelah Laboratorium Pengujian menyatakan lulus,
produk tersebut dikirim kebagian pengemasan untuk segera dikemas.
b. Produksi Krim
Alur produksi cairan dimulai dari diturunkannya SPK oleh PPIC kepada
Bagian Formulasi II. Selanjutnya Bagian Formulasi II akan menyerahkan CPB
dan BPBB kepada Penimbangan Sentral.
Proses produksi dimulai dengan pembuatan basis krim dengan cara
melarutkan fase air dan fase minyak sebagai bahan dasar. Pembuatan basis krim
dilakukan dengan peleburan untuk fase minyak dan pelarutan untuk fase cair
(dengan menggunakan heating tank), kemudian masing-masing fase disaring
dengan nilon berukuran 200 mesh. Selanjutnya fase air dicampur dengan fase
minyak dalam Planetary Mixer Miralles, sampai homogen. Campuran yang
dihasilkan didinginkan sampai suhunya 30-35º C dan dilakukan penimbangan.
Selanjutnya dilakukan pencampuran basis krim dengan bahan aktif, untuk
membentuk massa krim. Massa krim yang diperoleh ditimbang dan dikirim ke
ruang karantina. Selanjutnya Laboratorium Pengujian akan melakukan
pemeriksaan homogenitas, pH, viskositas dan kadar zat aktif. Setelah
Laboratorium menyatakan lulus, Bagian Formulasi II akan mengajukan BPBK
untuk melakukan pengemasan primer terhadap massa krim tersebut. Massa krim
ruahan, dan mengalami pemeriksaan oleh Laboratorium Pengujian untuk
selanjutnya dikirim kebagian pengemasan.
c. Pengolahan Air Produksi
Bagian Formulasi II juga bertanggung jawab terhadap proses pengolahan
air yang digunakan untuk produksi Bagian Formulasi I, Formulasi II dan
Formulasi III. Air yang dihasilkan digunakan untuk pembuatan sediaan cair,
sediaan injeksi, sediaan tablet dan pencucian wadah seperti botol, tutup botol dan
ampul.
Proses pengolahan dimulai dari air yang berasal dari PAM yang
dilewatkan ke dalam karbon filter sebanyak 2 kali. Kemudian pompa akan
mendistribusikan cairan ke filter yang berlapis-lapis mulai ukuran 30 µm, 10 µm
dan 5 µm. Selanjutnya hasil penyaringan dimasukkan ke dalam membran Reverse
Osmose System (RO). Sistem tersebut akan mendistribusikan air kedalam empat
bagian antara lain :
1. Bagian pertama, air akan masuk kedalam tangki-tangki penampungan yang
berkapasitas 5000 L, ait tersebut akan digunakan untuk pembuatan sediaan
krim dan mencuci botol.
2. Bagian kedua, air akan disaring dengan filter yang berukuran 1,5 µm dan
0,45 µm yang kemudian digunakan untuk mencuci ampul.
3. Bagian ketiga, air akan disaring dalam filter yang berukuran 1 µm dan 0,2
µm yang kemudian digunakan untuk pembuatan sediaan cairan tablet.
4. Bagian keempat, air akan dialirkan ke tangki unit destilasi kemudian
dicatridge filter 2,5 µm dan 0,2 µm untuk proses pembuatan sediaan injeksi
3. Bagian Formulasi III
Bagian Formulasi III dipimpin oleh seorang Asisten Manajer yang
membawahi Supervisor Injeksi, Supervisor Sirup Kering dan Supervisor Kapsul.
Bagian ini memproduksi injeksi, sirup kering dan kapsul.
a. Pembuatan Injeksi.
Bagian PPPI mengeluarkan SPK kepada Bagian Formulasi II untuk
melakukan produksi. Bagian formulasi II menyerahkan Catatan Pengolahan Batch
dan Bon Permintaan Bahan Baku kepada Penimbangan Sentral, setelah bahan
baku diterima dari Penimbangan Sentral kemudian dilakukan proses pelarutan.
Setelah dilakukan pelarutan kemudian ditambahkan aqua pro injeksi sampai
volume tertentu dan dilakukan pengukuran pH massa injeksi kemudian massa
dikirim ke KIP untuk dilakukan pemeriksaan meliputi bentuk, warna, pH dan
kejernihan larutan, apabila diluluskan kemudian dilakukan penyaringan dengan
filter ukuran 1,2 µ dan 0,45 µ kemudian dilakukan proses pengisian didalam
ampul. Ampul dicuci dengan air Reverse Osmosis Sistem yang telah disaring
menggunakan filter berukuran 1,5 µ dan 0,45 µ dan dikeringkan menggunakan
Hot Air Sterilizer pada suhu 170 ºC selama 1 jam, kemudian dilanjutkan proses
pengisian. Ampul yang telah diisi disterilkan dalam double door autoclave pada
suhu 110 ºC selama 30 menit, kemudian dilakukan tes kebocoran menggunakan
otoklaf selama 30 menit, dilanjutkan proses seleksi secara visual untuk memeriksa
adanya partikel asing dengan menggunakan bantuan lampu TL. Produk yang
diluluskan masuk ke Karantina In Proses sebagai produk ruahan, jika hasil telah
Proses sediaan injeksi dilakukan dalam ruangan steril yang berkaca tembus
pandang untuk memudahkan pengawasan dari luar ruangan. Tekanan udara di
dalam ruangan steril lebih tinggi dari pada di koridor untuk menghindari
kontaminasi/pencemaran yang masuk ke ruang produksi. Pegawai yang masuk ke
ruang steril harus melewati tiga pintu dan jumlah orang yang berada di ruang steril
terbatas untuk empat orang, hal ini dilakukan untuk menghindari pencemaran
ruangan. Pemeriksaan ruang steril dilakukan setiap satu bulan oleh bagian
pengujian.
Upaya pemeliharaan ruang steril dilakukan setiap hari dengan
membersihkan semua ruang steril dengan alkohol, apabila pada saat proses
pemeriksaan ruangan tidak memenuhi syarat maka dilakuakan fumigasi dengan
sublimasi paraformaldehid didiamkan selama 24 jam, kemudian asap dikeluarkan
dan untuk membersihkan sisa paraformaldehid digunakan amoniak 5% dan
dilakukan pembersihan dengan aqua pro injeksi kemudian dilap dengan alkohol
70%.
b. Produksi kapsul
Bagian PPPI mengeluarkan SPK kepada Bagian Formulasi III untuk
melakukan produksi. Bagian Formulasi III menyerahkan Catatan Pengolahan
Batch dan Bon Permintaan Bahan Baku kepada Penimbangan Sentral, setelah
bahan baku diterima dari penimbangan sentral kemudian dilakukan proses
pencampuran, sebelum dicampur dilakukan proses pengayakan terlebih dahulu
dengan Vibrating sieve mesh 35. Zat aktif dan zat tambahan dimasukkan ke dalam
alat pencampur V-mixer selama 15 menit, kemudian ditambahkan fase luar dan
dikirim ke Karantina In Proses untuk dilakukan pemeriksaan LOD, jika
dinyatakan memenuhi syarat dilanjutkan proses pengisian kapsul dengan mesin
Macofar atau MG 2. Setelah selesai pengisian produk, dilakukan proses polishing
dan seleksi kapsul kemudian dikirim ke Karantina In Proses untuk dilakukan
pemeriksaan, jika diluluskan dilanjutkan ke proses pengemasan.
c. Pembuatan Sirup Kering
Bahan baku yang diterima dari Penimbangan Sentral diperiksa
kesesuaiannya dengan CPB (Catatan Pengolahan Batch) dan BAP (Berita Acara
Produksi) jika sesuai bahan dicampur dalam mortir porselin sampai homogen,
dilakukan pengayakan dengan mesh 30 dilanjutkan pencampuran lagi dengan
intensive mixer, selanjutnya pencampuran akhir dengan V-mixer, kemudian massa
dikirim ke Karantina In Proses setelah dinyatakan lulus kemudian dilakukan
pengisian kedalam botol yang telah dicuci dan dikeringkan dilemari pengering.
Selama proses dilakukan pemeriksaan keseragaman bobot dan kekerasan
perekatan tutup botol dengan alat Torque meter setiap 30 menit yang bertujuan
untuk mencetak kestabilan mesin. Produk yang telah selesai pengisian dikirim
kembali ke Karantina In Proses untuk dilakukan pemeriksaan dan setelah
dinyatakan memenuhi syarat, dilanjutkan ke proses pengemasan.
4. Bagian Pengemasan
Bagian pengemasan dipimpin oleh Asisten Manajer dan dibawahi oleh 6
supervisor yaitu Supervisor Karantina In Proses, Supervisor Pengemasan Primer I
(solid), Supervisor Pengemasan Primer II (semi solid/cairan), Supervisor
Penandaan, Supervisor Pengemasan Sekunder I (solid), Supervisor Pengemasan