BAB II
TINJAUAN PUSTAKA
2.1. Sirosis Hati
2.1.1. Definisi
Kata sirosis berasal dari kata kirrhos yang merupakan bahasa Yunani, yang
berarti oranye atau kuning kecoklatan, dan osis, berarti kondisi. Istilah sirosis diperkenalkan pertama kali oleh Laennec pada tahun 1826.20,21 Definisi sirosis
berdasarkan Organisasi Kesehatan Dunia (WHO) adalah suatu proses difus yang ditandai dengan fibrosis dan perubahan arsitektur hati normal menjadi struktur nodul abnormal yang tidak memiliki organisasi lobular yang normal.22
Sirosis hati adalah penyakit hati yang menahun yang difus yang ditandai dengan adanya pembentukan jaringan ikat dan usaha regenerasi nodul. Distorsi
arsitektur hati akan menimbulkan perubahan sirkulasi mikro dan makro menjadi tidak teratur akibat penambahan jaringan ikat dan nodul tersebut.23 Banyak bentuk kerusakan hati yang ditandai fibrosis. Batasan fibrosis sendiri adalah penumpukan
berlebihan matriks ekstraselular (seperti kolagen, glikoprotein, proteoglikan) dalam hati. Respon fibrosis terhadap kerusakan hati bersifat reversibel. Namun pada sebagian
besar pasien sirosis, proses fibrosis biasanya tidak reversibel.21
Progresifitas kerusakan hati ini dapat berlangsung dalam waktu beberapa
2.1.2. Epidemiologi
Penyakit hati menahun dan sirosis dapat menimbulkan sekitar 35.000 kematian
per tahun di Amerika Serikat. Sirosis merupakan penyebab kematian utama yang kesembilan di AS, dan bertanggung jawab terhadap 1,2% seluruh kematian di AS. Banyak pasien yang meninggal pada dekade keempat atau kelima kehidupan mereka
akibat penyakit ini.20,21 Setiap tahun, 2000 kematian tambahan dikaitkan dengan kegagalan hati fulminan (KHF). KHF disebabkan hepatitis virus (misalnya, hepatitis A dan B), obat-obatan (misalnya asetaminofen), racun (misalnya Amanita phalloides,
yellow death cap mushroom), hepatitis autoimun, penyakit Wilson, atau berbagai etiologi lainnya. Penyebab kriptogenik bertanggung jawab atas sepertiga dari kasus
fulminan. Pasien dengan sindrom KHF memiliki tingkat kematian 50-80% kecuali mereka memperoleh transplantasi hati.21
Menurut organisasi kesehatan dunia (WHO), pada tahun 2000 sekitar 170 juta umat manusia menderita sirosis hepatis. Angka ini meliputi sekitar 3% dari seluruh populasi manusia di dunia dan setiap tahunnya kejadian baru sirosis hepatis bertambah
3 - 4 juta orang.22 Angka prevalensi penyakit sirosis hepatis di Indonesia, secara pasti belum diketahui, namun dari beberapa laporan rumah sakit umum pemerintah di
Indonesia berdasar diagnosis klinis saja didapati prevalensi sirosis hati yang dirawat di bangsal penyakit dalam umumnya berkisar antara 3,6 – 8,4% di Jawa dan Sumatera, sedangkan di Sulawesi dan Kalimantan di bawah 1%. Secara keseluruhan rata – rata
banyak ditemukan pada kaum laki-laki dibandingkan kaum wanita dengan
perbandingan 2,1 : 1 dan usia rata – rata 44 tahun (rentang usia 13 – 88 tahun) dengan kelompok terbanyak antara usia 40 – 50 tahun.25
2.1.3. Etiologi dan patogenesis
Terdapat banyak penyebab sirosis hati, beberapa diantaranya jarang terjadi, bahkan muncul di masa kecil (misalnya air minum dari pipa tembaga). Sirosis
merupakan penyakit yang diperoleh atau berbasis genetika. Penentuan etiologi pada tindakan diagnosis dini harus selalu menjadi prioritas, karena dapat membantu
pengobatan dan juga prognosis. Dengan menggabungkan data klinis biokimia, histologi, dan epidemiologi penyebab sirosis sebagian besar dapat ditentukan. Pada masa lalu penyakit hati alkohol merupakan penyebab sirosis yang paling menonjol di
Amerika Serikat. Akhir – akhir ini hepatitis C mulai meningkat jumlahnya sebagai penyebab utama hepatitis kronik maupun sirosis secara nasional. Di Indonesia, banyak
penelitian menunjukkan bahwa hepatitis B dan C merupakan penyebab sirosis yang lebih menonjol dibanding penyakit hati alkoholik.25 Banyak kasus sirosis kriptogenik ternyata disebabkan penyakit perlemakan hati non – alkoholik (non-alcoholic fatty
liver disease) NAFLD. Bila kasus – kasus sirosis kriptogenik diteliti, ternyata banyak pasien menunjukkan satu atau lebih faktor resiko klasik NAFLD seperti : obesitas,
Amerika mempunyai NAFLD, sekitar 2 – 3% orang Amerika menunjukkan steatosis
non – alkoholik (non – alcoholic steatohepatitis) NASH, yang deposisi lemaknya dalam hepatosit mengalami komplikasi berupa peradangan atau inflamasi hati dan
fibrosis. Diperkirakan 10% pasien NASH dikemudian hari berkembang menjadi sirosis. NAFLD dan NASH telah diperkirakan akan menjadi salah satu masalah kesehatan masyarakat utama pada dekade mendatang.21,24
Penyebab utama sirosis di Amerika Serikat adalah hepatitis C (26%), penyakit hati alkoholik (21%), hepatitis C plus penyakit hati alkoholik (15%), kriptogenik
(18%), hepatitis B yang bersamaan hepatitis D (15%), dan penyebab lain (5%).21,27 Penyebab lain penyakit hati menahun dan sirosis : hepatitis autoimun, sirosis bilier primer, sirosis bilier sekunder (berhubungan dengan obstruksi saluran empedu
ekstrahepar menahun), kolangitis sklerosing primer, hemokromatosis, penyakit
Wilson, defisiensi α-1 antitripsin, penyakit granulomatosa (contoh : sarkoidosis),
penyakit glycogen storage type IV, hepatitis imbas obat (contoh : metotreksat, α -metildopa, amiodaron), obstruksi aliran vena (contoh : sindrom Budd-Chiari, penyakit veno-oklusif), gagal jantung kanan kronik dan regurgitasi trikuspid.21,26,27
Terjadinya fibrosis hati menggambarkan kondisi ketidakseimbangan antara produksi matriks ekstraseluler dan proses degradasinya. Sel – sel stelata yang berada
dalam ruangan perisinusoidal merupakan sel penting untuk memproduksi matriks ekstraseluler. Beberapa faktor dapat dilepas atau diproduksi oleh sel – sel hepatosit, sel – sel Kupfer, dan endotel sinusoid pada saat terjadi kerusakan hati. Sebagai contoh
sirosis. TGF β-1 selanjutnya akan merangsang sel – sel stelata yang aktif untuk
memproduksi kolagen tipe I.20,21 Peningkatan deposisi kolagen dalam ruang Disse (
ruang antara hepatosit dan sinusoid) dan pengurangan ukuran fenestra endotel akan menimbulkan kapilarisasi sinusoid. Sel – sel stelata yang aktif juga mempunyai sifat
Tabel 2.1 Etiologi Sirosis Hati.20
Etiology Diagnostic evaluation
Infection
Hepatitis B HBsAg, anti-HBs, anti-HBc, HBV DNA
Hepatitis C Anti-HCV, HCV RNA
Hepatitis D Anti-HDV
Toxins
Alcohol History, AST/ALT ratio, liver biopsy Cholestasis
Primary biliary cirrhosis AMA, IgM, liver biopsy Secondary biliary cirrhosis MRCP, ERCP, liver biopsy Primary sclerosing cholangitis MRCP, ERCP, liver biopsy AutoImmune
Autoimmune hepatitis ANA, IgG level smooth muscle antibodies, liver-kidney microsomal antibodies, liver biopsy Vascular
Cardiac cirrhosis Echocardiogram, liver biopsy Budd-chiari syndrome CT, USG, MRI/MRA
Sinusoidal obstruction syndrome
History of offending drug use, liver biopsy
Metabolic
Hemochromatosis Iron studies, HFE gene mutation, liver biopsy Wilson disease Serum and urinary copper, ceruloplasmin, slit
lamp eye examination, liver biopsy Alpha-1 antitrypsin
deficiency
Alpha-1 antitrypsin level, protease inhibitor type, liver biopsy
NASH Liver biopsi
Cryptogenic Exclude NASH, drugs
2.1.4. Manifestasi klinis
Keluhan subjektif dari pasien sirosis bersifat non karakteristik dan ambigu. Kelelahan dikeluhkan sekitar 60-80% pasien, gangguan tidur (mungkin disebabkan
oleh gangguan irama melatonin), keluhan gangguan saluran cerna (50-60%), dan gangguan mental kadang dikeluhkan oleh pasien.29
Beberapa keluhan dan gejala yang sering timbul pada sirosis antara lain adalah:
kulit berwarna kuning, rasa mudah lelah, nafsu makan menurun, gatal, mual, penurunan berat badan, nyeri perut dan mudah berdarah (akibat penurunan produksi
faktor-faktor pembeku darah).20,21,30 Hepatic myelopati dengan paraparesis spastic jarang terjadi, umumnya terdapat pada tahap lanjut dari sirosis. Gejala dari neuropati perifer juga terjadi. Kadang terjadi meteorismus dan pada beberapa kasus timbul
asites. Takikardia, hipotensi, dan sistolik murmur yang menunjukkan sirkulasi hiperdinamik juga dapat terjadi. Spider naevi menunjukkan gangguan yang signifikan
pada sirkulasi sistemik dan pulmoner. Murmur dapat terdengar pada area umbilical (sindroma Cruveilhier-Baumgarten). Laki-laki dapat menampakkan gejala feminisasi, sedangkan wanita menunjukkan gejala hipogonadisme.29
Pasien sirosis juga dapat mengalami keluhan dan gejala akibat komplikasi dari sirosis hati tersebut. Pada beberapa pasien, komplikasi ini dapat menjadi gejala
pertama yang membawa pasien pergi ke dokter. Pasien sirosis dapat tetap dalam kondisi kompensata selama bertahun-tahun sebelum berubah menjadi dekompensata. Sirosis dekompensata dapat dikenal dari timbulnya bermacam komplikasi, seperti
fungsi hati, dan pengobatan terhadap komplikasi ini biasanya mengecewakan, kecuali
pasien mendapat transplantasi.20,21,27,30
Sesuai dengan konsensus Baveno IV, sirosis hati dapat diklasifikasikan
menjadi empat stadium klinis berdasarkan ada tidaknya varises, asites dan perdarahan varises : stadium 1 (tidak ada varises, tidak ada asites), stadium 2 (ada varises tanpa asites), stadium 3 (asites dengan atau tanpa varises), dan stadium 4 (perdarahan
dengan atau tanpa asites). Stadium 1 dan 2 dimasukkan dalam kelompok sirosis kompensata, sementara stadium 3 dan 4 dalam kelompok sirosis dekompensata.11
2.1.5. Diagnosis
Satu-satunya tes diagnosis sirosis hati yang paling akurat adalah biopsi hati.
Namun biopsi hati dapat menimbulkan komplikasi serius meskipun sangat jarang. Diagnosis kemungkinan sirosis dapat dibuat berdasarkan anamnesis, pemeriksaan fisik , pemeriksaan laboratorium rutin, maupun pemeriksaan pencitraan. Bila diagnosis
sirosis dapat ditegakkan, pemeriksaan lain dikerjakan untuk menentukan beratnya sirosis serta ada tidaknya komplikasi. Pemeriksaan lain juga dapat dibuat untuk
menentukan penyakit dasar yang menyebabkan sirosis seperti : ANA (Antinuclear antibody), ASMA (Anti – smooth muscle antibody), AMA (Anti – mitochondrial antibody) yang juga dapat ditemukan pada darah pasien hepatitis autoimun atau sirosis
bilier primer.11,20,21,27,30 Penilaian atau klasifikasi tingkat keparahan sirosis diukur dengan menggunakan skor Child – Pugh.13
Tabel 2.2 Klasifikasi Child – Pugh20
Skor
1 2 3
Parameter
Asites tidak ada ringan sedang/berat
Ensefalopati tidak ada ringan/sedang sedang/berat
Bilirubin (mg/dl) < 2,0 2-3 > 3,0
Albumin (mg/L) > 3,5 2,8-3,5 < 2,8
Waktu Prothrombin 1-3 4-6 > 6,0
Skor total Kelas Child Pugh
5-6 A
7-9 B
10-15 C
2.2. Varises Esofagus 2.2.1. Definisi
Penderita sirosis hati yang memiliki varises esofagus yang besar akibat
hipertensi portal beresiko 25-35% mengalami perdarahan serta 15-20 % beresiko kematian pada setiap episode perdarahan. Tingkat kematian bergantung kepada keadaan umum pasien dan beratnya perdarahan.20 Varises esofagus merupakan
kolateral portosistemik yang terbentuk setelah adanya dilatasi saluran pembuluh darah vena mulai dari distal esofagus akibat hipertensi portal. Varises esofagus sering terjadi pada 2 – 5 cm distal dari esofagus.31
2.2.2. Patofisiologi
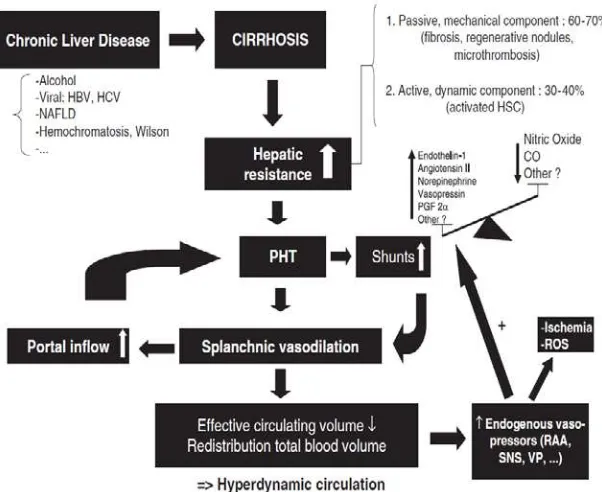
Pada sirosis, hipertensi portal terinisiasi melalui peningkatan resistensi
dan splanik yang meningkatkan aliran portal. Peningkatan resistensi vaskular
intrahepatik tidak hanya disebabkan oleh faktor mekanikal (seperti : jaringan fibrosis dan nodul - nodul regeneratif yang mendistorsi arsitektur pembuluh darah hepar),
tetapi juga oleh komponen dinamis reversibel yang dimediasi oleh peningkatan tonus vaskular disebabkan oleh kontraksi aktif miofibrolast di sekitar sinusoid hepatik dan
dalam septa fibrous. Komponen dinamik ini (menyumbang sekitar 30% pada
peningkatan resistensi vaskular intrahepatik) menggambarkan gangguan fungsional
dari sirkulasi hepar akibat dari peningkatan produksi vasokonstriktor (contoh : endotelin – 1, norepinephrin, angiotensin II, leukotriene, tromboxane A2) dan
penurunan pelepasan vasodilator endogen (terutama NO / nitric oxide).32,33,34,35 Sel stelata memiliki sifat kontraktil yang dapat dimodulasi oleh substansi vasoaktif antara lain NO dan endothelin yang dapat meningkatkan resitensi intrahepatik dan aliran
darah terutama pada sinusoidal.36 Angiogenesis juga telah menunjukkan pengaruh terhadap hipertensi portal melalui studi – studi yang menggambarkan pengaturan
peningkatan tekanan portal, sirkulasi hiperdinamik, neovaskularisasi splanchnic, dan kolateralisasi portosistemik yang diregulasi oleh VEGF (Vascular Endothelial Growth
Factor) dan PDGF (Platelet derived Growth Factor).37
Pada sirosis, gradien portosistemik dinilai dengan mengukur WHVP (Wedged Hepatic Venous Pressure) atau pengukuran tekanan sinusoid hepar dan dikurangi
Venous Pressure Gradient). Nilai normal HVPG adalah 3 – 5 mmHg.13 Nilai HVPG ≥
10 mmHg sudah menggambarkan hipertensi portal yang signifikan secara klinis dan ≥ 12 mmHg untuk terjadinya perdarahan varises akut, dan perubahan nilai HVPG yang
terjadi setiap waktu memiliki nilai prediksi untuk perkembangan varises esofagogastrik, resiko perdarahan variseal, perkembangan komplikasi hipertensi portal non – variseal (asites, sindrom hepatorenal, dan ensefalopati), dan
mortalitas.38,39,40,41,42 Pengukuran satu kali sangat bermanfaat dalam menentukan prognosis sirosis kompensata dan dekompensata, sedangkan pengukuran berulang
sangat berguna untuk monitor respon terhadap terapi farmakologi dan progresi penyakit hati. Pada pasien sirosis didapati peningkatan resistensi intrahepatik dan peningkatan aliran darah splanchnik. Faktor awal yang berperan yaitu peningkatan
resistensi intrahepatik sementara peningkatan aliran darah splanchnik meruapakan fenomena sekunder untuk mempertahankan atau memperburuk peningkatan hipertensi
Gambar 2.1 Patogenesis Hipertensi Portal 43
2.2.3. Epidemiologi
Varises dan perdarahan varises merupakan komplikasi sirosis yang diakibatkan
langsung dari hipertensi portal. Pasien dengan sirosis dan varises gastroeseofageal memiliki nilai HVPG setidaknya 10–12 mmHg. Varises gastroesofageal tampak pada
pertama kali, insidensi tahunan terbentuknya varises yang baru rata – rata 7% (berkisar
antara 5–10% per tahun.44,45,46
Tabel 2.3 Epidemiologi Varises Esofagus dan Korelasinya dengan Tingkat Keparahan Penyakit Hati 10
Setelah terbentuknya varises, ukuran varises akan bertambah dari kecil sampai
besar sebelum akhirnya ruptur dan berdarah. Progresi dari varises ukuran kecil hingga menjadi besar masih kontroversial, namun menunjukkan angka laju progresi varises
yang berkisar antara 5–30% per tahun.44,45,46,47 Perdarahan varises pertama memiliki angka insidensi sekitar 4% per tahun, dan resiko ini meningkat menjadi 15% per tahun pada pasien dengan varises ukuran medium sampai besar. Insidensi perdarahan ulang
berkisar antara 30 – 40% pada 6 minggu pertama.46
2.2.4. Perjalanan alamiah varises esofagus
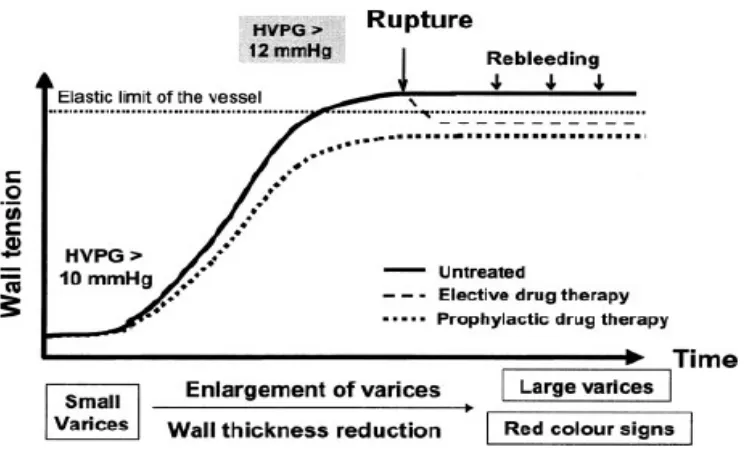
pasien akan memiliki progresi mengalami varises yang kecil. Bertambahnya waktu
dan sejalan dengan peningkatan sirkulasi hiperdinamik, aliran darah yang melalui varises akan meningkat sehingga meningkatkan tekanan pada dinding varises.
Perdarahan varises disebabkan ruptur terjadi ketika bertambahnya ketegangan maksimal pada dinding varises.10 Diameter pembuluh darah merupakan salah satu penentu tekanan variseal. Pada tekanan yang sama, pembuluh darah dengan diameter
besar akan ruptur sedangkan pembuluh darah dengan diameter kecil tidak akan ruptur. Selain diameter pembuluh darah, salah satu penentu tekanan pada dinding varises
adalah tekanan di dalam varix yang berkaitan langsung dengan HVPG. Oleh karena itu, penurunan HVPG seharusnya memicu penurunan tekanan pada dinding varises sehingga mengurangi resiko ruptur. Perdarahan varises tidak akan terjadi ketika
HVPG diturunkan menjadi < 12 mmHg, dan resiko perdarahan ulang juga menurun secara signifikan dengan penurunan HVPG lebih dari 20% nilai awal.13 Faktor lain
yang juga sangat konsisten dengan progresi varises adalah klasifikasi keparahan penyakit hati berdasarkan skor Child – Pugh, dan tampilan red wale marks (didefinisikan sebagai venula yang membesar dan memanjang pada permukaan
Gambar 2.2 Perjalanan Alamiah Varises Esofagus 46
2.2.5. Diagnosis
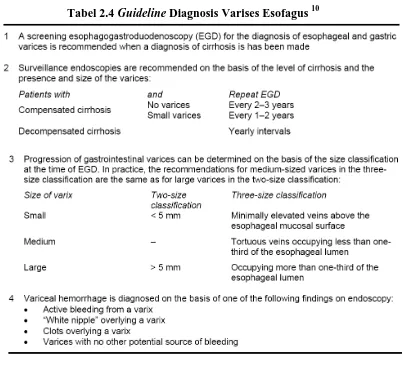
Pemeriksaan esophagogastroduodenoscopy (EGD) merupakan gold standar dalam mendiagnosis varises.13 Konsensus saat ini menyatakan bahwa setiap pasien
sirosis seharusnya menjalani skrining varises dengan endoskopi pada saat diagnosis. Tujuan dari skrining varises esofagus adalah untuk mendeteksi pasien yang memerlukan terapi profilaksis. Pemeriksaan endoskopi sebaiknya diulang setelah 2 – 3
tahun kemudian setelah endoskopi pertama pada pasien tanpa varises. Berdasarkan angka laju progresi besar varises yang berkisar 10 – 15 % per tahun, endoskopi
Tabel 2.4 Guideline Diagnosis Varises Esofagus 10
Telah lama diketahui bahwa gambaran varises secara endoskopi sangat krusial
untuk memprediksi pasien mana yang memiliki resiko tinggi untuk perdarahan varises dan juga yang mana akan memiliki keuntungan dari terapi. Oleh sebab itu dibutuhkan sistem yang divalidasi untuk klasifikasi gambaran varises esofagus secara endoskopi.
Pada tahun 1981, Beppu dkk. telah mengklasifikasikan varises esofagus berdasarkan gambaran endoskopi, dimana karakteristik dari varises yang terjadi diklasifikasikan
Tabel 2.5 Derajat Varises Esofagus dengan Pemeriksaan Endoskopi 49 Beppu’s Endoscopic Grades for Esophageal
Varices
Grade Characteristics of Varices
F1 Small and straight
F2 Moderately sized, tortuous, and occupying less than one third of the lumen
F3 Large, coiled, and occupying one third or more of the lumen
Pada tahun 2004 Japanese Research Society for Portal Hypertension juga telah merancang sistem klasifikasi yang baru untuk menggambarkan varises esofagus, sistem ini menggambarkan varises berdasarkan ukuran, bentuk, dan warna.50
Tabel 2.6 Sistem Klasifikasi Varises Esofagus (Japanese Research Society for
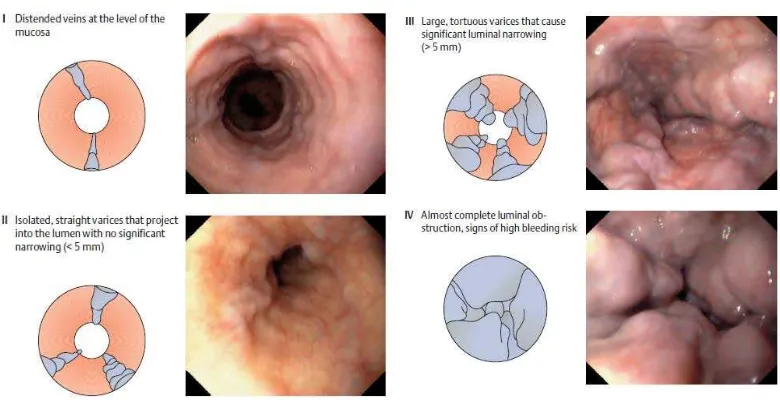
Dengan menggunakan endoskopi didapatkan gambaran varises esofagus
berdasarkan ukuran dan bentuk.
Gambar 2.3 Varises Esofagus dengan Endoskopi 50
2.2.6. Diagnosis varises esofagus non-endoskopi
Pemeriksaan gold standar untuk menegakkan diagnosis varises esofagus
adalah dengan menggunakan endoskopi, namun pemeriksaan endoskopi secara periodik dan berkala sangatlah mahal dan tidak semua pusat pemberi pelayanan
kesehatan terutama di daerah yang memiliki fasilitas endoskopi, serta adanya keterbatasan kompetensi dari seorang dokter untuk melakukan pemeriksaan endoskopi, sehingga dibutuhkan pemeriksaan (marker) non–invasive yang
Berdasarkan konsep bahwa perkembangan hipertensi portal akibat dari
fibrosis hati yang merupakan faktor kontribusi penting terhadap peningkatan resistensi hepatik, marker serum non–invasive dari fibrosis hati telah diuji sebagai prediktor
varises esofagus pada pasien sirosis dengan hasil yang menjanjikan. Beberapa tes yang sebelumnya divalidasi sebagai prediktor fibrosis hati seperti : Lok Score, APRI, Fib – 4, dan Forns index, juga dapat digunakan untuk memprediksi adanya varises
esofagus.18,51
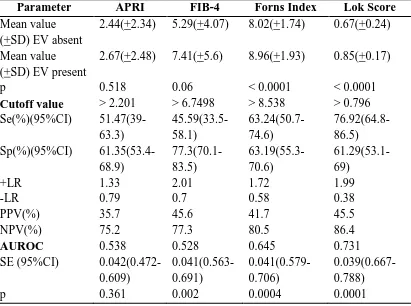
Penelitian mengenai beberapa pemeriksaan marker serum non-invasive
dalam memprediksi adanya varises esofagus pada penderita sirosis hati yang telah dipublikasikan mendapatkan bahwa Lok Score merupakan pemeriksaan non-invasive
terbaik dalam memprediksi adanya varises esofagus dan varises esofagus berukuran besar. Lok score dengan nilai cut-off >0.62 dan >0.796 memiliki sensitivitas (76.16% dan 76.92%) dalam memprediksi adanya varises esofagus dan varises esofagus yang
berukuran besar. namun penelitian tersebut tidak mengikutsertakan indeks FibroQ.51
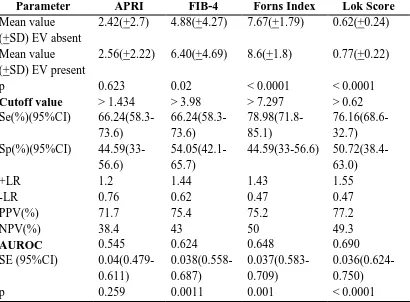
Tabel 2.8 Akurasi Marker Serum Non-invasive dalam Mendeteksi Adanya Varises Esofagus Berukuran Besar 51
Parameter APRI FIB-4 Forns Index Lok Score
Mean value (+SD) EV absent
2.44(+2.34) 5.29(+4.07) 8.02(+1.74) 0.67(+0.24)
2.3. Indeks FibroQ
Indeks FibroQ dikemukakan pertama sekali di tahun 2009 pada penderita hepatitis kronis. Menurut penelitinya, untuk nilai lebih besar dari 1,6 dapat memprediksi adanya fibrosis hati yang signifikan (significant fibrosis/Skor Metavir >2/F2,F3 dan
F4). Sementara untuk nilai lebih kecil dari 0,6 dapat menyingkirkan adanya fibrosis hati yang signifikan. Indeks ini juga dapat memprediksi adanya sirosis hati dengan
nilai > 2,6 dengan sensitivitas mencapai 100% dan spesifisitas 64,9%. Indeks FibroQ juga telah diteliti dan dibandingkan dengan beberapa marker serum non-invasive dalam memprediksi adanya fibrosis hati pada penderita hepatitis C, dimana didapatkan
bahwa indeks FibroQ merupakan pemeriksaan non-invasive terbaik dalam memprediksi adanya fibrosis hati yang signifikan maupun fibrosis hati yang luas
(extensive fibrosis/skor Metavir >3/F3 dan F4) dibandingkan FIB-4, AAR, API dan Lok score dengan nilai cut-off >1,6 untuk fibrosis hati yang signifikan (sensitivitas 77,6%, spesifisitas 65,9%, AUC:0,789 ) dan nilai cut-off >2,6 untuk fibrosis hati yang
Tabel 2.9 Kemampuan Marker-marker Fibrosis Non-invasive dalam Memprediksi Fibrosis yang Signifikan (F2,F3,F4) dan Fibrosis Hati Luas (F3,F4) 52
Sementara penggunaan indeks FibroQ dalam memprediksi ukuran varises esofagus hingga saat ini belum pernah dipublikasikan.
Rumus untuk menghitung Indeks FibroQ adalah: