BAHAN SEMINAR
PENETAPAN KADAR PARASETAMOL, KAFEIN DAN ASETOSAL DALAM SEDIAAN ORAL SECARA SIMULTAN DENGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
OLEH
RIKA KHAIRYAH PANE NIM 071524056
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
PENETAPAN KADAR PARASETAMOL, KAFEIN DAN ASETOSAL DALAM SEDIAAN ORAL SECARA SIMULTAN DENGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
Diajukan oleh :
RIKA KHAIRYAH PANE NIM 071524056
Medan, Nopember 2010
Disetujui Oleh : Disahkan Oleh :
Pembimbing I, Dekan,
Drs. Muchlisyam, M.Si., Apt. Prof. Dr.SumadioHadisahputra, Apt. NIP 195006221980021001 NIP 195311281983031002
Pembimbing II,
PENETAPAN KADAR PARASETAMOL, KAFEIN DAN ASETOSAL DALAM SEDIAAN ORAL SECARA SIMULTAN DENGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
ABSTRAK
Obat dalam betuk kombinasi sering digunakan untuk mengobati berbagai penyakit, termasuk diantaranya penyakit Flu. Kombinasi dari Parasetamol, Kafein dan Asetosal biasanya digunakan untuk memperkuat efek analgetiknya. Obat ini dapat dianalisis secara serempak (simultan) mengunakan metode Kromatografi Cair Kenerja Tinggi (KCKT).
Dalam beberapa literatur menyatakan untuk penetapan kadar campuran dari Parasetamol, Kafein dan Asetosal dapat dilakukan dengan beberapa komposisi fase gerak antara lain: Metanol - Dapar (Natrium Hidrogen fosfat, Tetrabutil Amonium fosfat, Asam fosfat), 3% Asam Asetat, Metanol - Dapar fosfat - Air, dan Dapar Amonium Asetat pH 4 - Metanol. Adapun fase gerak yang dipakai dalam penetapan kadar campuran dari Parasetamol, Kafein dan Asetosal dalam penelitian ini adalah Dapar Amonium Asetat pH 4 dan Metanol.
Analisis ini dilakukan menggunakan kolom Shim-pack VP-ODS (4,6 mm x 25 cm), detektor UV λ= 220 nm. Perbandingan fase gerak Dapar amonium Asetat pH4 -Metanol dengan perbandingan 95:5, 90:10, 80:20, dan 70:30. Dari hasil penelitian diperoleh perbandingan fase gerak yang terbaik adalah 95:5. Kemudian dengan perbandinagan fase gerak yang terpilih dilakukan perbandingan laju alir dari 0,5 ml/menit, 0,6 ml/menit, 0,7 ml/menit dan 0,8 ml/menit. Dari hasil penelitian diperoleh laju alir 0,8 ml/menit memberikan pemisahan dan hasil yang terbaik dengan waktu tambat 5,061 untuk Parasetamol, 7,274 untuk Kafein dan 8,222 untuk Asetosal, resolusi 8,688 dan 3,147; theoritical plate 8268,210 untuk Parasetamol, 10290,787 untuk Kafein dan 10824,424 untuk Asetosal.
Penentuan linieritas kurva kalibrasi menunjukkan hubungan yang linier antara luas puncak dengan konsentrasi, untuk Parasetamol pada konsentrasi 60 sampai 140 µg/ml dengan koefisien korelasi,r = 0.9982 dan persamaan regresi Y = 36915,4095X+533570,21 ; untuk Kafein pada konsentrasi 8 sampai 24 µg/ml dengan koefisien korelasi,r = 0.9997 dan persamaan regresi Y = 84645,7250X+3758,8600 ; untuk Asetosal pada konsentrasi 16 sampai 96 µg/ml dengan koefisien korelasi,r = 0.9994 dan persamaan regresi Y = 7028,4623X-1874,5674.
Parasetamol 1,67 mcg/ml dan 5,54 mcg/ml, untuk Kafein 0,45 mcg/ml dan 1,50 mcg/ml dan untuk Asetosal 7,43 mcg/ml dan 24,75 mcg/ml.
Hasil penelitian menunjukkan dengan menggunakan fase gerak Dapar Amonium Asetat pH4 - Metanol dapat digunakan untuk penetapan kadar dari campuran Parasetamol, Kafein dan Asetosal.
DETERMINATION OF PARACETAMOL, CAFFEIN AND ACETOSAL CONCENTRATIONS IN ORAL PREPARATION SIMULTANEOUSLY BY
HIGH – PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC)
ABSTRACT
The combined medications have been often used to treat a variety of diseases, in cluding, among others, flu. The combination of paracetamol, caffein and acetosal was neously by using High – Performance Liquid cromatography (HPLC).
Some literatures have suggested that determination of mixed concentration from Paracetamol, Caffein adn Acetosal could be made through several movable phase compositions including : Metanol – Dapar (Natrium Hydrogen Phosphate, Tetrabutyl Ammonium Phosphate, Acid Phosphate), 3% Acid acetat, Metanol – Dapar Phosphate – Water, and Dapar Ammonium Acetat pH 4 – Metanol. The movable phase used in determination of mixed concentrations from Parasetamol, Caffein and Acetosal in this research was Dapar Ammonium Acetat pH 4 and Metanol.
This analysis was by using Shim – pack VP-ODS coloumn (4,5 mm x 25 cm), detector UV = 220 nm. The ratio of movable phase of Ammonium Acetat pH 4 – Metanol was 95:5, 90:10, 80:20, 70:20. The result of research indicated that the best movable phase was 95:5 and then, with selected movable phase comparison, the flow rate comparison of 0,5 ml/m, 0,6 ml/m, 0,7 ml/m and 0,8 ml/m was conducted. The flow rate of 0,8 ml/m resulted in isolation and best result with delay time 5.061 for Paracetamol, 7.274 for Caffein and 8.222 for Acetosal, resolution 8.688 and 3.147 ; theoritical plate 8268.210 for Parasetamol, 10290.787 for Caffein and 10824.424 for Acetosal.
The linearity determination of calibration curve indicated a linear correlation between peak width to concentration, for Parasetamol in concentration of 60 to 140 µg/ml with coefficient of correlation, r = 0,9982 and regression equation Y = 36915.4095 X + 5333570.21 ; for Caffein in concentration of 8 to 24 µg/ml with coefficient of correlation, r = 0.9997 and regression equation Y = 84645.7250 X + 3758.8600; for Acetoal in concentration Y = 7028.4623 X – 1874.5674.
mcg/ml and 5.54 mcg/ml; for Caffein 0.45 mcg/ml and 1.50 mcg/ml ; and for Acetosal 7.43 mcg/ml and 24.75 mcg/ml, respectively.
The result of research indicated that movable phase of Dapar Ammonium Acetat pH 4 – Metanol could be used to determine the mixed concentration of Parasetamol, Caffein and Acetosal.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN... ii
ABSTRAK ... iii
ABSTRACT ... v
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat penelitian ... 4
BAB II METODOLOGI PENELITIAN ... 5
2.1 Alat-alat ... 5
2.2 Bahan-bahan ... 5
2.3 Sampel ... 5
2.4 Rancangan Penelitian ... 6
2.4.2 Penyiapan Bahan ... 6
2.4.2.1 Pembuatan Dapar Asetat ... 6
2.4.2.2 Pembuatan Pelarut ... 6
2.4.2.3 Pembuatan Fase Gerak ... 6
2.4.2.4 Pembuatan Larutan Induk Baku Parasetamol ... 7
2.4.2.5 Pembuatan Larutan Induk Baku Kafein ... 7
2.4.2.6 Pembuatan Larutan Induk Baku Asetosal ... 7
2.4.3 Prosedur Analisis ... 7
2.4.3.1 Penyiapan Alat KCKT... 7
2.4.3.2 Penentuan Komposisi Fase Gerak Dapar Amonium Asetat pH 4 : Metanol dan Laju Alir yang Optimum ... 8
2.4.3.3 Analisis Kualitatif ... 8
2.4.3.4 Analisis Kuantitatif ... 8
2.4.3.4.1 Penentuan Linieritas Kurva Kalibrasi Baku Pembanding Parasetamol, Kafein dan Asetosal ... 8
2.4.3.4.2 Penetapan Kadar Parasetamol, Kafein dan Asetosal dalam Sampel... 9
2.4.3.5 Analisis Data Penetapan Kadar secara Statistik.. 10
2.4.4 Metode Validasi ... 11
2.4.4.1 Akurasi ... 11
2.4.4.2 Presisi ... 12
BAB III HASIL DAN PEMBAHASAN ... 13
BAB IV KESIMPULAN DAN SARAN ... 27
4.1 Kesimpulan ... 27
4.2 Saran ... 27
DAFTAR PUSTAKA ... 28
DAFTAR TABEL
Halaman
Tabel 1 Data hasil analisis Parasetamol, Kafein dan Asetosal baku
pada berbagai perbandingan dengan komposisi fase
gerak dan laju alir.. ... 17
Tabel 2 Data hasil analisis Parasetamol, Kafein dan Asotosal baku
Pada berbagai Laju Alir dengan fase gerak Dapar Amonium.. ...
Asetat pH 4 – Metanol (95 : 5) ... 18
Tabel 3 Hasil Pengukuran kadar sediaan Tablet dan Puyer dari campuran
Parasetamol Kafein dan Asetosal ... 24
Tabel 4 Hasil penetapan kadar Parasetamol, Kafein dan Asetosal
dalam berbagai sediaan tablet dan puyer ... 24
Tabel 5 Data hasil pengujian Akurasi dan Presisi Parasetamol dengan
Metode penambahan baku ... 25
Tabel 6 Data hasil pengujian Akurasi dan Presisi Kafein dengan metode
Penambahan baku... 25
Tabel 7 Data hasil Akurasi dan Presisi Asetosal dengan metode
DAFTAR GAMBAR
Halaman
Gambar 1 Spektrum Inframerah dari Parasetamol baku . ... 13
Gambar 2 Spektrum Inframerah dari Kafein baku. ... 14
Gambar 3 Spektrum Inframerah dari Asetosal baku... 15
Gambar 4 Kromatogram Analisis campuran Parasetamol, Kafein dan Asetosal dengan fase gerak Dapar Amonium Asetat pH 4 dan
Metanol (80:20) dan laju alir 0,8 ml/menit. ... 16
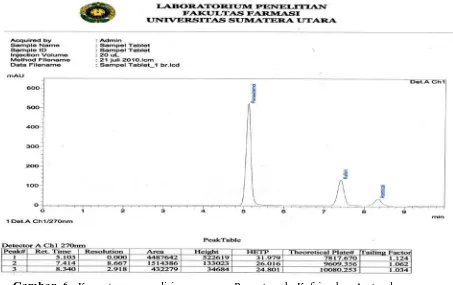
Gambar 5. Kromatogram Analisis campuran Parasetamol, Kafein dan Asetosal dengan fase gerak Dapar Amonium Asetat pH 4 dan
Metanol (95:5) dan laju alir 0,8 ml/menit. ... 19
Gambar 6. Kromatogram Analisis campuran Parasetamol, Kafein dan Asetosal dengan fase gerak Dapar Amonium Asetat pH 4 dan
Metanol (95:5) dan laju alir 0,8 ml/menit. ... ... 20
Gambar 7 Kurva Kalibrasi Parasetamol baku menggunakan KCKT dengan fase gerak Dapar Amonium Asetat pH 4 dan Metanol (95:5) dan laju alir 0,8ml/menit. ... 21
Gambar 8 Kurva Kalibrasi Kafein baku menggunakan KCKT dengan fase gerak Dapar Amonium Asetat pH 4 dan Metanol (95:5) dan laju alir 0,8ml/menit. ... 22
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Alat KCKT (Shimadzu), kolom, pre kolom dan Syringe 100 µl.. .. 29
Lampiran 2. Gambar alat ultrasonic cleaner dan penyaring.. ... 30
Lampiran 3. Spektrum Inframerah Parasetamol pada literatur Pharmaceutical Sub Stance (UV/IR).. ... 31
Lampiran 4. Spektrum Inframerah Kafein pada literatur Pharmaceutical
Sub Stance (UV/IR).. ... 32
Lampiran 5. Spektrum Inframerah Asetosal pada literatur Pharmaceutical
Sub Stance (UV/IR).. ... 33
Lampiran 6. Kromatogram Penyuntikan Parasetamol, Kafein dan Asetosal baku untuk mencari Perbandingan fase gerak Dapar Amonium
Asetat pH 4 dan Metanol untuk analisis ... 34
Lampiran 7. Kromatogram Penyuntikan Parasetamol, Kafein dan Asetosal baku dalam upaya mencari Laju Alir yang Optimum untuk
Analisis ... 36
Lampiran 8. Kromatogram Penyuntikan Parasetamol, Kafein dan Asetosal
pada pembuatan kurva Kalibrasi ... 38
Lampiran 9. Perhitungan persamaan regresi dari kurva kalibrasi
Parasetamol, Kafein dan Asetosal yang diperoleh pada KCKT pada Panjang gelombang 257 nm ... 41
Lampiran 10. Kromatogram hasil penyuntikan Tablet Poldan Mig
(PT. Sanbe Farma) ... 49
Lampiran 11. Analisis data statistik untuk mencari kadar Parasetamol, Kafein dan Asetosal sebenarnya dari Tablet Poldan Mig
(PT. Sanbe Farma) ... 51
Lampiran 12. Kromatogram hasil penyuntikan Puyer Bintang Toedjoe
(PT. Bintang Toedjoe) ... 55
Lampiran 13. Analisis data statistik untuk mencari kadar Parasetamol, Kafein dan Asetosal sebenarnya dari Puyer Bintang Toedjoe
Lampiran 14. Kromatogram hasil persen perolehan kembali dari sampel
Poldan Mig (PT. Sanbe Farma).. ... 61
Lampiran 15. Data hasil perolahan kembali Parasetamol , Kofein dan Asetosal Pada Tablet Poldan Mig (PT. Sanbe Farma) dengan metode penambahan baku ... 66
Lampiran 16. Analisa data statistik persen perolehan kembali pada Tablet Poldan Mig (PT. Sanbe Farma).. ... 68
Lampiran 17. Contoh perhitungan penimbangan sampel.. ... 73
Lampiran 18. Contoh perhitungan kadar perolehan kembali dengan metode penambahan bahan baku. ... 75
Lampiran 19. Contoh Perhitungan persen perolehan kembali ... 76
Lampiran 20 Contoh Perhitungan Kadar Kombinasi ... 80
Lampiran 21. Daftar spesifikasi sampel.. ... 81
Lampiran 22. Sertifikat pengujian Parasetamol BPFI.. ... 82
Lampiran 23. Sertifikat pengujian Kafein BPFI.. ... 83
Lampiran 24. Sertifikat pengujian Asetosal BPFI.. ... 84
Lampiran 25. Sertifikat pengujian Parasetamol baku... 85
Lampiran 26. Sertifikat pengujian Kafein baku.. ... 86
Lampiran 27. Sertifikat pengujian Asetosal baku... 87
DETERMINATION OF PARACETAMOL, CAFFEIN AND ACETOSAL CONCENTRATIONS IN ORAL PREPARATION SIMULTANEOUSLY BY
HIGH – PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC)
ABSTRACT
The combined medications have been often used to treat a variety of diseases, in cluding, among others, flu. The combination of paracetamol, caffein and acetosal was neously by using High – Performance Liquid cromatography (HPLC).
Some literatures have suggested that determination of mixed concentration from Paracetamol, Caffein adn Acetosal could be made through several movable phase compositions including : Metanol – Dapar (Natrium Hydrogen Phosphate, Tetrabutyl Ammonium Phosphate, Acid Phosphate), 3% Acid acetat, Metanol – Dapar Phosphate – Water, and Dapar Ammonium Acetat pH 4 – Metanol. The movable phase used in determination of mixed concentrations from Parasetamol, Caffein and Acetosal in this research was Dapar Ammonium Acetat pH 4 and Metanol.
This analysis was by using Shim – pack VP-ODS coloumn (4,5 mm x 25 cm), detector UV = 220 nm. The ratio of movable phase of Ammonium Acetat pH 4 – Metanol was 95:5, 90:10, 80:20, 70:20. The result of research indicated that the best movable phase was 95:5 and then, with selected movable phase comparison, the flow rate comparison of 0,5 ml/m, 0,6 ml/m, 0,7 ml/m and 0,8 ml/m was conducted. The flow rate of 0,8 ml/m resulted in isolation and best result with delay time 5.061 for Paracetamol, 7.274 for Caffein and 8.222 for Acetosal, resolution 8.688 and 3.147 ; theoritical plate 8268.210 for Parasetamol, 10290.787 for Caffein and 10824.424 for Acetosal.
The linearity determination of calibration curve indicated a linear correlation between peak width to concentration, for Parasetamol in concentration of 60 to 140 µg/ml with coefficient of correlation, r = 0,9982 and regression equation Y = 36915.4095 X + 5333570.21 ; for Caffein in concentration of 8 to 24 µg/ml with coefficient of correlation, r = 0.9997 and regression equation Y = 84645.7250 X + 3758.8600; for Acetoal in concentration Y = 7028.4623 X – 1874.5674.
mcg/ml and 5.54 mcg/ml; for Caffein 0.45 mcg/ml and 1.50 mcg/ml ; and for Acetosal 7.43 mcg/ml and 24.75 mcg/ml, respectively.
The result of research indicated that movable phase of Dapar Ammonium Acetat pH 4 – Metanol could be used to determine the mixed concentration of Parasetamol, Caffein and Acetosal.
BAB I PENDAHULUAN
1.1 Latar Belakang
Campuran Parasetamol, Kafein dan Asetosal banyak ditemukan dalam
kombinasi obat Flu yang beredar di pasaran. Parasetamol merupakan salah satu
obat Non-Steroid Anti-Inflammatory Drugs (NSAIDs) yang secara luas digunakan
dalam pengobatan demam dan mengurangi rasa sakit. Kafein merupakan stimulan
sistem saraf pusat, dan Asetosal merupakan obat anti nyeri dan anti demam juga.
Ketiga zat ini sering dikombinasikan untuk memperkuat efek analgetisnya (Tjay
dan Rahardja, 2002).
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi karena didukung oleh kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif
dan beragam sehingga mampu menganalisis berbagai cuplikan secara kualitatif
maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Ditjen
POM,1995).
Keberhasilan pemisahan dan teknik analisis pada metode KCKT
tergantung pada pemilihan cara kromatografi yang tepat, kombinasi fase diam dan
fase gerak yang sesuai, serta faktor-faktor lainnya seperti kolom, detektor,
kemampuan sistem pompa dan sistem pengolahan data. Untuk keperluan analisis
kimia maupun memperoleh kondisi yang diinginkan dalam kromatografi, perlu
efisiensi kolom, resolusi, faktor ikutan yang banyak dipengaruhi oleh fase diam
dan fase gerak dalam kolom (Sudaryo, 2001).
Dalam beberapa literatur dikatakan untuk penetapan kadar Parasetamol,
Kafein dan Asetosal dapat dilakukan dengan beberapa komposisi fase gerak yang
antara lain adalah : Metanol - Dapar (Natrium Hidrogen fosfat, Tetrabutil
Amonium fosfat, Asam fosfat), 3% Asam Asetat, Metanol - Dapar fosfat - Air,
dan Dapar Amonium Asetatat pH 4 - Matanol.
Berdasarkan hal tersebut diatas, penulis tertarik untuk melakukan
penetapan kadar dengan metode KCKT menggunakan kolom Shim-pack
VP-ODS (4,6 mm x 25 cm). Penetapan kadar dilakukan terhadap perbandingan fase
gerak Dapar Amonium Asetat pH 4 – Metanol.
Metode KCKT mempunyai beberapa keuntungan dibanding metode
analisis lain, diantaranya kolom dapat digunakan kembali, memiliki berbagai jenis
detector, waktu analisis umumnya relatif singkat, ketetapan dan ketelitian relative
tinggi serta dapat digunakan untuk menganalisis kebanyakan senyawa kimia
(Meyer, 2004).
Untuk memperoleh validasi metode ini, maka dilakukan uji akurasi yang
dinyatakan dalam persen perolehan kembali (% recovery) dan uji presisi yang
dinyatakan dalam Relative Stadart Deviation (RSD). Kemudian ditentukan batas
deteksi (limit of detection) dan batas kuatitasi (limit of quantitation) (Epshtein,
1.2 Perumusan Masalah
1. Apakah fase gerak Dapar Amonium Asetat pH 4 – Metanol dapat
memisahkan campuran Paracetamol, Kafein dan Asetosal dalam tablet
dengan menggunakan KCKT ?
2. Berapa perbandingan fase gerak Dapar Amonium Asetat pH 4 – Metanol
dalam analisis campuran Paracetamol, Kafein dan Asetosal ?
3. Apakah komposisi fase gerak Dapar Amonium Asetat pH 4 – Metanol
dapat digunakan dalam penetapan kadar dan validasi campuran
Paracetamol, Kafein dan Asetosal ?
1.3 Hipotesis
1. Metode KCKT dengan fase gerak Dapar Amonium Asetat pH 4 – Metanol
dapat memisahkan campuran Paracetamol, Kafein dan Asetosal dalam
sediaan.
2. Fase gerak Dapar Amonium Asetat pH 4 – Metanol pada perbandingan
tertentu dapat memisahkan campuran Paracetamol, Kafein dan Asetosal
dalam sediaan.
3. Komposisi fase gerak yang diperoleh dapat digunakan untuk penetapan
kadar campuran Paracetamol, Kafein dan Asetosal dalam sediaan.
1.4 Tujuan Penelitian
1. Melakukan pemisahan campuran Paracetamol, Kafein dan Asetosal
dengan metode Kromatografi Cair Kinerja Tinggi ( KCKT ) menggunakan
2. Mencari perbandingan komposisi fase gerak Dapar Amonium Asetat pH 4
– Metanol untuk memisahkan campuran Paracetamol, Kafein dan Asetosal
dalam sediaan.
3. Melakukan pengujian fase gerak Dapar Amonium Asetat pH 4 - Metanol
yang digunakan dalam penetapan kadar campuran Parasetamol, Kafein
dan Asetosal.
1.5 Manfaat Penelitian
Diharapkan fase gerak Dapar Amonium Asetat pH 4 – Metanol yang
terpilih dalam penelitian ini dapat digunakan oleh industri farmasi untuk analisis
BAB II
TINJAUAN PUSTAKA
2.1 PARASETAMOL 2.1.1 Sifat Fisikokimia
Rumus struktur :
Nama Kimia : 4- Hidroksiasetanilida
Rumus Molekul : C8H9NO2
Berat Molekul : 151,16
Pemerian : serbuk, putih, tidak berbau, rasa sedikit pahit.
Kelarutan : larut dalam air mendidih dan dalam natrium hidroksida 1 N,
mudah larut dalam etanol. (Depkes RI, 1995).
2.1.2 Farmakokinetik A. Absorpsi
Parasetamol diberikan secara oral, diserap dengan baik melalui saluran
cerna. Penyerapan dihubungkan dengan tingkat pengosongan lambung.
Konsentrasi darah puncak biasanya tercapai dalam 30 - 60 menit. Parasetamol
sedikit terikat pada protein plasma dan sebagian dimetabolisme oleh enzim
B. Efek Samping
Pada dosis terapi normal, asetaminofen bebas dari efek samping
bermakna. Kemerahan pada kulit dan reaksi alergi minor pada jumlah leukosit,
tetapi ini umumnya selintas. Nekrosis tubular ginjal dan koma hipoglikemia
merupakan komplikasi yang jarang dari terapi dosis besar jangka lama.
Asetaminofen dosis besar menyebabkan persediaan glutation di hati berkurang
dan N-asetil-benzokuinoneimin bereaksi dengan grup sulfihidril protein hati,
membentuk ikatan kovalen. Dapat terjadi nekrosis hati, suatu kondisi yang sangat
serius dan berpotensi mengancam kehidupan.
2.1.3 Kegunaan
Asetaminofen merupakan pengganti yang baik untuk analgesik dan antipiretik
aspirin pada penderita dengan keluhan saluran cerna dan pada mereka dengan
perpanjangan waktu perdarahan yang tidak menguntungkan. Asetaminofen
merupakan analgetik dan antipiretis. Asetaminofen tidak mengantagonis obat
urikosurik probenesid dan karena itu dapat digunakan pada penderita gout yang
mendapatkan obat itu.
2.2 KOFEIN
2.2.1 Sifat Fisikokimia
Rumus struktur :
Nama Kimia : 1,3,7-Trimetil xantin
Berat Molekul : 194,19
Pemerian : serbuk putih atau bentuk jarum mengkilat putih,biasanya
menggumpal, tidak berbau, rasa pahit.
Kelarutan : Agak sukar larut dalam air, dalam etanol, mudah larut dalam
kloroform, sukar larut dalam eter. (Depkes RI, 1995).
2.2.2 Farmakokinetik A. Absorpsi
Kafein per oral mudah diabsorbsi. Kafein tersebar ke seluruh tubuh
termasuk otak. Obat dapat melewati plasenta janin dan disekresikan ke dalam
ASI. Dimetabolisme di hati dan metabolitnya dikeluarkan di dalam urin.
B. Efek Samping
Kafein dosis sedang menyebabkan insomnia, ansietas dan agitasi. Dosis
tinggi diperlukan untuk memperlihatkan toksisitas berupa muntah dan konvulsi.
Dosis letal sekitar 10 g (kira-kira 100 cangkir kopi) yang menimbulkan aritmia
jantung. Kematian karena kafein sangat tidak mungkin. Letargi, iritabel dan sakit
kepala terjadi pada pengguna yang secara rutin minumg lebih dari 600 mg kopi
per hari ( sekitar 6 cangkir kopi per hari) dan mendadak berhenti. (Mycek, 2001).
2.2.3 Kegunaan
Kofein berkhasiat menstimulasi SSP, dengan efek menghilangkan rasa
letih, lapar dan mengantuk, juga daya konsentrasi dan kecepatan reaksi
dipertinggi, prestasi otak dan suasana jiwa diperbaiki. Kofein juga memperkuat
kontraksi jantung, vasodilatasi perifer dan diuretis. Kofein digunakan sebagai
penyegar. Zat ini sering dikombinasikan dengan Parasetamol atau asetosal untuk
2.3 ASETOSAL 2.3.1 Sifat Fisikokimia
Rumus struktur :
Nama Kimia : Asam asetat salisilat
Rumus Molekul : C9H8O4
Berat Molekul : 180,16
Pemerian : Hablur putih, umumnya seperti jarum atau lempengan
tersususun, atau serbuk hablur putih,tidak berbau atau berbau
lemah. Stabil di udara kering; di dalam udara lembab secara
bertahap terhidrolisa menjadi asam salisilat dan asam asetat.
Kelarutan : Agak sukar larut dalam air, mudah larut dalam etanol, larut
dalam kloroform dan dalam eter, agak sukar larut dalam
eter mutlak. (Depkes RI, 1995).
2.3.2 Farmakokinetik A. Absorpsi
Cepat dan praktis lengkap terutama dibagian pertama duodenum. Namun
karena bersifat asam sebagian zat diserap juga di lambung.
B. Efek Samping
Paling sering terjadi berupa iritasi mukosa lambung dengan risiko tukak
lambung dan pendarahan samar (occult).
2.3.3 Kegunaan
Selain sebagai analgetikum, Asetosal dewasa ini banyak di gunakan
sebagai alternatif dari antikoagulansia sebagai obat pencegah infark kedua setelah
terjadi serangan.Hal ini berkat daya antitrombotisnya.
2.3 Kromatografi
Dalam analisis kimia pada umumnya, komponen (zat) yang dianalisa harus
dipisahkan terlebih dahulu dari komponen lain atau zat pengganggu yang ada, lalu
dipekatkan, kemudian baru diidentifikasi atau diukur kuantitasnya. Banyak teknik
pemisahan zat yang digunakan, tetapi kromatografi adalah teknik yang paling
banyak dipakai, terutama untuk campuran yang kompleks. Suatu komponen
campuran yang tidak mungkin dipisahkan dengan cara yang lain, menggunakan
kromatografi dapat diselesaikan dalam waktu yang singkat dengan peralatan yang
relatif sederhana. Lebih dari itu, karena sifat pemisahannya yang spesifik, maka
selain digunakan sebagai metode pemisahan, kromatografi juga merupakan
metode penentuan zat baik kualitatif maupun kuantitatif.
Kromatografi dapat didefinisikan sebagai suatu teknik pemisahan zat
berdasarkan perbedaan kecepatan migrasi yang berlangsung dalam suatu sistem
yang terdiri dari dua macam fasa, dimana salah satu fasa bergerak atas fasa
Kromatografi apapun bentuknya mempunyai 2 macam fasa, yaitu fasa diam
dan fasa gerak. Berdasarkan jenis fasa gerak yang digunakan, kromatografi
dibedakan atas 2 golongan besar yaitu kromatografi gas bila fasa geraknya gas
dan kromatografi cair bila fasa geraknya cairan.
Pada kromatografi gas, fasa diam selalu ditempatkan di dalam kolom. Fasa
diam itu dapat berupa padatan atau cairan yang diemban oleh butiran halus zat
padat pendukung. Karena itu berdasarkan wujud fasa diamnya, kromatografi gas
dapat dibedakan atas kromatografi gas padat dan kromatografi gas cair.
Pada kromatografi cair, selain ditempatkan dikolom, fasa diam dapat pula
ditebarkan berupa lapis tipis diatas permukaan suatu pelat dari kaca yang disebut
kromatografi lapis tipis. Selain itu dapat pula menggunakan secarik kertas sebagai
fasa diamnya yang disebut kromatografi kertas. Kromatografi lapis tipis dan
kromatografi kertas dilakukan untuk membedakannya dari kromatografi yang
dilakukan di dalam sebuah kolom, yang dinamakan kromatografi kolom. Didalam
kromatografi cair pun dikenal pula kromatografi padat dan kromatografi
cair-cair, tergantung pada fasa diam yang digunakan. Selain berdasarkan wujud fasa
gerak dan fasa diam yang digunakan, kromatografi dapat dibedakan berdasarkan
mekanisme interaksi yang terjadi antara fasa diam dan komponen campuran yang
dipisahkan. Maka dikenal kromatografi adsorbsi, kromatografi partisi,
kromatografi penukar ion dan kromatografi eksklusi atau permiasi gel.
Mekanisme interaksi yang paling banyak dijumpai dilaboratorium adalah
adsorbsi dan partisi. Pada proses adsorbsi, molekul pelarut dan molekul zat
terlarut menempati permukaan zat padat pengadsorbsi (adsorbent). Dalam
oleh zat cair. Distribusi komponen dalam fasa diam itu karena daya larutnya. Pada
kromatografi cair, misalnya Kromatografi cair Kinerja Tinggi(KCKT), molekul
senyawa yang digunakan sebagai fasa diam diikatkan secara kimia pada
permukaan pertikel pendukung, menghasilkan kromatografi fasa terikat.
Berdasarkan perbandingan polaritas antara fasa diam dan fasa geraknya dikenal
kromatografi fasa normal bila fasa diam lebih polar dari fasa geraknya,
kromatografi fasa terbalik bila fasa gerak lebih polar daripada fasa diamnya.
Karena fasa diam yang digunakan tidak sebanyak pada kromatografi gas, maka
selektifitas pemisahan lebih mudah diperbaiki dengan merubah komposisi fasa
gerak. (Sudaryo, 2001).
2.4 Kromatografi Cair Kinerja Tinggi
Kromatogarfi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi karena didukung oleh kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif
dan beragam sehingga mampu menganalisa berbagai cuplikan secara kualitatif
maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Depkes RI,
1995).
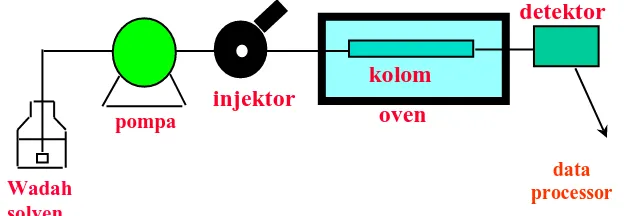
2.4.1 Komponen Kromatografi cair kinerja tinggi
Gambar 2.1. Bagan alat KCKT
pompa
injektor
kolom
oven
detektor
Wadah solven
2.4.2 Wadah Fase gerak
Wadah fase gerak terbuat dari bahan yang inert terhadap fase gerak. Bahan
yang umum digunakan adalah gelas dan baja anti karat. Daya tampung tandon
harus lebih besar dari 500 ml, yang dapat digunakan selama 4 jam untuk
kecepatan alir yang umumnya 1-2 ml/menit.
2.4.3 Pompa
Untuk menggerakkan fase gerak melalui kolom diperlukan pompa. Pompa
harus mampu menghasilkan tekanan 6000 Psi pada kecepatan alir 0,1–10
ml/menit. Pompa ada 2 jenis yaitu pompa volume konstan dan pompa tekanan
konstan. Pompa terbuat dari bahan yang inert terhadap semua pelarut. Bahan yang
umum digunakan adalah gelas baja antikarat dan teflon. Aliran pelarut dari pompa
harus tanpa denyut untuk menghindari hasil yang menyimpang pada detektor.
2.4.4 Injektor
Cuplikan harus dimasukkan ke dalam pangkal kolom (kepala kolom),
diusahakan agar sesedikit mungkin terjadi gangguan pada kemasan kolom.
Ada tiga jenis dasar injektor, yaitu:
a. Hentikan aliran/stop flow: Aliran dihentikan, injeksi dilakukan pada
kinerja atmosfir, sistem tertutup, dan aliran dilanjutkan lagi. Tehnik ini
bisa digunakan karena difusi di dalam aliran kecil dan resolusi tidak
dipengaruhi.
b. Septum: Injektor-injektor langsung ke aliran fase gerak umumnya sama
dengan yang digunakan pada kromatografi gas. Injektor ini dapat
tahan dengan semua pelarut-pelarut kromatografi cair. Disamping itu,
partikel kecil dari septum yang terkoyak (akibat jarum injektor) dapat
menyebabkan penyumbatan.
c. Katup putaran (loop valve): ditunjukkan secara skematik dalam Gambar 6,
tipe injektor ini umumnya digunakan untuk menginjeksi volume lebih
besar dari pada 10 µ l dan sekarang digunakan dengan cara automatis
(dengan adaptor khusus, volume-volume lebih kecil dapat diinjeksikan
secara manual). Pada posisi LOAD, sampel loop (cuplikan dalam putaran)
diisi pada tekanan atmosfir. Bila katup difungsikan, maka cuplikan di
dalam putaran akan bergerak ke dalam kolom.
Gambar 2.2 Tipe injektor katup putaran
2.4.5 Kolom
Kolom adalah jantung kromatografi. Berhasil atau gagalnya suatu analisis
tergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom
dapat dibagi menjadi dua kelompok:
• Kolom analitik: diameter khas adalah 2-6 mm. Panjang kolom tergantung
pada jenis kemasan. Untuk kemasan pelikular, panjang yang lumrah
adalah 50-100 cm. Untuk kemasan poros mikropartikilat, umumnya 10-30
• Kolom preparatif: umumnya memiliki diameter 6 mm atau lebih besar dan
panjang kolom 25 -100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan
pada temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi,
terutama untuk kromatografi penukar ion dan kromatografi eksklusi. Kemasan
kolom tergantung pada mode kromatografi cair kinerja tinggi yang digunakan.
2.4.6 Detektor
Detektor pada KCKT dikelompokkkan menjadi 2 golongan yaitu: \
• Detektor universal: Mampu mendeteksi zat secara umum, tidak bersifat
spesifik, dan tidak bersifat selektif, seperti detektor indeks bias dan
detektor spektrometri massa.
• Detektor spesifik: Hanya mendeteksi analit secara spesifik dan selektif,
seperti detektor UV-Vis, detektor fluoresensi dan elektrokimia
(Rohman,2007).
2.4.7 Fase Gerak
Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat
bercampur yang secara keseluruhan berperan dalam daya elusi dan resolusi. Daya
elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase
diam, dan sifat komponen-komponen sampel (Johnson dan Stevenson, 1991;
Munson, 1991 dan Rohman, 2007).
Terdapat keragaman yang luas dari solvent yang digunakan dalam semua
mode Kromatografi Cair Kinerja Tinggi, tetapi ada beberapa sifat yang diinginkan
Fase gerak harus:
• Murni; tidak ada pencemar/kontaminan
• Tidak bereaksi dengan pengemas
• Sesuai dengan detektor
• Melarutkan cuplikan
• Mempunyai viskositas rendah
• Mudah rekoveri cuplikan, bila diinginkan
• Tersedia diperdagangan dengan harga yang pantas
(Putra, 2003)
Elusi gradien dan isokratik
Elusi pada kromatografi cair kinerja tinggi dapat dibagi menjadi dua
sistem yaitu:
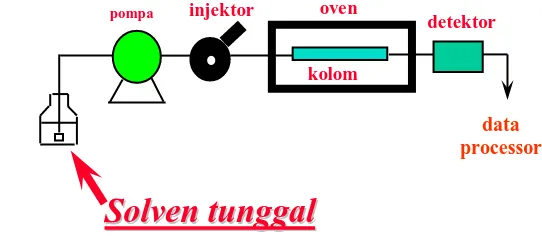
1. Sistem elusi isokratik. Pada sistem ini, elusi dilakukan dengan satu macam
atau lebih fase gerak dengan perbandingan tetap (komposisi fase gerak
tetap selama elusi)
[image:30.595.160.431.508.626.2]
Gambar 2.3 Sistem elusi isokratik
2. Sistem elusi gradien. Pada sistem ini, elusi dilakukan dengan campuran
fase gerak yang perbandingannya berubah-ubah dalam waktu tertentu
(komposisi fase gerak berubah-ubah selama elusi).
pompa injektor
kolom oven
detektor
S
S
o
o
l
l
v
v
e
e
n
n
t
t
u
u
n
n
g
g
g
g
a
a
l
l
2.4.8 Pengolahan Data
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai
puncak-puncak yang secara keseluruhan disebut sebagai kromatogram.
Gambar 2.4 Kromatogram
Guna kromatogram:
1. Kualitatif
waktu retensi selalu konstan dalam setiap kondisi kromatografi yang sama.
dapat digunakan untuk identifikasi.
2. Kuantitatif
luas puncak proporsional dengan jumlah sampel yang diinjesikan dan
dapat digunakan untuk menghitung konsentrasi.
3. Kromatogram dapat digunakan untuk mengevaluasi efisiensi pemisahan
dan kinerja kolom
2.5 Parameter Kromatografi Cair Kinerja Tinggi
Ada beberapa parameter yang perlu diperhatikan dalam memperoleh
kondisi yang diinginkan dalam kromatografi antara lain :
a. Waktu Retensi
W W1/2
H1/2 H
Rt
Waktu yang dibutuhkan suatu komponen untuk melewati suatu kolom
disebut waktu retensi yang dapat didefinisikan sebagai waktu yang diperlukan
untuk membawa keluar suatu komponen dari dalam kolom, dihitung mulai
diinjeksikan hingga keluar kolom tepat pada saat konsentrasi maksimum.
2. Faktor Selektifitas
Suatu kolom dinyatakan baik apabila kolom tersebut cukup selektif, dan
dikatakan selektif apabila kolom tadi mampu menahan berbagai komponen
dengan kekuatan yang berbeda-beda.
3. Efisiensi Kolom
Jumlah plat teoritik dalam suatu kolom sebanding dengan panjang kolom.
Karena itu jumlah plat teoritik suatu kolom dapat ditingkatkan dengan
memperpanjang kolom. Makin panjang kolom makin banyak jumlah plat
teoritiknya maka makin sempurna pemisahan.
4. Resolusi
Derajat pemisahan atau resolusi dari dua pita yang berdekatan
didefinisikan sebagai jarak antara puncak-puncak pita (atau pusat-pusat) dibagi
dengan luas pita rata-rata. Semakin tinggi harga N selalu memberikan resolusi
yang membaik. Oleh karena itu resolusi dapat diperbaiki dengan menambah
panjang kolom. (Putra, 2003).
5. Faktor Ikutan
Keasimetrisan puncak dinyatakan dengan faktor ikutan atau faktor
belakang disebut tailing, sebaliknya puncak yang landai bagian depan dan curam
bagian belakang disebut fronting.
2.6 Validasi
Validasi metode menurut United States Pharmacopeia (USP) dilakukan
untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel dan tahan
pada kisaran analit yang akan dianalisis. Suatu metode analis harus divalidasi
untuk verifikasi bahwa parameter-parameter kinerjanya cukup mampu untuk
mengatasi masalah dalam analisis. Parameter analisis yang ditentukan pada
validasi adalah akurasi, presisi, batas deteksi, batas kuantitasi, spesifikasi,
linieritas dan rentang, kekasaran (Ruggedness) dan ketahanan (Robutness).
Akurasi merupakan ketelitian metode analisis atau kedekatan antara nilai
terukur dengan nilai yang diterima. Akurasi dinyatakan sebagai persen perolehan
kembali (recovery) analit yang ditambahkan. Akurasi dapat ditentukan dengan
dua cara yaitu metode simulasi (spiked placebo recovery) dan metode
penambahan bahan baku (standard addition method).
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai relatif standar deviasi (RSD) dari sejumlah sampel yang
berbeda secara signifikan secara statistik.
Batas deteksi (limit of detection, LOD) didefinisikan sebagai konsentrasi
analit terendah dalam sampel yang masih dapat terdeteksi yang masih
memberikan respon signifikan.
Batas kuantitasi (limit of quantitation, LOQ) didefinisikan sebagai
dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan.
Batas deteksi dan batas kuantitasi dapat dihitung secara statistik melalui garis
BAB III
METODOLOGI PENELITIAN
Metode penelitian yang dilakukan adalah metode Experimental. Penelitian
ini dilaksanakan di Laboratorium Penelitian, Fakultas Farmasi Universitas
Sumatra Utara, Medan, pada bulan Maret hingga Juni 2010.
2.1 Alat – alat
Alat-alat yang digunakan dalam penelitian ini adalah satu unit alat KCKT
(Shimadzu) yang terdiri dari Vacum degasser, pompa, detektor UV/Vis, kolom
shimpac VP-ODS (4,6 mm x 25 cm), wadah fase gerak, penyuntik mikroliter (100
µ l), neraca analitik (Mettler Toledo), membran filter PTFE 0,5 µ m dan 0,2 µ m,
cellulose nitrat membran filter 0,45 µm, Spektrofotometer IR (Shimadzu IR
Prestige-21).
2.2 Bahan – bahan
Bahan-bahan yang digunakan dalam penelitian yaitu Metanol p.a (Merck),
Akuabidestilata (PT. Ikapharmindo putramas), Amonium Asetat p.a (Merck),
Asam Asetat Glacial p.a (Merck), Paracetamol, Kafein dan Asetosal BPFI (Badan
POM RI), Paracetamol, Kafein dan Asetosal baku pabrik (Kimia Farma ).
2.3 Sampel
sampel dianggap homogen. Dari hasil sampling diperoleh tablet Poldan Mix ( PT.
Sanbe Farma ), Puyer Bintang Toedjoe (PT. Bintang Toedjoe ).
2.4 Rancangan Penelitian
2.4.1 Uji Identifikasi Parasetamol, Kafein dan Asetosal Baku Pabrik (KimiaFarma) secara Spektrofotometri Inframerah
Dicampur 1 mg serbuk Parasetamol dengan 100 mg serbuk KBr dalam
lumpang digerus hinggga halus dan homogen, campuran tersebut diletakkan pada
sampel pan, kemudian dipasangkan pada DRS 8000 dan dianalisa pada bilangan
gelombang 4000 – 500 cm-1. Spektrum Inframerah yang diperoleh dibandingkan
dengan literatur.
Dengan perlakuan yang sama dilakukan terhadap Kafein dan Asetosal
2.4.2 Penyiapan Bahan
2.4.2.1 Pembuatan Dapar Asetat
Larutkan 77,1 g Amonium Asetat P dalam air, tambahkan 57 ml asam
asetat glasial P, encerkan dengan air secukupnya hingga 1000 ml (Ditjen
POM,1995).
2.4.2.2 Pembuatan Pelarut
Dicampur larutan Dapar Amonium Asetat pH 4 dan Metanol dengan
perbandingan 70:30, 80:20, 90:10 dan 95:5
2.4.2.3 Pembuatan Fase gerak Dapar Amonium Asetat pH 4 : Metanol
Sebelum digunakan Dapar Amonium Asetat pH 4 - Metanol (70:30, 80:20,
0,45 µ m dan membrane filtres PTFE 0,45 µ m, lalu diawaudarakan selama 20
menit.
2.4.2.4 Pembuatan Larutan Induk Baku Paracetamol
Ditimbang seksama sejumlah 50,0 mg Paracetamol BPFI, dimasukkan
kedalam labu 50 ml, dilarutkan dan diencerkan dengan pelarut hingga garis tanda
sehingga diperoleh larutan dengan konsentrasi 1000 mcg/ml, disaring filtratnya
digunakan sebagai larutan induk.
2.4.2.5 Pembuatan Larutan Induk Baku Kafein
Ditimbang seksama sejumlah 50,0 mg Kafein BPFI, dimasukkan kedalam
labu 50 ml, dilarutkan dan diencerkan dengan pelarut hingga garis tanda sehingga
diperoleh larutan dengan konsentrasi 1000 mcg/ml, disaring filtratnya digunakan
sebagai larutan induk.
2.4.2.6 Pembuatan Larutan Induk Baku Asetosal
Dtimbang seksama sejumlah 50,0 mg Asetosal BPFI, dimasukkan kedalam
labu 50 ml, dilarutkan dan diencerkan dengan pelarut hingga garis tanda sehingga
diperoleh larutan dengan konsentrasi 1000 mcg/ml, disaring filtratnya digunakan
sebagai larutan induk.
2.4.3 Prosedur Analisis 2.4.3.1 Penyiapan Alat KCKT
Masing-masing unit diatur, kolom yang digunakan Shimpac VP-ODS (4,6
mm x 25 cm), detektor UV/Vis, dengan laju alir 2 ml/menit, sensitifitas 1.000
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak
dibiarkan mengalir selama 30 menit sampai diperoleh garis alas yang datar,
menandakan sistem tersebut telah stabil.
2.4.3.2 Penentuan Komposisi Fase Gerak Dapar Amonium Asetat pH 4 : Metanol dan Laju Alir yang Optimum
Kondisi kromatografi divariasikan untuk mendapatkan hasil analisis yang
baik. Kondisi kromatigrafi yang divariasikan adalah perbandingan fase gerak dan
laju alir. Perbandingan fase gerak yakni larutan Dapar Amonium Asetat pH 4 dan
Metanol divariasikan 70:30, 80:20, 90:10 dan 95:5 Dari perbandingan fase gerak
yang terpilih ditentukan laju alir dari 0,5 ml/menit; 0,6 ml/menit; 0,7 ml/menit;
0,8ml/menit.
2.4.3.3 Analisis Kualitatif
Analisis kualitatif Parasetamol, kafein dan asetosal dilakukan dengan
membandingkan puncak yang memiliki waktu retensi hampir sama (identik), pada
kromatogram hasil analisis KCKT dari larutan baku pembanding Perasetamol,
kafein dan asetosal dengan larutan sampel pada panjang gelombang 257 nm.
2.4.3.4 Analisis kuatitatif
2.4.3.4.1 Penentuan Linieritas Kurva Kalibrasi Baku Pembanding Parasetamol,Kafein Dan Asetosal
Larutan induk baku Parasetamol, Kafein dan Asetosal masing-masing
dipipet 1,5 ml, 0,2 ml dan 0,4 ml ; 2 ml, 0,3 ml dan 0,8 ml ; 2,5 ml, 0,4 ml dan 1,6
ml ; 3 ml, 0,5 ml, 2 ml; 3,5 ml, 0,6 ml, 2,5 ml, masing-masing dimasukkan
Konsentrasi larutan Parasetamol berturut - turut adalah 60 ppm, 80 ppm, 100 ppm,
120 ppm, 140 ppm. Dan konsentrasi Kafein berturut - turut adalah 8 ppm, 12 ppm,
16 ppm, 20 ppm, 24 ppm. Sedangkan konsentrasi Asetosal berturut -turut adalah
16 ppm, 32 ppm, 64 ppm, 80 ppm, 100 ppm. Masiong - masing larutan
diawaudarakan selama ± 20 menit dan disaring melalui penyaring membran
Cellulose Nitrate 0,2 µ m. Kemudian filtrat larutan baku pembanding disuntikkan
sebanyak 100 µ l. Deteksi menggunakan detektor UV pada panjang gelombang
257 nm. Direkam kromatogram dan dibuat kurva kalibrasi dari luas puncak, lalu
dihitung persamaan regresi dan koefisien korelasi.
2.4.3.4.2 Penetapan Kadar Parasetamol, Kafein Dan Asetosal dalam Sampel
Diambil 20 tablet (20 bungkus serbuk) yang telah bersih dari selaput film,
ditimbang dan digerus homogen. Ditimbang serbuk setara dengan 50 mg Asetosal,
dimasukkan kedalam labu tentukur 50 ml dan ditambahkan dengan pelarut sampai
garis tanda. Dikocok, lalu disaring (beberapa ml filtrat dibuang ). Larutan lalu
disaring melalui penyaring membran Cellulosa Nitrate 0,2 µm dan diawaudarakan
selama ±20 menit. Kemudian disuntik sebanyak 10 µl kedalam sistem KCKT
melalui injektor loop 20 µl, menggunakan sistem elusi gradien dengan fase gerak
larutan dapar amonium asetat pH 4 - metanol (95:5), laju alir 0,8 ml/menit.
Deteksi menggunakan detektor UV pada panjang gelombang 257 nm. Direkam
kromatogram dan dicatat luas puncak. Kadarnya dihitung dengan mensubsitusikan
2.4.3.5 Analisis Data Penetapan Kadar Secara Statistik
Menurut Harmita (2004) data perhitungan kadar Parasetamol, Kafein Dan
Asetosal dapat dianalisis secara statistik menggunakan uji t.
Rumus yang digunakan adalah :
1 ) (
− −
=
∑
n X X SD
t hitung
n SD
X X
/
− =
Keterangan :
SD = Standar deviasi
X = Kadar sampel
X = Kadar rata-rata sampel
n = Jumlah perlakuan
α =tingkat kepercayaan
Data diterima jika ttabel < thitung< ttabel pada interval kepercayaan 99,5%
dengan nilai α = 0,005
Menurut Wibisono (2005) untuk menghitung kadar Parasetamol, Kafein
dan Asetosal dalam sampel dapat dilakukan secara statistik dengan rumus :
Keterangan :
μ = Kadar sebenarnya
X = Kadar sampel
n = Jumlah perlakuan
t = Suatu harga tergantung pada derajad kebebasan dan tinggkat kepercayaan
dk= Derajad kebebasan.
2.4.4 Metode Validasi
2.4.4.1. Akurasi ( Kecermatan )
Uji akurasi dengan parameter persen perolehan kembali (% Recovery)
dilakukan secara Standard Addition Method dengan membuat 3 konsentrasi analit
Parasetamol, Kafein Dan Asetosal dan baku pembanding dengan rentang spesifik
80%, 100%, 120%, setiap rentang mengandung 70% analit sampel dan 30% bahan
baku, pada perlakuan yang sama dengan perlakuan sampel.
Menurut WHO (1992) persen perolehan kembali dapat dihitung dengan
rumus:
% Perolehan kembali x100%
C B
A−
=
Keterangan :
A = Konsentrasi sampel yang diperoleh setelah penambahan bahan baku
B = Konsentrasi sampel sebelum penambahan bahan baku
2.4.4.2 Presisi (Keseksamaan)
Menurut Rohman (2007) uji presisi ditentukan dengan parameter Relatif
Standar Deviasi (RSD) dengan rumus:
% 100
x X SD
RSD=
Keterangan :
RSD = Standar Deviasi Relatif (%)
SD = Standar deviasi
X = Kadar rata-rata sampel
2.4.4.3 Batas Deteksi dan Batas Kuantitasi
Untuk menentukan batas deteksi (LOD) dan batas kuantitasi (LOQ)
digunakan rumus:
2 )
( 2
− − =
n Yi Y SB
Slope SB x LOD=3
Slope SB x LOQ=10
Keterangan :
SB = Simpangan baku
LOD = Batas Deteksi
BAB IV
HASIL DAN PEMBAHASAN
Baku Parasetamol, Kafein dan Asetosal yang diperoleh dari PT. Kimia
Farma dan PT. Bratako sebelum digunakan sebagai pembanding terlebih dahulu
diidentifikasi menggunakan Spektrofotometer FTIR pada rentang bilangan
gelombang 4000 – 500 cm-1, dengan metode pellet KBr.
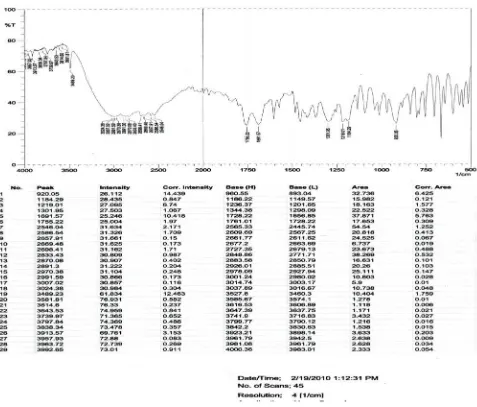
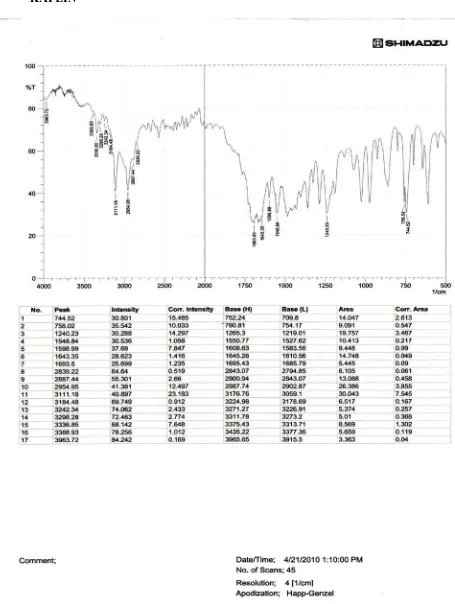
Spektrum Inframerah baku Parasetamol, Kafein dan Asetosal dapat dilihat
pada gambar dibawah ini :
[image:43.595.93.570.314.721.2]- PARASETAMOL
-KAFEIN
- ASETOSAL
Gambar 3. Spektrum Inframerah dari baku pabrik Aspirin (PT. Bratako)
Dari hasil spektrum Parasetamol, Kafein dan Asetosal diperoleh bentuk
spektrum yang hampir sama dengan spektrum pembanding yang terdapat pada
library (dapat dilihat pada Lampiran 3,4 dan 5). Bilangan gelombang pada daerah
sidik jari juga hampir sama dengan bilangan gelombang yang terdapat pada
literatur yaitu untuk Parasetamol pada bilangan gelombang 1506, 1657, 1565,
1263, 1227, 1612 cm-1. Sedangkan untuk Kafein pada bilangan gelombang 1658,
1698, 747, 1548, 1242, 760 cm-1 . Dan untuk Asetosal pada bilangan gelombang
Dari data spektrum yang diperoleh, dapat diambil kesimpulan bahwa baku
yang diidentifikasi adalah Parasetamol, Kafein dan Asetosal.
Tahap pertama dilakukan analisis campuran Parasetamol, Kafein dan
Asetosal baku dengan KCKT menggunakan kolom Shim-pack VP-ODS dan
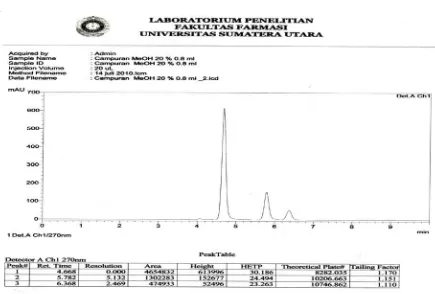
[image:46.595.114.549.239.533.2]kondisi kromatografi menurut USP XXX (2007). Kromatogram dapat dilihat pada
gambar 4.
Gambar 4. Kromatogram analisis campuran Parasetamol, Kafein dan Asetosal
dengankolom Shim-pack VP-ODS, fase gerak larutan Dapar Amonium Asetat pH4: Metanol (80:20) dan laju alir 0,8 ml/manit
Kromatogram pada gambar 4 menunjukkan hasil analisis yang baik
dengan resolusi 5.132 dan 2.469; teoretical plate 8282.035 untuk Parasetamol,
10206.663 untuk Kafein dan 10746.862 untuk Asetosal; Waktu tambat 4.668
untuk Parasetamol, 5.782 untuk Kafein, dan 6.368 untuk Asetosal.
Untuk mendapatkan pemisahan kromatogram yang lebih baik lagi maka
analisis campuran Parasetamol, Kafein dan Asetosal baku dengan KCKT
menggunakan berbagai komposisi fase garak pada laju alir 0,8 ml/ menit dapat
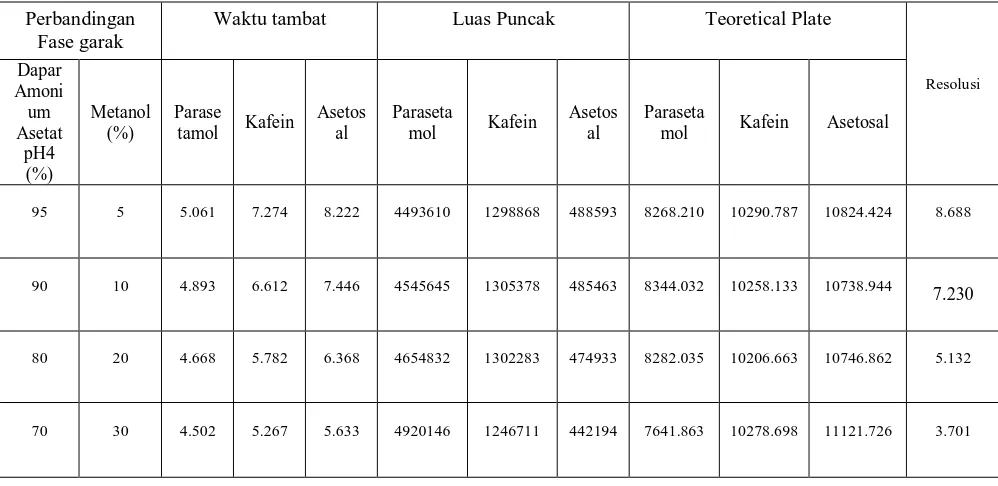
[image:47.595.84.583.200.443.2]dilihat pada tabel 1.
Tabel 1. Data hasil analisis Parasetamol, Kafein dan Asetosal baku pada berbagai perbandingan komposisi fase gerak dan laju alir 0,8 ml/ menit.
Tabel 1 menunjukkan bahwa semakin besar konsentrasi metanol dalam
fase gerak, maka waktu tambat Parasetamol, Kafein dan Asetosal semakin
singkat. Hal ini dikarenakan adanya kekuatan pelarut ( solvent strength ). Pada
kromatografi fase terbalik, konsentrasi metanol yang lebih besar akan
mengakibatkan fase gerak semakin kuat sifat nonpolarnya sehingga proses elusi
terjadi lebih cepat, oleh karena itu waktu tambat menjadi singkat (Snyder &
Kirkland,1979 ).
Efisiensi kolom pada HPLC dapat dilihat dari parameter theoritical plate
pada setiap kromatogram dan daya pisah dapat dilihat dari parameter resolusi.
Menurut USP XXX, theoritical plate setiap kromatogram dalam penetapan kadar
Perbandingan Fase garak
Waktu tambat Luas Puncak Teoretical Plate
Resolusi
Dapar Amoni um Asetat
pH4 (%)
Metanol (%)
Parase
tamol Kafein
Asetos al
Paraseta
mol Kafein
Asetos al
Paraseta
mol Kafein Asetosal
95 5 5.061 7.274 8.222 4493610 1298868 488593 8268.210 10290.787 10824.424 8.688
90 10 4.893 6.612 7.446 4545645 1305378 485463 8344.032 10258.133 10738.944
7.230
80 20 4.668 5.782 6.368 4654832 1302283 474933 8282.035 10206.663 10746.862 5.132
dan resolusi tadak lebih kecil dari 3,5. Dari hasil penelitian diperoleh
perbandingan fase gerak Dapar Amonium Asetat pH 4 - Metanol yang terbaik
untuk analisis adalah 95:5 dengan waktu tambat 5.061 untuk Parasetamol, 7.274
untuk Kafein dan 8.222 untuk Asetosal; theoritical plate 8268.210 untuk
Parasetamol, 10290 untuk Kafein dan 10824.424 untuk Asetosal; dengan resolusi
8.688.
Selanjutnya dari fase garak yang terpilih ditentukan laju alir yang optimal.
Data analisis campuran Parasetamol, Kafein dan Asetosal baku dengan KCKT
pada berbagai laju alir dengan fase gerak Dapar Amonium Asetat pH 4 - Metanol
[image:48.595.69.566.396.519.2](95:5) dapat dilihat pada tabel 2 dan kromatogram dapat dilihat pada lampiran7.
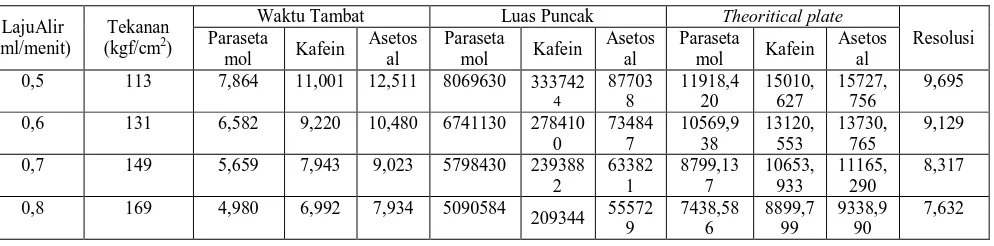
Tabel 2. Data hasil analisis Parasetamol, Kafein dan Asetosal baku pada berbagai Laju alir dengan fase gerak Dapar Amonium Asetat pH4 - Metanol (95:5)
LajuAlir (ml/menit)
Tekanan (kgf/cm2)
Waktu Tambat Luas Puncak Theoritical plate
Resolusi Paraseta
mol Kafein
Asetos al
Paraseta
mol Kafein
Asetos al
Paraseta
mol Kafein
Asetos al 0,5 113 7,864 11,001 12,511 8069630 333742
4 87703 8 11918,4 20 15010, 627 15727, 756 9,695
0,6 131 6,582 9,220 10,480 6741130 278410 0 73484 7 10569,9 38 13120, 553 13730, 765 9,129
0,7 149 5,659 7,943 9,023 5798430 239388 2 63382 1 8799,13 7 10653, 933 11165, 290 8,317
0,8 169 4,980 6,992 7,934 5090584
209344 55572 9 7438,58 6 8899,7 99 9338,9 90 7,632
Sama seperti pada penentuan perbandingan fase gerak Dapar Amonium
Asetat pH 4 - Metanol, parameter seperti waktu tambat, theoritical plate dan
resolusi menjadi penentu pemilihan laju alir yang optimum. Dari hasil penelitian
diperoleh laju alir yang terbaik untuk analisis adalah 0,8 ml/menit dengan waktu
tambat 4,980 untuk Paracetamol, 6,992 untuk Kafein dan 7,934 untuk Asetosal;
theoritical plate 7438,586 untuk Paracetamol, 8899,799 untuk Kafein dan
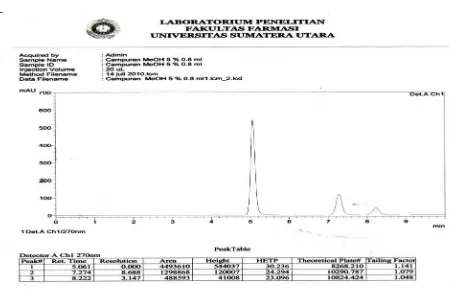
Kromatogram hasil optimasi metode KCKT yang dilakukan terhadap
campuran Parasetamol, Kafein dan Asetosal baku dengan fase gerak Dapar
Amonium Asetat pH 4 - Metanol (95:5) dan laju alir 0,8 ml/menit dapat dilihat
[image:49.595.113.563.183.472.2]pada gambar 5.
Gambar 5. Kromatogram analisis campuran Parasetamol, Kafein dan Asetosal dengan kolom Shim-pack VP-ODS, fase gerak larutan Dapar Amonium Asetat pH4: Metanol (95:5) dan laju alir 0,8 ml/manit.
Selanjutnya dari perbandingan fase gerak dan laju alir yang terpilih,
dilakukan analisis terhadap sampel Tablet Poldan Mig dan Puyer Bintang Toedjoe
dengan fase gerak larutan Dapar Amonium Asetat pH 4 : Metanol (95:5) dan laju
Gambar 6. Kromatogram analisis campuran Parasetamol, Kafein dan Asetosal dengankolom Shim-pack VP-ODS, fase gerak larutan Dapar Amonium Asetat pH4: Metanol (95:5) dan laju alir 0,8 ml/manit.
Gambar 6 menunjukkan optimasi KCKT dengan fase gerak larutan Dapar
Amonium Asetat pH 4 : Metanol (95:5) dan laju alir 0,8 ml/menit memberi hasil
optimal yang sama terhadap baku pembanding dengan waktu tambat 5,103 untuk
Paracetamol, 7,414 untuk Kafein dan 8,340 untuk Asetosal; theoritical plate
7817,670 untuk Paracetamol, 9609,356 untuk Kafein dan 10080,253 untuk
Asetosal; resolusi 8,667.
Dari kromatogram pada semua tablet dan puyer yang dianalisis diperoleh
waktu tambat dengan perbedaan tidak lebih dari 5% dengan 5,103 untuk
Paracetamol, 7,414 untuk Kafein dan 8,340 untuk Asetosal. Hal ini berarti bahwa
sampel yang digunakan dalam penelitian ini mengandung Paracetamol, Kafein
Analisis kuantitatif ditentukan berdasarkan luas pucak karena
kromatogram yang diperoleh tidak simetris. Pengukuran luas puncak tidak banyak
dipengaruhi oleh kondisi kromatografi dibandingkan dengan tinggi puncak,
kecuali laju alir. Oleh karena itu pengukuran luas puncak merupakan pilihan yang
terbaik dalam analisis kuantitatif secara KCKT (Poole,2003).
Penyuntikan larutan campuran Paracetamol, Kafein dan Asetosal baku
untuk kurva kalibrasi dilakukan secara simultan. Kurva kalibrasi Paracetamol,
Kafein dan Asetosal baku dengan rentan konsentrasi 60 ppm hingga 140 ppm
untuk Paracetamol, 8 ppm hingga 24 ppm untuk Kafein dan 16 ppm hingga 96
[image:51.595.113.575.388.678.2]ppm untuk Asetosal. Kurva kalibrasi dapat dilihat pada gambar 7,8 dan 9.
Gambar 8. Kurva kalibrasi Kafein baku menggunakan KCKT dengan kolom Shim-pack VPO-DS (4,6 x 250), fase gerak larutan Dapar Amonium Asetat pH 4 dan Metanol (95:5) dan laju alir 0,8 ml/manit.
[image:52.595.118.578.405.674.2]Dari kurva kalibrasi diperoleh hubungan yang linier antara luas puncak dan konsentrasi dengan koefisien korelasi r = 0,9982 untuk Paracetamol, 0,9997 untuk Kafein dan 0,9994 untuk Asetosal. Koefisien korelasi ini telah memenuhi persyaratan yaitu lebih basar dari 0,999 (Anonim,1994).
Berdasarkan harga r yang mendekati 1 berarti ada hubungan yang linier
antara luas puncak dan konsentrasi sehingga konsentrasi Paracetamol, Kafein dan
Asetosal dalam sampel dapat dihitung dangan persamaan regresi yaitu dengan
mensubsitusikan luas puncak terhadap Y (Rohman,2007).
Kromatogram hasil penyuntikan larutan campuran Paracetamol, Kafein
dan Asetosal baku pada pembuatan kurva kalibrasi menunjukkan puncak yang
melebar kebelakang (Tailing). Parameter yang dapat digunakan sebagai indikator
pucak yang tidak simetris yakni Tailing Factor. Tailing Factor dari kromatogram
penyuntikan Paracetamol, Kafein dan Asetosal baku untuk pembuatan kurva
kalibrasi diperoleh berkisar 1,124-1,127 untuk Prasetamol, 1,062-1,065 untuk
Kafein dan 1,034-1,037 untuk asetosal. Hasil analisis ini masih dapat diterima
karena tailing factor lebih kecil dari 2 (Anonim,1994).
Hasil pengolahan data dari sedíaan Tablet dan Puyer Parasetamol, Kafein
Tabel 3. Hasil pengukuran kadar sedíaan Tablet dan Puyer dari campuran Parasetamol, Kafein dan Asetosal
Nama Zat Perlakuan Poldan Mig Puyer Bintang Toedjoe Luas Area Kadar(%) Luas Area Kadar(%) Parasetamol 1 4487642 104,6013 4353716 101,0584
2 4496051 104,8237 4359761 101,2183 3 4496233 104,8282 4358269 101,1788
Kafein 1 1514386 107,2504 1063043 104,2860
2 1516924 107,4306 1063972 104,3775 3 1516605 107,4076 1065666 104,5443
Asetosal 1 432279 96,5168 460971 102,8954
2 432481 96,5617 460940 102,8885
3 431249 96,2879 459403 102,5468
Berdasarkan data pada tabel 3 yang diolah menggunakan perhitungan
statistik diperoleh kadar Parasetamol, Kafein dan Asetosal dalam sedíaan tablet
dan puyer dengan nama dagang seperti pada tabel 4.
Tabel 4. Hasil penetapan kadar Paracetamol, Kafein dan Asetosal dalam berbagai sedíaan Tablet dan Puyer.
No Nama Sediaan Paracetamol(%) Kafein(%) Asetosal(%) 1 Tablet Poldan
Mig ( PT. Sanbe
Farma)
104,7511±0,3020 107,3629±0,2283 96,4554±0,08475
2 Puyer Bintang Toedjoe (PT. Bintang
Toedjoe)
101,1518±0,04809 104,347±0,030 102,9122±0,0203
Sediaan tablet Parasetamol, Kafein dan Asetosal yang ditentukan kadarnya
berdasarkan luas area keseluruhannya memenuhi persyaratan yang ditetapkan
USP XXX (2007) yaitu mengandung Parasetamol, Kafein dan Asetosal tidak
kurang dari 90,0% dan tidak lebih dari 120% dari jumlah yang tertera Pada etiket.
Parameter validasi yang diuji adalah akurasi (kecermatan), presisi
(Keseksamaan), batas deteksi dan batas kuatitasi. Akurasi (kecermatan) metode
[image:54.595.109.518.402.521.2]dapat dilihat pada lampiran 13 Presisi (kecermatan) dinyatakan dalam simpangan
baku relatif. Data hasil pengujian akurasi dapat dilihat pada tabel 5,6 dan 7.
Tabel 5. Data hasil pengujian akurasi dan presisi Parasetamol dengan metode penambahan baku
No % R Luas Puncak Analit yang ditambahkan
(mg)
Perolehan Kembali (%)
1 80% 3562789 19,2 100,5625
3579183 19,2 102,3697
3550763 19,2 99,2369
2 100% 4378217 24 105,6879
4350858 24 103,2754
4355331 24 103,67
3 120% 5099175 28,8 102,1628
5067343 28,8 99,8236
5049861 28,8 98,5392
Rerata Perolehan Kembali 101,69
Simpangan Baku (SD) 2,34
Simpangan Baku relatif (RSD) 2,30
Tabel 6. Data hasil pengujian akurasi dan presisi Kafein dengan metode penambahan baku
No % R Luas Puncak Analit yang ditambahkan
(mg)
Perolehan Kembali (%)
1 80% 1131806 3,12 100,3653
1125017 3,12 98,3557
1135243 3,12 101,3814
2 100% 1441474 3,9 106,9102
1466027 3,9 112,7205
1448334 3,9 108,5333
3 120% 1696155 4,68 100,4273
1696155 4,68 100,4273
1693740 4,68 99,9636
Rerata Perolehan Kembali 103,23
Simpangan Baku (SD) 4,91
Simpangan Baku relatif (RSD) 4,75
Tabel 7. Data hasil pengujian akurasi dan presisi Asetosal dengan metode penambahan baku
No % R Luas Puncak Analit yang ditambahkan
(mg)
Perolehan Kembali (%)
1 80% 342269 12 85,8983
[image:55.595.111.518.163.366.2] [image:55.595.112.518.428.630.2]341855 12 85,4151
2 100% 445890 15 98,948
448433 15 100,3593
444888 15 97,7326
3 120% 504760 18 79,9733
514741 18 85,9516
512289 18 84,1761
Rerata Perolehan Kembali 89,58
Simpangan Baku (SD) 7,40
Simpangan Baku relatif (RSD) 8,25
[image:56.595.109.517.84.217.2]
Tabel 5,6 dan 7 menunjukkan bahwa rerata persen perolehan kembali yang
diperoleh untuk Parasetamol telah memenuhi persyaratan akurasi untuk validasi
prosedur analitik karena berada di antara rentang 98% - 102% yaitu 101,69%
sedangkan untuk Kafein dan Asetosal tidak memenuhi persyaratan akurasi untuk
validasi karena berada pada rentang 103,23% untuk Kafein dan 89,58% untuk
Asetosal. Simpangan baku relatif yang diperoleh untuk Parasetamol telah
memenuhi persyaratan presisi untuk validasi prosedur analitik karena lebih kecil
dari 2,5% yaitu 2,30%, sedangkan untuk kafein dan Asetosal tidak memenuhi
batas presisi untuk prosedur validasi karena lebih besar dari 2,5% yaitu 4,75 untuk
Kafein dan 8,25 untuk Asetosal ( USP XXX, 2007).
Batas deteksi dan batas kuantitasi dihitung dari persamaan regresi yang
diperoleh dalam kurva kalibrasi (Erner and Burgess, 2005). Batas deteksi dan
batas kuantitasi analisis Parasetamol, Kafein dan Asetosal adalah 1,67 µg/ml dan
5,54 µg/ml untuk Paracetamol, 0,45 µg/ml dan 1,50 µg/ml untuk Kafein
BAB V
KESIMPULAN DAN SARAN
4.1 Kesimpulan
Metode KCKT dengan fase gerak larutan Dapar Amonium Asetat pH 4
dan Metanol dapat memisahkan campuran Paracetamol, Kafein dan Asetosal
dalam tablet dan puyer.
Perbandingan fase gerak Dapar Amonium Asetat pH 4 dan Metanol 95:5
dengan laju alir 0,8 ml/menit dapat menghasilkan pemisahan yang baik dengan
waktu tambat 4,980 untuk Parasetamol, 6,992 untuk Kafein dan 7,934 untuk
Asetosal ; theoritical plate 7438,586 untuk Parasetamol, 8899,799 untuk Kafein
dan 9338,990 untuk Asetosal yang memenuhi persyaratan USP XXX (2007).
Hasil uji validasi KCKT pada penetapan kadar campuran Paracetamol,
Kafein dan Asetosal dalam tablet secara simultan memberikan hasil akurasi dan
presisi yang kurang baik. Dimana untuk Parasetamol memenuhi persyaratan
karena berada diantara rentang 98% - 102% yaitu 101,62%, sedangkan untuk
Kafein dan Asetosal tidak memenuhi persyaratan karena berada pada rentang
103,23% untuk Kafein dan 89,58% untuk Asetosal. Hal ini dikarenakan
kemungkinan adanya kesalahan peneliti pada saat penimbangan sampel dan
pengenceran yang sangat berpengaruh pada hasil validasi sebagaimana yang
terdapat pada Farmakope Indonesia Edisi III kasalahan pada penimbangan yang
diperkenankan tidak lebih dari 0,1% dari jumlah yang ditimbang. Dengan
demikian metode ini sebenarnya dapat digunakan pada validasi dan dapat
digunakan untuk penetapan kadar campuran Paracetamol, Kafein dan Asetosal
dalam tablet.
4.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut menggunakan fase gerak
DAFTAR PUSTAKA
Anonim. (2008). Pedoman Penulisan Skripsi. Fakultas Farmasi. Universitas Sumatera Utara.
Anonim. (2007). The United States Pharmacopeia 30th Edition. National Formulary. United States Pharmacopeia Convention. Hal. 3243.
Anonim. (1994). Chemistry Manufacturing Controls Coordinating Committee. Validation of Chromatographic Methods, Reviewer Gguidance. Rockville: Center for Drug Evaluation and Research/CDER, Food and Drug Administration/FDA. Pages 12,25.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 254-255, 650 – 651, 1009.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Reviw Artikel. Majalah Ilmu Kefarmasian, Volume I (3). Hal.117-135.
Indrayanto, G; Sunarto, A; Adriani, Y. Simultaneous assay of phenilpropolamine hydrocholoride, Caffein, Parasetamol, glycerylguayacolate and chlorphenilamine in silibat tablet using HPLC with diode array detection. J. Pharm. Biomed. Anal., 1995,13,1555 – 1559.
Poole, C.F. (2003). The Essence of Chromatography. Amsterdam: Elsevier Science B.V. Page 68-69
Rohman, A. (2007). Kimia Faramasi Analisis. Yogyakarta. Penerbit: Pustaka pelajar. Hal.18.
Snyder, L. And Kirkland, J. (1979). Introduction to Modern Liquid Chromatography. 2nd edition, By Jhon Wiley and Son. London. Page. 554.
Sudaryo. (2001). Pengantar Kromatografi. Surabaya. BBPOM Surabaya. Hal 4-14.
Tjay & Rahardja. (2002). Obat-Obat Penting. Edisi kelima. Jakarta. Penerbit PT. Elex Media Komputindo. Hal. 140.
Lampiran 1. Gambar Instrumen KCKT dan Syringe 100 µl
Seperangkat instrumen KCKT (Shimadzu Corp) dan komputer (Hewlett-Packard) sebagai perangkat pendukung.
Lampiran 2. Gambar Perangkat Pendukung Penelitian Lainnya
Sonifikator (Bronson 1510)
Lampiran 3. Spektrum Inframerah Parasetamol pada literatur Pharmaceutical
Lampiran 4. Spektrum Inframerah Kafein pada literatur Pharmaceutical Sub
Lampiran 5. Spektrum Inframerah Asetosal pada literatur Pharmaceutical Sub
Lampiran 6. Kromatogram Penyuntikan Paracetamol, Kafein dan Asetosal baku untuk mencari Perbandingan Fase Gerak Larutan Dapar Amonium Asetat pH4 dan Metanol yang optimum untuk analisis
Perbandingan fase gerak larutan Dapar Amonium Asetat pH4: Metanol 95:5 dengan tekanan 129 kgf/cm2
Lampiran 6. (lanjutan)
Perbandingan fase gerak larutan Dapar Amonium Asetat pH4: Metanol 80:20 dengan tekanan 149 kgf/cm2
Perbandingan fase gerak larutan Dapar Amonium Asetat pH4: Metanol 70:30 dengan tekanan 169 kgf/cm2
Kromatogram diatas merupakan hasil penyuntikan larutan Parasetamol,
Kafein dan Asetosal baku dalam upaya mencari perbandingan fase gerak Dapar
Amonium Asetat pH4: Metanol yang optimal untuk analisis menggunakan KCKT
dengan kolom Shim-Pack VP-ODS (4,5 x 250 mm), volume penyuntikan 20 µ l,
laju alir 0,8 ml/menit, detektor UV pada panjang gelombang 257 nm dan
Lampiran 7. Kromatogram Penyuntikan Paracetamol, Kafein dan Asetosal baku dalam upaya mencari Laju Alir yang Optimum untuk Analisis
Laju Alir 0,5 ml/menit dengan tekanan 112 kgf/cm2
Lampiran 7. (Lanjutan)
Laju Alir 0,7 ml/menit dengan tekanan 152 kgf/cm2
Laju Alir 0,8 ml/menit dengan tekanan 164 kgf/cm2
Kromatogram di atas merupakan hasil penyuntikan larutan Parasetamol,
Kafein dan Asetosal baku dalam upaya mencari laju alir yang optimum untuk
analisis menggunakan KCKT dengan kolom Shim-Pack VP-ODS (4,5 x 250 mm),
volume penyuntikan 20 µ l, perbandingan fase gerak larutan Dapar Amonium
Asetat pH4: Metanol (95:5), detektor UV pada panjang gelombang 257 nm dan
Lampiran 8. Perhitungan persamaan regresi dari kurva Kalibrasi Parasetamol,
Kafein dan Asetosal yang diperoleh dengan KCKT pada panjang
gelombang 257 nm.
a. Parasetamol
Data hasil Penyuntikan Larutan Parasetamol baku yang diperoleh
[image:68.595.113.515.415.607.2]dengan KCKT
Tabel konsentrasi (X) vs Luas Area (Y) untuk Parasetamol baku
No X Y XY X² Y²
1 60 2829442.1 169766526 3600 8,00574259725
2 80 3386628.3 270930264 6400 11,4692512428
3 100 4194584.0 419458400 10000 17,594534933056
4 120 5001208.4 600144960 14400 25,012081459264
5 140 5713693.0 799917020 19600 32,646287698249
∑ 500 21125555.8 2260217218 54000 94727901931148.9
b aX
Y= +