ANALISIS KANDUNGAN MINERAL KALSIUM, KALIUM, DAN MAGNESIUM OKRA HIJAU DAN OKRA MERAH
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH :
NADYA ZIPORA BR NAINGGOLAN NIM 141501182
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ANALISIS KANDUNGAN MINERAL KALSIUM, KALIUM, DAN MAGNESIUM OKRA HIJAU DAN OKRA MERAH
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH :
NADYA ZIPORA BR NAINGGOLAN NIM 141501182
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN MINERAL KALSIUM, KALIUM, DAN MAGNESIUM OKRA HIJAU DAN OKRA MERAH
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH :
NADYA ZIPORA BR NAINGGOLAN NIM 141501182
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 18 Juli 2018
Disetujui oleh:
Pembimbing , Panitia penguji,
Prof. Dr. Muchlisyam, M. Si, Apt.
NIP 195006221980021001 Dra. Tuty Roida Pardede, M.Si., Apt.
NIP 195401101980032001
Dra. Tuty Roida Pardede, M.Si., Apt.
NIP 195401101980032001
Dra. Sudarmi, M.Si., Apt.
NIP 195409101983032001 Medan, Oktober 2018
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Masfria, M. S., Apt.
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa atas berkat, rahmat, dan anugerah-Nya, penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul “Analisis Kandungan Mineral Kalsium, Kalium, dan Magnesium Okra Hijau dan Okra Merah secara Spektrofotometri Serapan Atom” dengan baik.
Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis hendak menyampaikan rasa terima kasih yang sebesar-besarnya kepada Dra. Tuty Roida Pardede, M.Si., Apt., selaku dosen pembimbing yang telah banyak mengarahkan dan memberikan dukungan sehingga skripsi ini dapat diselesaikan dengan baik. Penulis juga menyampaikan ucapan terima kasih kepada Bapak Prof. Dr. Muchlisyam, M.Si, Apt., dan Ibu Dra, Sudarmi, M.Si., Apt., selaku dosen penguji yang telah meluangkan waktu untuk memberikan saran dan kritikan dalam penyempurnaan skripsi ini.
Selanjutnya penulis hendak menyampaikan rasa hormat dan terima kasih kepada Ibu Prof. Dr. Masfria, M.S., Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara beserta jajaran dekanat yang telah memberikan fasilitas, motivasi, dan masukan selama masa pendidikan dan penelitian. Penulis menyampaikan rasa terima kasih kepada seluruh dosen Fakultas Farmasi Universitas Sumatera Utara yang telah membagikan ilmunya tanpa pamrih serta seluruh staf di lingkungan Fakultas Farmasi Universitas Sumatera Utara yang telah mendukung kelancaran penulis selama masa pendidikan dan masa penelitian.
Penulis juga mengucapkan terima kasih yang tak terhingga dan penghargaan yang tulus kepada Ayahanda Hasoloan Nainggolan dan Ibunda
Lusiana Purba yang selalu memberikan dukungan dan mendoakan penulis dalam menyelesaikan skripsi ini, untuk saudara laki-laki penulis Arnold Yoshua Nainggolan, Jonathan Nainggolan, dan Adolf Jeremy Nainggolan yang selalu mendoakan dan memberi semangat kepada penulis. Penulis juga mengucapkan terima kasih untuk yang terkasih Yohanes Marthin Hutabarat yang selalu memotivasi penulis dan yang selalu mendoakan penulis. Penulis juga mengucapkan terima kasih kepada sahabat penulis Trifena, Gracia, Claudia, Ruth, Debora, Falen, Elfina, Elsa, Ersya, Learnita, dan Asael yang telah mendukung penulis dalam menyelesaikan skripsi ini
Semoga skripsi ini dapat bermanfaat dan menjadi sumber informasi tambahan bagi kita semua khususnya di bidang farmasi..
Medan, Juni 2018 Penulis,
Nadya Zipora Nainggolan NIM 141501182
SURAT PERNYATAAN TIDAK PLAGIAT Saya yang bertanda tangan dibawah ini,
Nama : Nadya Zipora Br Nainggolan
Nomor Induk Mahasiswa : 141501182
Program Studi : S-1 Farmasi Reguler
Judul Skripsi : Analisis Kandungan Mineral Kalsium, Kalium, dan Magnesium Okra Hijau dan Okra Merah
secara Spektrofotometri Serapan Atom
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri dan belum pernah diajukan oleh orang lain untuk memperoleh gelar kesarjanaan di perguruan tinggi lain serta bukan plagiat karena kutipan yang ditulis telah disebutkan sumbernya di dalam daftar pustaka.
Apabila di kemudian hari ada pengaduan dari pihak lain karena didalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia menerima sanksi apapun oleh Program Studi Farmasi Fakultas Farmasi Universitas Sumatera Utara dan bukan menjadi tanggung jawab pembimbing.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, Juni 2018
Yang membuat pernyataan,
Nadya Zipora Br Nainggolan NIM 141501182
ANALISIS KANDUNGAN MINERAL KALSIUM, KALIUM, DAN MAGNESIUM OKRA HIJAU DAN OKRA MERAH SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Indonesia merupakan salah satu pusat keragaman tanaman okra yang dibudidayakan maupun yang liar yang terbanyak. Terdapat banyak sekali varietas okra, namun secara umum yang banyak dikenal adalah okra hijau dan okra merah.
Tujuan dari penelitian ini adalah untuk membandingkan kadar kalsium, kalium, dan magnesium yang terkandung dalam okra hijau dan yang terkandung dalam okra merah.
. Metode penelitian yang dilakukan yaitu analisis kualitatif dan kuantitatif.
Analisis kualitatif kalsium menggunakan asam sulfat, kalium menggunakan asam pikrat dan magnesium menggunakan larutan kuning titan. Analisis kuantitatif menggunakan Spektrofotometri Serapan Atom pada panjang gelombang untuk kalsium 422,7 nm; untuk kalium 766,5 nm; dan untuk magnesium 285,20 nm.
Dari hasil penelitian diperoleh kadar kalsium, kalium dan magnesium pada okra hijau masing-masing sebesar 45,43 ± 0,36 mg/100g; 243,58 ± 1,84 mg/100g; 88,86 ± 0,99 mg/100g, sedangkan kadar kalsium, kalium dan magnesium pada okra merah masing-masing sebesar 46,54 ± 0,33 mg/100g;
229,78 ± 1,63 mg/100g; dan 71,90 ± 0,33 mg/100g.
Kesimpulan dari penelitian ini adalah terdapat perbedaan kadar kalsium, kalium dan magnesium pada okra hijau dan okra merah. Kadar kalium dan magnesium pada okra hijau lebih tinggi daripada okra merah, sedangkan kadar kalsium pada okra merah lebih tinggi daripada okra hijau.
Kata kunci: okra, kalsium, kalium, magnesium, spektrofotometri serapan atom
ANALYSIS OF MINERAL CALSIUM, POTASSIUM, AND MAGNESIUM IN GREEN OKRA AND RED OKRA BY USING ATOMIC ABSORPTION
SPECTROPHOTOMETRY ABSTRACT
Indonesia is one of the largest centers of cultivated okra diversity and wild okra. There are many varieties of okra, but in general the widely known are green okra and red okra. The aim of this study was to compare the levels of calcium, potassium, and magnesium contained in green okra and contained in red okra.
The research method is done by qualitative and quantitative analysis.
Qualitative analysis of calcium using sulfuric acid, potassium using picric acid and magnesium using a titan yellow solution. Quantitative analysis using Atomic Absorption Spectrophotometry at wavelengths for calcium 422.7 nm; for potassium 766.5 nm; and for magnesium 285.20 nm.
The results showed that levels of calcium, potassium and magnesium in green okra were 45.43 ± 0.36 mg / 100g; 243.58 ± 1.84 mg / 100g; 88.86 ± 0.99 mg / 100g, while calcium, potassium and magnesium levels in red okra were 46.54 ± 0.33 mg / 100g; 229.78 ± 1.63 mg / 100g; and 71.90 ± 0.33 mg / 100g.
The conclusion of this study was the differences in calcium, potassium and magnesium levels in green and red okra. Levels of potassium and magnesium in green okra higher than red okra, while calcium levels in red okra higher than green okra.
Keywords: okra, calsium, potassium, magnesium, atomic absorption spectrophotometry
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR GAMBAR DALAM LAMPIRAN ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Okra ... 4
2.1.1 Sistematika Tumbuhan ... 4
2.1.2 Nama Lain ... 4
2.1.3 Deskripsi Tumbuhan ... 4
2.1.4 Kandungan Kimia dan Kegunaan ... 5
2.2 Mineral ... 6
2.2.1 Kalsium ... 6
2.2.2 Kalium ... 7
2.2.3 Magnesium ... 8
2.3 Spektrofotometri Serapan Atom ... 9
2.4 Validasi Metode Analisis ... 12
BAB III METODE PENELITIAN ... 15
3.1 Tempat dan Waktu Penelitian ... 15
3.2 Bahan ... 15
3.3 Alat ... 15
3.4 Pembuatan Pereaksi ... 16
3.4.1 Larutan HNO3 (1:1) ... 16
3.4.2 Larutan Asam Sulfat 1N ... 16
3.4.3 Larutan Natrium Hidroksida 1N ... 16
3.4.4 Larutan Kuning Titan 0,1 % b/v ... 16
3.4.5 Larutan Asam Pikrat 1% b/v ... 16
3.5 Prosedur Penelitian ... 16
3.5.1 Pengambilan Sampel ... 16
3.5.2 Penyiapan Sampel ... 17
3.5.3 Proses Destruksi Kering ... 17
3.5.4 Pembuatan Larutan Sampel ... 17
3.5.5 Analisis Kualitatif ... 18
3.5.5.1 Kalsium ... 18
3.5.5.1.1 Uji Kristal dengan Asam Sulfat 1N ... 18
3.5.5.2 Kalium... 18
3.5.5.2.1 Uji Kristal Kalium dengan Asam Pikrat .... 18
3.5.5.3 Magnesium ... 18
3.5.5.3.1 Reaksi Warna dengan Kuning Titan 0,1% . 18
3.5.6 Analisis Kuantitatif ... 18
3.5.6.1 Pembuatan Kurva Kalibrasi Kalsium... 18
3.5.6.2 Pembuatan Kurva Kalibrasi Kalium ... 19
3.5.6.3 Pembuatan Kurva Kalibrasi Magnesium ... 19
3.5.6.4 Penetapan Kadar Mineral dalam Sampel ... 20
3.5.6.4.1 Penetapan Kadar Kalsium ... 20
3.5.6.4.2 Penetapan Kadar Kalium ... 20
3.5.6.4.3 Penetapan Kadar Magnesium ... 20
3.5.7 Analisis Data Secara Statistik ... 21
3.5.7.1 Penolakan Hasil Pegamatan ... 21
3.5.7.2 Pengujian Beda Nilai Rata-Rata Sampel ... 21
3.5.8 Validasi Metode Analisis ... 23
3.5.8.1 Batas Deteksi dan Batas Kuantitasi ... 23
3.5.8.2 Uji Perolehan Kembali (Recovery) ... 23
3.5.8.3 Simpangan Baku Relatif ... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
4.1 Analisis Kualitatif ... 25
4.2 Analisis Kuantitatif ... 26
4.2.1 Kurva Kalibrasi Kalsium, Kalium dan Magnesium ... 26
4.2.2 Analisis Kadar Kalsium, Kalium dan Magnesium ... 27
4.2.3 Batas Deteksi dan Batas Kuantitasi ... 28
4.2.4 Uji Perolehan Kembali (Recovery) ... 29
4.2.5 Simpangan Baku Relatif ... 30
4.2.6 Pengujian Beda Nilai Rata-Rata Kadar Kalsium, dan Magnesium Pada Okra Hijau dan Okra Merah ... 31
BAB V KESIMPULAN DAN SARAN ... 33
5.1 Kesimpulan ... 33
5.2 Saran ... 33
DAFTAR PUSTAKA ... 34
LAMPIRAN ... 36
DAFTAR TABEL
Tabel Halaman 4.1 Hasil Analisis Kualitatif pada Okra Hijau dan Okra Merah ... 25 4.2 Kadar Kalsium, Kalium, dan Magnesium pada Sampel ...
4.3 Batas Deteksi dan Batas Kuantitasi... 28 4.4 Recovery Kalsium, Kalium, dan, Magnesium Okra Hijau ... 29 4.5 Recovery Kalsium, Kalium, dan, Magnesium Okra Merah .... 29 4.6 Simpangan Baku (SD) dan Simpangan Baku Relatif (RSD)
Kalsium, Kalium, dan Magnesium Okra Hijau ... 30 4.7 Simpangan Baku (SD) dan Simpangan Baku Relatif (RSD)
Kalsium, Kalium, dan Magnesium Okra Merah ... 31
DAFTAR GAMBAR
Gambar Halaman 4.1 Kurva Kalibrasi Kalsium... 26 4.2 Kurva Kalibrasi Kalium ... 26 4.3 Kurva Kalibrasi Magnesium ... 27
DAFTAR GAMBAR DALAM LAMPIRAN
Gambar Halaman
1 Spektrofotometer Serapan Atom Hitachi Z-2000 ... 37
2 Tanur (Stuart) ... 37
3 Okra Hijau ... 42
4 Okra Merah ... 42
5 Tanaman Okra Hijau ... 43
6 Tanaman Okra Merah ... 43
7 Growth Centre ... 44
8 Uji kualitatif kalsium dengan pereaksi asam sulfat 1N ... 45
9 Uji kualitatif kalium dengan pereaksi asam pikrat 1% ... 45
10 Uji kualitatif magnesium dengan larutan kuning titan 0,1% .. 45
DAFTAR LAMPIRAN
Lampiran Halaman 1 Hasil Identifikasi Sampel ... 36 2 Gambar Alat ... 37 3 Bagan Alir Penyiapan Sampel dan Destruksi Kering (Okra Hijau) ... 38 4 Bagan Alir Penyiapan Sampel dan Destruksi Kering (Okra Merah) ... 39 5 Bagan Alir Pembuatan Larutan Sampel, Analisa Kualitatif dan Kuantitatif ... 40 6 Gambar Okra Hijau dan Okra Merah ... 42 7 Uji Kualitatif Kalsium, Kalium, dan Magnesium ... 45 8 Data Kalibrasi Kalsium dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi dan Koefisien
Korelasi ... 46 9 Data Kalibrasi Kalium dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi dan Koefisien
Korelasi ... 48 10 Data Kalibrasi Magnesium dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 50 11 Contoh Perhitungan Kadar Kalsium, Kalium, dan
Magnesium ... 52 12 Hasil Analisis Kadar Kalsium, Kalium, dan Magnesium .... 55 13 Perhitungan, Batas Deteksi dan Batas Kuantitasi Kalsium, Kalium, Magnesium ... 57 14 Perhitungan Statistik Kadar Kalsium pada Okra Hijau dan
Okra Merah ... 60 15 Perhitungan Statistik Kadar Kalium pada Okra Hijau dan
16 Perhitungan Statistik Kadar Magnesium pada Okra Hijau
dan Okra Merah... 68 17 Recovery Kalsium, Kalium, dan Magnesium pada Okra
Hijau ... 72 18 Recovery Kalium, Kalium, dan Magnesium pada Okra
Merah ... 74 19 Contoh Perhitungan Recovery Kalsium, Kalium, dan
Magnesium Okra Hijau ... 76
20 Contoh Perhitungan Recovery Kalsium, Kalium, dan
Magnesium Okra Merah ... 80 21 Perhitungan Simpang Baku Relatif (RSD) Kalsium,
Kalium, dan Magnesium Okra Hijau dan Okra Merah ... 84 22 Persentase Perbedaan Kadar Kalsium, Kalium, dan
Magnesium Okra Hijau dan Okra Merah ... 90 23 Hasil Pengujian Beda Nilai Rata- Rata Kadar Kalsium
antara Okra Hijau dan Okra Merah ... 91 24 Hasil Pengujian Beda Nilai Rata- Rata Kadar Kalium
antara Okra Hijau dan Okra Merah ... 93 25 Hasil Pengujian Beda Nilai Rata - Rata Kadar
Magnesium antara Okra Hijau dan Okra Merah ... 95 26 Tabel Distribusi t ... 97 27 Tabel Distribusi F. ... 98
BAB I PENDAHULUAN
1.1 Latar Belakang
Tanaman okra (Abelmoschus esculentus L.) telah tersebar dan dibudidayakan di daratan Afrika, Amerika, Eropa dan Asia. Indonesia merupakan salah satu pusat keragaman okra yang dibudidayakan maupun yang liar yang terbanyak. Terdapat banyak sekali varietas okra, namun secara umum yang banyak dikenal adalah okra hijau dan okra merah. Penamaan tersebut didasarkan pada warna buah okra (Ikrarwati dan Rokhmah, 2016).
Buah muda okra dapat dimanfaatkan dengan cara dimasak sebagai sayur, digoreng, atau sebagai lalapan. Buah okra terdiri dari biji, lendir yang membungkus dan kulit buah. Ketika dimasak, buah okra akan mengeluarkan lendir karena itu biasa dimasak menjadi bahan baku pengental pada sup. Biji okra merupakan sumber protein sehingga biji okra sangat baik diolah menjadi sereal.
Selain mencukupi kebutuhan protein individu, biji okra juga memiliki potensi untuk lebih meningkatkan kesehatan dengan cara melepaskan peptida bioaktif yang dapat mengobati hipertensi (Ikrarwati dan Rokhmah, 2016; Castillo, dkk., 2017).
Mineral memegang peranan penting dalam pemeliharaan fungsi tubuh, baik tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan. Keseimbangan mineral di dalam tubuh diperlukan untuk pengaturan kerja enzim, pemeliharaan keseimbangan asam basa, pemeliharaan kepekaan otot dan saraf terhadap rangsangan (Almatsier, 2009).
Kalsium merupakan mineral paling banyak terdapat dalam tubuh yaitu 1,5-2% dari berat badan orang dewasa. Peningkatan kebutuhan kalsium terjadi pada masa pertumbuhan, kehamilan dan menyusui. Kalsium di tubuh berperan dalam pembentukan tulang dan gigi, mengatur pembekuan darah, katalisator reaksi-reaksi biologik, dan kontraksi otot. Kalium memegang peran penting dalam pemeliharaan keseimbangan cairan dan elektrolit serta keseimbangan asam basa.
Kebutuhan minimum akan kalium ditaksir sebanyak 2000 mg sehari. Magnesium memegang peranan penting dalam lebih dari tiga ratus jenis sistem enzim di dalam tubuh. Kecukupan magnesium rata-rata sehari untuk Indonesia ditetapkan sekitar 4,5 mg/kg berat badan (Almatsier, 2009).
Setiap 100 g okra mengandung 33 kcal energi; 7,45 g karbohidrat; 3,2 g serat pangan; 0,19 g lemak; 2 g protein; 90,19 g air; 82 mg kalsium; 0,62 mg besi;
57 mg magnesium; 299 mg kalium, dan 0,58 mg seng (Kumar, dkk., 2013).
Hasil informasi yang didapat dari masyarakat okra hijau mengandung mineral yang lebih banyak dibandingkan dengan okra merah. Belum ada literatur yang dapat menjelaskan perbedaan kadar mineral antara okra hijau dan okra merah. Berdasarkan hal tersebut maka penulis merasa perlu melakukan pemeriksaan kadar mineral kalsium, kalium, dan magnesium dari okra hijau dan okra merah.
Pada penelitian ini, pemeriksaan mineral kalsium, kalium, dan magnesium dengan menggunakan spektrofotometri serapan atom karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm) dan pelaksanaan nya relatif cepat dan sederhana, dan interferensinya sedikit (Gandjar dan Rohman, 2017).
1.2 Perumusan Masalah
1. Apakah kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah yang beredar di masyarakat sama dengan kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah berdasarkan literatur 2. Apakah ada perbedaan kadar kalsium, kalium, dan magnesium yang
terkandung dalam okra hijau dan yang terkandung dalam okra merah 1.3 Hipotesis
1. Kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah yang beredar di masyarakat sama dengan kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah berdasarkan literatur.
2. Terdapat perbedaan kadar kalsium, kalium, dan magnesium yang terkandung dalam okra hijau dan yang terkandung dalam okra merah.
1.4 Tujuan Penelitian
1. Untuk mengetahui apakah kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah yang beredar di masyarakat sama dengan kadar kalsium, kalium, dan magnesium dalam okra hijau dan okra merah berdasarkan literatur.
3. Untuk membandingkan kadar kalsium, kalium, dan magnesium yang terkandung dalam okra hijau dan yang terkandung dalam okra merah.
1.4 Manfaat Penelitian
Untuk memberikan informasi kepada masyarakat tentang kandungan kalsium, kalium, dan magnesium yang terdapat dalam okra hijau dan dalam okra merah.
BAB II
TINJAUAN PUSTAKA
2.1 Okra
2.1.1 Sistematika Tumbuhan
Menurut Herbarium Medanense, (2018), sistematika tumbuhan okra adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Malvales Famili : Malvaceae Genus : Abelmoschus
Spesies : Abelmoschus esculentus (L.) Moench.
2.1.2 Nama Lain
Okra dikenal dengan nama lain lady’s finger (Inggris), gumbo (Amerika), guin-gumbo (Spanyol), guibeiro (Portugal), bhindiin (India), kenkase (Etiopia)
(Gemede, dkk., 2015).
2.1.3 Deskripsi Tumbuhan
Okra adalah tanaman yang tumbuh di daerah tropis, subtropis dan daerah dengan temperatur hangat. Tanaman okra tumbuh subur di tanah humus dengan pH berkisar antara 6-6,7. Tinggi tanaman okra adalah sekitar 2 meter. Memiliki daun dengan diameter 10-20 cm, lebar dan kasar. Memiliki bunga dengan diameter 4-8 cm, 5 kelopak bunga berwarna putih hingga kuning, terkadang
berwarna merah atau ungu di dasar kelopak bunga. Buah dengan panjang 10- 25cm, berdiameter 1,5-3cm, meruncing di atas dan berisi biji berbentuk ginjal
(Roy, dkk., 2014).
2.1.4 Kandungan Kimia dan Kegunaan
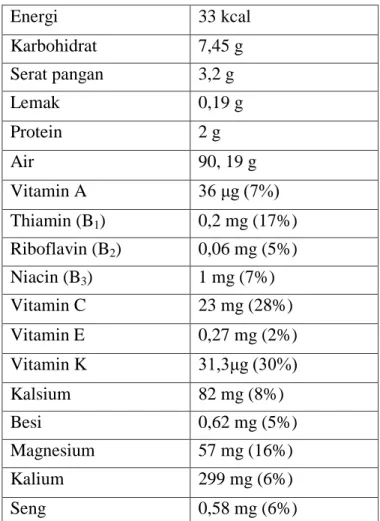
Menurut Kumar, dkk., (2013), komposisi nutrisi untuk setiap 100 g okra yang dikonsumsi ditunjukkan pada table 2.1
Tabel 2.1 Komposisi Nutrisi untuk Setiap 100 g okra (Kumar, dkk., 2013)
Energi 33 kcal
Karbohidrat 7,45 g
Serat pangan 3,2 g
Lemak 0,19 g
Protein 2 g
Air 90, 19 g
Vitamin A 36 μg (7%)
Thiamin (B1) 0,2 mg (17%) Riboflavin (B2) 0,06 mg (5%) Niacin (B3) 1 mg (7%)
Vitamin C 23 mg (28%)
Vitamin E 0,27 mg (2%)
Vitamin K 31,3μg (30%)
Kalsium 82 mg (8%)
Besi 0,62 mg (5%)
Magnesium 57 mg (16%)
Kalium 299 mg (6%)
Seng 0,58 mg (6%)
Buah muda okra dapat dimanfaatkan sebagai sayur, salad, sup, baik buah segar maupun yang direbus. Buah okra akan mengeluarkan lendir pada saat dimasak. Lendir buah okra memiliki manfaat untuk kesehatan ketika digunakan
mengikat kolestrol dan asam empedu membawa racun untuk dibuang oleh hati.
Okra mengandung berbagai nutrisi penting, dimana hampir dari setengahnya adalah serat larut dalam bentuk pektin yang membantu untuk menurunkan kadar serum kolestrol dan menurunkan resiko penyakit jantung. Fraksi lain dari okra adalah serat tidak larut yang dapat membantu saluran pencernaan tetap sehat.
Okra juga dikenal sebagai tanaman yang memiliki aktivitas antioksidan yang tinggi. Okra memiliki potensi yang menguntungkan bagi kesehatan dalam beberapa penyakit seperti penyakit kardiovaskular, diabetes tipe 2, penyakit pencernaan, dan beberapa penyakit kanker (Gemede, dkk., 2015).
2.2 Mineral
Mineral memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan.
Disamping itu, mineral berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier, 2009).
Mineral yang dibutuhkan manusia diklasifikasikan menjadi dua golongan, yaitu mineral makro dan mineral mikro. Mineral makro merupakan mineral yang jumlahnya relatif tinggi (>0,005% dari berat badan) di dalam jaringan tubuh. Mineral mikro disebut sebagai unsur renik (trace elements) terdapat <0,005% dari berat badan. Unsur-unsur mineral makro adalah kalsium, fosfor, kalium, sulfur, natrium, klor, magnesium. Unsur-unsur mineral mikro adalah besi, seng, selenium, mangan, tembaga, iodium (Baliwati, dkk., 2010).
2.2.1 Kalsium (Ca)
Kalsium merupakan mineral yang paling banyak terdapat didalam tubuh,
yaitu 1,5-2 % dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg.
Dari jumlah ini, 99% berada di dalam jaringan keras, yaitu tulang dan gigi terutama dalam bentuk hidroksiapatit. Jumlah yang dianjurkan per hari untuk bayi 300-400 mg, anak-anak sebesar 500 mg, remaja 600-700 mg dan dewasa sebesar 500-800 mg (Almatsier, 2009).
Kalsium mempunyai berbagai fungsi dalam tubuh yaitu : a. Pembentukan tulang dan gigi
b. Mengatur pembekuan darah c. Katalisator reaksi-reaksi biologik d. Kontraksi otot
Sumber kalsium utama adalah susu dan hasil susu, seperti keju.
Ikan dimakan dengan tulang termasuk ikan kering, kacang-kacangan dan hasil kacang-kacangan, tahu dan tempe, dan sayuran hijau merupakan sumber kalsium yang baik juga, tetapi bahan makanan ini mengandung banyak zat yang menghambat penyerapan kalsium, seperti serat, fitat dan oksalat. Susu nonfat merupakan sumber terbaik kalsium karena ketersediaan biologiknya tinggi.
Kebutuhan kalsium akan terpenuhi bila kita makan makanan yang seimbang tiap hari. Konsumsi kalsium hendaknya tidak melebihi 2500 mg sehari.
Kelebihan kalsium dapat menimbulkan batu ginjal atau gangguan pada ginjal (Almatsier, 2009).
2.2.2 Kalium (K)
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Sebanyak 95% kalium berada di dalam cairan intraseluler. Bersama natrium, kalium memegang peranan dalam
pemeliharaan keseimbangan asam basa. Bersama kalsium, kalium berperan dalam transmisi saraf dan relaksasi otot. Tekanan darah normal memerlukan perbandingan antara natrium dan kalium yang sesuai di dalam tubuh. Karena merupakan bagian essensial semua sel hidup, sehingga banyak terdapat dalam bahan makanan. Kekurangan kalium karena makanan jarang terjadi, sepanjang seseorang cukup makan sayuran dan buah segar. Kebutuhan minimum akan kalium ditaksir sebanyak 2000 mg sehari (Almatsier, 2009).
2.2.3 Magnesium (Mg)
Hampir 60% magnesium dalam tubuh terdapat pada tulang, 26% dalam otot, dan sisanya ada dalam jaringan lunak serta cairan tubuh. Magnesium memegang peranan penting dalam lebih dari tiga ratus sistem enzim di dalam tubuh. Di dalam cairan ekstraselular, magnesium berperan dalam transmisi saraf, kontraksi otot, dan pembekuan darah. Dalam hal ini, peranan magnesium berlawanan dengan kalsium dimana kalsium merangsang kontraksi otot sedangkan magnesium mengendorkan otot. Kalsium merangsang penggumpalan darah, sedangkan magnesium mencegah penggumpalan darah. Kalsium menyebabkan ketegangan saraf sedangkan magnesium melemaskan saraf. Selain itu, magnesium mencegah kerusakan gigi dengan cara menahan kalsium di dalam email gigi (Almatsier, 2009).
Sumber utama magnesium adalah sayuran hijau, serealia tumbuk, biji- bijian kacangkacangan. Daging, susu dan hasilnya serta cokelat juga merupakan sumber magnesium yang baik. Kekurangan magnesium jarang terjadi karena makanan. Kekurangan magnesium bisa terjadi karena penyakit yang menyebabkan muntah-muntah dan diare (Almatsier, 2009).
2.3 Spektrofotometri Serapan Atom (SSA)
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur mineral dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar total unsur mineral dalam suatu sampel dan tidak tergantung pada bentuk molekul mineral dalam sampel tersebut.
Cara ini cocok untuk analisis sekelumit mineral karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaanya relatif sederhana dan interferensinya sedikit (Gandjar dan Rohman, 2017).
Untuk banyak atom, perbedaan energi antara orbital keadaan dasar dan keadaan tereksitasinya terlalu besar agar eksitasi termal banyak elektron dapat berlangsung. Jika perbedaan energi terlalu besar untuk menghasilkan pembacaan emisi, Spektrofotometri Serapan Atom digunakan. Atom-atom logam diuapkan dalam suatu nyala dan radiasi dilewatkan melalui nyala tersebut. Dalam hal ini, atom-atom yang diuapkan, yang sebagian besar terdapat dalam keadaan dasarnya sehingga tidak memancarkan energi, akan menyerap radiasi dengan energi yang berkaitan dengan perbedaan antara keadaan dasar dan keadaan tereksitasinya (Watson, 2010).
Bagian instrumentasi spekrofotometri serapan atom adalah sebagai berikut:
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga terbuat dari logam atau dilapisi dengan logam tertentu (Gandjar dan Rohman, 2017).
2. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala (flame) dan dengan tanpa nyala (flameless) (Gandjar dan Rohman, 2017).
a. Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan untuk menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalkan gas batubara-udara, suhunya kira kira sebesar 18000C; gas alam-udara:
17000C; asetilen-udara suhunya sebesar 22000C dan gas asetilen-dinitrogen oksida sebesar 30000C. Pemilihan macam bahan pembakar dan gas pengoksidasi serta komposisi perbandingannya sangat mempengaruhi suhu nyala. Pada umumnya nyala dari gas asetilen-nitro oksida menunjukkan emisi latar belakang (background) yang kuat. Sumber nyala asetilen-udara merupakan sumber nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai bahan pembakar, sedangkan udara sebagai bahan pengoksidasi. Propana-udara dipilih untuk logam-logam alkali karena suhu nyala lebih rendah akan mengurangi banyaknya ionisasi. Nyala hidrogen- udara lebih jernih daripada nyala asetilen-udara dalam daerah UV (dibawah 220nm), dan juga karena sifatnya yang mereduksi maka nyala ini sesuai untuk penetapan arsenik dan selenium (Gandjar dan Rohman, 2017).
b. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit (hanya beberapa µl), lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi sinar yang memenuhi kaidah analisis kuantitatif (Gandjar dan Rohman, 2017).
3. Monokromator
Pada spektofomoteri serapan atom, monokromator dimaksudkan untuk memisahkan dan memilih panjang gelombang yang digunakan dalam analisis.
Disamping sistem optik, dalam monokromator juga terdapat suatu alat yang digunakan untuk memisahkan radiasi resonansi dan kontinu yang disebut dengan chopper (Gandjar dan Rohman, 2017).
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman (Gandjar dan Rohman, 2017).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2017).
2.4 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Tindakan ini dilakukan untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel dan tahan akan kisaran analit yang akan dianalisis (Harmita, 2004).
Menurut Harmita (2004), beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai kecermatan yang tinggi, dapat dilakukan dengan berbagai cara seperti menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik, pengontrolan suhu dan pelaksanaannya yang cermat, taat asas sesuai prosedur. Kecermatan ditentukan dengan dua cara yaitu:
i. Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam campuran bahan pembawa sediaan farmasi lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
ii. Metode penambahan baku (standard addition method)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan
dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut.
Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Presisi merupakan ukuran keterulangan metode analisis dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda signifikan secara statistik (Harmita, 2004).
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuan suatu metode mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel. Selektivitas biasanya dinyatakan sebagai derajat penyimpangan metode yang dilakukan terhadap sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai, senyawa sejenis, dan senyawa lain yang dibandingkan terhadap hasil analisis sampel yang tidak mengandung bahan lain yang ditambahkan (Harmita, 2004).
4. Linearitas dan Rentang
Liniearitas merupakan kemampuan suatu metode untuk memperoleh hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran yang diberikan. Linearitas suatu metode merupakan ukuran seberpa baik kurva kalibrasi yang menghubungkan antara absorbansi (y) dengan konsentrasi (x). Liniearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Rentang metode adalah pernyataan batas terendah dan tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan dan linearitas yang dapat diterima (Harmita, 2004).
5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah analit terkecil dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko.
Batas kuantitasi merupakan parameter pada analisis dan diartikan sebagai kuantitas analit terkecil dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama. Penentuan batas deteksi suatu metode berbeda-beda tergantung pada metode analisis itu menggunakan instrumen atau tidak. Pada analisis instrumen batas deteksi dapat dihitung dengan mengukur respon blanko beberapa kali lalu dihitung simpangan baku respon blanko (Harmita, 2004).
6. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu dan hari yang berbeda.
Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
BAB III
METODE PENELITIAN
Jenis penelitian yang dilakukan adalah penelitian deskriptif dengan maksud mengetahui dan membandingkan hasil kadar mineral kalsium, kalium dan magnesium pada okra hijau dan okra merah secara spektrofotometri serapan atom.
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan di Laboratorium Penelitian Farmasi Fakultas Farmasi Universitas Sumatera Utara pada bulan Februari 2018 – Mei 2018.
3.2 Bahan
Bahan-bahan yang digunakan berkualitas pro analisis keluaran E.Merck yaitu Asam nitrat 65% b/v kecuali Aqua demineralisata (PT. Ikapharmindo Putramas). Larutan baku kalsium 1000 μg/ml, larutan baku kalium 1000 μg/ml, larutan baku magnesium 1000 μg/ml, Asam sulfat 1N, Etanol 96%, Natrium hidroksida 2N, Asam pikrat 1% b/v dan Kuning titan 0,1% b/v.
3.3 Alat
Alat-alat yang digunakan dalam penelitian ini adalah Spektrofotometer Serapan Atom (Hitachi Zeeman-2000) dengan nyala udara-asetilen lengkap dengan lampu katoda Ca, K dan Mg, Neraca analitik (BOECO), Tanur (Stuart), Blender (Miyako), Hot plate (BOECO), Kertas saring Whatman no.42, Kurs porselen, dan Alat-alat gelas (Pyrex dan Oberol).
3.4 Pembuatan Pereaksi 3.4.1 Larutan HNO3 (1:1)
Larutan HNO3 65% b/v sebanyak 500 ml diencerkan dengan 500 ml air suling (Manan, 2009).
3.4.2 Larutan Asam Sulfat 1N
Sebanyak 3 ml larutan asam sulfat 96% v/v diencerkan dengan akuabides hingga 100 ml (Ditjen POM Depkes RI, 1979).
3.4.3 Larutan Natrium Hidroksida 2N
Sebanyak 80,02 gram NaOH dilarutkan dengan air suling hingga 1000 ml (Ditjen POM Depkes RI, 1979).
3.4.4 Larutan Kuning Titan 0,1% b/v
Larutan kuning titan 0,1% b/v dibuat dengan cara melarutkan 0,1 g titan yellow dalam 100 ml air suling (Manan, 2009).
3.4.5 Asam Pikrat 1% b/v
Sebanyak 1 gram asam pikrat dilarutkan dalam air suling hingga 100 ml (Manan, 2009).
3.5 Prosedur Penelitian 3.5.1 Pengambilan Sampel
Pengambilan sampel dengan cara sampling purposif. Bagian tanaman yang diambil sebagai sampel adalah buah okra hijau dan okra merah dari Pasar Garuda di Medan. Gambar dapat dilihat pada Lampiran 6, halaman 42 (Etikan, dkk., 2016).
3.5.2 Penyiapan Sampel
Sebanyak 500g okra hijau dan 500g okra merah dicuci bersih, ditiriskan, dikeringkan dengan cara diangin-anginkan. Kemudian masing-masing 500 gram okra hijau dan okra merah dihaluskan dengan cara diblender (Agoes, 2018).
3.5.3 Proses Destruksi Kering
Sampel yang telah dihaluskan okra hijau dan okra merah masing-masing ditimbang teliti sebanyak 25 g dimasukkan ke dalam kurs porselen, diarangkan diatas hot plate dengan suhu 100˚C, lalu diabukan di tanur mula-mula pada temperatur 100˚C dan secara perlahan-lahan dinaikkan secara interval 25˚C setiap 5 menit sampai temperatur menjadi 500˚C dan pengabuan dilakukan selama 72 jam untuk okra hijau dan okra merah. Setelah itu dibiarkan dingin di dalam desikator. Bagian alir proses destruksi kering dapat dilihat pada Lampiran 3 dan 4, halaman 38 dan 39 (Agoes, 2018).
3.5.4 Pembuatan Larutan Sampel
Hasil destruksi dilarutkan dengan 5 ml HNO3 (1:1) hingga larut sempurna, kemudian dimasukkan ke dalam labu tentukur 100 ml dan kurs porselen dibilas dengan aqua demineralisata sebanyak tiga kali. Hasil pembilasan dimasukkan ke dalam labu tentukur. Setelah itu dicukupkan volumenya dengan aqua demineralisata hingga garis tanda. Kemudian disaring dengan kertas saring whatman no.42 dengan membuang 5 ml larutan pertama hasil penyaringan untuk menjenuhkan kertas saring lalu dimasukkan ke dalam botol. Analisis yang sama dilakukan sebanyak 6 kali untuk masing-masing sampel. Bagian alir proses pembuatan larutan sampel dapat dilihat pada Lampiran 5, halaman 40 dan 41 (Agoes, 2018).
3.5.5 Analisis Kualitatif 3.5.5.1 Kalsium
3.5.5.1.1 Uji kristal dengan Asam sulfat 1N
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam sulfat 1N dan etanol 96% akan terbentuk endapan putih lalu diamati di bawah mikroskop. Jika terdapat kalsium akan terlihat kristal berbentuk jarum (Vogel, 1954).
3.5.5.2 Kalium
3.5.5.2.1 Uji Kristal Kalium dengan Asam Pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat kalium akan terlihat kristal berbentuk jarum besar (Vogel, 1954).
3.5.5.3 Magnesium
3.5.5.3.1 Reaksi warna dengan Kuning Titan 0,1% b/v
Dimasukkan 1 ml larutan sampel ke dalam tabung reaksi, lalu ditambahkan 5-6 tetes natrium hidroksida 2N dan 3 tetes kuning titan 0,1%.
Dihasilkan endapan merah terang (Vogel, 1954).
3.5.6 Analisis Kuantitatif
3.5.6.1 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 μg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan dengan aqua demineralisata hingga garis tanda (konsentrasi 50 μg/ml) (larutan baku I). Larutan bauku I dipipet 10 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan dengan aqua demineralisata hingga garis tanda (konsentrasi 10 μg/ml)
Larutan untuk kurva kalibrasi dibuat dengan memipet larutan induk baku II sebanyak 2.5 ml, 5 ml, 7,5 ml, 10 ml dan 12,5 ml, dilarutkan dalam labu 25 ml sehingga didapatkan konsentrasi berturut-turut 1 μg/ml, 2 μg/ml, 3 μg/ml, 4 μg/ml dan 5 μg/ml dan diukur pada panjang gelombang 422,7 nm dengan nyala udara- asetilen.
3.5.6.2 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalsium (1000 μg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan dengan aqua demineralisata hingga garis tanda (konsentrasi 50 μg/ml) (larutan baku I).
Larutan untuk kurva kalibrasi dibuat dengan memipet larutan induk baku I sebanyak 1 ml, 2 ml, 3 ml, 4 ml dan 5 ml, dilarutkan dalam labu 25 ml sehingga didapatkan konsentrasi berturut-turut 2 μg/ml, 4 μg/ml, 6 μg/ml, 8 μg/ml dan 10 μg/ml dan diukur pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.5.6.3 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku kalsium (1000 μg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan dengan aqua demineralisata hingga garis tanda (konsentrasi 50 μg/ml) (larutan baku I). Larutan bauku I dipipet 10 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan dengan aqua demineralisata hingga garis tanda (konsentrasi 10 μg/ml)
Larutan untuk kurva kalibrasi dibuat dengan memipet larutan induk baku II sebanyak 0.5 ml, 1 ml, 1,5 ml, 2 ml, dan 2,5 ml, dilarutkan dalam labu 25 ml sehingga didapatkan konsentrasi berturut-turut 0,2 μg/ml, 0,4 μg/ml, 0,6 μg/ml, 0,8 μg/ml, dan 1 μg/ml dan diukur pada panjang gelombang 285,2 nm dengan nyala udara-asetilen.
3.5.6.4 Penetapan Kadar Mineral dalam Sampel 3.5.6.4.1 Penetapan Kadar Kalsium
Larutan sampel okra hijau dan okra merah masing-masing sebanyak 2 ml dimasukkan ke dalam labu tentukur 100 ml dan diencerkan dengan aqua demineralisata hingga garis tanda. Diukur absorbansinya dengan spektrofotometri serapan atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh berada di dalam rentang nilai kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.4.2 Penetapan Kadar Kalium
Larutan sampel okra hijau dan okra merah masing-masing sebanyak 1 ml dimasukkan ke dalam labu tentukur 100 ml dan diencerkan dengan aqua demineralisata hingga garis tanda. Diukur absorbansinya dengan spektrofotometri serapan atom pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh berada di dalam rentang nilai kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.4.3 Penetapan Kadar Magnesium
Larutan sampel okra hijau dan okra merah sebanyak 0,4 ml dimasukkan ke dalam labu tentukur 100 ml dan diencerkan dengan aqua demineralisata hingga garis tanda. Diukur absorbansinya dengan spektrofotometri serapan atom pada panjang gelombang 285,2 nm. Nilai absorbansi yang diperoleh berada di dalam rentang nilai kurva kalibrasi larutan baku magnesium. Konsentrasi magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.7 Analisis Data Secara Statistik 3.5.7.1 Penolakan Hasil Pengamatan
Kadar kalsium, kalium dan magnesium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik.
Menurut Sudjana, (2002), standar deviasi dapat dihitung dengan rumus:
SD = √∑(Xi−X)²𝑛−1 Keterangan: Xi = Kadar mineral
X = Kadar rata-rata mineral n = Jumlah pengulangan Untuk mencari t hitung digunakan rumus:
t ℎ𝑖𝑡𝑢𝑛𝑔 = X − 𝑋̅
𝑆𝐷/√𝑛
dan untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 99%, α = 0.01, dk = n-1, dapat digunakan rumus:
Kadar Mineral :μ = X ± (t(α/2, dk) x SD / √n ) 𝑆𝐷/√𝑛 Keterangan : X = Kadar rata-rata mineral
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = interval kepercayaan
n = jumlah pengulangan
3.5.7.2 Pengujian Beda Nilai Rata-Rata Sampel
Menurut Sudjana (2002), sampel yang dibandingkan adalah independen dan jum- lah pengamatan masing-masing lebih kecil dari 30 dan variansi (σ) tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi kedua
populasi sama (σ1 = σ2) atau berbeda (σ1 ≠ σ2) dengan menggunakan rumus di bawah ini:
Keterangan : Fo = Beda nilai yang dihitung, S1 = Standar deviasi terbesar, S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka dilanjutkan uji dengan distribusi t dengan rumus :
(X1 – X2) to =
Sp √1/n1 + 1/n2
Keterangan : X1 = kadar rata-rata sampel 1 n 1 = Jumlah perlakuan sampel 1 X2 = kadar rata-rata sampel 2 n 2 = Jumlah perlakuan sampel 2 Sp = Simpangan baku
jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus : (X1 – X2)
to =
√S12
/n1 + S22
/n2
Keterangan : X1 = kadar rata-rata sampel 1 S1 = Standar deviasi sampel 1 X2 = kadar rata-rata sampel 2 S2 = Standar deviasi sampel 2 n1 = Jumlah perlakuan sampel 1 n2 = Jumlah perlakuan sampel 2 Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai kritis t, dan sebaliknya.
Fo = 2
2 2 1
S S
3.5.8 Validasi Metode Analisis
3.5.8.1 Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (µg/ml) =√(𝑌−𝑌𝑖)𝑛−2 2
Batas Deteksi (µg/ml) = 3 X 𝑆𝑌 𝑋𝑠𝑙𝑜𝑝𝑒⁄
Batas Kuantitasi (µg/ml) = 10 X 𝑆𝑌 𝑋𝑠𝑙𝑜𝑝𝑒⁄ 3.5.8.2 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu (Ermer dan McB. Miller, 2005).
Sampel 500 g diambil buahnya lalu dibersihkan dari pengotoran, dikeringkan dan dihaluskan. Sampel yang telah dihaluskan ditimbang secara seksama sebanyak 25 gram di dalam krus porselen, lalu ditambahkan larutan baku yaitu: 1,5 ml larutan baku kalsium (konsentrasi 1000 µg/ml), 5,6 ml larutan baku kalium (konsentrasi 1000 µg/ml), 1,2 ml larutan baku magnesium
(konsentrasi 1000 µg/ml), 5,4 ml larutan baku kalium (konsentrasi 1000 µg/ml), 1,5 ml larutan baku magnesium (konsentrasi1000 µg/ml) untuk okra merah, kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya.
Menurut (Harmita, 2004) persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
Persen Perolehan Kembali= CF-CA
CA* x 100%
Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku CF = Kadar logam dalam sampel setelah penambahan baku C*A = Kadar larutan baku yang ditambahkan dalam sampel 3.5.8.3 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut (Harmita, 2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut: RSD = 100%
X SD
Keterangan :
X = Kadar rata-rata sampel SD = Standar Deviasi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya mineral kalsium, kalium dan magnesium pada hijau dan okra merah. Data dapat dilihat pada Tabel 4.1 dan gambar dapat dilihat pada Lampiran 7 halaman 44.
Tabel 4.1 Hasil Analisis Kualitatif pada Okra Hijau dan Okra Merah
No. Mineral Pereaksi Hasil Reaksi Keterangan
1. Kalsium H2SO4 1N Terbentuk
Kristal
+
2. Kalium Asam Pikrat Terbentuk
Kristal Panjang +
3. Magnesium Natrium Hidroksida + Kuning Titan 0,1%
Endapan merah terang
+
Keterangan: + : mengandung mineral
Tabel 4.1 diatas menunjukkan bahwa okra hijau dan okra merah mengandung mineral kalsium, kalium dan magnesium. Sampel dikatakan positif mengandung mineral kalsium karena terbentuk kristal dengan penambahan asam sulfat 1N, mengandung mineral kalium karena terbentuk kristal panjang dengan penambahan asam pikrat dan mengandung magnesium karena menghasilkan endapan warna merah terang dengan penambahan larutan kuning titan 0,1%
b/v dan ditambah natrium hidroksida (Vogel, 1979).
4.2 Analisis Kuantitatif
4.2.1 Kurva kalibrasi Kalsium, Kalium dan Magnesium
Data hasil pengukuran absorbansi larutan baku dan perhitungan persamaan garis regresi kalsium, kalium dan magnesium masing-masing dapat dilihat pada Lampiran 8-10, halaman 45-50. Kurva kalibrasi larutan baku kalsium, kalium dan magnesium dapat dilihat pada Gambar 4.1, Gambar 4.2 dan Gambar 4.3.
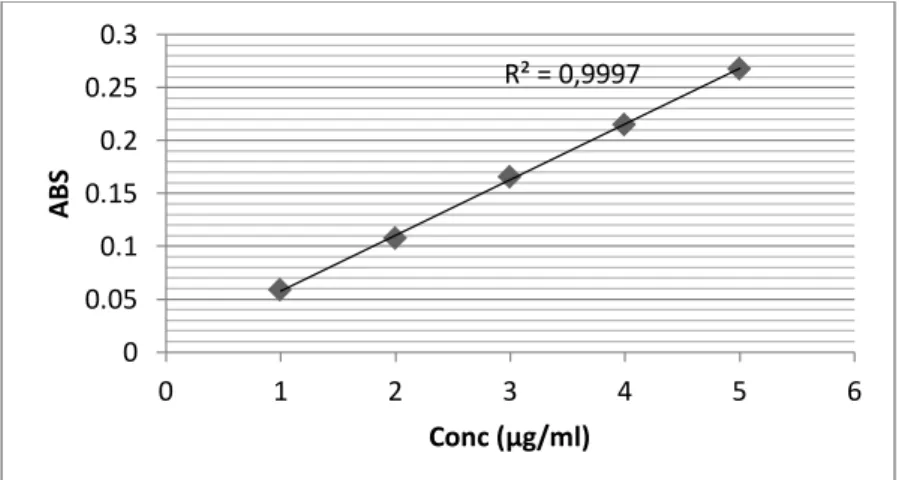
Gambar 4.1 Kurva Kalibrasi Kalsium
R² = 0,9997
0 0.05 0.1 0.15 0.2 0.25 0.3
0 1 2 3 4 5 6
ABS
Conc (μg/ml)
R² = 0,9994
0 0.2 0.4 0.6 0.8 1
0 2 4 6 8 10 12
ABS
Conc (μg/ml)
Gambar 4.3 Kurva Kalibrasi Magnesium
Dari pengukuran kurva kalibrasi tersebut diperoleh persamaan garis regresi untuk kalsium, kalium dan magnesium masing-masing yaitu Y = 0,0532X + 0,0025, Y=0,0907X + 0,0170, dan Y= 0,6981X + 0,0119
Berdasarkan kurva diatas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) untuk kalsium, kalium dan magnesium masing-masing sebesar 0,9997; 0,9994 dan 0,9995. Nilai r
≥ 0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi) (Ermer dan McB. Miller, 2005).
4.2.2 Analisis Kadar Kalsium, Kalium dan Magnesium pada Okra Hijau dan Okra Merah
Penentuan kadar kalsium, kalium, dan magnesium dilakukan secara spektrofotometri serapan atom. Konsentrasi mineral kalsium, kalium dan magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku masing-masing mineral. Data dan contoh perhitungan masing-masing dapat dilihat pada Lampiran 11 dan 12, halaman 51-55. Kadar kalsium, kalium dan magnesium pada sampel dapat dilihat pada Tabel 4.2.
R² = 0,9995
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8
0 0.2 0.4 0.6 0.8 1 1.2
ABS
Conc (μg/ml)
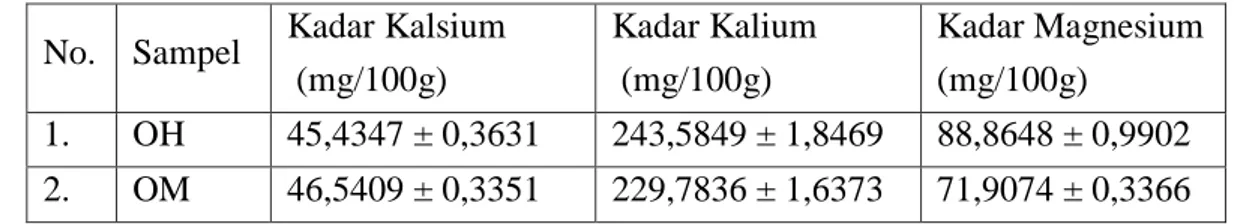
Tabel 4.2 Kadar Kalsium, Kalium dan Magnesium pada Sampel No. Sampel Kadar Kalsium
(mg/100g)
Kadar Kalium (mg/100g)
Kadar Magnesium (mg/100g)
1. OH 45,4347 ± 0,3631 243,5849 ± 1,8469 88,8648 ± 0,9902 2. OM 46,5409 ± 0,3351 229,7836 ± 1,6373 71,9074 ± 0,3366 Keterangan: OH = Okra Hijau; OM = Okra Merah
Setelah dilakukan uji statistik terhadap kadar sampel maka dapat dilihat bahwa kadar kalium dan magnesium dalam okra hijau lebih tinggi dibanding okra merah, sedangkan kadar kalsium dalam oka merah lebih tinggi dibanding okra hijau. Mineral kalsium dalam okra hijau sebesar 45,4347 ± 0,3631mg/100g dan okra merah sebesar 46,5409 ± 0,3351mg/100g. Mineral kalium dalam okra hijau sebesar 243,5849 ± 1,8469 mg/100g dan okra merah sebesar 229,7836 ± 1,6373mg/100g. Mineral magnesium dalam okra hijau sebesar 88,8648 ± 0,9902 mg/100g dan okra merah sebesar 71,9074 ± 0,3366 mg/100g. Penurunan kadar mineral kalsium sebanyak 2,3768%, kalium sebanyak 5,7251% dan magnesium sebanyak 19,0822%.
4.2.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalsium, kalium dan magnesium diperoleh batas deteksi dan batas kuantitasi dari kalsium, kalium dan magnesium yang perhitungannya dapat dilihat pada Lampiran 13, halaman 56-58. Batas deteksi dan batas kuantitasi dari kalsium, kalium dan magnesium pada sampel dapat dilihat pada Tabel 4.3.
Tabel 4.3 Batas Deteksi dan Batas Kuantitasi Kalsium, Kalium, dan Magnesium
No. Mineral Batas Deteksi
(µg/mL)
Batas Kuantitasi (µg/mL)
1. Kalsium 0,1595 0,5319
2. Kalium 0,4189 1,3964
3. Magnesium 0,0401 0,1338
Berdasarkan Tabel 4.3 diatas, dapat dilihat bahwa semua hasil kadar yang diperoleh pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi dan memenuhi syarat batas deteksi dan batas kuantitasi yang telah diperoleh.
4.2.4 Uji Perolehan Kembali (Recovery)
Data hasil dan contoh perhitungan uji perolehan kembali (recovery) kadar kalsium, kalium, dan magnesium pada okra hijau dan okra merah setelah penambahan masing-masing larutan baku kalsium, kalium, dan magnesium dalam sampel dapat dilihat pada Lampiran 17, 18, 19 dan 20, halaman 71-82. Uji perolehan kembali kalsium, kalium dan magnesium pada okra hijau dan okra merah dapat dilihat pada Tabel 4.4 dan Tabel 4.5.
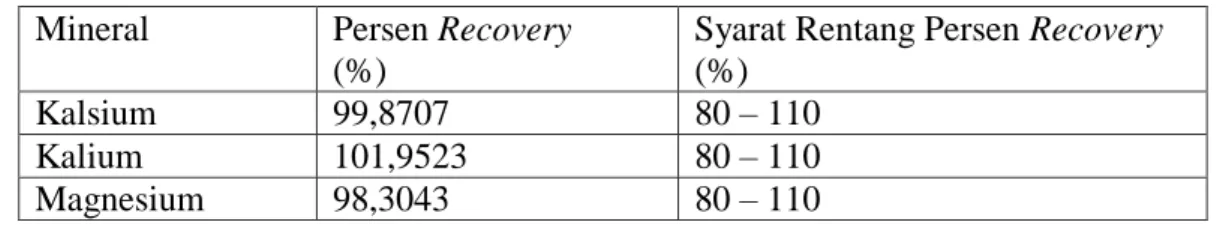
Tabel 4.4 Uji Perolehan Kembali (Recovery) Kalsium, Kalium dan Magnesium Okra Hijau
Mineral Persen Recovery (%)
Syarat Rentang Persen Recovery (%)
Kalsium 99,8707 80 – 110
Kalium 101,9523 80 – 110
Magnesium 98,3043 80 – 110
Tabel 4.5 Uji Perolehan Kembali (Recovery) Kalsium, Kalium dan Magnesium Okra Merah
Mineral Persen Recovery (%)
Syarat Rentang Persen Recovery (%)
Kalsium 97,2596 80 – 110
Kalium 98,7947 80 – 110
Magnesium 98,6092 80 – 110
Berdasarkan Tabel 4.4 dan Tabel 4.5 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) pada okra hijau untuk kalsium, kalium dan magnesium masing-masing sebesar 99,8707%; 101,9523%; dan 98,3043% dan
rata-rata hasil uji perolehan kembali (recovery) pada okra merah untuk kalsium, kalium dan magnesium masing-masing sebesar 97,2596%, 98,7947%, dan 98,6092%. Hasil uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80-120% (Ermer dan McB. Miller, 2005). Dari hasil persen uji perolehan kembali (recovery) yang diperoleh menunjukkan kecermatan (accuracy) kerja yang memuaskan pada saat pemeriksaan kadar kalsium, kalium
dan magnesium dalam sampel.
4.2.5 Simpangan Baku Relatif
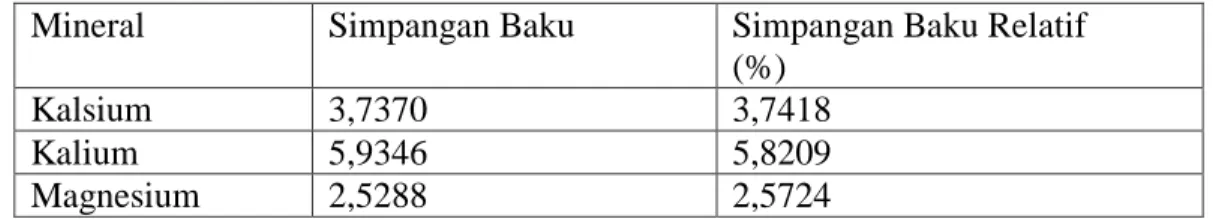
Data perhitungan simpangan baku (SD) dan simpangan baku relatif (RSD) untuk kalsium, kalium dan magnesium okra hijau dapat dilihat pada Lampiran 21 halaman 83-88. Simpangan baku (SD) dan simpangan baku relatif (RSD) kalsium, kalium dan magnesium pada okra hijau dan okra merah dapat dilihat pada Tabel 4.6. dan 4.7.
Tabel 4.6 Simpangan Baku (SD) dan Simpangan Baku Relatif (RSD) Kalsium, Kalium dan Magnesium pada Okra Hijau
Mineral Simpangan Baku Simpangan Baku Relatif
(%)
Kalsium 3,7370 3,7418
Kalium 5,9346 5,8209
Magnesium 2,5288 2,5724
Tabel 4.7 Simpangan Baku (SD) dan Simpangan Baku Relatif (RSD) Kalsium, Kalium dan Magnesium pada Okra Merah
Mineral Simpangan Baku Simpangan Baku Relatif
(%)
Kalsium 7,0572 7,2560
Kalium 10,4871 10,6150
Magnesium 4,1561 4,2147
Berdasarkan Tabel 4.6 dan Tabel 4.7 di atas, dapat dilihat nilai simpangan baku (SD) pada okra hijau untuk kalsium, kalium dan magnesium masing-masing sebesar, 3,7370, 5,9346, 2,5288 . Nilai simpangan baku relatif (RSD) yang diperoleh untuk kalsium, kalium dan magnesium masing-masing sebesar 3,7418%, 5,8209%, dan 2,5724%. Nilai simpangan baku (SD) pada okra merah untuk kalsium, kalium dan magnesium masing-masing sebesar, 7,0572, 10,4871, dan 4,1561. Nilai simpangan baku relatif (RSD) yang diperoleh untuk kalsium, kalium dan magnesium masing-masing sebesar 7,2560%, 10,6150%, 4,2147%. Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih 16%. Dari hasil yang diperoleh menunjukkan bahwa penelitian yang dilakukan ini memiliki keseksamaan (presisi) yang baik.
4.2.6 Pengujian Beda Nilai Rata-Rata Kadar Kalsium, Kalium, dan Magnesium Pada Okra Hijau dan Okra Merah
Pengujian beda nilai rata-rata kadar kalsium, kalium, dan magnesium pada sampel bertujuan untuk melihat apakah ada perbedaan yang signifikan pada rata-rata kadar kalsium, kalium, dan magnesium antara daun petai cina segar dan daun petai cina rebus. Uji statistik yang digunakan yaitu uji beda nilai rata-rata kadar kalsium, kalium, dan magnesium antara okra hijau dan okra merah yang
kadar yang signifikan antara kedua sampel diperoleh jika t0 atau thitung lebih tinggi atau lebih rendah dari nilai ttabel. Perhitungan beda nilai rata-rata kadar kalsium, kalium, dan magnesium pada okra hijau dan okra merah dapat dilihat pada Lampiran 23, 24, dan 25 halaman 90-95.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil analisis menunjukkan bahwa terdapat perbedaan kadar kalsium, kalium dan magnesium pada okra hijau dan okra merah yang beredar di masyarakat dibandingkan dengan di literatur. Hasil analisis kadar kalsium, kalium dan magnesium pada okra hijau yang beredar masing-masing sebesar 45,43 ± 0,36 mg/100g; 243,58 ± 1,84 mg/100g; dan 88,86 ± 0,99 mg/100g, sedangkan kadar kalsium, kalium dan magnesium pada okra merah yang beredar masing- masing sebesar 46,54 ± 0,33 mg/100g; 229,78 ± 1,63 mg/100g; dan 71,90 ± 0,3366 mg/100g
b. Analisis statistik menunjukkan bahwa terdapat perbedaan kadar kalsium, kalium dan magnesium pada okra hijau dan okra merah. Kadar kalium dan
magnesium pada okra hijau lebih tinggi daripada okra merah, sedangkan kadar kalsium pada okra merah lebih tinggi daripada okra hijau.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan analisis kandungan mineral lainnya serta diinformasikan kepada masyarakat bahwa okra hijau maupun okra merah dapat menjadi sumber mineral.
DAFTAR PUSTAKA
Agoes, A. S. (2018). Analisis Kadar Kalsium, Besi, Kalium dan Magnesium pada Kolang-Kaling (Arenga Pinnata Merr) Segar, Direbus dan Setelah Diproses Menjadi Manisan Secara Spektrofotometri Serapan Atom.
Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 19-20.
Almatsier, S. (2009). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Halaman 228-229, 233-237, 246-247.
Baliwati, Y. F., Khomsan, A dan Dwiriani, C. M. (2010). Pengantar Pangan dan Gizi. Cetakan III. Jakarta: Penebar Swadaya. Halaman 56.
Costillo, I. J. B., Angelia, M. R. N., Torio, M. A. O. dan Belina-Aldemita, M. D.
(2017). Antihypertensive Property of The Peptic and Chymotryptic Hydrolysates Derived From The Crude Protein Extract of Okra [Abelmoschus esculentus(L.) Moench] Seeds. International Food Research Journal, 24(6): 2586-2592.
Ditjen POM Depkes RI. (1979). Farmakope Indonesia. Cetakan I. Edisi Ketiga.
Jakarta: Departemen Kesehatan RI. Halaman 692.
Ermer, J., dan McB. Miller, J. H. (2005). Method Validation in Pharmaceutical Analysis.A Guide to Best Pratice. Weinheim: Wiley-VCH. Halaman 171.
Etikan, I., Musa, S. A., Alkassim, R. S. (2016). Comparison of Convenience Sampling and Purposive Sampling. American Journal of Theoretical and Applied Statistics. 2016: 5 (1): 1-4.
Gandjar, I. G., dan Rohman, A. (2017). Kimia Farmasi Analisis. Cetakan XVI.
Yogyakarta: Pustaka Pelajar. Halaman 18, 22-23, 298-322.
Gemede, H. F., Ratta, N., Haki, G. D., Woldegiorgis, A. Z., dan Beyene, F.
(2015). Nutritional Quality and Health Benefit of Okra (Abelmoschus esculentus): A Review. Journal Food Processing and Technology: 6: 6.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel Majalah Ilmu Kefarmasian. 1(3): 117- 135.
Ikrarwati dan Rokhmah, N. A. (2016). Budidaya Okra dan Kelor dalam Pot.
Jakarta: Balai Pengkajian Teknologi Pertanian Jakarta. Halaman 2-4.