OPTIMASI KOMPOSISI DAN KECEPATAN ALIR FASE GERAK METODE KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK UNTUK PENETAPAN KADAR ASAM ASKORBAT DALAM SEDIAAN LARUTAN
INJEKSI OBAT PEMUTIH KULIT MERK “X” Eunike Lystia Florentien Kelana Jeversoon
128114025 INTISARI
Asam askorbat merupakan salah satu agen pemutih kulit yang paling sering digunakan di masyarakat Indonesia. Kemampuannya melindungi kulit dari radiasi UV mampu mencegah pembentukan melanin pada kulit.
Penelitian ini bertujuan untuk menentukan kondisi optimal Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik sebagai metode yang digunakan dalam penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X”. Sistem KCKT fase terbalik menggunakan kolom Phenomenex® C18 dimensi 250
x 4,6 mm ukuran partikel 5µm dengan fase gerak metanol : 0,01 M bufer fosfat pH 3. Optimasi dilakukan dengan mengubah komposisi fase gerak yaitu 10 : 90; 20 : 80; 30 : 70; 40 : 60; 50 : 50 dan kecepatan alir fase gerak yaitu 0,7; 0,8; 0,9; 1,0; 1,1 dan 1,2 mL/menit menggunakan detektor ultraviolet pada panjang gelombang 244 nm.
Analisis hasil dilakukan dengan melakukan pengamatan terhadap nilai
tailing factor, nilai resolusi, nilai koefisien variansi, HETP, area under curve (AUC), tinggi puncak dan waktu retensi asam askorbat hasil pemisahan.
Kondisi optimum sistem KCKT fase terbalik yang diperoleh adalah fase gerak metanol : 0,01 M bufer fosfat pH 3 (40:60) dengan kecepatan alir 0,9 mL/menit. Kondisi ini telah memenuhi parameter pemisahan yang baik yaitu nilai
tailing factor 1,42 dan waktu retensi 3,03. Nilai koefisien variansi (% CV) yang diperoleh dari Uji Kesesuaian Sistem (UKS) untuk parameter tailing factor, HETP, AUC, tinggi puncak, dan waktu retensi secara berturut-turut adalah 0,36%, 0,47%, 0,05%, 0,23%, dan 0,04%.
ABSTRACT
Ascorbic acid is one of skin whitening agents which are most frequently used in Indonesia societies. Its ability to protect skin from UV radiation capables to inhibit the formation of melanin in human skin.
This study aims to determine the optimum conditions of Reversed-Phase High Perfomance Liquid Chromatography which is used as a method to analyze the ascorbic acid in injection solution of skin whitening product with brand “X”. The RP-HPLC system uses Phenomenex® C18 column and the dimension is 250 x 4.6 mm.
The size of the particle is 5 µm with methanol : 0.01 M phosphate buffer pH 3 as mobile phase. Optimization was done by varying the composition of mobile phase 10 : 90; 20 : 80; 30 : 70; 40 : 60; 50 : 50 and varying the flow rate of mobile phase 0.7; 0.8; 0.9; 1.0; 1.1 dan 1.2 mL/min using UV detector at 244 nm.
The analysis of the result was carried out by observing the tailing factor value, resolution value, coefficient of variation value, HETP, area under curve (AUC), peak height, and retention time of ascorbic acid.
The optimum condition of RP-HPLC which has been obtained is methanol : 0.01 M phosphate buffer pH 3 (40 : 60) as a mobile phase with flow rate 0.9 mL/min. These conditions have fulfilled the requirements of a good separation parameters which are 1.42 for tailing factor value and 3.03 for the retention time.Coefficient of variation (%CV) values which have been obtained from System Suitability Test (SST)for parameter of tailing factor, HETP, AUC, peak height, and retention time respectively were 0.36%, 0.47%, 0.05%, 0.23%, and 0.04%.
i
OPTIMASI KOMPOSISI DAN KECEPATAN ALIR FASE GERAK METODE KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK UNTUK PENETAPAN KADAR ASAM ASKORBAT DALAM
SEDIAAN LARUTAN INJEKSI OBAT PEMUTIH KULIT MERK “X”
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh:
Eunike Lystia Florentien Kelana Jeversoon NIM : 12814025
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
iv
HALAMAN PERSEMBAHAN
“Sometimes I just look up, smile and
say, I know that was You, God! For
You be glorified”
I am able to do all things through the one who
strengthens me - Philippians 4 : 13
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena atas
rahmat-Nya yang telah diberikan sehingga penulis mampu menyelesaikan skripsi
berjudul “Optimasi Komposisi dan Kecepatan Alir Fase Gerak Metode
Kromatografi Cair Kinerja Tinggi Fase Terbalik untuk Penetapan Kadar Asam
Askorbat dalam Sediaan Larutan Injeksi Obat Pemutih Kulit Merk “X” dengan
baik.
Dalam penyelesaian skripsi ini, tentu penulis memperoleh campur tangan
dari berbagai pihak. Pada kesempatan ini, penulis ingin mengucapkan terima
kasih kepada:
1. Aris Widayati, M.Si., Ph.D., Apt. dan Dr. Sri Hartati Yuliani, M.Si., Apt.
selaku Dekan dan Ketua Program Studi Fakultas Farmasi Universitas Sanata
Dharma.
2. Prof. Dr. Sudibyo Martono, M.S., Apt. selaku Dosen Pembimbing Utama
yang telah membimbing dan memberikan saran serta motivasi selama
penyusunan skripsi.
3. Florentinus Dika Octa Riswanto, M.Sc. selaku Dosen Pembimbing
Pendamping yang telah membimbing, dan memberikan saran serta motivasi
selama penyusunan skripsi.
4. Agustina Setiawati, M.Sc., Apt., selaku Kepala Penanggungjawab
Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam
viii
5. Mas Bimo dan Mas Kethul selaku laboran dan karyawan laboratorium
Fakultas Farmasi yang telah membantu penulis dalam proses pelaksanaan
penelitian di laboratorium.
6. Keluargaku tercinta papa, mama, cece Regi, Sammy, dan Ezra yang selalu
setia memberi semangat, perhatian, doa demi kelancaran studi dan
penyusunan naskah skripsi.
7. Teman-teman seperjuangan skripsi Petra Annie Anjani dan Rosalia Lestari
atas segala kerjasama, bantuan dan semangat dalam penyusunan skripsi ini
dari awal hingga akhir.
8. Jonathan Wijaya Setiawan, Sina Susanti, Ludwina Dearesthea Onevita,
Januaritha Dara Nastiandari, dan Prisca Nadya Verina Djala untuk
kesetiaannya menemani, menghibur, membantu penyelesaian skripsi ini dari
awal hingga akhir.
9. Teman-teman FSM-A 2012, FST-A 2012 dan seluruh angkatan 2012.
10. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan tugas akhir ini dengan baik.
Penulis berharap semoga tugas akhir ini dapat bermanfaat bagi semua pihak
terutama di bidang ilmu Farmasi.
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA . ... vi
D. Kromatografi Cair Kinerja Tinggi ... 15
E. Landasan Teori ... 25
F. Hipotesis ... 26
BAB III METODE PENELITIAN ... 27
A. Jenis dan Rancangan Penelitian ... 27
B. Variabel Penelitian ... 27
1. Variabel bebas ... 27
2. Variabel tergantung ... 27
3. Variabel pengacau terkendali ... 27
C. Definisi Operasional ... 28
4. Pembuatan larutan stok asam askorbat. ... 30
xi
6. Pembuatan larutan kerja asam askorbat yang digunakan untuk
optimasi komposisi dan kecepatan alir fase gerak ... 30
7. Penentuan panjang gelombang maksimum asam askorbat dengan spektrofotometer UV-Vis ... 31
8. Preparasi larutan sampel ... 31
9. Optimasi pemisahan asam askorbat dari matriks sampel dengan menggunakan metode KCKT fase terbalik ... 31
D. Penentuan Panjang Gelombang Maksimum Asam Askorbat Menggunakan Spektrofotometri UV-Vis ... 43
E. Optimasi Komposisi Fase Gerak ... 45
F. Optimasi Kecepatan Alir Fase Gerak ... 53
BAB V KESIMPULAN DAN SARAN ... 64
xii
B. Saran ... 64
DAFTAR PUSTAKA ... 65
xiii
DAFTAR TABEL
Halaman
Tabel I. Jenis bufer yang digunakan pada sistem KCKT fase terbalik ... 15
Tabel II. Indeks polaritas fase gerak campuran metanol : bufer fosfat 0,01 M
pH 3 ... 41
Tabel III. Waktu retensi, nilai tailing factor dan nilai resolusi baku asam
askorbat 100 µg/mL pada beberapa komposisi fase gerak pada
kecepatan alir 1 mL/menit ... 46
Tabel IV. Waktu retensi, nilai tailing factor dan nilai resolusi baku asam
askorbat 100 µg/mL pada komposisi metanol : bufer fosfat 0,01 M
pH 3 dengan perbandingan 40 : 60 pada beberapa kecepatan alir ... 54
Tabel V. Uji kesesuaian sistem asam askorbat konsentrasi 100 µg/mL
dengan fase gerak metanol : bufer fosfat 0,01 M pH 3 40 : 60 dan
kecepatan alir 0,9 mL/menit ... 62
Tabel VI. Uji kesesuaian sistem asam askorbat konsentrasi 100 µg/mL
dengan fase gerak metanol : bufer fosfat 0,01 M pH 3 40 : 60 dan
menggunakan fase gerak mengandung bufer fosfat dengan kecepatan alir 1 mL/menit ... 39
Gambar 8. Kromatogram asam askorbat konsentrasi 100 µg/mL menggunakan fase gerak metanol : bufer fosfat pH 5,6 dengan kecepatan alir 1 mL/menit ... 40
Gambar 9. Kromatogram asam askorbat konsentrasi 100 µg/mL menggunakan fase gerak metanol : bufer fosfat pH 3 dengan kecepatan alir 1 mL/menit ... 40
Gambar 10. Gugus kromofor dan auksokrom asam askorbat ... 44
Gambar 11. Spektra asam askorbat pada 3 seri konsentrasi ... 44
Gambar 12. Interaksi asam askorbat dengan fase diam oktadesilsilan ... 47
xvii
Gambar 25. Kromatogram sampel larutan injeksi obat pemutih kulit merk
“X” konsentrasi 100 µg/mL menggunakan komposisi fase
gerak metanol : bufer fosfat pH 3 dengan perbandingan 40 :
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Certificate of Analysis (CoA) baku asam askorbat. ... 68
Lampiran 2. Penimbangan asam askorbat ... 69
Lampiran 3. Perhitungan indeks polaritas fase gerak yang dioptimasi ... 69
Lampiran 4. Kromatogram asam askorbat pada Uji Kesesuaian Sistem
xix INTISARI
Asam askorbat merupakan salah satu agen pemutih kulit yang paling sering digunakan di masyarakat Indonesia. Kemampuannya melindungi kulit dari radiasi UV mampu mencegah pembentukan melanin pada kulit.
Penelitian ini bertujuan untuk menentukan kondisi optimal Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik sebagai metode yang digunakan dalam penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X”. Sistem KCKT fase terbalik menggunakan kolom Phenomenex® C18
dimensi 250 x 4,6 mm ukuran partikel 5µm dengan fase gerak metanol : 0,01 M bufer fosfat pH 3. Optimasi dilakukan dengan mengubah komposisi fase gerak yaitu 10 : 90; 20 : 80; 30 : 70; 40 : 60; 50 : 50 dan kecepatan alir fase gerak yaitu 0,7; 0,8; 0,9; 1,0; 1,1 dan 1,2 mL/menit menggunakan detektor ultraviolet pada panjang gelombang 244 nm.
Analisis hasil dilakukan dengan melakukan pengamatan terhadap nilai tailing factor, nilai resolusi, nilai koefisien variansi, HETP, area under curve (AUC), tinggi puncak dan waktu retensi asam askorbat hasil pemisahan.
Kondisi optimum sistem KCKT fase terbalik yang diperoleh adalah fase gerak metanol : 0,01 M bufer fosfat pH 3 (40:60) dengan kecepatan alir 0,9 mL/menit. Kondisi ini telah memenuhi parameter pemisahan yang baik yaitu nilai tailing factor 1,42 dan waktu retensi 3,03. Nilai koefisien variansi (% CV) yang diperoleh dari Uji Kesesuaian Sistem (UKS) untuk parameter tailing factor, HETP, AUC, tinggi puncak, dan waktu retensi secara berturut-turut adalah 0,36%, 0,47%, 0,05%, 0,23%, dan 0,04%.
xx ABSTRACT
Ascorbic acid is one of skin whitening agents which are most frequently used in Indonesia societies. Its ability to protect skin from UV radiation capables to inhibit the formation of melanin in human skin.
This study aims to determine the optimum conditions of Reversed-Phase High Perfomance Liquid Chromatography which is used as a method to analyze the ascorbic acid in injection solution of skin whitening product with brand “X”. The RP-HPLC system uses Phenomenex® C18 column and the dimension is 250 x
4.6 mm. The size of the particle is 5 µm with methanol : 0.01 M phosphate buffer pH 3 as mobile phase. Optimization was done by varying the composition of mobile phase 10 : 90; 20 : 80; 30 : 70; 40 : 60; 50 : 50 and varying the flow rate of mobile phase 0.7; 0.8; 0.9; 1.0; 1.1 dan 1.2 mL/min using UV detector at 244 nm.
The analysis of the result was carried out by observing the tailing factor value, resolution value, coefficient of variation value, HETP, area under curve (AUC), peak height, and retention time of ascorbic acid.
The optimum condition of RP-HPLC which has been obtained is methanol : 0.01 M phosphate buffer pH 3 (40 : 60) as a mobile phase with flow rate 0.9 mL/min. These conditions have fulfilled the requirements of a good separation parameters which are 1.42 for tailing factor value and 3.03 for the retention time. Coefficient of variation (%CV) values which have been obtained from System Suitability Test (SST) for parameter of tailing factor, HETP, AUC, peak height, and retention time respectively were 0.36%, 0.47%, 0.05%, 0.23%, and 0.04%.
1 BAB I
PENDAHULUAN
A. Latar Belakang
Produk pemutih kulit sudah menjadi salah satu produk yang paling banyak dicari oleh masyarakat saat ini. Beberapa penelitian menunjukkan 55%
dari 85% wanita Indonesia yang memiliki kulit gelap ingin memutihkan kulitnya (Saputri, 2011). Tujuan utama penggunaan produk pemutih kulit ini tidak lain
adalah untuk mencerahkan kulit, baik dengan meratakan warna kulit maupun merawat kulit sehingga terhindar dari masalah pigmentasi seperti bintik-bintik hitam, melasma, tanda bekas hamil dan keriput. Beberapa agen pemutih kulit yang
saat ini sering digunakan adalah arbutin, vitamin C (asam askorbat), kojic acid,
licorice extract, burner root extract, scutellaria extract, dan mulberry (Thongchai
dkk., 2007).
Peranan asam askorbat sebagai agen pemutih kulit adalah dengan menghambat pembentukan melanin dengan meminimalkan kemampuan radiasi
UV menginduksi sintesis melanin. Asam askorbat bertindak sebagai antioksidan dengan cara menetralkan radikal bebas yang terbentuk pada kompartemen air
dalam sel (Hwang dkk., 2009).
askorbat yang bereaksi secara reversibel dan asam dehidro askorbat dapat mengalami oksidasi lanjutan yang bereaksi secara ireversibel menjadi bentuk
yang tidak aktif, yaitu asam diketoglukonat. Reaksi oksidasi dapat diinduksi oleh paparan cahaya, peningkatan suhu, peningkatan pH, oksigen dan katalis logam (Novakova dkk., 2008). Sifat asam askorbat tersebut dapat mempengaruhi jumlah
asam askorbat dalam produk pemutih kulit.
Menurut Undang-Undang RI No. 8 tahun 1999 tentang Perlindungan
Konsumen, konsumen memiliki hak untuk memperoleh barang sesuai dengan yang kondisi atau jaminan yang telah dijanjikan dan pelaku usaha memiliki kewajiban untuk memberikan informasi terkait produk secara benar mengenai
kondisi barang dan menjamin mutu barang yang diproduksi atau diperdagangkan sehingga konsumen menerima barang yang sesuai dengan kondisi sebenarnya.
Jumlah asam askorbat yang tidak sesuai dengan yang tertera pada label dapat menurunkan efikasi produk pemutih kulit sehingga konsumen akan dirugikan. Menurut Farmakope Indonesia (1995), larutan injeksi asam askorbat yang dibuat
mengandung asam askorbat tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada label. Oleh karena itu, perlu dilakukan penetapan
kadar asam askorbat dalam produk pemutih kulit dengan bentuk sediaan larutan injeksi yang mengandung asam askorbat untuk menjamin efikasi produk.
Pengembangan metode dilakukan melalui tiga tahapan, yaitu : optimasi
metode, validasi metode dan aplikasi metode penetapan kadar (Suprianto, 2014). Sebelum melakukan penetapan kadar, perlu dilakukan tahapan optimasi pada
optimasi pada sistem Kromatografi Cair Kinerja Tinggi fase terbalik untuk mendapatkan kondisi yang optimal sehingga diperoleh hasil yang optimal yaitu
pemisahan yang baik pada senyawa asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X” yang akan ditetapkan kadarnya. Penggunaan metode KCKT fase terbalik menjadi pilihan utama dalam analisis asam askorbat
dikarenakan metode ini memiliki selektivitas yang lebih baik dibandingkan metode lainnya seperti titrasi dan spektrofotometri (Solichova dkk., 2008)
sehingga metode analisis yang dihasilkan dapat memberikan hasil pemisahan antara senyawa asam askorbat dengan produk degradasinya, yaitu asam dehidroaskorbat.
Penelitian mengenai asam askorbat dengan metode KCKT fase terbalik sudah pernah dilakukan oleh Ullah, A., Hussain, A., Ali, J., Khaliqurrehman and
Ullah, A. (2012) menggunakan panjang gelombang 300 nm, fase gerak campuran metanol dan bufer fosfat dengan perbandingan 20 : 80, pengaturan pH dilakukan
dengan penambahan meta phosporic acid mencapai pH 3 ± 0,1 dan kecepatan alir
fase gerak 1,0 mL/menit. Adanya perbedaan sistem KCKT melatarbelakangi perlunya dilakukan optimasi kondisi optimal suatu metode analisis agar diperoleh
pemisahan optimal asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X” sehingga dapat dilakukan analisis kualitatif dan analisis kuantitatif.
1. Rumusan masalah
Bagaimana komposisi dan kecepatan alir fase gerak yang dapat
memberikan pemisahan dengan bentuk puncak simetris, waktu retensi (tR), nilai
nilai koefisien variansi yang optimal untuk pemisahan asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X” dengan menggunakan metode
KCKT fase terbalik ? 2. Keaslian penelitian
Pengembangan dan validasi metode kuantifikasi asam askorbat dengan
menggunakan metode KCKT fase terbalik pernah dilakukan oleh Ullah, A.,
Hussain, A., Ali, J., Khaliqurrehman and Ullah, A. (2012) dengan judul “A Simple
and Rapid HPLC Method for Analysis of Vitamin-C in Local Packed Juices of
Pakistan”. Penelitian tersebut menggunakan kolom Inertsil ODS-3 C18 (250 mm x
4,6 mm), fase gerak campuran metanol : bufer fosfat dengan perbandingan
(20 : 80, v/v) pH 3 ± 0,1, dan kecepatan alir fase gerak 1,0 mL/menit untuk menganalisis asam askorbat dalam kemasan jus. Pengukuran dilakukan pada
panjang gelombang 300 nm.
Penelitian lain mengenai asam askorbat dilakukan oleh Wang, A., Cheng,
S., Sheu, C. And Kwan, C. (2011) dengan judul “Simultaneous Determination of
Five Whitening Agents by Ion-Pair Reversed-Phase High Perfomance Liquid
Chromatography”. Penelitian tersebut menggunakan kolom Inertsil ODS-3V (4,6
x 250 mm, 5µm), fase gerak campuran asetonitril : larutan bufer campuran
(50 mM natrium dihidrogen fosfat dan 2 mM n-heksadesiltrimetil amonium bromida) dengan elusi gradien komposisi asetoniril : larutan bufer campuran
1,0 mL/menit untuk menganalisis sediaan kosmetik lotion dan krim pemutih kulit. Pengukuran dilakukan pada panjang gelombang 270 nm.
Penelitian mengenai agen pemutih kulit juga dilakukan oleh Thongchai,
W., Liawruangrath, B. and Saisunee L. (2007) dengan judul “High-Perfomance
Liquid Chromatograpic Determination of Arbutin in Skin-Whitening Creams and
Medicinal Plant Extracts” menggunakan kolom ODS Hypersil® C18 (125 mm x 4
mm, 5 µm), fase gerak campuran air : metanol : 0,1 M hydrochloric acid (89 : 10 :
1, v/v), dan kecepatan alir fase gerak 1,0 mL/menit. Pengukuran dilakukan pada panjang gelombang 222 nm.
Sejauh penelitian penulis, analisis asam askorbat dalam sediaan larutan
injeksi obat pemutih kulit dengan menggunakan metode KCKT fase terbalik belum pernah dilakukan, sehingga dapat dilakukan optimasi sistem KCKT fase
terbalik untuk penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X”.
3. Manfaat penelitian
a. Manfaat teoritis. Memberikan sumbangan bagi ilmu pengetahuan tentang
pengembangan metode yang optimal dalam pemisahan dan penetapan kadar
asam askorbat.
b. Manfaat praktis. Memberikan informasi kondisi pemisahan asam askorbat
yang optimal untuk penetapan kadar asam askorbat dalam sampel produk
B. Tujuan
1. Tujuan umum
Mengetahui metode yang optimal dalam pemisahan dan penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih kulit merk “X” dengan metode KCKT fase terbalik.
2. Tujuan khusus
Mengetahui komposisi dan kecepatan alir fase gerak yang dapat
memberikan pemisahan dengan bentuk puncak, waktu retensi (tR), nilai resolusi
antara puncak asam askorbat dengan puncak terdekat senyawa lain, dan nilai koefisien variansi optimal pada hasil pemisahan asam askorbat dalam sediaan
7 BAB II
TINJAUAN PUSTAKA
A. Asam Askorbat
Asam askorbat (Gambar 1), secara kimia dikenal sebagai (2R)-2-[(1S)-1,2-dihidroksietil]-4,5-dihidroksifuran-3-on merupakan senyawa berbentuk kristal
tidak berwarna atau berbentuk serbuk kristal berwarna putih atau kuning pudar.
Asam askorbat dengan rumus kimia C6H8O6 memiliki berat molekul 176,1
g/mol, nilai pKa = 4,2; 11,6 (pada suhu 25°C), dan nilai log P (oktanol : air) 1,8. Kelarutan dalam air 1 : 3, dalam etanol 1 : 30, dalam metanol 1 : 10 dan dalam propilen glikol 1 : 20. Asam askorbat dapat larut dalam aseton, tidak larut dalam
benzena, kloroform, eter, petroleum eter, minyak, lemak, dan pelarut lemak (Moffat dkk., 2011). Asam askorbat bersifat fotosensitif dan mudah teroksidasi
(Ahuja dan Dong, 2005). Nilai asam askorbat adalah 556a pada pelarut asam,
λ 243 nm (Moffat dkk., 2011).
Gambar 1. Struktur Asam askorbat (Moffat dkk., 2011)
Asam askorbat merupakan salah satu agen pemutih kulit yang paling
sering digunakan (Thongchai dkk., 2007). Radiasi UV akan menstimulasi melanogenesis dengan mengaktivasi enzim tirosinase yang berperan sebagai oksidator dalam reaksi pembentukan melanin. Radiasi UV juga menginduksi
pembentukan reactive oxygen species (ROS). ROS berperan untuk memulai reaksi oksidasi selama proses pembentukan melanin. Asam askorbat menghambat
pembentukan melanin dengan meminimalkan kemampuan sinar UV menginduksi sintesis melanin. Asam askorbat bertindak sebagai antioksidan dengan cara menetralkan radikal bebas yang terbentuk pada kompartemen air dalam sel
(Hwang dkk., 2009). Dosis asam askorbat adalah 0,2-3 g per hari (Moffat dkk., 2011).
Larutan injeksi asam askorbat adalah larutan steril asam askorbat dalam air untuk injeksi yang dibuat dengan penambahan natrium hidroksida/natrium karbonat/natrium bikarbonat. Sediaan larutan injeksi asam askorbat mengandung
tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera pada label (Dirjen POM, 1995).
Asam askorbat bersifat mudah teroksidasi terutama dalam bentuk larutan. Degradasi asam askorbat dipengaruhi oleh beberapa faktor luar seperti paparan cahaya, oksigen, peningkatan suhu, peningkatan pH, dan katalis logam. Asam
askorbat mudah mengalami oksidasi menjadi bentuk asam dehidro askorbat yang bereaksi secara reversibel dan asam dehidro askorbat dapat mengalami oksidasi
Gambar 2. Reaksi degradasi asam askorbat (Sihite, 2010).
B. Spektrofotometer UV
1. Radiasi elektromagnetik dan penyerapan radiasi oleh molekul
Sinar ultraviolet merupakan salah satu jenis radiasi elektromagnetik yang memiliki suatu energi yang merambat dalam bentuk gelombang. Panjang
gelombang adalah jarak linier antara suatu titik pada satu gelombang dengan titik yang bersebelahan pada gelombang terdekatnya. Hubungan antara energi yang
dimiliki suatu radiasi elektromagnetik, frekuensi, dan panjang gelombang suatu senyawa dapat dilihat dari persamaan berikut:
λ
hc
E= (1)
Keterangan :
E = Energi radiasi cahaya
h = Tetapan planck (6,626 x 10-34 Joule) c = Kecepatan cahaya (2,998 x 1010 cm. s-1)
λ = panjang gelombang (Rohman dan Gandjar, 2007).
Suatu molekul bergerak dari tingkat energi yang lebih tinggi menuju tingkat energi yang lebih rendah dengan melepaskan suatu energi yang sering
elektromagnetik pada frekuensi yang sesuai sehingga menyebabkan energi molekul ditingkatkan ke level yang lebih tinggi, maka terjadi absorpsi energi oleh
molekul. Peristiwa absorpsi ini hanya dapat terjadi apabila terjadi kesetaraan antara perbedaan energi pada dua tingkat energi dengan jumlah energi foton yang diserap suatu molekul. Secara matematis, pernyataan tersebut dapat dinyatakan
dengan persamaan di bawah ini:
hυ
E
E2− 1= (2) Keterangan :
E1 = Energi pada tingkat yang lebih rendah E2 = Energi pada tingkat yang lebih tinggi
ʋ = frekuensi foton yang diabsorpsi (Rohman dan Gandjar, 2007).
Energi yang melompat dari suatu tingkat ke tingkat lain disebut transisi.
Transisi yang dimiliki oleh suatu molekul dengan struktur yang berbeda tidak sama sehingga spektra absorpsi dapat digunakan untuk analisis kualitatif.
Absrobansi suatu senyawa pada panjang gelombang tertentu sebanding dengan banyaknya molekul yang menyerap radiasi, sehingga spektra absorpsi juga dapat digunakan untuk analisis kuantitatif. Senyawa analit menjerap radiasi
elektromagnetik di daerah panjang gelombang UV-Vis yang mengakibatkan tereksitasinya elektron ketingkat energi yang lebih tinggi (Gambar 3). Elektron
Gambar 3. Skema eksitasi elekron (Rohman dan Gandjar, 2007)
Molekul-molekul yang memerlukan energi yang lebih banyak untuk
mengeksitasikan elektron maka akan menyerap panjang gelombang yang lebih pendek, sedangkan untuk molekul-molekul yang memerlukan energi yang lebih sedikit untuk mengeksitasikan elektron maka akan menyerap pada panjang
gelombang yang lebih panjang (Fessenden and Fessenden, 1997). Jumlah energi yang diserap oleh molekul-molekul disebut absorban. Hukum Lambert-Beer
menunjukkan bahwa absorbansi suatu senyawa dipengaruhi oleh absorptivitas molar, tebal kuvet dan konsentrasi molekul dalam senyawa analit (Rohman dan Gandjar, 2007). Hukum Lambert-Beer dapat dilihat melalui persamaan di bawah
ini:
A = ɛ b c (3)
Keterangan : A = absorban
ɛ = absorptivitas molar (M-1. cm-1) b = tebal kuvet (cm)
c = konsentrasi molekul dalam senyawa analit (Rohman dan Gandjar, 2007).
sampel, tetapi tergantung pada suhu, pelarut, struktur molekul, dan panjang gelombang radiasi. Dikatakan sebagai absorptivitas molar apabila konsentrasi
molekul zat analit dalam satuan Molar (M). Jika konsentrasi molekul zat analit berada dalam satuan persen berat/volume (g/100 mL), maka absorptivitas dapat
ditulis dengan 1%
1cm
E (Rohman dan Gandjar, 2007). Hubungan antara 1%
1cm
E dengan
absorptivitas molar (ɛ) dapat dilihat pada persamaan di bawah ini:
10
E = absorptivitas molekul dalam satuan konsentrasi (g/100 mL)
BM = bobot molekul (g/mol) (Rohman dan Gandjar, 2007).
Nilai 1%
1cm
E memberikan manfaat untuk mengetahui berapa besar
konsentrasi senyawa asam askorbat yang harus dipersiapkan sehingga diperoleh
absorbansi pada kisaran 0,2-0,8. Selain itu, manfaat dari informasi nilai E1%1cm
adalah terkait dengan sensitivitas senyawa untuk diukur dengan spektrofotometer
UV-Vis. Semakin besar nilai 1%
1cm
E suatu senyawa maka semakin sensitif senyawa
tersebut untuk dideteksi dan diukur dengan spektrofotometer UV-Vis. Nilai
asam askorbat adalah 556a pada pelarut asam, λ 243 nm (Moffat dkk., 2011).
Nilai tersebut dapat menunjukkan bahwa senyawa asam askorbat cukup sensitif dan dapat dideteksi dengan spektrofotometer UV-Vis. Nilai absorbtivitas molar
asam askorbat adalah 9791,15 M-1. cm-1. Nilai tersebut menunjukkan bahwa asam
yang memiliki rentang panjang gelombang antara 200-700 nm (Rohman dan Gandjar, 2007).
2. Gugus yang mempengaruhi penyerapan radiasi elektromagnetik
Gugus kromofor merupakan suatu gugus atau atom dalam suatu senyawa organik yang mampu menyerap radiasi sinar UV. Disamping itu, dalam suatu
molekul organik terdapat suatu gugus auksokrom yang merupakan suatu gugus
fungsional yang memiliki elektron bebas, seperti: -OH, -NH2, dan -OCH3.
Terikatnya gugus auksokrom pada gugus kromofor mampu menggeser pita absorpsi sehingga panjang gelombang yang dihasilkan akan lebih besar.
Ikatan terkonjugasi adalah ikatan rangkap yang berselang-seling dengan
ikatan tunggal dalam suatu struktur molekul senyawa. Adanya ikatan terkonjugasi dalam senyawa akan mempengaruhi panjang gelombang maksimalnya. Semakin
panjang ikatan terkonjugasinya, maka akan semakin besar panjang gelombang maksimalnya (Rohman dan Gandjar, 2007).
C. Larutan Bufer
Larutan bufer sering dipakai dalam analisis seperti penggunaanya sebagai
fase gerak dalam sistem KCKT. Jenis bufer paling sederhana terdiri atas suatu asam atau basa lemah yang dikombinasikan dengan suatu asam atau basa konjugatnya (Rohman dan Gandjar, 2007).
Larutan bufer (bufer) memiliki peranan penting dalam pemisahan senyawa asam ataupun basa dalam sistem KCKT. Penggunaan bufer dalam fase gerak
waktu retensi senyawa selama proses pemisahan menjadi lebih reprodusibel. Faktor-faktor yang perlu diperhatikan dalam penggunaan larutan bufer pada fase
gerak sistem KCKT fase terbalik adalah nilai pKa asam lemah atau basa lemah, kapasitas bufer, kelarutan komponen bufer, absorbansi pada daerah UV, dan stabilitas bufer (Snyder dkk., 2010).
Kapasitas bufer adalah kemampuan bufer untuk mempertahankan pH dan tergantung pada nilai pKa asam lemah atau basa lemah, konsentrasi bufer, dan pH
fase gerak. Asam lemah atau basa lemah yang menyusun bufer hendaknya memiliki nilai pKa dalam rentang ±1,0 unit dari pH fase gerak yang diinginkan (Snyder dkk., 2010).
Dalam sistem KCKT dengan detektor UV, penggunaan bufer dapat dikatakan ideal apabila memiliki absorban pada panjang gelombang di bawah
Tabel I. Jenis bufer yang digunakan pada sistem KCKT fase terbalik (Kazakevich and Lobrutto, 2007)
D. Kromatografi Cair Kinerja Tinggi
1. Definisi dan instrumen KCKT
Kromatografi cair kinerja tinggi adalah salah satu metode analisis untuk pemisahan suatu campuran senyawa kimia. Penggunaan pompa bertekanan tinggi
akan mengalirkan fase gerak ke dalam kolom sehingga akan terjadi pemisahan dengan cepat, terkontrol dan efektif. Baik buruknya pemisahan dipengaruhi oleh kondisi eksperimental seperti kondisi kolom, kemurnian pelarut, suhu, kecepatan
analit dengan fase diam dan fase gerak yang kemudian akan menghasilkan perbedaan waktu migrasi dari zat analit (Kazakevich and Lobrutto, 2007).
Ada dua macam jenis kromatografi cair kinerja tinggi dalam analisis, yaitu KCKT fase normal dan KCKT fase terbalik. KCKT fase normal adalah KCKT yang menggunakan fase diam bersifat lebih polar dibandingkan dengan
fase geraknya, sedangkan KCKT fase terbalik adalah KCKT yang menggunakan fase diam bersifat lebih non-polar dibandingkan dengan fase geraknya (Snyder
dkk., 2010).
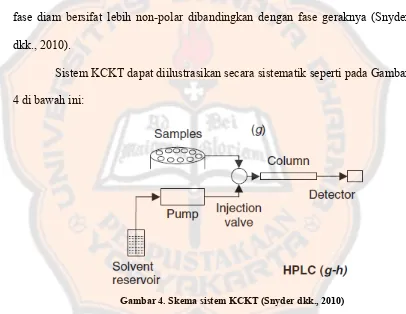
Sistem KCKT dapat diilustrasikan secara sistematik seperti pada Gambar 4 di bawah ini:
Gambar 4. Skema sistem KCKT (Snyder dkk., 2010)
Bagian-bagian dalam sistem KCKT fase terbalik, antara lain:
a) Kolom
Salah satu jenis kolom KCKT fase terbalik yang paling sering digunakan
adalah kolom tipe C18. Kolom C18 (Gambar 5) tersusun oleh suatu penyangga
silika gel (SiO2) dimana silika gel tersusun atas rantai -O-Si-O- dan pada bagian
relatif bersifat polar. Pada KCKT fase terbalik, modifikasi silika gel dilakukan dengan menutup gugus silanol (-SiOH) dengan suatu bagian organik yang
umumnya adalah suatu hidrokarbon rantai panjang untuk menghilangkan gugus hidroksil melalui reaksi silanisasi. Semakin panjang rantai karbon yang diikatkan pada silika maka akan semakin hidrofobik. Kebanyakan fase diam dengan
penyusun silika memiliki rentang pH yang dapat ditoleransi, yaitu pH 2-7. Apabila di bawah pH 2, maka akan terjadi hidrolisis yang menyebabkan
terjadinya pemutusan ikatan fase terikat dengan substrat silika. Apabila di atas pH 7, maka substrat silika akan terdisolusi sebagian dalam fase gerak yang polar. Salah satu dampak yang terlihat adalah terbentuknya puncak yang asimetris pada
pH di atas 3 akibat adanya interaksi antara bentuk ion zat analit dengan residu silanol (Kazakevich and Lobrutto, 2007).
Gambar 5. Struktur kolom C18 (Snyder dkk., 2010))
b) Fase gerak
Fase gerak atau eluen tersusun atas campuran pelarut yang saling bercampur yang secara keseluruhan berperan dalam elusi zat analit dan resolusi
dalam sistem KCKT. Daya elusi dan resolusi dipengaruhi oleh polaritas fase gerak, polaritas fase diam, dan sifat komponen analit. Pada sistem KCKT fase
Hal-hal yang perlu dipertimbangkan dalam pemilihan fase gerak adalah kompatibilitas pelarut yang digunakan, kelarutan analit dalam fase gerak, polaritas
fase gerak, transmisi cahaya, viskositas, stabilitas dan pH fase gerak (Kazakevich and Lobrutto, 2007).
Kompatibilitas antar komponen fase gerak perlu diperhatikan supaya
penyusun fase gerak dapat bercampur dengan baik. Campuran fase gerak harus dapat digunakan untuk melarutkan analit dengan baik. Apabila analit tidak terlarut
sempurna pada fase gerak yang digunakan, maka analit akan mengendap ketika proses penginjekan dilakukan. Hal lain yang perlu diperhatikan adalah transmisi cahaya dari fase gerak. Transmisi cahaya akan berkaitan erat dengan detektor UV
yang digunakan. Setiap fase gerak memiliki UV-cutoff yang berbeda satu sama
lain sehingga perlu diperhatikan ketika memilih komponen fase gerak. Perlu
dipastikan bahwa UV-cutoff pelarut fase gerak yang digunakan tidak mengganggu
deteksi analit pada detektor UV. Viskositas fase gerak perlu diperhatikan pula karena semakin besar viskosias fase gerak makan akan semakin besar tekanan
dalam kolom sistem KCKT (Kazakevich and Lobrutto, 2007).
Tingkat kepolaran fase gerak yang digunakan akan mempengaruhi elusi
analit dalam sistem KCKT. Kepolaran campuran komponen penyusun fase gerak dapat dilihat dari nilai indeks polaritasnya. Indeks polaritas fase gerak dapat dihitung dengan menggunakan persamaan di bawah ini:
n
P’camp = indeks polaritas campuran P’n = indeks polaritas pelarut ke-n
Indeks polaritas menunjukkan korelasinya dengan kepolaran suatu pelarut fase gerak. Semakin besar nilai indeks polaritasnya maka semakin polar
pelarut fase gerak yang digunakan (Snyder dkk., 2010).
Sebagian besar senyawa obat yang berada di pasaran dapat terionisasi pada pH tertentu, sehingga diperlukan pengaturan pH pada fase gerak untuk
mempertahankan kondisi pH fase gerak yang membawa analit agar analit tetap dalam bentuk molekulnya sampai detektor. Pengaturan pH dapat dilakukan
dengan penggunaan larutan bufer dalam komponen penyusun fase gerak. Hal yang perlu diperhatikan ketika menggunakan bufer adalah tingkat kelarutan bufer dalam pelarut yang digunakan karena pemilihan jenis bufer yang salah akan
mengakibatkan mengendap atau terpisahnya komponen bufer dalam fase gerak (Kazakevich and Lobrutto, 2007).
c) Detektor
Detektor yang digunakan untuk KCKT dapat digolongkan menjadi dua golongan, yaitu golongan detektor universal dan golongan detektor spesifik
mendeteksi analit secara spesifik dan selektif. Detektor UV merupakan salah satu jenis detektor spesifik yang hanya akan mendeteksi analit secara spesifik dan
selektif sesuai panjang gelombang yang digunakan. Dasar detektor UV adalah penyerapan radiasi UV pada kisaran panjang gelombang 200-400 nm oleh analit yang memiliki gugus kromofor pada strukturnya. Beberapa karakteristik detektor
berbanding lurus dengan konsentrasi analit dalam sampel (Rohman dan Gandjar, 2007).
2. Pemisahan yang optimal pada sistem KCKT
a. Bentuk puncak pemisahan asam askorbat. Bentuk puncak yang
diharapkan adalah simetris. Parameter bentuk puncak adalah asymmetry
factor (As) dan tailing factor (Tf). Nilai asymmetry factior (As) dihitung
pada 10% tinggi puncak. Perhitungan As dapat dilakukan dengan
persamaan yang tercantum pada Gambar 5. Apabila nilai As = 1, maka
dapat dikatakan puncak yang dihasilkan simetri. Akan tetapi, pada nilai
As < 2 puncak juga masih dikatakan baik (Snyder dkk., 2010). Tailing
factor (Tf) merupakan rasio antara lebar setengah tinggi puncak. Nilai
Tf = 1 menunjukkan bahwa puncak simetris, sedangkan nilai Tf ˃ 1
menunjukkan bahwa puncak mengalami tailing. Semakin besar nilai Tf
maka efisiensi kolom semakin menurun. Tailing factor (Tf) dapat
dihitung melalui persamaan yang tercantum pada Gambar 6 berikut:
Gambar 6. Perhitungan nilai As dan nilai Tf (Snyder dkk., 2010)
Pada saat migrasi, analit mengalami transfer antara fase diam atau fase
maka migrasi dalam kolom menjadi tidak teratur. Akibatnya, laju rata-rata analit relatif terhadap fase gerak sangat bervariasi dan menyebabkan pelebaran puncak
analit.
Berdasarkan teori laju, pelebaran puncak analit disebabkan oleh 3 faktor yang dapat diuraikan sebagai berikut:
1) Difusi Eddy
Difusi Eddy merupakan aliran tidak teratur yang menyebabkan terjadinya
pencampuran konvektif. Hal ini disebabkan oleh perbedaan jarak yang harus dilalui molekul yang satu dengan yang lain. Perbedaan jarak yang dilalui oleh molekul yang satu dengan yang lain disebabkan oleh perbedaan bentuk, ukuran
partikel pengisi kolom, cara pengisian kolom, dan diameter kolom. Perbedaan tersebut mengakibatkan perbedaan waktu elusi molekul-molekul dari kolom.
Suatu molekul solut dapat bergerak melalui kolom dekat dinding kolom yang memiliki kerapatan kemas partikel fase diam yang rendah, sehingga molekul tersebut dengan cepat akan terelusi. Berbeda dengan molekul solut yang melalui
bagian tengah kolom yang memiliki kerapatan kemas partikel fase diam yang tinggi, solut akan terelusi dengan kecepatan yang lebih rendah. Hal inilah yang
menyebabkan pelebaran puncak untuk tiap analit. Cara memperkecil efek ini adalah menggunakan fase diam yang memiliki partikel berdiameter kecil, diameter kolom kecil, pengemasan kolom yang rapat dan homogen (Rohman dan
2) Difusi longitudinal
Analit ketika berada dalam fase gerak melewati fase diam menyebar ke
segala arah secara difusi, baik dengan arah yang sama maupun berlawanan dengan aliran fase gerak sehingga akan menghasilkan bentuk puncak yang melebar simetris. Difusi longitudinal merupakan efek dari gerakan random molekul analit
dalam fase gerak karena adanya perbedaan konsentrasi. Ketika melintasi kolom, molekul-molekul akan berdifusi menyebar ke segala arah. Difusi ini dapat terjadi
di sepanjang kolom, baik pada fase gerak maupun fase diam. Akibatnya bentuk puncak analit yang semula sempit, dengan adanya difusi ke dalam fase gerak di sekelilingnya, akan melebarkan profil puncak. Efek ini dapat diperkecil dengan
menggunakan fase gerak yang bobot jenisnya lebih tinggi dengan kecepatan linier aliran ditingkatkan (Rohman dan Gandjar, 2007).
3) Transfer massa
Pengaruh transfer massa ini terjadi antara fase diam dengan fase gerak. Proses transfer massa tidak terjadi secara instan melainkan terjadi secara lambat
dalam hal kinetikanya. Fase gerak mengalir secara terus menerus mengakibatkan distribusi kesetimbangan analit dalam fase diam dan fase gerak tidak pernah ada.
Beberapa penyebab terjadinya puncak asimetris antara lain:
1) Konsentrasi analit terlalu besar yang membuat fase gerak tidak mampu
membawa analit dengan sempurna sehingga akan terbentuk tailing pada
puncak yang dihasilkan.
2) Adanya interaksi yang kuat antara analit dengan fase diam sehingga analit
sulit terelusi dari kolom dan membuat terbentuknya tailing pada puncak.
3) Terdapat kontaminan dalam sampel sehingga akan muncul suatu puncak
didepan puncak analit yang membuat terbentuknya fronting pada puncak
(Rohman dan Gandjar, 2007).
b. Waktu retensi (tR). Waktu retensi merupakan waktu yang dibutuhkan suatu
analit untuk melewati kolom. Waktu retensi (tR) dan faktor retensi (k’)
dihubungkan dengan persamaan:
tR = tM (l + k’) (6)
tM merupakan waktu yang dibutuhkan analit yang tidak tertahan
untuk melewati kolom. Analit yang tidak tertahan akan bermigrasi melewati
kolom dengan kecepatan yang sama dengan kecepatan fase gerak, sehingga
nilai faktor retensinya adalah nol (tR = tM). Analit yang mempunyai nilai
k’ > 0 akan tertahan secara proporsional dan menghasilkan waktu retensi
yang lebih besar daripada tM (Gandjar dan Rohman, 2007).
c. Resolusi (Rs). Resolusi adalah indikator pemisahan dua puncak yang
berdekatan. Pemisahan yang baik adalah pemisahan yang menghasilkan nilai
Rs≥ 1,5. Hubungan antara waktu retensi analit (tR) dengan lebar puncak (W)
0,5(W W)
jumlah lempeng (N) yang didasarkan pada konsep lempeng teoritis. Efisiensi kolom akan berpengaruh pada waktu retensi analit. Semakin tinggi jumlah lempeng teoritis maka semakin baik pula efisiensi kolom (Snyder dkk.,
2010).
Nilai Height Equivalent Theoritical Plate (HETP) merupakan tolok
ukur efisiensi kolom, dimana HETP dapat dihitung melalui persamaan berikut:
W = lebar puncak pada posisi setengah tinggi puncak
Nilai HETP berbanding terbalik dengan jumlah lempeng teoritis (N). Dengan begitu, semakin tinggi nilai N makan semakin kecil nilai HETP dan
E. Landasan Teori
Asam askorbat merupakan salah satu senyawa yang digunakan sebagai
agen pemutih kulit. Jumlah asam askorbat dalam produk pemutih kulit perlu untuk dipastikan kebenarannya dengan klaim label agar konsumen tidak dirugikan. Sifat asam askorbat yang mudah terdegradasi oleh paparan cahaya, peningkatan suhu,
peningkatan pH, oksigen dan katalis logam merupakan salah satu penyebab ketidaksesuaian jumlah asam askorbat dalam produk dengan klaim label. Dalam
penelitian ini, asam askorbat yang akan diteliti berada dalam sampel larutan injeksi obat pemutih kulit.
KCKT dapat digunakan untuk melakukan pemisahan asam askorbat dari
sampel larutan injeksi obat pemutih kulit. Pemisahan yang dilakukan dengan KCKT merupakan pemisahan yang berdasarkan tingkat kepolaran dan interaksi
analit dengan fase gerak dan fase diam pada metode KCKT ini. Analit yang sudah dipisahkan dengan KCKT akan dideteksi oleh detektor UV karena asam askorbat memberikan absorban pada panjang gelombang UV. Asam askorbat memiliki
gugus kromofor dan auksokrom pada struktur sebagai syarat senyawa yang dapat
dideteksi dengan detektor UV. Nilai 1%
1cm
E asam askorbat adalah 556a pada pelarut
asam, λ 243 nm. Nilai tersebut menunjukkan bahwa senyawa asam askorbat
cukup sensitif dan dapat dideteksi dengan detektor UV. Nilai absorbtivitas molar
asam askorbat adalah 9791,15 M-1. cm-1. Nilai tersebut menunjukkan bahwa asam
askorbat akan mengalami transisi π→π*. Jenis transisi ini merupakan transisi
yang cocok untuk analisis pada rentang panjang gelombang antara 200-400 nm
Sistem KCKT fase terbalik yang optimal diperlukan untuk melakukan penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih kulit,
sehingga di penelitian ini dilakukan optimasi sistem KCKT fase terbalik untuk mendapatkan metode KCKT fase terbalik yang mampu memisahkan asam askorbat dari matriks sampel secara optimal. Variabel yang akan dioptimasi dalam
penelitian ini adalah komposisi dan kecepatan alir fase gerak. Variasi perbandingan fase gerak dan kecepatan alir fase gerak dilakukan untuk melihat
perbandingan berapa yang akan memberikan pemisahan optimal. Parameter optimasi yang harus dipenuhi adalah bentuk puncak, nilai resolusi antara puncak asam askorbat dengan puncak terdekat senyawa lain, nilai koefisien variansi dari
nilai resolusi antara puncak asam askorbat dengan puncak terdekat senyawa lain, tailing factor, HETP, area under curve (AUC) dan waktu retensi asam askorbat.
F. Hipotesis
Metode KCKT fase terbalik detektor UV dengan komposisi dan
kecepatan alir fase gerak yang optimal dapat memberikan pemisahan dengan
bentuk puncak simetris yaitu nilai tailing factor < 2, waktu retensi (tR) kurang dari
10 menit, nilai resolusi antara puncak asam askorbat dengan puncak terdekat
senyawa lain > 1,5, dan nilai koefisien variansi ≤ 2% sehingga dapat digunakan
untuk penetapan kadar asam askorbat dalam sediaan larutan injeksi obat pemutih
27 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan ini merupakan jenis rancangan penelitian eksperimental analitik karena pada subjek uji diberikan perlakuan yaitu komposisi
dan kecepatan alir fase gerak.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah perbandingan komposisi fase
gerak yaitu metanol : 0,01 M bufer fosfat pH 3 dan kecepatan alir fase gerak yang digunakan.
2. Variabel tergantung
Variabel tergantung pada penelitian ini adalah pemisahan puncak dari
asam askorbat dari matriks sampel yang terlihat dari asymmetry factor, tailing
factor, nilai resolusi antara puncak asam askorbat dengan puncak terdekat
senyawa lain, nilai koefisien variansi, HETP, area under curve (AUC) dan waktu
retensi asam askorbat hasil pemisahan. 3. Variabel pengacau terkendali
a. Kemurnian pelarut yang digunakan, untuk mengatasinya digunakan
b. Kemurnian bahan baku yang digunakan, untuk mengatasinya digunakan
bahan baku yang telah terjamin kualitasnya dengan adanya Certificate of
Analysis (CoA).
C. Definisi Operasional
1. Asam askorbat merupakan salah satu agen pemutih kulit yang terdapat dalam
sediaan larutan injeksi obat pemutih kulit merk “X”.
2. Sistem KCKT fase terbalik yang digunakan adalah seperangkat alat KCKT
menggunakan jenis kolom C18 merek Phenomenex® (250 x 4,6 mm, ukuran
partikel 5 µm), dengan fase gerak campuran metanol : 0,01 M bufer fosfat
pH 3
3. Optimasi dilakukan dengan mengubah komposisi fase gerak dan kecepatan
alir fase gerak.
4. Parameter optimasi dengan menggunakan metode KCKT adalah bentuk
puncak, waktu retensi, nilai resolusi antara puncak asam askorbat dengan
puncak terdekat senyawa lainnya dan reprodusibilitas luas area dan waktu retensi.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah reference standard
asam askorbat (Supelco), metanol grade HPLC, asam fosfat 85% dan kalium
Whatman 0,45µm, dan produk pemutih kulit merk “X” yang diperoleh dari online
shop “Y”.
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah seperangkat alat KCKT
dengan detektor ultraviolet, Shimadzu LC-2010C, kolom C18 merek
Phenomenex® (dimensi 250 x 4,6 mm, ukuran partikel 5 µm), seperangkat
komputer (merek Dell B6RDZ1S Connexant system RD01-D850 A03-0382 JP
France S.A.S, printer HP Deskjet D2566 HP-024-000 625730), UV-Vis
Spechtrophotometer SP-3000plus merek OPTIMA dengan detektor silicon photo
diode, milipore, ultrasonikator Refsch, Tipe : T460 (Schwing 1 PXE, FTZ-Nr.
C-066/83, HF-Frequ:35 kHz), timbangan analitik SCALTEC (max 60/210 g, min
0,001 g), alat vakum GAST, dan seperangkat alat gelas yang lazim digunakan di laboratorium analisis.
F. Tata Cara Penelitian
1. Pembuatan asam fosfat 0,1 M
Larutan pekat H3PO4 dengan konsentrasi 85% diambil sejumlah 0,3 mL,
kemudian diencerkan dalam akua demineralisata 25,0 mL sehingga konsentrasi
H3PO4 menjadi 0,1 M.
2. Pembuatan bufer fosfat 0,01 M
Sejumlah 0,68 g KH2PO4 ditimbang seksama dan dilarutkan dalam akua
3. Pembuatan fase gerak
Fase gerak dibuat dengan mencampur antara metanol dan 0,01 M bufer
fosfat pH 3 dengan perbandingan 10 : 90; 20 : 80; 30 : 70; 40 : 60; dan 50 : 50 oleh sistem KCKT. Sebelumnya masing-masing fase gerak tersebut disaring
dengan penyaring Whatman 0,45 µm yang dibantu dengan pompa vakum
kemudian didegassing selama 15 menit menggunakan ultrasonicator.
4. Pembuatan larutan stok asam askorbat
Sejumlah 4,0 mg asam askorbat ditimbang seksama dan dilarutkan dalam
fase gerak hingga 10,0 mL sehingga konsentrasi menjadi 400 µg/mL.
5. Pembuatan larutan baku asam askorbat yang digunakan untuk
penentuan panjang gelombang maksimum
Dibuat larutan seri dengan 3 konsentrasi berbeda yaitu 40; 50; dan 60
µg/mL dengan mengencerkan 1,0; 1,25; dan 1,5 mL larutan stok menggunakan
fase gerak hingga 10,0 mL.
6. Pembuatan larutan kerja asam askorbat yang digunakan untuk optimasi
komposisi dan kecepatan alir fase gerak
Sejumlah 2,5 mL larutan stok asam askorbat dengan konsentrasi
400 µg/mL diambil dan diencerkan dalam fase gerak 10,0 mL sehingga diperoleh
konsentrasi larutan 100 µg/mL. Larutan disaring dengan menggunakan milipore
7. Penentuan panjang gelombang maksimum asam askorbat dengan
spektrofotometer UV-Vis
Masing-masing konsentrasi larutan seri baku asam askorbat 40; 50; dan
60 µg/mL dengan pelarut fase gerak, discan antara panjang gelombang 200-400
nm dengan spektrofotometer UV-Vis. Spektrum yang dihasilkan akan
menunjukkan panjang gelombang maksimum yang akan digunakan untuk deteksi pada sistem KCKT yaitu panjang gelombang yang menghasilkan absorbansi
maksimum dari ketiga konsentrasi tersebut. 8. Preparasi larutan sampel
Sediaan larutan injeksi obat pemutih kulit merk “X” yang mengandung
200 mg/mL asam askorbat (klaim label), diambil sejumlah 50 µL dan dimasukkan
ke dalam labu takar 10 mL, diencerkan dengan fase gerak sampai tanda batas
sehingga diperoleh larutan stok sampel yang memiliki konsentrasi asam askorbat
1000 µg/mL. Kemudian diambil sejumlah 2,0 mL larutan stok sampel dan
dimasukkan ke dalam labu takar 10 mL, diencerkan dengan fase gerak sampai
tanda batas sehingga diperoleh larutan sampel yang memiliki konsentrasi asam
askorbat 100 µg/mL. Larutan sampel disaring dengan menggunakan milipore dan
didegassing dengan ultrasonicator selama 15 menit.
9. Optimasi pemisahan asam askorbat dari matriks sampel dengan
menggunakan metode KCKT fase terbalik
a. Optimasi komposisi fase gerak. Larutan kerja asam askorbat dengan
konsentrasi 100 µg/mL diinjeksikan sejumlah 20 µL ke sistem KCKT.
menggunakan fase gerak metanol : 0,01 M bufer fosfat pH 3 dengan perbandingan 10 : 90; 20 : 80; 30 : 70; 40 : 60; dan 50 : 50 pada
kecepatan alir fase gerak 1,0 mL/menit. Dilakukan analisis hasil terhadap parameter nilai resolusi antara puncak asam askorbat dengan puncak
terdekat senyawa lain, waktu retensi dan nilai tailing factor dari berbagai
perbandingan fase gerak.
b. Optimasi kecepatan alir fase gerak. Larutan kerja asam askorbat dengan
konsentrasi 100 µg/mL diinjeksikan sejumlah 20 µL ke sistem KCKT.
Optimasi dilakukan pada panjang gelombang maksimum dengan menggunakan fase gerak metanol : 0,01 M bufer fosfat pH 3 dengan
perbandingan hasil optimasi pada kecepatan alir fase gerak 0,7; 0,8; 0,9; 1,0; 1,1; dan 1,2 mL/menit. Dilakukan analisis hasil terhadap parameter
nilai resolusi antara puncak asam askorbat dengan puncak terdekat
senyawa lain, waktu retensi dan nilai tailing factor dari berbagai
kecepatan alir fase gerak.
c. Pemisahan asam askorbat dari matriks larutan sampel dengan fase gerak
hasil optimasi. Larutan sampel dengan konsentrasi 100 µg/mL
diinjeksikan sejumlah 20 µL ke sistem KCKT. Pengamatan dilakukan
menggunakan komposisi dan kecepatan alir fase gerak hasil optimasi serta pada panjang gelombang maksimum yang telah ditentukan.
Kromatogram yang dihasilkan diamati dan dihitung parameter uji kesesuaian sistem yang meliputi nilai resolusi antara puncak asam
N dan HETP dari pemisahan asam askorbat dari matriks pada larutan sampel.
d. Uji kesesuaian sistem KCKT. Larutan baku asam askorbat dengan
konsentrasi 100 µg/mL diinjeksikan sebanyak 20 µL ke sistem KCKT
menggunakan fase gerak dan kecepatan alir fase gerak hasil optimasi.
Penginjekan larutan ini dilakukan sebanyak 6 kali. Pengamatan dilakukan pada panjang gelombang maksimum dan kemudian diamati kromatogram
asam askorbat hasil pemisahan dan dihitung nilai resolusi antara puncak asam askorbat dengan puncak terdekat senyawa lain, waktu retensi, nilai
k’, nilai tailing factor, area under curve (AUC), tinggi puncak, nilai N
dan HETP, serta % koefisien variansi pada masing-masing parameter tersebut.
G. Analisis Hasil
Hasil optimasi komposisi fase gerak dan kecepatan alir fase gerak
tertentu menghasilkan data kromatogram. Pemisahan asam askorbat dari matriks sampel paling baik dapat diketahui dengan melihat baik data kromatogram baku
maupun kromatogram sampel dan melakukan pengamatan terhadap nilai resolusi antara puncak asam askorbat dengan puncak terdekat senyawa lain, waktu retensi,
nilai k’, nilai tailing factor, AUC, tinggi puncak, nilai N dan HETP, serta
Pemisahan yang baik adalah pemisahan yang menghasilkan bentuk
puncak simetris, waktu retensi < 10 menit, memiliki nilai resolusi ≥ 1,5 terhadap
puncak terdekat, dan nilai koefisien variansi (% CV) ≤ 2% (Snyder dkk., 2010).
1. Bentuk puncak pemisahan asam askorbat
Bentuk puncak yang diharapkan adalah simetris. Parameternya adalah
asymmetry factor (As) dan tailing factor (Tf). Nilai asymmetry factior (As)
dikatakan baik (Snyder dkk., 2010).
2. Waktu retensi (tR)
Pengamatan waktu retensi dilakukan untuk melihat waktu yang dibutuhkan suatu senyawa berpisah dengan optimal dalam suatu campuran.
Apabila waktu yang didapatkan kurang dari 10 menit, maka dapat dikatakan waktu pemisahan efektif (Snyder dkk., 2010).
3. Nilai resolusi (Rs)
Pemisahan yang baik adalah pemisahan yang menghasilkan nilai resolusi
sebesar ≥1,5 (Rohman dan Gandjar, 2007).
4. Nilai HETP
Nilai HETP dapat dihitung melalui persamaan berikut:
N L
HETP=
Dimana : L = panjang kolom N = jumlah lempeng
dimana nilai N merupakan bilangan lempeng teoritik dan dapat dihitung dengan persamaan berikut:
W = lebar puncak pada posisi setengah tinggi puncak
Apabila nilai HETP semakin kecil, maka efisiensi kolom akan semakin baik dan pemisahan juga semakin baik.
36 BAB IV
HASIL DAN PEMBAHASAN
A. Pemilihan Pelarut
Pemilihan pelarut dalam analisis menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT) menjadi penting karena analit harus terlarut dalam
pelarut sebelum masuk ke sistem KCKT. Pelarut yang digunakan untuk melarutkan asam askorbat adalah campuran fase gerak metanol dan bufer fosfat
0,01 M yang dominan mengandung akua demineralisata. Asam askorbat dapat terlarut dalam akua demineralisata dan metanol. Kelarutan asam askorbat dalam air pada suhu 20°C adalah 290 g/L dan kelarutan dalam metanol adalah 125 g/L
(International Œnological Codex, 2007). Syarat pemilihan pelarut adalah dapat melarutkan analit dengan baik, tidak berinteraksi dengan analit dan tidak toksik.
Akua demineralisata merupakan jenis pelarut air yang bebas mineral. Proses mendapatkan akua demineralisata adalah dengan melewatkan air mineral yang mengandung ion melalui suatu kolom resin sehingga mineral yang ada akan
tertahan pada kolom resin (Falah dkk., 2009).
Degradasi asam askorbat akan meningkat dengan adanya ion logam
transisi seperti Cu2+ dan Fe3+. Menurut Khan dan Sarwar (1999), ion Cu2+, Fe3+,
Cr6+, Mn2+ dan V5+ mampu meningkatkan kecepatan reaksi degradasi asam
askorbat pada suhu ruang 25°C. Kandungan trace metal dalam akua
demineralisata sangat kecil (Soen dkk., 1966) sehingga penggunaan akua demineralisata diharapkan dapat meminimalkan risiko degradasi asam askorbat
B. Penentuan Fase Gerak
Berdasarkan polaritas fase diam dan fase gerak, metode KCKT yang
digunakan merupakan metode KCKT fase terbalik karena fase diam yang
digunakan yaitu oktadesilsilan (C18) yang bersifat non polar sedangkan fase gerak
bersifat lebih polar dibanding fase diam. Fase gerak yang paling sering digunakan
dalam penelitian menggunakan sistem KCKT fase terbalik adalah campuran air dengan pelarut organik seperti asetonitril dan metanol. Fase gerak yang dipakai
untuk sistem KCKT fase terbalik adalah pelarut organik yang bersifat mudah bercampur dengan air, viskositas relatif rendah, stabil di bawah kondisi yang digunakan. Jenis pelarut organik yang paling sering dan disarankan berturut-turut
adalah asetonitril, metanol, dan paling jarang digunakan adalah tetrahidrofuran (Snyder dkk., 2010).
Fase gerak yang digunakan dalam penelitian ini adalah campuran metanol dengan bufer fosfat 0,01 M pada pH 3. Sistem elusi fase gerak yang digunakan dalam penelitian ini adalah isokratik karena menggunakan campuran
fase gerak dengan perbandingan tetap sehingga polaritas fase gerak tetap selama proses elusi berlangsung.
Eluent strength (ε°) merupakan salah satu hal yang perlu diperhatikan
ketika memilih suatu pelarut dalam fase gerak. Eluent strength adalah
kemampuan pelarut organik untuk mengelusi suatu analit. Semakin besar nilai
eluent strength maka semakin besar kemampuan elusinya. Semakin besar nilai ε° maka semakin besar risiko terjadinya tumpang tindih antara puncak dua analit
maka fase gerak akan lebih sulit untuk mengelusi analit. Metanol memiliki nilai
ε° = 1,0 sedangkan asetonitril memiliki nilai ε° = 3,1 pada kolom C18. Apabila
dilihat dari nilai ε° menunjukkan kemampuan elusi asetonitril untuk mengelusi
analit lebih besar dari pada metanol. Namun, asetonitril tidak digunakan sebagai komposisi fase gerak dikarenakan biaya yang dibutuhkan terlalu mahal. Selain itu,
dengan menggunakan pelarut metanol, asam askorbat sudah dapat terelusi dengan baik dalam sistem KCKT yang digunakan. Oleh karena itu, untuk meningkatkan
efisiensi biaya dalam penelitian ini dipilih pelarut metanol sebagai komponen fase gerak.
Bufer fosfat merupakan salah satu komponen fase gerak yang digunakan.
Bufer fosfat mempunyai nilai pKa 2,1; 7,2 dan 12,3 dengan rentang pH berturut-turut adalah 1,1-3,1; 6,2-8,2; dan 11,3-13,3 (Supelco, 2001). Rentang pH tersebut
menunjukkan kapasitas bufer fosfat, yaitu kemampuan untuk mempertahankan pH secara efektif. Suatu larutan asam askorbat 5% dalam air memiliki pH 2,1 - 2,6, pH 10% larutan kalsium askorbat dalam air adalah antara 6,8 dan 7,4 dan pH
larutan natrium askorbat dalam air antara 7,0 dan 8,0. Stabilitas maksimum terjadi dekat pH 3 dan pH 6 (Sihite, 2010). Asam askorbat cukup stabil dalam larutan
dengan pH rendah seperti 2 atau 3 dengan anggapan bahwa tidak ada ion logam transisi dalam larutan. Peningkatan pH fase gerak menjadi > nilai pKa asam
askorbat yaitu 4,2 akan meningkatkan terbentuknya ion asam askorbat (AscH-)
yang berakibat pada stabilitas asam askorbat dalam larutan menurun (Buettner and Jurkiewics, 1996). Pada penelitian ini digunakan pH 3 dengan pertimbangan
orientasi, dilakukan pengukuran dengan menggunakan fase gerak tanpa mengandung bufer, mengandung bufer fosfat pH 3 dan bufer fosfat pada pH 5,6.
Akan tetapi, hasil puncak kromatogram yang diperoleh dari penggunaan fase gerak tanpa bufer dan bufer pH 5,6 terpecah menjadi beberapa bagian dan bentuk puncak yang tidak baik (Gambar 7 dan 8). Berbeda dengan puncak kromatogram
yang dihasilkan dengan menggunakan bufer fosfat pH 3 (Gambar 9). Oleh sebab itu, perlu digunakan bufer untuk mempertahankan pH selama berada dalam sistem
KCKT tetap pada rentang pH stabil larutan asam askorbat sehingga menghasilkan waktu retensi asam askorbat yang tetap dan meminimalkan terjadinya kerusakan asam askorbat akibat perubahan pH.
Gambar 7. Kromatogram asam askorbat konsentrasi 100 µg/mL, dengan parameter sebagai berikut:
Fase diam : Phenomenex®C18 dimensi 250 x 4,6 mm, 5 µm Fase gerak : metanol : air (40 : 60)
Gambar 8. Kromatogram asam askorbat konsentrasi 100 µg/mL, dengan parameter sebagai berikut:
Fase diam : Phenomenex®C18 dimensi 250 x 4,6 mm, 5 µm Fase gerak : metanol : bufer fosfat pH 5,6 (40 : 60)
Kecepatan alir : 1 mL/menit Volume injeksi : 20 µL Detektor : UV-244 nm
Gambar 9. Kromatogram asam askorbat konsentrasi 100 µg/mL, dengan parameter sebagai berikut:
Fase diam : Phenomenex®C18 dimensi 250 x 4,6 mm, 5 µm Fase gerak : metanol : bufer fosfat pH 3 (40 : 60)
Kecepatan alir : 1 mL/menit Volume injeksi : 20 µL Detektor : UV-244 nm
Selain kapasitas bufer, UV-cutoff merupakan hal lain yang perlu
diperhatikan dalam pemilihan bufer. UV-cutoff adalah panjang gelombang suatu
kuvet yang memiliki tebal 1 cm (Rohman dan Gandjar, 2007). Bufer fosfat
memiliki nilai UV-cutoff di bawah 200 nm (Supelco, 2001), sedangkan metanol
memiliki UV-cutoff 205 nm (Rohman dan Gandjar, 2007). Apabila pengukuran
analit dilakukan pada panjang gelombang UV-cutoff pelarut yang digunakan maka
akan terjadi kekacauan hasil sehingga hasil data menjadi bias. Panjang gelombang
yang digunakan dalam penelitian ini adalah 244 nm sehingga tidak terjadi bias
data akibat UV-cutoff.
Evaluasi polaritas fase gerak yang digunakan dapat dilihat dengan menggunakan parameter indeks polaritas (P’). Komposisi fase gerak yang digunakan pada penelitian ini adalah metanol : bufer fosfat 0,01 M pH 3 dengan
perbandingan 10:90; 20:80; 30:70; 40:60; dan 50:50. Menurut Mulja dan Suharman (1995), semakin besar nilai indeks polaritas campuran fase gerak, maka
semakin polar fase gerak yang digunakan. Indeks polaritas fase gerak yang digunakan untuk masing-masing komposisi dapat dilihat pada tabel II di bawah ini:
Tabel II. Indeks polaritas fase gerak campuran metanol : bufer fosfat 0,01 M pH 3 (Snyder dkk., 2010)
No. Komposisi Fase Gerak Indeks Polaritas Metanol Bufer fosfat 0,01 M pH 3
gerak metanol : bufer fosfat 0,01 M pH 3 yang akan di optimasi yaitu 10 : 90; 20 : 80; 30 : 70; 40 : 60 dan 50 : 50. Asam askorbat merupakan senyawa yang
bersifat polar sehingga cenderung akan lebih optimal terelusi dengan menggunakan fase gerak yang bersifat polar dalam sistem KCKT fase terbalik.
Fase gerak yang telah dipersiapkan, disaring dengan menggunakan
kertas Whatman 0,45 µm dengan maksud untuk menghilangkan partikel-partikel
yang dapat mengotori kolom dan mengganggu pengukuran. Selanjutnya, fase
gerak harus didegassing selama kurang lebih 15 menit untuk menghilangkan
gelembung gas yang dapat mengganggu detektor.
C. Larutan Baku
Baku asam askorbat yang digunakan adalah reference standard dengan
kemurnian 98,7 % yang didapatkan dari PT. Supelco dan memiliki Certificate of
Analysis (CoA) yang dapat dilihat pada lampiran 1 sehingga terjamin kemurniannya. Tujuan pembuatan larutan baku adalah memastikan di dalam
sampel terdapat zat asam askorbat yang hendak dianalisis. Tujuan tersebut dilihat dari kesamaan waktu retensi antara waktu retensi larutan baku dengan senyawa
analit dalam sampel.
Pada penentuan panjang gelombang maksimum dibuat larutan baku
dengan tiga level konsentrasi berbeda, yaitu 40, 50, dan 60 µg/mL pada pelarut