KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAN FRAKSI BUNGA
TUMBUHAN BROKOLI (Brassica oleracea L. var. botrytis L.)
SKRIPSI
OLEH :
RUTH MARLIANI SILALAHI NIM : 060804003
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAN FRAKSI BUNGA
TUMBUHAN BROKOLI (Brassica oleracea L. var. botrytis L.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RUTH MARLIANI SILALAHI NIM : 060804003
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAN FRAKSI BUNGA
TUMBUHAN BROKOLI (Brassica oleracea L. var. botrytis L.)
OLEH:
RUTH MARLIANI SILALAHI NIM : 060804003
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Agustus 2010
Pembimbing I Panitia Penguji
(Drs. Suryadi Achmad, M.Sc., Apt.) (Dr. Marline Nainggolan, MS., Apt) NIP. 195109081985031002 NIP. 195709091985112001
Pembimbing II (Dra. Saleha Salbi, M.Si., Apt) NIP. 194909061980032001
(Drs. Awaluddin Saragih, M.Si., Apt) (Drs. Syahrial Yoenoes, SU., Apt) NIP. 195008221974121002 NIP. 195112061983031001
(Drs. Suryadi Achmad, M.Sc., Apt.) NIP. 195109081985031002
Disahkan Oleh: Dekan
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat kasih dan karunianya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul ”Karakterisasi Simplisia, Skrining Fitokimia dan Uji Aktivitas
Antioksidan Ekstrak Etanol dan Fraksi Bunga Tumbuhan Brokoli (Brassica oleracea L. var. botrytis L.)”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Terimakasih dan penghargaan yang tulus kepada Ayahanda dan Ibunda
tercinta, B. Sidebang dan Riana Sinaga, yang tiada pernah ada hentinya berkorban dengan tulus ikhlas bagi kesuksesan penulis, juga kepada Adikku-adikku
tersayang (Tonggo Rosian Silalahi, Esra Erita Sari Silalahi, dan Wahyu Alfred Silalahi), yang selalu setia memberi doa, dorongan dan semangat.
Pada kesempatan ini penulis juga mengucapkan terima kasih yang tulus
dan ikhlas kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
USU Medan yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan.
2. Bapak Drs. Suryadi Achmad, M.Sc, Apt dan Drs. Awaluddin Saragih, M.Si,
Apt selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat selama penelitian hingga selesainya penyusunan skripsi ini.
memberikan kritik, saran, dan arahan kepada penulis dalam menyelesaikan
skripsi ini.
4. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik
selama perkuliahan dan Bapak Drs. David Sinurat, M.Si, Apt selaku penasehat akademis yang telah memberikan bimbingan kepada penulis selama ini.
5. Bapak kepala Laboratorium Farmakognosi dan Bapak kepala Laboratorium
Kimia Farmasi Kuantitatif yang telah memberikan bantuan dan fasilitas selama penulis melakukan penelitian.
6. Sahabat-sahabatku Apri, Leli, Mastin, Deni, Lia, Debo, Sabeth, Dina, Wati, Jon, Roni, Gokman, dan Jandri yang memberi bantuan, dukungan, dan motivasi. Rekan-rekan farmasi stambuk 2006, senior dan junior mahasiswa
fakultas farmasi, para asisten Laboratorium Farmakognosi dan Kimia Farmasi Kuantitatif serta kawan-kawan yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu
pengetahuan kefarmasian.
Medan, 11 Agustus 2010 Penulis
Karakterisasi Simplisia, Skrining Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Etanol dan Fraksi Tumbuhan Brokoli (Brassica oleracea L. var.
botrytis L.)
ABSTRAK
Dalam rangka meningkatkan pemanfaatan antioksidan alami dari tumbuhan, telah dilakukan pemeriksaan karakterisasi simplisia, skrining fitokimia, dan uji aktivitas antioksidan dengan metode aktivitas antiradikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) dari ekstrak etanol dan fraksi ekstrak n-heksan, etil asetat, dan etanol dari bunga tumbuhan brokoli botrytis L.). Serbuk simplisia bunga brokoli diekstraksi secara perkolasi dengan pelarut etanol 70%. Selanjutnya ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental. Dilakukan juga ekstraksi bertahap dengan pelarut n-heksana, etil asetat dan etanol. Selanjutnya ekstrak diuji terhadap DPPH sebagai radikal bebas untuk mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-17 dan ke-40 setelah penambahan pelarut metanol, berdasarkan hasil pengukuran operating time DPPH. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
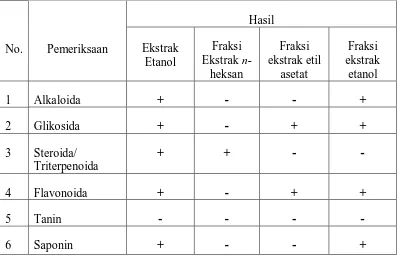
Hasil pemeriksaan karakterisasi simplisia diperoleh kadar air 5,33%, kadar sari yang larut dalam air 29,02%, kadar sari yang larut dalam etanol 12,09%, kadar abu total 0,80%, dan kadar abu yang tidak larut dalam asam 0,22%. Hasil skrining fitokimia pada masing-masing ekstrak, diperoleh hasil ekstrak etanol mengandung senyawa alkaloida, glikosida, steroida/triterpenoida, flavonoida, dan saponin; fraksi ekstrak n-heksan mengandung senyawa, steroida/ triterpenoda; fraksi ekstrak etil asetat mengandung senyawa glikosida dan flavonoid; dan fraksi ekstrak etanol mengandung alkaloida, glikosida, flavonoida dan saponin.
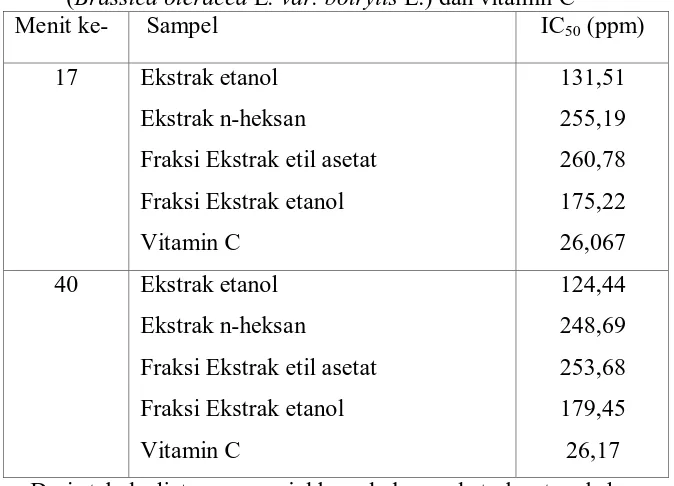
Hasil pengujian ini menunjukkan bahwa ekstrak etanol bunga brokoli memiliki aktivitas antioksidan sedang, fraksi ekstrak n-heksan dan etil asetat dengan aktifitas antioksidan sangat lemah, sedangkan fraksi ekstrak etanol dengan aktivitas antioksidan lemah. Ekstrak etanol, fraksi ekstrak n-heksan, etil asetat, dan etanol berturut-turut memiliki IC50 sebesar 131,51 ppm, 255,19 ppm, 260,78
ppm, dan 175,22 ppm pada menit ke-17, sedangkan pada menit ke-40 diperoleh IC50 berturut-turut sebesar 124,44 ppm, 248,69 ppm, 253,68 ppm, dan 179,45
ppm. Pembanding vitamin C memiliki IC50 sebesar 26,067 ppm pada menit ke 17
dan 26,17 ppm pada menit ke-40.
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karunianya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul ”Karakterisasi Simplisia, Skrining Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Etanol dan Fraksi Bunga Tumbuhan Brokoli (Brassica
oleracea L. var. botrytis L.)”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera
Utara.
Terimakasih dan penghargaan yang tulus kepada Ayahanda dan Ibunda tercinta, B. Sidebang dan Riana Sinaga, yang tiada pernah ada hentinya berkorban
dengan tulus ikhlas bagi kesuksesan penulis, juga kepada Adikku-adikku tersayang (Tonggo Rosian Silalahi, Esra Erita Sari Silalahi, dan Wahyu Alfred
Silalahi), yang selalu setia memberi doa, dorongan dan semangat.
Pada kesempatan ini penulis juga mengucapkan terima kasih yang tulus dan ikhlas kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis dapat
menyelesaikan pendidikan.
2. Bapak Drs. Suryadi Achmad, M.Sc, Apt dan Drs. Awaluddin Saragih, M.Si, Apt selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat
selama penelitian hingga selesainya penyusunan skripsi ini.
3. Ibu Dr. Marline Nainggolan, MS., Apt., Bapak Drs. Syahrial Yoenoes, SU.,
memberikan kritik, saran, dan arahan kepada penulis dalam menyelesaikan
skripsi ini.
4. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik
selama perkuliahan dan Bapak Drs. David Sinurat, M.Si, Apt selaku penasehat akademis yang telah memberikan bimbingan kepada penulis selama ini.
5. Bapak kepala Laboratorium Farmakognosi dan Bapak kepala Laboratorium
Kimia Farmasi Kuantitatif yang telah memberikan bantuan dan fasilitas selama penulis melakukan penelitian.
6. Sahabat-sahabatku Apri, Leli, Mastin, Deni, Lia, Debo, Sabeth, Dina, Wati, Jon, Roni, Gokman, dan Jandri yang memberi bantuan, dukungan, dan motivasi. Rekan-rekan farmasi stambuk 2006, senior dan junior mahasiswa
fakultas farmasi, para asisten Laboratorium Farmakognosi dan Kimia Farmasi Kuantitatif serta kawan-kawan yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu
pengetahuan kefarmasian.
Medan, 11 Agustus 2010 Penulis
Karakterisasi Simplisia, Skrining Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Etanol dan Fraksi Ekstrak n-Heksan, Etil Asetat, dan Etanol Bunga
Tumbuhan Brokoli (Brassica oleracea L. var. botrytis L.) ABSTRAK
Tumbuhan brokoli sayuran yang cukup sering dikonsumsi oleh masyarakat yang kaya akan nutrisi. Oleh karena itu, telah dilakukan pemeriksaan karakterisasi simplisia, skrining fitokimia, dan uji aktivitas antioksidan dengan metode aktivitas antiradikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) dari ekstrak etanol dan fraksi ekstrak n-heksan, etil asetat, dan etanol dari bunga tumbuhan brokoli. Serbuk simplisia bunga brokoli diekstraksi secara perkolasi dengan pelarut etanol 70%. Selanjutnya ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental. Dilakukan juga ekstraksi bertahap dengan pelarut n-heksana, etil asetat dan etanol. Selanjutnya ekstrak diuji terhadap DPPH sebagai radikal bebas untuk mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-17 dan ke-40 setelah penambahan pelarut metanol, berdasarkan hasil pengukuran operating time DPPH. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil pemeriksaan karakterisasi simplisia diperoleh kadar air 5,33%, kadar sari yang larut dalam air 29,02%, kadar sari yang larut dalam etanol 12,09%, kadar abu total 0,80%, dan kadar abu yang tidak larut dalam asam 0,22%. Hasil skrining fitokimia pada masing-masing ekstrak, diperoleh hasil ekstrak etanol mengandung senyawa alkaloida, glikosida, steroida/triterpenoida, flavonoida, dan saponin; fraksi ekstrak n-heksan mengandung senyawa, steroida/ triterpenoda; fraksi ekstrak etil asetat mengandung senyawa glikosida dan flavonoid; dan fraksi ekstrak etanol mengandung alkaloida, glikosida, flavonoida dan saponin.
Hasil pengujian ini menunjukkan bahwa ekstrak etanol bunga brokoli memiliki aktivitas antioksidan sedang, fraksi ekstrak n-heksan dan etil asetat dengan aktifitas antioksidan sangat lemah, sedangkan fraksi ekstrak etanol dengan aktivitas antioksidan lemah. Ekstrak etanol, fraksi ekstrak n-heksan, etil asetat, dan etanol berturut-turut memiliki IC50 sebesar 131,51 ppm, 255,19 ppm, 260,78
ppm, dan 175,22 ppm pada menit ke-17, sedangkan pada menit ke-40 diperoleh IC50 berturut-turut sebesar 124,44 ppm, 248,69 ppm, 253,68 ppm, dan 179,45
ppm. Pembanding vitamin C memiliki IC50 sebesar 26,067 ppm pada menit ke 17
dan 26,17 ppm pada menit ke-40.
Simplex Characterization, Phytochemical Screening and Antioxidant Activities Test of Ethanolic Extract and Fractions of n-Hexane, Ethyl Acetate
and Ethanolic of Broccoli (Brassica oleracea L. var. botrytis L.)
ABSTRACT
Broccoli (Brassica oleracea L. var. botrytis L.) family Brassicaceae is a plant which flowers are used as vegetables and often consumed by people who are rich in nutrients. Therefore,had been done the research of simplex characteristics, phytochemical screening, and the antioxidant activity test by using anti-free radical DPPH (1,1-diphenyl-2-picrylhydrazil) from etanolic extract and fraction of n-hexane, ethyl acetate and ethanolic fraction. The ethanolic extract were prepared by extracting with 70% ethanol in percolator. After extraction, extracts were concentrated and dried by using rotary evaporator and freeze dryer. Broccoli was also extracted gradually with n-hexane, ethyl acetate and ethanol. Then, the antioxidant activity of extracts were tested by using DPPH as free radical. Absorbance of DPPH was measured at 516 nm in 17th and 40th minutes after the addition of methanol solvent based on operating time measurement of DPPH solution after the addition of extract
The result of simplex characteristics gave the water content value 5.33%, the water soluble extract value 29.02%, the ethanol soluble extract value 12.09%, the total ash value 0.80%, and the acid insoluble ash value 0.23%. Based on phytochemical screening, ethanolic extract contains alkaloid, glycoside, steroid/ triterpene and flavonoid; n- hexane fraction contains , steroid/triterpene; ethyl acetate fraction contains glycoside and flavonoid; and ethanolic fraction contains alkaloid, glycoside, flavonoid and saponin.
In this study ethanolic extract of sprouting broccoli had medium antioxidant activity; n-hexane and ethyl acetat fractions had very weak antioxidant activity and the ethanolic fraction had weak antioxidant activity. The IC50 of
ethanolic extract, n-hexane, ethyl acetate, ethanolic fractions in 17th minutes in a row 131.51 ppm, 255.19 ppm, 260.78 ppm, and 175.22 ppm respectively. The IC50 of ethanolic extract, n-hexane, ethyl acetate, ethanolic fractions in 40th
minutes in a row 124.44 ppm, 248.69 ppm, 253.68 ppm, and 179.45 ppm respectively. Ascorbic acid was used as reference and its IC50 was 26.067 ppm in
17th minutes and 26.17 ppm in 40th minutes.
DAFTAR ISI
JUDUL... i
LEMBAR PENGESAHAN... iii
KATA PENGANTAR... iv
ABSTRAK... vi
ABSTRACT... vii
DAFTAR ISI... v
DAFTAR TABEL... xiii
DAFTAR GAMBAR... xiv
DAFTAR LAMPIRAN ... xv
BAB I. PENDAHULUAN... 1
1.1 Latar Belakang... 1
1.2 Perumusan Masalah... 3
1.3 Hipotesis... 3
1.4 Tujuan... 4
1.5 Manfaat... 4
BAB II. TINJAUAN PUSTAKA... 5
2.1 Uraian Tumbuhan... 5
2.1.1 Daerah Tumbuh... 5
2.1.2 Nama Daerah... 6
2.1.3 Nama Asing... 6
2.1.4 Sistematika Tumbuhan... 6
2.1.6 Morfologi Tumbuhan... 7
2.1.7 Kandungan Kimia... 8
2.1.8 Kegunaan... 8
2.2 Ekstraksi... 9
2.3 Radikal Bebas... 10
2.4 Antioksidan... 12
2.4.1 Antioksidan Alami... 14
2.4.2 Vitamin C... 14
2.4.3 Polifenol... 16
2.5 Spektrofotometer UV-Visibel... 16
2.6 Penentuan Aktivitas Antioksidan dengan Metode DPPH... 17
2.6.1 Pelarut... 20
2.6.2 Pengukuran Absorbansi-Panjang Gelombang... 20
2.6.3 Waktu Pengukuran... 21
BAB III. METODOLOGI PENELITIAN... 22
3.1 Alat... 22
3.2 Bahan... 22
3.3 Penyiapan Bahan Tumbuhan... 23
3.3.1 Pengambilan Bahan Tumbuhan... 23
3.3.2 Identifikasi Tumbuhan... 23
3.3.3 Pengolahan Bahan Tumbuhan... 23
3.4 Pembuatan Pereaksi... 23
3.4.1 Besi (III) Klorida... 23
3.4.3 Timbal (II) asetat 0,4 M... 24
3.4.4 Pereaksi Meyer... 24
3.4.5 Pereaksi Mollish... 24
3.4.6 Pereaksi Dragendorf... 24
3.4.7 Larutan Kloralhidrat... 24
3.4.8 Larutan Pereaksi Asam Sulfat 2N... 24
3.4.9 Pereaksi Bouchardat... 25
3.4.10 Pereaksi Liebermann-Burchard... 25
3.4.11 Larutan Pereaksi DPPH 0,5 mM... 25
3.5 Pemeriksaan Karakteristik Simplisia... 25
3.5.1 Pemeriksaan Makroskopik... 25
3.5.2 Pemeriksaan Mikroskopik... 25
3.5.3 Penetapan Kadar Air... 25
a. Penjenuhan Toluen... 26
b. Penetapan Kadar Air Simplisia... 26
3.5.4 Penetapan Kadar Sari yang Larut dalam Air... 26
3.5.5 Penetapan Kadar Sari yang Larut dalam Etanol... 27
3.5.6 Penetapan Kadar Abu Total... 27
3.5.7 Penetapan Kadar Abu yang Tidak Larut dalam Asam... 27
3.6 Skrining Fitokimia... 28
3.6.1 Pemeriksaan Alkaloida... 28
3.6.2 Pemeriksaan Flavonoida... 28
3.6.3 Pemeriksaan Glikosida ... 28
3.6.4 Pemeriksaan Saponin... 29
3.6.5 Pemeriksaan Tanin ... 30
3.6.6 Pemeriksaan Steroida/Triterpenoida ... 30
3.7 Pembuatan Ekstrak Etanol Bunga Brokoli... 30
3.8 Pembuatan Fraksi Ektrak Bunga Brokoli... 31
3.9 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel... 31
3.9.1 Prinsip Metode DPPH... 31
3.9.2 Pembuatan Larutan Blanko... 31
3.9.3 Penentuan Panjang Gelombang Serapan Maksimum... 32
3.9.4 Penentuan Operating Time Larutan DPPH dalam Metanol... 32
3.9.5 Pembuatan Larutan Induk... 32
3.9.6 Pembuatan Larutan Uji... 32
3.9.7 Penentuan Persen Peredaman... 33
3.9.8 Penentuan Nilai IC50... 33
BAB IV. HASIL DAN PEMBAHASAN... 34
4.1 Hasil Identifikasi Tumbuhan... 34
4.2 Hasil Karakterisasi Simplisia... 34
4.3 Hasil Skrining Fitokimia... 36
4.4 Hasil Analisis Aktivitas Antioksidan Sampel Uji... 36
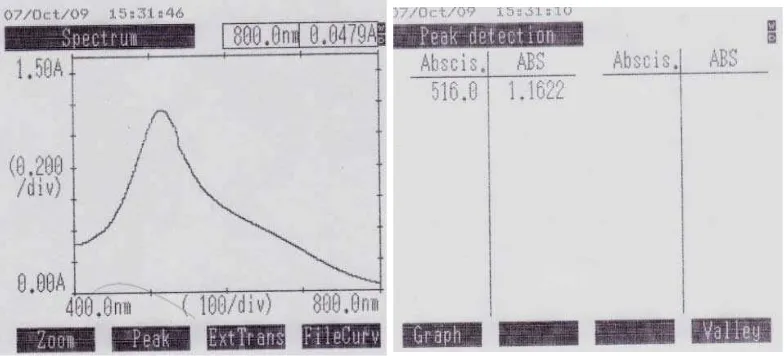
4.4.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum... 36
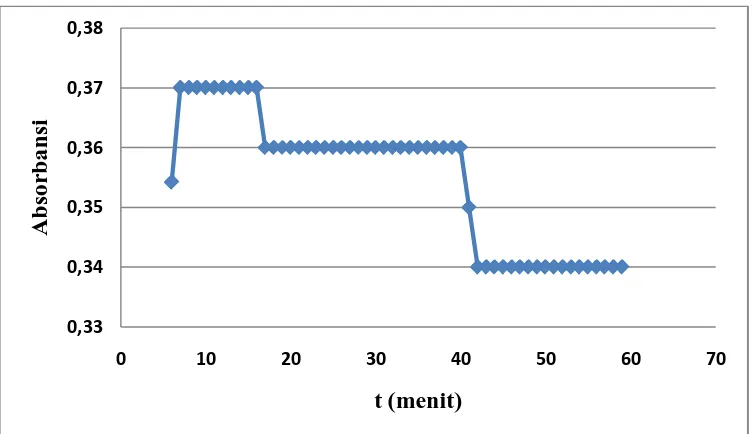
4.4.2 Hasil Penentuan Operating Time Larutan DPPH dalam Metanol... 37
4.6 Analisis Nilai IC50 (Inhibitory Concentration) Sampel Uji... 42
BAB V. KESIMPULAN... 45
5.1 Kesimpulan... 45
5.2 Saran... 45 DAFTAR PUSTAKA
DAFTAR TABEL
Tabel Halaman 1. Hasil Pemeriksaan Skrining Fitokimia Ekstrak dan fraksi
ekstrak etanol... 18
2. Hasil Pemeriksaan Skrining Fitokimia Fraksi Ekstrak Bunga Brokoli... 19
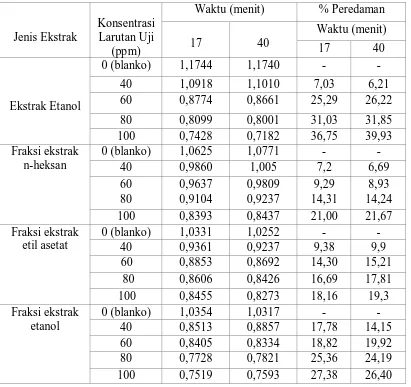
3. Hasil analisis Peredaman Radikal Bebas oleh Ekstrak etanol dan Fraksi Ekstrak Bunga Brokoli ... 24
4. Hasil Analisis Peredaman Radikal Bebas oleh Vitamin C ... 25
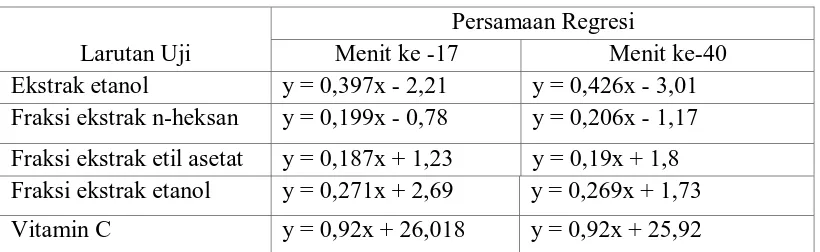
5. Hasil persamaan regresi linier yang diperoleh untuk ekstrak etanol, fraksi-fraksi ekstrak, dan vitamin C ... 25
6. Nilai IC50 ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli dan vitamin C ... 26
7. Hasil Pemeriksaan Karakteristik Serbuk Simplisia Bunga Brokoli ... 39
8. Data Absorbansi Ekstrak Etanol Bunga Brokoli ... 45
9. Data Absorbansi Fraksi Ekstrak n-heksan ... 47
10. Data Absorbansi Fraksi Etil Asetat ... 50
11. Data Absorbansi Fraksi Ekstrak Etanol ... 54
DAFTAR GAMBAR
Gambar Halaman 1. Kurva serapan maksimum larutan DPPH 40 ppm dalam
metanol secara spektrofotometri visibel... 20
2. Kurva Absorbansi Operating Time Larutan DPPH dalam Metanol... 21
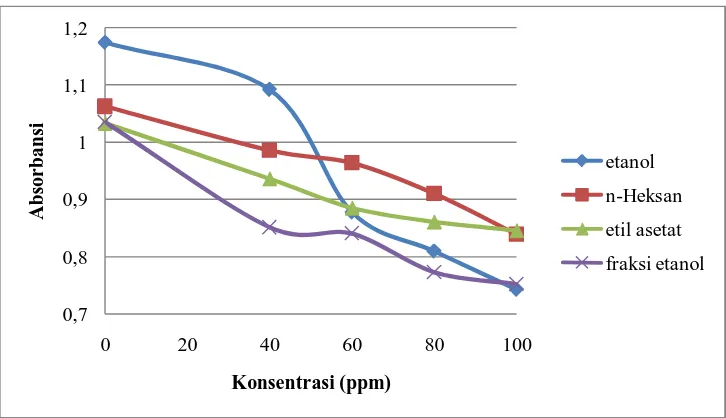
3. Hasil analisis aktivitas antioksidan sampel ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli pada menit ke-17... 22
4. Hasil analisis aktivitas antioksidan sampel ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli pada menit ke-40... 22
5. Hasil analisis aktivitas antioksidan vitamin C pada menit ke- 17 dan ke-40... 23
6. Ladang Brokoli... 32
7. Tumbuhan Brokoli... 32
8. Bunga Tumbuhan Brokoli (Brassica oleracea L. var. botrytis L.) segar... 33
9. Simplisia bunga brokoli. (Brassicae oleraceae Flos)... 33
10. Mikroskopik serbuk simplisia bunga brokoli... 34
11. Spektrofotometer UV-Visibel (Shimadzu mini 1240)... 34
12. Pembuatan Serbuk Simplisia Bunga Brokoli (Brassicae oleraceae Flos)... 35
13. Bagan Pembuatan Ekstrak Etanol Bunga Brokoli... 36
DAFTAR LAMPIRAN
Lampiran Halaman
1. Surat Hasil Identifikasi Tumbuhan... 32
2. Gambar Tumbuhan Brokoli (Brassica oleracea L. var. botrytis L.)... 33
3. Pengamatan Mikroskopik... 35
4. Gambar Alat Spektrofotometri... 35
5. Bagan Kerja... 35
6. Data Absorbansi Operating Time Larutan DPPH dalam metanol... 38
7. Hasil Pemeriksaan Karakteristik Serbuk Simplisia Bunga Brokoli... 39
8. Perhitungan Pemeriksaan Karakteristik Serbuk Simplisia... 40
9. Hasil Uji Antioksidan... 44
Karakterisasi Simplisia, Skrining Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Etanol dan Fraksi Ekstrak n-Heksan, Etil Asetat, dan Etanol Bunga
Tumbuhan Brokoli (Brassica oleracea L. var. botrytis L.) ABSTRAK
Tumbuhan brokoli sayuran yang cukup sering dikonsumsi oleh masyarakat yang kaya akan nutrisi. Oleh karena itu, telah dilakukan pemeriksaan karakterisasi simplisia, skrining fitokimia, dan uji aktivitas antioksidan dengan metode aktivitas antiradikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) dari ekstrak etanol dan fraksi ekstrak n-heksan, etil asetat, dan etanol dari bunga tumbuhan brokoli. Serbuk simplisia bunga brokoli diekstraksi secara perkolasi dengan pelarut etanol 70%. Selanjutnya ekstrak dipekatkan dengan alat rotary evaporator dan dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental. Dilakukan juga ekstraksi bertahap dengan pelarut n-heksana, etil asetat dan etanol. Selanjutnya ekstrak diuji terhadap DPPH sebagai radikal bebas untuk mengukur absorbansi DPPH pada panjang gelombang 516 nm pada menit ke-17 dan ke-40 setelah penambahan pelarut metanol, berdasarkan hasil pengukuran operating time DPPH. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil pemeriksaan karakterisasi simplisia diperoleh kadar air 5,33%, kadar sari yang larut dalam air 29,02%, kadar sari yang larut dalam etanol 12,09%, kadar abu total 0,80%, dan kadar abu yang tidak larut dalam asam 0,22%. Hasil skrining fitokimia pada masing-masing ekstrak, diperoleh hasil ekstrak etanol mengandung senyawa alkaloida, glikosida, steroida/triterpenoida, flavonoida, dan saponin; fraksi ekstrak n-heksan mengandung senyawa, steroida/ triterpenoda; fraksi ekstrak etil asetat mengandung senyawa glikosida dan flavonoid; dan fraksi ekstrak etanol mengandung alkaloida, glikosida, flavonoida dan saponin.
Hasil pengujian ini menunjukkan bahwa ekstrak etanol bunga brokoli memiliki aktivitas antioksidan sedang, fraksi ekstrak n-heksan dan etil asetat dengan aktifitas antioksidan sangat lemah, sedangkan fraksi ekstrak etanol dengan aktivitas antioksidan lemah. Ekstrak etanol, fraksi ekstrak n-heksan, etil asetat, dan etanol berturut-turut memiliki IC50 sebesar 131,51 ppm, 255,19 ppm, 260,78
ppm, dan 175,22 ppm pada menit ke-17, sedangkan pada menit ke-40 diperoleh IC50 berturut-turut sebesar 124,44 ppm, 248,69 ppm, 253,68 ppm, dan 179,45
ppm. Pembanding vitamin C memiliki IC50 sebesar 26,067 ppm pada menit ke 17
dan 26,17 ppm pada menit ke-40.
Simplex Characterization, Phytochemical Screening and Antioxidant Activities Test of Ethanolic Extract and Fractions of n-Hexane, Ethyl Acetate
and Ethanolic of Broccoli (Brassica oleracea L. var. botrytis L.)
ABSTRACT
Broccoli (Brassica oleracea L. var. botrytis L.) family Brassicaceae is a plant which flowers are used as vegetables and often consumed by people who are rich in nutrients. Therefore,had been done the research of simplex characteristics, phytochemical screening, and the antioxidant activity test by using anti-free radical DPPH (1,1-diphenyl-2-picrylhydrazil) from etanolic extract and fraction of n-hexane, ethyl acetate and ethanolic fraction. The ethanolic extract were prepared by extracting with 70% ethanol in percolator. After extraction, extracts were concentrated and dried by using rotary evaporator and freeze dryer. Broccoli was also extracted gradually with n-hexane, ethyl acetate and ethanol. Then, the antioxidant activity of extracts were tested by using DPPH as free radical. Absorbance of DPPH was measured at 516 nm in 17th and 40th minutes after the addition of methanol solvent based on operating time measurement of DPPH solution after the addition of extract
The result of simplex characteristics gave the water content value 5.33%, the water soluble extract value 29.02%, the ethanol soluble extract value 12.09%, the total ash value 0.80%, and the acid insoluble ash value 0.23%. Based on phytochemical screening, ethanolic extract contains alkaloid, glycoside, steroid/ triterpene and flavonoid; n- hexane fraction contains , steroid/triterpene; ethyl acetate fraction contains glycoside and flavonoid; and ethanolic fraction contains alkaloid, glycoside, flavonoid and saponin.
In this study ethanolic extract of sprouting broccoli had medium antioxidant activity; n-hexane and ethyl acetat fractions had very weak antioxidant activity and the ethanolic fraction had weak antioxidant activity. The IC50 of
ethanolic extract, n-hexane, ethyl acetate, ethanolic fractions in 17th minutes in a row 131.51 ppm, 255.19 ppm, 260.78 ppm, and 175.22 ppm respectively. The IC50 of ethanolic extract, n-hexane, ethyl acetate, ethanolic fractions in 40th
minutes in a row 124.44 ppm, 248.69 ppm, 253.68 ppm, and 179.45 ppm respectively. Ascorbic acid was used as reference and its IC50 was 26.067 ppm in
17th minutes and 26.17 ppm in 40th minutes.
BAB I PENDAHULUAN
1.1Latar Belakang
Dewasa ini dunia kesehatan banyak membahas tentang radikal bebas (free radical) dan antioksidan. Hal ini terjadi karena sebagian besar penyakit diawali
oleh karena oksidasi yang berlebihan dalam tubuh. Tampaknya oksigen merupakan sesuatu yang paradoksial dalam kehidupan. Molekul ini sangat
dibutuhkan oleh organisme aerob karena memberikan energi pada proses metabolisme dan respirasi, namun pada kondisi tertentu keberadaannya berimplikasi pada penyakit dan kondisi degeneratif, seperti aging, arthritis, kanker
(Winarsi, 2007).
Radikal bebas adalah suatu hasil samping reaksi metabolisme tubuh yang
merusak membran sel serta merusak dan merubah DNA sehingga terjadi mutasi atau sitotoksisitas. Radikal bebas diproduksi secara alami oleh tubuh dalam jumlah kecil, tetapi akan timbul masalah bila diproduksi terlalu banyak. (Kramer,
2004).
Zat antioksidan adalah substansi yang dapat menetralisir atau
menghancurkan radikal bebas. Radikal bebas adalah setiap molekul yang mengandung satu atau lebih electron yang tidak berpasangan. Radikal bebas juga terdapat di lingkungan sekitar kita yang berasal dari polusi udara, asap tembakau,
penguapan alkohol yang berlebihan, bahan pengawet dan pupuk, sinar ultra violet, X-rays, dan ozon. Radikal bebas dapat merusak sel tubuh apabila tubuh
menyebabkan mempercepat proses penuaan, sel kanker, penyakit hati, arthritis,
katarak, dan penyakit degeneratif lainnya (Anonim, 2009).
Eksplorasi bahan alami yang mempunyai aktivitas biologis menjadi salah
satu target para peneliti, setelah senyawa-senyawa sintetik yang mempunyai aktivitas biologi seperti senyawa antioksidan sintetik butylated hydroxytoluen (BHT), butylated hydroxyanisole (BHA) dan tertbutylhydroxyquinone (TBHQ)
dilarang penggunaannya karena bersifat karsinogenik. Berbagai studi mengenai BHA dan BHT menunjukkan bahwa komponen ini dapat menimbulkan tumor
pada hewan percobaan pada penggunakan dalam jangka panjang (Andarwulan, 1996).
Indonesia adalah salah satu negara dengan kekayaan alam terbesar di dunia. Kekayaan alam tersebut belum dimanfaatkan secara maksimal, dan berpeluang besar terdapat tumbuhan-tumbuhan yang berkhasiat sebagai
antioksidan. Tumbuhan brokoli
sayuran yang cukup sering dikonsumsi oleh masyarakat dengan kandungan nutrisinya yaitu protein, lemak, karbohidrat, vitamin C, serat, kalium, kalsium, dan karoten (Siemonsma, 1994). Senyawa antioksidan yang paling ampuh yang
tersimpan dalam brokoli adalah sulforafan, betakaroten, quersetin dan glutation (Winarsi, 2007).
Brokoli yang dikukus terbukti terjadi peningkatan kandungan polifenol dan tidak berpengaruh terhadap kandungan vitamin C (Gliszczynska, 2006). Oleh karena itu, pada penelitian ini dilakukan pengukusan sebelum pembuatan
Berdasarkan hal di atas, penulis tertarik untuk mengetahui karakterisasi
simplisia, skrining fitokimia dan aktivitas antioksidan dari ekstrak etanol, fraksi ekstrak n-heksan, fraksi etil asetat dan fraksi etanol dari bunga brokoli.
1.2Perumusan Masalah
1. Bagaimana karakterisasi simplisia bunga brokoli (Brassicae oleraceae Flos)?
2. Apakah ada perbedaan golongan senyawa kimia yang terkandung dalam ekstrak etanol dan fraksi bunga brokoli?
3. Apakah ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli memiliki kemampuan sebagai antioksidan?
4. Berapakah kekuatan antioksidan dari ekstrak etanol dan fraksi ekstrak
bunga brokoli dibandingkan dengan vitamin C?
5. Pada ekstrak maupun fraksi apa yang lebih baik kekuatan antioksidannya?
1.3Hipotesis
1. Dengan mengikuti cara pembuatan simplisia yang benar, maka dapat diketahui karakteristik simplisia bunga brokoli (Brassicae oleraceae Flos)
2. Terdapat perbedaan golongan senyawa kimia yang terkandung dalam ekstrak dan fraksi bunga brokoli berdasarkan pelarut yang digunakan.
3. Ekstrak etanol dan fraksi-fraksi bunga brokoli mempunyai aktivitas antioksidan.
4. Ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli memiliki aktivitas
antioksidan yang lebih kecil dari vitamin C.
5. Ekstrak etanol memiliki kekuatan antioksidan yang lebih baik
1.4Tujuan Penelitian
1. Untuk menentukan karakterisasi simplisia bunga brokoli (Brassicae oleraceae Flos).
2. Untuk megetahui perbedaan golongan senyawa kimia yang terkandung dalam ekstrak dan fraksi bunga brokoli berdasarkan pelarut yang digunakan.
3. Untuk mengetahui kekuatan antioksidan ekstrak etanol dan fraksi-fraksi bunga brokoli.
4. Untuk mengetahui besar kekuatan antioksidan ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli dibanding vitamin C.
5. Untuk mengetahui pada ekstrak maupun fraksi apa yang memiliki
kekuatan antioksidan yang lebih baik dibandingkan fraksi-fraksi bunga brokoli.
1.5 Manfaat Penelitian
1. Dapat diperoleh informasi tentang karakterisasi simplisia bunga brokoli (Brassicae oleraceae Flos)
2. Dapat diperoleh informasi golongan senyawa-senyawa kimia yang terkandung dalam ekstrak etanol dan fraksi-fraksi ekstrak bunga brokoli.
3. Dapat diketahui kekuatan antioksidan ekstrak etanol dan fraksi-fraksi bunga brokoli.
4. Dapat diketahui besar kekuatan antioksidan ekstrak etanol dan fraksi-
fraksi ekstrak bunga brokoli dibanding vitamin C.
5. Dapat diketahui pada ekstrak maupun fraksi apa yang memiliki kekuatan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, nama daerah, nama asing, morfologi tumbuhan, sistematika tumbuhan, sinonim tumbuhan, kandungan kimia
dan kegunaan dari tumbuhan.
2.1.1 Daerah Tumbuh
Brokoli sayuran sub tropik yang banyak dibudidayakan di Eropa dan Asia. Brokoli merupakan tanaman yang termasuk dalam tanaman dwimusim (biennial), yaitu
pertumbuhan vegetatif terjadi pada fase pertama dan pertumbuhan generatif (berbunga dan berbiji) pada fase berikutnya ( Muslim, 2009).
Tanaman brokoli termasuk cool season crop, sehingga cocok ditanam pada daerah pegunungan (dataran tinggi), yang beriklim sejuk. Di Indonesia, tanaman brokoli sebagai sayuran dibudidayakan secara luas pada daerah tinggi
seperti Bukit Tinggi (sumatera Barat), Karo (Sumatera Utara), Pangalengan (Jawa Barat), dan Sumber Brantas (Jawa Timur) ( Muslim, 2009).
Di Indonesia sayuran brokoli telah dikenal sejak abad ke-15, yaitu mulai penjajahan Belanda, sehingga lebih dikenal sebagai sayuran Eropa (Muslim, 2009).
Pada mulanya bunga brokoli dikenal sebagai sayuran daerah beriklim dingin (sub tropis), sehingga di Indonesia cocok ditanam di dataran tinggi antara
lembab. Kisaran temperatur optimum untuk pertumbuhan produksi sayuran ini
antara 15,5 - 18°C, dan maksimum 24°C. Setelah beberapa Negara di kawasan Asia berhasil menciptakan varietas-varietas unggul baru yang toleran terhadap
temperatur tinggi (panas), maka brokoli dapat ditanam di dataran menengah sampai tinggi (Rukmana, 1994).
2.1.2 Nama Daerah
Indonesia : Brokoli
2.1.3 Nama Asing
Broccoli (Inggris), Yang Hua Ye Chai (China), Asparkapsa (Estonia), Parsakaali (Finlandia), Chou broccoli (Perancis), Brokkoli (Jerman), Cavolo broccoli (Italia), Burokkori (Jepang), Brócolos (Portugis), Bróculos (Brazil),
Brokkoli, Kapústa sparzhevaia (Rusia), Brócoli, Bróculi, Brécol (Spanyol), Brokuł (Polandia), Brokolica (Slovenia), Brokolice (Cekoslovakia) (Rocha,
1995).
2.1.4 Sistematika Tumbuhan
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo
Famili : Cruciferae / Brassicaceae
Genus : Brassica
Spesies
2.1.5 Sinonim Tumbuhan
Sinonim: Brassica oleracea var. botrytis subvar. Cymosa, Brassica botrytis Miller, Brassica oleracea var botrytis cauliflora (Dalimartha, 1999).
2.1.6 Morfologi Tumbuhan
Brokoli memiliki tangkai daun agak panjang dan helai daun berlekuk-lekuk panjang. Tangkai bunga brokoli lebih panjang dan lebih besar dibandingkan
dengan kubis bunga. Massa bunga brokoli tersusun secara kompak membentuk bulatan berwarna hijau tua, atau hijau kebiru-biruan, dengan diameter antara
15-20 cm atau lebih (Rukmana, 1994).
Pada kondisi lingkungan yang sesuai, massa bunga brokoli dapat tumbuh memanjang menjadi tangkai bunga yang penuh dengan kuntum bunga, tiap bunga
terdiri atas 4 helai kelopak bunga (calyx), empat helai daun mahkota bunga (corolla), enam benang sari yang komposisinya empat memanjang dan dua
pendek. Bakal buah terdiri atas dua ruang, dan setiap ruang berisi bakal biji (Rukmana, 1994).
Biji brokoli memiliki bentuk dan warna yang hampir sama, yaitu bulat
kecil berwarna coklat sampai kehitaman. Biji tersebut dihasilkan oleh penyerbukan sendiri ataupun silang dengan bantuan sendiri ataupun serangga.
Buah yang terbentuk seperti polong-polongan, tetapi ukurannya kecil, ramping dan panjangnya sekitar 3-5 mm (Rukmana, 1994).
Sistem perakaran relatif dangkal, dapat menembus kedalaman 60-70 cm.
Akar yang baru tumbuh berukuran 0,5 mm, tetapi setelah berumur 1-2 bulan system perakaran menyebar ke samping pada kedalaman antara 20-30 cm
Bunga brokoli berwarna hijau dan masa tumbuhnya lebih lama dari kubis
bunga. Brokoli tersusun dari bunga-bunga kecil yang berwarna hijau, tetapi tidak sekompak kubis. Dibandingkan dengan kubis bunga, bunga brokoli akan terasa
lebih lunak setelah direbus (Dalimartha, 1999).
Panen bunga brokoli dilakukan setelah umurnya mencapai 60-90 hari sejak ditanam, sebelum bunganya mekar, dan sewaktu kropnya masih berwarna hijau.
Jika bunganya mekar, tangkai bunga akan memanjang dan keluarlah kuntum-kuntum bunga berwarna kuning. Nama Simplisia bunga brokoli: Brassicae
oleraceae Flos (Dalimartha, 1999). 2.1.7 Kandungan Kimia
Brokoli mengandung air, protein, lemak, karbohidrat, serat, kalsium, zat
besi, vitamin (A, C, E, tiamin, riboflavin, nikotinamid), beta karoten, dan glutation. Selain itu brokoli mengandung senyawa sianohidroksibutena (CHB),
sulforafan, dan iberin yang merangsang pembentukan glutation (Dalimartha, 1999).
2.1.7 Kegunaan
Bunga brokoli digunakan untuk mempercepat penyembuhan, mencegah dan menghambat perkembangan sel kanker (Dalimartha, 1999), yang disebabkan
oleh adanya kandungan karotenoid (beta-karoten), indol, dan sulforafan (Hembing, 2008).
Menurut Profesor Dipak Das dari Universitas Connecticut, brokoli
2.2 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari jaringan tumbuhan maupun hewan. Sebelum ekstraksi dilakukan biasanya
bahan-bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan tertentu (Harborne, 1987).
Beberapa metode ekstraksi dengan mengggunakan pelarut yaitu:
A. Cara dingin 1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi
kinetic sedangkan yang dilakukan pengulangan panambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut
remaserasi. 2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru
sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaman bahan, tahap perendaman
antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada
temperatur tititk didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperature lebih tinggi daripada temperature ruangan, yaitu secara umum dilakukan pada
temperatur 40-50°C. 3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ektaraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infludasi
Infludasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit. 5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit.
2.3 Radikal Bebas
Radikal bebas adalah spesies kimia yang memiliki satu atau lebih elektron yang tidak berpasangan pada orbital terluarnya, sehingga dapat menyerang senyawa-senyawa lain seperti DNA, membran lipid, dan protein. Radikal ini akan
merebut elektron dari molekul lain yang ada disekitarnya untuk menstabilkan diri, sehingga spesies kimia ini sering dihubungkan dengan terjadinya kerusakan sel,
Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang
tidak terkontrol,menghasilkan ikatan silang (cross-link) pada DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada
biomolekul ini. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif, yakni kanker, aterosklerosis, rematik, jantung koroner, katarak (Silalahi, 2006).
Oksigen dijumpai dalam bentuk diatomic molecule. Pada keadaan normal pada rantai pernafasan (respiratory chain), oksigen berperan sebagai akseptor
terakhir dari electron. Kemudian bersama-sama 2H+ akan membentuk satu molekul H2O. Selain itu, oksigen dapat menjadi toxic mutagenic gas yang
kemudian dikenal sebagai ROS (Reactive Oxygen Species). ROS merupakan
senyawa oksigen yang bersifat reaktif. Senyawa ini pada dasarnya dapat dikelompokkan menjadi 2, yaitu senyawa oksigen reaktif yang bersifat radikal
seperti radikal superoksida (O2-), radikal hidroksil (OH·), radikal peroksil (RO2·),
radikal hidroperoksil (HO2·), dan senyawa oksigen reaktif yang bersifat
nonradikal (oksidan) seperti hydrogen peroksida (H2O2), asam hipoklorat (HOCl),
ozon (O3), singlet oksigen (-O2) dan peroksinitrit (ONOO) (Sudiana, 2008).
Secara fisiologi tubuh memang menghasilkan ROS (radikal bebas atau
oksidan), adapaun sumber penghasil ROS, antara lain mitokondria, fagosit, xanthine oksidase, peroksisome, iskemi/reper fusi, jalur pada pembentukan asam arakhidonat, dan sebagainya. Bahan tersebut dihasilkan oleh tubuh untuk
membunuh bakteri yang masuk ke dalam tubuh. Namun bila radikal bebas atau oksidan dihasilkan oleh tubuh secara berlebihan, maka bahan tersebut akan
Scavenger enzyme, seperti superoksida dismutase (SOD), katalase atau glutation
peroksidase. Apabila rasio antara radikal bebas atau oksidan lebih besar daripada antiradikal bebas atau antioksidan, maka keadaan ini dikenal sebagai stress
oksidatif. (Sudiana, 2008)
Keberadaan radikal bebas juga bermanfaat bagi tubuh, yaitu untuk menbunuh komponen pathogen yang menginvasi tubuh. Meskipun demikian,
keberadaaan tidak diharapkan melebihi jumlah antioksidan dalam tubuh. Tubuh diperlengkapi dengan sel-sel inflamasi seperti sel granulosit, monosit, dan
makrofag, yang apat memproduksi senyawa-senyawa yang bersifat oksidan seperti H2O2, O2·-, ·OH, ClO-, dan O2. Senyawa-senyawa ini selain dapat
menghancurkan mikroorganisme dapat pula merusak sel-sel jaringan tubuh.
Ketika dalam tubuh terjadi peradangan hebat, hal itu dapat melibatkan sel-sel radang (inflammatory cells) sehingga menyebabkan kerusakan jaringan.
2.4 Antioksidan
Antioksidan atau reduktor berfungsi untuk mencegah terjadinya oksidasi atau menetralkan senyawa yang telah teroksidasi dengan cara menyumbangkan
hydrogen dan atau electron (Silalahi, 2006).
Menurut (Anies, 2009), antioksidan tubuh dikelompokkan menjadi 3 yakni:
(1). Antioksidan primer yang bekerja untuk mencegah pembentuk senyawa radikal baru menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi. Contohnya: enzim SOD yang berfungsi
sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas. Enzim SOD sebenarnya sudah ada dalam
mangan, seng, dan tembaga. Selenium (Se) juga berperan sebagai
antioksidan. Jadi jika ingin menghambat gejala dan penyakit degenerative,mineral-mineral tersebut hendaknya tersedia cukup dalam
makanan yang dikonsumsi setiap hari.
(2) Antioksidan sekunder yang berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai. Contoh: vitamin E, vitamin C, beta karoten, asam
urat, bilirubin, dan albumin.
(3) Antioksidan tersier yang memperbaiki kerusakan sel-sel dan jaringan yang
disebabkan radikal bebas. Contoh: enzim metionin sulfoksidan reduktase untuk memperbaiki DNA pada inti sel.
Antioksidan merupakan system pertahanan sel terhadap radikal bebas,
terdapat kriteria antioksidan yang efektif: (1). Antioksidan harus memiliki daya tarik-menarik yang besar terhadap jaringan. Dengan kata lain, antioksidan harus
dapat menyingkirkan radikal bebas sebelum merusak sel. (2). Antioksidan haruslah nontoksik. Hanya karena berfungsi sebagai antioksidan saat berada di dalam tabung percobaan, bukan berarti suatu zat dapat bekerja dengan baik di
dalam tubuh. (3). Antioksidan harus dapat mencapai lokasi yang membutuhkan perlindungan (Perricone, 2007)
Khasiat antioksidan untuk mencegah berbagai penyakit dan akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan buah-buahan yang kaya akan antioksidan tunggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih
efektif daripada suplemen antioksidan yang diisolasi (Silalahi, J., 2006)
Hasil penelitian menunjukkan bahwa buah-buahan, sayuran dan biji-bijian
bebas dalam tubuh, yang pada akhirnya dapat menekan proses penuaan dini
(Kosasih, 2004).
2.4.1 Antioksidan Alami
Data epidemiologi mendukung keterkaitan antara tingginya asupan sayur-sayuran dan buah-buahan dengan rendahnya penyakit kronis. Hal ini dikarenakan sayur-sayuran dan buah-buahan kaya akan zat gizi (vitamin, mineral, serat
pangan) serta berbagai kelompok zat bioaktif lain yang disebut zat fitokimia. Zat bioaktif ini bekerja secara sinergis, meliputi mekanisme enzim detoksifikasi,
peningkatan sistem kekebalan, pengurangan agregasi platelet, pengaturan sintesis kolesterol dan metabolisme hormon, penurunan tekanan darah, antioksidan, antibakteri, serta efek antivirus (Silalahi, 2006).
Khasiat antioksidan untuk mencegah berbagai penyakit akibat pengaruh oksidatif akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan
buah-buahan yang kaya akan antioksidan dan berbagai jenis daripada menggunakan antioksidan tungggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih efektif daripada sumplemen antioksidan yang diisolasi. Hal ini mungkin
dikarenakan oleh adanya komponen lain dan interaksinya dalam sayur-sayuran dan buah-buahan yang berperan secara positif (Silalahi, 2006).
Umumnya antioksidan yang ada dalam buah- buahan adalah vitamin C, vitamin E, karotenoid, flavonoid, dan komponen thiol (SH). Kontribusi aktifitas antioksidan komponen fenol lebih besar dibanding vitamin C dan karotenoid.
Sumber utama kapasitas antioksidan dari buah-buahan tidak hanya dari vitamin C tetapi juga dari komponen fenol (Ide,2009).
Rumus Bangun:
Vitamin C atau asam askorbat mempunyai berat molekul 178,13 dengan rumus bangun C6H8O6, dalam bentuk kristal tidak berwarna dengan titik cair
190-192°C. Asam askorbat mengandung tidak kurang dari 99,0% C6H8O6. Pemerian:
serbuk atau hablur putih atau agak kuning, tidak berbau, rasa asam, oleh pengaruh cahaya lambat laun menjadi gelap. Dalam keadaan kering, mantap di udara, dalam
larutan cepat teroksidasi. Kelarutan: mudah larut dalam air, agak sukar larut dalam etanol (95%) P, praktis tidak larut dalam kloroform P, dalam eter P dan dalam
benzene P. Penyimpanan dalam waah tertutup rapat, terlindung dari cahaya. Vitamin C mengandung khasiat sebagai antiskorbut (Departemen Kesehatan RI, 1979).
Vitamin C berhasil di isolasi untuk pertama kalinya pada tahun pada tahun
merupakan agen yang dapat mencegah
Asam askorbat adalah suatu reduktor. Sifat reduktor tersebut disebabkan oleh mudah terlepasnya atom-atom hydrogen pada gugus hidroksil yang terikat
pada atom C2 dan atom C3 (atom-atom C pada ikatan rangkap). Akibat pengaruh oksigen, zat-zat pengoksidasi lemah, atau oleh pengaruh enzim asam askorbat
ini juga terjadi di dalam tubuh. Karena memiliki sifat mudah teroksidasi, asam
askorbat digunakan sebagai antioksidan (Sumardjo, 2006).
Dalam semua percobaan adalah baik untuk menggunakan standar atau
"kontrol positif" di samping sampel utama yang sedang dipelajari. Sesuai standar yang secara luas digunakan adalah asam askorbat (Vitamin C) (Molyneux, 2004).
2.4.3 Polifenol
Gambar Struktur Dasar Polifenol
Senyawa fenol dapat di definisikan secara kimiawi oleh adanya satu cincin aromatik yang membawa satu (fenol) atau lebih (polifenol) substitusi hydroksil,
termasuk derifat fungsionalnya. Polifenol adalah kelompok zat kimia yang ditemukan pada tumbuhan. Zat ini memiliki tanda khas yakni memiliki banyak gugus fenol dalam molekulnya. Polifenol memiliki spektrum luas dengan sifat
kelarutan pada suatu pelarut yang berbeda-beda. Hal ini disebabkan oleh gugus hidroksil pada senyawa tersebut yang dimiliki berbeda jumlah dan posisinya.
Turunan polifenol sebagai antioksidan dapat menstabilkan radikal bebas dengan melengkapi kekurangan elektron yang dimiliki radikal bebas, dan menghambat terjadinya reaksi berantai dari pembentukan radikal bebas. Polifenol merupakan
2.5 Spektrofotometri UV-Visibel
Ahli kimia telah lama menggunakan warna sebagai bantuan dalam mengenali zat-zat kimia. Spektrofotometri dapat dianggap sebagai perluasan suatu
pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur absorpsi energy radiasi macam-macam zat kimia dan memungkinkan dilakukannya pengukuran kualitatif dari suatu zat dengan ketelitian yang lebih besar (Day,
1994).
Spektrofotometer pada dasarnya terdiri atas sumber sinar monokromator,
tempat sel untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau pencatat. Spektrometri serapan adalah pengukuran serapan radiasi elektromagnetik panjang gelombang tertentu yang sempit, mendekati
monokromatik, yang diserap zat. Spektrofotometri yang sering digunakan dalam dunia industri farmasi salah satu adalah spektrofotometri unltraviolet dengan
panjang gelombang 190-380 nm dan visible (cahaya tampak) dengan panjang gelombang 380-780 nm (Departemen Kesehatan RI, 1979).
2.6 Penentuan Aktivitas Antioksidan dengan Metode DPPH Ada berbagai cara untuk menentukan aktivitas antioksidan:
(1). BCB Method (β-Carotene Bleaching Methode) atau Metoda Pemutihan β -karoten (2). DPPH (2,2’-diphenyl-1-picrylhydrazil) Radical Scavenging Method (Metoda penangkapan Radikal DPPH) (3). Thiobarbituric Acid Reactive Species Assay (TBARS Assay) (4). Induction Period of Lard Oxidation assay (Rancimat
Assay) (Julhasratman, 2007).
Pada beberapa tahun belakangan ini, pengujian absorbansi oksigen radikal
dan cairan biologi lain. Metode analisa ini mengukur aktivitas dari antioksidan
pada makanan, serum dan cairan biologi lain. Metode analisa lain mengukur aktivitas dari antioksidan dalam melawan radikal bebas seperti 1,1-
diphenyl-2-picrylhydrazyl (DPPH) radikal, anion superoksida radikal (O2·), hidroksi radikal
(OH·) atau peroksi radikal (ROO·). Bermacam-macam metode yang digunakan untuk mengukur aktivitas antioksidan dari produk makanan dapat memberikan
hasil yang beragam tergantung pada spesifitas dari radikal bebas yang digunakan sebagai reaktan (Anonim, 2001).
Pada tahun 1922, Goldschmidt dan Renn menemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen kolorimetri untuk proses redoks. DPPH sangat berguna dalam berbagai
penyelidikan seperti inhibisi atau radikal polimerisasi kimia , penentuan sifat antioksidan amina, fenol atau senyawa alami (vitamin, ekstrak tumbuh-tumbuhan,
obat obat-obatan) dan untuk menghambat reaksi homolitik. DPPH berwarna sangat ungu seperti KMnO4 dan bentuk tereduksinya yaitu 1,1-difenil-2- picrylhydrazine (DPPH-H) yang berwarna oranye-kuning. DPPH tidak larut
dalam air (Ionita, 2003).
DPPH merupakan radikal bebas yang stabil pada suhu kamar dan sering
digunakan untuk mengevaluasi aktivitas antioksidan beberapa senyawa atau ekstrak bahan alam. DPPH menerima elektron atau radikal hidrogen akan membentuk molekul diamagnetik yang stabil. Interaksi antioksidan dengan DPPH
baik secara transfer elektron atau radikal hidrogen pada DPPH, akan menetralkan karakter radikal bebas dari DPPH dan membentuk DPPH tereduksi. Jika semua
berubah dari ungu tua menjadi kuning terang dan absorbansi pada panjang
gelombang 517 nm akan hilang. Perubahan ini dapat diukur secara stoikiometri sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul
DPPH akibat adanya zat antioksidan (Gurav, 2007).
DPPH merupakan suatu metode yang cepat, sederhana, dan murah untuk mengukur kapasitas antioksidan melibatkan makanan penggunaan radikal bebas,
1,1-Difenil-2-picrylhydrazyl (DPPH). DPPH secara luas digunakan untuk menguji
kemampuan untuk bertindak sebagai senyawa radikal bebas pemulung atau
hidrogen donor, dan untuk mengevaluasi aktivitas antioksidan makanan. Ini juga telah digunakan mengukur antioksidan dalam kompleks biologis sistem dalam beberapa tahun terakhir. Metode yang dapat DPPH digunakan untuk sampel padat
atau cair dan tidak spesifik untuk komponen antioksidan tertentu, tetapi berlaku untuk keseluruhan kapasitas antioksidan sampel. Ukuran dari total kapasitas
antioksidan akan membantu kita memahami sifat-sifat fungsional makanan (Prior et al, 1998).
Molyneux (2004) menyatakan bahwa suatu zat mempunyai sifat
antioksidan bila nilai IC50 kurang dari 200 ppm. Bila nilai IC50 yang diperoleh berkisar antara 200-1000 ppm, maka zat tersebut kurang aktif namun masih
berpotensi sebagai zat antioksidan.
Senyawa antioksidan mempunyai sifat yang relatif stabil dalam bentuk
radikalnya. Senyawa-senyawa yang berpotensi sebagai antioksidan dapat diprediksi dari golongan fenolat, flavonoid dan alkaloid, yang merupakan
senyawa-senyawa polar. Aktivitas antioksidan merupakan kemampuan suatu senyawa atau ekstrak untuk menghambat reaksi oksidasi yang dapat dinyatakan dengan persen penghambatan. Parameter yang dipakai untuk menunjukan
aktivitas antioksidan adalah harga konsentrasi efisien atau efficient concentration (EC50) atau Inhibition Concentration (IC50) yaitu konsentrasi suatu zat antioksidan
yang dapat menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan % penghambatan 50%. Zat yang mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50
yang rendah (Brand-Williams, 1995).
2.6.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut metanol atau etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.6.2 Pengukuran Absorbansi – Panjang Gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
uji sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm dan 520 nm. Bagaimanapun dalam praktiknya hasil pengukuran yang
karena panjang gelombang dapat diatur untuk memberikan absorbansi maksimum
sesuai dengan alat yang digunakan (Molyneux, 2004).
2.6.3 Waktu Pengukuran
Lamanya pengukuran menurut beberapa literatur, yang direkomendasikan adalah selama 30 menit dan ini telah dilakukan dalam beberapa penelitian khususnya belakangan ini (Kim, et al., 2002), waktu pengerjaan terpendek yaitu 5
menit(Lebeau,et al., 2000) atau 10 menit (Schwarz et al., 2001).
Berikut ini dapat dilihat resonansi DPPH dan reaksi DPPH dengan atom H
netral yang berasal dari senyawa-senyawa yang bersifat antioksidan:
Gambar Resonansi DPPH (1,1- diphenyl-2-picrylhydrazyl)
BAB III
METODOLOGI PENELITIAN
Jenis penelitian yang dilakukan adalah penelitian eksperimental.
Metodologi penelitian meliput i pengumpulan dan preparasi bahan, karakterisasi simplisia, pembuatan ekstrak etanol, fraksi ekstrak n-heksan, etil asetat, dan etanol, skrining fitokimia, dan uji aktivitas antioksidan dengan metode aktivitas
antiradikal bebas DPPH dengan menggunakan alat spektrofotometer visibel.
3.1 Alat
Alat-alat yang digunakan terdiri dari: Alat alat gelas laboratorium (Erlenmeyer, gelas beaker, gelas ukur, labu tentukur, tabung reaksi, gelas corong, labu alas bulat, pendingin Liebig), spektofotometer UV/Vis (Shimadzu mini
1240), penguap vakum putar (Heidolph VV 2000), freeze dryer (Modulyo/Edwards), mikroskop, krus porselin, tanur (Gallenkamp), neraca
analitis (Vibra), penangas air (Yenaco), desikator, timbangan, object glass, gelas penutup, lemari pengering, pisau, krus tang.
3.2 Bahan
Bahan yang digunakan dalam penelitian adalah bunga brokoli
adalah berkualitas pro analisis produksi Sigma: 1,1-diphenyl-2-picrylhydrazyl (DPPH); produksi E-Merck: metanol, toluen, raksa (II) klorida, kalium iodida, bismuth (III) nitrat, asam nitrat pekat, besi (III) klorida, asam klorida pekat, asam
sulfat pekat, timbal (II) asetat, kloralhidrat, kloroform, isopropanol, benzen, asam asetat anhidrit, natrium hidroksida, amil alkohol. Bahan kimia berkualitas teknis:
3.3 Penyiapan Bahan Tumbuhan
Penyiapan bahan tumbuhan meliputi pengambilan bahan tumbuhan, identifikasi tumbuhan, dan pengolahan bahan tumbuhan.
3.3.1 Pengambilan Bahan Tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan daerah lain. Bahan tumbuhan yang digunakan adalah
bunga brokoli yang diambil dari daerah Brastagi, Kabupaten Karo, Propinsi Sumatera Utara.
3.3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI).
Hasil dapat dilihat pada lampiran 1 halaman 31.
3.3.3 Pengolahan Bahan Tumbuhan
Bunga brokoli dikumpulkan, dibersihkan, dicuci, dikukus selama 3 menit, ditiriskan, kemudian diiriskan bagian kecambah bunganya. Bagian kecambah
bunga ditimbang sebagai berat basah. Bahan ini kemudian dikeringkan di lemari pengering hingga kering, yaitu jika simplisia tersebut diremas akan hancur, kemudian ditimbang sebagai berat kering.
3.4 Pembuatan Pereaksi 3.4.1 Besi (III) Klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling sampai 100 ml (Depkes RI, 1978).
3.4.2 Larutan HCl 2N
3.4.3 Timbal (II) asetat 0,4 M
Timbal (II) asetat sebanyak 15,17 g dilarutkan dalam air suling bebas CO2
hingga 100 ml (Depkes RI, 1978).
3.4.4 Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida, kemudian dilarutkan dalam air suling hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu
dilarutkan dalam 10 ml air suling. Kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml. (Depkes RI, 1978).
3.4.5 Pereaksi Mollish
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100 ml
(Depkes RI, 1978).
3.4.6 Pereaksi Dragendorf
Sebanyak 0,8 g bismut nitrat dilarutkan dalam asam nitrat pekat 20 ml
kemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam 50 ml air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih diambil dan diencerkan dengan air suling secukupnya hingga 100 ml (Depkes RI,
1978).
3.4.7 Larutan Kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air suling (Depkes, 1979).
3.4.8 Larutan Pereaksi Asam Sulfat 2 N
3.4.9 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya kemudian ditambahkan 2 g iodida sedikit demi sedikit cukupkan dengan air suling
(Depkes RI, 1978).
3.4.10 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrit dengan 5 ml asam sulfat
pekat tambahkan etanol hingga 50 ml (Merck, 1978).
3.4.10 Larutan Pereaksi DPPH 0,5 mM
Sebanyak 19,7 mg DPPH ditimbang, kemudian dilarutkan dalam metanol hingga volume 100 ml.
3.5 Pemeriksaan Karakteristik Simplisia 3.5.1 Pemeriksaan Makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar dari
simplisia bunga brokoli.
3.5.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia bunga
brokoli. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan tutup dengan kaca penutup, kemudian diamati di bawah
mikroskop.
3.5.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen).
a. Penjenuhan Toluen
Sebanyak 200 ml toluena dan 2 ml air suling dimasukkan ke dalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan Kadar Air Simplisia
Kemudian kedalam labu tersebut dimasukkan 5 gram serbuk simplisia yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah
toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan
toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume
air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1992).
3.5.4 Penetapan Kadar Sari yang Larut dalam Air
Sebanyak 5 gram serbuk simplisia dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan
persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di
udara (Depkes RI, 1995).
3.5.5 Penetapan Kadar Sari yang Larut dalam Etanol
Sebanyak 5 gram serbuk simplisia dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk menghindari
penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan
pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.5.6 Penetapan Kadar Abu Total
Sebanyak 2 gram serbuk yang telah digerus dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada suhu 600oC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh
bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.5.7 Penetapan Kadar Abu yang Tidak Larut dalam Asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
3.6. Skrining Fitokimia
Skrining fitokimia dilakukan menurut Depkes (1979) dan Farnsworth (1966) untuk mengetahui golongan senyawa alkaloida, glikosida, glikosida
antrakinon, saponin, tanin, dan steroida/triterpenoida. 3.6.1 Pemeriksaan Alkaloida
Ekstrak diitimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam
klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida:
diambil tabung reaksi, lalu kedalamnya dimasukkan 0,5 ml filtrat. Pada masing-masing tabung reaksi :
1. ditambahkan 2 tetes pereaksi Mayer
2. ditambahkan 2 tetes pereaksi Bouchardat 3. ditambahkan 2 tetes pereaksi Dragendorff
Alkaloida positif jika terjadi endapan atau kekeruhkan pada paling sedikit dua hari tiga percobaan diatas (Depkes, 1978).
3.6.2 Pemeriksaan Flavonoida
Sebanyak 10 g ekstrak ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g
serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan Glikosida
Ekstrak ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran
didinginkan dan disaring. Diambil 20 ml filrat ditambahkan 25 ml air suling dan
25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran isopropanol dan kloroform (2:3), dilakukan
berulang sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 50 C. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut: 0,1 ml larutan percobaan dimasukan dalam
tabung reaksi dan diuapkan diatas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Mollish. Kemudian secara perlahan-lahan ditambahkan 2 ml
asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan glikosida (Depkes, 1978).
3.6.3.1 Pemeriksaan Glikosida antrakinon
Ekstrak ditimbang sebanyak 0,2 g, kemudian ditambahkan 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena,
dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring, kocok lapisan benzena dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzena tidak berwarna menunjukan adanya antrakinon (Depkes, 1978).
3.6.4 Pemeriksaan Saponin
Ekstrak ditimbang sebanyak 0,5 g dan dimasukan ke dalam tabung
reaksi, lalu ditambahkan 10 ml air panas, dinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2N
3.6.5 Pemeriksaan Tanin
Ekstrak ditimbang sebanyak 1 g, dididihkan selama 3 menit dalam 100 ml air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1-2 tetes
peraksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukan adanya tanin (Depkes, 1978)
3.6.6 Pemeriksaan Steroida/Triterpenoida
Sebanyak 1 g sampel dimaserasi dengan 20 ml n-heksan selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan beberapa
tetes pereaksi Liebermann-Burchard. Timbulnya warna biru atau biru hijau menunjukan adanya steroida, sedangkan warna merah, merah muda atau ungu
menunjukkan adanya triterpenoida (Harborne, 1987). 3.7 Pembuatan Ekstrak Etanol Bunga Brokoli
Pembuatan ekstrak etanol bunga brokoli dilakukan dengan cara perkolasi. Prosedur pembuatan ekstrak: sebanyak 200 g serbuk simplisia dibasahi dengan
etanol 70 % dan dibiarkan selama 3 jam. Kemudian dimasukkan ke dalam alat perkolator, lalu dituang cairan penyari etanol sampai semua simplisia terendam
dan terdapat selapis cairan penyari diatasnya, mulut tabung perkolator ditutup dengan alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan dibiarkan tetesan ekstrak mengalir dengan kecepatan perkolat diatur 1 ml /menit,
perkolat ditampung. Perkolasi dihentikan pada saat beberapa tetes perkolat tidak bereaksi ketika ditambahkan serbuk Mg dan asam klorida pekat, kemudian
3.8 Pembuatan Fraksi Ektrak Bunga Brokoli
Pembuatan fraksi ekstrak bunga brokoli dilakukan dengan perkolasi bertingkat. Prosedur pembuatan ekstrak: sebanyak 200 g serbuk simplisia dibasahi
dengan n-heksan dan dibiarkan selama 3 jam. Kemudian dimasukkan ke dalam alat perkolator, lalu dituang cairan penyari n-heksan sampai semua simplisia terendam dan terdapat selapis cairan penyari diatasnya, mulut tabung perkolator
ditutup dengan alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan dibiarkan tetesan ekstrak mengalir dengan kecepatan perkolat diatur 1
ml/menit, perkolat ditampung. Perkolasi dihentikan pada saat beberapa tetes perkolat tidak bereaksi ketika ditambahkan serbuk Mg dan asam klorida pekat, kemudian dipekatkan dengan alat penguap vakum putar setelah itu di freeze dryer
hingga diperoleh ekstrak kental. Ampas dikeringkan lalu diekstraksi dengan menggunakan pelarut berturut-turut etil asetat dan etanol dengan prosedur yang
sama dengan di atas. Bagan pembuatan fraksi ekstrak dapat dilihat pada gambar 14 halaman 37 (DepKes RI, 1979).
3.9 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel 3.9.1 Prinsip Metode Aktivitas Antiradikal Bebas DPPH
Kemampuan sampel uji dalam meredam proses oksidasi DPPH
(1,1-diphenyl-2-picryl-hidrazyl) sebagai radikal bebas dalam larutan metanol (sehingga
terjadi peredaman warna ungu DPPH) dengan nilai IC50 (konsentrasi sampel uji
yang mampu meredam radikal bebas sebesar 50%) digunakan sebagai parameter
untuk menentukan aktivitas antioksidan sampel uji tersebut.
3.9.2 Pembuatan Larutan Blanko