Lampiran 1. Hasil Karakterisasi Edible Film
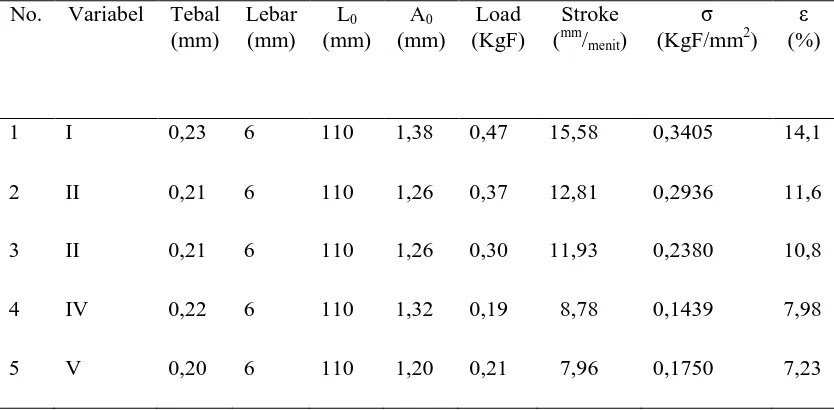
Tabel 1. Hasil Karakterisasi Edible Film
No. Variabel Tebal (mm)
Lebar (mm)
L0 (mm)
A0 (mm)
Load (KgF)
Stroke (mm/menit)
σ
(KgF/mm2)
ε
(%)
1 I 0,23 6 110 1,38 0,47 15,58 0,3405 14,1 2 II 0,21 6 110 1,26 0,37 12,81 0,2936 11,6 3 II 0,21 6 110 1,26 0,30 11,93 0,2380 10,8 4 IV 0,22 6 110 1,32 0,19 8,78 0,1439 7,98 5 V 0,20 6 110 1,20 0,21 7,96 0,1750 7,23
Keterangan: σ : Kuat tarik edible film (KgF/mm2)
No. Wavelength Absorbance Description
Lampiran 2. Hasil Analisa β-Karoten Dengan Spektroskopi UV
Lampiran 2.1 Hasil Spektroskopi UV Edible film dari 10 ml Ekstrak Kulit Manggis, 31 ml Air, 6 g Tepung tapioka, 2% Kitosan, dan 2 ml Gliserin
Spectrum Point Pick Report
07/16/2014 01:16:08 PM Data Set: sampel 6 g pati+ ekstrak kulit manggis - RawData1.50744
Wavelength Range (nm.): 200.00 to 500.00 Scan Speed: Medium Sampling Interval: 1.0
Auto Sampling Interval: Disabled Scan Mode: Auto Instrument Properties
Instrument Type: UV-1800 Series Measuring Mode: Absorbance
No. Wavelength Absorbance Description 1 446.00 0.07947
A
bs
.
Lampiran 2.2 Hasil Spektroskopi UV Edible film dari 10 ml ekstrak kulit manggis,
30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin
Spectrum Point Pick Report
07/16/2014 01:17:38 PMData Set: 7 g pati + ekstrak kulit manggis - RawData
0.57158
Wavelength Range (nm.): 200.00 to 500.00 Scan Speed: Medium Sampling Interval: 1.0
Auto Sampling Interval: Disabled Scan Mode: Auto Instrument Properties
Instrument Type: UV-1800 Series Measuring Mode: Absorbance
Slit Width: 1.0 nm Light Source Change
Lampiran 3. Hasil Analisa Permukaan Dengan SEM
Gambar 3.1 Hasil SEM Edible film dari 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin
Lampiran 4. Hasil Analisa Gugus Fungsi Dengan FT-IR
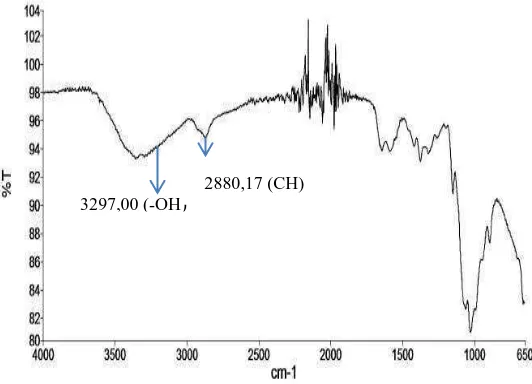
Gambar 4.1 Grafik FT-IR Tepung tapioka
Gambar 4.2 Grafik FT-IR Gliserin
3297,98 (-OH)
3297,00 (-OH)
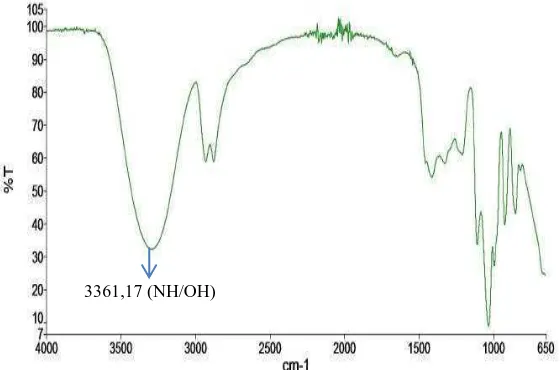
Gambar 4.3 Grafik FT-IR Kitosan
Gambar 4.4 Grafik FT-IR Edible film dari 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin
3361,17 (NH/OH)
3294,37 (-OH)
2930,49 (CH)
3500 3000 2500 2000 1500
Gambar 4.5 Grafik FT-IR Edible film dari 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin
3297,61 (-OH)
Lampiran 5. Gambar Penelitian
Lampiran 5.1 Kulit Buah Manggis
Gambar 5.1 kulit buah manggis
Lampiran 5.2 Edible film
Gambar 5.2. Edible film dari 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin
Lampiran 5.3 Uji Kadar Nutrisi Edible film meliputi Kadar Air, Kadar Abu, Kadar Lemak, Kadar Protein, Kadar Karbohidrat dan Analisa β-Karoten
Gambar 5.4 Uji kadar air Gambar 5.5 Uji kadar abu
Gambar 5.6 Uji kadar protein metode kjeldhal
DAFTAR PUSTAKA
Agoes,G. (2007). Teknologi Bahan Alam. Bandung : Penerbit ITB Press.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta : Direktorat Jendral Pengawasan Obat dan Makanan.
Gontard,N.,Guilbert,S. dan Cuq,J.L. 1993. Water and Glyserol as Plasticizer Affect Mechanical and Water Barrier Properties at an Edible Wheat Gluten Film. USU : J. Food Science.
Hafdani, F.N. and Sadeghinia. N., 2011. A Review on Application of Chitosan as
a Natural Antimicrobial. World Academy of Science. Engineering and
Technology, 50.
Henriette, M.C. Azeredo, de Britto, D. and Assis., O.B.G., 2010. Chitosan Edible Films and Coating – Review, Embrapa Tropical Agroindustry, Brazil : Fortaleza CE.
Hui,Y.H. 2006. Handbook of food Science, Technology, and Enggineering. Volume I. USA: CRC Press.
Khopkar. 2010. Konsep Dasar Kimia Analitik. Jakarta: Penerbit Universitas Indonesia .
Krochta, J.M.; E.A. Baldwin and M.Nisperos-Carriedo (Eds.). 1994. Edible Coatings and Films to Improve Food Quality. Lancaster: Technomic Pub. Co,Inc.
Minner,C.S. 1953. Glyserol. New York: Reinhold Publishing Corporation.
Nazaruddin. 1994. Buah Komersial. Jakarta: Penebar Swadaya.
Rismayani. 2007. Usaha tani dan Pemasaran Hasil Pertanian. Medan: USU Press.
Sagala,S.T. 2013. Karakterisasi Pembuatan Edible Film Dari Campuran Tepung Rumput Laut (Eucheuma sp.) Kitosan dan Gliserin.[Skripsi]. Medan : Universitas Sumatera Utara, Departemen Kimia.
Sediaoetama,A.D. 1989. Ilmu Gizi. Jilid I. Jakarta: Penerbit Dian Rakyat.
Stevens,M.P. 2000. Kimia Polimer. Cetakan Pertama. Jakarta: Pradnya Paramita
Sudarmadji,S. 1992. Analisa Bahan Makanan dan pertanian. Jakarta: Erlangga.
Sugita.P. 2009.Kitosan: Sumber biomaterial masa depan. Bogor: IPB Press.
Sunarjono,H. 2000. Prospek Berkebun Buah. Jakarta: Penebar Swadaya.
Wahyu.M.K. 2008.Pemanfaatan Pati Singkong Sebagai Bahan Baku Edible Film. Bandung. UNPAD Press
Winarno,F.G. 1992. Pengantar teknologi Pangan. Jakarta: PT. Gramedia.
Wirjosentono,B. 1995. Perkembangan Polimer di Indonesia. Orasi Ilmiah Lustrum 6.Medan : Universitas Sumatera Utara.
Yuliarti,N. 2007. Awas Bahaya Dibalik Lezatnya Makanan. Yogyakarta: ANDI Offset.
BAB 3
- Neraca analitis Mettler Toledo
- Gelas beaker Pyrex
- Labu takar Permacolor
- Gelas ukur Pyrex
- Thermometer YZ
- Alat Torse Tokyo test Machine
- Alat SEM (Scanning Electron Microscopy) JSM-6360
- Alat Spektrofotometer FT-IR
- Alat Spektroskopi UV
- Labu alas Pyrex
- Gelas Erlenmeyer Pyrex
- Pipet volumetrik Pyrex
- Buret Pyrex
- Tanur Memmert
- Alat Soklet Gerhard Born
- Kertas saring Whatman no. 41
- Tepung tapioka Sanghee
3.2 Prosedur Penelitian 3.2.1 Pengambilan Sampel
Sampel berupa manggis yang diperoleh dari Pasar sore, Padang bulan Medan, buah manggis memiliki nama latin Garcinia mangostana L. Proses preparasi sampel dilakukan dengan mengekstraksi kulit manggis dengan metode ekstraksi maserasi (perendaman) dengan menggunakan pelarut etanol dan air dengan perbandingan 1 : 2 sehingga menghasilkan filtrat kulit manggis.
3.2.2 Pembuatan Larutan Pereaksi 3.2.2.1 Pembuatan larutan CH3COOH 1%
Dipipet 1 mL larutan CH3COOH glasial kemudian dimasukkan kedalam labu
takar 100 mL. diencerkan dengan aquadest hingga garis tanda.
3.2.2.2 Pembuatan larutan kitosan 2%
Ditimbang 1 g kitosan kemudian dimasukkan kedalam gelas beaker. Ditambahkan
50 mL larutan CH3COOH1% . Didiamkan selama ± 1 jam hingga seluruh kitosan
larut.
3.2.3 Cara Kerja 3.2.3.1 Preparasi Sampel
Buah manggis dikupas dan diambil kulit bagian dalamnya kemudian diekstraksi dengan menggunakan pelarut etanol dan air (perbandingan 1:2) dan dihaluskan dengan blender, diendapkan selama 24 jam kemudian disaring dan dipanaskan pada suhu 90-950C selama 10 menit untuk menguapkan etanol kemudian didinginkan pada suhu kamar dan diperoleh ekstrak kulit buah manggis.
3.2.3.2 Pembuatan Edible Film
manggis sambil diaduk hingga homogen. Kemudian ditambahkan larutan kitosan 2% dan 2 mL gliserin. Diaduk hingga homogen dan dibiarkan mengental. Campuran dituang ke plat akrilik dan diratakan. Dikeringkan didalam oven pada suhu ± 40oC selama ± 2 hari. Dilakukan prosedur yang sama untuk tepung tapioka dengan variasi 4 g, 5 g, 6 g, dan 7 g dan akuades dengan variasi 33 ml, 32 ml, 31 ml, dan 30 ml.
3.2.4 Pengukuran Ketebalan Edible Film
Edible film yang diperoleh dipotong dengan ukuran 10 cm x 10 cm, kemudian dilakukan pengukuran dengan menggunakan jangka sorong sebanyak lima kali dari lima sisi, yaitu sudut sisi kiri atas, sudut sisi kanan atas, sudut sisi kiri bawah, sudut sisi kanan bawah dan tengah. Kemudian, dicari rata-rata dari ketebalan tersebut.
3.2.5 Pengukuran Kuat Tarik dan Kemuluran
Kekuatan tarik adalah salah satu sifat dasar dari bahan polimer yang terpenting dan sering digunakan untuk karakteristik suatu bahan polimer. Kekuatan tarik suatu bahan didefinisikan sebagai besarnya beban maksimum (Fmaks) yang
digunakan untuk memutuskan spesimennya bahan dibagi dengan luas penampang awal (A0).
Keterangan :
σ = kekuatan tarik bahan (kgf/mm2)
F = tegangan maksimum ( kgf )
Keterangan:
ɛ = Kemuluran (%)
I0 = Panjang spesimen mula-mula (mm)
It = Panjang spesimen setelah diberi beban (mm)
3.2.6 Analisa SEM (Scanning Electron Microscopy
SEM (Scanning Electron Microscopy) adalah alat yang dapat membentuk bayangan permukaan spesimen secara makroskopik. Berkas elektron dengan diameter 5-10 nm diarahkan pada spesimen interaksi berkas elektron dengan spesimen menghasilkan beberapa fenomena yaitu hamburan balik berkas elektron, sinar x, elektron sekunder, absorbansi elektron.
Dalam hal ini, dilihat permukaan dari pencampuran tepung tapioka dengan ekstrak kulit manggis, kitosan dan gliserin berdasarkan sifat mekanik edible film yang optimal.
3.2.7 Analisa FT – IR (Fourier Transform Infra Red)
3.2.8 Penentuan Kadar Nutrisi 3.2.8.1. Penentuan kadar air
Edible film ditimbang sebanyak 1-2 g dalam cawan timbang yang telah diketahui
beratnya. Dikeringkan di dalam oven pada suhu 1050 C selama 3 jam.Didinginkan di dalam desikator. Kemudian ditimbang hingga diperoleh bobot tetap.
3.2.8.2. Penentuan kadar abu
Edible film ditimbang sebanyak 2 g dalam sebuah cawan porselen yang telah
diketahui beratnya. Dikeringkan di dalam oven. Diabukan di dalam tanur pengabuan pada suhu maksimum 6000 C selama 3 jam. Didinginkan dalam desikator. Kemudian ditimbang hingga diperoleh bobot tetap.
3.2.8.3. Penentuan kadar lemak
Edible film ditimbang sebanyak 2 g, dimasukkan kedalam selongsong kertas yang
3.2.8.4. Penentuan kadar protein
Edible film ditimbang sebanyak 2 g dan dimasukkan kedalam labu kjeldhal 100
ml. tambahkan 2 g selenium dan 25 ml H2SO4(p). dipanaskan di atas pemanas
listrik atau api pembakar sampai mendidih dan larutan menjadi jernih
kehijau-hijauan (sekitar 2 jam). dibiarkan dingin, kemudian dimasukkan kedalam labu ukur 100 ml dan diencerkan dengan aquadest hingga garis tanda. Dipipet 50 ml NaOH(aq) 40 % dan 1-2 tetes indikator campuran. disuling selama lebih kurang 10
menit. ditampung NH3(g) di dalam gelas Erlenmeyer yang berisi 10 ml larutan
borat 2 % yang telah dicampur indikator. Bilas ujung pendingin dengan aquadest. Titrasi dengan larutan HCl 0,1 N.
3.2.8.5. Penentuan Kadar Karbohidrat (by difference)
Penentuan karbohidrat (termasuk kadar serat) secara by difference dihitung sebagai 100 % dikurangi kadar air, abu, protein, dan lemak (Winarno F.G., 1992).
)
3.2.8.6. Penentuan Kadar β-Karoten
Sebanyak 0,1 g edible film dilarutkan dengan akuades dalam labu takar 25 mL. Diencerkan hingga garis tanda kemudian dihomogenkan. Dimasukkan ke dalam
kuvet kemudian diukur absorbansinya pada panjang gelombang 446 nm dengan menggunakan alat spektroskopi UV. Dicatat absorbansinya. Kemudian dihitung nilai beta karotennya dengan menggunakan rumus:
3.2.8.7. Penentuan Nilai Organoleptik
Uji ini meliputi warna, bau, rasa dan tekstur yang ditentukan dengan uji kesukaan
oleh 15 orang panelis, dimana para panelis bukan perokok dan sebelum mencicipinya diharuskan minum air putih terlebih dahulu. Uji ini ditentukan
dengan skala hedonik sebagai berikut:
Tabel 3.1 Skala Hedonik Uji Organoleptik
Uji Kesukaan (skala hedonik) Skala numerik
Amat sangat suka 5
Sangat suka 4
Suka 3
Kurang suka 2
3.3 Bagan Penelitian 3.3.1 Preparasi Sampel
dibersihkan diiris tipis–tipis
dicampurkan dengan etanol dan air dengan perbandingan 1 : 2 ( 50 ml : 100 ml ) dihancurkan dengan blender
diendapkan selama 24 jam disaring
dipanaskan pada suhu 90-95 o C selama 10 menit didinginkan pada suhu kamar
Kulit manggis
filtrat residu
3.3.2 Pembuatan Edible Film
Ditimbang sebanyak 3 g
Dimasukkan kedalam gelas beaker Ditambahkan 34 mL aquadest Dipanaskan diatas hotplate (± 650C)
Ditambahkan 10 mL ekstrak kulit manggis
Ditambahkan larutan kitosan 2% ( )
Ditambahkan 2 mL gliserin
Diaduk hingga homogen dan mengental
Dituang ke plat akrilik dan diratakan Dikeringkan didalam oven (±40oC)
catatan: dilakukan hal yang sama untuk tepung tapioka 4, 5, 6, 7 gram dengan variasi penambahan aquades
Tepung Tapioka
Edible Film Larutan Putih
3.3.3 Pengujian Edible Film
Uji Fisik Edible Film Uji Nutrisi
Uji SEM Uji FT-IR Kuat Tarik dan
Kemuluran Pengukuran Ketebalan
Kadar Karbohidrat Kadar Protein Kadar Lemak Kadar Abu
Kadar Air
3.3.3.1 Analisa kadar nutrisi Edible Film
3.3.3.1.1 Penentuan kadar abu
Dimasukkan kedalam cawan porselen yang telah diketahui beratnya
Dipanaskan dalam tanur pada suhu 6000 C selama 3 jam hingga diperoleh abu berwarna keputih-putihan
Abu
Diulangi sampai diperoleh berat Dihitung kadar abunya
Didinginkan dalam desikator Ditimbang
2 g edible film
3.3.3.1.2 Penentuan kadar lemak
Lemak
Didinginkan di dalam desikator
Ditimbang sampai berat konstan
Dihitung kadar lemaknya
Hasil
Dimasukkan ke dalam gelas beaker
Ditambahkan 30 ml HCl(aq) 25% dan 20 ml aquadest serta
beberapa butir batu didih
Dibungkus dengan paper thimbal
Disaring dalam keadaan panas dan cuci dengan aquadest panas hingga tidak bereaksi asam lagi
Ditutup gelas beaker dengan kaca arloji dan dididihkan selama 15 menit
Dimasukkan kedalam alat soklet
Dikeringkan kertas saring berikut isinya pada suhu 100-1050 C
Diekstraksi dengan larutan heksana selama 2-3 jam pada suhu ± 800C
Didestilasi larutan heksana dari ekstrak lemak pada suhu 100-1050C
3.3.3.1.3 Penentuan kadar protein
Dimasukkan kedalam labu kjeldhal 100 ml
Larutan jernih kehijau-hijauan
Dibilas ujung pendingin dengan aquadest Didestilasi selama lebih kurang 10 menit Ditunggu sampai larutan dingin
Ditambahkan 50 ml NaOH(aq) 40%
Ditambahkan 2 g campuran selenium dan 25 ml H2SO4(p)
Dipipet 50 ml larutan yang telah diencerkan dan dimasukkan ke dalam alat destilasi
Dimasukkan ke dalam labu ukur 100 ml dan diencerkan dengan aquadest
Dipanaskan diatas pemanas listrik atau api pembakar sampai mendidih dan larutan menjadi jernih kehijauan
Ditampung destilat di dalam 10 ml larutan asam borat 2% yang telah dicampur dengan indikator
Dititrasi dengan larutan HCl(aq) 0,1 N
Larutan ungu
Hasil
Dihitung % N Destilat dalam asam borat 2%
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Dari hasil penelitian karakterisasi edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin yang telah dilakukan, diperoleh karakteristik dan kandungan nutrisi edible film sebagai berikut :
Tabel 4.1. Hasil Analisa Karakteritik Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin
No . Parameter Penambahan Tepung tapioka
6 g 7 g
1. Kuat tarik 0,2936 KgF/mm2 0,3405 KgF/mm2
2. Ketebalan 0,21 mm2 0,23 mm2
3. Kemuluran 11,6 % 14,1 %
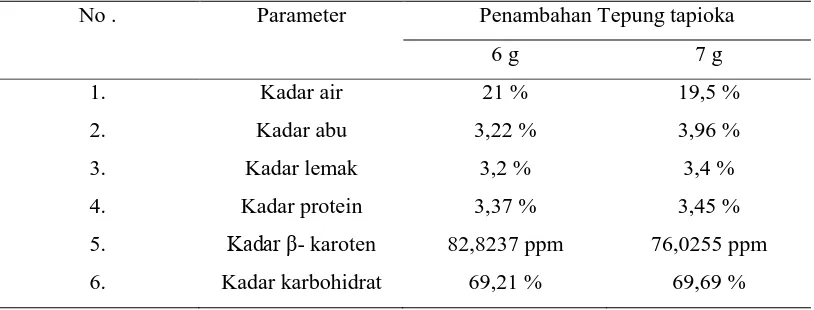
Tabel 4.2. Hasil Analisa Kandungan Nutrisi Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin
No . Parameter Penambahan Tepung tapioka
6 g 7 g
1. Kadar air 21 % 19,5 %
2. Kadar abu 3,22 % 3,96 %
3. Kadar lemak 3,2 % 3,4 %
4. Kadar protein 3,37 % 3,45 %
5. Kadar β- karoten 82,8237 ppm 76,0255 ppm
4.1.1. Hasil Analisa Kuat Tarik Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
Penentuan kuat tarik Edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut :
Kuat Tarik =
Panjang sampel mula-mula (lo) : 110 mm
4.1.2. Hasil Analisa Kadar Air Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
Penentuan Kadar air Edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut:
Kadar Air = 100%
Berat cawan + berat sampel edible film setelah kering : 52,79 g
Berat uap air yang hilang = (Berat cawan + Berat edible film dari ekstrak kulit manggis) – (Berat cawan + Berat sampel dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
Penentuan Kadar abu Edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut:
Kadar abu = 2 1100%
Dimana, Mo : Berat Sampel (g)
M1 : Berat Crusible Kosong (g) M2 : Berat Crusible + Abu (g) dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
N.A = 0,014 100%
V = volume HCl untuk titrasi sampel
fp = faktor pengenceran
4.1.5. Hasil Analisa Kadar Lemak Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
Penentuan Kadar lemak Edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut:
%
W1 = Berat sampel + labu setelah ekstraksi
W2 = Berat labu kosong
Berat Sampel : 5 g
Berat Labu kosong : 156,53 g
Berat Sampel + labu setelah ekstraksi : 156,80 g
Kadar Lemak = 100% Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
Penentuan Kadar karbohidrat Edible film dari ekstrak kulit manggis dengan penambahan tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut:
% Karbohidrat = 100% - (% Protein + % Lemak + % Air + % Abu)
% Karbohidrat = 100% - (3,45%+3,4%+19,5%+3,96%)
4.1.7. Hasil Analisa Kadar β-Karoten Edible film dari Ekstrak Kulit Manggis dengan Tepung tapioka, Kitosan dan Gliserin pada Penambahan Tepung tapioka sebanyak 7 g
β-karoten Edible film dari ekstrak kulit manggis, tepung tapioka, kitosan dan gliserin dapat dihitung sebagai berikut:
Kadar β-karoten =
Absorbansi pada panjang gelombang 446 nm ( diperoleh dari hasil Spektroskopi
UV ) = 0,0794
4.1.8. Hasil Analisa SEM (Scanning Electron Microscopy)
Hasil pemeriksaan SEM menunjukkan bentuk permukaan dari edible film ekstrak kulit manggis, tepung tapioka, kitosan, dan gliserin sebagai pemlastis . Dari foto/gambar SEM menunjukkan hasil terbaik pada pembuatan edible film dengan penambahan tepung tapioka yaitu pada penambahan 7 g tepung tapioka, 2%
4.1.9. Hasil Analisa FT-IR (Fourier Transform Infra Red)
4500 4000 3500 3000 2500 2000 1500 1000 500 3361,17
Gambar 4.1 Spektrum Senyawa Hasil Penelitian dengan FT-IR
Table 4.3 Interpretasi Gugus Fungsi Senyawa Hasil Analisis FT-IR
Gugus Fungsi Frekuensi (cm-1) Hasil Frekuensi (cm-1) Teori
CH
4.1.10. Hasil Analisa Organoleptik Edible film dari Ekstrak Kulit Manggis dengan Penambahan Tepung tapioka, Kitosan dan Gliserin
Berdasarkan uji organoleptik edible film dari ekstrak kulit manggis,dengan penambahan tepung tapioka, kitosan dan gliserin kepada panelis dapat dilihat hasilnya dalam grafik sebagai berikut :
4.2 Pembahasan Penelitian 4.2.1 Analisa Kuat Tarik
Berdasarkan hasil pengukuran kuat tarik, edible film yang dihasilkan dari penelitian dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung memberikan hasil kuat tarik bagus. Hal ini dikarenakan proses pencampuran yang merata dan lebih stabil, serta gaya intermolekul antara penyusun tepung tapioka yang saling menguatkan sehingga edible film yang dihasilkan lebih kuat dan tidak mudah patah ketika ditarik.
4.2.2 Persen Kemuluran dan Ketebalan
Berdasarkan hasil uji kemuluran, edible film dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin dihasilkan persen kemuluran sebesar 11,6 %. Sedangkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 14,1 %. Dari hasil tersebut dapat dilihat bahwa edible film dengan penambahan 7 g tepung tapioka menghasilkan % kemuluran yang lebih tinggi. Hal ini dikarenakan semakin tinggi kuat tarik dari edible film maka akan semakin tinggi juga persen kemuluran dari edible film tersebut.
Hal ini dikarenakan makin tinggi konsentrasi tepung tapioka yang ditambahkan maka ketebalan edible film makin meningkat dan juga semakin tinggi volume air yang ketika digunakan akan mengalami pengurangan ketika di panaskan sehingga menyebabkan permukaan edible film semakin menipis atau berkurang ketebalannya.
4.2.3 Analisa Kadar Air
Kadar air edible film yang dihasilkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin yaitu sebesar 19,5 %. sedangkan pada variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin diperoleh kadar air yang lebih besar yaitu 21%, untuk itu edible film dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin memiliki kelembaban yang lebih besar sehingga tidak layak untuk dijadikan edible film.
Nilai kadar air yang tinggi akan menyebabkan mudahnya bakteri untuk berkembang biak dan mengakibatkan kontaminasi sehingga akan terjadi perubahan pada bahan pangan dan edible film tidak layak pakai.
4.2.4 Analisa Kadar Abu
4.2.5 Analisa Kadar Protein
Kadar protein yang dihasilkan pada edible film dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 3,37 % sedangkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 3,45 %. Kadar protein ini dapat dipengaruhi oleh suhu, pH, dan kelembaban udara.
Dari hasil yang diperoleh kadar protein dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin lebih rendah. Hal ini dikarenakan pengaruh kadar air yang terdapat pada edible film. Kadar air edible film pada penambahan 6 g tepung tapioka tinggi. Sehingga kadar protein pada perbandingan ini nilainya lebih rendah. Hal ini disebabkan karena tingginya kadar air maka kecepatan reaksi hidrolisis protein oleh enzim pada
edible film akan semakin cepat.
Pada proses hidrolisis tersebut akan mengakibatkan gugus N yang terdapat pada edible film akan terbebaskan. Gugus N tersebut akan berubah menjadi nitrit. Karena kadar nitrit pada analisa protein tidak terdeteksi. Akibatnya kadar protein pada edible film dengan variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin menurun.
4.2.6 Analisa Kadar Lemak
Kadar lemak yang dihasilkan pada variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 3,2 % sedangkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 3,4 %. Dari hasil tersebut, kadar lemak pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin lebih tinggi. Hal ini dikarenakan tepung tapioka mengandung lemak sehingga semakin banyak ditambahkan tepung tapioka maka komposisi lemak pada edible
4.2.7 Analisa Kadar Karbohidrat
Kadar karbohidrat yang dihasilkan pada variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 69,21 % sedangkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 69,69%. Kadar karbohidrat ini diperoleh karna adanya penambahan tepung tapioka pada edible film. Semakin banyak penambahan tepung tapioka maka semakin banyak kandungan karbohidrat pada
edible film yang dihasilkan.
4.2.8 Analisa Kadar β-Karoten
Kadar β-karoten yang dihasilkan pada variasi 10 ml ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 82,8237 ppm, sedangkan pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin adalah 76,0255 ppm. Kandungan β-karoten tersebut
berasal dari ekstrak kulit manggis yang dipakai sebagai bahan dasar pembuatan
edible film. Tapi dengan pemanasan pada suhu yang tinggi akan merusak kadar β -karoten. Dari hasil diperoleh edible film dengan variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin terigu lebih rendah. Hal ini dikarenakan penambahan tepung tapioka yang terlalu banyak sehingga membutuhkan proses pemanasan yang lebih lama dan mengakibatkan kadar β-karoten nya berkurang.
4.2.9 Analisa SEM (Scanning Electron Microscopy)
Hasil yang diperoleh pada analisa SEM dapat disimpulkan bahwa pada
edible film dengan variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung
tapioka, 2% kitosan, dan 2 ml gliserin memperlihatkan morfologi permukaan dari
edible film yang lebih teratur dan compatible dibandingkan pada variasi 10 ml
ekstrak kulit manggis, 31 ml air, 6 g tepung tapioka, 2% kitosan, dan 2 ml gliserin. Hal ini disebabkan proses pencampuran yang merata sehingga menghasilkan morfologi edible film yang teratur dan memiliki pori-pori yang rapat.
4.2.10 Analisa FTIR (Fourier Transform Infra Red)
Dari lampiran 4.1 memberikan spektrum dengan serapan pada daerah 3297,98cm
-1 menunjukkan adanya gugus hidroksil (OH) yang berasal dari unit α
-glukosa, dari lampiran 4.2 memberikan spektrum dengan serapan pada daerah 3297,00 cm
-1
menunjukkan adanya gugus hidroksil (OH) yang berasal dari gliserin serta
serapan pada daerah bilangan gelombang 2880,17 cm-1 menunjukkan adanya CH
alifatis, pada lampiran 4.3 memberikan spektrum dengan serapan pada daerah 3361,17 cm-1 menunjukkan adanya gugus hidroksil (OH) atau gugus -NH, lampiran 4.5 yaitu edible film dengan uji mekanik optimal pada penambahan 7 g tepung tapioka memberikan spektrum dengan serapan pada daerah 3297,61 cm-1 menunjukkan adanya gugus hidroksil (OH) atau gugus –NH, lampiran 4.4 yaitu
edible film pada penambahan 6 g tepung tapioka memberikan spektrum dengan
serapan pada daerah 3294,37 cm-1 menunjukkan adanya gugus hidroksil (OH) atau gugus –NH. Hal ini menunjukkan adanya interaksi antara tepung tapioka, kitosan dan gliserin pada edible film yang dibuat.
4.2.11 Uji Organoleptik
Dari hasil penelitian diperoleh edible film dengan variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin dengan rata-rata 3,07 (suka) karena semakin meningkat penambahan tepung tapioka pada
edible film akan mengakibatkan tekstur edible film tersebut lebih halus.
Untuk uji organoleptik terhadap warna, edible film dengan penambahan 6 g tepung tapioka lebih disukai dengan rata-rata 3,4 (suka) karena warnanya lebih cerah, merata dan lebih menarik. Sedangkan pada penambahan 7 g tepung tapioka warnanya sedikit lebih gelap karena lebih banyak penambahan tepung tapioka. Penambahan tepung tapioka yang lebih banyak membuat edible film berwarna gelap.
Uji organoleptik terhadap rasa, menurut (Soekarto, 1985) rasa makanan yang kita kenal sehari-hari sebenarnya bukanlah satu tanggapan, melainkan campuran dari tanggapan cicip, bau yang diramu oleh kesan-kesan seperti penglihatan, sentuhan, dan pendengaran. Peramuan rasa itu ialah suatu sugesti
kejiwaan terhadap makanan yang menetukan nilai pemuasan orang yang memakannya. Edible film dengan penambahan 6 g tepung tapioka disukai dengan rata-rata 3,2 (suka). Hal ini dikarenakan edible film yang dihasilkan memiliki rasa yang renyah dan sedikit manis.
Uji organoleptik terhadap aroma, Menurut Kartika (1988) bau atau aroma dapat didefenisikan sebagai sesuatu yang dapat diamati dengan indera pembau. Dalam industri pangan pengujian terhadap aroma dianggap penting karena dengan cepat dapat menghasilkan penilaian terhadap produk tentang diterima atau ditolak.
Edible film dengan variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kandungan gizi yang dihasilkan dari edible film yang terbaik adalah pada variasi 10 ml ekstrak kulit manggis, 30 ml air, 7 g tepung tapioka, 2% kitosan, dan 2 ml gliserin menunjukan hasil yang lebih baik karena mengandung nutrisi yang lebih banyak dengan kadar karbohidrat 69,69%, kadar protein 3,45%, kadar lemak 3,4%, kadar abu 3,96%, kadar air 19,5%, dan kadar β-karoten 76,0255 ppm.
Uji organoleptik dari edible film terhadap warna 3,2, rasa 3,07, tekstur 3,07, aroma 3,27 dengan rata-rata 3 (suka) karena edible film berwarna lebih
cerah, rasanya renyah, teksturnya lebih halus dan lebih menarik sehingga edible
film ini lebih disukai oleh panelis.
Karekteristik edible film meliputi kuat tarik yang diperoleh 0,3405 KgF/mm2, kemuluran 14,1 % dan ketebalan 0,23 mm. Dan hasil uji SEM memiliki permukaan yang lebih halus, berpori-pori kecil, dan rapat serta lebih kompatibel.
5.2 Saran
BAB 2
TINJAUAN PUSTAKA
2.1 Manggis
Manggis (Garcinia mangostana L.) merupakan tanaman budidaya didaerah tropis. Tumbuhan ini tumbuh subur pada kondisi dengan banyak mendapat sinar matahari, kelembaban tinggi, dan musim kering yang pendek (untuk menstimulasi pembungaan),pada kondisi kering, diperlukan irigasi untuk menjaga kelembaban tanah. Tumbuhan ini ditanam hingga ketinggian 1000 m dpl (20-400C) di daerah tropis namun pertumbuhan maksimal berlangsung di daerah dataran rendah.
2.1.1 Taksonomi dan Morfologi Manggis
Kedudukan taksonomi dari Garcinia mangostana Linn.yaitu :
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Guttiferanales
Famili : Guttiferae
Genus : Garcinia
Spesies : Garcinia mangostana Linn.
Tanaman yang berasal dari biji umumnya membutuhkan 10-15 tahun untuk mulai berbuah. Tingginya mencapai 10-25 meter dengan ukuran kanopi sedang serta tajuk yang rindang berbentuk piramida. Diameter batang 25-35 cm dan kulit batang kayu biasanya berwarna coklat gelap atau hamper hitam, kasar
dan cenderung mengelupas. Getah manggis berwarna kuning (getah kuning) atau resin ada pada semua jaringan utama tanaman.
Letak daun berhadapan, merupakan daun sederhana dengan tangkai daun pendek yang berhubungan dengan tunas, panjang tangkai daun 1,5 -2 cm dengan helaian daun berbentuk bulat telur, bulat panjang atau elips dengan panjang 15-25cm x lebar 7-13 cm, mengkilap, tebal dan kaku, ujung daun meruncing (acuminate) dan licin (glabrous).
Perkembangan buah manggis di Indonesia sangat menggembirakan. Selama periode tahun 1986-1990 ekspor manggis terus meningkat. Pada tahun 1986 baru mencapai 3,7 ton; tahun berikutnya bertambah menjadi 35,7 ton, tahun 1989 menjadi 278 ton dan tahun 1990 mencapai 357,6 ton. Sementara itu, luas lahan baru diproyeksikan sekitar 194.996 hektar yang tersebar di Pulau Jawa seluas 31.781 ha, Sumatera 106.397 ha, Bali 207 ha, Nusa Tenggara Barat 13.175 ha, Kalimantan 13.773 ha, Sulawesi 26.919 ha, Maluku 2.884 ha dan sebagian luas direncanakan di Irian Jaya (Ashari, 2006).
2.1.2 Kandungan
Komponen terbesar dari buah manggis adalah air, yaitu 83%. Komponen protein dan lemak yang dikandung sangat kecil. Buah manggis mengandung vitamin A, mengandung vitamin B1 dan vitamin C.
Kandungan yang terdapat dalam bagian buah manggis antara lain gula
sakarosa, dekstrosa dan levulosa. Dalam takaran tiap 100 gram kulit buah manggis terdiri dari 79,2 gram air, 0,5 gram protein, 19,8 gram karbohidrat, 0,3 gram serat, 11 mg kalsium, 17 mg fosfor, 0,9 mg besi, 14 IU vitamin A, 82,1 ppm
β-karoten, 0,09 mg vitamin B1 (Thiamin), 0,06 mg vitamin B2 (riboflavin), dan 0,1 mg vitamin B5 (niasin). Kulit buah manggis merupakan bagian buah manggis yang membungkus daging buah. Rasio bagian buah yang dikonsumsi dengan bagian buah yang dibuang, lebih tinggi bagian buah yang dibuang, dalam hal ini kulit buahnya yang mencapai 2/3 bagian buah atau 66,6%.
2.1.3 Khasiat dan Kegunaan
Berbagai hasil penelitian menunjukan kulit buah manggis kaya akan antioksidan, terutama antosianin, xanthone, tannin, dan asam fenolat. Radikal bebas (atom atau kelompok atom yang dalam keadaan bebas alias tidak terikat gugus lain) dapat menangkap molekul hydrogen, asam lemak, logam berat yang pada akhirnya memicu beragamnya penyakit degeneratif.
Oleh sebab itu diperlukan upaya untuk memanfaatkannya. Kendala dalam pemanfaatan kulit buah manggis adalah rasanya pahit.Rasa pahit pada kulit buah manggis tersebut ada kaitannya dengan kandungan tannin yang terdapat didalam jaringan kulit buah manggis. Senyawa tannin merupakan asam tanat, secara teoritis suatu senyawa yang bersifat asam dapat dinetralkan dengan larutan basa, yang akan membentuk garam tannat dan air. Kulit buahnya dapat pula digunakan sebagai bahan membuat cat antikarat (cat berwarna hitam yang tahan cuci). Kulit kayunya dapat digunakan untuk ramuan obat tradisional obat penyakit perut
(Sunarjono, 2000).
2.1.4 Senyawa Antioksidan pada Kulit Buah Manggis
Senyawa antioksidan yang terdapat pada kulit buah manggis antara lain sebagai berikut :
1. Xanton
2. Antosianin
Antosianin adalah kelompok pigmen yang berwarna merah sampai biru yang terdapat pada tanaman. Pigmen ini banyak ditemukan pada buah-buahan, sayuran dan bunga. Pigmen antosianin tergolong kedalam turunan benzopiran. Senyawa antosianin memiliki kemampuan sebagai antioksidan dan berperan cukup penting dalam mencegah penyakit neuronal, kardiovaskuler, kanker dan diabetes.
3.Tanin
Tanin mempunyai rasa sepat dan dapat digunakan dalam menyamak kulit. Tanin terdiri atas berbagai asam fenolat.Beberapa senyawa tanin mempunyai aktivitas antioksidan, menghambat pertumbuhan tumor, dan menghambat enzim seperti reverse transcriptase dan DNA topoisomerase, antidiare, hemostatik, dan antihemoroid (Yunitasari, 2011).
2.2 Ekstraksi
Metode ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara :
1. Maserasi
Maserasi berasal dari kata “macerare” artinya melunakkan. Maserat adalah hasil
2. Perkolasi
Perkolasi adalah suatu cara penarikan memakai alat yang disebut perkolator dimana simplisia terendam dalam cairan penyari, zat-zat akan terlarut dan larutan tersebut akan menetes secara beraturan (Syamsuni, 2006). Keuntungan dari metode perkolasi ini adalah proses penarikan zat berkhasiat dari tumbuhan lebih sempurna, sedangkan kerugiannya adalah membutuhkan waktu yang lama dan peralatan yang digunakan mahal (Agoes, 2007).
3.Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan pelarut akan terdestilasi menuju pendingin dan akan kembali ke labu (Depkes, 2000).
4.Sokletasi
Sokletasi adalah ekstraksi kontinu menggunakan alat soklet, dimana pelarut akan terdestilasi dari labu menuju pendingin, kemudian jatuh membasahi dan merendam sampel yang mengisi bagian tengah alat soklet setelah pelarut mencapai tinggi tertentu maka akan turun ke labu destilasi, demikian berulang-ulang (Depkes, 2000).
2.3. Karotenoid
Berdasarkan daya larutnya dalam pelarut organik, karotenoid dapat digolongkan dalam dua kelompok pigmen, yaitu karoten dan xantofil. Karoten sangat larut dalam petroleum eter dan kurang larut dalam etanol, sedangkan xantofil sebaliknya. Karoten mempunyai susunan kimia yang hanya terdiri dari atom-atom C dan H, sedangkan xantofil terdiri dari atom-atom C, H, dan O.
Molekul karoten terdiri dari gugus isoprenoid. Jumlah atom C pada karoten adalah 40, mempunyai 11 ikatan rangkap dan 10 gugus metil. Karoten banyak terdapat pada wortel, pisang, pepaya, jeruk, buah merica, cabai dan lain-lain. Pada buah semangka dan tomat banyak terkandung karotenoid, khususnya pigmen likopen. Warna kuning pada nenas juga disebabkan adanya pigmen karotenoid.
Gambar. 2.2 Beta-Karoten (Muchtadi, 2010)
Gambar. 2.3 Likopen (Muchtadi, 2010)
Banyak anggapan yang menyatakan bahwa warna bahan makanan yang semakin kuning berarti kadar vitamin A semakin tinggi (beta karoten merupakan provitamin A). Hal ini ternyata tidak selalu benar untuk semua bahan makanan. Contohnya warna kuning dari kuning telur bukan disebabkan oleh karoten, melainkan oleh beta-lutein.
Dalam pengolahan sayuran dan buah-buahan, kerusakan karotenoid selama pemasakan sangat sedikit. Tetapi pada proses pengeringan, adanya kerusakan karotenoid perlu diperhatikan, karena karoten mudah teroksidasi terutama pada suhu yang sangat tinggi. Demikian pula dalam proses penyimpanan, kadar karoten dalam bahan pangan akan menurun. Karena itu pada proses pengeringan dan penyimpanan bahan pangan digunakan lapisan pati untuk melindungi karoten dari proses oksidasi (Muchtadi, 2010).
2.4. Spektrofotometer UV
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi.
Spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang gelombang.
2.5. Kitosan
Kitosan adalah poli - ( 2 – amino – 2 – deoksi –β - ( 1 – 4 ) – D – glukopiranosa ) dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin.
Gambar 2.5 Struktur Polimer Kitosan
Kitosan merupakan padatan amorf yang berwarna putih kekuningan
dengan rotasi spesifik [α]D11
-3 hingga -100 (pada konsentrasi asam asetat 2%). Kitosan larut pada kebanyakan larutan asam organik pada pH sekitar 4,0 tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alkohol,
dan aseton.
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun cara enzimatik. Namun proses kimiawi menghasilkan kitosan dengan bobot molekul yang beragam dan deasetilasinya juga sangat acak. Deasetilasi secara enzimatik bersifat selektif dan tidak merusak struktur rantai kitosan, Sehingga menghasilkan kitosan dengan karakteristik yang lebih seragam agar dapat memperluas bidang aplikasinya (Sugita et al, 2009).
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Dibidang industri, kitin dan kitosan berperan antara lain sebagai koagulan polielektrolit pengolahan limbah cair, pengikat dan penjerap ion logam, mikroorganisme, mikroalga, pewarna, residu pestisida, lemak, tannin, PCB (poliklorinasi bifenil), mineral dan asam organik, media kromatografi afinitas, gel dan pertukaran ion, penyalut berbagai serat alami dan sintetik, pembentuk film dan membran mudah terurai, meningkatkan kualitas kertas, pulp, dan produk tekstil. Sementara dibidang pertanian dan pangan, kitin dan kitosan digunakan antara lain untuk pencampur ransum pakan ternak, antimikroba, anti jamur, serat bahan pangan, penstabil, pembentuk gel, pembentuk tekstur, pengental dan pengemulsi produk olahan pangan, pembawa zat aditif makanan, flavor, zat gizi, pestisida, herbisida, virusida tanaman, dan deasidifikasi buah-buahan, sayuran dan penjernih sari buah. fungsinya sebagai antimikroba dan antijamur juga diterapkan dibidang kedokteran. Kitin dan kitosan dapat mencegah pertumbuhan Candida albicans dan Staphylacoccus aureus. selain itu, biopolymer tersebut juga berguna sebagai antikoagulan, antitumor, antivirus, pembuluh darah-kulit dan ginjal sintetik, bahan
pembuat lensa kontak, aditif kosmetik, membran dialisis, bahan shampoo dan kondisioner rambut, zat hemostatic, penstabil liposom, bahan ortopedik, pembalut luka dan benang bedah yang mudah diserap, serta mempertinggi daya kekebalan, antiinfeksi (Sugita et al, 2009).
2.6. Gliserin
Gliserol (gliserin) merupakan suatu senyawa poliol sederhana, tidak berwarna, tidak berbau, dan cairan kental yang banyak digunakan dalam formulasi farmasi. Gliserol memiliki tiga gugus hidroksil yang menyebabkan kelarutannya dalam air dan sifat higroskopisnya. Gliserin adalah cairan kental yang berwarna dan memiliki rasa manis. Penggunaan Gliserin paling umum adalah dalam sabun dan produk kecantikan lainnya seperti lotion.
Beberapa jumlah bahan tetap setiap bar dari sabun, dan tambahan dapat ditambahkan untuk menghasilkan hasil yang jelas dan kualitas pelembab ekstra. Ekstra juga meningkatkan aspek pembersihan sabun.
Gliserin dapat dilarutkan dengan mudah menjadi alkohol dan air, tetapi tidak menjadi minyak. Senyawa kimia murni disebut Gliserol, yang menunjukkan bahwa itu adalah alkohol. Faktanya gliserol mudah menyerap air dari udara sekitarnya berarti gliserin yang higroskopis. Ketika produk kecantikan yang mengandung senyawa ini digunakan pada kulit, dapat membantu menjaga kelembaban. Gliserin yang merupakan produk samping dari industri oleokimia yang memiliki sifat higroskopis, larut dalam air dan alkohol, tidak berwarna, tidak berbau dan memiliki rasa manis.
Gambar 2.6 Rumus Molekul Gliserin
Gliserin banyak digunakan untuk farmasi, bahan makanan, kosmetik, emulsifier dan minyak pelumas. Adapun kegunaan gliserin adalah sebagai berikut :
1.Farmasi
Gliserin banyak digunakan sebagai salep, obat batuk, pembuatan multi vitamin, vaksin, obat infeksi, stimulan jantung, antiseptik, pencuci mulut, pasta gigi.
3.Kosmetik
Gliserin yang memiliki sifat tidak beracun tidak menyebabkan iritasi dan tidak berwarna digunakan untuk pelembut dan pelembab kulit, krem kulit, sabun, pembersih wajah. Gliserin juga digunakan sebagai pelarut parfum, pewarna dan pembersih kendaraan (Minner, 1953).
2.7. Tepung tapioka
Ubi kayu/Singkong yang juga disebut Kaspe, dalam bahasa Latin disebut Manihot
Esculenta Crantz, merupakan tanaman yang banyak mengandung karbohidrat.
Oleh karna itu singkong dapat digunakan sebagai sumber karbohidrat disamping beras, selain itu dapat pula digunakan untuk keperluan bahn baku industri seperti: tepung tapioka, pellet, gaplek, gula pasir, gasohol, protein sel tunggal dan asam sitrat. Tepung tapioka dengan kadar amilosa yang rendah tetapi berkadar amilopektin yang tinggi ternyata merupakan sifat yang khusus dari singkong yang
tidak dimiliki oleh jenis tepung lainnya, sehingga tepung tapioka mempunyai kegunaan yang lebih luas (Rismayani, 2007).
Amilum atau dalam kehidupan sehari-hari disebut pati terdapat pada umbi, daun, batang dan biji-bijian. Amilum terdiri atas dua macam yaitu amilosa dan sisanya amilopektin. Amilosa terdiri atas 250-300 unit D-glukosa yang terikat
dengan ikatan α1,4 glikosidik, jadi molekulnya merupakan rantai terbuka.
Amilopektin juga terdiri atas molekul D-glukosa yang sebagian besar mempunyai ikatan 1,4-glikosidik dan sebagian lagi ikatan 1,6-glikosidik (Poedjiadi, 1994).
Gambar 2.7 Struktur Amilosa
Amilopektin. Suatu polisakarida yang jauh lebih besar daripada amilosa, mengandung 1000 satuan glukosa atau lebih per molekul. Seperti rantai dalam amilosa, rantai utama dari amilopektin mengandung 1,4-α-D-glukosa. Ikatan pada titik percabangan ialah ikatan 1,6-α-glikosida.
Gambar 2.7 Struktur Amilopektin
2.8. Edible film
Edible film didefinisikan sebagai suatu material berbentuk lapisan tipis yang
dapat dikonsumsi dan dapat digunakan sebagai penghalang kelembaban, oksigen dan gerakan zat terlarut pada makanan. Edible film dapat digunakan untuk lapisan pembungkus makanan yang atau dapat ditempatkan sebagai lapisan antara komponen makanan (Giulbert, 1986).
Edible film telah banyak menerima perhatian pada beberapa tahun
Fungsi dari edible film sebagai penghambat perpindahan uap air, menghambat pertukaran gas, mencegah kehilangan aroma, mencegah perpindahan lemak, meningkatkan karakteristik fisik, dan sebagai pembawa zat aditif. Edible
film yang terbuat dari lipida dan juga film dua lapis (bilayer) ataupun campuran
yang terbuat dari lipida dan protein atau polisakarida pada umumnya baik digunakan sebagai penghambat perpindahan uap air dibandingkan dengan edible
film yang tebuat dari protein dan polisakarida dikarenakan lebih bersifat
hidrofobik (Hui,2006).
Metode pembuatan edible film yang sering digunakan yaitu metode casting, yaitu dengan mendispersikan bahan baku edible film, pengaturan pH larutan, pemanasan larutan, pencetakan, pengeringan, dan pelepasan dari cetakan. (Wahyu, 2008).
2.8.1 Sifat-sifat edible film
Sifat fisik film meliputi sifat mekanik dan penghambatan. Sifat mekanik menunjukkan kemampuan kekuatan film dalam menahan kerusakan bahan selama pengolahan, sedangkan sifat penghambatan menunjukkan kemampuan film melindungi produk yang dikemas.
Beberapa sifat edible film antara lain sebagai berikut : 1.Ketebalan edible film
Ketebalan film merupakan sifat fisik yang dipengaruhi oleh konsentrasi padatan terlarut dalam larutan film. Ketebalan film akan mempengaruhi laju transmisi uap air, gas dan senyawa volatile.
2.Perpanjangan edible film atau elongasi
3.Peregangan edible film atau tensile strength
Peregangan edible film merupakan kemampuan bahan dalam menahan tekanan yang diberikan saat bahan tersebut berada dalam regangan maksimumnya. Kekuatan peregangan menggambarkan tekanan maksimum yang dapat diterima oleh bahan atau sampel.
4.Kelarutan film
Persen kelarutan edible film adalah persen berat kering dari film yang terlarut setelah dicelupkan di dalam air selama 24 jam.
5.Laju transmisi uap air
Laju transmisi uap air merupakan jumlah uap air yang hilang per satuan waktu dibagi dengan luas area film. Oleh karena itu salah satu fungsi edible film adalah untuk menahan migrasi uap air maka permeabilitasnya terhadap uap air harus serendah mungkin (Gontard, 1993).
2.9. Karakterisasi Edible Film
2.9.1. Fourier Transform Infrared (FTIR)
Spektrofotometer inframerah pada umumnya digunakan untuk menentukan gugus fungsi suatu senyawa organik dan mengetahui informasi struktur suatu senyawa organik dengan membandingkan daerah sidik jarinya.
Cahaya tampak terdiri dari beberapa range frekuensi elektromagnetik yang
disimpan, dan ditransformasikan dalam hitungan detik, teknik ini memudahkan penelitian reaksi-reaksi polimer seperti degradasi atau ikat silang. Persyaratan-persyaratan ukuran sampel yang sangat kecil mempermudah kopling instrument FTIR dengan suatu mikroskop untuk analisis bagian-bagian sampel polimer yang sangat terlokalisasi. Dan kemampuan untuk substraksi digital memungkinkan seseorang untuk melahirkan spektrum-spektrum lainnya yang tersembunyi (Steven, 2001).
2.9.2. Scanning Electron Microscopy (SEM)
Mikroskop electron adalah sebuah mikroskop yang dapat melakukan pembesaran objek sampai 2 juta kali. Mikroskop ini menggunakan elektrostatik dan elektromagnetik untuk pembesaran objek serta resolusi yang jauh lebih bagus daripada mikroskop cahaya (Sagala, 2013).
SEM adalah alat yang dapat membentuk bayangan permukaan spesimen
secara makroskopik. Berkas elektron dengan diameter 5-10 nm diarahkan pada spesimen interaksi berkas elektron dengan spesimen menghasilkan beberapa fenomena yaitu hamburan balik berkas elektron, sinar x, elektron sekunder, absorbs elektron.
2.10. Analisa Kadar Nutrisi Edible Film 2.10.1 Analisa Kadar Air
Kadar air sangat berpengaruh terhadap mutu bahan pangan, dan hal ini merupakan salah satu sebab mengapa di dalam pengolahan pangan air tersebut sering dikeluarkan atau dikurangi dengan cara penguapan atau pengentalan dan pengeringan. Pengurangan air disamping bertujuan mengawetkan juga untuk mengurangi besar dan berat bahan pangan (Winarno, 1980).
2.10.2. Analisa Kadar Abu
Abu adalah zat anorganik sisa hasil pembakaran suatu bahan organik. Kandungan abu dan komposisinya tergantung pada macam bahan dan cara pengabuannya.
Penentuan abu total dapat digunakan untuk berbagai tujuan yaitu antara lain: 1.Untuk menentukan baik tidaknya suatu proses pengolahan.
Misalnya pada proses penggilingan gandum diharapkan dapat dipisahkan antara bagian endosperm dengan kulit dan lembaganya. Apabila masih banyak kulit atau lembaga terikut dalam endosperm maka tepung gandum yang dihasilkan akan mempunyai kadar abu yang relatif tinggi.
2.Untuk mengetahui jenis bahan yang digunakan.
2.10.3 Analisa Kadar Lemak
Lemak adalah sekelompok ikatatan organik yang terdiri atas unsur-unsur karbon (C), hidrogen, (H), dan oksigen (O), yang mempunyai sifat dapat larut dalam pelarut lemak, seperti n-heksan, petrolueum benzene, eter. Lemak di dalam bahan makanan yang memegang peranan penting ialah disebut lemak netral atau trigliserida yang molekulnya terdiri atas satu molekul gliserol dan tiga asam lemak.
Lemak dalam bahan makanan ditentukan dengan metode ekstraksi beruntun di dalam alat soxhlet, dengan mempergunakan pelarut seperti n-heksan,petroleum benzene atau eter. Bahan makanan yang akan ditentukan kadar lemaknya, dipotong-potong setelah dipisahkan dari bagian yang tidak dimakan seperti kulit dan lainnya. Bahan makanan kemudian dihaluskan atau dipotong kecil-kecil dan dimasukkan kedalam alat soxhlet untuk diekstraksi. Ekstraksi dilakukan berturut-turut beberapa jam dengan dipanaskan. Setelah diperkirakan
selesai, cairan hasil ekstraksi diuapkan dan residu yang tertinggal ditimbang dengan teliti. Persentase lemak (residu) terhadap berat jumlah asal bahan makanan yang diolah dapat dihitung dan kadar lemak bahan makanan tersebut dinyatakan dalam gram persen (Sediaoetama, 1985).
2.10.4. Analisa Kadar Protein
Analisa protein metode kjeldhal pada dasarnya dapat dibagi menjadi tiga tahapan antara lain :
1.Tahap destruksi
Pada tahap ini sampel dipanaskan dalam asam sulfat pekat sehingga terjadi destruksi menjadi unsur-unsurnya. Elemen karbon, hidrogen teroksidasi menjadi CO, CO2 dan H2O. Sedangkan nitrogennya (N) akan berubah menjadi (NH4)2SO4.
Reaksi : (C,H,N,O,S)n + H2SO4(p) (NH4)2SO4 + SO2↑ + CO2↑ + H2O↑
Hijau Bening
2.Tahap destilasi
Pada tahap destilasi, ammonium sulfat dipecah menjadi ammonia (NH3) dengan
penambahan NaOH sampai alkalis dan dipanaskan. Ammonia yang dibebaskan selanjutnya akan ditangkap oleh larutan asam standar. Asam standar yang dapat dipakai adalah asam klorida atau asam borat 4% dalam jumlah yang berlebihan.
Untuk mengetahui asam dalam keadaan berlebih, diberi indikator tashiro. Destilasi diakhiri bila sudah semua ammonia terdestilasi sempurna dengan ditandai destilat tidak bereaksi basa.
Reaksi: (NH4)2SO4 + 2NaOH Na2SO4 + 2NH4OH
Hijau Bening
NH4OH NH3(g) + H2O(l)
NH3(g) NH3(l)
2NH3(l) + 4H3BO4 (NH4)2B4O7 + 5H2O
Larutan Biru Larutan Hijau
Reaksi: (NH4)2B4O7 + 2HCl 2NH4Cl + H2B4O7 + 5H2O
Larutan Hijau Larutan Ungu
2.10.5 Analisa kadar karbohidrat
Ada beberapa cara analisis yang dapat digunakan untuk menentukan kandungan karbohidrat dalam bahan makanan yaitu dengan cara perhitungan kasar (Proximate analysis) atau juga disebut Carbohydrate by Difference.
Perhitungan kasar (Proximate analysis) merupakan suatu analisis dimana kandungan karbohidrat termasuk serat kasar diketahui bukan melalui analisis tetapi melalui perhitungan, sebagai berikut:
% karbohidrat = 100 % - % ( protein + lemak + abu + air )
Perhitungan Carbohydrate by Difference adalah penentuan dalam bahan
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Bahan kemasan yang berasal dari polimer petrokimia atau yang lebih dikenal dengan plastik, merupakan bahan pengemas yang paling banyak digunakan. Namun ternyata, polimer plastik mempunyai berbagai kelemahan, yaitu sifatnya yang tidak tahan panas, mudah robek, dan yang paling penting adalah dapat menyebabkan kontaminasi melalui transmisi monomernya ke bahan yang dikemas. Kelemahan lain dari plastik adalah sifatnya yang tidak dapat dihancurkan secara alami (non-biodegradable) sehingga menyebabkan beban bagi lingkungan apabila tidak dilakukan daur ulang (recycling). Untuk itu diperlukan pengembangan jenis kemasan dari bahan organik dan bahan-bahan terbarukan (renewable) sebagai suatu jenis kemasan yang bersifat ramah lingkungan dan dikenal sebagai edible film (lembaran kemasan).
Secara umum edible film dapat didefenisikan sebagai lapis tipis yang melapisi suatu bahan pangan dan layak dimakan, digunakan pada makanan dengan cara pembungkusan atau diletakkan diantara komponen makanan yang dapat digunakan untuk memperbaiki kualitas makanan, memperpanjang masa simpan, meningkatkan efisiensi ekonomis, menghambat perpindahan uap air
(Krochta, 1992).
Pati merupakan homopolimer glukosa dengan ikatan alfa glikosida dan merupakan rantai gula panjang. Berbagai macam pati tidak sama sifatnya tergantung pada panjang rantai atom C nya, apakah lurus atau bercabang rantai molekulnya (Winarno, 1984).
Kitosan memiliki sifat antimikroba, karena dapat menghambat bakteri patogen dan mikroorganisme pembusuk, termasuk jamur, bakteri gram-positif , bakteri gram negative (Hafdani, 2011). Kitosan digunakan sebagai pelapis (film) pada berbagai bahan pangan, tujuannya adalah menghalangi oksigen masuk dengan baik, sehingga dapat digunakan sebagai kemasan berbagai bahan pangan dan juga dapat dimakan langsung, karena kitosan tidak berbahaya terhadap kesehatan (Henriette, 2010).
Gliserol juga dapat berfungsi sebagai plastisizer. Plastisizer merupakan
bahan aditif untuk mendapatkan sifat mekanis yang lunak, ulet dan kuat agar meningkatkan sifat plastisitasnya (Wirjosentono,1995).
Dari penelitian sebelumnya, Menurut Agung Endro Nugroho (2008) yang
berjudul “Manggis (Garcinia mangostana L.) : Dari Kulit Buah Yang Terbuang
Hingga Menjadi Kandidat Suatu Obat” menyatakan bahwa, Kulit buah manggis
ternyata mengandung senyawa golongan xanton. Dari percobaan isolasi yang dipandu uji aktivitas diketahui senyawa paling aktifnya adalah alfa-mangostin, gamma-mangostin dangarsinon-E.Ekstrak kulit buah manggis dan senyawa aktifnya memiliki aktivitas farmakologi yaitu alergi, inflamasi, oksidan, kanker, antimikroorganisme, aterosklerosis, dan bahkan anti-HIV.
Menurut Zoraya Mashithah (2012) yang berjudul “Pembuatan edible film
dari campuran ekstrak wortel (Daucus carota L.) dengan tepung tapioka, tepung
terigu dan gliserin” menghasilkan edible film dengan warna lebih cerah, rasanya
Menurut Arini Aulia (2012) yang berjudul “Pembuatan edible film dari
ekstrak buah papaya (Carica papaya L.) dengan campuran tepung tapioka, tepung
terigu dan gliserin” menghasilkan edible film dengan perbandingan tepung tapioka
: tepung terigu (7,5 g : 2,5 g) memberikan hasil yang lebih baik dari segi karakteristik dan kadar nutrisi.
Menurut Jimmy (2013) yang berjudul “Karakterisasi edible Film Dari
Campuran Tepung Tapioka, Kitosan, Gliserin, dan Ekstrak Mangga (Mangifera
indica L.)” menghasilkan permukaan edible film yang lebih optimal dengan
menggunakan 6 g tepung tapioka yang dibuktikan dari uji tarik sebesar 0,2285 KgF/mm2, kemuluran 48,91% dan swelling 6,42% dan permukaan yg sedikit berserat.
Menurut Oriza (2013) yang berjudul “Karakterisasi dan analisa kadar
nutrisi edible film dari campuran ekstrak daun sirsak (Annona muricata) dengan
tepung tapioka, kitosan dan gliserin”menjelaskan bahwa hasil edible yang terbaik
pada campuran 4 g tepung tapioka, 32 ml akuades, kitosan 2%, 2 ml gliserin dan 10 g ekstrak daun sirsak dengan hasil ketebalan 0,032 mm, kuat tarik sebesar 0,468 KgF/mm2 , dan kemuluran 37,36%. Dari hasil SEM dapat dilihat permukaan
edible film yang rata, rapat, halus dan juga berpori-pori kecil.
1.2 Perumusan Masalah
Permasalahan pada penelitian ini adalah :
1. Bagaimanakah kadar nutrisi dari edible film yang meliputi kadar air, abu,
protein, lemak, karbohidrat, serta kandungan β-karoten.
2. Bagaimanakah karakteristik fisik dari edible film yang meliputi ketebalan, kuat tarik, kemuluran, uji SEM, uji FT-IR serta uji organoleptik.
1.3 Pembatasan Masalah
Dalam penelitian ini objek masalah dibatasi sebagai berikut :
1. Sampel kulit manggis yang digunakan berasal dari Pasar sore, Padang Bulan Medan.
2. Parameter yang diteliti adalah sifat mekanik (ketebalan, pemanjangan film / elongation dan kuat regang putus / tensile strength) dan sifat fisik (analisa Scanning Electron Microscope / SEM dan analisa Spectroscopy
Fourier Transform Infra Red / FT-IR).
3. Analisa kadar nutrisi yang dilakukan adalah analisa kadar air, kadar abu, kadar protein, kadar lemak, dan kadar karbohidrat dan analisa β-karoten.
1.4 Tujuan Penelitian
Penelitian yang dilakukan bertujuan untuk :
1. Untuk mengetahui kandungan gizi dari edible film yang dapat digunakan sebagai bahan pengemas makanan.
2. Untuk mengetahui karakteristik fisik dari edible film.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah :
1. Menghasilkan edible film sebagai bahan pengemas makanan yang bersifat
mudah terdegradasi secara alami serta ramah lingkungan
2. Menghasilkan edible film dengan penambahan ekstrak kulit manggis yang
bermanfaat bagi kesehatan berdasarkan kandungan dari kulit manggis
1.6 Lokasi Penelitian
Lokasi penelitian dilakukan di Laboratorium Biokimia/KBM, Laboratorium Mikrobiologi USU, Laboratorium Penelitian FMIPA USU. dan Laboratorium Farmasi USU Medan.
1.7 Metodologi Penelitian
Penelitian ini merupakan penelitian eksperimental laboratorium, Adapun langkah-langkah analisisnya sebagai berikut :
1. Ekstrak kulit manggis diperoleh dengan mengekstraksi kulit manggis secara maserasi dengan pelarut etanol dan penambahan air ( perbandingan 1:2 ) dan diendapkan selama 24 jam.
2. Edible film dibuat dengan mencampurkan tepung tapioka dalam ekstrak
4. Analisa FT-IR edible film yang dihasilkan ditentukan dengan analisa spektroskopi.
5. Uji Kuat tarik edible film yang dihasilkan ditentukan dengan
menggunakan alat Torsee’s Electrinic system Tokyo testing machine. 6. Analisa Kadar protein edible film yang dihasilkan ditentukan dengan
metode Kjedahl.
7. Analisa Kadar lemak edible film yang dihasilkan ditentukan dengan cara ekstraksi kontinu dengan alat soklet.
8. Penentuan Kadar air edible film yang dihasilkan ditentukan dengan metode pengeringan dalam oven pada suhu 100 – 105oC.
9. Penentuan kadar abu edible film yang dihasilkan ditentukan dengan metode pembakaran dalam tanur pada suhu 600oC hingga diperoleh abu berwarna putih.
10.Penentuan Kadar Karbohidrat edible film yang dihasilkan ditentukan dengan menghitung selisih antara 100% dengan jumlah persentase kadar air, abu, protein, dan lemak.
11.Penentuan kadar β-karoten edible film yang dihasilkan ditentukan dengan menggunakan spektrofotometer UV dengan panjang gelombang 446 nm. 12.Uji organoleptik terhadap warna, rasa, bau, dan tekstur edible film yang
KARAKTERISASI EDIBLE FILM DARI EKSTRAK KULIT MANGGIS (Garcinia mangostana L.) DENGAN PENAMBAHAN TEPUNG TAPIOKA,
KITOSAN DAN GLISERIN SEBAGAI PEMLASTIS
ABSTRAK
Telah dilakukan penelitian tentang karakterisasi edible film dari ekstrak kulit manggis (Garcinia mangostana L.) dengan penambahan tepung tapioka, kitosan dan gliserin sebagai pemlastis. Edible film dibuat dengan mencampurkan tepung tapioka dengan variasi 3,4,5,6 dan 7 gram, kitosan dengan komposisi tetap 2% (w/v), dan ekstrak kulit manggis dengan komposisi tetap sebanyak 10 ml, dipanaskan dalam air dengan variasi 34,33,32,31 dan 30 ml, ditambahkan gliserin dengan komposisi tetap sebanyak 2 ml dan diaduk hingga homogen. Setelah homogen, dicetak diatas plat akrilik, dikeringkan didalam oven selama 2 hari. Karakterisasi edible film secara fisik diperoleh pengukuran ketebalan 0,23 mm, kuat tarik 0,3405 Kg F/mm2 dan kemuluran 14,1 %. Uji morfologi SEM (Scanning Electron Microscopy) menghasilkan edible film yang rata, rapat dan permukaan yang kompatibel. Serta analisa spektrum FTIR (Fourier Transform
Infrared) menunjukkan spektrum pada daerah 3297,61 cm-1 menunjukkan adanya gugus hidroksil (OH) atau gugus –NH. Analisa kadar nutrisi edible film menghasilkan kadar karbohidrat 69,69%, kadar protein 3,45%, kadar lemak 3,4%, kadar air 19,5%, kadar abu 3,96%, dan kadar β - karoten 76,0255%.
THE CHARACTERIZATION OF EDIBLE FILM FROM PEEL EXTRACTS OF MANGOSTEEN ( Garcinia mangostana L. ) BY THE ADDITION OF TAPIOCA STARCH, CHITOSAN AND
GLYCEROL AS PLASTICIZERS
ABSTRACT
The research has done on the characterization of edible films from peel extracts of mangosteen (Garcinia mangostana L.) by the addition of tapioca starch, chitosan and glycerol as plasticizers. Edible films made by mixing starch with 3,4,5,6 and 7 grams variations, chitosan with a fixed composition of 2% (w/v), and mangosteen peel extract with fixed composition as much as 10 ml, heated in water with 34 variations, 33;32;31 and 30 ml, was added glycerin to keep the composition as much as 2 ml and stirred until homogeneous. Once homogeneous, printed on acrylic plate, dried in an oven for 2 days. Characterization of edible film obtained by physically measuring 0.23 mm thickness, tensile strength 0.3405 kgF / mm2 and elongation 14.1 %. morphology test of SEM (Scanning Electron
Microscopy) produces edible film is flat, tight and compatible surface structure.
Also FTIR (Fourier Transform Infrared) spectrum analysis showed that spectrum at 3297.61 cm-1 range showed that hidrocyl group (OH) or –NH group exist Analysis of nutrient content of edible film produces 69.69% carbohydrate content, 3.45% protein content, 3.4% fat content, 19.5% moisture content, 3.96% ash content, and 76.0255 ppm β-carotene content.
KARAKTERISASI EDIBLE FILM DARI EKSTRAK KULIT
MANGGIS (Garcinia mangostana L.) DENGAN
PENAMBAHAN TEPUNG TAPIOKA,
KITOSAN DAN GLISERIN
SEBAGAI PEMLASTIS
SKRIPSI
SUMARIAH
100802001
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI EDIBLE FILM DARI EKSTRAK KULIT MANGGIS (Garcinia mangostana L.) DENGAN PENAMBAHAN TEPUNG TAPIOKA,
KITOSAN DAN GLISERIN SEBAGAI PEMLASTIS
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
SUMARIAH 100802001
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA