LAPORAN PRAKTIK KERJA PROFESI
FARMASI INDUSTRI
di
PT. Kimia Farma (Persero) Tbk.
Plant Bandung
Disusun Oleh :
Firdhany Armanda, S. Farm. NIM 083202120
PROGRAM PENDIDIKAN PROFESI APOTEKER
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Lembar Pengesahan
LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. Kimia Farma (Persero) Tbk.
Plant Bandung
Laporan ini disusun untuk melengkapi salah satu syarat untuk memperoleh Gelar Apoteker pada Fakultas Farmasi Universitas Sumatera Utara Medan
Disusun Oleh:
Firdhany Armanda, S. Farm. 083202120 Yade Metri Permata, S. Farm. 083202177
PT. Kimia Farma (Persero) Tbk. Plant Bandung Pembimbing,
Drs. Beben Budiman, Apt. Asisten Manager Produksi III
Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji syukur penulis ucapkan kehadirat Allah SWT atas berkat dan rahmat-Nya sehingga penulis dapat menyelesaikan Praktik Kerja Profesi Apoteker di PT. Kimia Farma (Persero) Tbk. Plant Bandung yang dilaksanakan pada tanggal 5 Oktober – 25 November 2009. Praktik Kerja Profesi Apoteker ini diselenggarakan sebagai salah satu syarat dalam meraih gelar Apoteker pada Program Profesi Apoteker Fakultas Farmasi Universitas Sumatera Utara.
Pelaksanaan Praktik Kerja Profesi Apoteker di PT. Kimia Farma (Persero) Tbk. Plant Bandung ini bertujuan agar calon apoteker nantinya dapat menjalankan fungsi dan peranan strategis seorang apoteker dalam kegiatan di Industri Farmasi. Praktik Kerja Profesi Apoteker ini dapat berjalan dengan lancar karena bantuan dari berbagai pihak. Untuk itu, izinkanlah pada kesempatan ini penulis mengucapkan terima kasih kepada:
1. Prof. Dr. Sumadio Hadisahputra, Apt. selaku dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Pihak PT. Kimia Farma (Persero) Tbk. Plant Bandung
a. Drs. Abdullah Basuki., Apt. selaku Manager Plant Bandung yang telah memberikan kesempatan untuk melaksanakan PKPA di PT. Kimia Farma (Persero) Tbk. Plant Bandung.
c. Drs. Yanyan Solehuddin., Apt. selaku Asisten Manager Sistem Mutu di PT. Kimia Farma (Persero) Tbk. Plant Bandung dan penanggung jawab tim PKPA.
d. Ibu Dedah Jubaedah, selaku supervisor ekstraksi kina yang telah membimbing dalam penyusunan tugas khusus evaluasi cinchonidin tetra sulfat di PT. Kimia Farma (Persero) Tbk. Plant Bandung. e. Seluruh staf dan karyawan PT Kimia Farma (Persero) Tbk. Plant
Bandung yang telah membantu selama pelaksanaan Praktik Kerja Profesi Apoteker.
Penulis menyadari bahwa laporan Praktik Kerja Profesi Apoteker ini masih belum sempurna. Oleh karena itu kritik dan saran yang bersifat membangun sangat penulis harapkan demi kesempurnaan laporan ini. Semoga laporan ini bermanfaat bagi pembaca yang ingin mengetahui dan mengkaji lebih dalam tentang industri farmasi.
Bandung, November 2009
DAFTAR ISI
Halaman
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR GAMBAR ... vii
BAB I PENDAHULUAN... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 2
BAB II TINJAUAN UMUM INDUSTRI FARMASI... 3
2.1 Sejarah PT. Kimia Farma (Persero). Tbk... 3
2.2 Visi dan Misi... 6
2.3 Lokasi dan Sarana Produksi... 6
2.4 CPOB ... ... 8
BAB III TINJAUAN KHUSUS PT. KIMIA FARMA (PERSERO) Tbk. PLANT BANDUNG... 10
3.1 Umum dan Administrasi Personalia ... 10
3.2 Perencanaaan Produksi dan Pengendalian Inventori (PPPI) ... 15
3.3 Produksi ... 16
3.3.1 Bagian Produksi I ... 19
3.3.2 Bagian Produksi II ... 24
3.3.3 Bagian Produksi III ... 22
3.4 Pemastian Mutu ... ... 27
3.4.1 Bagian Sistem Mutu... 29
3.4.3 Bagian Pengembangan Produk ... 34
3.4.4 Bagian Pengendalian Mutu ... 35
3.5 Pembelian ... 36
3.6 Penyimpanan... 38
3.7 Teknik dan Pemeliharaan ... 39
3.8 Keselamatan, Kesehatan Kerja dan Lingkungan (K3L) ... 42
BAB IV PEMBAHASAN ... 46
BAB V KESIMPULAN DAN SARAN ... 49
5.1 Kesimpulan ... 49
5.2 Saran ... 49
DAFTAR PUSTAKA ... 50
TUGAS KHUSUS ... 51
DAFTAR GAMBAR
Halaman Gambar 1. Struktur Organisasi PT. Kimia Farma Tbk. Plant Bandung ... 11 Gambar 2. Struktur Organisasi Umum dan Administrasi PT. Kimia Farma Tbk. Plant Bandung ... 12 Gambar 3. Struktur Organisasi Perencanaaan Produksi dan Pengendalian
Inventori PT. Kimia Farma Tbk. Plant Bandung ... 14 Gambar 4. Struktur Organisasi Bagian Produksi PT. Kimia Farma Tbk.
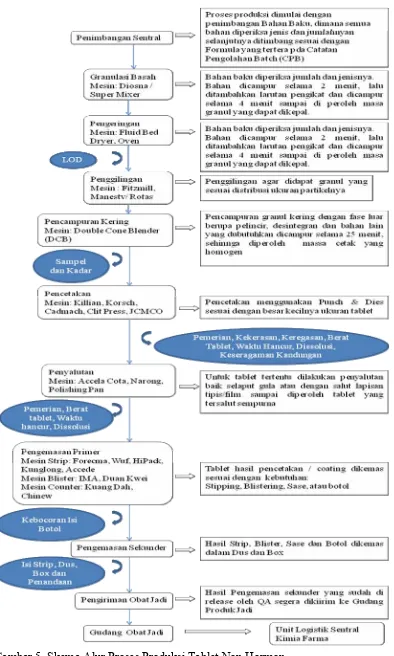
Plant Bandung ... 18 Gambar 5. Skema Alur Proses Produksi Tablet Non Hormon ... 21 Gambar 6. Struktur Organisasi Pemastian Mutu PT. Kimia Farma Tbk.
Plant Bandung ... 28 Gambar 7. Struktur Organisasi Pembelian PT. Kimia Farma Tbk.
Plant Bandung ... 37 Gambar 8. Struktur Organisasi Penyimpanan PT. Kimia Farma Tbk.
Plant Bandung ... 38 Gambar 9. Skema Alur Proses Penerimaan Barang ... 39 Gambar 10. Struktur Organisasi Teknik dan Pemeliharaan PT. Kimia Farma Tbk. Plant Bandung ... 40 Gambar 11. Struktur Organisasi K3L PT. Kimia Farma Tbk. Plant Bandung ... 42 Gambar 12. Skema Instalasi Pengolahan Air Limbah PT. Kimia Farma Tbk.
Plant Bandung ... 45 Gambar 13.Gambar Tanaman Chinchona succirubra... 55 Gambar 14. Gambar tanaman Chinchona ledgeriana... 56 Gambar 15. Grafik Perbandingan % Rendemen Crude CdTS Terhadap Input
Kulit Kina Succirubra Tahun 2008 dan 2009 ... 64 Gambar 16. Grafik Perbandingan % Rendemen Crude CdTS
Terhadap Input Bahan Tahun 2008 dan 2009... 65 Gambar 17. Grafik Perbandingan % Rendemen dari MLQ CdTS Tahun 2008
BAB I
PENDAHULUAN 1.1 Latar Belakang
Salah satu tujuan dari pembangunan nasional adalah pembangunan di bidang kesehatan dengan mewujudkan dan meningkatkan derajat kesehatan seluruh masyarakat Indonesia. Beberapa langkah kerja yang dilakukan pemerintah dalam rangka pembangunan nasional di bidang kesehatan meliputi tercukupinya ketersediaan obat, meratanya pendistribusian obat, serta terjangkaunya harga obat oleh masyarakat. Oleh karena itu, pengadaan dan produksi obat yang dalam hal ini dilakukan oleh industri farmasi akan mempengaruhi ketersediaan obat yang dibutuhkan masyarakat.
satunya dengan mendapatkan sertifikat International Organization for Standardization (ISO).
Keberhasilan pelaksanaan CPOB dan penerapan ISO dipengaruhi oleh kualitas sumber daya manusia yang terlibat dalam industri farmasi. Oleh karena itu suatu industri farmasi dituntut untuk mempunyai tenaga kerja yang kompeten, profesional dan berwawasan luas. Apoteker adalah salah satu profesi yang memegang peranan penting di industri farmasi. Calon apoteker yang ingin terjun di industri farmasi perlu melihat langsung penerapan dari konsep-konsep farmasi industri yang ada di lapangan. Untuk mendukung tercapainya hal tersebut, Program Profesi Apoteker Fakultas Farmasi Universitas Sumatera Utara bekerja sama dengan industri farmasi melaksanakan kegiatan Praktik Kerja Profesi (PKP) bagi peserta program profesi yang telah memilih bidang industri farmasi. Salah satu industri farmasi yang digunakan sebagai tempat PKP adalah PT. Kimia Farma (Persero) Tbk Plant Bandung.
1.2 Tujuan PKP
Setelah mengikuti Praktek Kerja Profesi diharapkan peserta program profesi mampu:
1. Memahami peran dan tanggung jawab apoteker di industri farmasi.
BAB II
TINJAUAN UMUM PT. KIMIA FARMA (PERSERO) Tbk. 2.1Sejarah PT. Kimia Farma (Persero) Tbk.
PT. Kimia Farma (Persero) Tbk. merupakan salah satu Badan Usaha Milik Negara (BUMN) yang bergerak di bidang kefarmasian, mulai dari produksi bahan baku obat, produksi obat jadi, sampai pada pemasaran yang meliputi Apotek dan Pedagang Besar Farmasi (PBF).
Pada tahun 1896, melalui akte notaris B.V. Houthuisen No. 12 tanggal 29 Juni 1896 di Bandung, didirikan sebuah pabrik kina oleh pemerintah Hindia Belanda dengan nama Bandoengsche Kinine Fabriek N. V, yang mula-mula hanya menghasilkan garam kina dari kulit kina. Pengolahan pabrik kina ini kemudian diserahkan pada Indische Combinatie Voor Chemische Industrie (Inschen) pada tanggal 14 Januari 1939 dan Inschen sendiri telah memiliki pabrik yodium di Watudakon yang didirikan pada tahun 1926.
Pada tahun 1942 dalam perang dunia II, pabrik kina Bandung dikuasai oleh angkatan darat Jepang yang diberi nama Rikuyun Kinine Seizoshyo. Selama Jepang berkuasa pembuatan pil dan tablet kina masih dilakukan, tetapi hasil kina tersebut diangkut ke Jepang dan sebagian lagi dikirim ke tempat-tempat lain untuk kepentingan Jepang dalam perang di Pasifik. Untuk keperluan dalam negeri, yaitu orang Indonesia, Jepang hanya menyediakan hasil pabrik yang disebut tota kina, yaitu kina yang belum dipisahkan dari alkaloid-alkaloid lainnya.
Combinatie Voor Chemische Industrie dengan akte Mr. R. Soewardi No. 47/1954 tanggal 3 November 1954.
Tahun 1958, berhubung adanya sengketa Irian Barat antara Indonesia dan Belanda, maka semua perusahaan Belanda yang ada di Indonesia dikuasai oleh pemerintah RI dengan membentuk Badan Pimpinan Umum (BPU) berdasarkan PP No. 23 tahun 1958. Berdasarkan UU No. 86 tahun 1958, perusahaan di bawah BPU ini menjadi milik RI yang pelaksanaannya diserahkan kepada Badan Nasionalisasi Perusahaan-perusahaan Belanda (BANAS). Pada tahun 1960, pabrik kina diberi nama Perusahaan Negara (PN) Farmasi dan Alat Kesehatan Bhinneka Kina Farma berdasarkan SP Menkes No. 57/959/BPK/Kob tanggal 18 Juli 1960. Pada tahun 1961, berdasarkan PP No. 85 tanggal 17 April 1961, namanya diubah menjadi Perusahaan Negara Farmasi (PNF) dan Alat-alat Kesehatan Bhinneka Kina Farma yang meliputi pabrik Yodium di Watudakon Mojokerto, Jawa Timur.
Pada tahun 1971, berdasarkan PP No. 16 tahun 1971 dalam lembaran negara RI No. 18 tahun 1971, PNF dan Alat-alat Kesehatan Bhinneka Kimia Farma unit I sampai unit IV diubah menjadi PT. (Persero) Kimia Farma terhitung mulai bulan Agustus 1971 melalui Akte Notaris Sulaeman Ardjasasmita tanggal 16 Agustus 1971 dan mengganti nama semua unit perusahaan yaitu Unit I menjadi Unit Perdagangan, Unit II menjadi Unit Produksi Jakarta, Unit III menjadi Unit Produksi Bandung, Unit IV menjadi Unit Produksi Yogyakarta. Pada pertengahan 1974, PNF Sari Husada (PT Kimia Farma Unit Produksi Yogyakarta) memisahkan diri dari PT. (Persero) Kimia Farma.
Tahun 1990, Unit Produksi Bandung menjadi tiga unit yaitu Unit Formulasi Bandung, Unit Produksi Manufaktur Bandung, dan Unit Produksi Manufaktur Watudakon. Pemisahaan unit ini diikuti dengan penggabungan pabrik pil KB ke dalam Produksi Formulasi Bandung.
Pada bulan Juli 2002, dilakukan perubahan struktur organisasi di mana Unit Produksi Formulasi Bandung, Unit Produksi manufaktur Bandung, serta Unit Produksi Manufaktur Semarang bergabung menjadi Plant Bandung. Begitu pula dengan Unit Produksi Jakarta dan Unit Produksi Tanjung Morawa Medan bergabung menjadi Plant Jakarta. Penggabungan ini dilakukan sebagai langkah efisiensi dan efektivitas untuk meningkatkan kempetensi guna pengembangan perusahaan.
dilebur menjadi Plant Bandung. Dengan berbagai pertimbangan antara lain, untuk efisiensi, baik SDM, birokrasi dan dana, pada tahun 2003 Unit Produksi Bandung tanpa Unit Produksi Manufaktur Semarang diubah menjadi Plant Bandung sampai sekarang.
2.2Visi dan Misi PT. Kimia Farma (Persero) Tbk. 2.2.1 Visi
Komitmen pada peningkatan kualitas kehidupan, kesehatan, dan lingkungan.
2.2.2 Misi
- Mengembangkan industri kimia dan farmasi dengan melakukan penelitian dan pengembangan produk yang inovatif.
- Mengembangkan bisnis pelayanan kesehatan terpadu yang berbasis jaringan distribusi dan jaringan apotek.
- Meningkatkan kualitas SDM dan mengembangkan sistem informasi perusahaan.
2.3Lokasi dan Sarana Produksi
PT. Kimia Farma (Persero) Tbk. terdiri dari 2 bidang usaha: 1. Holding :
a. Plant Jakarta b. Plant Bandung c. Plant Semarang
g. Unit Logistik Sentral 2. Anak perusahaan :
a. PT. Kimia Farma Trading & Distribution (PBF) b. PT. Kimia Farma Apotek
Jenis produksi yang dihasilkan oleh PT Kimia Farma (Persero) Tbk. Plant Bandung berdasarkan jenis dan bentuk sediaan adalah sebagai berikut:
1. Produksi bahan baku obat yang menghasilkan:
- Kina Sulfat
- Kina HCl
2. Produksi formulasi obat yang menghasilkan:
- Tablet non hormone
- Tablet hormon Mikrodiol (Pil KB)
- Alat Kontrasepsi dalam rahim (AKDR)
- Serbuk : Garam oralit
- Sirup : Paracetamol, Dekstromethorpan.
- Suspensi: Kloramfenikol, Kotrimoksazol.
- Fitofarmaka : Enkasari, Batugin.
Sebagai penunjang pelaksanaan kegiatan perusahaan, terdapat sarana-sarana yang digunakan dalam produksi di Bandung, antara lain:
2. Alat-alat yang digunakan, baik itu alat- alat produksi misalnya Fluid Bed Dryer, Super Mixer, Granulator Diosna, Ultra Turax, maupun alat-alat laboratorium misalnya HPLC, Spektrofotometer dan Polarimeter.
3. Bangunan penunjang kebutuhan para pekerja misalnya kantin, mushola, toilet, poliklinik.
2.4CPOB
Cara Pembuatan Obat yang Baik (CPOB) harus diterapkan dalam setiap industri farmasi sesuai dengan kebijakan pemerintah yaitu Surat Keputusan Menteri Kesehatan RI No. 43/ Menkes/ II/1988 pada tanggal 2 Februari 1988. Pada tahun 2006, pemerintah Indonesia telah memperbarui CPOB ini yang kemudian lebih dikenal dengan CPOB Terkini atau cGMP (Current GMP). Penerapan CPOB menyangkut seluruh aspek produksi dan pengendalian mutu bertujuan untuk menjamin bahwa setiap produk obat yang dibuat senantiasa akan memenuhi persyaratan mutu yang telah ditentukan sesuai dengan tujuan penggunaannya.
Aspek CPOB Terkini (CPOB 2006) terdiri atas sistem manajemen mutu, personalia, bangunan dan sarana penunjang, peralatan, sanitasi dan higiene, produksi, pengawasan mutu, inspeksi diri dan audit mutu, penanganan keluhan terhadap produk, penarikan kembali produk dan produk kembalian, dokumentasi, pembuatan dan analisis berdasarkan kontrak, kualifikasi dan validasi.
BAB III
TINJAUAN KHUSUS
PT. KIMIA FARMA (PERSERO) Tbk. PLANT BANDUNG
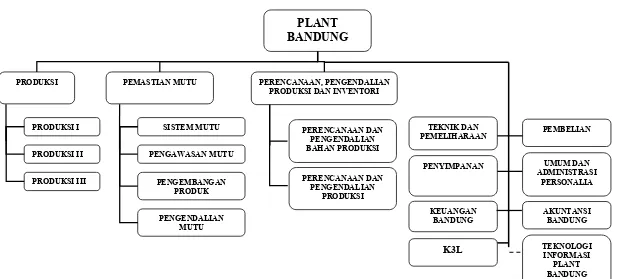
Manager Plant Bandung membawahi tiga manager yaitu Manager Produksi, Manager Pemastian Mutu dan Manajer PPPI, serta delapan bagian yang dikepalai oleh Asisten Manager yaitu Bagian Teknik dan Pemeliharaan, Bagian Penyimpanan, Bagian Pembelian, Bagian Umum & Administrasi Personalia, Bagian Keuangan, Bagian Akuntansi, Bagian K3L, dan Bagian Teknologi Informasi plant Bandung. Struktur Organisasi PT Kimia Farma (Persero) Tbk Plant Bandung dapat dilihat pada gambar 1.
3.1Umum dan Administrasi Personalia
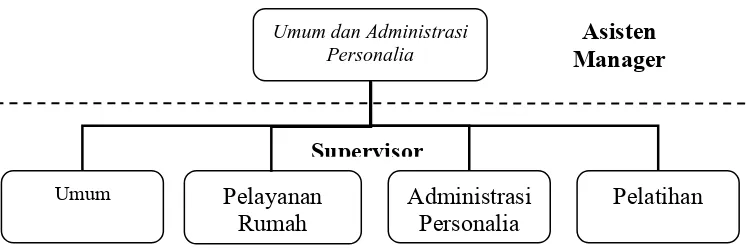
Bagian Umum dan Administrasi Personalia secara struktural dibawah langsung oleh Plant Manager, oleh karena itu dalam tugasnya, Asisten Manager Umum dan Administrasi Personalia bertanggung jawab langsung kepada Plant Manager. Struktur organisasi umum dan administrasi personalia dapat dilihat pada gambar 2.
Secara umum tugas dan wewenang dari Asisten Manager Umum dan Administrasi Personalia adalah:
1. Mengawasi kebenaran laporan absensi dan penilaian prestasi kerja pegawai. 2. Mengusulkan kenaikan pangkat dan golongan pegawai atas rekomendasi dari
pemimpin setiap bagian.
Gambar 1. Struktur Organisasi PT. Kimia Farma Tbk. Plant Bandung PLANT
BANDUNG
Gambar 2. Struktur Organisasi Umum dan Administrasi Personalia PT. Kimia Farma Tbk. Plant Bandung
Asisten Manager bagian Personalia dalam menjalankan tugas dan wewenangnya dibantu oleh 4 orang Supervisor, yaitu: supervisor bagian administrasi, supervisor bagian pelatihan, supervisor bagian rumah tangga dan supervisor bagian umun.
Sistem Penilaian Kinerja Pegawai dilakukan setiap satu tahun sekali berdasarkan hasil kerja yang dicapai, dimana proses penilaian dilakukan terhadap penilaian tugas pokok, tugas individual, perilaku dan juga absensi. Penilaian dilakukan oleh atasan masing – masing dan terakhir diserahkan ke Bagian Personalia. Dalam hal pengembangan sumber daya manusia, disusun rencana training selama 1 tahun dengan tujuan untuk peningkatan kompetensi, sedangkan untuk peningkatan SDM perusahaan dilakukan pelatihan bagi pegawai yang berprestasi yang selanjutnya ilmu yang diperoleh dapat diinduksi kepada pegawai-pegawai lainnya. Masa kerja pegawai-pegawai sampai usia 55 tahun.
Sistem rekruitmen pegawai dilakukan melalui 2 jalur yaitu untuk lulusan Sarjana dilaksanakan di Kantor Pusat Jakarta dan penempatannya dilaksanakan oleh Pusat sesuai dengan kebutuhan masing-masing unit. Sedangkan yang berasal
dari lulusan Program Diploma III kebawah dapat dilakukan rekruitmen pada unit produksi setempat setelah mendapat izin dari pusat.
Pembagian gaji dilakukan 2 kali dalam sebulan yang terdiri dari gaji (gaji pokok, tunjangan jabatan dan tunjangan perusahaan) dan upah lembur. Selain penghasilan tersebut perusahaan juga memberikan tunjangan lainnya, seperti tunjangan hari raya (THR), tunjangan hari tua, tunjangan intensif lainnya dan pensiun.
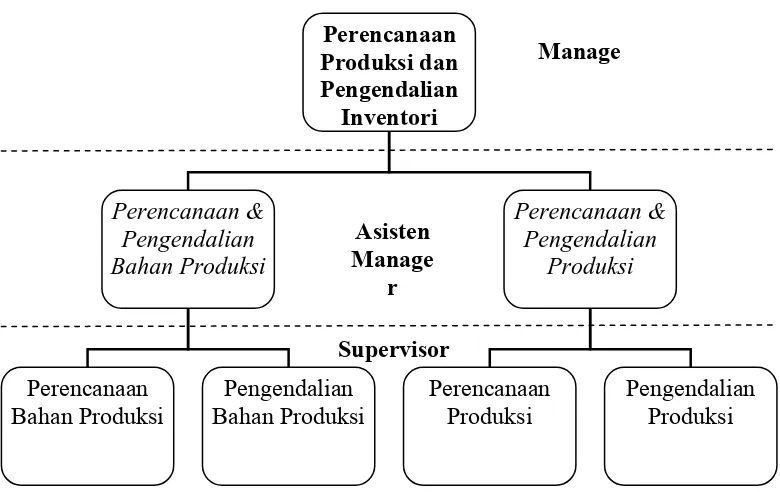
3.2Perencanaaan Produksi dan Pengendalian Inventori (PPPI)
Gambar 3. Struktur Organisasi Perencanaan Produksi dan Pengendalian Inventori PT. Kimia Farma Tbk Plant Bandung
Bagian PPPI bertanggung jawab memenuhi pesanan pemasaran secara tepat, baik tepat mutu, tepat jumlah maupun tepat waktu. Tugas dari PPPI antara lain adalah:
1. Menerima pesanan dari pemasaran dan mengevaluasinya menjadi konfirmasi pesanan.
2. Menghitung kebutuhan bahan dan memesan bahan produksi. 3. Merencanakan jadwal penyerahan produk.
4. Menerbitkan Surat Perintah Kerja Produksi.
5. Melakukan pengendalian dan monitoring produksi. 6. Mengendalikan persediaan agar optimal.
7. Berkoordinasi dengan pemasaran, ULS, produksi, pembelian, pemastian mutu, akutansi dan beberapa fungsi terkait.
1. Bagian Perencanaan dan Pengendalian Bahan Produksi terdiri atas bagian Perencanaan Bahan Produksi dan bagian Pengendalian Bahan Produksi yang bertugas menjamin ketersediaan bahan produksi berupa bahan baku maupun bahan kemas sehingga tidak terjadi kekosongan bahan maupun kelebihan stok untuk proses produksi. Rincian tugasnya antara lain:
a. Merencanakan kebutuhan bahan baku/bahan kemas b. Melakukan pemesanan bahan baku/bahan kemas c. Monitoring kedatangan dan jumlah bahan d. Melakukan pengendalian bahan
e. Melakukan evaluasi stok bahan
2. Bagian Perencanaan dan Pengendalian Produksi terdiri atas bagian Perencanaan produksi dan bagian Pengendalian produksi. Rincian tugas bagian ini meliputi :
a. Penjadwalan produksi
b. Penerbitan Surat Perintah Kerja (SPK) produksi, SPK coating dan SPK kemas
c. Evaluasi hasil produksi
d. Mengatur dan memantau kegiatan proses produksi sampai hasil jadi
di gudang. Masing-masing bahan dihitung berdasarkan rata-rata pemakaian perbulan, prediksi kebutuhan yang akan datang, dan lead time. Buffer stock untuk setiap bahan dapat berbeda, tergantung dari rata-rata pemakaian perbulan dan lead time. Buffer stock untuk bahan baku fast moving atau lead time-nya lama biasanya lebih banyak daripada barang yang slow moving atau lead time-nya pendek.
3.3Produksi
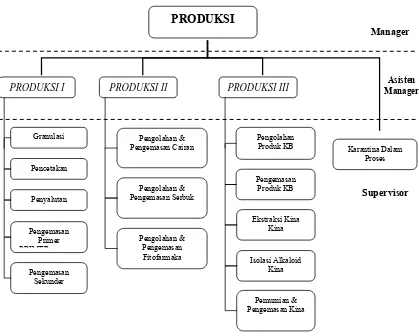
Secara Struktural bagian produksi dikepalai oleh seorang manager yang bertanggung jawab langsung kepada manager plant. Manager bagian produksi dalam melaksanakan tugasnya dibantu oleh 3 orang asisten manager, yaitu Asisten manager Bagian Produksi I (Sediaan Tablet), Bagian Produksi II (Sediaan Suspensi, Sirup, Oralit serbuk, Fitofarmaka) dan Bagian Produksi III, (Bahan baku Kina, Tablet Hormon, dan AKDR (Alat Kontrasepsi Dalam Rahim). Struktur organisasi produksi dapat dilihat pada gambar 4.
Tugas dan tanggung jawab manager produksi adalah sebagai berikut :
1. Bertanggung jawab atas terlaksananya pembuatan obat mulai dari perolehan bahan baku, pengolahan, pengemasan, sampai pengiriman obat ke gudang jadi.
2. Memberikan pengarahan teknis dan administratif untuk pelaksanaan pengolahan produksi dan pengemasan.
3. Bertanggung jawab untuk memeriksa catatan pengolahan batch serta menjamin bahwa produksi dilaksanakan sesuai prosedur pengolahan dan pengemasan batch.
Alur kegiatan bagian produksi :
1. Bagian produksi bekerja berdasarkan SPK produksi dari PPPI yang disahkan oleh Plant Manager yang disertai CPB dan BSTBB.
2. Bagian Penimbangan Sentral (PS) merekap kebutuhan bahan baku dan meminta gudang, kemudian bahan baku ditimbang.
3. Proses produksi dimulai:
a. Selama proses produksi, dilakukan IPC (oleh bagian produksi).
b. Setelah produksi selesai dan bagian pengawasan mutu telah menyatakan produk ruahan tersebut memenuhi spesifikasi dan mengeluarkan Laporan Analisa (LA), maka PPPI akan menurunkan SPK pengemasan yang disahkan Plant Manager beserta Catatan Kemasan Batch (CKB) dan Bon Serah Terima Bahan Kemas (BSTBK).
4. Produk jadi yang dihasilkan akan dikirim ke gudang obat jadi.
Gambar 4. Struktur Organisasi Produksi PT. Kimia Farma Tbk Plant Bandung Pada proses produksi, ada beberapa parameter kritis yang harus diperhatikan karena berpengaruh terhadap mutu akhir produk. Beberapa faktor yang harus diperhatikan adalah cahaya, suhu, kelembaban relatif (Rh), tekanan udara, jumlah mikroba dan jumlah partikel. Dalam mengendalikan parameter kritis tersebut, tiap industri farmasi diwajibkan untuk memiliki sistem tata udara (Priyambodo, 2007). Pengaturan udara di ruang produksi menggunakan sistem AHU, dimana untuk ruang produksi tablet hormon digunakan 100% fresh air, sedangkan untuk ruang produksi non hormon digunakan 20% fresh air dan 80% resirkulasi. Ruang produksi dibagi menjadi 3 area yaitu white area, grey area, black area (Anonim, 2009). Di PT. Kimia Farma Plant Bandung hanya ada 2 area
Manager
Supervisor
Asisten Manager PRODUKSI
PRODUKSI I PRODUKSI II
yaitu grey area dan black area. Grey area diperuntukkan untuk ruang penimbangan, ruang granulasi, ruang pencetakan, ruang pengemasan primer. Sedangkan produk yang sudah dikemas primer dan akan diberi kemasan sekunder dilakukan di black area. PT. Kimia Farma Plant Bandung tidak memiliki white area karena Plant Bandung tidak memproduksi sediaan steril. Tekanan udara pada masing-masing ruangan juga diatur. Untuk ruang produksi, tekanan udaranya dibuat lebih rendah daripada ruang koridor sehingga partikel-partikel akan mengalir ke ruang produksi dimana terdapat Dust Collector yang akan menghisap partikel-partikel untuk ditampung.
Pada ruang produksi, udara yang masuk dikendalikan partikelnya dengan cara menyaring menggunakan prefilter, medium filter dan HEPA filter. Penggunaan filter dengan efisiensi bertingkat dimaksudkan agar HEPA Filter lebih mudah dalam pemeliharaannya. Selama proses produksi ada parameter kritis yang harus diperhatikan karena pada parameter tersebut rawan terjadi perubahan yang dapat mempengaruhi mutu produk akhir. Oleh karena itu selama proses produksi dilakukan IPC. Apabila ditemukan ketidaksesuaian spesifikasi maka segera dilakukan perbaikan sesuai dengan tingkat kesalahan yang dihadapi. Apabila kesalahan dinilai berat, maka proses produksi dihentikan dulu dan dilakukan investigasi untuk menemukan penyebab kesalahan agar dapat ditentukan langkah perbaikan yang sebaiknya dilakukan.
3.3.1 Bagian Produksi I
Alur proses produksi dimulai dari Surat Perintah kerja (SPK) yang dikeluarkan oleh PPPI disertai dengan Catatan Pengolahan Batch (CPB) dan Bon Serah Terima Bahan Baku/Bahan Kemas (BSTBB/BK). SPK yang dikeluarkan oleh PPPI berisi juga target kapan produksi tersebut harus sudah selesai. Karena itu bagian produksi harus dapat merencanakan jadwal produksi dengan baik, memeriksa jadwal pemakaian mesin dan merencanakan kapasitas mesin yang akan dipakai serta merencanakan lead time proses. SPK ini diserahkan ke manager produksi untuk diteruskan ke asisten manager terkait kemudian ke Penimbangan Sentral (dengan disertai BSTBB), selanjutnya PS menyerahkan hasil penimbangan ke bagian produksi (Supervisor granulasi).
3.3.2 Bagian Produksi II
Bagian produksi II terdapat 3 supervisor yaitu Supervisor Pengolahan dan Pengemasan Cairan, Supervisor Pengolahan dan Pengemasan Serbuk, Supervisor Pengolahan dan Pengemasan Fitofarmaka.
Bagian Produksi II merupakan bagian yang memproduksi sediaan serbuk, cairan, dan fitofarmaka. Sediaan serbuk yang diproduksi adalah serbuk oralit, sedangkan yang termasuk sediaan cairan adalah sirup dan suspensi. Contoh sediaan sirup antara lain sirup dekstrometorfan, sirup parasetamol, Ercivit, OB Sari, dan sirup ferrous sulfat. Sedangkan sediaan suspensi diantaranya suspensi kotrimoksazol dan suspensi kloramfenikol. Contoh produk fitofarmaka yang dihasilkan Plant Bandung adalah Batugin Eliksir dan Enkasari.
3.3.3 Bagian Produksi III
Bagian produksi III terdapat 5 supervisor yaitu Supervisor Pengolahan Produk KB, Supervisor Pengemasan Produk KB, Supervisor Ekstraksi Kina, Supervisor Isolasi Alkaloida Kina dan Supervisor Pemurnian dan Pengemasan Kina.
Bagian Produksi III merupakan bagian yang memproduksi tablet Oral Kontrasespsi, AKDR, dan Bahan baku kina.
1. Sediaan Oral Kontrasepsi (Tablet Hormon)
Hasil produksi: Mikrodiol Limas dan Mikrodiol Program (program pemerintah). Satu blister isinya: 21 tablet Oral kontrasepsi yang isinya Ethynilestradiol 0,03 mg dan Levonorgestrel 0,15 mg per tablet dan 7 tablet placebo yaitu tablet yang tidak mengandung bahan aktif hormon.
ruang produksinyapun terdiri dari dua bagian yang terpisah, yaitu untuk pembuatan tablet placebo dan untuk pembuatan tablet OC. Ruang penyimpanan bahan dan ruang penimbangannyapun tersendiri untuk menghindari adanya kontaminasi silang. Ruang produksi tablet OC merupakan ruang yang memiliki pengaturan sistem tekanan udara yang khusus, yaitu tekanan di dalam ruang produksi tablet OC dibuat lebih negatif dibanding tekanan koridor, yang bertujuan untuk mencegah keluarnya udara dari dalam ruang produksi OC. Selain itu pada pintu keluar dilengkapi dengan air shower untuk menghilangkan partikel-partikel serbuk hormon. Penimbangan hormon dilakukan didalam Laminar Air Flow
(LAF) karena jumlah yang ditimbang sangat kecil serta untuk menghindari kontaminasi hormon dalam ruangan. Terdapat juga dust collector yang digunakan untuk menghisap dan menampung debu, caranya debu yang terhisap akan disaring, kemudian debu ditampung ke bawah dan udara yang tidak mengandung debu dibuang keluar.
Pada prinsipnya, pembuatan tablet hormon sama dengan tablet non hormon, yaitu dibuat dengan proses granulasi basah. Alur kerja dibedakan menjadi dua yaitu produksi tablet plasebo dan produksi tablet OC. Untuk produksi tablet plasebo, setelah bahan ditimbang di Penimbangan Sentral dilakukan proses pencampuran bahan, kemudian dilanjutkan dengan proses granulasi basah dengan mesin Roto G yang berkapasitas 40-50 kg. Selanjutnya dilakukan pengayakan massa basah dengan mesin Wet Granulator. Setelah diayak basah, dilakukan pengeringan pada Fluid Bed Dryer. Pada proses ini dilakukan In Process Control
(IPC) Loss On Drying (LOD = susut pengeringan) untuk mengetahui kadar air dalam granul kering yang sudah diayak. Selanjutnya granul diayak kering dengan mesin Oscillator. Massa granul yang dihasilkan kemudian dicampur dengan fase luar (bahan pelincir) pada mesin Double Cone Blender. Massa yang sudah dicampur fase luar ini disebut massa cetak, dimana kemudian akan dilakukan proses pencetakan dengan mesin Cadmach CTX. Selama proses pencetakan dilakukan pemeriksaan IPC yang meliputi keseragaman bobot, ketebalan, diameter tablet, kekerasan, kerapuhan dan waktu hancur. Tablet yang telah dicetak akan dikarantina untuk diperiksa oleh laboratorium pengujian yang meliputi pemerian, keseragaman bobot, ketebalan, diameter tablet, kekerasan, kerapuhan, dan waktu hancur.
pemeriksaan IPC susut pengeringan (LOD) untuk mengetahui kadar air dalam granul kering. Selanjutnya granul diayak kering dengan mesin Fitz Mill. Massa granul yang yang dihasilkan kemudian dicampur dengan fase luar (bahan pelincir) dengan mesin pencampur. Kemudian dilakukan proses pencetakan dengan mesin
Killian/Fette. Selama proses pencetakan dilakukan pemeriksaan IPC yang meliputi keseragaman bobot, ketebalan, diameter tablet, kekerasan, kerapuhan. Saat tablet telah dicetak juga dilakukan pemeriksaan oleh Laboratorium Pengujian yang meliputi kadar, keseragaman kandungan, disolusi, pemerian, keseragaman bobot, ketebalan, diameter tablet, kekerasan, kerapuhan, waktu hancur.
Setelah tablet plasebo dan tablet OC dinyatakan lulus uji, selanjutnya memasuki proses pengemasan blistering dengan mesin Blister Uhlmann. Di sini dilakukan IPC meliputi uji kebocoran, estetika, dan kelengkapan penandaan pada kemasan. Selanjutnya dilakukan pengemasan sekunder dengan IPC meliputi estetika dan perhitungan jumlah blister.
2. AKDR (Alat Kontrasepsi dalam Rahim)
Produk yang dihasilkan oleh bagian AKDR yaitu Copper T Limas (Lingkaran Emas), Copper T Libi (Lingkaran Biru), Copper T BKKBN untuk program pemerintah, Copper T ekspor, yang diekspor ke luar negeri terutama ke negara asia seperti Korea.
3. Bahan Baku Kina
Di bagian produksi kina ada tiga bagian, yaitu bagian ekstraksi kina, bagian isolasi alkaloid kina dan bagian pemurnian dan pengemasan kina.
tanaman Cinchona succirubra dan Cinchona ledgeriana. Kedua jenis tanaman tersebut memiliki kandungan yang berbeda, untuk tanaman Cinchona succirubra
lebih banyak mengandung alkaloid cinchonidine sedangkan tanaman Cinchona ledgeriana lebih banyak mengandung alkaloid quinine.
Bagian dari tanaman kina yang diambil hanya kulit pohonnya. Sumber tanaman sebagian besar diimpor dari luar negeri seperti Afrika dan sebagian lagi berasal dari perkebunan sendiri yaitu dari Kebun Tanaman Obat Bintang (KTO Bintang). Tanaman yang dipanen yaitu tanaman pada usia 8 tahun, namun sebelum dipanen dilakukan perantingan untuk meningkatkan kandungan alkaloida pada kulit kina. Tanaman kina setelah dikupas kulitnya, dikeringkan sampai berbentuk kulit kering/brangkal kemudian digiling kasar. Kulit kina yang disimpan di gudang kulit kina sudah dalam bentuk gilingan kasar. Selanjutnya dilakukan penggilingan halus dan siap untuk diekstraksi.
Alur produksi kina dimulai dengan ekstraksi padat-cair, yaitu 1 ton kulit kina halus diekstraksi dengan pelarut SGO (Special Gas Oil) dalam kondisi basa dalam ekstraktor. Setelah itu SGO dikeluarkan, sedangkan ampas tetap di dalam. SGO yang ditampung ini mengandung garam kina, selanjutnya SGO dipindahkan ke reaktor untuk dilakukan ekstraksi cair-cair dengan cara ditambahkan H2SO4
dan Natrium Sulfat Water. Setelah itu didiamkan agar memisah, lapisan atas merupakan SGO sedangkan lapisan bawah adalah H2SO4, keduanya dipisahkan
dan alkaloid yang tertarik ke fase polar H2SO4 didiamkan selama 3-5 malam
dengan penambahan NaHCO3, disentrifugasi, didapat Mlq dan kristal S (sulfat).
Mlq ditransfer ke pemurnian alkaloid kina untuk pengambilan Cd (Cinchonidine). Mlq dari proses sebelumnya yang telah dikumpulkan, ditambah asam tartrat sehingga menjadi Qn(Quinine), Cd (Cinchonidine) tartrat, lalu dibasakan sehingga menjadi Qn dan Cd (dominan Cd).
3.4Pemastian Mutu
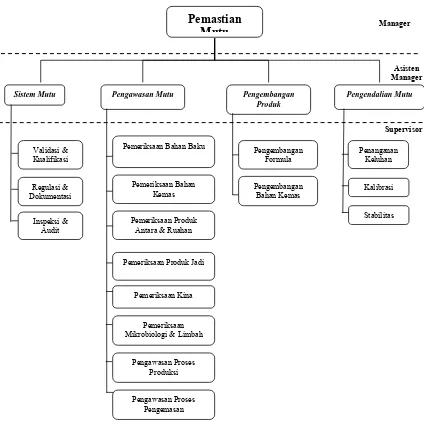
Gambar 6 . Struktur Organisasi Pemastian Mutu PT. Kimia Farma Tbk Plant Bandung
Tugas Bagian Pemastian Mutu ini adalah menjamin bahwa produk yang dihasilkan terjamin mutu, khasiat dan keamanannya, yang dimulai dari bahan baku datang sampai bahan tersebut diproses menjadi produk yang dilepas di pasaran. Bagian ini juga menjamin bahwa sistem, fasilitas, dan prosedur memadai untuk dijalankan dan diikuti dengan benar sehingga produk yang dihasilkan terjamin dan memenuhi spesifikasi. Bagian Pemastian mutu juga menjamin bahwa prosedur, system (Software), mesin dan alat penunjang produksi (Hardware), dan Manager
Asisten Manager Pemastian
Mutu
Sistem Mutu Pengawasan Mutu Pengembangan Produk Mikrobiologi & Limbah
juga personel yang terlibat (Brainware) dapat menghasilkan mutu produk yang diinginkan dan sesuai spesifikasi.
3.4.1 Bagian Sistem Mutu
Sistem Mutu adalah bagian dari seluruh sistem manajemen yang mencakup struktur organisasi, kegiatan perencanaan, tanggung jawab dan wewenang, proses, prosedur dan sumber daya untuk menerapkan, mengembangkan, mencapai, meninjau dan memelihara kebijakan mutu.
Adapun tujuan penerapan Sistem Mutu adalah:
1. Secara konsisten menyediakan produk yang memenuhi persyaratan pelanggan dan memenuhi peraturan-peraturan perundangan dalam hal mutu.
2. Meningkatkan kepuasan pelanggan melalui penerapan yang efektif dari sistem, termasuk melakukan perbaikan terus menerus.
Manfaat dari Sistem Mutu ini adalah: 1. Bagi karyawan:
- Kejelasan tugas dan wewenang.
- Peningkatan prestasi kerja dan kepuasan kerja karena sistem dan prosedur kerja yang baik.
- Keyakinan akan kebenaran cara penanganan pekerjaan. 2. Bagi pelanggan:
- Menumbuhkan rasa yakin terhadap perusahaan
- Akan mendapatkan pelayanan sesuai dengan yang diharapkan atau yang telah dijanjikan.
Sistem mutu terdiri dari : 1. Validasi dan Kualifikasi
Tugas bagian ini adalah:
- Menyusun Rencana Induk Validasi (RIV) - Memonitor pelaksanaan validasi
- Bersama dengan tim validasi melaksanakan validasi yang dikoordinator supervisor validasi yang terdiri dari validasi proses, analisa, pembersihan, instalasi.
- Melaporkan dan menindaklanjuti hasil validasi 2. Regulasi dan Dokumentasi
Tugas bagian ini adalah: - Dokumen CPOB dan ISO - Pembuatan Dossier
- Pembuatan Questionaire
- Penggandaan CPB-CKB
- Registrasi Produk Jadi dan NIE (Nomor Izin Edar) - Tugas tambahan yaitu Arsip Technical Drawing
3. Inspeksi dan Audit Tugas bagian ini adalah:
- Mengkoordinasikan pelaksanaan dan perencanaan audit internal dan eksternal
- Membuat rencana tindak lanjut hasil audit
- Membuat notulen hasil RTM dan mendokumentasikannya - Melaporkan tindak lanjut dari RTM
3.4.2 Pengawasan Mutu
Bagian Pengawasan Mutu bertugas melakukan pengujian terhadap bahan baku, bahan kemas, produk ruahan, produk jadi, pengujian mikrobiologi dan limbah cair, pengawasan kina mulai dari bahan baku sampai produk jadi, IPC pengawasan produksi, dan IPC pengawasan kemasan produk jadi. Bagian Pengawasan Mutu bertanggungjawab untuk menjamin bahwa produk yang diterima oleh konsumen dan yang dilepas ke pasaran sesuai dengan spesifikasi yang telah ditetapkan. Tanda lulus pengujian adalah dengan menempelkan label diterima yang bewarna hijau disertai nomor Laporan Analisa (LA), sedangkan yang tidak lulus pengujian dengan menempelkan label ditolak yang bewarna merah yang juga disertai dengan nomor Laporan Analisa (LA). Bahan/produk yang masih diperiksa diberi label karantina bewarna kuning.
Bagian Pengawasan Mutu terdiri dari 8 supervisor yang bertanggung jawab terhadap:
1. Pemeriksaan Bahan Baku
Sebagai tanda bahan masih diperiksa akan diberi label kuning, label hijau berarti telah lulus pemeriksaan dan label merah berarti bahan ditolak karena out of spesification. Sebagai bukti kalau Bagian Pengawasan Mutu telah memeriksa, maka diterbitkan Laporan Analisa (LA). Semua bahan baku baik bahan aktif obat maupun bahan pembantunya, akan diperiksa oleh seksi ini kecuali kina dan bahan pembantu proses pembuatan kina. Jumlah yang disampling √N+1 untuk masing-masing batch dan bila yang datang hanya 3 batch atau kurang maka akan disampling semua. Jika ada bahan baku tertentu yang masih disimpan dalam gudang dalam waktu relatif lama maka akan disampling ulang. Contohnya untuk vitamin tiap 6 bulan sekali akan diperiksa ulang, bahan aktif setahun sekali dan bahan pembantu 2 tahun sekali.
2. Pemeriksaan Bahan Kemas
Dilakukan pemeriksaan pada saat barang datang. BTBS dari Bagian Gudang akan diserahkan ke seksi pemeriksaan bahan kemas. Kemudian akan dilakukan sampling √N+1 dalam kardus-kardus yang datang itu. Bila dalam kardus tersebut terdapat dus yang lebih kecil lagi dalam bentuk ikatan maka akan disampling sebanyak √N+1, pemeriksaan meliputi jumlah, estetika, penampilan sesuai apa tidak dengan spesifikasi. Bahan kemas yang disimpan dalam waktu tertentu di gudang juga akan diperiksa ulang tiap 2 tahun sekali. Contoh bahan kemas yang juga diperiksa oleh seksi ini : aluminium foil, leaflet, botol.
3. Pemeriksaan Produk Antara dan Ruahan
memenuhi spesifikasi akan direalease untuk mengikuti proses selanjutnya, jika tidak lulus uji akan diinvestigasi kesalahannya untuk menentukan langkah perbaikan.
4. Pemeriksaan Produk Jadi
Pemeriksaan untuk produk jadi dilakukan sebelum produk dikirim ke gudang prduk jadi. Produk yang sedang diuji maka akan diberi label karantina (label kuning) dan dilakukan pemeriksaan seperti pemeriksaan isi strip, dus, box dan penandaan. Jika pruduk sudah lulus uji maka akan dikeluarkan laporan analisa dan produk dikirim ke ULS (Unit Logistik Sentral).
5. Pemeriksaan Kina
Pada pemeriksaan kina, dilakukan pemeriksaan kadar kina yang terdapat dalam bahan baku. Jika memenuhi persyaratan maka akan masuk gudang dan jika tidak masuk persyaratan akan dikembalikan ke supplier. Tugas dari seksi ini adalah melakukan pemeriksaan bahan baku (kulit kina), produk antara dan produk akhir termasuk bahan pembantu dalam proses pembuatan.
6. Pemeriksaan Mikrobiologi dan Limbah Cair Tugas dari seksi ini adalah melakukan:
- Pemeriksaan produk jadi yang memerlukan pemeriksaan mikrobiologi, contoh AKDR, fitofarmaka.
- Pemeriksaan air yang dipergunakan untuk proses produksi.
- Pemantauan ruang proses produksi (pada saat bekerja) apakah memenuhi syarat mikrobiologi meliputi angka kuman dan angka jamur serta bakteri patogen.
7. Pengawasan Dalam Proses Produksi
Supervisor ini melakukan pengawasan selama proses produksi, yaitu:
- Hasil proses pencampuran menjadi massa cetak atau cairan (produk ruahan atau produk antara) diperiksa di Pengawasan Mutu.
- Pada proses produksi tablet, pemeriksaan yang dilakukan IPC produksi meliputi pemeriksaan kebenaran bahan dan jumlahnya sesuai apa tidak dengan CPB, pemeriksaan fisik granul, pemeriksaan uji kekerasan dan bobot tablet. - Pada proses produksi cairan dan serbuk, pemeriksaannya meliputi kebenaran
bahan dan jumlah sesuai CPB, tes kebocoran, volume untuk sediaan cair, pemeriksaan berat untuk serbuk dan penandaannya (ED dan no. Batch).
8. Pengawasan Dalam Proses Pengemasan
Supervisor ini melakukan pengawasan selama proses pengemasan, yaitu pengecekan bahan kemas sebelum dan sesudah proses pengemasan.
3.4.3 Bagian Pengembangan Produk
Teknologi Formulasi merupakan bagian dari Pengelolaan Mutu yaitu unit kerja teknologi produksi dan pengembangan dalam skala kecil. Bagian ini bertanggung jawab terhadap pengembangan produk baru dan produk lama di lingkungan Plant Bandung.
Pengembangan produk terdiri dari 2 supervisor yaitu pengembangan formula dan pengembangan bahan pengemas.
1. Pengembangan Formula Tugas & tanggung jawab :
pengawasan mutu. Jika bagian pengembangan produk tidak bisa menangani permasalahan maka akan dikirim ke unit Risbang (Riset dan Pengembangan).
- Memperbaiki produk yang bermasalah (NCP), perbaikan bisa dilakukan di bagian produksi, jika bagian produksi tidak bisa menangani maka akan dikirim ke bagian pengembangan produk.
- Melakukan trial untuk bahan baku alternatif, baik zat aktif maupun bahan pembantu alternatif.
- Melakukan perbaikan metode analisa yang bermasalah. - Mencari metode analisa alternatif.
2. Pengembangan Bahan Kemas Tugas & tanggung jawab :
- Menyiapkan rancangan kemasan produk baru sampai spesifikasinya - Melakukan revisi kemasan karena adanya peraturan baru
- Membuat formula bahan kemas dan pembuatan CKB
- Melakukan trial bahan kemas design baru atau dari supplier baru 3.4.4 Bagian Pengendalian Mutu
Pengendalian mutu terdiri dari 3 supervisor yaitu: 1. Penanganan Keluhan
Tugas dari bagian ini adalah:
- Menerima dan meregistrasi keluhan pelanggan
- Koordinasi dengan bagian stabilitas untuk keluhan mengenai mutu
- Koordinasi dengan bagian penyimpanan dan membuat laporan rekomendasi tindak lanjut keluhan dan laporan penanganan keluhan
2. Stabilitas
Uji stabilitas dilakukan untuk produk baru dan produk lama. Stabilitas dapat diuji dalam 2 cara yaitu uji stabilitas dipercepat, dan uji stabilitas real time. Produk yang diuji stabilitas pada waktu yang sebenarnya maka akan disimpan dalam lemari khusus (Climetic Chamber) selama waktu pengujiannya dan dalam jumlah yang telah diperhitungkan untuk jangka waktu pengujian yang telah ditentukan.
3. Kalibrasi
Kalibrasi adalah suatu pengujian satuan alat ukur dengan cara dibandingkan dengan standar alat ukur yang mampu telusur dan teruji baik secara nasional maupun internasional. Tujuan dilakukan kalibrasi :
- Memelihara serta merawat peralatan pengukuran sehingga selalu dalam kondisi yang siap pakai dan sesuai standart.
- Memastikan peralatan pengukuran memiliki akurasi yang sesuai dengan tuntunan pengukurannya.
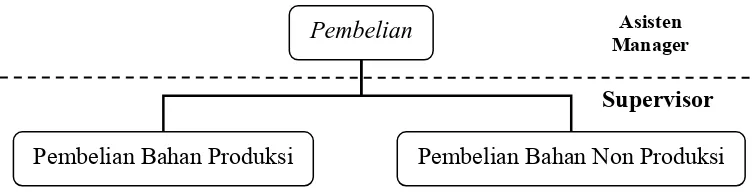
3.5Pembelian
Gambar 7. Struktur Organisasi Pembelian PT Kimia Farma Tbk Plant Bandung Bahan produksi meliputi bahan baku dan bahan pengemas. Bahan pengemas yang diadakan di unit adalah bahan pengemas skunder seperti dus, etiket, dan lain-lain, sedangkan bahan pengemas seperti botol, dan polycel, pengadaannya diakukan di kantor pusat. Bahan pendukung produksi merupakan bahan yang digunakan untuk mendukung jalannya proses produksi seperti punch
dan dies pada pembuatan tablet.
Permintaan terhadap bahan produksi dan non produksi dilakukan oleh PPPI. Berdasarkan permintaan tersebut, dibuat permintaan harga kepada distributor dengan mengacu kepada daftar distributor handal dari hasil kinerja pemasok pada tahun sebelumnya. Daftar distributor handal disusun dan dievaluasi 1 tahun sekali dalam rapat tinjauan manajemen akhir tahun oleh Plant Manager,
Manager Representative, seluruh manajer dan asisten manajer. Kriteria evaluasi distributor handal didasarkan pada persentase ketepatan mutu bahan dan waktu yang didata dari seluruh jenis bahan yang dikirim oleh distributor selama 1 tahun. Selain itu, faktor harga juga perlu dipertimbangkan, sehingga distributor yang dipilih adalah yang memenuhi 3 kriteria, yaitu tepat harga, tepat mutu, dan tepat waktu. Setelah dibuat permintaan harga kepada distributor, dilakukan evaluasi dan negosiasi harga. Jika sesuai maka dikeluarkan surat pesanan. Barang yang
Pembelian
Pembelian Bahan Produksi Pembelian Bahan Non Produksi Supervisor
telah dibeli disimpan di gudang. Jika ada barang yang tidak memenuhi syarat, maka bagian gudang menginformasikan ke bagian pembelian.
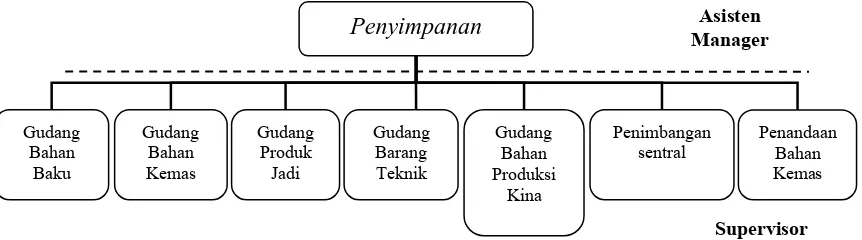
3.6Penyimpanan
Secara Struktural bagian penyimpanan dikepalai oleh seorang asisten manager yang bertanggung jawab langsung kepada manager plant. Asisten manager bagian pembelian dalam melaksanakan tugasnya dibantu oleh 7 orang supervisor, yaitu supervisor gudang bahan baku, supervisor gudang bahan kemas, supervisor produk jadi, supervisor gudang barang teknik, supervisor gudang bahan produksi kina, supervisor penimbangan sentral, dan supervisor penandaan bahan kemas. Struktur organisasi produksi dapat dilihat pada berikut:
Gambar 8. Sruktur Organisasi Penyimpanan PT. Kimia Farma Tbk Plant Bandung Tugas bagian pembelian adalah melakukan pembelian bahan produksi yaitu bahan baku dan bahan kemas, dan melakukan pembelian bahan non produksi yang meliputi alat tulis kantor, alat-alat penunjang produksi, alat laboratorium dan keperluan laboratorium.
Untuk pembelian yang pengadaannya ditangani oleh kantor pusat, maka bagian PPPI membuat Surat Permohonan Pengadaan Barang, yang disahkan oleh Plant Manager dan ditujukan ke Manager Pengadaan Produksi, selanjutnya kantor
pusat akan memesan bahan ke Pemasok barang dan menerbitkan Surat Pesanan (SP) yang juga dikirimkan ke Plant Bandung.
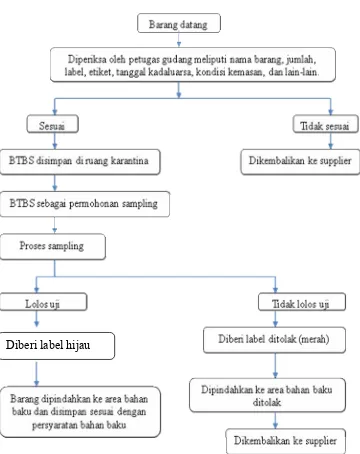
Alur proses penerimaan barang:
Gambar 9. Skema Alur Proses Penerimaan Barang 3.7Teknik dan Pemeliharaan
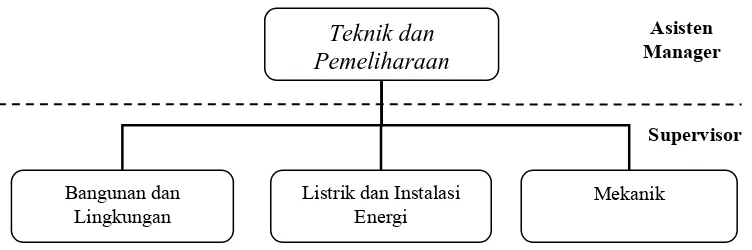
Secara sruktural bagian teknik dan pemeliharaan dikepalai oleh seorang aisten manager yang bertanggung jawab langsung kepada manager plant. Asisten
manager bagian teknik dan pemeliharaan dalam melaksanakan tugasnya dibantu oleh 3 orang supervisor, yaitu supervisor bangunan dan lingkungan, supervisor listrik dan instalasi energi, dan supervisor mekanik. Struktur organisasi produksi dapat dilihat pada gambar berikut:
Gambar 10. Struktur Organisasi Teknik dan Pemeliharaan PT. Kimia Farma Tbk. Plant Bandung
Bagian teknik dan pemeliharaan membawahi 3 supervisor , yaitu:
1. Supervisor bangunan dan lingkungan yang bertanggung jawab terhadap pemeliharaan bangunan produksi, pemeliharaan gedung perkantoran, pemeliharaan perumahan, dan pemeliharaan instalasi air.
2. Supervisor listrik dan instalasi energi yang bertanggung jawab terhadap instalasi listrik, AC, boyler, dan komponen elektronik.
3. Supervisor mekanik yang bertanggung jawab terhadap perbaikan dan pemeliharaan mesin produksi, modifikasi mesin, dan instalasi pipa.
Alur kerja teknik dan Pemeliharaan:
1. Dimulai apabila ada kerusakan atau gangguan pada salah satu bagian. Bagian tersebut akan membuat Surat Perintah Perbaikan Teknik (SPPT) yang ditujukan ke Bagian Teknik dan Pemeliharaan.
2. Setelah diterima, bagian teknik dan pemeliharaan akan memisahkan menurut supervisor yang berhubungan dengan masalah tersebut.
3. Supervisor akan menulis kebutuhan barang untuk perbaikan sarana. Jika
sparepart tersebut sudah ada di gudang teknik maka bagian teknik dan pemeliharaan dapat langsung memperbaiki peralatan tersebut dengan mengirim Surat Pemintaan Barang Teknik (SPBT) ke gudang teknik. Apabila dibutuhkan sparepart dan di gudang tidak tersedia (habis) maka diterbitkan Surat Permintaan Pesanan Barang oleh gudang teknik yang disahkan oleh AMTP.
Apabila kerusakan tidak dapat diperbaiki oleh bagian teknik dan pemeliharaan maka dapat melibatkan pihak ketiga.
1. Bagian teknik dan pemeliharaan akan mencari pihak ketiga dan meminta penawaran terlebih dahulu dan dilaporkan kepada bagian terkait.
2. Apabila Plant Manager setuju maka bagian teknik dan pemeliharaan akan membuat SPK kepada pihak ketiga.
Jika peralatan tersebut telah diperbaiki (SP), maka bagian teknik akan memeriksa peralatan tersebut dan bila sudah sesuai, maka Kepala Bagian terkait akan menandatangani SPK di kolom persetujuan dan kolom mengetahui untuk ditandatangani oleh Plant Manager
Pengecekan rutin terhadap peralatan dilakukan setiap hari sebelum mesin digunakan oleh operator dan apabila terdapat masalah/ kerusakan maka dilaporkan ke bagian teknik dan pemeliharaan .
Secara struktural bagian K3L dikepalai oleh seorang asisten manager yang bertanggung jawab langsung kepada manager plant. Asisten manager bagian K3L dalam melaksanakan tugasnya dibantu oleh 2 orang supervisor, yaitu supervisor lingkungan dan supervisor keselamatan dan kesehatan kerja. Struktur organisasi produksi dapat dilihat pada gambar berikut:
Gambar 11. Struktur Organisasi K3L PT. Kimia Farma Tbk. Plant Bandung Tugas supervisor Keselamatan dan Kesehatan Kerja (K3):
- Mendata semua yang berhubungan dengan rambu-rambu keselamatan seperti tanda exit di setiap bangunan.
- Memantau alat pemadam kebakaran dan hydrant yang tersedia di PlantBandung
- Membuat denah yang berhubungan dengan evakuasi dan letak alat pemadam kebakaran dan hydrant
- Mengadakan pelatihan pemadam kebakaran
- Mengawasi prosedur yang berhubungan dengan K3 di semua bagian.
Pada Instalasi Pengolahan Air Limbah (IPAL) sebagian besar mengelola limbah yang berasal dari proses kulit kina dan sebagian lagi dari limbah formulasi. Limbah yang dihasilkan dibedakan menjadi limbah padat dan limbah cair. Limbah ini akan diolah yang melibatkan proses fisika, kimia dan biologi.
Keselamatan &Kesehatan Kerja dan
Lingkungan Keselamatan &
Kesehatan Kerja
Asisten Manager
Proses fisika
Limbah berupa ampas kina dari ekstraktor yang masih mengandung air dipisahkan secara fisika dengan pengadukan mekanik. Limbah padat ini kemudian diendapkan, dicuci berkali-kali dan limbah padat kering ditimbun dan dikirim ke tempat pembuangan sampah ampas, lalu diproses menjadi briket, sedangkan limbah cair masuk ke bak penampungan untuk diproses secara kimia.
Proses kimia
Pada proses ini dilakukan penambahan asam fosfat untuk menetralkan limbah cair yang bersifat basa. Selanjutnya limbah diproses secara biologi. Fungsi dari asam fosfat disini juga untuk menurunkan nilai COD (Chemical Oxygen Demand)
Proses biologi
BAB VI PEMBAHASAN
PT. Kimia Farma (Persero) Tbk.Plant Bandung merupakan salah satu BUMN dalam bidang kesehatan yang memproduksi obat dengan tujuan meningkatkan derajat kesehatan masyarakat secara optimal. Sebagai suatu industri yang memproduksi obat, maka seluruh aspek CPOB harus diterapkan. Aspek-aspek tersebut meliputi sistem manajemen mutu, personalia, peralatan, bangunan, sanitasi dan hygiene, produksi, pengawasan mutu, inspeksi diri dan audit mutu, penanganan terhadap produk, penarikan kembali produk dan produk kembalian, dokumentasi, pembuatan dan analisis berdasarkan kontrak, kualifikasi dan validasi
Personalia atau SDM memegang peranan yang penting dalam suatu perusahaan sehingga harus dikelola dengan baik dengan tujuan untuk meningkatkan produktivitas dan kemampuan kerja. PT. Kimia Farma (Persero) Tbk. Plant Bandung juga melakukan pelatihan-pelatihan bagi karyawan-karyawannya sesuai dengan tugasnya ataupun mengenai CPOB. Tujuan dari pelatihan ini adalah untuk menjamin agar karyawan terbiasa bekerja dengan persyaratan CPOB yang berkaitan dengan tugasnya. Catatan pelatihan karyawan mengenai CPOB disimpan dan efektivitas program pelatihan dinilai untuk menentukan prestasi karyawan tersebut, apakah mereka telah memiliki kualifikasi yang memadai dan berpengaruh terhadap kenaikan jabatan bagi karyawan tersebut.
pelaksanaan kerja, pembersihan dan pemeliharaan. Selain itu juga memiliki lokasi sedemikian rupa untuk mencegah terjadinya pencemaran dari lingkungan sekelilingnya, seperti pencemaran udara, tanah dan air. PT. Kimia Farma (Persero) Tbk. Plant Bandung memiliki lokasi yang kurang strategis karena letaknya di tengah kota. Namun tindakan preventif seperti pengolahan limbah cair dan ampas kina telah ditangani dengan cukup efektif. Ruangan dalam gedung produksi telah memenuhi persyaratan CPOB meliputi dinding, lantai dan langit-langit terbuat dari epoxy dengan permukaan yang halus, rata dan licin serta pertemuan antara dinding dengan lantai tidak membentuk sudut sehingga lebih mudah dibersihkan, tidak menyerap lembab serta tidak menahan debu. Ruang produksi juga telah dilengkapi dengan sistem sirkulasi udara yang dapat mengurangi debu dengan pengaturan tekanan udara sehingga dapat menekan kontaminasi silang. Selain itu terdapat juga ruang antara yang memisahkan Grey Area dan Black Area. Pada pelaksanaannya ruang antara masih memungkinkan terjadinya kontaminasi silang karena kedua pintu dibuka bersamaan. Hal ini terjadi karena kedisiplinan karyawan yang kurang. Idealnya adanya air lock antar ruang yang berbeda area, apabila salah satu pintu terbuka, maka pintu lain tidak terbuka sehingga mengurangi debu yang lolos ke ruang sebelahnya. Bangunan produksi tablet hormon dipisahkan dengan produksi yang lain karena sangat berbahaya efeknya jika terjadi kontaminasi silang.
sebelum dan sesudah produksi dan hanya peralatan yang dinyatakan memenuhi persyaratan saja yang boleh digunakan dalam proses produksi. Peralatan yang digunakan untuk menimbang, mengukur dan menguji harus diperiksa ketelitiannya secara teratur serta dikalibrasi secara periodik. Hasil pemeriksaan dan kalibrasi dicatat dan disimpan untuk mengetahui pemeriksaan berikutnya.
Sanitasi dan hygiene di lingkungan Plant Bandung telah dilaksanakan cukup baik dan dapat dilihat dari kebersihan lingkungan yang selalu terjaga. Selain itu, untuk mendukung terciptanya hygiene maka karyawan yang memasuki ruang produksi menggunakan pakaian khusus yang disediakan, sarung tangan, masker, tutup kepala dan sepatu khusus. Pembersihan ruangan dilakukan secara rutin setiap hari sesuai protap yang ada. Pembersihan peralatan, perlengkapan dan ruangan produksi dilakukan sebelum dan sesudah proses produksi. Fasilitas pendukung sanitasi seperti ventilasi, toilet dan tempat sampah sudah cukup memadai.
BAB V
KESIMPULAN DAN SARAN 5.1Kesimpulan
- Peran apoteker di industri farmasi adalah melakukan kegiatan managerial baik dalam hal perencanaan dan pengendalian produksi, perencanaan dan pengendalian bahan, pelaksanaan proses produksi, serta pelaksanaan kegiatan pengawasan mutu yang menjamin mutu dari produk yang dihasilkan.
- PT. Kimia Farma (Persero) Tbk. Plant Bandung dalam kegiatan produksi dan pengawasan mutunya telah melaksanakan CPOB dengan tujuan untuk menjamin bahwa produk yang dihasilkan senantiasa memenuhi persyaratan mutu yang telah ditentukan sesuai dengan tujuan penggunaannya.
5.2 Saran
DAFTAR PUSTAKA
Anonim, (2009). PT. Kimia Farma (Persero) Tbk. diakses 10 November 2009.
Ditjen POMa, (2006), Pedoman Cara Pembuatan Obat yang Baik, Jakarta: Depkes RI.