UJI DAYA ANTIBAKTERI DAN ANTIOKSIDAN DARI EKSTRAK ETANOL DAUN BANGUN-BANGUN (Coleus amboinicus Lour.)
SKRIPSI
OLEH:
HERMIN PANJAITAN 050804023
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
UJI DAYA ANTIBAKTERI DAN ANTIOKSIDAN DARI EKSTRAK ETANOL DAUN BANGUN-BANGUN (Coleus amboinicus Lour.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
HERMIN PANJAITAN NIM : 050804023
FAKULTAS FARMASI
LEMBAR PENGESAHAN SKRIPSI
UJI DAYA ANTIBAKTERI DAN ANTIOKSIDAN DARI EKSTRAK ETANOL DAUN BANGUN-BANGUN (Coleus amboinicus Lour.)
OLEH:
HERMIN PANJAITAN NIM : 050804023
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Desember 2009
Pembimbing I Panitia Penguji
(Dra. Saleha Salbi, M.Si., Apt.) (Dr. Ginda Haro, M.Sc., Apt.)
NIP. 130 817 963 NIP. 195108161980031002
Pembimbing II
(Dra. Saleha Salbi, M.Si., Apt.) (Dra. Masfria, MS., Apt.) NIP. 130 817 963
NIP 195707231986012001
(Drs. Syahrial Yoenoes, SU.,Apt.) NIP. 195112061983031001
(Dra. Erly Sitompul, M.Si.,Apt NIP. 195006121980021001
Disahkan Oleh: Dekan
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan berkat dan kasih karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul ”Uji Daya Antibakteri dan Antioksidan dari Ekstrak Etanol Daun Bangun-Bangun (Coleus amboinicus Lour.)”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana Farmasi pada Fakultas Farmasi, Universitas Sumatera Utara.
Tujuan dari penelitian ini adalah untuk mengetahui aktivitas antibakteri dan antioksidan dari ekstrak etanol Daun Bangun-Bangun (Coleus amboinicus Lour.). Melalui penelitian diketahui bahwa ekstrak etanol Daun Bangun-Bangun (Coleus amboinicus Lour.) memiliki aktivitas antibakteri dan antioksidan. Hendaknya hasil penelitian ini dapat menjadi informasi mengenai sumber antibakteri dan antioksidan baru dengan pemanfaatan Daun Bangun-Bangun (Coleus amboinicus Lour .)
Penulis juga ingin menyampaikan rasa terimakasih yang sebesar-besarnya kepada Ibu Dra. Saleha Salbi, M.Si, Apt.,dan Ibu Dra. Masfria, MS, Apt.,yang telah membimbing penulis dengan penuh kesabaran hingga selesainya penyusunan skripsi ini. Ucapan terimakasih juga disampaikan kepada Dekan Fakultas Farmasi Universitas Sumatera Utara, Prof. Dr. Sumadio Hadisahputra, Apt., yang telah memberikan fasilitas selama masa pendidikan, dan juga kepada Bapak Prof. Dr. Jansen Silalahi, M.App.Sc.,Apt.,selaku dosen wali yang telah memberi bimbingan dan dorongan kepada penulis selama perkuliahan, dan kepada Bapak Dr. Ginda Haro, M.Sc.,Apt, Ibu Dra. Saleha Salbi, M.Si.,Apt., Bapak Drs. Syahrial Yoenoes, SU, Apt., Ibu Dra. Erly Sitompul, M.Si, Apt., selaku dosen penguji yang memberikan masukan dalam penyusunan skripsi ini, kepada seluruh staf Laboratorium Sintesa Bahan Obat/ Kimia Organik buat fasilitas yang diberikan demi kelancaran penelitian ini. Dan tidak lupa juga penulis menyampaikan terimakasih kepada teman-temanku, Intan, Rianti, Susan, Yuli, Ernita, Siska, Juni, Dian, Anggelia, Riris, Kak Susi, Ester, Andi, Harry, Sandri, Tagor, Iwanto, Januar, Victor, seluruh asisten SBO/KO, dan seluruh Farmasi stambuk 2005 yang namanya tidak dapat ditulis satu persatu, yang telah banyak membantu penulis dalam proses penelitian hingga selesainya penulisan skripsi ini.
Medan, Desember 2009 Penulis,
Uji daya Antibakteri dan Antioksidan dari Ekstrak Etanol daun Bangun-Bangun (Coleus amboinicus Lour.)
Abstrak
Tumbuhan banyak mengandung senyawa kimia yang berkhasiat obat seperti senyawa polifenol, yang biasa digunakan sebagai antibakteri dan antioksidan. Salah satu tumbuhan yang mengandung senyawa polifenol adalah daun bangun-bangun. Penelitian ini bertujuan untuk mengetahui daya antibakteri dan antioksidan ekstrak etanol daun bangun-bangun.
Sampel (daun bangun-bangun) diperoleh dari daerah Tembung kabupaten Deli Serdang. Ekstrak dihasilkan dengan cara maserasi menggunakan etanol. Daya antibakterinya diukur dengan metode difusi agar menggunakan punch hole kemudian diukur diameter hambat pertumbuhan bakteri Staphylococcus aureus dan Escherichia coli. Daya antioksidannnya diukur dengan metode penghambatan oksidasi minyak kedelai selama penyimpanan pada suhu 40oC (0, 3, 5, dan 7 hari), dengan BHT sebagai pembanding.
Hasil penelitian menunjukkan bahwa ekstrak etanol daun bangun-bangun mempunyai daya antibakteri yang cukup besar yaitu pada konsentrasi 4% memiliki diameter hambatan 27,16 mm untuk Staphylococcus aureus dan 24,15 mm untuk bakteri Escherichia coli. Daya antioksidan meningkat dengan peningkatan jumlah ekstrak yang ditambahkan yaitu pada konsentrasi 1%(b/b) daya antioksidan sebesar 50,76%, pada konsentrasi 2%(b/b) daya antioksidan sebesar 54,97%, tetapi daya antioksidan ekstrak dengan konsentrasi 1% dan 2%, masih lebih rendah dari daya antioksidan BHT 0,02% (daya antioksidannya 58,80%). Namun pada konsentrasi ekstrak 3%(b/b) daya antioksidan lebih tinggi dari BHT yaitu 63,89%.
Kata kunci: daun bangun-bangun (Coleus amboinicus Lour.), ekstrak etanol,
Examination of Antibacterial and Antioxidant bangun-bangun’s leaf (Coleus amboinicus Lour.) ethanol extract
Abstract
Plant contain various chemical compounds such as polyphenolic compounds which usually used as antibacterial and antioxidant. One of plant contain polyphenolic compounds is bangun-bangun leaf. The purpose of this research is to examine antibacterial and antioxidant of bangun-bangun’s leaf ethanol extract.
Sample (bangun-bangun’s leaf) was obtained from Tembung’s area, Deli Serdang District. Extract was obtained by maseration with ethanol. Antibacterial activity was measured by agar difution methode, using punch hole, and then diameter inhibition of bacteri Staphylococcus aureus and Escherichia coli was measured. Antioxidant activity measured by method of the oxidation inhibition of soybean oil during storage at 40oC (0, 3, 5, and 7 days) with BHT as positive control.
The result of this research showed that the antibacterial activity of bangun-bangun’s leaf ethanol extract is had large enough, with its concentration 4% had zone inhibition 27,16 mm for Staphylococcus aureus and 24,15 mm for Escherichia coli. The antioxidant activity is increased with the increase of the amount extract added. At 1% of concentration, showed that the antioxidant activity was 50,76%, at 2% of concentration the antioxidant activity was 54,97%. But the antioxidant activity extract with 1% and 2% of concentration was lower than BHT 0,02% (antioxidant activity 58,80%). But at 3% of concentration was higher than BHT which antioxidant activity was 63,89%.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian... 3
1.5 Manfaat Penelitian ... 4
1.6 Kerangka penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
BAB III METODOLOGI PENELITIAN... 17
3.1 Alat – alat ... 17
3.2 Bahan – bahan ... 17
3.3 Penyiapan bahan ... 18
3.3.2 Determinasi tumbuhan ... 18
3.3.3 Pengolahan bahan ... 19
3.4 Pembuatan pereaksi ... 19
3.4.1 Larutan Pereaksi Mayer ... 19
3.4.2 Larutan Pereaksi Dragendorff ... 19
3.4.3 Larutan Pereaksi Bouchardat ... 19
3.4.4 Larutan Pereaksi Molish ... 19
3.4.5 Larutan Pereaksi Besi (III) Klorida ... 20
3.4.6 Larutan Pereaksi Timbal (II) Asetat 0,4 M ... 20
3.4.7 Larutan Natrium Hidroksida ... 20
3.4.8 Pereaksi Lieberman-Burchard ... 20
3.4.9 Pereaksi Asam Klorida 2 N ... 20
3.4.10 Pereaksi Asam Sulfat 2 N... 20
3.4.11 Larutan standard Natrium Tiosulfat 0,002 N ... 20
3.4.12 Pembakuan Larutan standard Natrium Tiosulfat 0,002 N ... 21
3.4.13 Larutan HCl 25% ... 21
3.4.14 Indikator kanji ... 21
3.4.15 Larutan NaOH 12% ... 22
3.5 Penetapan kadar air ... 22
3.6 Pembuatan ekstrak ... 23
3.7 Skrining Fitokimia Serbuk daun bangun-bangun (Coleus amboinicus Lour) ... 23
3.7.1 Pemeriksaan Alkaloida ... 23
3.7.3 Pemeriksaan Glikosida ... 24
3.7.4 Pemeriksaan Glikosida antrakinon ... 24
3.7.5 Pemeriksaan saponin ... 25
3.7.6 Pemeriksaan tannin ... 25
3.7.7 Pemeriksaan Steroida/Triterpenoida ... 25
3.8 Penentuan Daya Antibakteri ... 26
3.10.1 Pengujian daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Staphylococcus aureus ... 29
3.10.2 Pengujian daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Escherichia coli ... 29
3.11.1 Pembuatan minyak kedelai ... 30
3.11.2 Pemurnian minyak kedelai ... 30
3.11.2.1 Degumming ... 30
3.11.2.2 Alkali refining... 30
3.11.2.3 Bleaching ... 31
3.12 Pengujian daya antioksidan... 31
BAB IV HASIL DAN PEMBAHASAN ... 33
BAB V KESIMPULAN DAN SARAN... 42
5.1Kesimpulan ... 42
5.2Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Halaman Tabel 1. Hasil Skrining Fitokimia daun bangun-bangun
(Coleus amboinicus Lour.) ... 33 Tabel 2. Hasil uji daya antibakteri ekstrak etanol
DAFTAR GAMBAR
Halaman Gambar 1. Mekanisme Autooksidasi Asam Lemak Tak Jenuh
oleh Spesies Oksigen Reaktif ... 13 Gambar 2. Mekanisme Reaksi BHT sebagai Antioksidan ... 16 Gambar 3. Grafik lama penyimpanan (hari) –Vs- bilangan
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Hasil Identifikasi /Determinasi Tumbuhan ... 45
Lampiran 2 Hasil Identifikasi Kacang Kedelai (Soja max L.) ... 46
Lampiran 3 Data Perhitungan Penetapan Kadar Air ... 47
Lampiran 4 Data Data Pembakuan Larutan Natrium Tiosulfat... 48
Lampiran 5 Data-Data Hasil Titrasi Minyak Kedelai Kontrol ... 49
Lampiran 6 Data-Data Hasil Titrasi Minyak Kedelai dengan Penambahan Pembanding BHT 0,02% ... 50
Lampiran 7 Data-Data Hasil Titrasi Minyak Kedelai Dengan Penambahan Ekstrak etanol daun bangun-bangun 1% ... 51
Lampiran 8 Data Data Hasil Titrasi Minyak Kedelai dengan Penambahan Ekstrak etanol Daun bangun-bangun 2% ... 52
Lampiran 9 Data Data Hasil Titrasi Minyak Kedelai dengan Penambahan Ekstrak etanol Daun bangun-bangun 3% ... 53
Lampiran 10 Contoh Perhitungan Bilangan Peroksida ... 54
Lampiran 11 Contoh Perhitungan Persamaan Garis Regresi ... 55
Lampiran 12 Contoh Perhitungan Penentuan daya Antioksidan ... 56
Lampiran 13 Bangun-bangun (Coleus amboinicus Lour) ... 57
Lampiran 14 Kacang Kedelai ... 58
Lampiran 15 Flowsheet preparasi minyak kedelai ... 59
Lampiran 16 Flowsheet penentuan bilangan peroksida ... 60
Lampiran 17 Flowsheet pembuatan inokulum bakteri... 61
Lampiran 18 Flowsheet Pengujian daya Antibakteri ... 62
Lampiran 20 Gambar uji daya antibakteri ekstrak etanol daun bangun-bangun terhadap pertumbuhan
bakteri Staphylococcus aureus ... 64 Lampiran 21 Gambar uji daya antibakteri ekstrak etanol
daun bangun-bangun terhadap pertumbuhan
Uji daya Antibakteri dan Antioksidan dari Ekstrak Etanol daun Bangun-Bangun (Coleus amboinicus Lour.)
Abstrak
Tumbuhan banyak mengandung senyawa kimia yang berkhasiat obat seperti senyawa polifenol, yang biasa digunakan sebagai antibakteri dan antioksidan. Salah satu tumbuhan yang mengandung senyawa polifenol adalah daun bangun-bangun. Penelitian ini bertujuan untuk mengetahui daya antibakteri dan antioksidan ekstrak etanol daun bangun-bangun.
Sampel (daun bangun-bangun) diperoleh dari daerah Tembung kabupaten Deli Serdang. Ekstrak dihasilkan dengan cara maserasi menggunakan etanol. Daya antibakterinya diukur dengan metode difusi agar menggunakan punch hole kemudian diukur diameter hambat pertumbuhan bakteri Staphylococcus aureus dan Escherichia coli. Daya antioksidannnya diukur dengan metode penghambatan oksidasi minyak kedelai selama penyimpanan pada suhu 40oC (0, 3, 5, dan 7 hari), dengan BHT sebagai pembanding.
Hasil penelitian menunjukkan bahwa ekstrak etanol daun bangun-bangun mempunyai daya antibakteri yang cukup besar yaitu pada konsentrasi 4% memiliki diameter hambatan 27,16 mm untuk Staphylococcus aureus dan 24,15 mm untuk bakteri Escherichia coli. Daya antioksidan meningkat dengan peningkatan jumlah ekstrak yang ditambahkan yaitu pada konsentrasi 1%(b/b) daya antioksidan sebesar 50,76%, pada konsentrasi 2%(b/b) daya antioksidan sebesar 54,97%, tetapi daya antioksidan ekstrak dengan konsentrasi 1% dan 2%, masih lebih rendah dari daya antioksidan BHT 0,02% (daya antioksidannya 58,80%). Namun pada konsentrasi ekstrak 3%(b/b) daya antioksidan lebih tinggi dari BHT yaitu 63,89%.
Kata kunci: daun bangun-bangun (Coleus amboinicus Lour.), ekstrak etanol,
Examination of Antibacterial and Antioxidant bangun-bangun’s leaf (Coleus amboinicus Lour.) ethanol extract
Abstract
Plant contain various chemical compounds such as polyphenolic compounds which usually used as antibacterial and antioxidant. One of plant contain polyphenolic compounds is bangun-bangun leaf. The purpose of this research is to examine antibacterial and antioxidant of bangun-bangun’s leaf ethanol extract.
Sample (bangun-bangun’s leaf) was obtained from Tembung’s area, Deli Serdang District. Extract was obtained by maseration with ethanol. Antibacterial activity was measured by agar difution methode, using punch hole, and then diameter inhibition of bacteri Staphylococcus aureus and Escherichia coli was measured. Antioxidant activity measured by method of the oxidation inhibition of soybean oil during storage at 40oC (0, 3, 5, and 7 days) with BHT as positive control.
The result of this research showed that the antibacterial activity of bangun-bangun’s leaf ethanol extract is had large enough, with its concentration 4% had zone inhibition 27,16 mm for Staphylococcus aureus and 24,15 mm for Escherichia coli. The antioxidant activity is increased with the increase of the amount extract added. At 1% of concentration, showed that the antioxidant activity was 50,76%, at 2% of concentration the antioxidant activity was 54,97%. But the antioxidant activity extract with 1% and 2% of concentration was lower than BHT 0,02% (antioxidant activity 58,80%). But at 3% of concentration was higher than BHT which antioxidant activity was 63,89%.
BAB I PENDAHULUAN 1.1Latar belakang
Obat tradisional telah dikenal luas pemakaiannya di Indonesia, baik untuk pemeliharaan kesehatan maupun untuk pengobatan penyakit-penyakit tertentu. Defenisi obat tradisional menurut UU No 23 tahun 1992 adalah bahan atau ramuan bahan berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan galenika, atau campuran dari bahan tersebut yang telah digunakan secara turun temurun oleh masyarakat.
Salah satu tumbuhan yang digunakan sebagai obat tradisional adalah daun bangun-bangun yang merupakan salah satu tanaman yang secara turun-temurun digunakan masyarakat Sumatera Utara sebagai menu sayuran sehari-hari bagi ibu-ibu yang baru melahirkan untuk memperlancar ASI.
Daun bangun-bangun berkhasiat sebagai karminatif, meningkatkan keluarnya ASI (laktagoga), menghilangkan nyeri (analgesik), pereda demam (antipiretik), batuk, difteri, sakit gigi, sariawan, keracunan tempe bongkrek, dan sebagai antiseptik (Dalimartha, 2004). Akan tetapi, penggunaan daun bangun-bangun pada masyarakat khususnya di Sumatera Utara hanya bagi ibu-ibu yang baru melahirkan, sementara jika ditinjau dari kandungan senyawa kimianya, daun bangun-bangun memiliki potensi yang baik sebagai antibakteri dan sebagai antioksidan alami.
Dari penelitian yang dilakukan oleh Christin Marganingsih Santosa dan Triana Hertiani (2005) tentang efek ekstrak air daun bangun-bangun pada aktivitas fagositosis netrofil tikus putih (Rattus norvegicus), menunjukkan bahwa ekstrak daun bangun-bangun mampu meningkatkan pertahanan tubuh dengan cara meningkatkan sifat fagositik sel netrofil, dimana sel netrofil merupakan komponen seluler sistem pertahanan tubuh yang berfungsi utama dalam fagositosis segala macam benda asing yang masuk ke dalam tubuh, dan dalam penelitian ini, sebagai benda asing digunakan bakteri Staphylococcus aureus.
pencemaran air, bila air minum yang sudah tercemar oleh bakteri ini dikonsumsi, maka dapat menyebabkan diare (Lay dan Hastowo, 1992)
Berdasarkan uraian diatas, dilakukan pengujian daya antibakteri dari ekstrak etanol daun bangun-bangun terhadap bakteri Staphylococcus aureus sebagai bakteri gram positif dan bakteri Escherichia coli sebagai bakteri gram negatif serta pengujian daya antioksidan dari ekstrak etanol daun bangun-bangun. 1.2Perumusan masalah
Adapun yang menjadi permasalahan dalam penelitian ini adalah:
- Apakah ekstrak etanol daun bangun-bangun mempunyai daya antibakteri terhadap bakteri Staphylococcus aureus dan Escherichia coli
- Apakah ekstrak etanol daun bangun-bangun mempunyai daya antioksidan 1.3Hipotesis
Hipotesis penelitian ini adalah:
- Ekstrak etanol daun bangun-bangun mempunyai daya antibakteri terhadap bakteri Staphylococcus aureus dan Escherichia coli
- Ekstrak etanol daun bangun-bangun mempunyai daya antioksidan 1.4Tujuan Penelitian
Tujuan penelitian ini adalah:
- Untuk mengetahui daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Staphylococcus aureus dan Escherichia coli
1.5 Manfaat penelitian
Manfaat penelitian ini sebagai sumber informasi kegunaan dari daun bangun-bangun sebagai antibakteri dan antioksidan, sehingga pemakaiannya pada masyarakat semakin luas.
1.6 Kerangka Penelitian
Variabel bebas Variabel terikat
- Konsentrasi ekstrak etanol daya hambat pertumbuhan bakteri Staphylococcus aureus dan
Escherichia coli
- konsentrasi ekstrak yang ditambahkan ke dalam minyak
BAB II
TINJAUAN PUSTAKA 2.1. Uraian Tumbuhan
Uraian tumbuhan meliputi, sistematika tumbuhan, nama daerah, morfologi tumbuhan, kandungan senyawa kimia, serta penggunaan tumbuhan.
2.1.1 Sistematika tumbuhan
Sistematika tumbuhan bangun-bangun adalah: Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Dicotyledonnae Ordo : Solanales Famili : Labiateae Genus : Coleus
Spesies : Coleus amboinicus Lour. (Depkes RI, 2000) 2.1.2 Nama umum
Nama umum/dagang : Daun jinten 2.1.3 Nama Daerah
Sumatera : Bangun-bangun (Batak), Sukan (Melayu)
Jawa : Ajiran (Sunda), Daun Jinten (Jawa Tengah), Daun Kambing (Madura)
Bali : Iwak
2.1.4 Morfologi Tumbuhan
Coleus amboinicus Lour. merupakan tumbuhan semak menjalar, batangnya berkayu, lunak, beruas-ruas, ruas yang menempel ditanah akan tumbuh akar, mudah patah, penampang bulat, diameter pangkal ± 15 mm, tengah ± 10 mm, dan ujung ± 5 mm, batang yang masih muda berambut kasar dan hijau pucat. Berakar tunggang, berwarna putih kotor. Daunnya tunggal, mudah patah, bulat telur, tepi beringgit, ujung dan pangkal membulat, berambut, panjang 6,5-7 cm, lebar 5,5-6,5 cm, tangkai panjang 2,4-3 cm, pertulangan menyirip dan berwarna hijau muda. Bunganya majemuk, bentuk tandan, berambut halus, kelopak bentuk mangkok, setelah mekar pecah menjadi lima, berwarna hijau keunguan, putik satu, panjangnya ± 17 mm, kepala putik coklat, benang sari empat, kepala sari kuning, mahkota bentuk mangkok berwarna ungu (Depkes RI, 2000).
2.1.5 Kandungan kimia
Daun Coleus amboinicus mengandung saponin, flavonoida, polifenol dan minyak atsiri ( Depkes RI ,2000)
2.1.6 Penggunaan Tumbuhan
Daun bangun-bangun (Coleus amboinicus ) digunakan sebagai obat sariawan, obat batuk, karminatif, meningkatkan keluarnya ASI (laktagoga), analgesik, antipiretik, antiseptik (Dalimartha. S, 2004)
2.2 Bakteri
2.2.1. Bakteri gram positif
Dinding sel bakteri gram positif tersusun atas beberapa lapisan peptidoglikan, dan strukturnya tebal dan keras. Dinding selnya juga tersusun atas teichonic acid yang mengandung alkohol (seperti gliserol) dan posfat (Tortora,
2001). Staphylococcus termasuk bakteri gram positif dengan familia Micrococcaceae. Staphylococcus merupakan bakteri yang selnya berbentuk bulat, biasanya tersusun dalam rangkaian tak beraturan seperti anggur. Bakteri ini tumbuh pada suhu 37ºC dan mempunyai pigmen putih sampai kuning tua. Salah satu contoh dari bakteri Staphylococcus adalah Staphylococcus aureus. Adapun sistematika dari bakteri Staphylococcus aureus adalah sebagai berikut:
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacteriales Suku : Micrococcaceae Genus : Staphylococcus
Species : Staphylococcus aureus (Baskoro,1996). 2.2.2. Bakteri Gram Negatif
habitat alaminya adalah saluran usus manusia dan hewan. Salah satu contoh bakteri yang termasuk dalam familia Enterobacteriaceae adalah Escherichia coli. Bakteri ini merupakan bakteri yang dibutuhkan oleh manusia dalam jumlah tertentu, tetapi dapat juga menimbulkan penyakit jika melebihi flora normal. Morfologinya berupa koloni yang bundar, cembung, tipis dengan tepi yang nyata (Nugroho dan Maulany, 1996).
Adapun sistematika dari bakteri Escherichia coli adalah sebagai berikut: Divisi : Schizophyta
Kelas : Schizomycetes Ordo : Eubacteriales Suku : Enterobacteriaceae Genus : Escherichia
Species : Escherichia coli (Baskoro, 1996).
2.2.3 Fase Pertumbuhan Bakteri (Hadioetomo, 1986; Lay dan Hastowo, 1992)
Fase pertumbuhan bakteri meliputi fase lamban, fase logaritma, fase statis dan fase penurunan atau kematian.
a. Fase Lamban (lag phase)
b. Fase Logaritma (exponential phase)
Fase ini terjadi setelah sel bakteri menyesuaikan diri terhadap lingkungan baru. Ciri-ciri fase ini yaitu sel membelah dengan laju yang konstan, jumlah sel bakteri baru meningkat secara eksponensial, massa menjadi dua kali lipat dengan laju yang sama dan keadaan pertumbuhan seimbang.
c. Fase Statis (stationary phase)
Dalam fase ini kecepatan tumbuh sama dengan kecepatan mati. Ciri-ciri fase ini beberapa sel mati sedangkan yang lain tumbuh dan membelah sehingga jumlah sel yang hidup menjadi tetap.
d. Fase Penurunan (period of decline) atau Fase Kematian
Ciri-ciri fase ini yaitu sel yang mati lebih cepat daripada terbentuknya sel-sel baru karena jumlah nutrisi berkurang, terjadi akumulasi zat toksin dan laju kematian mengalami percepatan menjadi eksponensial.
2.2.4 Uji Aktivitas Antimikroba
Penentuan kepekaan bakteri patogen terhadap antimikroba dapat dilakukan dengan beberapa metode seperti metode dilusi, difusi dan turbidimetri.
1. Metode dilusi
2. Metode difusi
Metode yang paling sering digunakan dan biasanya menggunakan cakram. Ada beberapa jenis cakram yaitu cakram kertas, cakram silinder dan punch hole. Cakram tersebut yang berisi sejumlah tertentu obat ditempatkan pada permukaan medium padat yang sebelumnya telah diinokulasi bakteri uji pada permukaannya. Setelah diinkubasi, diameter zona hambatan sekitar cakram dipergunakan untuk mengukur kekuatan hambatan obat terhadap mikroorganisme yang uji (Mudihardi, dkk, 2001).
3. Metode Turbidimetri
Jumlah sel bakteri dapat dihitung dengan cara mengetahui kekeruhan (turbiditas) kultur. Semakin keruh suatu kultur, semakin banyak jumlah selnya. Prinsip dasar metode turbidimetri adalah jika cahaya mengenai sel maka sebagian cahaya diserap dan sebagian cahaya diteruskan. Jumlah cahaya yang diserap proporsional (berbanding lurus dengan jumlah bakteri (Irianto. K, 2002)
2.3. Minyak Kedelai
pada industri modern umumnya minyak kedelai diekstraksi menggunakan pelarut n-heksana. Setelah minyak terekstrak, pelarut biasanya dipisahkan dari minyak dengan proses penguapan yang akan menghasilkan minyak kasar yang siap untuk diproses lebih lanjut (Snyder and Kwon, 1987).
2.3.1 Oksidasi Minyak Kedelai
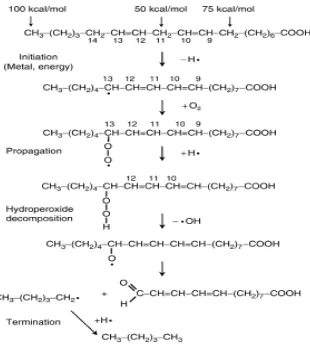
Minyak kedelai mengandung asam lemak tidak jenuh yang tinggi, yaitu asam oleat 22,3%, asam linoleat 54,5% dan asam linolenat 8,3% (Theodore.J, 1983). Tingginya kadar asam lemak tidak jenuh pada minyak kedelai menyebabkan minyak dapat dengan mudah dioksidasi oleh molekul oksigen membentuk hidroperoksida. Proses oksidasi ini dapat menyebabkan hilangnya nilai gizi dan terbentuknya rasa, warna dan bau yang tidak diinginkan, bahkan dapat menyebabkan terbentuknya zat racun. Panas, cahaya, logam dan spesies oksigen reaktif dapat memfasilitasi pembentukan radikal dari lemak. Oksidasi lemak oleh spesies oksigen reaktif melibatkan tiga langkah, yaitu inisiasi, propagasi, dan terminasi. Pada tahap inisiasi terjadi serangan spesies oksigen reaktif yang mampu melepaskan sebuah atom hidrogen dari sebuah gugus metilen. Serangan ini menghasilkan radikal bebas dari asam lemak dan kemudian bereaksi dengan O2 membentuk radikal peroksil (ROO.). Radikal peroksil bersama dengan
Inisiasi : RH R. + H Propagasi : R. + O2 ROO.
ROO.+ RH ROOH + R. Terminasi : R.+ R. R-R
R. + ROO. ROOR ( Deman. J, 1980)
Adanya ikatan rangkap pada asam lemak memperlemah ikatan C-H pada atom karbon yang dekat dengan ikatan rangkap tersebut sehingga atom H pada ikatan tersebut dapat dengan mudah diambil oleh spesies oksigen reaktif menghasilkan radikal bebas dari asam lemak tidak jenuh. Mekanisme reaksi autooksidasi pada asam linoleat dapat dilihat pada gambar 1.
Produk oksidasi primer senyawa lemak adalah hidroperoksida yang bersifat relatif stabil pada temperatur ruangan atau tanpa adanya logam. Akan tetapi pada suhu yang tinggi (terutama pada suhu diatas 60oC) atau adanya logam meskipun dalam jumlah yang sangat sedikit dapat berperan sebagai prooksidan, yang kemudian membentuk produk oksidasi sekunder aldehid dan keton (Cahyadi, 2006).
Gambar 1. Mekanisme Autoksidasi Asam Lemak Tak Jenuh oleh Spesies Oksigen Reaktif
2.4. Radikal Bebas
Oksigen (RBO), yaitu hidroksil (OH.), Superoksida (O2 .
-), Nitrogen monoksida (NO.
), dan peroksil (ROO
.) (Silalahi, J, 2006). 2.5 Pengukuran oksidasi lemak
Metode uji oksidasi lemak dapat dikelompokkan menjadi dua yaitu yang bersifat uji prediksi atau sebagai indikator. Pengujian prediktif menggunakan kondisi pengujian yang diakselerasi untuk mengetahui stabilitas dari lemak atau makanan yang akan diolah, mengukur efektifitas antioksidan, dan umur simpan produk makanan. Dalam kelompok ini contohnya adalah AOM (Active Oxigen Method), OSI (Oxidative Stability Index), angka iodine, OBT (Oxygen Bomb Test). Pengujian yang berfungsi sebagai indikator dimaksudkan untuk mengukur secara kuantitatif tingakat oksidasi lemak pada makanan. Contoh dalam kelompok ini adalah angka peroksida, Uji TBA, nilai anisidin, nilai heksanal, dan asam lemak bebas (Raharjo, 2006).
Bilangan peroksida
Bilangan peroksida didefenisikan sebagai miliekivalen peroksida per kilogram sampel. Pengukuran dilakukan dengan titrasi iodometri yang didasarkan pada reduksi hidroperoksida (ROOH) dengan ion iodida (I-). Iodium yang terbentuk sesuai dengan konsentrasi peroksida yang ada. Iodium yang dibebaskan kemudian dititrasi dengan larutan standard natrium tiosulfat menggunakan indikator amilum. Adapun reaksi kimia penentuan bilangan peroksida seperti berikut: ROOH + 2H+ + 2KI I2 + ROH + H2O + 2K+
I2 + amilum+ 2Na2S2O3 2NaI + amilum + Na2S4O6
Biru tidak berwarna
2.6 Antioksidan
Antioksidan merupakan senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas. Antioksidan atau reduktor berfungsi untuk mencegah terjadinya oksidasi atau menetralkan senyawa yang telah teroksidasi (Silalahi, J, 2006). Atas dasar fungsinya, antioksidan dapat dibedakan menjadi lima:
(a) Antioksidan primer, merupakan sistem enzim pada tubuh manusia, contohnya: enzim superoksida dismutase.
(b) Antioksidan sekunder, yang berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar, contohnya vitamin E, vitamin C dan betakaroten.
(c) Antioksidan tersier, yang bekerja memperbaiki sel sel dan jaringan yang rusak karena serangan radikal bebas, misalnya sistem enzim metionin sulfoksidan reduktase.
(d) Oxygen scavenger, yang mampu mengikat oksigen sehingga tidak mendukung reaksi oksidasi reduksi, misalnya vitamin C.
(e) Chelators atau sequestrant, yang dapat mengikat logam yang mengkatalisis reaksi oksidasi misalnya asam sitrat (Kumalaningsih, 2006).
Antioksidan yang paling umum adalah senyawa fenol atau amina aromatis. Mekanisme antioksidan erat kaitannya dengan proses transfer atom hidrogen dari gugus fenol senyawa antioksidan kepada substrat. Gugus fenol pada antioksidan inilah yang memiliki kemampuan untuk menangkap radikal bebas dari rantai peroksidasi (ROO.) dengan reaksi sebagai berikut:
Kemudahan antioksidan untuk memberikan atom hidrogennya pada radikal bebas menunjukkan aktivitas dari antioksidan tersebut. Fenol yang kehilangan atom hidrogennya akan menjadi radikal ArO., yang dapat menjadi stabil kembali melalui penyusunan ulang atau resonansi. Mekanisme antioksidan fenol seperti Butylated Hydroxytoluen (BHT), dalam menangkap radikal bebas dapat dilihat dalam reaksi.
BAB III
METODOLOGI PENELITIAN
Jenis penelitian yang dilakukan adalah penelitian eksperimental. Metodologi penelitian meliputi pengumpulan dan preparasi bahan, pembuatan ekstrak etanol daun bangun-bangun, skrining fitokimia, isolasi minyak kedelai, pengujian daya antibakteri terhadap pertumbuhan bakteri Staphylococus aureus dan Escherichia coli dengan metode difusi agar menggunakan punch hole, kemudian daya hambat (Zona jernih) diukur dengan menggunakan jangka sorong serta pengujian daya antioksidan melalui pengukuran bilangan peroksida. Penelitian ini dilakukan di Laboratorium Farmakognosi Fakultas Farmasi USU, Laboratorium Sintesa Bahan Obat Fakultas Farmasi USU, dan Laboratorium Mikrobiologi Departemen Biologi FMIPA USU.
3.1 Alat-alat yang digunakan
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas, oven (Gallenkamp), autoklaf (Webeco), inkubator (Fisher Scientific), lemari pendingin (Precicion), neraca kasar, neraca analitik (Mettler AE 200), jarum ose, jangka sorong, pinset, bunsen, pencetak lubang (punch hole), bola karet, vacuum rotary evaporator (Buchi).
3.2 Bahan-bahan yang digunakan
Bahan tumbuhan yang digunakan adalah daun bangun-bangun (Coleus amboinicus L.) berwarna hijau tua, serta kacang kedelai. Bahan kimia yang
magnesium, timbal (II) asetat, natrium tiosulfat, kalium bikromat, natrium karbonat, natrium hidroksida, asam klorida, kecuali Butil Hidroksitoluen/BHT (sigma), nutrient agar (Difco), arang aktif, etanol hasil destilasi.
Bakteri yang digunakan : Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 25922
3.3 Penyiapan bahan
Penyiapan bahan meliputi pengambilan bahan, determinasi tumbuhan dan pengolahan bahan tumbuhan.
3.3.1 Pengambilan bahan
Pengambilan bahan dilakukan secara purposif yaitu tanpa membandingkan dengan tanaman yang sama dari daerah lain. Bahan diambil pada sore hari, dan bagian yang diambil adalah daun bangun-bangun (Coleus amboinicus L.) yang masih segar, berwarna hijau tua. Daun bangun-bangun diambil dari Tembung, Kampung Tapanuli, Kabupaten Deli Serdang. Kacang kedelai sebagai bahan pembuatan minyak kedelai yang digunakan sebagai media pengukuran bilangan peroksida, diambil dari pajak Sore Padang Bulan.
3.3.2 Determinasi tumbuhan
3.3.3 Pengolahan bahan
Daun bangun-bangun yang telah dikumpulkan, dibersihkan (disortasi basah), dicuci dengan air sampai bersih, kemudian ditiriskan lalu disebarkan, setelah itu daun ditimbang. Kemudian daun dikeringkan di oven dengan suhu tidak melebihi 60°C sampai daun kering dan mudah rapuh, berat dari daun yang kering ditimbang. Kemudian disimpan di tempat yang terlindung dari sinar matahari.
3.4 Pembuatan larutan pereaksi 3.4.1 Pereaksi Mayer
Larutan raksa (II) klorida P 2,266% b/v sebanyak 60 ml dicampur dengan 10 ml larutan kalium iodida P 50 % b/v, kemudian ditambahkan air secukupnya hingga 100 ml (Depkes RI, 1980).
3.4.2 Pereaksi Dragendorff
Larutan bismut nitrat P 40% b/v dalam asam nitrat P sebanyak 20 ml dicampur dengan 50 ml kalium iodida P 54,4% b/v, didiamkan sampai memisah sempurna. Lalu diambil lapisan jernihnya dan diencerkan dengan air secukupnya hingga 100 ml (Depkes RI, 1980).
3.4.3 Pereaksi Bouchardat
Sebanyak 4 g Kalium iodida P dilarutkan dalam air secukupnya, lalu ditambahkan 2 g iodium P kemudian ditambahkan air hingga 100 ml (Depkes RI, 1980).
3.4.4 Pereaksi Molish
3.4.5 Larutan besi (III) klorida 1% b/v
Sebanyak 1 g besi (III) klorida dilarutkan dalam air secukupnya hingga 100 ml (Depkes RI, 1980).
3.4.6 Larutan timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat P dilarutkan dalam air bebas karbon dioksida hingga 100 ml (Depkes RI, 1980).
3.4.7 Larutan Natrium Hidroksida 2 N
Sebanyak 8,001 g natrium hidroksida, dilarutkan dalam air secukupnya hingga 100 ml (Depkes RI, 1980).
3.4.8 Pereaksi Liebermann-Burchard
Sebanyak 20 ml asam asetat anhidrat dicampur dengan 1 ml asam sulfat pekat. Larutan ini harus dibuat baru ( Harborne, 1987).
3.4.9 Larutan asam klorida 2 N
Larutan asam klorida pekat sebanyak 17 ml ditambahkan air suling sampai 100 ml (Ditjen POM, 1979).
3.4.10 Larutan asam sulfat 2 N
Larutan asam sulfat pekat sebanyak 9,8 ml ditambahkan air suling sampai 100 ml (Ditjen POM, 1979).
3.4.11 Larutan Standar Natrium Tiosulfat 0,002 N
3.4.12 Pembakuan Larutan Standar Na2S2O30,002 N
Ditimbang dengan seksama sebanyak 4,2 mg kalium bikromat yang sebelumnya telah dihaluskan dan dikeringkan pada suhu 1200C selama 4 jam, dan dilarutkan dalam 100 ml air suling dalam erlenmeyer. Digoyang hingga larut, dan ditambah dengan cepat 60 mg kalium iodida, 40 mg natrium bikarbonat dan 5 ml asam klorida. Ditutup erlenmeyer dengan plastik dan karet, dikocok hingga larut, kemudian dibiarkan ditempat yang gelap selama 10 menit. Dititrasi iodium yang dibebaskan dengan larutan natrium tiosulfat hingga berwarna hijau kekuningan, kemudian ditambahkan 3 ml larutan kanji dan dilanjutkan titrasi hingga warna biru hilang. Kemudian normalitas larutan dihitung (Ditjen POM, 1995).
N = BEg x V1
Keterangan: N = Normalitas Na2S2O3
g = Berat K2Cr2O7 yang ditimbang (mg)
V = Volume Na2S2O3yang terpakai (ml)
3.4.13 Larutan HCl 25%
Dipipet asam klorida 37% sebanyak 67,65 ml, kemudian diencerkan dengan air suling secukupnya sampai 100 ml (Ditjen POM, 1979).
3.4.14 Indikator Kanji
Ditimbang sebanyak 500 mg tepung kanji, kemudian disuspensikan dalam 5 ml air suling. Lalu ditambahkan air mendidih sedikit demi sedikit hingga 100 ml. Dididihkan beberapa menit hingga menjadi transparan, kemudian didinginkan (Ditjen POM, 1979).
3.4.15 Larutan NaOH 12%
Ditimbang NaOH sebanyak 12 g, kemudian dilarutkan dalam air suling hingga 100 ml (Ditjen POM, 1979).
3.5 Penetapan Kadar Air 3.5.1 Penjenuhan Toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,01 ml
3.5.2 Penetapan kadar air
Ke dalam labu yang berisi toluen jenuh diatas, dimasukkan 5 g serbuk daun bangun-bangun yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluene memisah sempurna, volume air dibaca dengan ketelitian 0,01 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen. (Ditjen POM, 1979). Hasil selengkapnya dapat dilihat pada lampiran 3.
3.6 Pembuatan Ekstrak
Pembuatan ekstrak dilakukan dengan cara maserasi yaitu sebanyak 400 g serbuk daun bangun-bangun ditambahkan dengan etanol 96% sebanyak 3000 ml, ditutup dan dibiarkan selama 5 hari terlindung dari cahaya, sambil berulang-ulang diaduk. Setelah 5 hari sari diserkai, ampas diperas. Cuci ampas dengan etanol 96% sebanyak 1000 ml kemudian ditutup dan terlindung dari cahaya selama 2 hari, kemudian dienap tuangkan dan disaring. Maserasi dihentikan jika maserat tidak berwarna dan diuji secara kualitatif dengan Besi (III) klorida tidak memberikan hasil positif. Maserat yang dihasilkan dirotary evaporator pada suhu tidak lebih dari 50°C, hingga diperoleh ekstrak kental, ekstrak kental dipindahkan ke dalam eksikator ( Ditjen POM, 1979).
3.7 Skrining fitokimia daun bangun-bangun (Coleus amboinicus Lour.) 3.7.1 Pemeriksaan Alkaloida
Serbuk daun bangun-bangun ditimbang sebanyak 0,5 g, kemudiaan ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring, filtrat dipakai untuk uji alkaloida. Diambil 3 tabung reaksi, lalu ke dalam masing-masing tabung reaksi dimasukkan 0,5 ml filtrat.
Pada tabung I : ditambahkan 2 tetes pereaksi mayer Pada tabung II : ditambahkan 2 tetes pereaksi dragendorff Pada tabung III : ditambahkan 2 tetes pereaksi bouchardat
3.7.2 Pemeriksaan Flavonoida
Sebanyak 10 g serbuk simplisia ditambah air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas. Kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium Dan 1 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terdapat warna merah kekuningan atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.7.3 Pemeriksaan Glikosida
Sebanyak 3 g serbuk daun bangun-bangun ditimbang, lalu disari dengan 30 ml campuran dari 7 bagian etanol 95% dan 3 bagian air suling. Kemudiaan direfluks selama 10 menit, didinginkan, lalu disaring. Diambil 20 ml filtrat , ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran 2 bagian isopropanol dan 3 bagian kloroform, perlakuan ini diulangi sebanyak 3 kali. Sari air dikumpulkan dan ditambahkan Na2SO4 anhidrat, disaring, kemudiaan
diuapkan pada temperatur tidak lebih dari 500C, sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut: Sepersepuluh ml larutan percobaan dimasukkan dalam tabung reaksi, kemudian diuapkan di atas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes larutan perekasi Molish, lalu ditambahkan dengan hati-hati 2 ml asam sulfat pekat, terbentuk cincin ungu pada batas kedua cairan, menunjukkan adanya ikatan gula (glikon) (Depkes RI, 1995).
3.7.4 Pemeriksaan Glikosida Antrakinon
dikocok dan didiamkan. Lapisan benzen dipisahkan dan disaring, kemudian kocok dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah menunjukkan adanya antrakinon (Depkes RI, 1995).
3.5.5 Pemeriksaan Saponin
Sebanyak 0,5 g serbuk daun bangun-bangun dimasukkan ke dalam tabung reaksi, ditambahkan 10 ml air suling panas, didinginkan, kemudian dikocok kuat-kuat selama 10 detik. Saponin positif jika terbentuk busa yang stabil tidak kurang dari 10 menit setinggi 1 sampai 10 cm dan dengan penambahan 1 tetes asam klorida 2 N buih tidak hilang (Depkes RI, 1995).
3.7.6 Pemeriksaaan Tannin
Sebanyak 0,5 g serbuk daun bangun-bangun disari dengan 10 ml air suling lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru atau kehitaman menunjukkan adanya tannin (Depkes RI, 1989).
3.7.7 Pemeriksaan Triterpenoid/ Steroida
3.8 Penentuan aktivitas antibakteri 3.8.1 Sterilisasi Alat dan Bahan
Alat dan bahan yang digunakan dalam uji aktivitas antibakteri ini disterilkan lebih dahulu sebelum dipakai. Media pertumbuhan disterilkan di autoklaf pada suhu 121°C selama 15 menit dan alat-alat gelas disterilkan di oven pada suhu 160-170°C selama 1-2 jam. Jarum ose dibakar dengan nyala bunsen. 3.8.2 Pembuatan Media
3.8.2.1 Larutan NaCl 0,9% Komposisi : Natrium klorida 9 g
Air suling hingga 1000 ml Cara pembuatan:
Ditimbang natrium klorida 9 g, lalu dilarutkan dalam air suling sedikit demi sedikit dalam labu ukur 1000 ml sampai larut sempurna. Lalu ditambahkan air suling sampai garis tanda. Disterilkan di autoklaf pada suhu 1210C selama 15 menit (Depkes RI, 1995).
3.8.2.2 Nutrient Agar
Komposisi : bacto-beef extract 3 g Bacto-peptone 5 g Bacto agar 15 g
Aqua ad 1000 ml
Cara pembuatan:
larut sempurna. Disterilkan dalam autoklaf pada temperatur 1210C selama 15 menit ( DIFCO, 1977)
3.8.2.3 Pembuatan agar Miring
Ke dalam tabung reaksi steril dimasukkan 3 ml media nutrien agar steril, didiamkan pada temperatur kamar sampai sediaan membeku pada posisi miring kira-kira 450C. Kemudian disimpan dalam lemari pendingin.
3.8.2.4 Suspensi Standar Mc. Farland (Lennete, et al., 2005) Komposisi: Larutan asam sulfat 0,18 M 99,5 ml Larutan barium klorida 0,048 M 0,5 ml Cara pembuatan:
Dicampurkan kedua larutan di atas ke dalam tabung reaksi dan dikocok homogen. Apabila kekeruhan suspensi bakteri uji sama dengan kekeruhan suspensi standar, berarti konsentrasi suspensi bakteri adalah 108 CFU/ml.
3.8.4 Pembuatan Stok Kultur Bakteri 3.8.4.1 Bakteri Staphylococcus aureus
Diambil satu ose koloni bakteri Staphylococcus aureus dengan menggunakan jarum ose steril, lalu ditanamkan pada media Nutrient Agar miring dengan cara menggores, setelah itu diinkubasi dalam inkubator pada suhu 36 ± 1ºC selama 18-24 jam.
3.8.4.2 Bakteri Escherichia coli
menggores, setelah itu diinkubasi dalam inkubator pada suhu 36 ± 1ºC selama 18-24 jam.
3.8.5 Penyiapan Inokulum
3.8.5.1 Bakteri Staphylococcus aureus
Dari stok kultur Staphylococcus aureus yang telah tumbuh diambil dengan jarum ose steril lalu disuspensikan dalam tabung yang berisi 10 ml larutan natrium klorida 0,9%, kemudian diinkubasi selama 2 jam, sampai didapat kekeruhan suspensi bakteri sama dengan kekeruhan suspensi standar Mc. Farland, berarti konsentrasi suspensi bakteri adalah 108 CFU/ml. Setelah itu dilakukan pengenceran dengan memipet 0,1 ml suspensi bakteri (108 CFU/ml), dimasukkan ke dalam tabung steril dan ditambahkan larutan natrium klorida 0,9% sebanyak 9,9 ml dan dikocok homogen. Dari sini diperoleh suspensi bakteri dengan konsentrasi 106 CFU/ml.
3.8.5.2 Bakteri Escherichia coli
3.9 Pengenceran ekstrak etanol
Ditimbang ekstrak etanol daun bangun-bangun sebanyak 0,4 gram, lalu ditambahkan etanol hasil destilasi sampai 10 ml, sehingga didapat konsentrasi ekstrak 4%. Kemudian dilakukan pengenceran, hingga di dapat konsentrasi 3%, 2%, 1%, 0,8%, 0,5%, 0,4%, 0,3%,0,2%, 0,1%.
3.10 Pengujian daya antibakteri
3.10.1 Pengujian daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Staphylococcus aureus.
Sebanyak 20 ml Nutrien Agar dengan suhu 45-500C dimasukkan ke dalam tabung reaksi steril, lalu ditambahkan 0,1 ml inokulum ke dalam media, kemudian divorteks agar media dan suspensi bakteri tercampur merata, setelah itu dituang media Nutrient Agar ke dalam cawan petri steril, dibiarkan memadat. Pada media yang telah padat, dilubangi dengan pencetak lubang (punch hole) lalu diteteskan ekstrak etanol daun bangun-bangun masing-masing sebanyak 0,1 ml dengan berbagai konsentrasi, dibiarkan 15 menit, kemudian diinkubasi dalam inkubator pada suhu 36 ± 1ºC selama 18-24 jam, setelah itu diukur diameter daerah hambatan (zona jernih) dengan menggunakan jangka sorong. Digunakan etanol sebagai kontrol. (Percobaan dilakukan sebanyak 3 kali).
3.10.2 Pengujian daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Escherichia coli
media yang telah padat dilubangi dengan pencetak lubang (punch hole) lalu diteteskan ekstrak etanol daun bangun-bangun masing-masing sebanyak 0,1 ml dengan berbagai konsentrasi, dibiarkan 15 menit, kemudian diinkubasi dalam inkubator pada suhu 36 ± 1ºC selama 18-24 jam, setelah itu diukur diameter daerah hambatan (zona jernih) dengan menggunakan jangka sorong. Digunakan etanol sebagai kontrol. (Percobaan dilakukan sebanyak 3 kali).
3.11 Isolasi minyak kedelai
3.11.1 Pembuatan Minyak Kedelai
Kacang kedelai dibersihkan dari pengotor, kemudian dihaluskan dengan menggunakan blender hingga menjadi pecahan kecil. Kemudian ditimbang sebanyak 50 g, lalu dibungkus dengan kertas saring, dimasukkan ke dalam alat soklet ditambahkan pelarut n-heksana. Dipasang kondensor, lalu disokletasi sampai filtrat tidak berwarna. Pemisahan minyak dan pelarut dapat dilakukan dengan menggunakan alat rotary evaporator vakum.
3.11.2 Pemurnian Minyak Kedelai 3.11.2.1 Degumming
Degumming dilakukan untuk untuk memisahkan fospolipid yang terhidrasi
dari minyak. Minyak kedelai hasil sokletasi ditambahkan air suling 2% dari berat minyak, aduk rata kemudian dipanaskan pada suhu 700C selama 30 menit. Campuran minyak disentrifugasi. (Snyder & Kwon, 1987).
3.11.2.2 Alkali Refining
Alkali refining dilakukan untuk memisahkan sabun yang terbentuk.
dengan air yang telah dipanaskan pada suhu 940C dan kemudian campuran disentrifugasi (Snyder & Kwon, 1987).
3.11.2.3 Bleaching
Bleaching dilakukan untuk menghilangkan/memucatkan warna. Minyak
kedelai hasil alkali refining ditambah karbon aktif sebanyak 1% dari berat minyak, diaduk merata lalu disaring (Snyder & Kwon, 1987).
3.12 Pengujian daya antioksidan
Penentuan daya antioksidan dilakukan berdasarkan peningkatan bilangan peroksida. Aksi oksigen terhadap minyak kedelai ditentukan dengan membandingkan nilai peroksida kontrol dengan nilai peroksida setelah penyimpanan selama 7 hari pada suhu 400C. Ditimbang 0,5 g minyak kedelai, dimasukkan ke dalam wadah berwarna gelap, ditambahkan sebanyak 1% (b/b), 2% (b/b), 3% (b/b) ekstrak etanol daun bangun-bangun. Diinkubasi pada suhu 400C selama 7 hari. Peningkatan bilangan peroksida dapat dilihat dalam 7 hari pada penyimpanan selama 0, 3, 5, dan 7 hari. Kemudian diberi perlakuan yang sama terhadap minyak kedelai kontrol (tanpa penambahan ekstrak etanol daun bangun-bangun), minyak kedelai dengan penambahan BHT 0,02% (b/b) (Pohan, 2002).
sampai berwarna kuning muda. Kemudian ditambah 0,5 ml indikator kanji, dan titrasi dilanjutkan sampai warna biru hilang (Ronald, E.,2005).
Dari hasil titrasi yang diperoleh ditentukan angka peroksidanya yang dinyatakan sebagai meq oksigen aktif per-kg dengan rumus:
Bilangan Peroksida =
Metode yang digunakan untuk menetukan daya antioksidan dari sampel adalah metode Saito dan Ishihara (Pohan, 2002). Daya antioksidan dihitung dari plot angka peroksida selama penyimpanan pada suhu 400C selama penyimpanan 0, 3, 5, dan 7 hari. Daya antioksidan diperkirakan dengan membandingkan slope linier dari minyak kedelai sebagai kontrol dengan plot angka peroksida minyak kedelai dengan penambahan ekstrak.
% Aktivitas antioksidan =
c y c
S S S −
X 100%
Keterangan:Sc = Slope dari plot angka peroksida minyak kedelai kontrol
Sy = Slope dari angka peroksida minyak kedelai dengan penambahan
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Identifikasi Tumbuhan
Tumbuhan yang digunakan pada penelitian ini adalah daun bangun-bangun dan kacang kedelai, yang masing-masing gambarnya dapat dilihat pada Lampiran 13 halaman 57 dan Lampiran 14 halaman 58. Hasil identifikasi daun bangun-bangun yang dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bogor menunjukkan bahwa daun bangun-bangun termasuk dalam suku Lamiaceae species Coleus amboinicus Lour., seperti yang tertera pada Lampiran 1 halaman 45.
4.2 Hasil Skrining Fitokimia
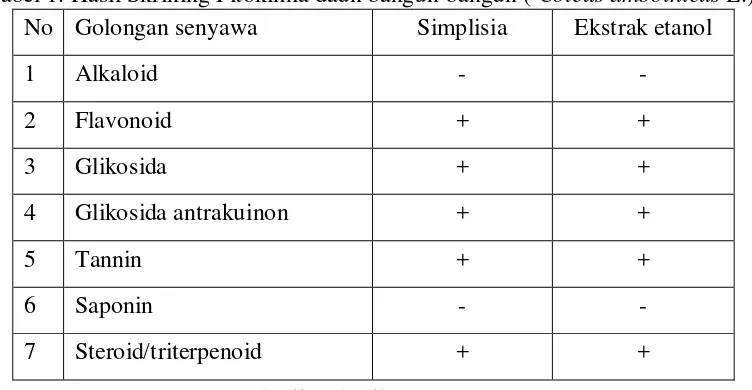
Skrining fitokimia terhadap daun bangun-bangun ( Coleus amboinicus L.) menunjukkan adanya golongan senyawa metabolit sekunder terlihat pada tabel 1. Tabel 1. Hasil Skrining Fitokimia daun bangun-bangun ( Coleus amboinicus L.)
No Golongan senyawa Simplisia Ekstrak etanol
1 Alkaloid - -
2 Flavonoid + +
3 Glikosida + +
4 Glikosida antrakuinon + +
5 Tannin + +
6 Saponin - -
7 Steroid/triterpenoid + +
Dari tabel 1 diperoleh hasil bahwa senyawa alkaloid tidak memberikan endapan putih dengan pereaksi mayer dan dengan pereaksi dragendorff tidak memberikan endapan kecoklatan. Senyawa flavonoid memberikan hasil positif dengan membentuk warna merah kekuningan pada lapisan amil alkohol. Senyawa glikosida memberikan hasil positif dengan terbentuk cincin ungu. Senyawa glikosida antrakinon memberikan hasil positif dengan terbentuknya warna merah setelah penambahan NaOH. Senyawa triterpenoid/steroid memberikan hasil positif dengan terbentuknya warna biru hijau setelah diberikan pereaksi Liebermann-Burchard. Senyawa tanin memberikan hasil positif dengan terbentuknya warna hijau setelah ditambah larutan FeCl3. Senyawa saponin tidak
memberikan reaksi positif karena tidak terbentuk busa yang stabil selama 10 menit pada saat pengocokan dengan air suling.
Senyawa-senyawa yang berkhasiat sebagai antibakteri dan antioksidan adalah golongan senyawa polifenol seperti flavonoid, tanin, glikosida.
Hasil penetapan kadar air pada daun bangun-bangun adalah 8,26% dan kadar ini memenuhi syarat, dimana Menurut Depkes RI, 1995 kadar air secara umum tidak lebih dari 10%, hasil penentuan kadar air dapat dilihat pada lampiran 3 halaman 60. Hasil penyarian 400 gram serbuk daun bangun-bangun yang dilakukan dengan metode maserasi diperoleh ekstrak kental 32,5 gram.
4.3 Daya Antibakteri
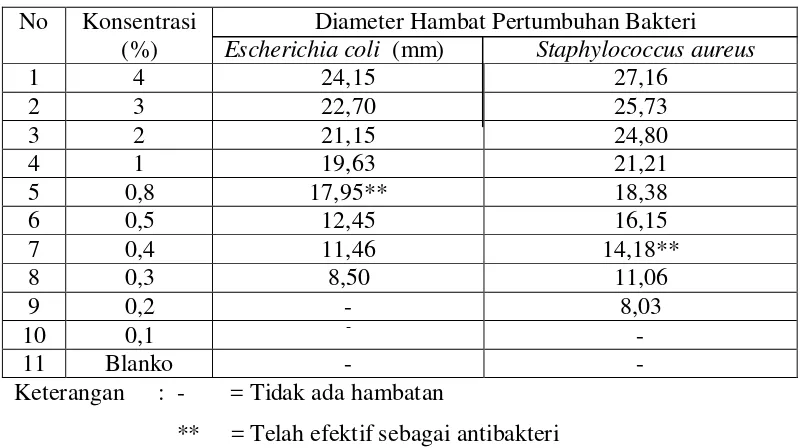
Tabel 2. Hasil uji daya antibakteri ekstrak etanol daun bangun-bangun terhadap bakteri Escherichia coli dan Staphylococcus aureus
No Konsentrasi (%)
Diameter Hambat Pertumbuhan Bakteri Escherichia coli (mm) Staphylococcus aureus blanko = Etanol hasil destilasi
Hasil uji daya antibakteri ekstrak etanol daun bangun-bangun (Coleus amboinicus L.) menunjukkan bahwa ekstrak etanol tersebut mempunyai potensi yang baik dalam menghambat pertumbuhan bakteri Gram positif (Staphylococcus aureus) dan bakteri Gram negatif (Escherichia coli). Hal ini dapat dilihat dari
menghambat pertumbuhan bakteri lagi, sementara pada bakteri Staphylococcus aureus tidak memberikan daya hambat yang memuaskan pada konsentrasi 0,3%
dan tidak menghambat pertumbuhan bakteri lagi pada konsentrasi 0,1%. Dari tabel diatas juga dapat dilihat bahwa bakteri Staphylococcus aureus lebih peka terhadap ekstrak etanol daun bangun-bangun (Coleus amboinicus L.) dibandingkan dengan bakteri Escherichia coli yang dapat dilihat dari luas zona bening yang dihasilkan diantara kedua bakteri tersebut. Hal ini dapat disebabkan karena bakteri Staphylococcus aureus tidak memiliki membran luar, sedangkan bakteri Escherichia coli memiliki membran luar yang tersusun atas lipopoliisakarida, lipoprotein, dan posfolipid . membran luar ini memiliki fungsi khusus seperti sebagai barier antibiotik tertentu (seperti penisilin), detergen. (Tortora.G., 2001).
Kemampuan ekstrak etanol daun bangun-bangun (Coleus amboinicus L.) dalam menghambat pertumbuhan bakteri Staphylococcus aureus dan Escherichia coli disebabkan adanya senyawa-senyawa polifenol seperti flavonoid, dan tanin
bangun-bangun terdapat flavonoid, tannin, minyak atsiri yang dapat bersifat sebagai antimikroba.
4.4 Daya Antioksidan
Penentuan daya antioksidan berdasarkan peningkatan bilangan peroksida. Penentuan bilangan peroksida digunakan larutan standard natrium tiosulfat yang harus dibakukan terlebih dahulu. Data pembakuan dan perhitungan normalitas natrium tiosulfat dapat dilihat pada Lampiran 4 halaman 48. Data volume hasil titrasi minyak kedelai kontrol, minyak kedelai dengan penambahan BHT 0,02% dan minyak kedelai dengan penambahan ekstrak etanol daun bangun-bangun dapat dilihat pada Lampiran 5 halaman 49 hingga Lampiran 9 halaman 53. Bilangan peroksida dari minyak kedelai kontrol, minyak kedelai dengan penambahan BHT 0,02% dan minyak kedelai dengan penambahan ekstrak etanol daun bangun-bangun dapat dihitung dengan cara seperti yang tertera pada Lampiran 10 halaman 54.
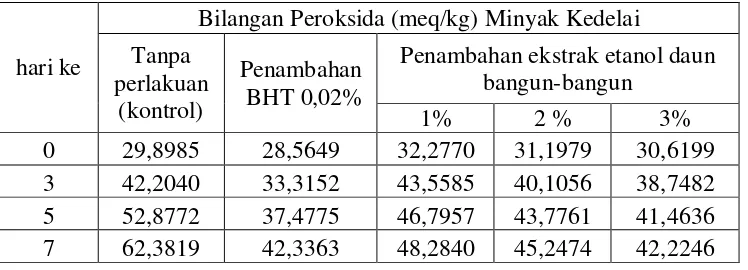
Tabel 3. Data Penentuan Bilangan Peroksida Minyak Kedelai Kontrol, Minyak Kedelai dengan Penambahan Pembanding (BHT 0,02%) serta
Minyak Kedelai dengan Penambahan Ekstrak etanol daun bangun-bangun 1%, 2%, 3% Selama Penyimpanan pada Suhu 400C
hari ke
Bilangan Peroksida (meq/kg) Minyak Kedelai Tanpa
perlakuan (kontrol)
Penambahan BHT 0,02%
Penambahan ekstrak etanol daun bangun-bangun Keterangan: Setiap hasil didapat dari data rata rata tiga kali penetapan
Dari Tabel 3. terlihat peningkatan bilangan peroksida minyak kedelai kontrol, penambahan pembanding BHT 0,02% dan penambahan ekstrak etanol daun bangun-bangun 1%, 2%, dan 3%. Peningkatan bilangan peroksida minyak kedelai pada penambahan ekstrak etanol daun bangun-bangun sebanyak 1% terjadi pada hari ke 3 (43,5585 meq/kg) dan kenaikan terus meningkat hingga hari ke 7 (47,0920 meq/kg). Begitu juga pada penambahan ekstrak etanol daun bangun-bangun sebanyak 2%, terlihat peningkatan bilangan peroksida pada hari ke-3 (40,1056 meq/kg) dan kenaikan terus meningkat hingga hari ke 7 (45,2474 meq/kg). Dan pada penambahan ekstrak etanol daun bangun-bangun 3% terlihat peningkatan bilangan peroksida pada hari ke-3 (38,7482 meq/kg) dan kenaikan terus meningkat hingga hari ke 7 (42,2246 meq/kg). Peningkatan bilangan peroksida pada penambahan ekstrak sebanyak 1% dan 2% ini lebih kecil dari peningkatan bilangan peroksida kontrol.
yang terlarut dalam minyak yang bersifat antioksidan dengan mendonorkan hidrogen terhadap radikal bebas sehingga dapat menurunkan bilangan peroksida.
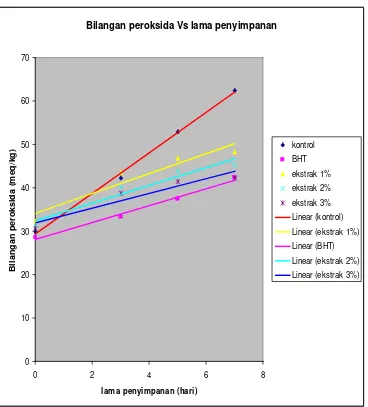
Grafik linier bilangan peroksida dapat dibuat dengan menghitung persamaan regresi dengan cara seperti yang tertera pada Lampiran 10 halaman 44. Grafik linier plot bilangan peroksida kedalam grafik lama penyimpanan (hari) Vs bilangan peroksida (meq/kg) dapat dilihat pada Gambar 3.
Bilangan peroksida Vs lama penyimpanan
0
Dari Gambar 3 dapat terlihat perbedaan slope dari kelima grafik bilangan peroksida. Slope dari minyak kedelai dengan penambahan pembanding BHT 0,02% (1,926) lebih kecil dibandingkan dengan slope minyak kedelai kontrol (4,675) dan slope minyak kedelai dengan penambahan ekstrak 1% (2,302) dan 2% (2,105), namun nilai slope BHT 0,02% lebih besar dibandingkan dengan penambahan ekstrak 3% (1,688). Slope yang semakin kecil menunjukkan peningkatan bilangan peroksida yang semakin kecil. Salah satu faktor yang mengkatalisis terjadinya peningkatan bilangan peroksida ini adalah panas, dimana panas mempercepat terbentuknya radikal bebas oksigen. Radikal ini mengambil atom hidrogen dari asam lemak tak jenuh membentuk asam lemak radikal, yang kemudian bereaksi kembali dengan radikal oksigen membentuk radikal peroksil yang kemudian mengambil atom hidrogen dari asam lemak tak jenuh lainnya membentuk peroksida (Akoh dan Min, 2004).
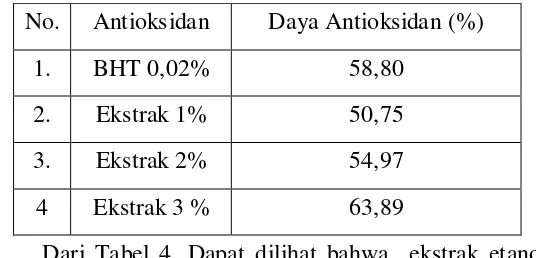
Daya antioksidan dihitung dengan membandingkan slope linier dari minyak kedelai kontrol dengan plot angka peroksida minyak kedelai dengan penambahan ekstrak etanol daun bangun-bangun seperti yang tertera pada Lampiran 11 halaman 58. Hasil daya antioksidan tertera pada Tabel 4.
Tabel 4. Data Hasil Penentuan daya Antioksidan No. Antioksidan Daya Antioksidan (%)
1. BHT 0,02% 58,80
2. Ekstrak 1% 50,75
3. Ekstrak 2% 54,97
4 Ekstrak 3 % 63,89
meningkat dengan bertambahnya jumlah ekstrak yang ditambahkan kedalam minyak kedelai yaitu 50,75 % pada penambahan ekstrak 1% dan meningkat menjadi 54,97% pada penambahan ekstrak 2%. Daya antioksidan dari pembanding (BHT) masih berada diatas daya antioksidan dari ekstrak tersebut, yakni sebesar 58,80%, meskipun jumlah BHT yang ditambahkan hanya sebesar 0,02%. Namun pada konsentrasi ekstrak 3%, daya antioksidannya lebih tinggi dibandingkan antioksidan pembanding BHT yakni sebesar 63,89%.
BAB IV
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Dari penelitian daya antibakteri ekstrak etanol daun bangun-bangun (Coleus amboinicus Lour.) dengan metode difusi agar menggunakan punch hole memiliki daya antibakteri sebagai berikut pada konsentrasi 4% memiliki diameter hambat 24,15 mm untuk Escherichia coli dan 27,16 mm untuk Staphylococcus aureus. Dan pada konsentrasi 0,8% memberikan daerah hambat pertumbuhan
yang memuaskan terhadap bakteri Escherichia coli yaitu 17,95 mm, sementara bakteri Staphylococcus aureus telah memberikan daerah hambat yang memuaskan pada konsentrasi 0,4% yaitu 14,18 mm.
Dari penelitian daya antioksidan yang dilakukan terhadap ekstrak etanol daun bangun-bangun (Coleus amboinicus Lour.) dengan metode pengukuran bilangan peroksida, menunjukkan adanya daya antioksidan sebagai berikut, pada penambahan ekstrak sebanyak 1% daya antioksidannya sebesar 50,75% dan pada penambahan ekstrak 2% meningkat menjadi 54,97%, dan pada penambahan ekstrak 3 % menjadi 63,89%.
5.2 Saran
DAFTAR PUSTAKA
Akoh, C.C. dan Min, D.B.(2008). Food Lipids: Chemistry, Nutrition and Biotechnology. Edition. New York: CRC Press. P.299-304, 390
Cahyadi, W.(2006). Analisis dan Aspek Kesehatan Bahan Tambahan makanan. Cetakan Pertama. Jakarta: Bumi aksara. Hal 137-144
Christin, M. dan Triana, H. (2005). Kandungan Senyawa Kimia dan Efek Ekstrak Air Daun Bangun-bangun pada Aktivitas Fagositois Netrofil tikus Putih (rattus norvegicus. dalam Majalah Farmasi Indonesia. ugm.ac.id/files/news/3._16-3-2005-bu-christin.pdf
Dalimartha,S. (2004). Atlas Tumbuhan Obat Indonesia. Jilid V. Jakarta: Trubus Agriwidya. Hal. 25-27
Depkes RI. (1980). Materia Medika Indonesia. Jilid IV. Jakarta: Depkes RI. Hal.131-137
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Depkes RI. Hal 333-337
Depkes RI. (2000). Inventaris Tumbuhan Obat Indonesia. Jilid I. Jakarta: Depkes RI. Hal.79-80
DIFCO. (1977). DIFCO Manual of Dehydrated Culture Media and Reagents for Microbiological and Clinical Laboratory Procedures. 9th Edition. Michigan: DIFCO Laboratories Incorporated. P.32-33
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Depkes RI. Hal. 9, 649, 713
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Depkes RI. Hal. 896
Farnsworth, N. R. (1966). Biological and Phytochemical Screening Of Plants. Journal of Pharmaceutical Sciences. Volume 55, Number 3. Page 264 Harborne, J. B. (1987). Metode Fitokimia Penuntun Cara Modern Menganalisis
Tumbuhan. Penerjemah: K. Padmawinata dan I. Soediro. Edisi III. Bandung: ITB Press. Hal.102
Irianto, K. (2002). Mikrobiologi. Jilid I. Jakarta: Yrama Widya. Hal. 13-14
Lay, B. W. dan Hastowo, S. (1992). Mikrobiologi. Bogor: Penerbit Institut Pertanian Bogor. Hal. 72-77
Lennete,et al. (2005). Mc. Farlands Standars. Diambil dari: URL: HYPERLINK http: //www.quelab.com/htmleng/2900a/html
Mudihardi, E, dkk. (2001). Mikrobiologi Kedokteran. Jakarta: Penerbit Salemba Medika. Hal 235
Pelczar, M. J. (1986). Dasar – Dasar Mikrobiologi. Penerjemah: Ratna Sari, dkk, Edisi I. Jakarta: UI Press. Hal 86
Pohan, S. (2002). Pengaruh Jenis Pelarut Pengekstraksi Terhadap Aktivitas Antioksidan dari Ekstrak Serbuk Daun Teh (Camellia sinensis L.). Skripsi. Farmasi. FMIPA USU. Medan. Hal. 16
Raharjo, S.(2006). Kerusakan Oksidatif pada Makanan. Cetakan Pertama. Yogyakarta: UGM Press. Hal 129;148
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Bandung: ITB. Hal 71 – 72
Ronald, E.W. (2005). Handbook Of Food Analitycal Chemistry, Water, Protein, Enzymes, Lipid and Charbohydrat. USA: John Wiley & Sons. P.518-519
Silalahi, J.( 2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Hal. 38-55
Snyder, H.E. dan Kwon, T.W.(1987). Soybean Utilization. New York: Avi Book. P. 104-111
Tortora, G.J. (2001). Microbiology an Introduction. Seventh Edition. New York: Addison Wesley Longman, Inc. P.86-88
Lampiran 3. Data Perhitungan Penetapan Kadar Air Hasil Penjenuhan toluen = 1,8 ml
Berat sampel 1 = 5,015 gram Berat sampel 2 = 5,015 gram Berat sampel 3 = 5,075 gram Volume air yang dibaca
Sampel 1 = 2,20 ml Sampel 2 = 2,20 ml Sampel 3 = 2,25 ml
Kadar 1 = 2,2 05,0 1 5−1,8 0x1 0 0% = 7,97%
Kadar 2 = 2,2 05,0 1 5−1,8 0x1 0 0% = 7,97%
Kadar 3 = 2,2 55,0 7 5−1,8 0x1 0 0% = 8,86%
Lampiran 4. Data Data Pembakuan Larutan Natrium Tiosulfat
Berat Kalium Bikromat ditimbang: B1 = 4,2 mg
Volume Natrium Tiosulfat terpakai: V1 = 45,30 ml
Lampiran 10. Contoh Perhitungan bilangan Peroksida
Angka peroksida ini dinyatakan dalam meq oksigen aktif per kg dengan rumus sebagai berikut:
PV = V x NM x1 0 0
Dimana :V = Jumlah ml larutan Natrium tiosulfat yang distandarisasi N = Normalitas dari Natrium tiosulfat yang digunakan M = berat sampel (g)
Data data hasil titrasi minyak kedelai kontrol: Volume titrasi : 8,25 ml
N Na2S2O3 : 0,0018 N
Berat sampel : 0,5131 g
Bilangan Peroksida = 0,5 1 3 1 0 0 1 , 0 2 5 , 8 x
X 1000 = 28,5965 Meq/kg
Lampiran 11. Contoh Perhitungan Persamaan Garis Regresi Data data bilangan peroksida minyak kedelai kontrol
X Y XY X2 Y2
Lampiran 12. Contoh Perhitungan Penentuan daya Antioksidan Dari Lampiran 11 diperoleh :
Slope Grafik minyak kedelai kontrol = 4,675
Slope Grafik minyak kedelai dengan penambahan pembanding (BHT 0,02%) =1,926
Dari grafik minyak kedelai kontrol dan grafik minyak kedelai dengan penambahan pembanding (BHT 0,02%) diperoleh aktivitas antioksidan :
% Daya Antioksidan BHT = S c x1 0 0% S y S c−
= 4,6 7 54,6 7 5−1,9 2 x 100% = 58,80%
Lampiran 15. Flowsheet preparasi minyak kedelai
Disokletasi dengan pelarut n-heksan
Dipisahkan dengan rotaryevaporator
Ditambahkan air suling 2% dari berat minyak
Dipanaskan pada suhu 700C selama 30 menit
Didinginkan
Disentrifugasi
Ditambahkan NaOH 12 % sebanyak 8% dari berat minyak Disentrifugasi
Dicuci dengan air suling panas Disentrifugasi
Ditambah karbon aktif 1% dari berat minyak Disaring
1800 g kacang kedelai
Campuran minyak dengan n-heksan
Minyak kedelai
Lapisan bawah Lapisan atas
Lapisan bawah
Lapisan atas
Lapisan bawah Lapisan atas
Lampiran 16. Flowsheet penentuan bilangan peroksida
Ditimbang 0,5 g minyak
Ditambahkan asam asetat:klorofom (3:2)
Ditambahkan 1 ml KI jenuh Dikocok selama 1 menit Didiamkan selama 5 menit Ditambahkan 30 ml air suling Dititrasi dengan Na2S2O3 yang
sudah distandarisasi sampai mendekati TAT
Ditambah indikator amilum Dititrasi dengan Na2S2O3 sampai
warna biru hilang
• Dilakukan pengujian sebanyak 3 kali
• Dilakukan pengujian pada hari ke-0, 3, 5, 7. Minyak kedelai (kontrol)
Larutan kuning muda
Lampiran 17. Flowsheet pembuatan inokulum bakteri
Diambil 1 ose isolat bakteri
Dimasukkan ke dalam 10 ml larutan NaCl 0,9% steril
Di vorteks
Diinkubasi selama 2 jam
Divorteks sampai didapat kekeruhan yang sama dengan suspensi Mc.Farland
Dipipet 0,1 ml suspensi bakteri
Dimasukkan ke dalam 9,9 ml NaCl 0,9% steril
Stok kultur bakteri
Suspensi bakteri (konsentrasi108 CFU/ml)
Lampiran 18. Flowsheet Pengujian daya Antibakteri
0,1 ml inokulum bakteri
dicampur homogen dengan 20 ml NA steril dalam cawan petri steril dibiarkan sampai media memadat
media padat
dimasukkan 0,1 ml larutan uji
diinkubasi pada suhu 36 ± 1ºC selama 18-24 jam diukur diameter zona bening
diameter zona hambat
dilubangi dengan punch hole
Lampiran 19. Uji daya antibakteri ekstrak etanol daun bangun-bangun
No Konsentrasi (%)
Diameter hambatan (mm)
Escherichia coli Staphylococcus aureus
I II III D* I II III D*
1 4 23,90 24,10 24,45 24,15 26,35 27,4 27,75 27,16 2 3 22,15 22,15 22,70 22,36 25,60 25,55 26,05 25,73 3 2 20,85 21,25 21,35 21,15 24,95 24,40 25,05 24,80 4 1 19,35 19,45 20,10 19,63 21,10 21,20 21,35 21,21 5 0,8 17,80 17,95 18,10 17,95 18,90 18,20 18,05 18,38 6 0,5 12,35 12,40 12,60 12,45 16,15 16,30 16,00 16,15 7 0,4 10,90 11,60 11,90 11,46 14,00 14,15 14,40 14,18 8 0,3 8,75 8,50 8,25 8,50 11,20 11,05 10,95 11,06
9 0,2 - - - - 8,15 8,00 7,95 8,03
10 0,1 - - - -
11 Blanko - - - -
Keterangan: D* : diameter rata-rata tiga kali pengamatan - : Tidak ada daya hambatan
Lampiran 20. Hasil uji daya antibakteri ekstrak etanol daun bangun-bangun terhadap pertumbuhan bakteri Staphylococcus aureus