Lampiran 1. Perhitungan Bilangan Iodin (IV), Bilangan Peroksida (PV), Kandungan Asam Lemak bebas (FFA), dan Kandungan Air Minyak Kemiri Hasil Pemurnian
a. Bilangan Iodin
�� = (�� − ��)�(���2��3)�(12,69) �
IV = (47,30−25,09)�(0,1001)�(12,69)
0,2040
IV = 138,28 b. Bilangan Peroksida
PV = (��−��)�(���2��3)�1000
W
PV = (6,03−0)�(0,002)�1000
5,0461
PV = 2,38 c. Kandungan Asam Lemak Bebas
FFA = Vt x N KOH x 28,2
W
FFA = 1,77 � 0,1 � 28,2
5,0461
FFA = 0,99 % d. Kadar Air
% Kadar Air = W0 −W1 �1
x 100 %
% Kadar Air = 50−46,728
46,728 x 100 %
Lampiran 8. SFC Lemak Margarin Hasil Blending dan Interesterifikasi
Lampiran 9. Gambar Alat dan Proses Pembuatan Lemak Margarin
A. Proses Ekstraksi Minyak Kemiri B. Minyak Kemiri Hasil Ekstraksi
E.Blending RBDPS dengan Minyak Kemiri
I. Lemak Margarin hasil interesterifikasi dengan perbandingan
RBDPS : Minyak Kemiri (90:10, 80:20, 70:30)
L. Lemak Margarin hasil interesterifikasi dengan perbandingan RBDPS : Minyak Kemiri (60:40, 50:50) H. Lemak Margarin hasil blending dengan
perbandingan RBDPS : Minyak Kemiri (90:10, 80:20, 70:30)
M. Lemak Margarin hasil interesterifikasi dengan perbandingan RBDPS : Minyak
Kemiri (40:60, 30:70) J. Lemak Margarin hasil blending
dengan perbandingan RBDPS : Minyak Kemiri (60:40, 50:50)
K. Lemak Margarin hasil blending dengan perbandingan RBDPS : Minyak
DAFTAR PUSTAKA
Agilent Technologies. 2003. Understanding Your Chensation. Edition 06/03. Agilent Technologies Deutschland GmbH Hewlett-Packard Strasse 8. Germany. Akoh, C.C. 1995. Lipid-Based Fat Substitutes. Department of Food Science and
Technology, The University of Georgia, Athens, GA 30603-7610. Akoh, C.C., 1998, Fat Replacers. Food Technology, INFORM 52(3).
Arlene, A., Jessica, N.R., Suharto, I. 2010. Pengaruh Temperatur dan Ukuran Biji
terhadap Perolehan Minyak Kemiri pada Ekstraksi Biji Kemiri dengan Penekanan Mekanis. Prosiding Seminar Nasional Teknik Kimia.
Yogyakarta.
Barus, P. 2006. Studi Reaksi Interesterifikasi antara RBDPS dengan Minyak Kelapa
atau Minyak Kemiri menjadi CBS atau Margarin yang Mengandung Asam Lemak Omega-3 dan Omega-6. Disertasi. Program Doktor Ilmu Kimia.
USU. Medan.
Basiron, Y., Jalani, B.S., and Chan, K.W. 2000. Advanced in Oil Palm Research. Malaysian Palm Oil Board Ministry of Primary Industries Malaysia.
Belitz, H.D., W.Grosch. 1997. Food Chemistry. Springer Verlag, Berlin, Heidelberg. Che Man and Swe, 1997. Thermal Analysis of Failed-Batch Palm Oil by Differential
Scanning Calorimetry. MOSTA Short Course III, March 10-11. Malaysia.
Gandhi, N. N. 1997. Aplication of Lipase. JAOCS, Vol 74(6).
Geise, J. 1996. Fats, Oil, and Fat Replacers. Food Technology, April.
Ginting, E. 2013. Sintesis Basa Schiff Campuran melalui Ozonolisis Minyak Biji
Kemiri (Alleurites mollucana Wild) yang Diikuti Kondensasi dengan Anilina yang Berfungsi Sebagai Inhibitor Korosi pada Logam Seng. Skripsi
Hamilton, R.J., and Rossel, J.B. 1986. Analysis of Oils and Fats. Elsevier Science Publishing & Co. Inc., New York.
Harjono, 2009. Pembuatan Sabun Mandi. Penebar Swadaya, Jakarta.
Haryati, Che Man, Ghazali, and Jinap. 1998. Monitoring of Transesterification of
Palm Oil by Differential Scanning Calorimetry. Presented at World
Congress and Exhibition of The International Oil Palm Conference. Nusa Dua, Bali.
Hauman, B.F. 1994. Tools: Hydrogenation, Interesterification. INFORM 5(6).
Hendrayati. 2010. Asam Lemak Trans, Lemak Total, Sindrom Metabolik. Vol X. Edisi 2. Media Gizi Pangan. Makassar.
Hunter, T.L., Pederson, L.S., Nielsen, P.M., Cristensen, M.W., Holm, D.H.C. 2007.
Enzymatic Interesterification. Palm Oil Development.
Kaban, J. S. Sitompul, dan S.S. Brahmana. 1991. Studi Perubahan Cis ke Trans dari
Hasil Reaksi Interesterifikasi antara Stearin Kelapa Sawit dengan Minyak Jagung dan Minyak Kedelai dalam Proses Pembuatan Margarin Nabati.
Laporan Penelitian, FMIPA USU, Medan.
Ketaren, S, 2008. Pengantar Teknologi Lemak dan Minyak Pangan. UI Press, Jakarta.
Khopkar, S.M. 2003. Konsep Dasar Kimia Analitik. UI Press, Jakarta.
Lingga, L. 2012. Sehat dan Sembuh dengan Lemak. PT Elex Media Komputindo, Jakarta.
Mardoni, M.M., Tjandrawati, Y. 2007. Perbandingan Metode Kromatografi Gas dan
Berat Jenis pada Penetapan Kadar Etanol dalam Minuman Anggur.
http://www.usu.ac.id/mardoni.pdf.
Melton, S.L. 1996. Nutritional Needs for Fat and the Role of Fat in the Diet. JAOCS, Campaign. Illionis.
Moussata, C.O., and C.C. Akoh. 1998. Influence of Lipase-Catalized
Interesterification on the Oxidative Stability of Melon Seed Oil Triacylglycerol. JAOCS. Vol 75 no. 9.
O’Brien, R.D. 1998. Fats and Oils, Formulating and Processing for Applications. Technical Publishing, Company Inc, Lancaster USA.
Pande, G., and Akoh, C.C. 2012. Enzymatic Synthesis of Trans-Free Structured
Margarine Fat Analogs with High Stearate Soybean Oil and Palm Stearin and Their Characterization. Department of Food Science and Technology,
University of Georgia, Athens.
Perkins, E.G. 1991. Analysis of Fats, Oil, and Derivatives. JAOCS Press, Illionis. Perryman, S., Stone, M. 2006. Trans Fat NewLabels. Department of Food Science
and Human Nutrition. Colorado State University.
Petrauskite, V.W., DE Greyt, M Kellens and A Huyghebaert. 1998. Physical and
Chemical Properties of Trans Free Fats Produced by Chemical Interesterification of Vegetable Oil Blends. JAOCS,75,4.
Potters, N.N. 1986. Food Science. 4th Ed. AVI Publishing Company Inc. Wesport, Connecticut.
Ramayana, 2003. Pembuatan Lemak Margarin dari Minyak Kelapa, Minyak Kelapa
Sawit, dan Stearin Kelapa Sawit melalui Interesterifikasi dan Blending Berkecepatan Tinggi pada Suhu Kamar Program Pascasarjana Universitas
Sumatera Utara, Medan.
Sari, N. 2016. Analisa Asam Lemak Trans dan Kandungan Lemak Padat pada
Pembuatan CBS melalui Reaksi Interesterifikasi antara RBDPS, RBDPO, dan Minyak Kelapa. Program Pascasarjana Universitas Sumatera Utara,
Medan.
Sudarmadji, S., Haryono, B., dan Suhardi. 1996. Analisa Bahan Makanan dan
Pertanian. Edisi II, Fakultas Teknologi Pertanian Universitas Gajah Mada,
Yogyakarta.
Sudjadi. 1986. Metode Pemisahan. Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta.
Tarigan, D. 2007. Transformasi Asam Lemak Tak Jenuh Minyak Kemiri Menjadi
Surfaktan Alkanolamida Di, Tetra dan Heksahidroksi Oktadekanoat.
Disertasi. Sekolah Pascasarjana. USU. Medan.
Tarigan, J. 2009. Ester Asam Lemak. Karya Ilmiah. USU. Medan. Halaman 9-10. Tjeng, M. 2011. Perbandingan Kandungan Lemak Trans pada Pembuatan Coating
Fat dari Minyak Inti Sawit melalui Reaksi Hidrogenasi Parsial, Interesterifikasi, dan Metode Blending. Disertasi. Program Doktor Ilmu
Kimia. USU. Medan.
Weiss, T.J. 1983. Food Oils and Their Users. Second Edition, Avi Publishing Company, Connecticut 12-15.
Willis. 1998. Lipid Modification Strategies in the Production of Nutritionaly
Functional Fats and Oil. Crit.Rev, Food Sci.Nutr, CRC Pres, Canada.
Wong, D.W.S., 1989. Mechanism and Theory in Food Chemistry. Van Nostrand Reinhold, New York.
Winarno, F.G. 1991. Kimia Pangan dan Gizi. Gramedia, Jakarta.
BAB 3
METODE PENELITIAN
3.1. Alat– Alat Penelitian
Adapun alat –alat yang digunakan dalam penelitian ini adalah:
- Kromatografi Gas Shimazu
- Pulsed NMR Anlyzer Bruker NMS 120
- Melting Point Apparatus - Shaker
- Water Bath
- Rotary evaporator Heidolph
- Oven Lab-line
- Labu takar 250 mL Pyrex
- Beaker glass 250 mL Pyrex
- Beaker glass 500 mL Pyrex
- Gelas ukur 250 mL Pyrex
- Gelas ukur 100 mL Pyrex
- Labu leher tiga 250 mL Pyrex
- Corong pisah 1 L Pyrex
3.2. Bahan – Bahan Penelitian
Adapun bahan yang digunakan dalam penelitian ini adalah: - RBDPS
- Minyak kemiri - n-heksana
- H3PO4 p.a. (E. Merck)
- Etanol p.a. (E. Merck)
- Metanol p.a. (E. Merck)
- Benzena p.a. (E. Merck)
- H2SO4 p.a. (E. Merck)
- Na2SO4 anhidrat p.a. (E. Merck)
- NaOC2H5 p.a. (E. Merck)
- Asam sitrat 20% - Kertas saring biasa - Bleaching eart
- Fenolftalien p.a. (E. Merck)
- Natrium Tiosulfat p.a (E. Merck)
- Asam Asetat p.a (E. Merck)
- Sikloheksana p.a (E. Merck)
- Larutan Wijs p.a (E. Merck)
- Kalium Iodida p.a (E. Merck)
- Kloroform p.a (E. Merck)
3.3. Prosedur Penelitian 3.3.1. Ekstraksi Minyak Kemiri
Sebanyak 3000 gram daging dari biji buah kemiri kemiri digiling hingga menjadi serbuk halus. Serbuk halus yang diperoleh direndam menggunakan pelarut n-heksana sebanyak 6 liter selama 2 hari dan setiap selang waktu 6-8 jam sekali dilakukan pengadukan. Hasil perendaman selanjutnya disaring, sekaligus residu yang tertinggal dalam saringan dibilas dengan n-heksana. Filtrat dari hasil saringan dikeringkan air dengan Na2SO4 anhidrat. Selanjutnya filtrat diuapkan menggunakan rotary evaporator sehingga diperoleh minyak kemiri. Adapun prosedur selanjutnya yang dilakukan adalah pemucatan (bleaching) dan penghilangan getah (degumming) yang merupakan bagian dari pemurnian dari minyak kemiri.
3.3.2. Pemurnian Minyak Kemiri
Sebanyak 100 ml minyak kemiri ditambah 0,05% H3PO4 dan dicampur dengan 2%
bleaching earth di dalam gelas Erlenmeyer bercabang volume 300 ml. Selanjutnya
3.3.3. Pembuatan Metil Ester Asam Lemak
Pembuatan metil ester asam lemak dilakukan terhadap RBDPS, minyak kemiri, lemak margarin hasil blending, dan lemak margarin hasil interesterifikasi. Ke dalam labu leher tiga yang telah dilengkapi kondensor bola dan tabung CaCl2 serta pengaduk magnet dimasukkan 20 g sampel lemak/minyak, 40 ml metanol, dan 80 ml benzena. Campuran tersebut diaduk dan didinginkan, kemudian diteteskan H2SO4(p) sebanyak 2 ml secara perlahan. Campuran tersebut kemudian direfluks selama 3 jam. Pelarut benzena dan methanol yang berlebih diuapkan dengan alat rotary evaporator. Residu yang diperoleh kemudian diekstraksi dengan 100 ml n-heksana dan dicuci dengan aquadest sebanyak 3 kali. Lapisan atas diambil, kemudian dikeringkan dengan Na2SO4 anhidrat lalu disaring. Filtrat yang diperoleh lalu diuapkan dengan alat rotary evaporator sehingga diperoleh metil ester asam lemak sebagai hasil. Hasil yang diperoleh dianalisis dengan Kromatografi Gas Cair untuk diuji komposisi asam lemaknya.
3.3.4. Blending RBDPS dengan Minyak Kemiri pada Perbandingan 90:10, 80:20, 70:30, 60:40, 50:50, 40:60 dan 30:70 (v/v)
3.3.5. Interesterifikasi RBDPS dengan Minyak Kemiri pada Perbandingan 90:10, 80:20, 70:30, 60:40, 50:50, 40:60, dan 30:70 (v/v)
Interesterifikasi dilakukan dengan memasukkan RBDPS dengan minyak kemiri masing-masing 100 ml untuk setiap perbandingan ke dalam labu leher tiga yang telah dilengkapi termometer dan stopper. Kemudian ditambahkan Natrium etoksida sebanyak 0,2 g yang dilarutkan dalam etanol. Campuran tersebut dipanaskan pada suhu 90oC selama 90 menit sambil diaduk. Setelah itu katalis dinonaktifkan dengan menggunakan larutan asam sitrat 20% sebanyak 20 ml. Pengadukan dilanjutkan selama 15 menit. Hasil pengadukan dimasukkan ke dalam corong pisah, kemudian dipisah lapisan bawah dan lapisan atas dianalisis FAC, TFA, komposisi trigliserida, titik lebur, dan SFC.
3.3.6. Analisis Minyak Hasil Pemurnian dan Hasil Reaksi
3.3.6.1 Penentuan Bilangan Iodin (IV), Bilangan Peroksida (PV), Asam Lemak Bebas (FFA), dan Kandungan Air
3.3.6.1.1. Penentuan Bilangan Iodin
Untuk penentuan bilangan iodin dilakukan terhadap minyak kemiri hasil pemurnian
(mengikuti metode Wijs, AOAC, 1995).
Bilangan Iodin = (B−S) X N X 12,69
Berat Sampel (gram )
Dimana : B = Volume Titrasi Blanko (ml) S = Volume Titrasi Sampel (ml) N = Normalitas Na2S2O3 (0,1N)
3.3.6.1.2. Penentuan Bilangan Peroksida
Penentuan bilangan peroksida terhadap minyak kemiri hasil pemurnian (mengikuti metode AOAC, 1995).
Ke dalam gelas Erlenmeyer dimasukkan 5 gram minyak kemiri, kemudian dipanaskan selama ± 1 menit. Dilarutkan minyak dengan kloform dan asam asetat dengan perbandingan 1 : 1. Ditambahkan 0,5 ml KI jenuh ke dalam campuran dan diaduk selama ± 2 menit. Ditambahkan 30 ml aquadest dan indikator amilum 1%. Dititrasi campuran dengan Na2S2O3 0,002 N sampai terjadi perubahan warna menjadi putih dan dicatat volume Na2S2O3 yang digunakan. Dilakukan titrasi terhadap blanko dengan prosedur yang sama. Bilangan iodin dapat ditentukan dengan rumus :
Bilangan Peroksida = (S−B) X N X 1000 Berat Sampel (gram)
Dimana : B = Volume Titrasi Blanko (ml) S = Volume Titrasi Sampel (ml) N = Normalitas Na2S2O3 (0,1N)
3.3.6.1.3. Penentuan Kandungan Asam Lemak Bebas
Penentuan kandungan asam lemak bebas terhadap minyak kemiri hasil pemurnian (mengikuti metode AOAC, 1995).
Larutan tersebut dititrasi dengan larutan NaOH 0,02 N sampai menjadi warna merah lembayung. Dicatat volume NaOH yang digunakan, selanjutnya dihitung persentasi asam lemak bebas dengan rumus sebagai berikut :
Asam Lemak Bebas (%) = NNaOH x VNaOH x 25,6 Berat Sampel (gram)
Dimana : N = Normalitas NaOH (N) V = Volume NaOH (ml)
3.3.6.1.4. Penentuan Kadar Air
Minyak kemiri hasil pemurnian yang diperoleh ditimbang dan dipanaskan dalam oven pada suhu 110 0C selama 90 menit, kemudian dimasukkan ke dalam desikator dan ditimbang berat hingga konstan.
% Kadar Air = W0 −W1
�1
x 100 %
Dimana : W0 = Berat Awal W1 = Berat Akhir
3.3.6.2. Penentuan Komposisi Asam Lemak (FAC) dan Asam Lemak Trans (TFA) dengan Kromatografi Gas Cair
yang sudah dalam bentuk metil ester asam lemak diinjeksikan ke dalam septum Kromatografi Gas Cair. Diperoleh komposisi asam lemak berdasarkan puncak yang terbentuk pada kromatogram.
3.3.6.3. Penentuan Komposisi Trigliserida dengan Kromatografi Gas Cair
Sampel yang akan diuji komposisi trigliseridanya adalah RBDPS, minyak kemiri, lemak margarin hasil blending, dan lemak margarin hasil interesterifikasi. Pada analisis komposisi trigliserida, temperatur oven diatur kenaikannya mulai dari 1000C selama 0,5 menit dengan kenaikan suhu rata-rata 500C sampai dicapai temperatur maksimum 3600C. kondisi kolom kromatografi gas cair diatur pemisahannya dengan kecepatan rata-rata 2,5 menit, dimana dalam sekali penginjeksian sampel dibutuhkan waktu 31,50 menit. Sampel dipipet ±3 µl dan dimasukkan ke dalam vial tube 1,5 ml, lalu ditambah 1,5 ml n-heksana kemudian diaduk. Diinjeksikan larutan ke dalam septum Kromatografi Gas. Diperoleh komposisi trigliserida berdasarkan puncak yang terbentuk pada kromatogram.
3.3.6.4. Penentuan Kandungan Lemak Padat (SFC)
3.3.6.5. Penentuan Titik Cair Lemak Margarin
3.4. Bagan Penelitian
3.4.1. Ekstraksi Minyak Kemiri
Biji Kemiri
Dipisahkan dari kulit buah Dikeringkan
Dihaluskan Serbuk Kemiri
Ditambahkan n-heksana sampai terendam
Dimaserasi selama 48 jam Disaring
Filtrat Residu
Dirotarievaporator hingga pelarut habis
Minyak Kemiri (Residu)
3.4.2. Pemurnian Minyak Kemiri
100 ml Minyak Kemiri
Ditambahkan 0,05 % H3PO4 Ditambahkan 2 % bleaching eart Diaduk dan dipanaskan pada suhu 105oC dalam keadaan vakum selama 90 menit
Disaring
Minyak Kemiri Residu
Analisis Kadar Air, Bilangan Asam, Bilangan Iodin, Bilangan Peroksida
Analisis FAC dan TFA
Analisis Komposisi Trigliserida
3.4.3. Pembuatan Metil Ester Asam Lemak
20 g sampel lemak/minyak
Dimasukkan ke dalam labu leher tiga Ditambahkan 40 ml metanol
Ditambahkan 80 ml benzena
Dirangkai alat refluks yang dilengkapi tabung CaCl2
Diteteskan H2SO4(p) sebanyak 2 ml secara perlahan-lahan melalui corong penetes Direfluks selama 3 jam pada suhu 70-80oC Campuran
Didinginkan pada suhu kamar
Diuapkan kelebihan metanol dan benzena dengan rotary evaporator
Destilat Residu
Diekstraksi dengan 100 ml n-heksana
Dicuci dengan 10 ml aquadest sebanyak 3 kali
Lapisan atas Lapisan bawah
Dikeringkan air dengan Na2SO4 anhidrous
Disaring
Filtrat Residu
Diuapkan pelarutnya dengan alat rotari evaporator
Hasil
Analisis Kromatografi Gas
3.4.4. Blending RBDPS dengan Minyak Kemiri
Dimasukkan ke dalam beaker glass
Ditambahkan 10 ml minyak kemiri
Diaduk selama 5 menit sambil
dipanaskan pada suhu 55
0C
Hasil
Analisis FAC
dan TFA
Analisis
Komposisi TG
Analisis
Titik Lebur
Analisis
SFC
RBDPS
Diukur sebanyak 90 ml
Dicairkan
3.4.5. Interesterifikasi RBDPS dengan Minyak Kemiri
100 ml Campuran RBDPS dengan Minyak Kemiri pada perbandingan 90:10
Dimasukkan ke dalam labu leher tiga
Ditambahkan NaOC2H5 0,2 g yang dilarutkan dalam etanol
Dipanaskan pada suhu 90oC selama 90 menit Didinginkan
Ditambahkan 20 ml asam sitrat 20% Campuran
Dipisahkan dengan corong pisah
Lapisan atas Lapisan bawah
(Asam Sitrat+NaOC2H5)
Hasil
Analisis Titik lebur Analisis FAC dan
TFA Analisis SFC
Analisis Komposisi TG
3.4.6. Analisis Hasil Penelitian
3.4.6.1. Penentuan Kandungan Lemak Padat (SFC)
Sampel
Dipanaskan sampai suhu 70oC
Disaring
Residu Filtrat
Dimasukkan ke dalam 12 vial masing-masing ± 3ml
Dipanaskan semua vialdi water bath suhu 60oC selama 30 menit
Dipindahkan semua vial ke water bath suhu 0oC selama 1 jam
Dibagi masing-masing vial ke beberapa water bath
Water Bath 0oC
Water Bath 5oC
Water Bath 10oC
Water Bath 15oC
Water Bath 20oC
Water Bath 25oC
Water Bath 30oC
Water Bath 33oC
Water Bath 35oC
Water Bath 38oC
Water Bath 40oC
Water Bath 45oC
Dibiarkan masing-masing vial pada water bath selama 30 menit
3.4.6.2. Penentuan Titik Cair Lemak Margarin
Lemak Margarin
Dimasukkan ke dalam tabung kapiler berdiameter 1 mm menggunakan spuit injeksi
Dibekukan dalam refrigerator selama 16 jam
Diikat tabung kapiler pada termometer sehingga tabung berisi minyak sejajar dengan ujung termometer
Dicelupkan ke dalam beaker glass 500 ml yang berisi air setengah penuh
Dipanaskan dengan kecepatan 0,5oC/menit sambil diaduk
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Hasil Ekstraksi dan Pemurnian Minyak Kemiri
Dari sebanyak 3000 g inti biji buah kemiri yang telah dihaluskan dan diekstraksi menggunakan pelarut n-heksana melalui perendaman diperoleh minyak kemiri sebanyak 1560,2 g (52 %). Minyak kemiri hasil ekstraksi kemudian dimurnikan melalui proses pemucatan (Bleaching) menggunakan bleaching eart dan penghilangan getah (degumming) menggunakan Asam Posfat. Hasil analisis minyak yang diperoleh antara lain : kadar air 0,070 %, kandungan asam lemak bebas 0,99 %, bilangan iodin 138,28, dan bilangan peroksida 2,39.
4.1.2. Komposisi Asam Lemak dan Trigliserida Minyak Kemiri dan Komposisi Asam Lemak dan Trigliserida RBDPS
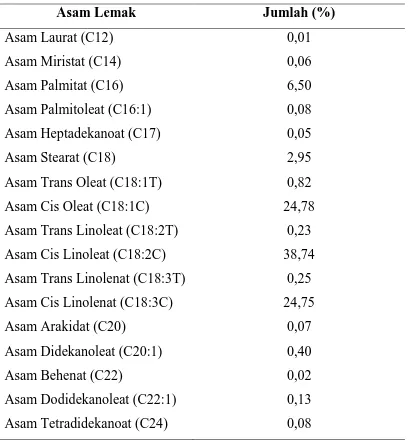
Tabel 4.1. Komposisi asam lemak minyak kemiri
Asam Lemak
Jumlah (%)
Asam Laurat (C12)
0,01
Asam Miristat (C14)
0,06
Asam Palmitat (C16)
6,50
Asam Palmitoleat (C16:1)
0,08
Asam Heptadekanoat (C17)
0,05
Asam Stearat (C18)
2,95
Asam Trans Oleat (C18:1T)
0,82
Asam Cis Oleat (C18:1C)
24,78
Asam Trans Linoleat (C18:2T)
0,23
Asam Cis Linoleat (C18:2C)
38,74
Asam Trans Linolenat (C18:3T)
0,25
Asam Cis Linolenat (C18:3C)
24,75
Asam Arakidat (C20)
0,07
Asam Didekanoleat (C20:1)
0,40
Asam Behenat (C22)
0,02
Asam Dodidekanoleat (C22:1)
0,13
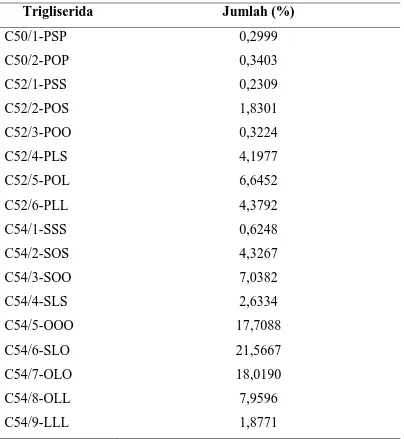
Tabel 4.2. komposisi trigliserida minyak kemiri
Trigliserida
Jumlah (%)
C50/1-PSP
0,2999
C50/2-POP
0,3403
C52/1-PSS
0,2309
C52/2-POS
1,8301
C52/3-POO
0,3224
C52/4-PLS
4,1977
C52/5-POL
6,6452
C52/6-PLL
4,3792
C54/1-SSS
0,6248
C54/2-SOS
4,3267
C54/3-SOO
7,0382
C54/4-SLS
2,6334
C54/5-OOO
17,7088
C54/6-SLO
21,5667
C54/7-OLO
18,0190
C54/8-OLL
7,9596
Tabel 4.3. Komposisi asam lemak RBDPS
Asam Lemak
Jumlah (%)
Asam Laurat (C12)
0,17
Asam Miristat (C14)
1,23
Asam Palmitat (C16)
58,61
Asam Palmitoleat (C16:1)
0,11
Asam Heptadekanoat (C17)
0,10
Asam Stearat (C18)
4,86
Asam Trans Oleat (C18:1T)
0,06
Asam Cis Oleat (C18:1C)
27,43
Asam Trans Linoleat (C18:2T)
0,11
Asam Cis Linoleat (C18:2C)
6,13
Asam Trans Linolenat (C18:3T)
0,02
Asam Cis Linolenat (C18:3C)
0,10
Asam Didekanoat (C20)
0,34
Asam Didekanoleat (C20:1)
0,09
Asam Dodidekanoat (C22)
0,05
Asam Dodidekanoleat (C22:1)
0,01
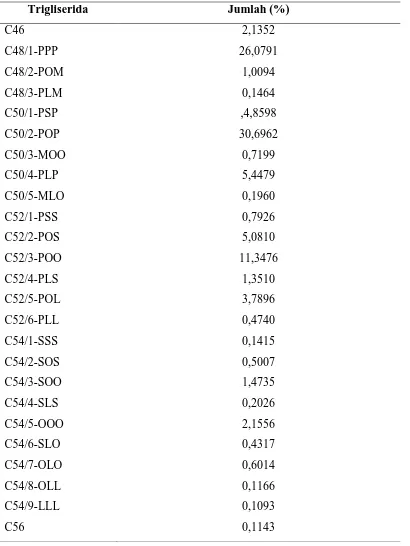
Tabel 4.4. komposisi trigliserida RBDPS
Trigliserida Jumlah (%)
C46 2,1352
C48/1-PPP 26,0791
C48/2-POM 1,0094
C48/3-PLM 0,1464
C50/1-PSP ,4,8598
C50/2-POP 30,6962
C50/3-MOO 0,7199
C50/4-PLP 5,4479
C50/5-MLO 0,1960
C52/1-PSS 0,7926
C52/2-POS 5,0810
C52/3-POO 11,3476
C52/4-PLS 1,3510
C52/5-POL 3,7896
C52/6-PLL 0,4740
C54/1-SSS 0,1415
C54/2-SOS 0,5007
C54/3-SOO 1,4735
C54/4-SLS 0,2026
C54/5-OOO 2,1556
C54/6-SLO 0,4317
4.1.3. Komposisi Asam Lemak (FAC) dan Asam Lemak Trans (TFA) dari Lemak Margarin Hasil Blending dan Interesterifikasi RBDPS dengan Minyak Kemiri
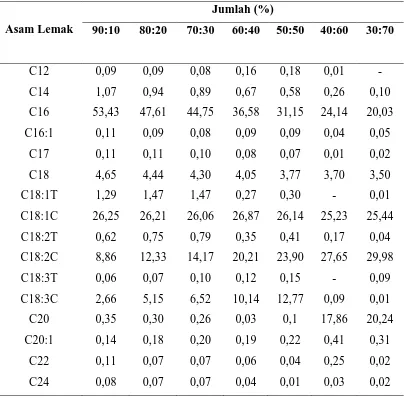
[image:73.612.112.517.291.689.2]Hasil analisis kromatografi gas menunjukkan komposisi asam lemak dari hasil blending dan interesterifikasi RBDPS dengan minyak kemiri dengan perbandingan 90:10 sampai 30:70. Komposisi asam lemak dan asam lemak trans dari lemak margarin hasil blending dan interesterifikasi dapat dilihat pada tabel 4.5 dan tabel 4.6. Tabel 4.5. Komposisi Asam Lemak dan Asam Lemak Trans Lemak Margarin Hasil
Blending RBDPS dengan Minyak Kemiri
Asam Lemak
Jumlah (%)
90:10 80:20 70:30 60:40 50:50 40:60 30:70
C12 0,09 0,09 0,08 0,16 0,18 0,01 -
C14 1,07 0,94 0,89 0,67 0,58 0,26 0,10 C16 53,43 47,61 44,75 36,58 31,15 24,14 20,03 C16:1 0,11 0,09 0,08 0,09 0,09 0,04 0,05
C17 0,11 0,11 0,10 0,08 0,07 0,01 0,02 C18 4,65 4,44 4,30 4,05 3,77 3,70 3,50
C18:1T 1,29 1,47 1,47 0,27 0,30 - 0,01
C18:1C 26,25 26,21 26,06 26,87 26,14 25,23 25,44 C18:2T 0,62 0,75 0,79 0,35 0,41 0,17 0,04 C18:2C 8,86 12,33 14,17 20,21 23,90 27,65 29,98
C18:3T 0,06 0,07 0,10 0,12 0,15 - 0,09
C18:3C 2,66 5,15 6,52 10,14 12,77 0,09 0,01 C20 0,35 0,30 0,26 0,03 0,1 17,86 20,24 C20:1 0,14 0,18 0,20 0,19 0,22 0,41 0,31
Tabel 4.6. Komposisi Asam Lemak dan Asam Lemak Trans Hasil Interesterifikasi RBDPS dengan Minyak Kemiri
Asam Lemak
Jumlah (%)
90:10 80:20 70:30 60:40 50:50 40:60 30:70
C12 0,15 0,12 0,10 0,11 0,16 0,03 0,01 C14 1,10 0,99 0,87 0,71 0,57 0,12 0,08 C16 53,06 48,73 43,39 37,72 30,78 24,14 19,66 C16:1 0,62 0,22 0,19 0,12 0,15 0,04 0,05
C17 0,11 0,11 0,09 0,08 0,07 0,04 0,02 C18 4,57 4,44 4,30 3,98 3,74 3,54 3,48
C18:1T 1,27 1,35 1,44 0,32 0,30 - 0,01
C18:1C 25,70 25,77 25,80 25,74 26,07 25,52 25,41 C18:2T 0,91 0,80 0,87 0,45 0,45 0,08 0,11 C18:2C 8,93 11,82 14,97 20,08 20,08 27,51 30,01 C18:3T 0,13 0,10 0,14 0,12 0,12 0,08 0,05 C18:3C 2,70 4,83 7,15 10,20 10,20 0,06 0,03 C20 0,34 0,28 0,26 0,03 0,03 18,15 20,24 C20:1 0,14 0,18 0,20 0,20 0,2 0,25 0,30
4.1.4. Komposisi Trigliserida dari Lemak Margarin Hasil Blending dan Interesterifikasi RBDPS dengan Minyak Kemiri
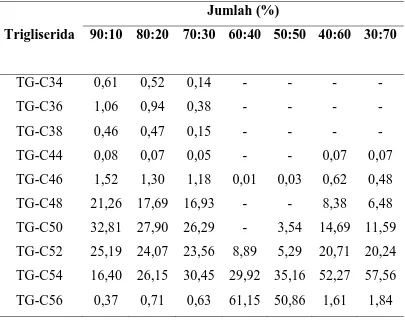
[image:75.612.112.517.353.673.2]Hasil analisis kromatografi gas menunjukkan komposisi trigliserida lemak margarin hasil blending dan interesterifikasi RBDPS dengan minyak kemiri dengan perbandingan 90:10, 80:20, 70:30, 60:40, 50:50, 40:60, dan 30:70. Dari komposisi trigliserida lemak margarin yang diperoleh dapat dilihat ada tidaknya pertukaran gugus asil baik untuk lemak margarin hasil blending maupun lemak margarin hasil interesterifikasi. Komposisi trigliserida dari lemak margarin hasil blending dapat dilihat pada tabel 4.7, sedangkan komposisi trigliserida dari lemak margarin hasil interesterifikasi dapat dilihat pada tabel 4.8.
Tabel 4.7. Komposisi Trigliserida dari Lemak Margarin Hasil Blending RBDPS dengan Minyak Kemiri
Trigliserida
Jumlah (%)
90:10 80:20 70:30 60:40 50:50 40:60 30:70
TG-C34
0,61
0,52
0,14
-
-
-
-
TG-C36
1,06
0,94
0,38
-
-
-
-
TG-C38
0,46
0,47
0,15
-
-
-
-
TG-C44
0,08
0,07
0,05
-
-
0,07
0,07
TG-C46
1,52
1,30
1,18
0,01
0,03
0,62
0,48
TG-C48
21,26 17,69 16,93
-
-
8,38
6,48
TG-C50
32,81 27,90 26,29
-
3,54
14,69 11,59
TG-C52
25,19 24,07 23,56
8,89
5,29
20,71 20,24
TG-C54
16,40 26,15 30,45 29,92 35,16 52,27 57,56
Tabel 4.8. Komposisi Trigliserida dari Lemak Margarin Hasil Interesterifikasi RBDPS dengan Minyak Kemiri
Trigliserida
Jumlah (%)
90:10 80:20 70:30 60:40 50:50 40:60 30:70
TG-C34
1,49
0,80
0,52
-
-
-
-
TG-C36
2,02
1,37
0,87
-
-
-
-
TG-C38
0,85
0,71
0,48
-
-
-
-
TG-C44
0,05
0,07
0,05
-
-
0,12
0,06
TG-C46
1,51
1,35
1,13
0,04
0,01
0,64
0,46
TG-C48
21,46 19,72 16,33
-
-
8,31
6,28
TG-C50
31,16 28,27 24,55
6,11
-
14,21 11,34
TG-C52
24,50 23,83 22,64
-
-
20,62 20,21
TG-C54
16,32 23,17 32,49 58,91 57,52 51,07 58,18
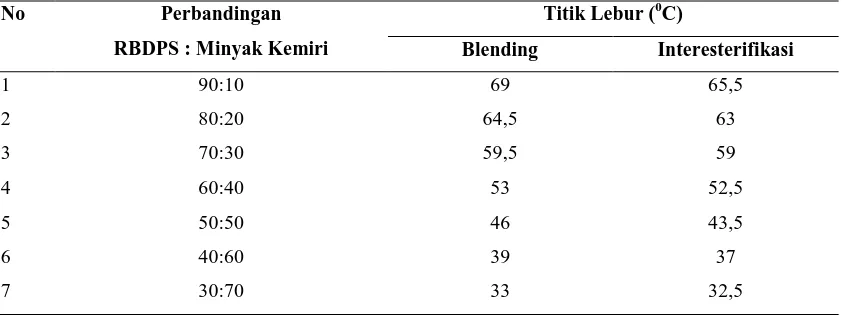
4.1.5. Titik Lebur Lemak Margarin Hasil Blending dan Interesterifikasi RBDPS dengan Minyak Kemiri
Titik lebur hasil blending dan interesterifikasi RBDPS dengan minyak kemiri pada berbagai perbandingan dapat dilihat pada tabel 4.9.
Tabel 4.9. Data titik lebur lemak margarin hasil blending dan interesterifikasi pada berbagai perbandingan
No Perbandingan
RBDPS : Minyak Kemiri
Titik Lebur (0C)
Blending Interesterifikasi
1 90:10 69 65,5
2 80:20 64,5 63
3 70:30 59,5 59
4 60:40 53 52,5
5 50:50 46 43,5
6 40:60 39 37
7 30:70 33 32,5
4.1.6. Kandungan Lemak Padat (SFC) Lemak Margarin
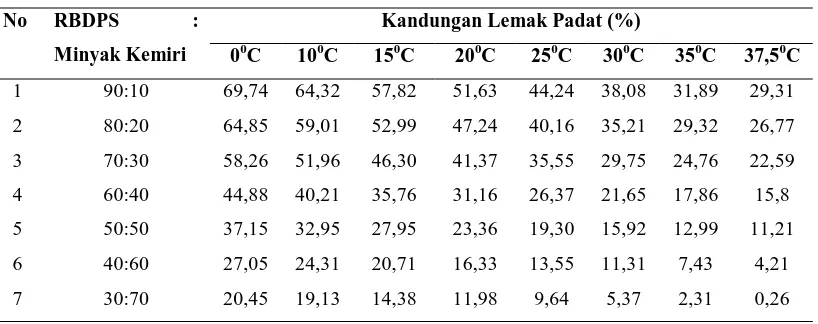
[image:77.612.113.534.209.367.2]Data hasil pengujian nilai kandungan lemak padat (SFC) hasil blending dan interesterifikasi RBDPS dengan minyak kemiri menggunakan alat pulsed NMR dengan perbandingan 90:10, 80:20, 70:30, 60:40, 50:50, 40:60, dan 30:70 pada suhu 00C, 100C, 150C, 200C, 250C, 300C, 350C, dan 400C. hasilnya dapat dilihat masing-masing pada tabel 4.10 dan tabel 4.11.
Tabel 4.10. Data Kandungan Lemak Padat (SFC) Hasil Blending
No RBDPS :
Minyak Kemiri
Kandungan Lemak Padat (%)
00C 100C 150C 200C 250C 300C 350C 37,50C 1 90:10 73,89 70,85 64,48 58,06 49,60 42,42 34,86 32,52
2 80:20 67,45 62,06 56 50,21 43,22 37 30,72 27,83
3 70:30 58,32 52,21 46,57 41,64 35,73 29,97 25,07 22,87
4 60:40 48,93 43,49 38,14 32,30 26,63 22,40 18,97 17,28
5 50:50 39,94 35,17 30,71 25,97 21,34 18,08 14,49 12,95
6 40:60 28,47 25,55 22,72 17,91 14,67 12,34 8,32 5,41
[image:77.612.109.510.529.701.2]Tabel 4.11. Data Kandungan Lemak Padat (SFC) Hasil Interesterifikasi
No RBDPS :
Minyak Kemiri
Kandungan Lemak Padat (%)
00C 100C 150C 200C 250C 300C 350C 37,50C 1 90:10 69,74 64,32 57,82 51,63 44,24 38,08 31,89 29,31
2 80:20 64,85 59,01 52,99 47,24 40,16 35,21 29,32 26,77
3 70:30 58,26 51,96 46,30 41,37 35,55 29,75 24,76 22,59
4 60:40 44,88 40,21 35,76 31,16 26,37 21,65 17,86 15,8
5 50:50 37,15 32,95 27,95 23,36 19,30 15,92 12,99 11,21
6 40:60 27,05 24,31 20,71 16,33 13,55 11,31 7,43 4,21
7 30:70 20,45 19,13 14,38 11,98 9,64 5,37 2,31 0,26
4.2. Pembahasan
4.2.1. Analisis Hasil Pemurnian Minyak Kemiri
Minyak kemiri yang diperoleh dari hasil ekstraksi dimurnikan melalui tahap penghilangan getah (degumming) menggunakan asam fosfat dan tahap (bleaching) menggunakan bleaching eart. Minyak kemiri yang diperoleh memiliki warna kuning pucat, dimana sebelumnya warna minyak kemirinya orange kekuningan.
4.2.2. Komposisi Asam Lemak dan Trigliserida
Ekstraksi minyak kemiri dari buah kemiri yang telah dihaluskan menggunakan pelarut n-heksana diperoleh kandungan minyak sebesar 52%. Dari tabel 4.1 dapat dilihat bahwa minyak kemiri memiliki komposisi asam lemak tak jenuh yang dominan. Diantara ketiga asam lemak tak jenuh yang dominan, asam linoleat memiliki jumlah terbanyak (38,97%) diikuti oleh asam oleat (25,61%) dan asam linolenat (25%). Sementara asam lemak yang paling sedikit jumlahnya adalah asam laurat (0,0104%).
Komposisi trigliserida dari minyak kemiri dapat dilihat pada tabel 4.2. Trigliserida dengan komposisi terbesar adalah trigliserida dengan susunan asam lemak stearat, linoleat, dan oleat sebesar (SLO) 21,56%, sedangkan trigliserida dengan komposisi terkecil adalah trigliserida dengan susunan asam lemak palmitat, stearat, dan palmitat sebesar (PSP) 0,29%. Dari komposisi trigliserida yang diperoleh dapat disimpulkan bahwa komposisi trigliserida yang dominan terdiri dari asam-asam lemak yang tak jenuh.
komposisi asam lemak dari lemak margarin juga dipengaruhi oleh banyaknya minyak kemiri yang ditambahkan dalam setiap perbandingan. Semakin banyak minyak kemiri menyebabkan lemak margarin yang dihasilkan memiliki kandungan asam lemak tak jenuh yang lebih tinggi.
Untuk perubahan komposisi trigliserida dapat dilihat pada lemak margarin hasil interesterifikasi dengan perbandingan 80:20 (RBDPS:Minyak Kemiri). Jumlah TG-C50 dari lemak margarin tersebut adalah 27,90 %, sedangkan jumlah TG-C50 untuk minyak kemiri dari RBDPS dan minyak kemiri masing-masing adalah 0,64% dan 41,91%. Dari persentase tersebut dapat dilihat adanya pertukaran gugus asil pada masing-masing trigliserida dari RBDPS dan minyak kemiri, sehingga dihasilkan lemak margarin bersifat semipadat.
4.2.3. Kandungan Asam Lemak Trans Lemak Margarin
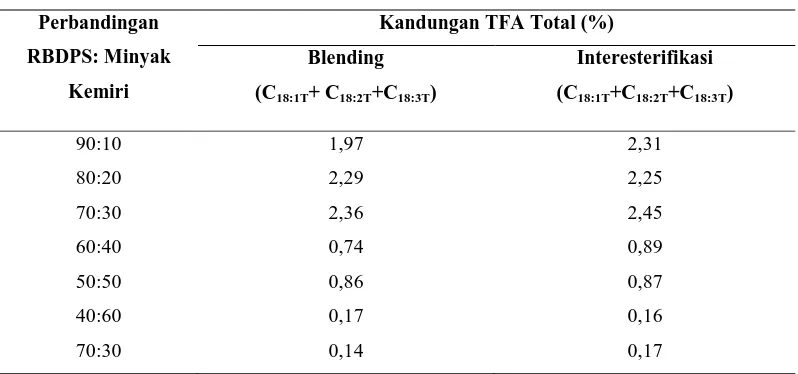
[image:80.612.118.517.515.702.2]Analisis kandungan asam lemak trans lemak margarin dilakukan sekaligus dengan analisis kandungan asam lemak dari lemak margarin hasil blending dan interesterifikasi menggunakan Kromatografi Gas Shimazu. Data kandungan TFA total dari lemak margarin hasil blending dan interestrifikasi dapat dilihat pada tabel 4.12.
Tabel 4.12. Kandungan TFA Total Lemak Margarin Hasil Blending dan Interesterifikasi pada Berbagai Perbandingan
Perbandingan
RBDPS: Minyak
Kemiri
Kandungan TFA Total (%)
Blending
(C18:1T+ C18:2T+C18:3T)
Interesterifikasi
Kandungan asam lemak trans lemak margarin hasil blending dan interesterifikasi tidak jauh berbeda, meskipun kandungan asam lemak trans lemak margarin hasil interesterifikasi lebih tinggi. Hal ini menunjukkan bahwa proses interesterifikasi tidak mempengaruhi kualitas lemak margarin yang akan dihasilkan.
Asam lemak trans hanya akan sedikit terbentuk pada reaksi interesterifikasi dengan suhu 900C dalam waktu 90 menit dengan adanya katalis Natrium etoksida karena trans isomer akan terbentuk mulai suhu 1100C. Temperatur yang tinggi akan menghasilkan lebih banyak TFA. Tekanan yang tinggi dari katalis Ni akan mengurangi TFA. Klasifikasi kandungan asam lemak trans :
High trans product : >20% TFA
Low trans product : <5% TFA (minimal trans fat) Zero trans product : <0,5% TFA
(Perryman, et.al., 2006).
Struktur molekul asam lemak tak jenuh di alam berbentuk cis dan struktur ini dapat diubah dalam bentuk trans karena proses pemanasan pada suhu yang tinggi. Asam lemak trans sangat ditakuti sebagai pemicu jantung koroner dan penyakit lainnya. Dalam penelitian ini, kandungan asam lemak trans yang diperoleh masih aman dikonsumsi terdapat pada lemak margarin hasil blending dan interesterifikasi pada perbandingan 30:70 (RBDPS:Minyak Kemiri), dimana nilai total TFA-nya masing-masing adalah 0,14% dan 0,17%.
4.2.4. Titik Lebur
Titik lebur dari lemak margarin hasil blending dengan perbandingan 90:10, 80:20, 70:30, 60:40, 50:50, 40:60, dan 30:70 masing-masing adalah 690C; 64,50C; 59 0
C; 530C, 460C; 390C; dan 330C, sedangkan titik lebur lemak margarin hasil interesterifikasi adalah 65,50C; 630C; 590C; 52,50C; 43,50C; 370C; dan 32,50C. Terjadinya perubahan titik lebur berkaitan dengan adanya pencampuran secara fisik antara RBDPS dengan minyak kemiri dalam proses blending, sedangkan perubahan titik lebur dari lemak margarin hasil interesterifikasi karena adanya penataan ulang molekul-molekul asam lemak dari minyak atau lemak yang semula sehingga titik lebur menjadi berubah .Lemak margarin yang dihasilkan harus padat pada suhu kamar (270C) dan mencair pada suhu tubuh (32-370C).
Lemak margarin hasil interesterifikasi memiliki titik lebur yang lebih rendah dibandingkan lemak margarin hasil blending. Dari ketujuh perbandingan, lemak margarin hasil blending dengan perbandingan 30:70 memiliki titik lebur terendah yaitu 380C, demikian juga dengan hasil interesterifikasi pada perbandingan 30:70 memiliki titik lebur terendah yaitu 37,50C. Reaksi interesterifikasi yang melibatkan reaksi pertukaran gugus asil menyebabkan pertukaran yang lebih merata dari struktur RBDPS dan minyak kemiri sehingga dihasilkanlah produk lemak margarin dengan titik lebur yang lebih rendah.
4.2.5. Reaksi Interesterifikasi
O C O C O C C H O H2 C H2 C O O H R1 R2 R3 O C O C O C -CH O H2 C H2 C O
O R2
R3 R1 O C O C O C H2 C H2 C O
O R2
R3 O
-C
H R1 O C
O C O C H2 C H2 C O
O R2
R3
O -C H R1
--C2H5OH
-OC 2H5
Na+ O C O C O C O H2 C H2 C O
O R2
R3 O C O C H2 C H2 C O
O R5
R6 C H C R1 O
-CH2R4 O -O C O C O C O H2 C H2 C O
O R2
R3 O C O C H2 C H2 C O
O R5
R6 C H C R1 O +
CH2R4 O
R2 H2 C C O O O C O H2 C R3 O C O -O C H R1 C O
CH2R4
O C
O
H2
C R5
O C
O H2
C R6
R2 H2 C C O O O C O H2 C R3 O -+ O O O C O C H R1 C C C O H2
C R5
O
H2
C R4
O H2
C R6
R2 H2 C C O O O C O H2 C R3 O C O
-H2C R4
C H R1 C O O O C O R5 O C O R6 O O O C C C O O O H2 C R4 H2
C R2
H2 C R3
O O O C C C O O O H
-C R1 H2 C R5 H2 C R6
+ H
+
O
H
[image:84.612.115.492.83.658.2]O O O C C C O
OCH H2 C H2 C H R1 R2 O R3 -OC 2H5
O O O C C C O OCH -H2 C H2 C R1 R2 O R3 O C O H
C R1
O O
C
-O
H2
C R2
C O
H2
C R3
O O O C C O -H2 C O R3 C H R1 C O CH2
-C2H5OH
R2 O -O O C C O C H H2 C O R3 R1 C O H2
C R2
[image:85.612.115.504.85.572.2]O O O O C C C H H2 C O R3 C H O -CH2 R1 O O O C C C O O H2 C CH -H2 C R2 R1 O R3 H+ O O O C C C O O H2 C H2 C H2 C R2 R1 O R3 R2
4.2.6. Kandungan Lemak Padat (SFC)
Analisis kandungan lemak padat (SFC) lemak margarin hasil blending dan interesterifikasi RBDPS dan miyak kemiri dilakukan menggunakan alat pulsed NMR Analizer Bruker NMS 120. Berkurangnya jumlah RBDPS dan bertambahnya jumlah minyak kemiri menyebabkan menurunnya nilai kandungan lemak padat dari lemak margarin yang dihasilkan. Hal ini menunjukkan bahwa kandungan lemak padat berbanding lurus dengan titik lebur.
Nilai kandungan lemak padat (SFC) lemak margarin hasil blending dan interesterifikasi menunjukkan hasil yang berbeda. Lemak margarin hasil interesterifikasi memiliki nilai kandungan lemak padat yang lebih rendah dibandingkan lemak margarin hasil blending. Adanya katalis Natrium etoksida menyebabkan adanya pertukaran gugus asil antar trigliserida baik secara intermolekular atau maupun intramolekular, sehingga lemak margarin yang dihasilkan lebih padu dan memiliki titik lebur yang lebih rendah.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Perbandingan antara RBDPS dengan minyak kemiri untuk menghasilkan lemak margarin baik metode blending maupun interesterifikasi ditinjau dari nilai SFC dan TFA total adalah 30:70 (v/v), dimana nilai SFC lemak margarin hasil blending sebesar 2,43% pada suhu 350C dengan jumlah TFA total sebesar 0,14%, sedangkan lemak margarin hasil interesterifikasi diperoleh nilai SFC nya sebesar 2,31% pada suhu 350C dengan persentase TFA total sebesar 0,17%
2. Dari hasil penelitian yang diperoleh, perubahan kandungan asam lemak trans (TFA) oleat (C18:1T), linoleat (C18:2T), dan linolenat (C18:3T) lemak margarin hasil interesterifikasi dibandingkan dengan blending tidak jauh berbeda. Hal ini menunjukkan bahwa baik metode blending dan interesterifikasi akan menghasilkan lemak margarin dengan kandungan asam lemak trans (TFA) yang masih aman dikonsumsi.
5.2 Saran
1. Sebaiknya peneliti selanjutnya melakukan blending dan interesterifikasi selain antara minyak kemiri dan RBDPS untuk diuji kemampuannya membentuk lemak margarin.
BAB 2
TINJAUAN PUSTAKA
2.1. Lemak dan Minyak
Minyak merupakan trigliserida yang berwujud cairan pada suhu kamar dan umumnya diperoleh dari sumber nabati, sedangkan lemak merupakan trigliserida yang pada suhu kamar berwujud padatan dan umumnya bersumber dari hewani.
Minyak dan lemak adalah trigliserida yang merupakan bagian terbesar dari kelompok lipida. Pembentukan trigliserida dihasilkan dari proses esterifikasi suatu molekul gliserol dengan tiga molekul asam lemak (yang sama atau dapat berbeda) membentuk suatu molekul trigliserida dan tiga molekul air (Perkins, 1991).
Trigliserida dapat berwujud padat atau cair, dan hal ini tergantung dari komposisi asam lemak yang menyusunnya. Sebagian besar minyak nabati berbentuk cair karena mengandung sejumlah asam lemak tidak jenuh, yaitu asam oleat, asam linoleat, atau asam linolenat dengan titik cair yang rendah. Lemak hewani pada umumnya berbentuk padat pada suhu kamar karena banyak mengandung asam lemak jenuh, misalnya asam palmitat dan stearat yang mempunyai titik cair lebih tinggi (Silalahi, 2002). Struktur trigliserida dapat dilihat pada gambar 2.1.
[image:89.612.246.395.507.612.2]O O O R1 O R2 O R3 O
Gambar 2.1. Struktur Trigliserida (Silalahi, 2002)
inti sawit termasuk yang tinggi kejenuhannya karena memiliki asam laurat. Secara umum lemak mengandung suatu campuran trigliserida yang akan berbeda pada setiap komposisi dan posisi asam lemaknya pada molekul trigliserida, hal ini menyebabkan molekul dalam lemak dapat melembut atau mengeras. Oleh karena itu, lemak dapat berbentuk cair pada temperatur kamar, tetapi umumnya mengandung molekul lemak padat (suspended solid) pada minyak cairnya. Jika lemak cair didinginkan, beberapa molekul lemak akan memadat dan sebagian membentuk kristal lemak dari bagian yang cair (Weiss, 1983).
Minyak dan lemak merupakan komponen makanan yang memiliki fungsi tersendiri. Sebagai nutrisi, lemak memiliki lima fungsi yaitu sebagai sumber energi, material pembangun struktur sel, sumber asam lemak esensial pada manusia, pelarut vitamin A, D, E, K, dan pengontrol serum lipida dan lipoprotein (Melton, 1996).
Disamping fungsinya sebagai nutrisi, lemak juga merupakan komponen makanan dan pemberi rasa dalam makanan. Lemak memberikan cita rasa yang merupakan suatu kombinasi yang memberikan rasa lembut, lezat, bentuk dan aroma pada makanan. Lemak juga sebagai pembawa senyawa cita rasa lipofilik yang disebabkan oleh adanya prekursor untuk pembentuk cita rasa (Akoh, 1995).
Selain mempunyai efek positif, lemak juga mempunyai efek negatif, kebanyakan lemak akan menyebabkan meningkatnya resiko kegemukan dan beberapa jenis penyakit kanker, kolesterol yang tinggi di dalam darah dan penyakit jantung koroner . Pengurangan konsumsi lemak dapat menurunkan resiko terkena penyakit jantung dan jika manusia yang memilki kelebihan berat badan melakukan diet lemak dapat menurunkan resiko penyakit jantung koroner (Geise, 1996).
misalnya mentega dan lemak yang digunakan dalam kembang gula, dan lemak yang dimasak bersama bahan pangan atau dijadikan sebagai medium, misalnya minyak goreng, shortening, dan lemak babi. Kadang-kadang untuk tujuan ini dapat juga digunakan mentega atau margarin. Lemak atau minyak yang ditambahkan ke dalam bahan pangan atau yang dijadikan sebagai bahan pangan perlu memenuhi persyaratan dan sifat-sifat tertentu. Sebagai contoh ialah persyaratan atau sifat-sifat lemak yang digunakan untuk pembuatan mentega atau margarin berbeda dengan persyaratan minyak yang dijadikan shortening atau minyak goreng (Potter, 1986).
2.2. Minyak Kemiri
Tanaman kemiri tumbuh secara alami di hutan campuran dan hutan jati pada ketinggian 150-1000 m di atas permukaan laut. Tanaman kemiri tidak begitu banyak menuntut persyaratan tumbuh, sebab dapat tumbuh di tanah kapur, tanah berpasir dan jenis tanah lainnya (Arlene, et.al,. 2010).
Tanaman kemiri (Alleurites mollucana) berpohon besar dengan tinggi 25-40 meter, beranting banyak, mempunyai tunas muda yang tertutup rapat oleh bulu yang berwarna putih keabu-abuan atau cokelat. Daun muda, berlekuk tiga atau lima, sedang daun tua, berbentuk bulat dengan ujung meruncing. Daun tersebut mempunyai kelenjar berwarna hijau kekuningan (Ketaren, 2008). Penyebaran kemiri di Indonesia hampir meliputi seluruh kepulauan. Daerah budidaya kemiri utama untuk wilayah Indonesia dapat dijumpai di Provinsi Sumatera Utara, Sumatera Barat, Bengkulu, Lampung, Kalimantan Barat, Bali, Sulawesi Selatan, Maluku, dan Nusa Tenggara Timur dengan luasan total mencapai 205.532 ha (Ginting, 2013).
dari hasil pengepresan dapat dipakai sebagai pupuk karena mengandung sekitar 8,5% Nitrogen dan lebih dari 4% asam fosfat.
[image:92.612.111.514.187.322.2]Kandungan bagian buah (biji) mengandung asam lemak jenuh dan asam lemak tidak jenuh sebesar 55-65 persen yang ditunjukkan pada tabel 2.1.
Tabel 2.1. Kandungan asam lemak dalam minyak kemiri
Asam Lemak Rantai Karbon Kandungan (%)
Asam palmitat C16;0 5,5
Asam stearat C18:0 6,7
Asam oleat C18:1 10,5
Asam linoleat C18:2 48,5
Asam linolenat C18:3 28,5
Sumber: (Ketaren, 2008)
Minyak biji kemiri biasanya digunakan sebagai bahan dasar pembuatan cat atau pernis, tinta cetak, dan pengawet kayu dan bahan pembuatan sabun. Di Filipina, minyak ini sudah lama digunakan untuk melapisi bagian dasar perahu agar tahan terhadap korosi akibat air laut. Daging buah kemiri juga dapat digunakan sebagai bumbu masak (Ketaren, 2008).
2.3. Stearin Kelapa Sawit
kelapa sawit akan berada di atas dan stearin berada di bagian bawah (Kaban dan Brahmana, 1991; O’Brien, 1998).
Minyak kelapa sawit diperoleh dari pemurnian minyak kelapa sawit yang diproses beberapa tahap, yaitu; (a) penghilangan getah (degumming), (b) pemucatan (bleaching), (c) penghilangan bau (deodorization), dan (d) pendinginan (winterization). Skema pemurnian minyak kelapa sawit dapat dilihat pada gambar 2.2.
Crude Palm Oil (CPO)
+ H3PO4
+ Bleaching Eart
+ Filter
Filtrat (DBP Oil)
Residu (ampas bleaching eart)
Deodorizing
ALB, Air RBDP Oil
Kristalisasi Fraksinasi
Filter
[image:93.612.147.509.249.516.2]RBD Olein RBD Stearin
Gambar 2.2. Skema Proses Pemurnian dan Pengolahan CPO
2.4. Lemak Margarin dan Margarin
Lemak margarin adalah lemak yang digunakan sebagai bahan baku utama dalam pembuatan margarin. Lemak margarin ini umumnya berasal dari lemak nabati dan lemak hewani. Lemak yang digunakan pada pembuatan margarin ini secara fisik maupun kimiawi mempunyai sifat-sifat yang sama dengan lemak yang lainnya.
Pada prinsipnya persyaratan dasar yang harus dipenuhi pada pembuatan margarin adalah kandungan lemak padat, titik cair, bilangan peroksidanya. Standar mutu margarin internasional menetapkan maksimum bilangan peroksida 6 mg O2/100 gram. Karena bilangan peroksida ini suatu ukuran kandungan peroksida dalam margarin yang sangat menentukan stabilitas oksidatif lemak margarin. Selanjutnya titik cair margarin berkaitan dengan nilai nutrisi dan kemampuan darah membawa zat makanan yang mengandung margarin (Ramayana, 2003).
sawit, minyak jagung, dan minyak bunga matahari (O’Brien, 1998). Beberapa jenis margarin beserta tampilan yang dibutuhkan dapat dilihat pada tabel 2.2.
Tabel 2.2. Persyaratan Tampilan Beberapa Jenis Margarin
Jenis Margarin Syarat Tampilan
Tub Memisah pada suhu 50C-100C
Paket Memisah pada suhu 150C (iklim sedang) dan 200C-250C (iklim tropis)
Industri atau bakery Berbentuk krim
Pastry Tercampur dengan baik
Sumber : (Basiron, 2000)
Banyak jenis margarin yang tersedia di pasaran, masing-masing dibuat untuk memenuhi keinginan konsumen. Jenis margarin yang paling umum adalah table
margarine, bakery margarine, dan puff pastry margarine. Sifat fisis yang baik
diperlukan untuk margarin berkualitas. Sifat-sifat ini termasuk yaitu stabilitas emulsi tanpa ada lemak yang terpisah, tekstur permukaan yang mengkilap, tidak ada butiran, dapat dioleskan dengan baik, dan bersih dengan melebur di mulut. Sifat fisis dari kekerasan dan spreadability margarin sangat berhubungan dengan proporsi lemak padatan dan cairan pada suhu yang diberikan. Lemak yang digunakan untuk semua jenis margarin biasanya campuran dari minyak cair dan padat sehingga akan memberikan kandungan padatan yang diinginkan pada jarak tertentu (Barus, 2006).
2.5. Asam Lemak Trans (TFA)
minyak kedelai, minyak jagung, minyak biji kapas, minyak biji bunga matahari, minyak zaitun, dan minyak canola. Lemak trans yang ada di pasaran umumnya terbuat dari minyak kedelai dan minyak biji jagung yang harganya relatif lebih murah dibandingkan minyak tak jenuh lainnya (Lingga, 2012). Struktur asam oleat cis dan asam oleat trans dapat dilihat pada gambar 2.3.
C
H H
O
OH
Asam oleat Cis
H
H
C O
OH
[image:96.612.117.512.206.415.2]Asam oleat Trans (Asam Elaidat)
Gambar 2.3. Struktur Cis dan Trans Asam Oleat (Tjeng, 2011)
Keberadaan asam lemak trans di dalam makanan menimbulkan dampak negatif terhadap kesehatan yaitu sebagai pemicu penyakit jantung koroner (PJK). Pengaruh negatif asam lemak trans dengan mempengaruhi kadar low density
lipoprotein (LDL) yang disebut kolesterol jahat. LDL ini adalah kolesterol yang
mengangkut paling banyak kolesterol di dalam darah. Kadar LDL yang tinggi akan menyebabkan mengendapnya kolesterol dalam arteri dan high density lipoprotein (HDL) yang dikenal sebagai kolesterol baik. Kolesterol HDL mengangkut kolesterol lebih sedikit, dapat membuang kelebihan kolesterol jahat di pembuluh darah arteri kembali ke hati untuk diproses dan dibuang. Jadi, HDL dapat mencegah kolesterol mengendap di arteri dan melindungi dari arteroklerosis (terbentuknya plak pada dinding pembuluh darah). Dengan mengkonsumsi asam lemak trans akan menaikkan kadar LDL dan menurunkan HDL (Hunter, 2007).
2.6. Modifikasi Minyak dan Lemak 2.6.1. Hidrogenasi
Hidrogenasi minyak dan lemak yang dikembangkan oleh W Norman pada tahun 1902 bertujuan untuk mengubah minyak cair menjadi lemak setengah padat yang sesuai untuk produk-produk seperti shortening dan margarin. Hidrogenasi merupakan metode yang paling banyak diterapkan untuk industri dalam memodifikasi minyak dan lemak (Silalahi, 1999).
membentuk radikal kompleks antara hidrogen, nikel, dan asam lemak tak jenuh. Setelah terjadi penguraian nikel dan radikal asam lemak, akan dihasilkan suatu tingkat kejenuhan yang lebih tinggi. Radikal asam lemak dapat terus bereaksi dengan hidrogen, membentuk asam lemak yang jenuh. Reaksi hidrogenasi parsial dapat dilihat pada gambar 2.4.
O O O C C C O O O
(H2C)16
(CH2)7
(CH2)7
C
H CH (CH2)7 CH3
C
H CH (CH2)7 CH3
H3C +H2
Ni O O O C C C O O O
(H2C)16
(CH2)7
(CH2)7
H2
C H2
C (CH2)7 CH3
C
[image:98.612.115.507.188.366.2]H CH (CH2)7 CH3 H3C
Gambar 2.4. Reaksi Hidrogenasi Parsial (Tjeng, 2011)
Proses hidrogenasi dilakukan untuk menjenuhkan ikatan rangkap di dalam rantai asam lemak, namun gas hidrogen dapat juga bereaksi dengan komponen non gliserida dalam minyak seperti karoten. Hal ini sangat tidak menguntungkan. Masalah yang harus diperhatikan selanjutnya adalah reaksi selektivitas (Gunstone dan Norris, 1983).
2.6.2. Blending
asam lemak dari minyak yang dicampurkan mempunyai komposisi asam lemak yang titik lelehnya tinggi (Willis, et.al. 1998).
Namun demikian, blending memiliki banyak kelemahan, karena perbedaan ukuran molekular, dua jenis minyak ada kemungkinan tidak kompatibel satu sama lainnya dan dapat membentuk campuran eutektik (Moussata dan Akoh, 1998). Selain itu hasil yang diperoleh kurang stabil dalam jangka waktu yang cukup lama karena hanya merupakan interaksi fisik dua atau lebih jenis minyak. Blending juga salah satu cara menghindari terjadinya asam lemak trans, bentuk trans yang dihasilkan metode hidrogenasi. Blending dilakukan dengan pengadukan yang kuat sehingga fase pendispersinya dapat bercampur dan dispersi ini dapat dipertahankan dengan menambah zat pengemulsi seperti lesitin (Haumann, 1994).
Beberapa penelitian mengenai blending yang telah dilakukan adalah oleh Mariati pada tahun 2001 dengan melakukan blending antara lemak kakao, RBD minyak sawit, dan minyak kemiri, sedangkan Ramayana (2003) telah melakukan blending antara minyak kelapa, minyak kelapa sawit, dan stearin kelapa sawit untuk membuat lemak margarin.
2.6.3. Interesterifikasi
Alkoholisis adalah reaksi dimana suatu ester diubah menjadi ester yang lain dengan mereaksikannya dengan suatu alkohol. Secara umum, reaksinya dapat dituliskan sebagai berikut:
+ H3C OH
C OCH3 O + O O O C O R1 C O R2 C O R3 R1 C OCH3 O R1 C OCH3 O R1 OH OH OH
Trigliserida/Ester Metil Ester Asam Lemak Gliserol
3
sedangkan asidolisis adalah reaksi dimana suatu ester diubah menjadi ester lain dengan mereaksikannya dengan suatu asam. Secara umum, reaksinya dapat dituliskan sebagai berikut:
C11H23 C
OH O + O O O C O R1 C O R2 C O R3 O O O C O
C11H23
C O R2 C O R3
Trigliserida/Ester Asam Lemak
(Tarigan, 2009).
O O O C C C O O O H2 C H2 C H2 C R1 R2 R3 O C O H 2
C R4
O C O H
2
C R5
O C O
H2
C R6
NaOC2H5
O O O C C C O O O H2 C H2 C H2 C R4 R2 R3 O O O C C C O O O H2 C H2 C H2 C R1 R5 R6 Trigliserida-1 Trigliserida-2 Trigliserida-3 Trigliserida-4 (a) O O O C C C O O O H2 C H2 C H2 C R1 R2 R3 Trigliserida-1
NaOC2H5 O C
O H
2
C R2
O C O H
2
C R1
O C O
H2
C R3
Trigliserida-2
[image:101.612.113.500.86.459.2](b)
Gambar 2.5. Reaksi Pertukaran Ester : (a) Reaksi Pertukaran Intermolekular, (b) Reaksi Pertukaran Intramolekular (Sari, 2016).
Interesterifikasi kimia menghasilkan suatu randomisasi gugus asil dalam trigliserida. Interesterifikasi kimia dapat terjadi tanpa menggunakan katalis, tetapi membutuhkan suhu yang sangat tinggi, pencampaian kesetimbangan (equilibrium) sangat lamban, trigliserida akan mengalami dekomposisi dan polimerisasi serta banyak menghasilkan asam lemak bebas (Silalahi, 1999).
Akumulasi produk hidrolisis berlangsung terus hingga tercapai suatu kesetimbangan (Willis, et.al. 1998).
2.7. Titik Lebur pada Lemak
Lemak dan minyak hewani dan nabati merupakan campuran dari gliserida dan komponen lainnya, sehingga tidak mempunyai titik lebur yang tepat, tetapi melebur/mencair diantara kisaran suhu tertentu. Asam lemak selalu menunjukkan kenaikan titik lebur dengan semakin panjangnya rantai karbon. Asam lemak yang derajat ketidakjenuhannya semakin tinggi, mempunyai titik lebur yang semakin rendah. Asam lemak yang berstruktur trans mempunyai titik lebur yang lebih tinggi daripada asam lemak yang berstruktur cis (Moran dan Rajah, 1994).Titik lebur lemak merupakan suatu sifat empiris yang berhubungan dengan sifat fisik lemak. Titik lebur berhubungan langsung terhadap temperatur dimana lemak mengkristal atau memadat. Semakin tinggi temperatur, maka titik lebur semakin tinggi, tergantung dari sifat poliformis kristal lemak. Titik lebur lemak tidak merupakan suhu yang tepat, tetapi merupakan kisaran suhu tertentu. Hal ini disebabkan karena minyak atau lemak disusun dari campuran gliserida dan komponen lainnya. Asam lemak seu menunjukkan kenaikan titik lebur, dengan semakin panjangnya rantai karbon dan semakin jenuhnya lemak tersebut (Sudarmadji, 1996).
2.8. Kandungan Lemak Padat
[image:103.612.106.519.251.357.2]Kandungan lemak padat merupakan ukuran dari jumlah padatan yang ada dalam lemak. Solid Fat Content (SFC) merupakan analisa lemak dan minyak yang diterima secara umum dalam industri makanan. SFC berkaitan dengan persentase minyak yang berupa padatan pada berbagai suhu (Tjeng, 2011). Nilai standar SFC untuk lemak margarin pada beberapa suhu dapat dilihat pada tabel 2.3 dibawah ini.
Tabel 2.3. Nilai Standar SFC Lemak Margarin
Analisis SFC
Temperatur Nilai SFC (%)
100C 12-40
210C 8-23
33,30C 2-4
Sumber : (O’Brien, 2008)
2.8.1.Dilatometri
Metode awal yang digunakan untuk memperkirakan persentase padatan pada lemak adalah dilatometry (AOCS Cd 10-57). Hasilnya disebut solid fat index. Namun, metode ini memakan waktu dan bersifat subjektif. Metode tradisional ini merupakan metode yang lambat, tidak dapat diulang, dan membutuhkan zat kimia (Tjeng, 2011).
lemak diukur dengan alat dilatometri. Dilatasi lemak ini memberikan suatu petunjuk perbandingan antara lemak padat dan lemak cair dalam sampel semi padat (Hamilton, 1986). Pada sistem pengukuran BS (British Standart), dilatasi diukur dalam satuan mm3/gr lemak dengan nilai range dari 10 untuk minyak cair sempurna hingga 2000-2500 untuk lemak padat (Hamilton and Rossell,1986).
2.8.2 .Differential Scanning Calorimetry (DSC)
DSC telah diusulkan sebagai alternatif yang mungkin untuk menggantikan dilatometri akan tetapi hasil DSC dipengaruhi oleh panas penggabungan, kecepatan kristalisasi dan peleburan ukuran sampel.
Che Man dan Swe (1997) menggunakan DSC untuk memonitor penyebab dari kristalisasi yang bermutu rendah dari batch palm oil yang gagal. Mereka menemukan bahwa termogram pendinginan dari palm oil dari batch yang gagal berbeda dari kristalisasi yang bagus. Mereka menunjukkan bahwa temperatur dan waktu pemanasan adalah berpengaruh pada termogram, dan menunjukkan korelasi antara termogram dan pembentukan kristal yang terjadi. Pemanasan atau pendinginan dan massa sampel juga mempengaruhi profil dari DSC termogram palm oil dan palm kernel oil yang telah dilaporkan beberapa peneliti (Haryati et. al. 1998) juga mendapatkan bahwa profil DSC juga bisa digunakan untuk menentukan sifat dari minyak-minyak lain seperti titik lebur, titik keruh, dan bilangan iodin.
2.8.3.Pulsed NMR
makanan. Pemakaian pulsed NMR dalam analisa lemak yaitu dengan penentuan kandungan lemak padat. Pulsed NMR memberikan pengukuran yang langsung dari padatan yang terdapat di dalam lemak yang diukur dibawah temperatur 40oC (Hamilton, 1986).
Fraksi dari fase padat yang diukur dengan pulsed NMR dapat didefenisikan sebagai perbandingan jumlah proton-proton fase padat dengan jumlah proton-proton dalam sampel. Tidak ada koreksi yang dibuat untuk membedakan proton antara fase padat dan fase cair. Nilainya dinyatakan dalam persentase, yang selalu disertai dengan penentuan temperatur.
Jika suatu sampel yang mengandung proton ditempatkan dalam suatu medan magnet yang sangat kuat, proton-proton bersifat seperti magnet batang yang sangat kecil dan cenderung searah dengan arah medan. Bila medan yang kedua digunakan dalam bentuk pulsa gelombang radio, penjajaran dapat diubah 900. Energi yang diserap oleh proton-proton memberikan gaya dorong untuk proses istirahat tertentu yang memungkinkan energi berubah antara proton-proton mereka sendiri atau antara proton-proton dengan kisi-kisi (Silalahi, 2002).
2.9. Kromatografi Gas
Kromatografi gas adalah suatu teknik untuk memisahkan zat yang mudah menguap dengan cara melewatkan aliran gas pada suatu fase yang tidak bergerak (stationary
phase). Pemisahan ini berdasarkan sifat-sifat penyerapan isi kolom untuk
Gambar 2.6. Diagram Alir Kromatografi Gas
Senyawa yang dapat dipisahkan dengan kromatografi gas sangat banyak, namun ada batasan-batasannya. Senyawa tersebut harus mudah menguap dan stabil pada temperatur pengujian. Temperatur ini berkisar 50-3000C. Jika senyawa yang diuji tidak dapat menguap dan stabil pada temperatur pengujian, maka senyawa tersebut bias diderivatisasi agar dapat dianalisis dengan kromatografi gas (Mardoni et.
al., 2007).
Cara kerja kromatografi gas antara lain: sampel diinjeksikan melalui suatu sampel injection port yang temperaturnya dapat diatur, senyawa-senyawa dalam sampel akan menguap dan akan dibawa oleh gas pengemban menuju kolom. Zat terlarut akan teradsorpsi pada bagian atas kolom oleh fase diam, kemudian akan merambat dengan laju rambatan masing-masing komponen yang sesuai dengan nilai
temperature 2200C dan waktu analisis dalam sekali penginjeksian adalah 36,25 menit. Untuk masing-masing trigliserida dideteksi berdasarkan berat molekulnya seperti halnya urutan trigliserida Miristat Miristat Palmitat (C44:0) memiliki berat molekul yang sama dengan Miristat Palmitat Miristat (C44:0) akan memberikan waktu retensi yang sama dalam analisis komposisi trigliserida (Agilent, 2003).
2.9.1. Fase Mobil (Gas Pembawa)
Faktor yang menyebabkan suatu senyawa bergerak melalui kolom kromatografi gas adalah keatsirian yang merupakan sifat senyawa itu dan aliran gas melalui kolom. Aliran gas dipaparkan dengan dua peubah, aliran yang diukur dalam ml/menit dan penurunan tekanan antara pangkal dan ujung kolom (Gritter, 1991).
Fase mobil (gas pembawa) dipasok dari tangki melalui pengaturan pengurangan tekanan, kemudian membawa cuplikan langsung ke dalam kolom. Jika hal ini terjadi, cuplikan tidak menyebar sebelum proses pemisahan. Cara ini cocok untuk cuplikan yang mudah menyerap.
Gas pembawa ini harus bersifat inert dan harus sangat murni. Seringkali gas pembawa ini harus disaring untuk menahan debu uap air dan oksigen. Gas yang sering digunakan adalah N2, H2, He, dan Ar (Hendrayati, 2010).
2.9.2. Injeksi Sampel
Sejumlah kecil sampel yang akan dianalisis diinjeksikan pada mesin menggunakan semprit kecil. Jarum semprit menembus lempengan karet tebal (lempengan karet ini disebut septum) yang mana akan mengubah bentuknya kembali secara otomatis ketika semprit ditarik keluar dari lempengan karet tersebut.
Komponen pilihan gas pembawa terutama tergantung pada karakteristik detektor (Hendrayati, 2010).
Cuplikan dimasukkan ke dalam ruang suntik melalui gerbang suntik, biasanya berupa lubang yang ditutupi dengan pemisah karet. Ruang suntik harus dipanaskan tersendiri, terpisah dari kolom, biasanya pada suhu 10-150C lebih tinggi daripada suhu kolom maksimum. Jadi seluruh cuplikan diuapkan segera setelah disuntikkan dan dibawa ke kolom (Gritter, 1991).
2.9.3. Kolom
Ada dua tipe utama kolom dalam kromatografi gas-cair. Tipe pertama, kolom partisi, berisi bahan padat inert menyangga lapisan tipis cairan, disebut kromatografi gas cair (GLC). Tipe kedua, kolom adsorpsi berisi partikel penyerap yang umumnya digunakan untuk analisa gas permanen dan hidrokarbon rendah, disebut kromatografi gas padat (GSC).
Kolom biasanya dibuat dari baja tak berkarat dengan panjang antara 1 sampai 4 meter, dengan diameter internal sampai 4 mm. kolom digulung sehingga dapat disesuaikan dengan oven yang terkontrol secara termostatis. Kolom dipadatkan dengan tanah diatomae, yang merupakan batu yang sangat berpori. Tanah ini dilapisi dengan cairan bertitik didih tinggi dan biasanya polimer lilin.
2.9.4. Detektor
Elusi zat terlarut dari kolom mengatur ketidakseimbangan antara dua sisi detektor yang direkam secara elektrik. Laju aliran gas pembawa adalah hal yang sangat penting, dan biasanya pengukur aliran untuk itu tersedia. Secara normal gas-gas yang muncul dialirkan keluar pada tekanan atmosfer.
Dalam mekanisme reaksi, pembakaran senyawa organik merupakan hal yang sangat kompleks. Selama proses, sejumlah ion-ion dan elektron-elektron dihasilkan dalam nyala. Kehadiran ion dan elektron dapat dideteksi. Seluruh detektor ditutup dalam oven yang lebih panas dibanding dengan temperatur kolom. Hal itu menghentikan kondensasi dalam detektor. Jika tidak terdapat senyawa organik datang dari kolom, kita hanya memiliki nyala hidrogen yang terbakar dalam air.
Ketika dibakar, itu akan menghasilkan sejumlah ion-ion dan elektron-elektron dalam nyala. Ion positif akan beratraksi pada katoda silinder. Ion-ion negatif dan elektron-elektron akan beratraksi pancarannya masing-masing yang merupakan anoda. Hal ini serupa dengan apa yang terjadi selama elektrolisis normal.
Kekurangan utama dari detektor ini adalah perusakan setiap hasil y