EFEK HEPATOPROTEKTIF PEMBERIAN JANGKA PANJANG INFUSA HERBA Bidens pilosa L. TERHADAP AKTIVITAS ALT-AST SERUM
PADA TIKUS BETINA TERINDUKSI KARBON TETRAKLORIDA
Leonardo Susanto Utomo, C. J. Soegihardjo Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
INTISARI
Penelitian ini bertujuan untuk mendapatkan informasi tentang efek hepatoprotektif pemberian infusa Herba Bidens pilosa L. jangka panjang dapat menurunkan aktivitas ALT dan AST serum pada tikus betina terinduksi karbon tetraklorida, serta mendapatkan dosis efektifnya.
Penelitian ini bersifat eksperimental murni dengan rancangan acak lengkap pola searah. Penelitian yang dilakukan menggunakan 30 ekor tikus betina galur Wistar, umur 2-3 bulan, dan berat ± 130-200 gram. Tikus dibagi ke dalam enam kelompok perlakuan secara acak. Kelompok I merupakan kontrol hepatotoksin Karbon tetraklorida diberikan secara i.p. dengan dosis 2,0 ml/kgBB. Kelompok II merupakan kontrol negatif yaitu pemberian olive oil 2,0 mL/kgBB. Kelompok III merupakan kontrol perlakuan yaitu pemberian infusa Herba Bidens pilosa L. secara per oral dengan dosis 2,0 g/kgBB. Kelompok IV-VI diberikan infusa Herba
Bidens pilosa L. (dosis 0,5;1,0;2,0 g/kgBB) selama 6 hari berturut-turut, kemudian pada hari ke-7 diberi Karbon tetraklorida dengan dosis 2,0 mL/kgBB secara intraperitonial. Setelah 24 jam diambil darahnya melalui sinus orbitalis mata, lalu diukur aktivitas serum ALT-AST. Data yang diperoleh diuji secara statistik one way ANOVA dengan taraf kepercayaan 95% dan dilanjutkan uji Scheffe atau uji T berpasangan.
Hasil penelitian menunjukan adanya efek hepatoprotektif infusa herba
Bidens pilosa L. dilihat dari penurunan aktivitas ALT dan AST serum. Efek hepatoprotektif dari dosis 0,5;1,0;2,0 g/kgBB adalah 74,6;87,5;50,2%. Dari data yang diperoleh dosis efektif herba Bidens pilosa L. adalah 1,0 g/kgBB.
ABSTRACT
The aim of this research were to prove information about hepatoprotective effect of Bidens pilosa L. herbs infusion for reducing activities of ALT and AST serum in female rats induced by carbon tetrachloride and get a value of effective dose.
This research was pure experimental research with randomized complete direct sampling design. This research used female Wistar rats, age about 2-3 months, and ± 130-200 gram weight. Rats were divided randomly into six groups. Group I (control hepatotoxins) were given with carbon tetrachloride 2.0 ml/kgBW i.p. Group II (negative control) were given olive oil 2.0 ml/kgBW. Group III (control infusion) were given infusion of Bidens pilosa L. herbs 2.0 g/kgBW. Group IV-VI (treatment group) were given Bidens pilosa L. herb infusion orally once a day for six days in a row with dose 0.5; 1.0; and 2.0 g/kgBW, then in seventh day the treatments group were given carbon tetrachloride 2.0 ml/kgBW i.p. After 24 hours, blood collected from the orbital sinus region and then measured ALT and AST serum activities. The obtained data ALT and AST serum activities were analyzed using one-way ANOVA with 95% significancy level and continued with Scheffe test or paired T test.
The results showed that administration infusion of Bidens pilosa L. herb has a hepatoprotective effect by reducing ALT and AST activities. Hepatoprotective effects from the lowest to highest doses were 74.6%; 87.5%, 50.2%. From the data, the effective dose of Bidens pilosa L. herb infusion was 1.0 g/kgBW.
EFEK HEPATOPROTEKTIF PEMBERIAN JANGKA PANJANG INFUSA HERBA Bidens pilosa L. TERHADAP AKTIVITAS ALT-AST SERUM
PADA TIKUS BETINA TERINDUKSI KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Menenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Leonardo Susanto Utomo
NIM : 118114105
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
HALAMAN PERSEMBAHAN
“Pindahkanlah pikiran
kedalam tubuhmu !
Jangan biarkan tubuh memaksa pikiranmu,
karena tubuh akan selalu menyerah”
–
Leonardo Susanto-
“
Shobai wa kusa no tane
”
“There are as many ways of making a living as seeds of grass”
–
Japanese Proverbs-
kupersembahkan skripsiku ini untuk...
Tuhan yang Maha Kuasa,
Papa dan Mama yang telah berjuang membesarkanku selama ini dalam
situasi apapun,
Kakak-adikku :
Brianata Susanto Utomo, S.Ked.
Asgard Susanto Utomo
Natasha Susanto Utomo
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas berkat-Nya penulis dapat
menyelesaikan penulisan skripsi dengan judul “Efek Hepatoprotektif
Pemberian Jangka Panjang infusa herba Bidens pilosa L. terhadap Aktivitas
ALT-AST SERUM pada Tikus Betina Terinduksi Karbon Tetraklorida”.
Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana
Farmasi di Fakultas Farmasi, Universitas Sanata Dharma,Yogyakarta.
Penulis menyadari bahwa dalam panjangnya proses pelaksanaan dan
penyusunan skripsi ini banyak pihak telah memberi bimbingan, bantuan dan
dukungan. Oleh karena itu, pada kesempatan ini penulis mengucapkan terima
kasih kepada:
1. Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ketua Program Studi Fakultas Farmasi Universitas Sanata Dharma.
3. Bapak Prof. Dr. C. J. Soegihardjo, Apt. selaku Dosen Pembimbing sekaligus
Dosen Penguji skripsi yang telah banyak memberikan bimbingan, masukan,
kritik, koreksi, dan saran selama penelitian hingga berakhirnya penyusunan
skripsi.
4. Bapak Ipang Djunarko, M.Sc., Apt. sebagai Dosen Penguji skripsi atas
motivasi, bantuan dan masukan demi kemajuan skripsi ini.
5. Ibu Phebe Hendra, M.Si., Ph.D., Apt. sebagai Dosen Penguji skripsi atas
6. Ibu Agustina Setiawati, M.Sc., Apt. selaku Kepala Laboratorium Fakultas
Farmasi yang telah memberikan ijin dalam penggunaan semua fasilitas
laboratorium untuk kepentingan penelitian ini.
7. Bapak Yohanes Dwiatmaka, M.Si., atas bantuan dalam determinasi tanaman
Bidens pilosa L.
8. Bapak Heru, Bapak Suparjiman, dan Bapak Kayatno selaku laboran bagian
Farmakologi dan Toksikologi, Bapak Wagiran selaku laboran Farmakognosi
Fitokimia, serta Bapak Kunto selaku laboran Kimia Analisis atas segala
bantuan selama pelaksanaan skripsi ini.
9. Papa, mama dan keluarga atas doa, dukungan, dan kasih sayang sehingga
penulis semangat dalam penulisan skrispsi ini.
10. Irene Deandra Indarto, S.T., atas segala doa, perhatian, motivasi, dukungan,
waktu dan kasih sayangnya.
11. Rekan-rekan penelitian “Bidens pilosa L.” Alexander Budi Kuncoro,
Apriyanto Gomes, Prasetyo Handy Kurniawan, dan Vina Alvionita atas kerja
sama, perjuangan, dan suka duka dalam menyelesaikan skripsi ini.
12. Seluruh teman-teman angkatan 2011, FKK B 2011, serta PCC, yang selalu
menghibur, mendukung, serta memotivasi penulis dalam penyelesaian skripsi
ini.
13. Semua pihak yang tidak dapat penulis sebutkan satu per satu yang turut
Penulis menyadari bahwa banyak kesalahan dan kekurangan dalam
penulisan skripsi ini. Untuk itu penulis mengharapkan kritik dan saran yang
membangun agar penulisan skripsi ini menjadi lebih baik. Akhir kata, semoga
skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan khususnya di
bidang farmasi, serta semua pihak yang berkepentingan.
Penulisaaaaaaaaaaaaa
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA... vi
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
INTISARI ... xvii
ABSTRACT... xviii
BAB I. PENGANTAR ... 1
A. Latar Belakang... 1
1. Perumusan masalah ... 3
2. Keaslian penelitian ... 3
B. Tujuan Penelitian ... 4
1. Tujuan umum ... 4
2. Tujuan khusus ... 5
BAB II. PENELAAHAN PUSTAKA ... 6
A. Tanaman Bidens pilosa L. ... 6
1. Taksonomi ... 6
2. Morfologi... 6
3. Kandungan kimia & kegunaan ... 7
B. Hati ... 8
1. Anatomi dan fisiologi hati ... 8
2. Kerusakan sel-sel hati ... 10
3. Perlemakan hati ... 11
4. Hepatotoksin ... 12
5. ALT dan AST... 13
C. Karbon tetraklorida... 14
D. Infusa ... 16
E. Landasan Teori... 17
F. Hipotesis ... 18
BAB III. METODOLOGI PENELITIAN ... 19
A. Jenis dan Rancangan Penelitian ... 19
B. Variabel dan Definisi Operasional ... 19
1. Variabel utama ... 19
2. Variabel pengacau... 19
C. Bahan Penelitian ... 21
4. Alat uji hepatoprotektif... 22
E. Tata Cara Penelitian... 23
1. Determinasi tanaman Herba Bidens pilosa L ... 23
2. Pengumpulan bahan uji ... 23
3. Pembuatan serbuk herba Bidens pilosa L.... 23
4. Penetapan kadar air pada serbuk herba Bidens pilosa L. ... 23
5. Pembuatan infusa herba Bidens pilosa L. ... 24
6. Pembuatan larutan karbon tetraklorida konsentrasi 50% ... 24
7. Uji pendahuluan ... 24
8. Pengelompokkan dan perlakuan hewan uji ... 25
9. Pembuatan serum ... 26
10. Pengukuran aktivitas serum ALT-AST ... 27
F. Tata Cara Analisis Hasil ... 27
BAB IV. HASIL DAN PEMBAHASAN ... 29
A. Hasil Determinasi Tanaman ... 29
B. Penyiapan Bahan ... 29
1. Pembuatan serbuk herba Bidens pilosa L... 29
2. Penetapan kadar air serbuk herba Bidens pilosa L. ... 30
1. Penentuan dosis hepatotoksin karbon tetraklorida... 30
2. Penentuan dosis infusa... 31
3. Penentuan waktu pencuplikan darah ... 31
D. Hasil Uji Efek hepatoprotektif infusa herba Bidens pilosa L. ... 34
1. Kontrol negatif olive oil... 37
2. Kontrol hepatotoksin karbon tetraklorida dosis 2,0 mL/kgBB ... 39
3. Kontrol infusa herba Bidens pilosa L. dosis 2,0 g/kgBB ... 41
4. Kelompok perlakuan infusa dosis 0,5;1,0; dan 1,0 g/kgBB pada tikus betina galur Wistar terinduksi karbon tetraklorida dosis 2,0 mL/kgBB ... 41
E. Rangkuman Pembahasan... 45
BAB V. KESIMPULAN DAN SARAN ... 47
A. Kesimpulan ... 47
B. Saran ... 47
DAFTAR PUSTAKA ... 48
LAMPIRAN ... 51
DAFTAR TABEL
Tabel I. Purata aktivitas serum ALT ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB... 31
Tabel II. Hasil uji Scheffe aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 33
Tabel III. Purata aktivitas serum AST ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB... 33
Tabel IV. Hasil uji Scheffe aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 34
Tabel V. Purata ± SE aktivitas serum ALT dan AST tikus betina galur Wistar pada kelompok perlakuan ... 35
Tabel VI. Hasil uji Scheffe aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan ... 35
Tabel VII. Hasil uji Scheffe aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan ... 37
Tabel VIII. Purata ± SE aktivitas serum ALT dan AST setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0 dan 24 jam ... 38
DAFTAR GAMBAR
Gambar 1. Tanaman herba Bidens pilosa L... 7
Gambar 2. Struktur Quercetin (Bartolome et al., 2013). ... 7
Gambar 3. Satu bagian dari lobus hati terdiri dari pembuluh darah, sel hepatik, sinusoid hati, dan percabangan vena portal dan arteri hepatik (Carol and Glenn, 2009) ... 9
Gambar 4. Struktur mikroskopik hati yang mengalami steatosis (Rubin and
Farber, 1999). ... 12
Gambar 5. Metabolisme karbon tetraklorida dengan adanya oksigen dan molekul organik. RH menggambarkan asam lemak tak jenuh. (Weber, Boll, dan Stampfl., 2003). ... 16
Gambar 6. Diagram batang purata aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mg/kgBB .. 32
Gambar 7. Diagram batang purata aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mg/kgBB .. 33
Gambar 8. Diagram batang purata aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan ... 36
Gambar 9. Diagram batang purata aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan ... 36
Gambar 10. Diagram batang purata aktivitas serum ALT setelah pemberian olive oil dosis 2,0 mL/kgBB pada selang waktu 0 dan 24 jam... 38
DAFTAR LAMPIRAN
Lampiran 1. Foto serbuk herba Bidens pilosa L. ... 52
Lampiran 2. Foto pembuatan infusa herba Bidens pilosa L. ... 52
Lampiran 3. Foto infusa herba Bidens pilosa L. ... 52
Lampiran 4. Surat pengesahan determinasi tanaman herba Bidens pilosa L. ... 53
Lampiran 5. Surat pengesahan Medical and Health Research Ethics Committee (MHREC) ... 54
Lampiran 6. Analisis statistik aktivitas serum ALT pada uji pendahuluan dosis hepatotoksin karbon tetraklorida 2 mL/kgBB ... 55
Lampiran 7. Analisis statistik aktivitas serum AST pada uji pendahuluan dosis hepatotoksin karbon tetraklorida 2 mL/kgBB ... 57
Lampiran 8. Analisis statistik aktivitas serum ALT pada kelompok kontrol olive oil 2 mL/kgBB ... 59
Lampiran 9. Analisis statistik aktivitas serum AST pada kelompok kontrol olive oil 2 mL/kgBB ... 61
Lampiran 10. Analisis statistik aktivitas serum ALT pada perlakuan infusa herba Bidens pilosa L. setelah induksi karbon tetraklorida 2 mL/kgBB ... 64
Lampiran 11. Analisis statistik aktivitas serum AST pada perlakuan infusa herba Bidens pilosa L. setelah induksi karbon tetraklorida 2 mL/kgBB ... 67
INTISARI
Penelitian ini bertujuan untuk mendapatkan informasi tentang efek hepatoprotektif pemberian infusa Herba Bidens pilosa L. jangka panjang dapat menurunkan aktivitas ALT dan AST serum pada tikus betina terinduksi karbon tetraklorida, serta mendapatkan dosis efektifnya.
Penelitian ini bersifat eksperimental murni dengan rancangan acak lengkap pola searah. Penelitian yang dilakukan menggunakan 30 ekor tikus betina galur Wistar, umur 2-3 bulan, dan berat ± 130-200 gram. Tikus dibagi ke dalam enam kelompok perlakuan secara acak. Kelompok I merupakan kontrol hepatotoksin Karbon tetraklorida diberikan secara i.p. dengan dosis 2,0 ml/kgBB. Kelompok II merupakan kontrol negatif yaitu pemberian olive oil 2,0 mL/kgBB. Kelompok III merupakan kontrol perlakuan yaitu pemberian infusa Herba Bidens pilosa L. secara per oral dengan dosis 2,0 g/kgBB. Kelompok IV-VI diberikan infusa Herba
Bidens pilosa L. (dosis 0,5;1,0;2,0 g/kgBB) selama 6 hari berturut-turut, kemudian pada hari ke-7 diberi Karbon tetraklorida dengan dosis 2,0 mL/kgBB secara intraperitonial. Setelah 24 jam diambil darahnya melalui sinus orbitalis mata, lalu diukur aktivitas serum ALT-AST. Data yang diperoleh diuji secara statistik one way ANOVA dengan taraf kepercayaan 95% dan dilanjutkan uji Scheffe atau uji T berpasangan.
Hasil penelitian menunjukan adanya efek hepatoprotektif infusa herba
Bidens pilosa L. dilihat dari penurunan aktivitas ALT dan AST serum. Efek hepatoprotektif dari dosis 0,5;1,0;2,0 g/kgBB adalah 74,6;87,5;50,2%. Dari data yang diperoleh dosis efektif herba Bidens pilosa L. adalah 1,0 g/kgBB.
ABSTRACT
The aim of this research were to prove information about hepatoprotective effect of Bidens pilosa L. herbs infusion for reducing activities of ALT and AST serum in female rats induced by carbon tetrachloride and get a value of effective dose.
This research was pure experimental research with randomized complete direct sampling design. This research used female Wistar rats, age about 2-3 months, and ± 130-200 gram weight. Rats were divided randomly into six groups. Group I (control hepatotoxins) were given with carbon tetrachloride 2.0 ml/kgBW i.p. Group II (negative control) were given olive oil 2.0 ml/kgBW. Group III (control infusion) were given infusion of Bidens pilosa L. herbs 2.0 g/kgBW. Group IV-VI (treatment group) were given Bidens pilosa L. herb infusion orally once a day for six days in a row with dose 0.5; 1.0; and 2.0 g/kgBW, then in seventh day the treatments group were given carbon tetrachloride 2.0 ml/kgBW i.p. After 24 hours, blood collected from the orbital sinus region and then measured ALT and AST serum activities. The obtained data ALT and AST serum activities were analyzed using one-way ANOVA with 95% significancy level and continued with Scheffe test or paired T test.
The results showed that administration infusion of Bidens pilosa L. herb has a hepatoprotective effect by reducing ALT and AST activities. Hepatoprotective effects from the lowest to highest doses were 74.6%; 87.5%, 50.2%. From the data, the effective dose of Bidens pilosa L. herb infusion was 1.0 g/kgBW.
BAB I PENGANTAR
A. Latar Belakang
Hati merupakan organ terbesar dalam tubuh yang memiliki peran penting
bagi manusia, hati berfungsi untuk proses metabolisme seperti karbohidrat, lemak
dan protein serta memetabolisme xenobiotik (Stine dan Brown, 2006). Fungsi hati
sebagai pemetabolisme maka hati rentan terkena penyakit. Penyakit hati dapat
disebabkan oleh obat, bahan kimia, alkohol, toksin, atau infeksi virus (Crowley,
2001).
Penyakit yang sering muncul pada organ hati adalah perlemakan hati, yang
dibagi menjadi dua yaitu diperantarai alkohol dan tidak diperantarai alkohol.
Perlemakan hati tidak diperantarai alkohol (NAFLD) prevalensinya cukup tinggi
di negara-negara bagian Asia-Pasifik. Prevalensi NAFLD di Indonesia mencapai
30% dan menduduki peringkat pertama dibandingkan dengan negara Asia-Pasifik
lainnya (Amarapurkar et al, 2007). NAFLD (Non-Alcoholic Fatty Liver Disease)
yang tidak ditangani akan berkembang menjadi NASH (Non-Alcoholic
Steatohepatitis), bahkan kanker hati (Starley, Calcagno and Harrison, 2010).
Selama dekade terakhir, penggunaan pengobatan herbal untuk
pengobatan NAFLD telah mengalami kemajuan dan menjadi perhatian karena
ketersediaan luas selain itu efek samping yang rendah dan mekanisme terapi
tanaman telah banyak diteliti dan berpotensi dalam pengobatan NAFLD (Xiao,
Fai So, Liong and Tipoe, 2013).
Karbon tetraklorida merupakan senyawa yang sering digunakan untuk
permodelan kerusakan hati. Senyawa karbon tetraklorida akan metabolisme oleh
sitokrom P450 menjadi radikal bebas trikolorometil yang dapat menyebabkan
kerusakan hati, salah satunya dapat menyebabkan perlemakan hati.
Herba Bidens pilosa L. merupakan tanaman yang ditemukan di bagian
Amerika Selatan, namun sekarang sudah ditemukan di semua negara wilayah
tropis dan subtropis termasuk Indonesia. Herba Bidens pilosa L. memiliki potensi
sebagai antioksidan. Menurut Kviecinski et al. (2011), herba Bidens pilosa L.
pada fraksi etil asetat, memiliki senyawa metabolit flavonoid yang dapat
menangkap radikal bebas dan berpotensi menjadi hepatoprotektor. Penelitian
tersebut didukung oleh penelitian Silva et al., (2011) yang menyatakan bahwa
polyasetilen dan flavonoid adalah metabolit yang mendominasi di tanaman Bidens
pilosa L.
Menurut Kviecinski et al. (2011) pemberian fraksi etil asetat Bidens pilosa
L. selama sepuluh hari dapat memberikan efek hepatoprotektif pada tikus yang
terinduksi karbon tetraklorida. Penelitian lain dilakukan Hendra dan Mahendra
(2011) pemberian jangka panjang infusa daun Macaranga tanarius L. yaitu
selama enam hari berturut-turut dapat memberikan efek hepatoprotektif.
Penelitian ini menggunakan sediaan berupa infusa karena melihat
kedekatan dengan kebiasaan masyarakat dimana sediaan infusa ini mirip dengan
yang ingin diambil juga larut dalam air sehingga metode infusa dapat digunakan
untuk mengekstrak metabolit tersebut dari herba Bidens pilosa L. (Xu et al.,
2008).
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif pemberian
jangka panjang infusa herba Bidens pilosa L. pada tikus betina terinduksi karbon
tetraklorida. Dengan adanya penelitian ini, diharapkan dapat menambah
pengetahuan dan memberikan informasi tentang tanaman hepatoprotektif.
1. Perumusan masalah
Berdasarkan latar belakang diatas dapat dirumuskan permasalahan sebagai
berikut :
a. Apakah pemberian jangka panjang infusa herba Bidens pilosa L. mempunyai
pengaruh hepatoprotektif dengan menurunkan aktivitas ALT-AST serum pada
tikus betina galur Wistar terinduksi karbon tetraklorida?
b. Berapakah dosis efektif infusa herba Bidens pilosa L. jangka panjang yang
memiliki efek hepatoprotektif paling besar pada tikus betina galur Wistar
terinduksi karbon tetraklorida?
2. Keaslian penelitian
Penelitian tentang efek hepatoprotektif pemberian jangka panjang infusa
herba Bidens pilosa L. pada tikus betina galur Wistar terinduksi karbon
tetraklorida belum pernah dilakukan sebelumnya. Penelitian yang telah dilakukan
berkaitan dengan herba Bidens pilosa L. yaitu :
1. Penelitian yang dilakukan oleh Kviecinski, et al (2011). Pada penelitian
efek hepatoprotektif dari fraksi etil asetat herba Bidens pilosa L. asal Brazil
yang mengandung kuersetin – derivat flavonoid. Selain itu, juga ditemukan
adanya efek hepatoprotektif.
2. Penelitian yang dilakukan oleh Ariyanti (2007) menguji aktivitas antioksidan
dari fraksi air ekstrak metanolik herba Bidens pilosa L., namun tidak dilakukan
uji aktivitas ekstrak herba Bidens pilosa L. sebagai hepatoprotektif.
3. Penelitian yang dilakukan oleh Silva et al., (2011) melaporkan bahwa
polyasetilen dan flavonoid adalah metabolit yang mendominasi dalam
fitokimia herba Bidens pilosa L.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat menambah pengetahuan tentang tanamann
herba Bidens pilosa L. yang memiliki potensi hepatoprotektif.
b. Manfaat praktis
Penelitian ini diharapkan mampu memberikan informasi kepada
masyarakat tentang dosis efektif penggunaan jangka panjang infusa herba
Bidens pilosa L. yang memberikan proteksi terhadap perlemakan hati.
B. Tujuan Penelitian 1. Tujuan umum
Tujuan umum dari penelitian ini adalah untuk mengetahui kemampuan
infusa herba Bidens pilosa L. terhadap perbaikan fungsi hati tikus betina galur
2. Tujuan khusus
a. Pemberian jangka panjang infusa herba Bidens pilosa L. mempunyai
pengaruh hepatoprotektif dengan menurunkan aktivitas serum ALT dan
AST pada tikus betina galur Wistar terinduksi karbon tetraklorida.
b. Mengetahui besar dosis efektif hepatoprotektif infusa herba Bidens pilosa L.
BAB II
1. Taksonomi
: Asterales
Keluarga : Asteraceae
Marga : Bidens
Varietas : Bidens pilosa L. (Bartolome, Villasenor, and Yang, 2013).
2. Morfologi
Tanaman Bidens pilosa Linn. merupakan tanaman berbatang lunak yang
berasal dari Amerika. Bidens pilosa L. tumbuh di dekat air, kebun atau ladang,
halaman rumah, dan pinggiran jalan pada ketinggian 250-2.500 meter dpl. Tinggi
tanaman ini dapat mencapai 150 cm
PENELAAHAN PUSTAKA
A. Tanaman Bidens pilosa L.
Klasifikasi dari tumbuhan Bidens pilosa L. adalah sebagai berikut.
Divisi : Spermatophyta
Kingdom : Plantae
Sub Kingdom : Tracheobionta
Superdivisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Gambar 1. Tanaman herba Bidens pilosa L.
Gambar 1 menunjukan morfologi dari tanaman herba Bidens pilosa L.
dengan batang berbentuk segi empat berwarna hijau, daun terbagi tiga, berbentuk
bulat telur dengan tepi bergerigi. Bunga bertangkai panjang, mahkota bunga
berwarna putih dengan putik berwarna kuning (Sugiarto and Putera, 2008).
3. Kandungan kimia & kegunaan
Gambar 2. Struktur Quercetin (Bartolome et al., 2013).
Senyawa bioaktif primer yang terkandung dalam Bidens pilosa L. adalah
polyynes, flavonoid, phenylpropanoids, asam lemak, dan fenolat. Senyawa
tersebut dilaporkan efektif dalam pengobatan tumor, inflamasi/memodulasi
penyakit kardiovaskular. Menurut penelitian yang ada, Bidens pilosa L. diklaim
dapat mengobati lebih dari 40 macam penyakit dan ada 201 senyawa yang telah di
identifikasi dari Bidens pilosa L. Salah satunya adalah flavonoid quercetin yang
ditunjukkan pada Gambar 2 (Bartolome, Villasenor and Yang, 2013).
B. Hati 1. Anatomi dan fisiologi hati
Hati merupakan organ terbesar di tubuh yang berada di kuadran kanan atas
rongga abdomen. Hati terbungkus oleh sebuah kapsul fibroelastik yang disebut
kapsul Glisson dan secara makroskopik dipisahkan menjadi lobus kiri dan lobus
kanan. Kapsul Glisson berisi pembuluh darah, pembuluh limfe, dan saraf. Kedua
lobus hati tersusun oleh unit-unit yang lebih kecil disebut lobulus. Lobulus terdiri
atas sel-sel hepatosit atau disebut dengan hepatosit yang menyatu dalam suatu
lempeng. Hepatosit dianggap sebagai unit fungsional hati. Sel-sel hati dapat
melakukan pembelahan sel dan mudah diproduksi kembali saat dibutuhkan untuk
mengganti jaringan yang rusak (Corwin, 2007).
Hati menerima darah dari vena portae hepatis dan arteri hepatica
sebanyak 70% dan 30% (Wibowo dan Paryana, 2009). Vena porta hepatica
membawa darah masuk ke hati dari saluran cerna dan limfa, sedangkan arteri
hepatica membawa darah dari aorta ke hati. Darah yang masuk ke hati melalui
vena. Volume total darah yang masuk dalam hati adalah 1500 ml setiap menitnya
(Price and Wilson, 2005).
Lobulus merupakan unit yang fungional dari hati. Lobulus memiliki
milimeter. Terdapat kurang lebih 50.000 – 100.000 lobulus di hati. Sel-hel hepatik
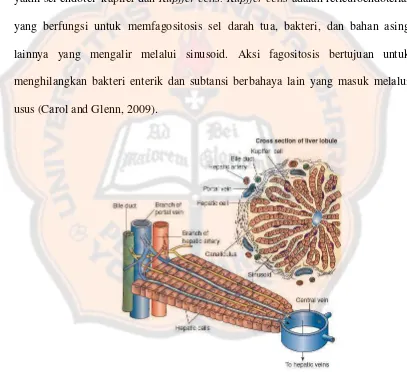
membentuk plat memutari vena sentral seperti jari-jari pada roda (Gambar 3).
Lempeng sel hepatosit dipisahkan oleh kapiler sinusoidal berdinding tipis yang
disebut sinusoid yang membentang dari pinggiran lobulus ke vena pusat. Sinusoid
disuplai darah melalui vena porta arteri hepatika. Sinusoid dilapisi dua buah sel,
yakni sel endotel kapiler dan Kupffer cells. Kupffer cells adalah reticuloendotelial
yang berfungsi untuk memfagositosis sel darah tua, bakteri, dan bahan asing
lainnya yang mengalir melalui sinusoid. Aksi fagositosis bertujuan untuk
menghilangkan bakteri enterik dan subtansi berbahaya lain yang masuk melalui
usus (Carol and Glenn, 2009).
Gambar 3. Satu bagian dari lobus hati terdiri dari pembuluh darah, sel hepatik, sinusoid hati, dan percabangan vena portal dan arteri hepatik
(Carol and Glenn, 2009)
Vena porta hepatica membawa darah yang mengandung nutrisi tidak
mengandung oksigen. Peredaran darah yang membawa oksigen hanya sekitar 30%
menyebabkan sel hati relatif kekurangan oksigen, sehingga mengakibatkan hati
rentan terhadap kerusakan (Wiboyo dan Paryana, 2009).
Hati memiliki peranan yang penting dalam setiap metabolisme dalam
tubuh dan bertanggung jawab dalam 500 aktivitas yang berbeda. Fungsi utama
dari hati adalah membentuk dan mengekskresi empedu, kemudian akan disimpan
dalam kandung empedu (Price and Wilson, 2005).
Fungsi lain dari hati adalah untuk metabolisme lemak dan detoksifikasi
sejumlah zat endogen dan eksogen. Fungsi hati untuk detoksifikasi sangat penting
dan dilakukan melalui reaksi oksidasi, reduksi, hidrolisis atau konjugasi dari zat
yang berbahaya diubah menjadi zat yang secara fisiologis tidak aktif (Price and
Wilson, 2005).
Peran hati untuk eliminasi adalah melalui metabolisme obat induk menjadi
metabolitnya. Hati dapat memetabolisme obat menjadi metabolitnya tergantung
dari aktifitas enzim pemetabolisme yang terdapat pada reticulum endoplasma
halus dan sitosol di hepatosit. Jumlah obat bebas yang dibawa masuk ke dalam
hepatosit dipengaruhi oleh jumlah protein pengikat obat di dalam darah (DiPiro et
al., 2008).
2. Kerusakan sel-sel hati
Hati merupakan organ yang rentan terhadap berbagai metabolisme, racun,
mikroba, dan serangan neoplastik. Penyakit hati yang utama adalah hepatitis
karena virus, penyakit hati alkoholik, Non Alcoholic Fatty Liver Disease
pada umumnya dapat dapat ditutupi karena besarnya cadangan hati, namun bila
gangguan penyakit menyebar atau ada gangguan aliran cairan empedu, dampak
yang di terima hati akan sangat membahayakan (Kumar, Abbas, Fausto and
Aster, 2010).
Berdasarkan manifestasi klinik dan pola spesifik pada
histopatologi, kerusakan hati dibagi menjadi:
1. Nekrosis sentrilobular, terjadi pada induksi obat yang bersifat
hepatotoksik mengakibatkan adanya metabolisme yang beracun.
Kerusakan yang terjadi menyebar ke luar mulai dari tengah lobus.
2. Steatonecrosis, kerusakan sel hati akut dengan penumpukan lemak
pada sel-sel hati hal ini terjadi karena adanya obat-obat yang
mempengaruhi proses oksidasi asam lemak di dalam mitokondria.
3. Phospholipidosis, merupakan akumulasi dari phospholipid sebagai
pengganti asam lemak. Phospholipid dapat menelan badan lisosom
pada sel hati.
4. Nekrosis hepatoselular tergeneralisasi, hampir mirip dengan terjadinya
perubahan karena adanya infeksi hati oleh virus. Waktu terjadinya satu
minggu setelah terinduksi zat beracun (DiPiro et al., 2008).
3. Perlemakan hati
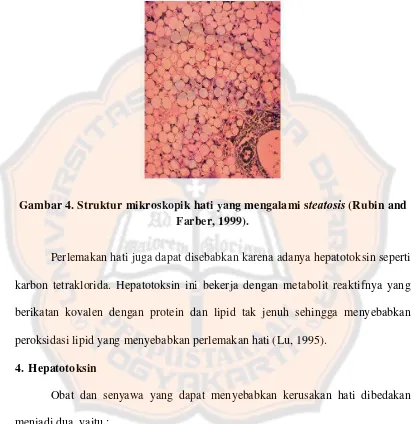
Perlemakan hati adalah keadaan dimana jumlah lemak dihati melebihi 5%
dari berat hati. Perlemakan hati (Gambar 4) terjadi karena adanya akumulasi
beberapa hal seperti kelebihan asam lemak, trigleserida yang tidak dapat di
transport, dan turunnya sintesis lipoprotein (Gregus and Klaaseen, 2001).
Gambar 4. Struktur mikroskopik hati yang mengalami steatosis (Rubin and Farber, 1999).
Perlemakan hati juga dapat disebabkan karena adanya hepatotoksin seperti
karbon tetraklorida. Hepatotoksin ini bekerja dengan metabolit reaktifnya yang
berikatan kovalen dengan protein dan lipid tak jenuh sehingga menyebabkan
peroksidasi lipid yang menyebabkan perlemakan hati (Lu, 1995).
4. Hepatotoksin
Obat dan senyawa yang dapat menyebabkan kerusakan hati dibedakan
menjadi dua, yaitu :
a) Teramalkan
Merupakan obat atau senyawa yang bila diberikan dapat
mempengaruhi sebagian besar orang yang menelan senyawa tersebut dalam
teramalkan bergantung kepada dosis pemberian. Contoh dari obat-obat tipe
ini adalah parasetamol, salisilat, dan tetrasiklin (Forrest, 2006).
b) Tak teramalkan
Merupakan senyawa atau obat yang sifatnya tidak toksik pada hati,
tetapi jika diberikan kepada orang tertentu dapat menimbulkan efek toksik.
Frekuensi terjadinya sangat jarang hanya 1:1000 orang. Hepatotoksin ini
tidak bergantung pada dosis pemberian. Contoh obat-obat dalam jenis ini
adalah isoniazid, halothane, dan chlorpromazine (Forrest, 2006).
5. ALT dan AST
Kerusakan hati dapat dideteksi dengan mengukur indeks fungsional dan
dengan mengamati produk hepatosit yang rusak. Uji yang sering digunakan, salah
satunya adalah uji enzim. Uji enzim ini dapat menunjukkan adanya penyakit atau
cedera pada sel hati (Sacher and McPherson, 2002).
Enzim yang sering berkaitan dengan kerusakan hepatoseluler adalah
aminotransferase. Aminotransferase mengkatalisis pemindahan reversibel satu
gugus amino antara asam amino dan sebuah asam alfa-keto, yang berfungsi dalam
pembentukan asam-asam amino yang dibutuhkan untuk penyusunan protein di
hati. Alanin aminotransferase (ALT) berfungsi memindahkan satu gugus amino
antara alanin dan asam alfa-ketoglutamat. Aspartat aminotransferase (AST)
berfungsi mengkatalisis reaksi antara asam aspartat dan asam alfa-ketoglutamat
(Sacher and McPherson, 2002). Penentuan enzim ALT dan AST adalah cara yang
sering digunakan untuk mendeteksi kerusakan hati, enzim yang dibebaskan
Enzim ALT terdapat pada beberapa jaringan tapi konsentrasinya lebih
banyak terdapat di hati, sedangkan enzim AST sebagian besar ada di otot rangka,
hati, dan tersebar ke seluruh jaringan. Berdasarkan hal tersebut, maka enzim ALT
menjadi petunjuk yang lebih spesifik terhadap rusaknya hati dari pada AST
(Zimmerman, 1999).
C. Karbon Tetraklorida
Karbon tetraklorida merupakan cairan jernih yang mudah menguap, tidak
berwarna, dan memiliki bau khas. Karbon tetraklorida memiliki rumus molekul
CCl4, BM 153,82 dan sangat sukar larut dalam air, dapat bercampur dengan etanol
mutlak dan dengan eter (Dirjen POM, 1995). Karbon tetraklorida merupakan
senyawa yang mudah larut lemak dan bisa digunakan untuk model hepatotoksin
perlemakan pada hati (Wahyuni, 2005).
Penggunaan karbon tetraklorida untuk menginduksi toksisitas dipengaruhi
oleh dosis dan durasi dari pemejanan. Dosis yang rendah dapat menyebabkan
kerusakan homeostasis dari lipid dan dapat terjadi apoptosis. Pemejanan karbon
tetraklorida dengan dosis tinggi atau pemejanan dengan durasi yang panjang dapat
menyebabkan perlemakan hati, fibrosis, sirosis hingga kanker (Weber, Boll, and
Stampfl., 2003).
Karbon tetraklorida (CCl4) akan dimetabolisme oleh sitokrom P450
menjadi senyawa radikal bebas CCl3* (triklorometil). Radikal bebas ini dapat
mengikat molekul seluler seperti asam nukleat, protein dan lipid. Pengaruh adanya
metabolisme lipid. Bila radikal bebas triklorometil berikatan dengan DNA, maka
dapat menyebabkan kanker hati (Weber, Boll, and Stampfl., 2003).
Menurut Weber, Boll, and Stampfl (2003), sekresi dari VLDL dari
hepatosit mengalami penurunan yang besar karena adanya induksi dari CCl4.
Badan Golgi dari hati menjadi sasaran CCl4 sehingga menyebabkan kehilangan
fungsi. Badan Golgi memiliki peran untuk mengatur sintesis, maturasi, dan
sekresi dari VLDL.
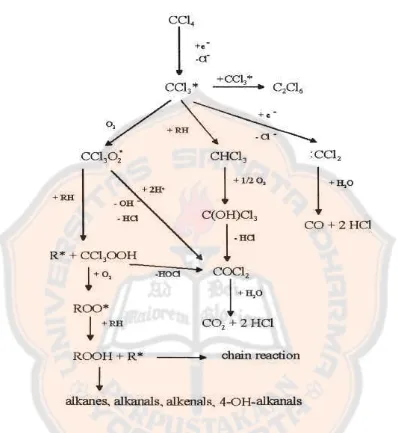
Metabolisme dari CCl4 (Gambar 5), setelah terbentuk radikal bebas
triklorometil (CCl3*) akan terbentuk triklorometil peroksi radikal (CCl3OO*)
karena bereaksi dengan oksigen. Radikal bebas ini lebih reaktif dari pada radikal
bebas triklorometil (CCl3*). Radikal bebas triklorometil peroksi radikal akan
mengikat asam lemak tak jenuh yang menginisiasi proses peroksidasi lipid.
Peroksidasi lipid yang terjadi dapat membentuk radikal lipid. (Weber, Boll, and
Gambar 5. Metabolisme karbon tetraklorida dengan adanya oksigen dan molekul organik. RH menggambarkan asam lemak tak jenuh. (Weber, Boll,
dan Stampfl., 2003).
D. Infusa
Infusa didefinisikan sebagai sediaan cair yang dibuat dengan
mengekstraksi simplisia nabati direbus air pada suhu 90°C selama 15 menit
(Badan Pengawas Obat dan Makanan, 2010). Infusa dapat dibuat dengan cara
mencampur simplisia dengan derajat halus yang sesuai dalam panci dengan air
sejak mencapai suhu 90°C yang disertai dengan pengadukan. Penyaringan
dilakukan menggunakan kain flanel yang disertai dengan menambahkan air panas
secukupnya melalui ampas hingga diperoleh volume infus yang dikehendaki
(Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
E. Landasan Teori
Hati merupakan organ yang penting bagi tubuh karena perannya untuk
metabolisme dan detoksifikasi subtansi berbahaya yang masuk ke dalam tubuh.
Hati dapat rusak karena berbagai hal seperti induksi bahan kimia, virus ataupun
penggunaan obat-obatan yang dapat merusak hati. Salah satu kerusakan hati yang
prevalensinya cukup tinggi di Indonesia adalah perlemakan hati (steatosis), yaitu
mencapai 30%. Perlemakan hati yang tidak diatasi dapat berkembang menjadi
kanker hati.
Senyawa karbon tetraklorida (CCl4) merupakan senyawa yang sering
digunakan untuk permodelan dalam kerusakan hati. Karbon tetraklorida yang
dimetabolisme oleh sitokrom P450 akan diubah menjadi senyawa radikal bebas
CCl3* (triklorometil). Senyawa radikal bebas trikolorometil ini akan berikatan
dengan molekul seluler seperti asam nukleat, lipid, dan protein yang dapat
menyebabkan perlemakan hati.
Menurut penelitian dari Kviecinski et al. (2011), melaporkan bahwa salah
satu kandungan dari tanaman Bidens pilosa L adalah flavonoid. Flavonoid adalah
antioksidan yang memiliki aktivitas menangkap radikal bebas yang berpotensi
metabolit flavonoid (Silva et al., 2011). Senyawa flavonoid ini terlarut dalam
pelarut polar, sehingga diharapkan infusa herba Bidens pilosa L. dapat
memberikan efek hepatoprotektif pada tikus betina terinduksi karbon tetraklorida.
F. Hipotesis
Pemberian jangka panjang infusa herba Bidens pilosa L. mempunyai efek
hepatoprotektif dengan menurunkan aktivitas ALT dan AST serum pada tikus
BAB III
METODELOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan
rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional 1. Variabel utama
a. Variabel bebas
Variabel bebas penelitian ini adalah variasi dosis dalam pemberian
jangka panjang infusa herba Bidens pilosa L.
b. Variabel tergantung
Variabel tergantung penelitian ini adalah penurunan aktivitas ALT
-AST serum akibat pemberian jangka panjang infusa herba Bidens pilosa L.
pada tikus betina galur Wistar terinduksi karbon tetraklorida.
2. Variabel pengacau
a. Variabel pengacau terkendali
Variabel pengacau terkendali penelitian ini adalah kondisi hewan uji,
yaitu tikus betina galur Wistar dengan berat badan 130-200 g dan umur 2-3
bulan, frekuensi pemberian infusa herba Bidens pilosa L. satu kali sehari
rute pemberian secara per oral (p.o). Herba Bidens pilosa L. diperoleh dari
Sleman, Daerah Istimewa Yogyakarta.
b. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi
patologis dan fisiologis tikus betina galur Wistar yang digunakan sebagai
hewan uji.
3. Definisi operasional
a. Herba Bidens pilosa L.
Herba Bidens pilosa L. adalah semua bagian tumbuhan di atas tanah
(batang, daun, bunga, dan biji) Bidens pilosa L.
b. Infusa herba Bidens pilosa L.
Infusa serbuk kering herba Bidens pilosa L. 16% didapatkan dengan
cara menginfudasi 8,0 g serbuk kering herba Bidens pilosa L. dalam 50,0 ml
air pada suhu 90°C selama 15 menit.
c. Dosis efektif
Dosis yang memberikan efek hepatoprotektif paling besar dengan
penurunan aktivitas ALT dan AST serum yang berbeda bermakna jika
dibandingkan dengan variasi dosis lainnya.
d. Efek hepatoprotektif
Efek hepatoprotekif adalah kemampuan infusa herba Bidens pilosa L.
pada dosis tertentu untuk melindungi hepar dari hepatotoksin dengan
menurunkan aktivitas ALT dan AST serum yang secara statistik berbeda
e. Jangka panjang
Jangka panjang adalah pemberian infusa herba Bidens pilosa L. satu
kali sehari selama enam hari berturut-turut.
C. Bahan Penelitian
1. Bahan utama
a. Hewan uji yang digunakan adalah tikus betina galur Wistar dengan umur
2-3 bulan dengan berat badan 130-200 g yang diperoleh dari
Laboratorium Hayati Imono Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
b. Bahan uji yang digunakan adalah herba Bidens pilosa L. yang diperoleh
dari Dusun Jenengan, Desa Maguwoharjo, Kecamatan Depok, Sleman,
Daerah Istimewa Yogyakarta.
2. Bahan kimia
a. Bahan hepatotoksin yang digunakan adalah karbon tetraklorida
(Merck®) .
b. Kontrol negatif yang digunakan adalah olive oil yang diperoleh dari PT.
Brataco.
c. Pelarut untuk infusa digunakan aquadest yang diperoleh dari
Laboratorium Farmakognosi-Fitokimia Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
e. Blanko pengukuran aktivitas ALT-AST serum menggunakan aqua
bidestilata yang diperoleh dari Laboratorium Kimia Analisis dan
Instrumental Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
f. Reagen serum ALT-AST dari DiaSys®.
D. Alat penelitian 1. Alat pembuatan serbuk kering herba Bidens pilosa L.
Alat-alat yang digunakan antara lain oven, mesin penyerbuk, dan ayakan.
2. Alat pembuatan infusa herba Bidens pilosa L.
Panci lapis alumunium, stopwatch, thermometer, beaker glass, gelas ukur,
labu takar, corong, cawan porselen, batang pengaduk, penangas air, timbangan
analitik, dan kain flanel.
3. Alat uji penetapan kadar air
Moisture balance, beaker glass, dansendok.
4. Alat uji hepatoprotektif
Seperangkat alat gelas berupa beaker glass, gelas ukur, tabung reaksi, labu
ukur, pipet tetes, batang pengaduk (Pyrex Iwaki Glass®), timbangan analitik
Mettler Toledo®, sentrifuge Centurion Scientific®, vortex Genie Wilten®, spuit
injeksi p.o. dan i.p., pipa kapiler, tabung Eppendorf, Microlab 200 Merck®,
E. Tata Cara Penelitian 1. Determinasi tanaman Herba Bidens pilosa L
Determinasi dilakukan dengan mencocokkan ciri-ciri tanaman herba Bidens
pilosa L. dengan buku acuan karangan Backer tahun 1963. Determinasi dilakukan
oleh Bapak Yohanes Dwiatmaka, M.Si., dosen Jurusan Farmasi, Fakultas Farmasi,
Universitas Sanata Dharma Yogyakarta.
2. Pengumpulan bahan uji
Bahan uji yang digunakan adalah herba Bidens pilosa L. yang meliputi
semua bagian tumbuhan di atas tanah (batang, daun, bunga, dan biji), dipilih yang
masih bagus dan terhindar dari penyakit. Bahan uji diperoleh dari Dusun Jenengan,
Sleman, DIY pada bulan Juli 2014.
3. Pembuatan serbuk herba Bidens pilosa L.
Herba Bidens pilosa L. dicuci bersih, dipotong-potong, dan
dikering-anginkan. Setelah itu, untuk mengoptimalkan pengeringan dilakukan pengeringan
dengan menggunakan oven pada suhu 500C selama 24 jam. Setelah benar-benar kering, herba diserbuk dan diayak dengan ayakan nomor 40.
4. Penetapan kadar air pada serbuk herba Bidens pilosa L.
Serbuk kering herba Bidens pilosa L. yang sudah diayak dimasukkan ke
dalam alat moisture balance sebanyak 5 g kemudian diratakan. Bobot serbuk
kering herba tersebut ditetapkan sebagai bobot sebelum pemanasan (bobot A),
pemanasan (bobot B). Kemudian dilakukan perhitungan terhadap selisih bobot A
terhadap bobot B yang merupakan kadar air serbuk herba Bidens pilosa L.
5. Pembuatan infusa herba Bidens pilosa L.
Untuk membuat infusa herba Bidens pilosa L. dengan konsentrasi 16%,
serbuk kering herba Bidens pilosa L. diambil sejumlah 8,0 g, dibasahkan dengan
16,0 mL aquades kemudian ditambah dengan 50 mL aquadest. Campuran ini
kemudian dipanaskan di atas heater pada suhu 90°C selama 15 menit, dihitung
ketika suhu pada campuran mencapai 90°C. Jika air yang diperoleh kurang, maka
air dapat ditambahkan selagi panas melalui ampas rebusan hingga volume
mencapai 50,0 mL.
6. Pembuatan larutan karbon tetraklorida konsentrasi 50%
Larutan karbon tetraklorida dibuat dalam konsentrasi 50% dengan
mencampur larutan karbon tetraklorida dan olive oil dengan perbandingan volume
1:1.
7. Uji pendahuluan
a. Penetapan dosis infusa herba Bidens pilosa L.
Pada penelitian ini digunakan 3 peringkat dosis yaitu rendah (dosis I),
tengah (dosis II), dan tinggi (dosis III). Dosis III ditetapkan dengan cara
sebagai berikut :
D x BB = C x V
Keterangan :
D = Dosis III
C = Konsentrasi tertinggi infusa herba Bidens pilosa L. yang bisa dibuat
V = ½ Vmax
D x 200g = 16 % x 0,25 mL
D x 0,2 kg = 0,16 g/mL x 2,5 mL
D = 2,0 g/kgBB
Peringkat dosis dibuat dengan faktor kelipatan dua sehingga didapat dosis I
sebesar 0,5 g/kgBB ; dosis II sebesar 1,0 g/kgBB dan dosis III sebesar
2,0g/kgBB.
b. Penetapan dosis hepatotoksik karbon tetraklorida
Berdasarkan penelitian yang dilakukan oleh Priya, Swati, dan Vilasrao
(2013), bila karbon tetraklorida dengan dosis 2,0 mL/kg diberikan secara
intraperitonial pada tikus betina, maka dapat menyebabkan kerusakan organ
hati yang ditandai dengan peningkatan serum ALT-AST tanpa menyebabkan
kematian. Sehingga pada penelitian ini digunakan dosis 2,0 mL/kgBB.
c. Penetapan waktu pencuplikan darah
Penetapan waktu pencuplikan darah ditentukan melalui orientasi
dengan 5 ekor tikus. Setiap ekor tikus diambil darahnya melalui sinus
orbitalis mata menggunakan pipa kapiler pada jam ke-0, 24, dan 48 setelah
pemberian karbon tetraklorida. Kemudian diukur aktivitas serum ALT-AST.
8. Pengelompokkan dan perlakuan hewan uji
Sejumlah empat puluh dua ekor tikus dibagi secara acak ke dalam enam
a. Kelompok I (kontrol hepatotoksin) diberi larutan karbon tetraklorida dengan
dosis 2,0 mL/kg BB secara intraperitonial. Pengambilan darah dilakukan
setelah 24 jam.
b. Kelompok II (kontrol negatif) diberi olive oil 2,0 mL/kgBB secara
intraperitonial. Pengambilan darah dilakukan setelah 24 jam.
c. Kelompok III (kontrol infusa) diberi infusa herba Bidens pilosa L. dosis
tinggi selama enam hari berturut-turut secara p.o. Pengambilan darah
dilakukan pada hari ke tujuh.
d. Kelompok IV (dosis I) diberi infusa herba Bidens pilosa L. dosis 0,5 g/kgBB
secara p.o sekali sehari selama enam hari berturut-turut.
e. Kelompok V (dosis II) diberi infusa herba Bidens pilosa L. dosis 1,0 g/kgBB
secara p.o sekali sehari selama enam hari berturut-turut.
f. Kelompok VI (dosis III) diberi infusa herba Bidens pilosa L. dosis 2,0
g/kgBB secara p.o sekali sehari selama enam hari berturut-turut. Pada hari ke
tujuh kelompok IV, V, dan VI diberi karbon tetraklorida dengan dosis 2,0
mL/kg BB secara intraperitonial. Setelah 24 jam, diambil darahnya melalui
sinus orbitalis mata, lalu diukur aktivitas serum ALT-AST.
9. Pembuatan serum
Pembuatan serum dilakukan dengan mengambil darah tikus melalui bagian
sinus orbitalis mata, kemudian didiamkan selama 15 menit. Sentrifuge dengan
kecepatan 8000 rpm selama 15 menit setelah terpisah, bagian supernatan diambil,
10. Pengukuran aktivitas serum ALT-AST
Pengukuran aktivitas serum ALT-AST dilakukan menggunakan alat
Microlab 200 Merck di Labolatorium Fakultas Farmasi Sanata Dharma,
Yogyakarta. Pengukuran aktivitas Serum ALT dilakukan dengan cara
mencampurkan 100 mL serum dengan 1000 mL reagen I ditunggu selama 2 menit
kemudian ditambahkan 250 mL reagen II, dan ditunggu selama 1 menit sebelum
diukur menggunakan Mircrolab. Pengukuran aktivitas serum AST juga dilakukan
dengan hal yang sama, namun digunakan reagen untuk pengukuran aktivitas AST.
F. Tata Cara Analisis Hasil
Data aktivitas serum ALT-AST diuji dengan Saphiro-Wilk untuk
mengetahui distribusi data tiap kelompok hewan uji. Apabila didapat distribusi
data yang normal maka analisis dilanjutkan dengan analisis pola searah (One Way
ANOVA) dengan taraf kepercayaan 95% untuk mengetahui perbedaan
masing-masing kelompok. Kemudian dilanjutkan dengan uji Scheffe untuk melihat
perbedaan masing-masing antar kelompok bermakna (signifikan) (p<0,05) atau
tidak bermakna (tidak signifikan) (p>0,05). Namun, bila didapatkan distribusi
tidak normal, maka dilakukan analisis dengan uji Kruskal Wallis untuk
mengetahui perbedaan aktivitas serum ALT-AST antar kelompok. Setelah itu,
dilanjutkkan dengan uji Mann Whitney untuk mengetahui perbedaan tiap
Perhitungan persen efek hepatoprotektif terhadap hepatotoksin karbon
tetraklorida diperoleh dengan rumus:
1− (purata ALT perlakuan−purata ALT kontrol negatif)
(purata ALT kontrol hepatoksin−purata ALT kontrol negatif) × 100%
1− (purata AST perlakuan−purata AST kontrol negatif)
BAB IV
HASIL DAN PEMBAHASAN
Tujuan dari penelitian ini adalah untuk mengetahui efek anti
hepatoprotektif dari infusa herba Bidens pilosa L. terhadap tikus putih betina
terinduksi karbon tetraklorida (CCl4) berdasarkan aktivitas enzim ALT dan AST
dalam darah.
A. Hasil Determinasi Tanaman
Pada penelitian hepatoprotektif ini digunakan herba Bidens pilosa L.
sebagai bahan yang akan diuji aktivitasnya. Determinasi bertujuan untuk
memastikan bahan yang digunakan adalah herba Bidens pilosa L.,sehingga tidak
terjadi kesalahan dalam penyiapan bahan. Determinasi dilakukan oleh bapak
Yohanes Dwiatmaka, M.Si. di Laboratorium Farmakognosi-Fitokimia Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta dengan menggunakan buku
acuan karangan Backer(1963). Bagian tanaman yang dideterminasi adalah batang,
daun, bunga, dan biji. Proses determinasi dilakukan hingga tingkat spesies. Hasil
determinasi membuktikan bahwa bahan yang digunakan benar dari tanaman
Bidens pilosa L.
B. Penyiapan Bahan 1. Pembuatan serbuk herba Bidens pilosa L.
Herba Bidens pilosa L.dibuat serbuk agar memperbesar luas kontak herba
dengan pelarut, sehingga senyawa fitokimia yang terdapat pada herba Bidens
2. Penetapan kadar air serbuk herba Bidens pilosa L.
Tujuan dari penetapan kadar air adalah untuk mengetahui kandungan air
dalam serbuk herba Bidens pilosa L. Penetapan kadar air dilakukan dengan
metode Gravimetri dengan menggunakan alat moisture balance. Serbuk
dipanaskan dalam alat pada suhu 1050C selama 15 menit. Hasil perhitungan menunjukkan bahwa kadar air serbuk herba Bidens pilosa L.. adalah 8,61%.
Kadar air serbuk herba Bidens pilosa L. sudah baik karena persyaratan serbuk
simplisia yang baik menurut Farmakope IV adalah kurang dari 10%.
C. Uji Pendahuluan 1. Penentuan dosis hepatotoksin karbon tetraklorida
Pada penelitian ini, karbon tetraklorida digunakan sebagai hepatotoksin.
Tujuan dari penentuan dosis hepatotoksin karbon tetraklorida adalah mengetahui
pada dosis berapa karbon tetraklorida dapat menyebabkan kerusakan hati pada
tikus yang dilihat dari peningkatan aktivitas serum ALT dan AST. Menurut Thapa
and Walia (2007), karbon tetraklorida dapat menginduksi kerusakan hati yang
ditandai dengan kenaikan 3-4x serum ALT dan AST dari normal. Pada penelitian
ini digunakan dosis karbon tetraklorida 2,0 ml/kgBB, karena menurut penelitian
Janakat and Merie (2002), pada dosis tersebut karbon tetraklorida dapat
menginduksi terjadinya hepatotoksik. Dengan dosis 2,0 mL/kgBB, aktivitas serum
ALT-AST dapat meningkat yang menunjukkan adanya kerusakan hati tanpa
menimbulkan kematian. Pemberian secara i.p. bertujuan untuk menghindari
2. Penentuan dosis infusa
Penentuan dosis infusa herba Bidens pilosa L. dengan tujuan mengetahui
dosis infusa herba Bidens pilosa L. yang akan digunakan dalam penelitian ini.
Dosis infusa herba Bidens pilosa L. ditetapkan dengan cara pembuatan infusa
dengan konsentrasi maksimal dan didasarkan volume maksimal yang dapat
diberikan ke tikus secara per oral. Dari hasil uji pendahuluhan, konsentrasi
maksimal yang dapat dibuat adalah 16 %. Volume maksimal yang diberikan
adalah secara p.o. adalah 5.0 mL. Pada penelitian ini digunakan ½ dari volume
yang dapat diberikan, yaitu 2,5 mL. Dari hasil perhitungan, didapatkan dosis
infusa herba Bidens pilosa L. adalah 2,0 g/kgBB, dan dibuat tiga peringkat dosis
yaitu 2,0; 1,0; dan 0,5 g/kgBB.
3. Penentuan waktu pencuplikan darah
Tujuan dari penentuan waktu pencuplikan darah ini adalah untuk
mendapatkan waktu efek hepatotoksik yang maksimal dari karbon tetraklorida
(CCl4) dilihat dari peningkatan aktivitas serum ALT dan AST. Karbon
tetraklorida dosis 2,0 mL/kgBB diinduksikan pada tikus, kemudian dilakukan
pencuplikan darah dengan selang waktu 0, 24, dan 48 jam.
Hasil pengujian aktivitas sertum ALT dapat dilihat pada tabel I
Tabel I. Purata aktivitas serum ALT ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mL/kgBB
Selang waktu (jam) Purata aktivitas serum ALT ± SE (U/L)
0 51,2 ± 3,7
24 153,0 ± 2,1
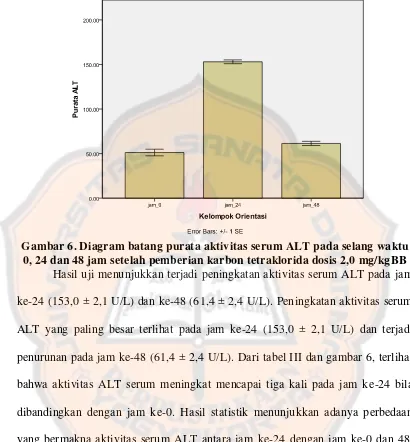
Gambar 6. Diagram batang purata aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mg/kgBB
Hasil uji menunjukkan terjadi peningkatan aktivitas serum ALT pada jam
ke-24 (153,0 ± 2,1 U/L) dan ke-48 (61,4 ± 2,4 U/L). Peningkatan aktivitas serum
ALT yang paling besar terlihat pada jam ke-24 (153,0 ± 2,1 U/L) dan terjadi
penurunan pada jam ke-48 (61,4 ± 2,4 U/L). Dari tabel III dan gambar 6, terlihat
bahwa aktivitas ALT serum meningkat mencapai tiga kali pada jam ke-24 bila
dibandingkan dengan jam ke-0. Hasil statistik menunjukkan adanya perbedaan
yang bermakna aktivitas serum ALT antara jam ke-24 dengan jam ke-0 dan 48.
Pada jam ke-0 dan 48 memiliki perbedaan namun tidak bermakna, yang artinya
aktivitas serum ALT pada jam ke-48 sudah kembali normal seperti pada jam ke-0.
Tabel II. Hasil uji Scheffe aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mL/kgBB
Selang waktu (jam) Jam ke-0 Jam ke-24 Jam ke-48
0 BB BTB
24 BB BB
48 BTB BB
Keterangan:
BB = Berbeda bermakna (p<0,05), BTB = Berbeda tidak bermakna (p>0,05)
Serum AST juga diukur pada jam yang sama hasil dapat dilihat pada tabel III.
Tabel III. Purata aktivitas serum AST ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mL/kgBB
Selang waktu (jam) Purata aktivitas serum AST ± SE (U/L)
0 109,0 ± 4,6
24 425,6 ± 10,4
48 150,6 ± 7,0
Gambar 7. Diagram batang purata aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mg/kgBB
Dari hasil pengukuran diatas, aktivitas serum AST paling tinggi terjadi
penurunan menjadi (150,6 ± 7,0 U/L). Hal tersebut juga terjadi pada serum ALT,
dimana aktivitasnya paling tinggi pada jam ke-24. Secara statistik uji
kebermakanaan, aktivitas serum AST memiliki antara nilai yang berbeda
bermakna setiap waktu pencuplikan.
Tabel IV. Hasil uji Scheffe aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2,0 mL/kgBB
Selang waktu (jam) Jam ke-0 Jam ke-24 Jam ke-48
0 BB BB
24 BB BB
48 BB BB
Keterangan:
BB = Berbeda bermakna (p<0,05)
Dari hasil uji pendahuluan ini, CCl4 memiliki efek hepatotoksik paling
tinggi pada jam ke-24, sehingga pada penelitian ini pencuplikan darah dilakukan
24 jam setelah dipejankan CCl4 dengan dosis 2,0 mL/kgBB.
D. Hasil Uji Efek hepatoprotektif infusa herba Bidens pilosa L.
Pada penelitian ini, digunakan tiga peringkat dosis infusa herba Bidens
pilosa L. untuk diuji efek hepatoprotektifnya, yaitu 0,5 g/kgBB; 1,0 g/kgBB, dan
2,0 g/kgBB yang diberikan sekali sehari selama enam hari berturut-turut.
Parameter yang digunakan dalam melihat efek hepatoprotektif adalah ada
tidaknya penurunan aktivitas serum ALT dan didukung data dari aktivitas serum
AST. Data tersebut disajikan dalam bentuk purata ± SE dengan satuan U/L (tabel
V).
Data dianalisis menggunakan analisis pola searah. Dari hasil uji,
didapatkan bahwa hasil aktivitas serum ALT-AST memiliki distribusi normal dan
untuk melihat kebermaknaan dari peningkatan aktivitas serum ALT-AST yang
dapat dilihat pada tabel VI dan VII.
Tabel V. Purata ± SE aktivitas serum ALT dan AST tikus betina galur Wistar pada kelompok perlakuan
Kelompok Purata aktivitas serum ALT ± SE (U/L)
I : Kelompok kontrol hepatotoksin karbon tetraklorida 2,0 mL/kgBB II : Kelompok kontrol negatif olive oil 2,0 mL/kgBB
III : Kelompok kontrol IHBP 2 g/kgBB
IV : Kelompok IHBP 0,5 g/kgBB + karbon tetraklorida 2 mL/kgBB V : Kelompok IHBP 1 g/kgBB + karbon tetraklorida 2 mL/kgBB VI : Kelompok IHBP 2 g/kgBB + karbon tetraklorida 2 mL/kgBB IHBP : Infusa Herba Bidens pilosa L.
Tabel VI. Hasil uji Scheffe aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan
IHBP = Infusa herba Bidens pilosa L.
Gambar 8. Diagram batang purata aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan
Tabel VII. Hasil uji Scheffe aktivitas serum AST tikus betina galur Wistar
IHBP = Infusa herba Bidens pilosa L.
BB = Berbeda bermakna (p<0,05), BTB = Berbeda tidak bermakna (p>0,05)
1. Kontrol negatif olive oil
Tujuan dari pengujian kelompok ini adalah untuk mengetahui pengaruh
pelarut hepatotoksin terhadap peningkatan aktivitas serum ALT-AST, diharapkan
pelarut olive oil tidak mempengaruhi aktivitas serum ALT-AST. Pada kontrol
negatif ini digunakan dosis sesuai dengan hepatotoksin, yaitu 2,0 mL/kgBB. Dari
hasil percobaan, didapatkan purata aktivitas serum AST dan serum ALT adalah
101,8 ±3,8 U/Ldan 57,2 ± 3,1 U/L. Uji statistik dilakukan untuk mengetahui
pengaruh olive oil terhadap peningkatan aktivitas serum ALT-AST dengan cara
Tabel VIII. Purata ± SE aktivitas serum ALT dan AST setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0 dan 24 jam
Selang waktu (jam)
Purata aktivitas serum ALT ± SE (U/L)
Purata aktivitas serum AST ± SE (U/L)
0 55,2 ± 2,1 105,2 ± 1,4
24 57,2 ± 3,1 101,8 ±3,8
Tabel IX. Hasil uji t-test aktivitas serum ALT dan AST pemberian olive oil dosis 2,0 mL/kgBB pada selang waktu 0 dan 24 jam
Selang waktu (jam) Aktivitas serum ALT Aktivitas serum AST Jam ke-0 Jam ke-24 Jam ke-0 Jam ke-24
Jam ke-0 BTB BTB
Jam ke-24 BTB BTB
Keterangan:
BTB = Berbeda tidak bermakna (p>0,05)
Gambar 11. Diagram batang purata aktivitas serum AST setelah pemberian olive oil dosis 2,0 mL/kgBB pada selang waktu 0 dan 24 jam
Dari tabel dan gambar, terlihat bahwa aktivitas serum serum ALT-AST
pada jam ke-0 dan jam ke-24 ada sedikit perubahan, namun memiliki perbedaan
yang tidak bermakna secara statistik. Dari hasil tersebut, dapat disimpulkan bahwa
olive oil tidak berpengaruh pada aktivitas serum serum ALT-AST dan tidak
menimbulkan kerusakan pada hati. Nilai aktivitas serum serum ALT-AST
kelompok ini yang akan digunakan sebagai acuan nilai normal aktivitas serum
serum ALT-AST pada penelitian selanjutnya.
2. Kontrol hepatotoksin karbon tetraklorida dosis 2,0 mL/kgBB
Hepatoksin yang digunakan dalam penelitian ini adalah karbon
tetraklorida, karena menurut beberapa penelitian, karbon tetraklorida dapat
menyebabkan kerusakan hati terutama perlemakan hati (steatosis). Tujuan
melihat pengaruh hepatotoksin terhadap kerusakan hati pada tikus betina. Selain
itu, juga digunakan untuk melihat efek hepatoprotektif dengan cara dibandingkan
kelompok perlakuan infusa herba Bidens pilosa L.
Dari tabel, nilai purata aktivitas serum ALT yang didapat adalah 174,4 ±
2,9 U/L. Data tersebut dibandingkan dengan nilai normal yang didapat dari
kontrol negatif olive oil, yaitu 57,2 ± 3,1 dan diuji statistik yang menunjukkan
adanya perbedaan yang bermakna.
Menurut Zimmerman (1999), peningkatan aktivitas serum ALT sejumlah
3x dari normal menunjukkan terjadinya perlemakan hati. Peningkatan yang terjadi
pada kontrol hepatoksin ini mencapai 3x, sehingga pada kontrol hepaktoksin
karbon tetraklorida dosis 2,0 mL/kgBB dapat menyebabkan perlemakan hati.
Aktivitas serum AST juga dilihat pada tabel, nilainya adalah 409,6 ± 7,8
U/L, sedangkan pada kontrol negatif olive oil nilainya adalah 101,8±3,8 U/L.
Pada aktivitas serum AST, juga terlihat adanya peningkatan setelah diberikan
hepatoksin pada tikus betina. Peningkatan yang terjadi mencapai 4x lipat yang
menurut Zimmerman (1999), merupakan tanda dari terjadinya perlemakan hati.
Hasil uji Scheffe di tabel menunjukkan adanya peningkatan yang
bermakna antara aktivitas serum ALT-AST kontrol negatif olive oil dengan
kontrol hepatoksin karbon tetraklorida. Hal tersebut menunjukkan bahwa
hepatoksin dapat menyebabkan kerusakan hati, khususnya perlemakan hati dan
nantinya data kontrol hepatoksin ini akan digunakan untuk menghitung efek
3. Kontrol infusa herba Bidens pilosa L. dosis 2,0 g/kgBB
Tujuan dari dilakukan kontrol infusa herba Bidens pilosa L.untuk melihat
pemberian infusa herba Bidens pilosa L. tidak memberi pengaruh terhadap
aktivitas serum ALT-AST. Dosis yang digunakan adalah dosis tertinggi, yaitu
sebesar 2,0 g/kgBB. Uji dilakukan dengan cara memberikan infusa herba Bidens
pilosa L. dengan dosis 2,0 g/kgBB secara p.o. pada tikus selama 6 hari
berturut-turut. Kemudian, pada hari ke-7 diukur aktivitas serum ALT-AST. Tabel
menunjukkan bahwa kelompok kontrol infusa herba Bidens pilosa L. memiliki
nilai aktivitas serum ALT 55,8 ± 2,06 U/L, yang bila dibandingkan dengan
kelompok kontrol negatif olive oil memiliki perbedaan yang tidak bermakna.
Aktivitas serum AST kontrol infusa herba Bidens pilosa L.adalah sebesar
102,2 ± 4,14 U/L, bila dibandingkan dengan nilai kontrol negatif olive oil (101,8
± 3,8) memiliki perbedaan yang tidak bermakna. Hasil statistik menunjukan
bahwa infusa herba Bidens pilosa L. yang diberikan selama 6 hari berturut-turut
tidak mempengaruhi aktivitas serum ALT-AST normal.
4. Kelompok perlakuan infusa dosis 0,5; 1,0; dan 1,0 g/kgBB pada tikus betina galur Wistar terinduksi karbon tetraklorida dosis 2,0 mL/kgBB
Evaluasi terhadap efek hepatoprotektif infusa herba Bidens pilosa L. pada
tikus betina terinduksi karbon tetraklorida dilihat dari ada tidaknya penurunan
aktivitas serum ALT-AST, karena adanya praperlakuan pemberian infusa herba