Gambar 1. Ikan Cakalang Segar
Gambar 2. Ikan Cakalang Loin Masak
Gambar 3. Uji Kualitatif Kalsium
Gambar 4. Uji Kualitatif Besi
Gambar 5. Uji Kualitatif Magnesium
Lampiran 4. Gambar Alat Spektrofotometer Serapan Atom dan Alat Tanur
KristalKalsiu m Sulfat
Endapan merah terang ikan cakalangsegar
Endapan merah terang cakalang loin masak Larutan merah
pada cakalang loin masak Larutan merah
Gambar 6.Atomic Absorption Spectrophotometer Hitachi Z-2000
Lampiran 5. Bagan Alir Proses Destruksi Kering (Ikan Cakalang Segar)
Dihaluskan dengan blender
Dibelah kedua sisi ikan dari ekor hingga ke bagian atas ikan, lalu diambil daging putih ikan tanpa mengikutkan daging yang berwarna gelap
Dilakukan selama 48 jam dan dibiarkan hingga dingin dalam tanur hingga suhu ± 27oC
Dibuang bagian kepala, sirip, isi perut, duri, kulit dan ekor ikan dan dicuci bersih dengan akua demineralisata
Hasil Ikan Cakalang Segar
Diarangkan di atas hot plate suhu 100
o
Cselama ± 8 jam
Ditambahkan 5 ml HNO3 (1:1)
Dilanjutkan destruksi Sampel yang dihaluskan
Ditimbang sampel kemudian dicuci bersih
Ditimbang ± 25 g
Dimasukkan ke dalam krus porselen
Lampiran 6. Bagan Alir Proses Destruksi Kering (Cakalang Loin Masak)
Ikan Cakalang Loin Masak
Diarangkan di atas hot plate suhu 100 oCselama ± 8 jam
Hasil
Sampel yang telah Dihaluskan
Ditimbang 1000 gram dari 5000 gram ikan yang ada didalam kemasan
Ditimbang ± 25 g
Dimasukkan ke dalam krus porselen
Ditambahkan 5 ml HNO3 (1:1)
Dihaluskan dengan blender
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dilakukan selama 48 jam dan dibiarkan hingga dingin di dalam tanur hingga suhu ± 27oC
Lampiran 7. Bagan Alir Pembuatan Larutan Sampel
Dilarutkan dalam 5 ml HNO3 (1:1)
Dibilas krus porselen sebanyak tiga kali dengan akua demineralisata dimasukkan dalam labu tentukur, lalu dicukupkan dengan akua demineralisata hingga garistanda.
Dimasukkan ke dalam botol
Larutan Sampel
Disaring dengan kertas saring Whatman No. 42
Filtrat
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan Atom pada
λ 422,7 nm untuk kalsium, λ 248,3 nm
untuk kadar besi dan pada λ 285,2 nm untuk magnesium dengan nyala udara-asetilen
Dipindahkan ke dalam labu tentukur 50 ml
Untuk mineral Ca dan Fe, Dipipet 2,5 ml dimasukan dalam labu tentukur 25 mldicukupkan dengan akua demineralisata hingga garis tanda (pengenceran 10 ) dan 5 ml dalam labu tentukur 25 ml (pengenceran) untuk mineral Mg dicukupkan dengan akua demineralisata
Hasil
Lampiran 8. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No. Konsentrasi (X)
Lampiran 8. (Lanjutan)
r = ∑XY − [ (∑X )(∑Y )
n ]
��∑X2– (∑X)² / n � (∑Y2− (∑Y)² / n )
r = 1,0454 – �
(15 � 0,284 ) 6 � ��55 −(15)2
6 ��0,01987492 − (0,284 )2
6 �
r = 1,0454 – 0,71 �(17,5)(0,006432254 )
r = 0,3354 √0,112564
r = 0,3354
0,3355
Lampiran 9. Data Kalibrasi Besidengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No. Konsentrasi (X)
Lampiran 9. (Lanjutan)
r = ∑XY − [ (∑X )(∑Y )
n ]
��∑X2– (∑X)² / n � (∑Y2− (∑Y)² / n )
r = 1,037 – �
(30 � 0,1414 ) 6 � ��220−(30 )2
6 ��0,00488944− (0,1414 )2
6 �
r = 1,037 – 0,707 �(70)(0,01557 )
r = 0,33 √0,10899
r = 0,33
0,33013
Lampiran 10. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
Lampiran 10. (Lanjutan)
r = ∑XY − [ (∑X )(∑Y )
n ]
��∑X2– (∑X)² / n � (∑Y2− (∑Y)² / n )
r = 22,9724 – �
(30 � 3,525 ) 6 � ��220 −( 30)2
6 ��2,39953943 − (3,1525 )2
6 �
r = 22,9724 – 15,7624 �(70)(0,743163388 )
r = 7,2099 √52,021437186
r = 7,2099
7,2125
Lampiran 10. Hasil analisis kadar kalsium, besi dan magnesium dalam ikan cakalang segar
1. Kalsium
Sampel Berat Sampel (g)
Sampel Berat Sampel (g)
Lampiran 12. Contoh Perhitungan Kadar Kalsium, Besi dan Magnesium pada Daging Ikan Cakalang Segar
1. Contoh Perhitungan Kadar Kalsium Berat sampel yang ditimbang = 25,1072 g Absorbansi (Y) = 0,0684
Persamaan regresi: Y = 0,0191657 X – 0,0005809524
X = Y + 0,0005809524 0,0191657
X = 0,10684 + 0,0005809524 0,0191657
X = 3,5991 µg/ml Konsentrasi kalsium = 3,5991 µg/ml
Kadar kalsium (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 3,5991 µg/ml x 50 ml x 10 25,1072 g
= 71,676 µg/g
= 0,071676 mg/g= 7,1676 mg/100 g 2. Contoh Perhitungan Kadar Besi
Berat sampel yang ditimbang = 25,1072g Absorbansi (Y) = 0,0155
Persamaan regresi: Y = 0,0047143 X – 0,0000047619
X = Y + 0,00000476 0,0047143
X = 0,0155 + 0,00000476 0,0047143
Lampiran 12.(Lanjutan)
Kadar besi (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 3,2888 µg/ml x 50 ml x 10 25,1072 g
= 65,496µg/g = 0,065496 mg/g = 6,5496 mg/100 g 3. Contoh Perhitungan Kadar Magnesium
Berat sampel yang ditimbang = 25,1072 g Absorbansi (Y) = 0,3167
Persamaan regresi: Y = 0,1029986 X+ 0,01042381
X = Y – 0,01042381 0,1029986
X = 0,3167– 0,01042381 0,1029986
X =2,9735µg/ml Konsentrasi magnesium = 2,9735µg/ml
Kadar magnesium (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 2,9735 µg/ml x 50 ml x 5 25,1072 g
Lampiran 13. Contoh Perhitungan Kadar Kalsium, Besi dan Magnesium pada Cakalang Loin Masak
1. Contoh Perhitungan Kadar Kalsium Berat sampel yang ditimbang = 25,1068 g Absorbansi (Y) = 0,0565
Persamaan regresi: Y = 0,0191657 X – 0,0005809524
X = Y + 0,0005809524 0,0191657
X = 0,0565 + 0,0005809524 0,0191657
X = 2,9782 µg/ml Konsentrasi kalsium = 2,9782 µg/ml
Kadar kalsium (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 2,9782 µg/ml x 50 ml x 10 25,1068 g
= 59,312µg/g
= 0,059312 mg/g= 5,9312mg/100 g 2. Contoh Perhitungan Kadar Besi
Berat sampel yang ditimbang = 25,1072 g Absorbansi (Y) = 0,0126
Persamaan regresi: Y = 0,0047143 X – 0,0000047619
X = Y + 0,00000476 0,0047143
X = 0,0126 + 0,00000476 0,0047143
Lampiran 13.(Lanjutan)
Konsentrasi besi = 2,6737µg/ml
Kadar besi (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 2,6737 µg/ml x 50 ml x 10 25,1068 g
= 53,247µg/g = 0,053247 mg/g = 5,3247mg/100 g 3. Contoh Perhitungan Kadar Magnesium
Berat sampel yang ditimbang = 25,1068 g Absorbansi (Y) = 0,2977
Persamaan regresi: Y = 0,1029986 X + 0,01042381
X = Y – 0,01042381 0,1029986
X = 0,2977– 0,01042381 0,1029986
X =2,7891µg/ml Konsentrasi magnesium = 2,7891 µg/ml
Kadar magnesium (µg/g) = konsentrasi (µg/ml) x volume (ml) x faktor pengenceran berat sampel (g)
= 2,7891 µg/ml x 50 ml x 5 25,1068 g
Lampiran 14. Perhitungan Statistik Kadar Kalsium, Besi dan Magnesium pada Daging Ikan Cakalang Segar
1. Perhitungan Statistik Kadar Kalsium
No. Xi
Data diterima jika t hitung< t tabel.
Lampiran 14.(Lanjutan)
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan data ke-4 dan data ke-6.
Lampiran 14.(Lanjutan)
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar kalsium dalam ikan cakalang segar: µ = Xi ± (t(α/2, dk) x SD /√n)
= 7,1566±(3,1824x 0,01267/√4) = (7,1566 ± 0,0201) mg/100 g 2. Perhitungan Statistik Kadar Besi
Lampiran 14.(Lanjutan)
Data diterima jika t hitung< t tabel.
t hitung =
Lampiran 14.(Lanjutan)
Data diterima jika t hitung< t tabel.
t hitung =
Xi = 6,5067
Data diterima jika t hitung< t tabel.
t hitung =
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar besi dalam ikan cakalang segar: µ = Xi ± (t(α/2, dk) x SD /√n)
Lampiran 14.(Lanjutan)
3. Perhitungan Statistik Kadar Magnesium
No. Xi
Kadar (mg/100 g) (Xi - Xi) (Xi - Xi)
2
1. 2,96090 0,00376 0,000014110
2. 2,95699 -0,00015 0,0000000225
3. 2,95878 0,0016 0,00000256
4. 2,95679 -0,00035 0,0000001225
5. 2,95623 -0,00091 0,000000830
= √0,00000667096
= 0,00258
Pada interval kepercayaan 95% dengan nilai α = 0,05, dk = 5 diperoleh nilai t tabel = α /2, dk = 2,5706
Data diterima jika t hitung< t tabel.
Lampiran 14.(Lanjutan)
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan data ke-1 dan ke-6.
No. Xi
Kadar (mg/100 g) (Xi - Xi) (Xi - Xi)
2
2. 2,95690 -0,00021 0,000000044
3. 2,958699 0,00158 0,000002504
4. 2,95679 0,00041 0,000000168
= √0,000001214533
= 0,0011
Pada interval kepercayaan 95% dengan nilai α = 0,05, dk = 3 diperoleh nilai t tabel = α /2, dk = 3,1824
Data diterima jika t hitung< t tabel.
t hitung =
t hitung2 =
|−0,00021 |
0,0011 /√4 = 0,3818
Lampiran 14.(Lanjutan)
t hitung3 =
|0,00158 |
0,0011 /√4 = 2,8728
t hitung4=
|0,00041 |
0,0011 /√4 = 0,7454
t hitung5 =
|−0,00097 |
0,0595/√4 = 1,7636
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar magnesium dalam cakalang segar: µ = Xi ± (t(α/2, dk) x SD /√n)
Lampiran 15. Perhitungan StatistikKadar Kalsium, Besi dan Magnesium Pada Cakalang Loin Masak
1. Perhitungan Statistik Kadar Kalsium
No. Xi
Data diterima jika t hitung< t tabel.
Lampiran 15.(Lanjutan)
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan data ke-2 dan data ke-5.
t hitung =
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar kalsium dalam ikan cakalangloin masak: µ = Xi ± (t(α/2, dk) x SD /√n)
= 5,9510±(3,1824x 0,0166/√4) = (5,9510± 0,0264) mg/100 g 2. Perhitungan Statistik Kadar Besi
= �0,041732336 − 1
Data diterima jika t hitung< t tabel.
t hitung =
data ke-4 dan ke-5.
Pada interval kepercayaan 95% dengan nilai α = 0,05, dk =3 diperoleh nilai t tabel = α /2, dk = 3,1824
Data diterima jika t hitung< t tabel.
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar besi dalam ikan cakalang loin masak: µ = Xi ± (t(α/2, dk) x SD /√n)
= 5,2608 ±(3,1824x 0,05522/√4) = (5,2608 ± 0,0878) mg/100 g
Lampiran 15.(Lanjutan)
3. Perhitungan Statistik Kadar Magnesium
No. Xi
Kadar (mg/100 g) (Xi - Xi) (Xi - Xi)
2
1. 2,77726 0,000001 0,0000000001
2. 2,77816 0,00089 0,0000007921
3. 2,77518 -0,00209 0,0000043681
4. 2,77837 0,0011 0,00000121
5. 2,77635 -0,00092 0,0000008646
6. 2,77829 0,00101 0,0000010404
∑Xi =
t hitung =
= √0,0000007625
= 0,000873
Pada interval kepercayaan 95% dengan nilai α = 0,05, dk = 4 diperoleh nilai t tabel = α /2, dk = 2,7765
Data diterima jika t hitung< t tabel.
t hitung =
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan data ke-5.
No. Xi
Kadar (mg/100 g) (Xi - Xi) (Xi - Xi)
2
1. 2,77726 -0,00076 0,0000005776
2. 2,77816 -0,00014 0,0000000196
4. 2,77837 0,00035 0,0000001225
6. 2,77829 0,00027 0,0000000729
= �0,00000079264− 1
= �0,00000079263
= √0,0000002642
= 0,000514
Pada interval kepercayaan 95% dengan nilai α = 0,05, dk = 3 diperoleh nilai t tabel = α /2, dk = 3,1284
Lampiran 15.(Lanjutan) Data diterima jika t hitung< t tabel.
t hitung =
|Xi−Xi | SD /√n
t hitung 1 =
|−0,00076 |
0,000514 /√4 = 1,101
t hitung 2 =
|−0,00014 |
0,000514 /√4 = 0,5447
t hitung 4 =
|0,00035 |
0,000514 /√4 = 1,3618
t hitung6 =
|0,00027 |
0,000514 /√4 = 1,0505
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar magnesium dalam cakalang loin masak: µ = Xi ± (t(α/2, dk) x SD /√n)
Lampiran 16. Hasil Analisis Kadar Kalsium, Besi dan Magnesium Sebelum dan Sesudah Penambahan Masing-Masing Larutan Baku Pada Cakalang Loin Masak
1. Hasil Analisis Kadar Kalsium (Ca) Sebelum Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
Rata-rata 25,1111 5,9510
2. Hasil Analisis Kadar Kalsium (Ca) Setelah Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
3. Hasil Analisis Kadar Besi (Fe) Sebelum Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
Lampiran 16.(Lanjutan)
4.Hasil Analisis Kadar Besi (Fe) Setelah Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
Rata-rata 25,1088 9,2348
5.Hasil Analisis Kadar Magnesium (Mg) Sebelum Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
150,6666 16,6636
Rata-rata 25,1111 2,7772
6. Hasil Analisis Kadar Magnesium (Mg) Setelah Ditambahkan Larutan Baku Sampel Berat Sampel
(g)
Lampiran 17. Perhitungan Uji Perolehan Kembali Kadar Kalsium, Besi dan Magnesium dalam Cakalang Loin Masak
1. Perhitungan Uji Perolehan Kembali Kadar Kalsium Sampel 1
Persamaan regresi: Y = 0,0191657 X −0,0005809524 X = 0,0751− 0,0005809524
0,00191657 = 3,948768 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,9487 µg/ml CF =
Konsentrasi (µg/ml )
Berat Sampel (g) x Volume (ml) x Faktor Pengenceran
= 3,9487 µg/ml
25,1086 g x 50 ml x 10
= 78,634 µg/g = 0,078634 mg/g = 7,8634 mg/100 g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 7,8634mg/100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,9312+5,9207+5,9517+5,9710+5,9812+5,9500)mg/100 g 6
=5,9510mg/100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat Sampel rata−rata (g) x Volume (ml)
= 1000 µg/mL
25,1088 g x 0,5 ml
Lampiran 17.(Lanjutan)
Persamaan regresi: Y = 0,0191657 X −0,0005809524 X = 0,0754 + 0,0005809524
0,00191657 = 3,9644 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,9644 µg/ml CF =
Kadar sampel 2 setelah ditambah larutan baku (CF) = 7,8944mg/100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,9312+5,9207+5,9517+5,9710+5,9812+5,9500)mg/100 g 6
=5,9510mg/ 100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
Lampiran 17.(Lanjutan)
Persamaan regresi: Y = 0,0191657 X −0,0005809524 X = 0,0748 + 0,0005809524
0,00191657 = 3,93311 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 3,93311 µg/ml CF =
Kadar sampel 3 setelah ditambah larutan baku (CF) = 7,8322 mg/100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,93123 +5,92070 +5,95170 +5,97103 +5,98121 +5,95007 )mg/100 g 6
= 5,9510mg/ 100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
Lampiran 17.(Lanjutan)
Rata–rata % perolehan kembali kalsium= (96,03%+ 97,6%+94,48%)
3 = 96,03%
2. Perhitungan Uji Perolehan Kembali Kadar Besi Sampel 1
Persamaan regresi: Y = 0,0047143 X −0,0000047619 X = 0,0220 +0,0000047619
0,0000047143 = 4,667676 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,6676 µg/ml CF =
Kadar sampel 1 setelah ditambah larutan baku (CF) = 9,2949 mg/100 g
Lampiran 17.(Lanjutan)
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,3247 +5,2824 +5,2400 +5,1542 +5,4074 +5,1963)mg/100 g 6
= 5,2675 mg/100 g
Berat sampel rata-rata uji recovery = 25,1088g
C*A =
Persamaan regresi: Y = 0,0047143 X −0,0000047619 X = 0,0223 +0,0000047619
0,0000047143 = 4,731313 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,731313µg/ml CF =
Konsentrasi (µg/ml )
Berat Sampel (g) x Volume (ml) x Faktor Pengenceran
= 4,731313 µg/ml
25,1091g x 50 ml x 10= 94,215 µg/g = 9,4215 mg/100 g
Kadar sampel 2 setelah ditambah larutan baku (CF) = 9,4215 mg/100g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,3247 +5,2824 +5,2400 +5,1542 +5,4074 +5,1963)mg/100 g 6
= 5,2675 mg/ 100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Berat Sampel rata−rata (g) x Volume (ml)
= 1000 µg/mL
Lampiran 17.(Lanjutan)
Persamaan regresi: Y = 0,0047143 X −0,0000047619 X = 0,0217 +0,0000047619
0,0000047143 = 4,6040 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,6040 µg/ml CF =
Kadar sampel 3 setelah ditambah larutan baku (CF) = 9,16821 mg/ 100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(5,3247 +5,2824 +5,2400 +5,1542 +5,4074 +5,1963)mg/100 g
6 = 5,2675 mg/100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Lampiran 17.(Lanjutan)
= 1000 µg/mL
25,1088 g x 1 ml
= 39,826 µg /g = 0,039826 mg/g = 3,9826 mg/100 g Maka % perolehan kembali besi = CF − CA
C∗A x 100%
= 9,1682 mg/100 g−5,2675 mg/100 g
3,9826 mg/100 g x 100%
= 97,95%
Rata–rata % perolehan kembali besi = (101,12%+ 104,30%+97,95%)
3 =101,12 %
3. Perhitungan Uji Perolehan Kembali Kadar Magnesium Sampel 1
Persamaan regresi: Y = 0,01029986 X+ 0,01042381 X = 0,5048−0,01042381
0,01029986 = 4,7998 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,79986 µg/ml
CF =
Konsentrasi (µg/ml )
Berat Sampel (g) x Volume (ml) x Faktor Pengenceran
= 4,7998 µg/ml
25,1086 g x 50 ml x 5
= 47,790 µg /g
= 0,047790 mg/g = 4,7790 mg/100 g
Kadar sampel 1 setelah ditambah larutan baku (CF) = 4,7790 mg/ 100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
Lampiran 17.(Lanjutan)
CA =
(2,7772 +2,7781 +2,7751 +2,7783 +2,7763 +2,7782 )mg/100 g 6
= 2,7772/100 g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Persamaan regresi: Y = 0,01029986 X+ 0,01042381 X = 0,5039−0,01042381
0,01029986 =4,7910 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,7910 µg/ml CF =
Kadar sampel 2 setelah ditambah larutan baku (CF) = 4,7702mg/ 100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(2,7772 +2,7781 +2,7751 +2,7783 +2,7763 +2,7782 )mg/100 g
Lampiran 17.(Lanjutan)
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Persamaan regresi: Y = 0,01029986 X+ 0,01042381 X = 0,5054−0,01042381
0,01029986 = 4,80566 µg/ml
Konsentrasi setelah ditambahkan larutan baku = 4,80566 µg/ml CF =
Kadar sampel 3 setelah ditambah larutan baku (CF) = 4,7848 mg/ 100 g
Kadar rata-rata sampel sebelum ditambahkan larutan baku (CA) adalah kadar
rata-rata dari keenam sampel: CA =
(2,7772 +2,7781 +2,7751 +2,7783 +2,7763 +2,7782 )mg/100 g
6 =2,7772/100g
Berat sampel rata-rata uji recovery = 25,1088g
Kadar larutan standar yang ditambahkan (C*A) adalah:
C*A =
Konsentrasi baku yang ditambahkan (µg/ml )
Lampiran 17.(Lanjutan)
= 1000 µg/mL
25,1088 g x 0,5ml = 19,913 µg/g = 1,9913 mg/100 g
Maka % perolehan kembali magnesium = CF − CA
C∗A x 100%
= 4,7848 mg/100 g− 2,7772 mg/100 g
1,9913 mg/100 g x 100%
= 100,81 % Rata–rata % perolehan kembali magnesium adalah
= (100,52%+ 100,08%+100,81%)
Lampiran 18. Perhitungan Simpangan Baku Relatif (RSD) pada Sampel Ikan Cakalang
1. Kalsium
No. (%) Perolehan Kembali
(Xi) (Xi - Xi) (Xi - Xi)
No. (%) Perolehan Kembali
Lampiran 18.(Lanjutan) Lampiran 18.(Lanjutan)
= �10,08065= 3,1750 RSD = SD
Xi x 100%
= 3,1750
101,12 x 100%= 3,14 %
3. Magnesium
No. (%) Perolehan Kembali
(Xi) (Xi - Xi) (Xi - Xi)
2
1.
100,52 -0,05 0,0025
2.
100,08 0,392 0,153664
3.
100,81 -0,342 0,11964
∑Xi = 301,41 ∑(Xi - Xi)2
= 0,273128 Xi = 100,47
SD = �∑(Xi n −− Xi )2 1
= �0,273128
3−1
= �0,136564 = 0,3695 RSD = SD
Xi x 100%
= 0,3695
Lampiran 19. Perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ) 1. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalsium
Y = 0,0191657 X −0,0005809524 Slope = 0,0191657
No.
0,0005809524 0,00028095
0,0000000789 2.
1,0000 0,0173
0,018584747 -0,0012847
0,0000016506 3.
2,0000 0,0390
0,037750447 0,0012495
0,0000015613 4.
3,0000 0,0566
0,056916147 -0,0003161
0,0000000999 5. 4,0000 0,0767 0,076081847 0,0006180 0,00000038204 6. 5,0000 0,0947 0,0952476 -0,0005476 0,00000029988
Lampiran 19.(Lanjutan)
2. Perhitungan Batas Deteksi dan Batas Kuantitasi Besi Y = 0,0047143 X - 0,00000476157
0,0000 -0,0003 0,0000047615 7
-0,00029523
8 0,00000007165 2. 2,0000 0,0102 0,00942381 0,00077619 0,0000006024 3. 4,0000 0,0185 0,018852382 -0,0035238 0,00000012417 4.
6,0000 0,0283
0,028280954 0,00001904
0,00000000036 2 5. 8,0000 0,0371 0,037709526 0,0006095 0,000000371 6. 10,0000 0,0476 0,04713809 0,00046191 0,0000002133
Lampiran 19.(Lanjutan)
3. Perhitungan Batas Deteksi dan Batas Kuantitasi Logam Magnesium Y = 0,1029986 X + 0,001042381
0,010523810 0,000110751 2.
2,0000 0,2184
0,21642095
-0,001979048 0,000003917 3.
4,0000 0,4262
0,42241810
-0,003781905 0,000014303 4. 6,0000 0,6431 0,62841524 0,014684762 0,000215642 5. 8,0000 0,8384 0,83441238 0,003987619 0,000015901 6.
10,0000 1,0265
1,0404952
-0,013909524 0,000193475
= �0,000553988
4
= √0,000138497
= 0,01176
Batas deteksi = 3 x �
SY X
� �
slope
= 3 x 0,01176
0,1029986
= 0,3425 µg/ml Batas kuantitasi = 10 x �
SY X
� �
slope
= 10 x 0,1176
0,1029986
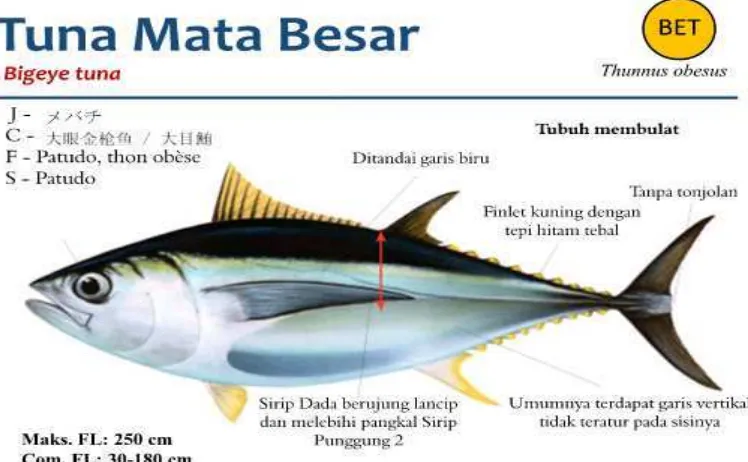
Lampiran 21.Jenis – JenisTuna Berdasarkan berdasarkan Indian Ocean Tuna Commission (IOTC) pada tahun2013
Keterangan gambar :
Maks. FL : panjang maksimum fork lenght
Com. FL : panjang fork leght umumdi Samudera Hindia J-nama bahasa Jepang
C- nama bahasa Cina F- nama bahasa Perancis S- nama bahasa Spanyol
Gambar 8. TunaAlbakora
Lampiran 21.(Lanjutan)
Gambar 10. Tuna Mata Besar
Lampiran 21.(Lanjutan)
Gambar 12. Cakalang
Lampiran 21.(Lanjutan)
Gambar 14. Tongkol Krai
Gambar 15. Tongkol Komo
DAFTAR PUSTAKA
Achionye-Nzeh, Adedoyin., Oyebanji., and Mohammed. (2011). Mineral Composition of Some Marine and Fresh Water Fishes. Agriculture And Biology Journal of North America. Vol:2(7): 1114.
Adawyah, R. (2008). Pengolahan dan Pengawetan Ikan. Jakarta: PT Bumi Aksara. Halaman 1, 12.
Apridar. (2014). Daya Saing Ekspor Ikan Tuna Indonesia. Yogyakarta: Graha Ilmu. Halaman 7.
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal228, 235, 241 –242, 249, 253.
Barasi, M.E. (2007). Nutrition at a Glance. Penerjemah: Halim, H. (2009). At a Glance Ilmu Gizi. Jakarta: Erlangga. Hal. 54,55.
Budiyanto, H. A.K. (2009). Dasar-dasar Ilmu Gizi. Malang: UMM Press. Halaman 84, 86.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 650.
Ditjen POM RI. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman 1127, 1135, 1172, 1183.
Ditjen PEN RI. (2012). Ikan Tuna Indonesia.Warta EksporEdisi Juni.Jakarta: Kementerian Perdagangan RI. Halaman 6, 11.
Drummond, K. E dan Brefere, L. M(2007). Nutrition for Food Service and Culinary Professionals. Sixth Edition. New Jersey: John Wily & Sons, Inc. Pages:257 - 258, 269.
Ermer, J., dan McB. Miller, J.H. (2005). Method Validation in Pharmaceutical Analysis.Weinheim: Wiley-VchVerlag GmbH & Co. KGaA. Pages. 171.
H Kordi K, M.G.(2011). Buku Pintar Budi Daya 32 Ikan Laut Ekonomis. Yogyakarta:ANDI. Halaman 323-324, 328.
H Kordi K, M.G.(2015). Pengelolaan Perikanan Indonesia. Yogyakarta: Pustaka Baru Press. Halaman 123-125.
Harmita. (2004). PetunjukPelaksanaan Validasi Metode dan Cara Perhitungannya.Review Artikel. Majalah Ilmu Kefarmasian. Vol. 1 (3): 117-119, 121-122, 130-131.
Harris, D. C. (2007). Quantitative Chemical Analysis. Sevent Edition. USA: W. H Freeman and Company. Halaman 455.
IOTC. (2013).Identification of Tuna and Tuna-Like Species in Indian Ocean Fisheries Draft. Indian Ocean Tuna Commission.IOTC-2013 SC16- INF10. Pages:1-14, 28.
Irianto, H. E dan Arkabarsyah, T. M. I. (2009).Pengalengan Tuna Komersial. Jakarta: Balai Besar Riset Pengolahan Produk dan Bioteknologi Kelautan dan Perikanan. Jurnal.Vol. 2 (2): 45.
Isaac, R.A. (1990). Plants. Dalam: Herlich, K. (1990).Official Methods of Analysis of the Association of Official Analytical Chemists. Edisi kelima belas. Arlington: AOAC International Pages 42.
Kartasapoetra, G. dan Marsetyo, H. (1995). Ilmu Gizi (Korelasi Gizi, Kesehatan Dan Produktivitas Kerja). Cetakan Kedua. Jakarta: Rineka Cipta. Halaman 97.
Karunarathna, K, A. A. Uand Attygalle,M. V. E. (2009). Mineral Spectrum in Different Body Parts of Five Species of Tuna Consumed in Sri Lanka. Vidyodaya Journal of Science Srilanka. Vol:14(II): 103-111.
Karunarathna, K, A.A. Udan Attygalle, M.V.E. (2010). Nutritional evaluation in five species of tuna. Vidyodaya Journal of Science Srilanka. Vol:15 (I ): 7-16.
Khopkar, S. M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptoraharjo, A., dan Nurhadi, A. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Halaman 275.
Kristianingrum, S. (2012). Kajian Berbagai Proses Destruksi Sampel dan Efeknya. Prosiding Seminar Nasional Penelitian. Pendidikan dan Penerapan MIPA, Fakultas MIPA. Universitas Negeri Yogyakarta. Halaman 197.
Kuncoro, E. B dan Wiharto, F. E. A. (2009). Ensiklopedi Populer Ikan Air Laut. Yogyakarta: ANDI. Halaman 100.
Rohman,A. (2007). Kimia Famasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 298, 319-321.
Sizer, F. S dan Whitney, E. (2006). Nutrition Concepts and Controversies. Tenth Edition. USA: Thomson Wadsworth. Pages: 275, 277.
SNI. (2014).SNI 2014 : 7968. Tuna Loin Masak Beku. Jakarta: Badan Standarisasi Nasional. Halaman 2, 10.
Sudjana. (2005). MetodeStatistika.EdisiKeenam. Bandung: Tarsito. Halaman 93. Sundari, D., Almasyhuri dan Lamid, A. (2015).Pengaruh Proses Pemasakan
terhadap Komposisi Zat Gizi Bahan Pangan Sumber Protein.Jurnal Media Litbangkes.Vol. 25 (1): 235–242.
Svehla, G. (1979). Vogel Textbook of Macro and Semimicro Qualitative Inorganic Analysis. Bagian I. Diterjemah: Setiono, L. dan Pudjaatmaka, A.H. (1985). Analisis Anorganik Kualitatif Makro dan Semimikro. Jakarta: Penerbit Kalman Media Pustaka.
Yuniastuti, A (2008).Gizi dan Kesehatan. Yogyakarta: Graha Ilmu. Halaman 62.
BAB III
METODE PENELITIAN
Metode yang digunakanadalah metode deskriptif yang bertujuan untuk menggambarkan sifat dari suatu keadaan secara sistematis yaitu untuk memeriksa mineral kalsium, besi dan magnesium pada ikan cakalang kemasan dan segar.
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi dan Laboratorium Kimia Farmasi Kualitatif Universitas Sumatera Utara pada bulan Maret 2016 – Mei 2016.
3.2 Alat-alat
Alat yang digunakan pada penelitian ini adalah Spektrofotometer SerapanAtom dengan nyala udara-asetilen lengkap dengan lampu katoda Ca, Fe, dan Mg, hot plate (BOECO Germany), cawan porselin, neraca analitik (BOECO Germany),tanur (Nabertherm), blender, kertas saring Whatman No.42, dan alat – alat gelas (Pyrex dan Oberol).
3.3 Bahan-Bahan 3.3.1 Sampel
3.3.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisa keluaran E. Merck(larutan baku kalsium konsentrasi 1000 µg/ml, larutan baku besikonsentrasi 1000 µg/ml, larutan baku magnesium konsentrasi 1000 µg/ml, asam nitrat, kuning titan, NaOH, H2SO4, NH4CNS), kecuali akua demineralisata
(Laboratorium Penelitian Fakultas Farmasi USU).
3.4 Identifikasi Sampel
Identifikasi sampel Ikan Cakalang dilakukan di Laboratorium Sistematika Hewan, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
3.5 Pembuatan Pereaksi 3.5.1 Larutan HNO3 (1:1)
Asam Nitrat 65% v/vsebanyak 100 ml diencerkan dengan akuademineralisata 100 ml (Ditjen POM, 1979).
3.5.2 Larutan Kuning Titan 0,1% b/v
Larutan kuning titan 0,1% b/v dibuat dengan cara melarutkan 0,1 g kuning titan dalam 100 ml akuademineralisata (Ditjen POM RI, 1995).
3.5.3 Larutan NaOH 2 N
Sebanyak 80,02 gramNaOH dilarutkan dengan akuademineralisata hingga 1000 ml (Ditjen POM RI, 1995).
3.5.4 Larutan H2SO4 1 N
Sebanyak 3 ml larutan H2SO4 96% v/v diencerkan dengan
3.5.5 Larutan NH4CNS 0,1 N
Dilarutkan 8 g ammonium tiosianat dalam akuademineralisata hingga 1000 ml (Ditjen POM RI, 1995).
3.6 Prosedur Penelitian 3.6.1 Pengambilan Sampel
Sampel yang digunakan adalahikan cakalang segar hasil tangkapan di Samudera Indonesiabagian barat pulau Sumatera seperti Nias,perairan utara Nanggroe Aceh Darussalam yang berada di sebelah ujung barat Pulau Sumatera yang ada di PT. Anugerah Samudera Hindia kabupaten Tapanuli Tengahdan ikancakalang loin masak produksi perusahaan tersebut.Metode pengambilan sampel dilakukan dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan, dimana sampel ditentukan atas dasar pertimbangan bahwa semua sampel mempunyai karakteristik yang sama dengan yang diteliti (Sudjana, 2005).
3.6.2 Penyiapan Sampel
dalamkrus porselin yang telah diberi kode sampel. Perlakuan penimbangan dan penetapan kadar besi, kalsium dan magnesium, dilakukan sebanyak 6 kali pada masing-masing sampel.
3.6.3 Proses Destruksi
Sampel yang telah dihaluskan ditimbangsebanyak 25 g dalam krus porselen, diarangkan di atas hot platetemperatur 100°C selama ± 8 jam kemudian ditambahkan 5 ml HNO3 (1:1) dandilanjutkan proses destruksi.Pengabuan
dilakukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit. Pengabuan dilakukan selama ± 48 jam (dihitung saat suhu sudah 500°C) hingga arang menjadi berwarna abu-abu hingga putih.Krusporselen dibiarkan hingga dingin di dalam tanur (suhu ± 27ºC). Krus porselen dikeluarkan dan disimpan dalam desikator.
3.6.4 Pembuatan Larutan Sampel
Sampel hasil destruksi dilarutkan dengan 5 ml HNO3 (1:1), lalu
3.7 Pemeriksaan Kualitatif
3.7.1 Pemeriksaan Kualitatif Kalsium dengan Asam Sulfat 1 N
Larutan zat diteteskan 1-2 tetes pada object glassditambahkan kemudian ditetesi dengan larutan asam sulfat dan etanol 96% akan terbentuk endapan putih lalu diamati di bawah mikroskop. Jika terdapat kalsium akan terlihat kristal berbentuk jarum (Svehla, 1979).
3.7.2 Pemeriksaan Kualitatif Besi dengan larutan NH4CNS 0,1 N
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel hasil destruksi, tambahkan 3 tetes ammonium tiosianat 0,1 N. Terbentuk larutan berwarna merah (Svehla, 1979).
3.7.3 Pemeriksaan Kualitatif Magnesium dengan Larutan Kuning Titan 0,1% b/v
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambah 5-6tetes NaOH 2 N dan 3 tetes pereaksi kuning titan. Dihasilkan endapan merah terang (Svehla, 1979).
3.8 Pemeriksaan Kuantitatif
3.8.1 Pembuatan Kurva Kalibrasi Kalsium, Besi dan Magnesium 3.8.1.1 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 μg/ml) dipipet 2,5 ml, dimasukkan kedalam labu tentukur 50 ml, dicukupkan dengan akua demineralisata hingga garis tanda (Konsentrasi 50 μg/ml) (LIB II).
3.8.1.2 Pembuatan Kurva Kalibrasi Besi
Larutan baku besi (1000 μg/ml) dipipet 2,5 ml, dimasukkan kedalam labu tentukur50 ml,dicukupkan dengan akua demineralisata hingga garis tanda (Konsentrasi 50 μg/ml) (LIB II).
Dipipet 1; 2; 3; 4; dan 5 ml dari LIB II dimasukkan kedalam labu tentukur 50 ml (konsentrasi 2, 4, 6, 8, 10μg/ml) dicukupkan dengan akua demineralisata hingga garis tanda. Diukur pada panjang gelombang 248,3 nm dengan nyala udara asetilen.
3.8.1.3 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku magnesium (1000 μg/ml) dipipet sebanyak 2,5 ml, dimasukkan ke dalam labutentukur 50 ml dan dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi 50μg/ml) (LIB II).
Larutan untuk kurva kalibrasi magnesium dibuat dengan memipet 1, 2, 3, 4, dan 5 ml dari LIB II, dimasukkan kedalam labu tentukur 50 ml (konsentrasi 2; 4; 6; 8; 10 μg/ml) dicukupkan dengan akua demineralisata hingga garis tanda.Diukur pada panjang gelombang 285,2 nm dengan nyala udara asetilen. 3.8.2 Penetapan Kadar Kalsium, Besi dan Magnesium dalam Ikan Cakalang
Segar dan Cakalang Loin Masak
harus berada didalam rentang nilai kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium, besi dan magnesium dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
Kadar kalsium, besi, magnesium dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar (µg/g) =C × V × Fp W
Keterangan: C = Konsentrasi logam dalam larutan sampel (µg/mL) V = Volume larutan sampel (mL)
Fp = Faktor pengenceran W = Berat sampel (g)
3.9 Analisis Statistik
Menurut (Sudjana, 2005) kadar kalsium, besi dan magnesium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar deviasi menggunakan rumus sebagai berikut:
SD =
�
∑(Xi − Xi )2n − 1
Keterangan: Xi = Kadar sampel (mg/100g)
Xi = Kadar rata-rata sampel (mg/100g) n = Jumlah pengulangan
Untuk mencari t hitung digunakan rumus:
t hitung =
dan untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 95%, α = 0,005, dk = n-1, dapat digunakan rumus:
Kadar mineral: µ = Xi ± (t(α/2, dk) x SD /√n)
Keterangan: Xi = Kadar rata-rata sampel (mg/100g) SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = Interval kepercayaan n = Jumlah pengulangan
3.10 Validasi Metode
3.10.1 Uji Perolehan Kembali (recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu (Ermer, 2005).
Sampel (ikan cakalang) yang telah dihaluskan ditimbang sebanyak 25 gram didalam krus porselen, lalu ditambahkan 2,5 ml larutan standar kalsium (konsentrasi 1000 µg/ml), 2,5 ml larutan standar besi(konsentrasi 1000 µg/ml), dan 5 ml larutan standar magnesium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya pada prosedur dekstruksi sampel dan pengukuran masing-masing logam pada panjang gelombang 422,7 nm, 248,3 nmdan285,2nm.
Persen Perolehan Kembali = ��−��
��∗ �100%
Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku
CF = Kadar logam dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan
3.10.2 Uji Keseksamaan (Presisi)
Uji keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relative adalah:
��� =���̅ �100%
Keterangan:
�̅ : Kadar rata-rata sampel SD : Standard Deviation
RSD :Relative Standard Deviation
3.10.3 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit Of Quantitation)
Batas deteksimerupakanjumlahterkecilanalitdalamsampel yang dapatdideteksi yang masihmemberikanresponsignifikan.Sebaliknya,
bataskuantitasmerupakankuantitasterkecilanalitdalamsampel yang masihdapatmemenuhi kriteriacermatdanseksama.
Menurut Harmita (2004), danRohman (2007)
Simpangan Baku =�∑(Y−Yi )2
n−2
Batas Deteksi (LOD) = 3��
�����
Batas Kuantitasi (LOQ)= 10��
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya mineral kalsium, besi dan magnesium dalam sampel. Gambar analisis dapat dilihat pada Lampiran 3, Halaman 42.
Tabel 4.1 Hasil Analisis Kualitatif Kalsium, Besi dan Magnesium dalam Sampel
No Ion yang dianalisis
Pereaksi
Hasil Reaksi Sampel Keterangan 1
Kalsium Asam sulfat 1N
+ etanol 96% Kristal jarum
Tabel 4.1 diatas menunjukkan bahwa hasil reaksi dari masing-masing ion membuktikan bahwa larutan sampel mengandung kalsium, besi dan magnesium. Sampel dinyatakan positif mengandung mineral kalsium karena terdapat kristal jarum setelah penambahan H2SO4 1 N dan etanol 96% yang diamati dibawah
jikadengan pereaksi kuning titan 0,1% dan natrium hidroksida 2 N menghasilkan endapan berwarna merah terang.
Hasil pengukuran dengan spektrofotometer serapan atom menunjukkan adanya absorbansi kalsium pada panjang gelombang yaitu 422,7, besi 248,3 nm dan magnesium 285,2 nm sesuai dengan literatur (Khopkar, 1985). Hal ini juga membuktikan bahwa sampel mengandung mineral kalsium, besi dan magnesium 4.2 Analisis Kuantitatif
4.2.1 Kurva Kalibrasi Kalsium, Besi dan Magnesium
Kurva kalibrasi larutan baku kalsium, besi dan magnesiumdapat dilihat pada Gambar 4.1, Gambar4.2 dan Gambar 4.3.
Absorbansi Y = 0,0191657 X – 0,0005809524
Konsentrasi (µg/ml)
Gambar 4.1 Kurva Kalibrasi Larutan Baku Kalsium Absorbansi Y= 0,0047143 X – 0,0000047619
Konsentrasi (µg/ml)
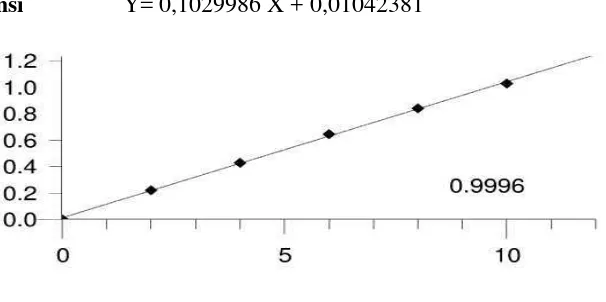
Absorbansi Y= 0,1029986 X + 0,01042381
Konsentrasi (µg/ml)
Gambar 4.3 Kurva Kalibrasi Larutan Baku Magnesium
Kurva kalibrasi kalsium, besi dan magnesium diperoleh dengan cara mengukur absorbansi dari larutan baku kalsium, besi dan magnesium pada panjang gelombang masing-masing. Dari pengukuran kurva kalibrasi untuk ketiga mineral tersebut diperoleh persamaan garis regresi yaituY = 0,0191657 X – 0,0005809524 pada kalsium, Y= 0,0047143 X – 0,0000047619 pada besi dan Y= 0,1029986 X + 0,01042381 pada magnesium.
Keterangan:
X = Konsentrasi (µg/ml) Y = Absorbansi
4.2.2 Analisis Kadar Kalsium, Besi dan Magnesium pada Daging Ikan Cakalang Segar dan Cakalang Loin Masak
Penentuan kadar kalsium, besi dan magnesium dilakukan secaraSpektrofotometriSerapan Atom dimana sampel terlebih dahulu didestruksi. Proses destruksi dalam preparasi sampel digunakan untuk memutuskan ikatan antara senyawa organik dengan mineral yang dianalisis sehingga mineral terbebas dari sampel. Destruksi terbagi dua yaitu destruksi basah dan destruksi kering. Dalam penelitian, digunakan destruksi kering karena matriks dari daging ikan yang berbentuk padat, pada ikan juga memiliki kandungan proksimat yang cukup tinggi seperti kadar air, protein, lemak, karbohidrat, yang dapat mengganggu pengukuran dan tidak memerlukan banyak pereaksi. Kemudian abu dilarutkan dengan asam nitrat lalu di cukupkan dengan akua demineralisata hingga garis tanda dan diukur pada Spektrofotometri Serapan Atom. Sumber nyala yang digunakan adalah Udara-Asetilen (UA) dengan suhu nyala 2200°C yang dapat mengatomisasi hampir semua elemen. Sumber nyala untuk analisis kalsium adalah asetilen-dinitrogen oksida (N2O) sebesar 3000°C akan tetapi pada
penelitian ini digunakan Udara-Asetilen. Untuk analisis Ca menggunakan nyala tersebut harus ditambahkan penyangga Sr dan La , namun Sr dan La tidak tersedia di laboratorium tempat penelitian dilakukan. Sr dan La berfungsi untuk mencegah pembentukan ikatan Ca-fosfat yang bersifat refraktoris (Rohman, 2007).
penentuan kadar magnesium adalah sebesar 5 kali. Data dan contoh perhitungan dapat dilihat pada Lampiran 11, Lampiran 12, Lampiran 13 dan Lampiran 14 Halaman 53, 54, 56, 58.
Analisis dilanjutkan dengan perhitungan statistik (perhitungan dapat dilihat pada Lampiran 14 dan Lampiran 15,( Halaman 58 sampai Halaman 77). Tabel 4.2. Hasil Analisis Kadar Kalsium, Besi dan Magnesium dalam Sampel
dengan perhitungan statistik
No. Sampel Kadar Kalsium
Kadar kalsium dan magnesium dalam daging ikan cakalang segar yang diperoleh pada penelitian ini lebih rendah yakni (7,1566 ± 0,0201) mg/100 dan (2,9572 ± 0,0017) mg/100 gdibandingkan daging ikan cakalang segar dalam penelitian Karunarathna dan Attygalle, (2009) yakni (12,79 ±3,38) mg/100 g pada kalsium, dan magnesium (70,70 ±7,63) mg/100 g. Hal ini dapat disebabkan perbedaan habitat dan tempat penangkapan dari ikan cakalang.
Kadar besi dalam ikan cakalang segar yaitu (6,5067 ± 0,0946) mg/100 g
cukup tinggi dibandingkan dalam penelitian Karunarathna dan Attygalle dengan kadar (1,52 ±0,3) mg/100 g. Hal ini dapat disebabkan juga karena perbedaan habitat dan tempat penangkapan dari ikan cakalang sehingga ikan cakalang dari sibolga sangat baik dikonsumsi untuk memenuhi asupan besi dalam tubuh.
atau spesies ikan, umur dan fase reproduksi pada ikan. Faktor eksternal berupa faktor yang ada pada lingkungan hidup ikan berupa habitat, ketersediaan pakan dan kualitas perairan tempat ikan hidup serta habitat ikan berpengaruh terhadap kandungan kimia di dalam dagingnya seperti kadar air, protein, lemak, karbohidrat, asam amino dan asam lemak.
4.3 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kalsium, besi dan magnesium setelah penambahan masing-masing larutan baku kalsium, besi dan magnesium dalam sampel dapat dilihat pada Lampiran 16,Halaman 78. Perhitungan persen recovery kalsium, besi dan magnesium dalam sampel dapat dilihat pada
Lampiran 17,Halaman 80 sampai Halaman 89. Persen recovery kalsium, besi dan magnesium dalam sampel dapat dilihat pada Tabel 4.3.
Tabel 4.3 Persen Uji Perolehan Kembali (recovery) Kadar Kalsium, Besi dan Magnesium
No. Mineral yangDianalisis Recovery (%) Syarat Rentang Persen Recovery (%)
1. Kalsium (Ca 96,03
80 – 120
2. Besi (Fe) 101,12
3. Magnesium (Mg) 100,47
uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80% – 120% (Ermer dan McB. Miller, 2005).
4.4 Uji Keseksamaan (Presisi)
Nilai simpangan baku dan simpangan baku relatif untuk kalsium, besi dan magnesium pada sampel dapat dilihat pada Tabel 4.4 sedangkan perhitungannya dapat dilihat pada Lampiran 18, Halaman 91.
Tabel 4.4 Nilai Simpangan Baku dan Simpangan Baku RelatifKalsium, Besi, dan Magnesium Dalam Sampel.
Mineral Simpangan baku (SD) Simpangan Baku Relatif (RSD)
Kalsium 1,5620 1,6244%
Besi 3,1750 3,1446%
Magnesium 0,3695 0,3678%
Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16 % dan untuk analit dengan kadarpart per billion (ppb) RSD nya adalah tidak lebih dari 32 %. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik.
4.5 Batas Deteksi (Limit of Detection) dan Batas Kuantitasi(Limit Of Quantitation)
Tabel 4.5 Batas Deteksi dan Batas Kuantitasi Kalsium, Besi dan Magnesium dalam Sampel
Sampel Mineral LOD (µg/ml) LOQ (µg/ml) Ikan
Cakalang
Kalsium 0,1579 0,5264
Besi 0,3763 1,2544
Magnesium 0,3425 1,1417
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Daging ikan cakalang segar dan cakalang loin masak mengandung kalsium (Ca), besi (Fe) dan magnesium (Mg).
b. Hasil pada penetapan kadarkalsium, besi dan magnesium yang diperoleh padadaging ikan cakalang segar dan cakalang loin masak memiliki kadar yang berbeda. Kadar kalsium, besi dan magnesium pada ikan cakalang segar yaitu sebesar (7,1566± 0,0201) mg/100 g, (6,5067±0,0946) mg/100 g dan (2,9572 ± 0,0017) mg/100 g sedangkan pada cakalang loin masakyaitu sebesar (5,9510± 0,0264) mg/100g, (5,2608 ±0,0878) mg/100 gdan (2,7780± 0,0008) mg/100 g.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Ikan Tuna
Ikan tuna merupakan primadona ekspor ikan laut konsumsi asal Indonesia. Banyak kapal komersial besar yang khusus dimaksudkan menangkap ikan tuna.Ikan tuna adalah pengembara lautan luas yang bermigrasi dalam rentang yang jauh.Salah satu ciri ikan tuna adalah kecepatan berenangnya yang mencapai 50 km/jam. Ukurannya termasuk raksasa, dapat mencapai lebih dari 1,5meter dengan berat ratusan kilo(Kuncoro dan Wiharto, 2009).
Wilayah perairan nusantara merupakan tempat berpijah atau kawin berbagai jenis ikan, termasuk ikan tuna, terutama di perairan Selat Makassar dan Laut Banda. Ikan tuna yang hidup di perairan laut Indonesia dikelompokkan menjadi dua jenis, yakni ikan tuna besar dan ikan tuna kecil. Ikan tuna besar meliputi madidihang (yellowfin tuna), albakora(albacore), tuna mata besar (big eye tuna), dan tuna sirip biru (southern bluefin tuna). Sementara itu, ikan tuna
kecil terdiri dari cakalang (skipjack tuna), tongkol (eutynnus affinis), tongkol kecil (auxis thazard)dan ikan abu-abu(thunnus tonggol). Ikan cakalang dapat dijumpai di seluruh perairan laut Indonesia, kecuali paparan Sunda bagian Selatan, Selat Malaka, Selat Karimata, dan Laut Jawa(Ditjen PEN RI, 2012).
Berdasarkan Harmonized Systempada tahun 1996 menyatakan ikan tuna yang diperdagangkan secara internasional dapat dikelompokkan menjadi jenis albacoretuna, skipjacktuna, yellowfintuna, dan big-eyetunayang mencakup tiga
bentuk produk ikan tuna, yaitu tuna segar atau daging utuh (fresh or chilledwhole), tuna beku utuh (frozen whole) dan tuna olahan (preserved)
(Apridar, 2014).
2.1.1 Sistematika Ikan Cakalang
Sistematika ikancakalang (Katsuwonus pelamis) atau skipjack tuna menurut(Matsumoto et al,1984)sebagai berikut :
Kingdom
Phylum
Class
Ordo
Family
Genus : Katsuwonus
Spesies : Katsuwonus pelamis
Nama Asing : skipack tuna(Amerika Serikat, Kanada, Afrika Selatan),striped tuna(Australia), bonite (Prancis),katsuo(Jepang)
Nama Umum : cakalang
Nama lokal : tjakalang, tjakalang-lelaki, tjakalang-perempuan, tjakalang- merah, cakalang
berat sekitar 0,5 – 11,5 kg serta panjang sekitar 30-80 cm. Ikan cakalang mempunyai ciri-ciri khusus yaitu tubuhnya mempunyai bentuk menyerupai torpedo (fusiform), bulat dan memanjang, serta mempunyai gill rakers (tapis insang) sekitar 53-63 buah. Ikan cakalang memiliki dua sirip punggung yang letaknya terpisah.Sirip punggung pertama terdapat 14-16 jari-jari keras, pada sirip punggung perut diikuti oleh 7-9 finlet. Terdapat sebuah rigi-rigi (keel) yang sangat kuat diantara dua rigi rigi yang lebih kecil pada masing-masing sisi dan sirip ekor (Matsumoto et al,1984).
Cakalang dapat mencapai panjang 100 cm dan berat 25 kg, namun ukuran umum yang tertangkap antara 40-60 cm. Cakalang terdapat di tiga samudera dunia dan hidup pada suhu 9-31 ºC, tetapi menyukai suhu air yang lebih panas 26–28 ºC. Karena itulah cakalang banyak ditemukan di sepanjang garis khatulistiwa sepanjang tahun. Meskipun demikian, cakalang juga banyak ditemukan di sepanjang pantai selatan Jepang(H Kordi K, 2015).
2.1.2 Manfaat Ikan cakalang
Ikan tuna seperti cakalang (Katsuwonus pelamis) mempunyai kandungan omega-3 lebih banyak dari ikan tawar, yaitu mencapai 28 kali.Konsumsi ikan tuna 30 g sehari dapat mereduksi resiko kematian akibat penyakit jantung hingga 50%. Sementara sebuah studi di Harvard tahun 2004, menyebutkan bahwa konsumsi ikan tuna 1-4 kali setiap minggu dapat meningkatkan omega-3 dan mencegah heart arrhytmia hingga 28%.Publikasi CancerEpidemology Biomakers and
Preventionpada tahun2004menunjukkan bahwa konsumsi ikan yang kaya akan
asam lemak seperti tuna dapat mengurangi penyakit leukimia, multiple myeloma, dan non-hodgkins lymphoma. Studi ini dilakukan pada 6800 orang kanada yang menunjukkan bahwa ikan kaya akan asam lemak seperti tuna mengurangi resiko leukimia hingga 28%, multiple myeloma 365, non-hodgkins lymphoma 29% dan mencegah kanker payudara. Hal itu karena kandungan omega-3 tuna dapat menghambat enzim proinflammatory yang disebut cyclooxygenase 2(COX 2), enzim pendukung terjadinya kanker payudara.Omega-3 juga dapat mengaktifkan reseptor di membran sel yang disebut proliferator-actived receptor (PPAR)-a yang dapat menangkap aktivitas sel penyebab kanker (H Kordi K, 2015).
radikal bebas penyebab berbagai jenis kanker.Konsumsi 100 g tuna dapat memenuhi 52,9 % kebutuhan selenium dalam tubuh (H Kordi K, 2015).
2.2 Cakalang Loin Masak (Skipjack Loin Cooked)
Cakalang loin masak merupakan produk olahan tuna yang mengalami pemasakan (cooked). Cookedtuna loin merupakan jenis olahan tuna yang mengalami proses pemasakan yang biasanya dikemas dalam plastik yang ditujukan untuk pasar ekspor (Ditjen PEN RI, 2012).
Tuna loin masak beku merupakan produk olahan tuna yang mengalami pemasakan, pembentukan loin dan pembekuan. Bahan baku yang digunakan adalah semua jenis tuna hasil penangkapan seperti cakalang dan berasal dari perairan yang tidak tercemar. Bahan baku yang akan diolah dapat berupa ikan utuh segar dan ikan utuh beku yang dicuci dengan air yang memenuh persyaratan kualitas air minum ataupun es yang telah memenuhi persyaratan (SNI, 2014).Menurut Suwanrangsi et al pada tahun 1995 pemeriksaan mutu terhadap bahan baku yang diterima harus dilakukan minimal dengan pengujian organoleptik. Setiap bahan baku yang tidak memenuhi persyaratan harus ditolak atau dapat digunakan untuk jenis pengolahan lain yang sesuai (Irianto dan Akbarsyah, 2007).
menggunakan uap panas yang suhu dan waktunya telah ditentukan. Ikan yang telah masak dikeluarkandandidinginkan. Dilanjutkan dengan proses pembersihan, pembentukan loin, penimbangan daging putih dan pengemasan (packing) dengan bahan pengemas plastik lalu diberi kode untuk setiap kemasan. Setelah itu, dilanjutkan dengan pemeriksaan serpihan logam (metal detecting), perapihan (forming), pencelupan panas (shrinking) dan pembekuan (freezing). Proses pembekuan dilakukan dalam ruangan pendingin khusus pada suhu -18 ºC sampai - 25 ºC dan disimpan dalam gudang beku (cold storage) sebelum dimuat untuk diekspor.
2.3 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan.Di samping itu, mineral berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier, 2004).
2.3.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5 – 2% dari berat badan orang dewasa (Almatsier, 2004). Sekitar 99% dari total kalsium dalam tubuh ditemukan pada tulang dan gigi. Kalsium juga berada dalam sirkulasi darah yang pada tingkat konstan dipertahankan sehingga selalu tersedia untuk digunakan.Kalsium membantu kontraksi otot termasuk otot
jantung, pengiriman impuls saraf, pembekuan darah dan sekresi hormon tertentu
(Drummond dan Brefere, 2007).
Kesehatan tulang kunci terletak pada keseimbangan kalsium tubuh.Sel-sel
membutuhkan akses berkelanjutan ke kalsium, sehingga tubuh mempertahankan
konsentrasi kalsium yang konstan dalam darah.Untuk melindungi terhadap
kehilangan tulang, asupan kalsium yang tinggi dalam kehidupan sangat direkomendasikan sejak dini.Kalsium yang disimpan sedikit di skeleton pada saat anak-anak dan remaja diduga sangat besar menyebabkan osteoporosis pada saat dewasa (Sizer dan Whitney, 2006).Kalsium diekskresikan lewat urin serta feses dan untuk mengganti kehilangan ini diperlukan kalsium melalui makanan. Kalsium tambahan diperlukan dalam keadaan tertentu seperti pada masa pertumbuhan mulai dari anak-anak hingga usia remaja, dan pada saat hamil untuk memenuhi kebutuhan janin (Budiyanto, 2004).
merupakan sumber kalsium yang baik. Serealia, kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, serta sayuran hijau merupakan sumber kalsium yang baik (Almatsier, 2004).
2.3.2 Besi
Besi merupakan mineral mikro yang paling banyak terdapat di dalam tubuh manusia dan hewan.Besi mempunyai beberapa fungsi esensial di dalam tubuh, sebagai alat angkut oksigen dari paru-paru ke jaringan tubuh, sebagai alat angkut elektron di dalam sel dan sebagai bagian terpadu berbagai reaksi enzim di dalam jaringan tubuh (Almatsier, 2004).
Kurang lebih dari 60% dari besi yang terkandung dalam tubuh ditemukan dalam hemoglobin dan 15% besi dalam tubuh disimpan di sumsum tulang.sisanya disimpan sebagai feritin di hati, sumsum tulang, dan limpa. Feritin merupakan protein yang mengandung sampai dengan 4000 atom besi. Kadar feritin dalam plasma mencerminkan cadangan besi. Status normal feritin serum > 15 µg/L, dan hemoglobin>120g/L pada wanita dan >130 g/L pada pria(Barasi, 2007).
. Kebutuhan akan zat besi untuk berbagai jenis kelamin dan golongan usia adalah sebagai berikut: untuk laki-laki dewasa 10 mg/hari, wanita yang mengalami haid 12 mg/hari dan anak-anak 8 mg – 15 mg/hari. Zat besi yang tidak mencukupi bagi pembentukan sel darah, akan mengakibatkan anemia, menurunkan kekebalan tubuh, sehingga sangat peka terhadap serangan penyakit (Budiyanto, 2004).
Marsetyo, 1991).Absorpsi besi terutama terjadi dibagian atas usus halus dengan bantuan alat khusus/ protein khusus.Ada dua jenis alat angkut/ protein khusus di dalam sel mukosa usus yang membantu penyerapan besi yaitu transferin dan feritin.Transferin merupakan protein yang disintesis didalam hati yang membawa besi ke sumsum tulang belakang dan organ tubuh lain. Kelebihan besi akan disimpan sebagai protein feritin dan hemosiderin dihati (Almatsier, 2004).
2.3.3 Magnesium
Kuranglebih dari 60% dari 20-28 mg magnesium di dalam tubuh terdapat di dalam tulang dan gigi, 26% di dalam otot dan selebihnya di dalam jaringan lunak lainnya serta cairan tubuh. Di dalam cairan sel ekstraselular magnesium berperan dalam transmisi saraf, konraksi otot dan pembekuan darah.Dalam hal ini peranan magnesium berlawan dengan kalsium.Kalsium menyebabkan ketegangan saraf sedangkan magnesium melemaskan saraf (Almatsier, 2004).
Magnesium fungsinya sangat penting bagi banyak sel, magnesium memegang peranan penting dalam proses lebih dari tiga ratus jenis enzim dalam tubuh. Magnesium dibutuhkan untuk pelepasan energi dan penggunaan energi langsung dari nutrisi, dan secara langsung berperngaruh dalam metabolisme kalium, kalsium dan vitamin D. Magnesium dan kalsium bekerja sama untuk memfungsikan otot tetapi kalsium berperan dalam kontraksi otot sedangkan magnesium merelaksasikannya. Pada gigi, magnesium mencegah kerusakan gigi dengan cara menahan kalsium dalam email gigi (Sizer dan Whitney, 2006).
diuretika juga dapat menyebabkan kekurangan magnesium.Kekurangan magnesium berat menyebabkan kurang nafsu makan, gangguan dalam pertumbuhan, mudah tersinggung, gugup, kejang, gangguan sistem saraf pusat, halusinasi, koma, dan gagal jantung (Almatsier, 2004).
2.4 Metode destruksi
Destruksi merupakan suatu perlakuan pemecahan senyawa menjadi unsur-unsurnya sehingga dapat dianalisis.Istilah destruksi ini disebut juga perombakan, yaitu dari bentuk organik logam menjadi bentuk logam-logam anorganik. Pada dasarnya ada dua jenis destruksi yang dikenal dalam ilmu kimia yaitu destruksi basah (oksida basah) dan destruksi kering (oksida kering). Kedua destruksi ini memiliki teknik pengerjaan dan lama pemanasan atau pendestruksian yang berbeda(Kristianingrum, 2012).
2.4.1 Metode Destruksi Basah
2.4.2 Metode Destruksi Kering
Destruksi kering merupakan perombakan logamorganik di dalam sampel menjadilogam-logam anorganik dengan jalan pengabuan sampel dalam muffle furnace dan memerlukan suhu pemanasan tertentu. Pada umumnya dalam
destruksi kering ini dibutuhkan suhu pemanasan antara 400-800oC, tetapi suhu ini sangat tergantung pada jenis sampel yang akan dianalisis. Untuk menentukan suhu pengabuan dengan sistem ini terlebih dahulu ditinjau jenis logam yang akan dianalisis(Kristianingrum, 2012).
2.5 Spektrofotometri Serapan Atom
2.5.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok untuk analisis logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit Pada analisis Ca dibutuhkan penambahan senyawa penyangga seperti Sr dan La untuk mencegah ikatan antara ion fosfat dan kalsium yang akan membentuk Ca-fosfat yang bersifat refraktoris (Rohman, 2007).
akanmemperoleh energi sehingga suatu atom pada keadaan dasar dapat dinaikkan tingkat energinya ke tingkat eksitasi (Khopkar, 1985).
Berdasarkan (Harris, 2007) sistem peralatan spektrofotometer serapan atom dapat dilihat padagambar berikut :
Gambar 2.1Sistem peralatan spektrofotometri serapan atom (Harris, 2007) 2.5.2 Gangguan-gangguan pada spektrofotometri serapan atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel (Rohman, 2007).
Menurut Rohman (2007), gangguan-gangguan yang terjadi pada spektrofotometri serapan atom adalah:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
3. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi di dalam nyala.
4. Gangguan oleh penyerapan non-atomik.
2.6 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Tindakan ini dilakukan untuk menjamin bahwametode analisis akurat,spesifik, reprodusibel, dan tahan akan kisaran analit yang akan dianalisis (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
2.6.1 Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai kecermatan yang tinggi, dapat dilakukan dengan berbagai cara seperti menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik, pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai prosedur. Kecermatan ditentukan dengan dua cara yaitu:
− Metodesimulasi (spiked-placebo recovery)
− Metode penambahan baku (standard additionmethod)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya.Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut.Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
2.6.2 Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Presisi merupakan ukuran keterulangan metode analisis dan biasanya dinyatakan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda signifikan secara statistik (Harmita, 2004).
2.6.3 Batas Deteksi dan Batas Kuantitasi
BAB I PENDAHULUAN
1.1 Latar Belakang
Indonesia adalah salah satu negara penting dalam produksi dan perdagangan ikan tuna dunia dan menempati posisi lima besar dalam produksi tuna dunia.Produksi tuna Indonesia diekspor ke Jepang, Amerika serikat, dan Uni Eropa Spesies tuna yakni madidihang, tuna mata besar, albakor, tuna sirip biru, cakalang dan tongkol. Cakalang merupakan salah satu dari jenis tuna yang hidup di perairan laut Indonesia(H Kordi K, 2011).
Kelebihan produk perikanan dibanding produk hewani lainnya adalah kandungan protein yang cukup tinggi, daging ikan mudah untuk dicerna dalam tubuh, daging ikan juga mengandung asam-asam lemak tidak jenuh dengan kadar kolesterol sangat rendah, selain itu daging ikan juga mengandung sejumlah mineral, seperti K, Cl, P, Mg, Ca, Fe, Mn, Zn, F, Cuserta vitamin A dan D.Ikan juga dapat digunakan sebagaibahan obat-obatan, pakan ternak, dan lainnya (Adawyah, 2008).