(KCKT) FASE TERBALIK PADA PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR
(OHT) RHEUMAKUR ®
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Katarina Kusmiyanti NIM: 078114063
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK PADA PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR
(OHT) RHEUMAKUR ®
Skripsi yang diajukan oleh: Katarina Kusmiyanti
NIM: 078114063
telah disetujui oleh
Dosen Pembimbing
iii
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK PADA PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR
(OHT) RHEUMAKUR ®
Oleh:
Katarina Kusmiyanti NIM: 078114063
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal : 1 April 2011
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
Ipang Djurarko, M.Sc., Apt.
Panitia Penguji: Tanda tangan
iv
Tugas kita bukanlah untuk berhasil.
Tugas kita adalah untuk MENCOBA, karena di
dalam mencoba itulah kita membangun kesempatan
untuk BERHASIL.
(Mario Teguh)
Kupersembahkan karyaku ini untuk
Papa tercinta M. Sukarta, Ibu tersayang Yustina Sriyatun
Mba Sela, ‘dek Titus
Sahabatku
v
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaiman layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 24 Maret 2011 Penulis
vi
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Katarina Kusmiyanti
Nomor Mahasiswa : 078114063
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
“OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK PADA PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR
(OHT) RHEUMAKUR ® “
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 1 April 2011 Yang menyatakan
vii
Puji dan syukur kepada Tuhan Yang Maha Esa, yang telah melimpahkan berkat rahmat-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Optimasi Metode Kromatografi Cair Kinerja Tinggi (KCKT) Fase Terbalik pada Penetapan Kadar Kurkumin Dalam Sediaan Kapsul Lunak Obat Herbal Terstandar (OHT) Rheumakur®” sebagai salah satu syarat memperoleh gelar
Sarjana Farmasi (S. Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis mengucapkan terima kasih kepada semua pihak yang mendorong, memotivasi dan memberikan saran hingga selesainya skripsi ini, terutama kepada: 1. Bapak Ipang Djunarko M.Sc, Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
2. Ibu Christine Patramurti, M.Si, Apt. selaku dosen pembimbing yang telah banyak meluangkan waktunya dalam membimbing penulis, memberikan masukan, kritik, solusi, dan memberikan dukungan kepada penulis selama penyusunan skripsi ini.
3. Bapak Jeffry Julianus, M.Si. selaku dosen penguji yang memberikan kritik dan saran untuk skripsi ini.
4. Bapak Yohanes Dwiatmaka, M.Si. selaku dosen penguji yang memberikan kritik dan saran untuk skripsi ini.
5. Bapak Prof. Dr. Sudibyo Martono, M.S., Apt. atas pemberian baku kurkumin yang berguna bagi penelitian.
viii
sehingga berguna dalam proses penyusunan skripsi.
8. Seluruh staff laboratorium, staff keamanan, dan kebersihan di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta terutama Mas Bimo, Pak Parlan, Mas Ottok, dan Mas Kunto, serta Pak Timbul.
9. Perpustakaan Universitas Sanata Dharma atas koleksi buku-buku serta akses internetnya sehingga penulis memperoleh bahan-bahan yang cukup lengkap dalam penulisan skripsi ini
10. Kedua orang tuaku, Bapak Markus Sukarta dan Ibu Yustina Sriyatun atas doa dan dukungan semangat yang diberikan kepada penulis.
11. Mbak Gisela Kusria,dan Adek Titus Marcel Kusraynaldi yang selalu menjadi obat serta semangat saat penulis mengalami kejenuhan dalam menulis skripsi. 12. Dian Prahara Florentino Wara yang selalu mendukung penulis belajar menjadi lebih baik, memberikan saran dan kritik, dan memberikan dorongan semangat dalam menyusun skripsi ini.
13. Benny Nugroho selaku teman seperjuangan selama penelitian dan penyusunan skripsi.
14. Dika, Lala, Nana Upil, Pakde Toro yang telah meluangkan waktu untuk memberikan diskusi terkait penelitian dan semangat yang diberikan kepada penulis.
ix
Bimo, Ping-ping, Sano, Tika atas kebersamaan dan semangat yang diberikan. 17. Teman-teman kos putri gita dan hiddent kos yang menjadi teman
seperjuangan di Yogyakarta.
18. Mbak Lini, Iphent, Kak Ety, Mbak Dhin atas kebersamaan dan dukungan yang diberikan.
19. Teman-teman FST “Jumawa” 2007 atas pengalaman, keceriaan, dan kebersamaan yang tak kan terlupakan.
20. Semua teman-teman Farmasi angkatan 2007, terima kasih atas kebersamaanya.
21. Semua pihak yang tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa skripsi ini masih terdapat banyak kekurangan. Oleh karena itu penulis mengharapkan kritik dan saran untuk membantu penulis dalam perkembangan selanjutnya. Akhir kata, semoga skripsi ini berguna bagi pembaca.
x
Hal
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
xi
C. Kurkumin ... 7 D. Spektrofotometri Visibel ... 11 E. Kromatografi Cair Kinerja Tinggi ...
1. Definisi dan instrumentasi KCKT ... 2. Kromatografi Partisi ... 3. Pemisahan puncak dalam kromatografi ... 4. Analisis kualitatif dan analisis kuantitatif ...
12 BAB III. METODE PENELITIAN ...
xii
xiii
4. Fase gerak metanol p.a : asam asetat glasial 2% dengan perbandingan 95:5 ... BAB V. KESIMPULAN DAN SARAN . ... A. Kesimpulan ... B. Saran ... DAFTAR PUSTAKA ... LAMPIRAN ... BIOGRAFI PENULIS ...
xiv
Tabel I. Perbedaan kapsul keras dengan kapsul lunak ... Tabel II. Karakteristik beberapa pelarut pada KCKT ... Tabel III. Pemisahan yang diinginkan dalam metode KCKT ... Tabel IV. Komposisi fase gerak metanol p.a : asam asetat glasial 2% . Tabel V. Nilai indeks polaritas dari masing-masing komposisi fase gerak metanol p.a:asam asetat glasial 2% ... Tabel VI. Tekanan kolom ... Table VII. Hasil pemisahan kurkumin ... Tabel VIII. Hasil optimasi pemisahan kurkumin pada fase gerak metanol
p.a:asam asetat glasial 2% (95:5) ...
Tabel IX. Data hasil perhitungan CV resolusi pada fase gerak metanol p.a:asam asetat glasial 2% ...
7 14 24 29
35 42 43
57
xv
Gambar 1. Logo Obat Herbal Terstandar ... Gambar 2. Struktur dari kurkuminoid ... Gambar 3. Reaksi degradasi kurkumin pada pH basa ... Gambar 4. Produk fotodegradasi kurkumin ... Gambar 5. Peralatan KCKT ... Gambar 6. Reaksi silanisasi ... Gambar 7. Reaksi pembuatan kolom oktadesilsilan... Gambar 8. Difusi Eddy ... Gambar 9. Difusi molekular ... Gambar 10. Transfer massa fase diam dan fase gerak ... Gambar 11. Pemisahan dua senyawa ... Gambar 12. Penentuan peak asymmetry dan peak tailing factor ... Gambar 13. Distribusi analit dalam fase gerak dan fase diam ... Gambar 14. Reaksi hidrolisis kolom oktadesilsilan ... Gambar 15. Spektra serapan kurkumin dengan pelarut campuran metanol
p.a dan asam asetat glasial 2% pada pH 4 ... Gambar 16. Gugus kromofor dan auksokrom kurkumin ... Gambar 17. A = baku kurkumin 3,5 ppm; B = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 70:30 kecepatan alir 0,5 ml/menit ... Gambar 18. C = baku kurkumin 3,5 ppm; D = sampel OHT Rheumakur®
xvi
70:30 kecepatan alir 1,0 ml/menit ... Gambar 19. E = baku kurkumin 3,5 ppm; F = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 70:30 kecepatan alir 1,5 ml/menit ... Gambar 20. A = baku kurkumin 3,5 ppm; B = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 0,5 ml/menit ... Gambar 21. C = baku kurkumin 3,5 ppm; D = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 1,0 ml/menit ... Gambar 22. E = baku kurkumin 3,5 ppm; F = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 1,5 ml/menit ... Gambar 23. A = baku kurkumin 3,5 ppm; B = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 0,5 ml/menit ... Gambar 24. C = baku kurkumin 3,5 ppm; D = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 1,0 ml/menit ... Gambar 25. E = baku kurkumin 3,5 ppm; F = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 1,5 ml/menit ...
xvii
pada fase gerak metanol p.a : asam asetat glasial 2% 95:5 kecepatan alir 0,5 ml/menit ... Gambar 27. C = baku kurkumin 3,5 ppm; D = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 95:5 kecepatan alir 1,0 ml/menit ... Gambar 28. E = baku kurkumin 3,5 ppm; F = sampel OHT Rheumakur®
pada fase gerak metanol p.a : asam asetat glasial 2% 95:5 kecepatan alir 1,5 ml/menit ... Gambar 29. Gugus polar dan nonpolar dari kurkumin ... Gambar 30. Interaksi kurkumin dengan fase gerak metanol p.a:asam asetat glasial 2% membentuk interaksi hidrogen ... Gambar 31. Interaksi kurkumin dengan fase diam oktadesilsilan ...
55
55
56 59
xviii
Lampiran 1. Sertifikat analisis kurkumin ... Lampiran 2. Hasil Uji Stabilitas Kurkumin pada pH 3-5 dengan
Spektrofotometer Visibel pada rentang 200-500 nm ... Lampiran 3. Perhitungan Kepolaran Fase Gerak ... Lampiran 4. Kromatogram hasil optimasi kecepatan alir pada fase gerak metanol p.a:asam asetat glasial 2%(70:30) ... Lampiran 5. Nilai Asymmetry Factor (AF) peak kurkumin pada fase gerak metanol p.a:asam asetat glasial 2% (70:30) dan contoh perhitungannya ... Lampiran 6. Kromatogram hasil optimasi kecepatan alir pada fase gerak metanol p.a:asam asetat glasial 2%(80:20) ... Lampiran 7. Nilai Asymmetry Factor (AF) peak kurkumin pada fase gerak metanol p.a:asam asetat glasial 2% (80:20) dan contoh perhitungannya ... Lampiran 8. Kromatogram hasil optimasi kecepatan alir pada fase gerak metanol p.a:asam asetat glasial 2%(90:10) ... Lampiran 9. Nilai Asymmetry Factor (AF) peak kurkumin pada fase gerak metanol p.a:asam asetat glasial 2% (90:10) dan contoh perhitungannya ... Lampiran 10. Kromatogram hasil optimasi kecepatan alir pada fase gerak metanol p.a:asam asetat glasial 2%(95:5) ...
xix
gerak metanol p.a:asam asetat glasial 2% (95:5) dan contoh perhitungannya ... Lampiran 12. Nilai resolusi dan HETP pada fase gerak metanol p.a:asam asetat glasial 2 % (95:5) ... Lampiran 13. Reprodusibilitas: Kromatogram pemisahan kurkumin
xx
Kurkumin merupakan senyawa alam yang memiliki banyak khasiat bagi kesehatan dan banyak digunakan dalam berbagai sediaan obat tradisional. Salah satu obat tradisional yang mengandung kurkumin yaitu obat herbal terstandar (OHT) Rheumakur® yang memiliki efek farmakologis sebagai anti inflamasi.
Dalam produk OHT perlu dilakukan analisis untuk mengetahui kebenaran kandungan kurkumin dalam kapsul lunak OHT Rheumakur® ini. Metode yang
digunakan yaitu dengan Kromatografi cair Kinerja Tinggi (KCKT) fase terbalik. Penelitian ini merupakan penelitian eksperimental deskriptif. Sistem KCKT yang digunakan fase terbalik dengan kolom reversed phase C18 dengan
fase gerak metanol p.a:asam asetat glasial 2% dan menggunakan detektor visibel pada λ 432 nm. Optimasi yang dilakukan dengan mengubah-ubah komposisi fase
gerak metanol p.a:asam asetat glasial 2% (70:30), (80:20), (90:10), dan (95:5) dan mengubah-ubah kecepatan alir yaitu 0,5; 1,0; dan 1,5 ml/menit.
Kondisi optimum sistem KCKT yang digunakan adalah fase gerak metanol p.a:asam asetat glasial 2% 95:5 pada kecepatan alir 1,0 ml/menit. Kondisi ini memenuhi parameter pemisahan yang baik yaitu bentuk peak simetri, waktu retensi efisien sebesar 2,699 menit, nilai resolusi 3,905, dan nilai HETP sebesar 0,053.
xxi
Curcumin is a natural compound that has many health giving properties and is widely used in various traditional medicinal preparations. One of the traditional medicine that contains curcumin which is a Scientific Based Herbal Medicine (SBHM) Rheumakur® which has a pharmacological effect as an
anti-inflammatory. In SBHM product, analysis is needed to know the truth content of curcumin in SBHM Rheumakur ® soft capsules. The method used is by Reversed
Phase-High Performance Liquid Chromatography (RP-HPLC).
This research is a descriptive experimental research. HPLC system used in reverse phase with column C18 with mobile phase methanol p.a: glacial acetic
acid 2% and using visible detector at λ 432 nm. Optimization is performed by varying the composition of mobile phase of methanol p.a: glacial acetic acid 2% (70:30), (80:20), (90:10), and (95:5) and varying the flow rate of 0.5; 1.0; and 1.5 ml/min.
The optimum conditions of HPLC systems used were mobile phase of methanol p.a: glacial acetic acid 2% 95:5 at flow rate 1.0 ml/min. These conditions meet the parameters of good separation of the form of peak symmetry, retention time efficient of 2.699 minutes, 3.905 resolution value, and the HETP value of 0.053.
1
PENGANTAR
A. Latar Belakang
Obat tradisional di masyarakat luas telah banyak digunakan untuk mengobati berbagai macam penyakit. Obat tradisional banyak digunakan berdasarkan pengalamanan maupun dari perbincangan dari mulut ke mulut mengenai khasiat yang dimiliki serta cara penggunaan suatu obat tradisional. Obat tradisional yang sering digunakan di masyarakat adalah kunyit yang kandungan zat aktifnya kurkumin. Kurkumin banyak digunakan karena memiliki banyak khasiat, seperti analgesik, antiinflamsi, antikanker, antimikrobial, antioksidan (Aggarwal et al., 2006). Dalam penelitian ini dilakukan penelitian tentang kurkumin dalam sediaan kapsul lunak obat herbal terstandar (OHT) Rheumakur®
yang memiliki khasiat antiinflamasi.
Obat Herbal Terstandar (OHT) merupakan pengembangan dari obat tradisional yang bahan bakunya telah mengalami standarisasi dan melalui tahap uji praklinis. Proses produksi OHT dilakukan berdasarkan cara pembuatan obat tradisional yang baik (CPOTB). Salah satu produk OHT yang mengandung kurkumin adalah Rheumakur®.
Dalam sediaan kapsul lunak OHT Rheumakur® terkandung lebih dari satu macam ekstrak. Komposisi OHT Rheumakur® terdiri dari kurkuminoid 10
tepat untuk memperoleh efek farmakologis yang diharapkan. Dosis yang tepat dapat dilihat berdasarkan kebenaran kadar yang tertera dalam label. Apabila kadar yang tertera dalam kapsul kurang dari yang tertera dalam label maka efek terapi yang dihasilkan kurang optimum.
Berdasarkan alasan tersebut di atas maka diperlukan suatu penelitian mengenai penjaminan kualitas tentang kebenaran kandungan senyawa dan dosis dalam OHT tersebut. Penjaminan mutu bertujuan untuk menjamin terciptanya produk yang aman dan berkualitas pada obat tradisional khususnya OHT yang mengandung kurkumin. Penjaminan mutu ini dapat dibuktikan dengan membandingkan kebenaran kandungan yang terdapat dalam label dengan hasil penelitian yang dilakukan.
Metode yang dipilih dalam menetapkan kadar kurkumin dalam sediaan kapsul lunak Rheumakur® yaitu menggunakan kromatografi cair kinerja tinggi
(KCKT) fase terbalik. Metode KCKT ini bersifat selektif dalam memisahkan senyawa dalam multikomponen, memiliki sensitifitas yang tinggi dan dapat diperoleh pemisahan yang baik.
Penelitian ini merupakan bagian dari rangkaian penelitian penetapan kurkumin dalam sampel yang terdiri dari optimasi metode, validasi metode, dan penetapan kadar. Dalam penelitian ini peneliti mengambil bagian dalam optimasi metode. Tujuan dari optimasi untuk mendapatkan kondisi optimum metode KCKT yang dapat memisahkan kurkumin dari senyawa-senyawa lain yang terdapat dalam sediaan kapsul lunak OHT Rheumakur®. Kondisi optimum
nilai HETP (Height Equivalent to a Theoretical Plate) yang semakin kecil, dan nilai resolusi ≥ 1,5 (Snyder, Kirkland, and Glajh, 1997).
Optimasi perlu dilakukan karena dalam penelitian ini digunakan metode KCKT dengan sistem baru yaitu penggunaan komposisi fase gerak yang belum pernah digunakan sebelumnya untuk menetapkan kadar kurkumin dalam kapsul lunak OHT Rheumakur®. Selain itu OHT Rheumakur® belum pernah diteliti
sebelumnya sehingga diperlukan sistem yang baru untuk memperoleh pemisahan yang baik. Optimasi dilakukan dengan mengubah-ubah komposisi fase gerak dan variasi kecepatan alir. Pada perbandingan fase gerak dan kecepatan alir yang optimal akan dihasilkan pemisahan yang optimum.
1. Permasalahan
Berdasarkan latar belakang tersebut, permasalahan yang muncul adalah bagaimana komposisi fase gerak dan kecepatan alir yang optimal yang mampu menghasilkan pemisahan yang baik untuk penetapan kadar kurkumin dalam sediaan kapsul lunak OHT Rheumakur® menggunakan metode KCKT fase
terbalik, dilihat dari bentuk peak, waktu retensi, nilai resolusi dan nilai HETP yang dihasilkan?
2. Keaslian Penelitian
2006). Penelitian dengan judul “Curcumin Quantification in Dosage Forms using High Performance Liquid Chromatography” juga pernah dilakukan menggunakan fase diam C18 dengan komposisi fase gerak asetonitril:asam asetat 2% (45:55)
(Musfiroh, Indriyati, Susilawati, dan Percekawati, 2007). Namun optimasi metode kromatografi cair kinerja tinggi (KCKT) pada penetapan kadar kurkumin dalam kapsul lunak OHT Rheumakur® menggunakan fase gerak campuran metanol p.a
dan asam asetat glasial 2% belum pernah dilakukan. 3. Manfaat Penelitian
a. Manfaat Metodologis. Penelitian ini dapat menghasilkan sumbangan ilmiah mengenai metode penelitian dalam melakukan optimasi metode untuk menetapkan kadar kurkumin dalam sediaan kapsul OHT menggunakan metode KCKT fase terbalik.
b. Manfaat Praktis. Penelitian ini dapat digunakan sebagai metode optimasi untuk analisis kurkumin dalam sediaan kapsul OHT dan dapat memberikan informasi bagi konsumen mengenai mutu, keamanan, dan manfaat kurkumin dalam kapsul lunak OHT Rheumakur®.
B. Tujuan Penelitian
6
PENELAAHAN PUSTAKA
A. Obat Herbal Terstandar (OHT)
Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan (BPOM) Republik Indonesia nomor : HK.00.05.4.2411, penggolongan obat bahan alam Indonesia berdasarkan cara pembuatan serta jenis klaim penggunaan dan tingkat pembuktian khasiat, dikelompokkan menjadi jamu, obat herbal terstandar, dan fitofarmaka.
Obat Herbal Terstandar (OHT) harus memenuhi kriteria yaitu aman sesuai dengan persyaratan yang ditetapkan, klaim kasiat dibuktikan secara ilmiah/pra klinik, telah dilakukan standardisasi terhadap bahan baku yang digunakan dalam produk jadi, memenuhi persyaratan mutu yang berlaku (BPOM RI, 2004).
Gambar 1. Logo Obat Herbal Terstandar (OHT)
Rheumakur® merupakan salah satu produk OHT yang diproduksi oleh
PT. Phytochemindo Reksa dalam bentuk sediaan kapsul lunak. Tiap kapsul mengandung 10 mg kurkuminoid dan 100 mg minyak atsiri kunyit dan temulawak. Rheumakur® memiliki khasiat untuk membantu mengurangi gejala
B. Kapsul
Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut. Cangkang umumnya terbuat dari gelatin, tetapi dapat juga terbuat dari pati atau bahan lain yang sesuai. Berdasarkan bentuknya kapsul dalam farmasi dibedakan menjadi 2, yaitu kapsul keras (capsulae durae, hard capsule) dan kapsul lunak (capsulae molles, soft capsule) yang perbedaannya dapat dilihat di tabel I.
Tabel I. Perbedaan kapsul keras dengan kapsul lunak
Kapsul Keras Kapsul Lunak
Terdiri atas tubuh dan tutup
Tersedia dalam bentuk kosong
Isi biasanya padat, dapat juga cair
Satu kesatuan
Cara pakai per oral
Selalu sudah terisi
Isi biasanya cair, dapat juga padat
Bisa oral, vaginal, rectal, topikal
Kapsul cangkang lunak yang dibuat dari gelatin, sedikit lebih tebal dari dibanding kapsul cangkang keras dan dapat diplastisasi dengan penambahan senyawa poliol, seperti sorbitol atau gliserin. Kapsul lunak dapat mengandung pigmen atau pewarna, bahan opak seperti titanium dioksida, pengawet,pengharum dan pemanis atau sukrosa 5%. Cangkang gellatin lunak umumnya mengandung air 6-13%. Cangkang kapsul lunak tidak dipakai di apotek, tetapi diproduksi secara besar-besaran di dalam pabrik dan biasanya diisi dengan cairan. Kapsul lunak yg bekerja long action, umumnya berisi granaula dan disebut Spansule.
C. Kurkumin
(temulawak) berkisar antara 1 – 2 %. Kurkumin merupakan senyawa aktif yang penting dan bertanggung jawab terhadap aktivitas biologis pada Curcuma sp. (Aggarwal et al., 2006).
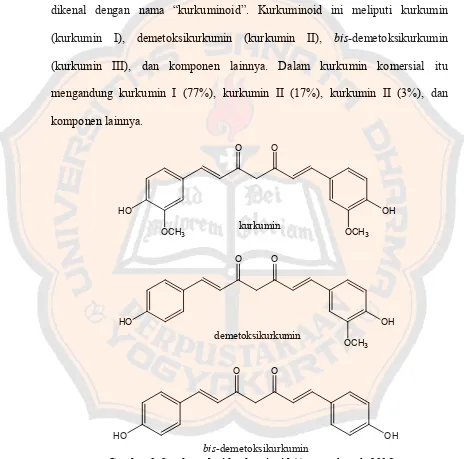
Kunyit mengandung kurkumin bersama dengan konstituen lain yang dikenal dengan nama “kurkuminoid”. Kurkuminoid ini meliputi kurkumin (kurkumin I), demetoksikurkumin (kurkumin II), bis-demetoksikurkumin (kurkumin III), dan komponen lainnya. Dalam kurkumin komersial itu mengandung kurkumin I (77%), kurkumin II (17%), kurkumin II (3%), dan
Gambar 2. Struktur dari kurkuminoid (Aggarwal et al., 2006)
melting point 183°C, berat molekul 368,37 g/mol. Secara spektrofotometri, kurkumin memiliki absorbansi maksimum pada panjang gelombang 430 nm dalam pelarut metanol (Aggarwal et al., 2006).
Stabilitas kurkumin dipengaruhi oleh pH lingkungan dan cahaya. Kurkumin akan mengalami reaksi hidrolisis di dalam air, tergantung pada pH lingkungan. Kecepatan degradasi pada pH < 7 lebih lambat dibanding pH >7. Ketidakstabilan kurkumin pada pH alkali disebabkan oleh gugus metilen aktif (Tonnesen dan Karlsen, 1985). Produk degradasi kurkumin dalam lingkungan alkali (pH 7-10) akan mengalami disosiasi dan menghasilkan asam ferulat dan feruloil metan, yang selanjutnya feruloil metan dapat terdegradasi menjadi vanilin, dengan reaksi seperti pada gambar 3.
O O
Selain pH alkali, kestabilan kurkumin dipengaruhi oleh adanya cahaya. Adanya cahaya dapat menyebabkan terjadinya degradasi fotokimia kurkumin. Produk fotodegradasi kurkumin dapat dilihat pada gambar 4.
O O
Gambar 4. Produk fotodegradasi kurkumin (Sudaryono, Nourmamode, Gardrat, Grelier, Bravic, Chasseau, Castellan, 2003)
efek samping (adenoma, lymphoma) (Bermawie, Rahardjo, Wahyuno dan Ma’mun, 2006).
D. Spektrofotometri Visibel
Spektrofotometri visibel merupakan teknik analisis spektroskopik yang memakai sumber radiasi elektromagnetik sinar tampak (380-780) dengan memakai instrumen spektrofotometer (Mulja dan Suharman, 1995). Spektrofotometri visibel termasuk dalam spektrofotometri serapan yang melakukan pengukuran suatu interaksi antara radiasi elektromagnetik (REM) dengan molekul atau atom dari suatu zat kimia (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
Molekul suatu senyawa dapat memberikan serapan radiasi elektromagnetik jika memiliki kromofor yaitu gugus penyerap dalam molekul. Pada senyawa organik dikenal pula gugus auksokrom yaitu gugus jenuh yang bila terikat pada kromofor dapat mengubah panjang gelombang serapan dan intensitas serapan maksimum, cirinya adalah heteroatom yang terikat langsung pada kromofor (Sastrohamidjojo, 2002).
konsentrasi zat penyerap linier (Bassett, Denney, Jeffery, dan Medham, 1994). Hubungan antara transmitan atau absorban terhadap intensitas radiasi atau konsentrasi zat yang dianalisis dan tebal larutan yang mengabsorpsi sebagai :
(1)
(2)
Dimana T = persen transmitan
Io = intensitas radiasi yang datang
It = intensitas radiasi yang diteruskan
ε = daya serap molar (L mol-1 cm -1)
c = konsentrasi (mol L-1)
b = tebal larutan (cm)
A = serapan / absorbansi (Mulya dan Suharman, 1995).
E. Kromatografi Cair Kinerja Tinggi (KCKT) 1. Definisi dan instrumentasi KCKT
Kromatografi adalah suatu teknik pemisahan komponen-komponen dalam campuran yang dialirkan oleh fase yang bergerak, dapat berupa gas atau zat cair, melalui fase diam yang berupa zat cair atau zat padat (Skoog, West, dan Holier, 1994).
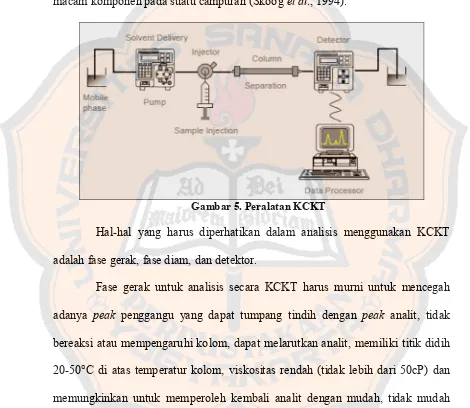
dengan kecepatan dan efisiensi tinggi (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995). Peralatan KCKT dapat dilihat pada gambar 5.
KCKT merupakan metode kromatografi cair yang paling banyak digunakan dalam analisis pemisahan, identifikasi dan penetapan kadar berbagai macam komponen pada suatu campuran (Skoog et al., 1994).
Gambar 5. Peralatan KCKT
Hal-hal yang harus diperhatikan dalam analisis menggunakan KCKT adalah fase gerak, fase diam, dan detektor.
kolom. Maka dari itu, fase gerak perlu di degassing untuk menghilangkan gas terlarut (Dean, 1995).
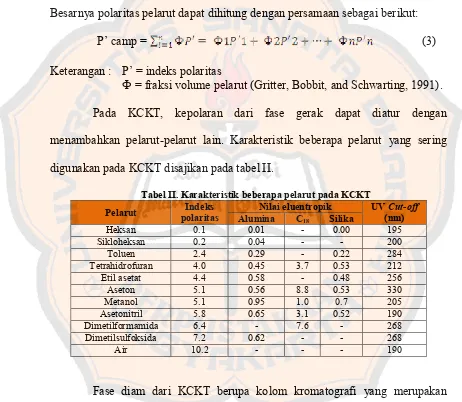
Pemilihan fase gerak yang digunakan terutama berdasarkan kepolaran campuran pelarut yang semakin linier dengan pelarut murni. Tingkat kepolaran pelarut menggambarkan kekuatan pelarut dalam mengelusi suatu senyawa. Besarnya polaritas pelarut dapat dihitung dengan persamaan sebagai berikut:
P’ camp = (3)
Keterangan : P’ = indeks polaritas
Ф = fraksi volume pelarut (Gritter, Bobbit, and Schwarting, 1991). Pada KCKT, kepolaran dari fase gerak dapat diatur dengan menambahkan pelarut-pelarut lain. Karakteristik beberapa pelarut yang sering digunakan pada KCKT disajikan pada tabel II.
Tabel II. Karakteristik beberapa pelarut pada KCKT
Pelarut polaritas Indeks Alumina Nilai eluentropik C UV (nm) Cut-off
18 Silika tempat pemisahan komponen-komponen yang terdapat dalam sampel. Oktadesilsilan (C18) merupakan fase diam yang paling banyak digunakan karena
Persyaratan detektor KCKT adalah sensitifitas harus tinggi (10-8 – 10-15 g
analit/detik); kestabilan dan reprodusibilitas yang baik; memberikan respon yang linier terhadap konsentrasi analit; dapat bekerja pada temperatur kamar sampai 400°C; tidak terpengaruh oleh perubahan temperatur dan kecepatan fase gerak; mudah didapat dan mudah dioperasikan; selektif terhadap berbagai macam analit di dalam fase gerak; tidak merusak analit; dapat menghilangkan “zone broadening” dengan adanya pengaruh minimal internal volume (Mulja dan Suharman, 1995).
Secara umum detektor dibagi menjadi 2 kategori yaitu bulk property detectors dan solute property detectors. Bulk property detectors merupakan jenis detektor yang mengukur sifat fisik solut dan fase gerak. Detektor tipe ini relatif tidak sensitif dan menghendaki temperatur yang terkendali, contohnya detektor indeks bias. Solute property detectors merupakan detektor yang hanya mengukur sifat solut. Detektor ini 1000 kali lebih sensitif dan mampu mengukur solut sampai satuan nanogram atau lebih kecil lagi, contohnya detektor UV-Vis (Munson, 1991).
2. Kromatografi Partisi
perbandingan konsentrasi analit dalam fase diam (Cs) dan dalam fase gerak (Cm) (Rohman dan Gandjar, 2007).
(4)
Kolom yang biasa digunakan dalam kromatografi partisi fase terbalik adalah kolom dengan kemasan fase terikat yang memiliki sifat stabil karena fase diamnya terikat secara kimia pada penyangga, sehingga tidak mudah terelusi oleh fase gerak. Penyangga pada fase terikat biasanya terbuat dari silika yang sudah diseragamkan, berpori, dan umumnya mempunyai diameter 3,5 atau 10 µm (Skogg et al., 1998).
Pada KCKT partisi fase terbalik biasanya mengandung bagian organik yang terikat secara kimia dengan gugus silanol pada permukaan silika. Bagian organik tersebut umumnya hidrokarbon rantai panjang, sehingga fase gerak umumnya polar. Gugus silanol permukaan dapat direaksikan dengan berbagai cara menempelkan berbagai jenis gugus organik. Kemasan fase terikat dengan tipe ikatan siloksan (Si-O-Si-O) dibuat dengan mereaksikan organoklorosilan dengan gugus silanol pada permukaan silika gel. Reaksi silanasi sebagai berikut:
Si OH Cl Si(CH3)R Si O Si(CH3)R HCl
Gambar 6. Reaksi silanisasi
Si OH Cl Si (CH2)17CH3 Si O Si (CH2)17CH3 HCl
Gambar 7. Reaksi pembuatan kolom oktadesilsilan
Gugus yang ditempelkan pada silanol pada umumnya adalah hidrokarbon rantai panjang. Panjang pendeknya rantai karbon mempengaruhi tertambatnya senyawa pada fase diam.
Gugus silanol yang tidak bereaksi karena adanya halangan sterik dapat memberikan kepolaran yang tidak dikehendaki dan menyebabkan pengekoran pada puncak kromatogram. Untuk mengurangi jumlah gugus silanol yang masih bebas, reaksi dilanjutkan dengan penambahan trimetilklorosilan yang dapat mencapai gugus silanol karena ukurannya yang lebih kecil dibandingkan organoklorosilan lain. Penambahan trimetilklorosilan dapat menutupi banyak gugus silanol yang masih bebas, namun tidak semua gugus tersebut dapat tertutupi (Skoog et al., 1998).
3. Pemisahan puncak dalam kromatografi
a. Efisiensi kolom. Pemisahan puncak-puncak dalam kromatografi memiliki hubungan yang erat dengan efisiensi kolom. Pada efisiensi kolom terdapat dua teori yang menjelaskan tentang pemisahan puncak dalam kromatografi yaitu teori lempeng dan teori laju.
Berdasarkan teori lempeng, jumlah lempeng (N) yang didasarkan pada konsep lempeng teoritis pada destilasi kolom digunakan sebagai ukuran efisiensi kolom N didefinisikan sebagai berikut:
(5)
Dimana merupakan lebar setengah puncak kromatogram, tR merupakan
waktu retensi (Rohman dan Gandjar, 2007).
Suatu ukuran alternatif yang bergantung pada panjang kolom kromatografi adalah tinggi lempeng (H) atau biasa disebut dengan tinggi setara pelat teori (HETP = Height Equivalent Theoritical Plate). Hubungan HETP dan jumlah lempeng (N) serta panjang kolom (L) dapat dirumuskan dengan:
(6)
Teori lempeng hanya menggambarkan laju migrasi secara kuantitatif, tetapi tidak dapat menggambarkan pengaruh variabel-variabel lain yang menyebabkan terjadinya pelebaran peak yang akan dijelaskan menurut teori laju. Pada waktu migrasi, solut mengalami transfer dalam fase diam dan fase gerak berkali-kali. Solut hanya dapat bergerak jika berada dalam fase gerak sehingga migrasi di dalam kolom juga tidak teratur dan mengakibatkan laju rata-rata solut relatif terhadap fase gerak juga sangat bervariasi sehingga terjadi pelebaran peak solut (Noegrohati, 1994).
Menurut teori laju, efisiensi kolom dinyatakan dengan persamaan Van Deemter yang dinyatakan dengan persamaan sebagai berikut:
(7)
(8)
Dimana λ = tetapan ukuran ketidakteraturan kemasan dp = diameter rata-rata partikel penyangga D = kedifusian linarut dalam fase gerak k' = faktor kapasitas
µ = kecepatan alir
γ = faktor koreksi kelikuan saluran dalam kolom
Dari persamaan di atas dapat dilihat terdapat tiga variabel yang mempengaruhi efisiensi kolom, yaitu:
Difusi Eddy menggambarkan ketidakhomogenan kecepatan alir dan panjang lintasan di sekitar partikel terpack-ing. Difusi Eddy dinyatakan sebagai A ( ). Lintasan alir yang tidak sama pasti ditemukan dalam kolom terpack-ing.
kecil. Molekul solut yang melewati bagian tengah kolom akan mencapai akhir kolom lebih lambat. Hal ini yang menyebabkan perbedaan laju tiap molekul melalui kolom berbeda-beda. Untuk meminimalkan difusi Eddy maka diameter rata-rata partikel dalam kolom harus sekecil mungkin dan seseragam mungkin (Willard, Merrit, Dean, and Settle, 1988). Difusi Eddy yang terjadi di dalam kolom dapat dilihat pada gambar 8.
Gambar 8. Difusi Eddy (Meyer, 2004)
Difusi longitudinal atau difusi molekular dinyatakan dengan B (2γD/µ) yang menggambarkan efek dari difusi longitudinal, pergerakan acak dari molekul dalam fase gerak. Pengaruh difusi longitudinal terhadap ketinggian lempeng menjadi sangat signifikan hanya pada kecepatan fase gerak yang rendah. Kecepatan difusi solut yang tinggi pada fase gerak dapat menyebabkan molekul solut terdispers secara aksial sementara dengan lambat bermigrasi melalui kolom.
Gambar 9. Difusi molekular (Christian, 2004)
Transfer massa dinyatakan dengan Cstationery dan Cmobile . Cstationery
lambat dalam fase diam, sementara molekul lainnya melalui kolom bersama dengan fase gerak. Untuk melintasi hal ini diperlukan fase diam yang lebih encer. Sedangkan Cmobile menggambarkan adanya peristiwa dimana solut dalam fase
diam bertemu dengan fase gerak yang masih baru. Peristiwa transfer massa fase diam dan fase gerak dapat digambarkan sebagai berikut (Gambar 10).
Gambar 10. Transfer massa antara fase diam dan fase gerak (Meyer, 2004)
b. Waktu tambat (tR) dan resolusi. Waktu tambat atau waktu retensi
adalah selang waktu yang diperlukan analit mulai saat injeksi sampai keluar dari kolom dan sinyalnya ditangkap detektor, dinyatakan sebagai tR (Mulja dan
Suharman, 1995). Waktu tambat dari suatu komponen yang tidak ditambat oleh fase gerak disebut sebagai waktu hampa (t0). Waktu tambat merupakan fungsi dari
kecepatan alir fase gerak dan panjang kolom. Jika fase gerak mengalir lebih lambat ataupun kolom semakin panjang, waktu tambat dan waktu hampa akan semakin besar (Meyer, 2004). Menurut Snyder et al (1997) waktu retensi yang diinginkan dalam suatu proses analisis secara KCKT adalah kurang dari 10 menit. Faktor resolusi (R) adalah ukuran pemisahan dari dua puncak berdekatan yang dapat diukur dengan persamaan:
Harga tR1 dan tR2 merupakan waktu retensi senyawa yang dapat diukur
pada titik maksimum puncak, harga w1 dan w2 merupakan lebar alas puncak
(Johnson dan Stevenson, 1991). Untuk pemisahan yang baik R harus ≥ 1,5 karena berarti pemisahan senyawa ≥ 99,7% (Sastrohamidjojo, 2002).
Gambar 11. Pemisahan dua senyawa (Meyer, 2004)
Harga R > 1,5 disebut baseline resolution, yaitu pemisahan sempurna dari dua puncak dengan ukuran sama. Bila kedua puncak yang berdekatan memiliki perbedaan ukuran yang signifikan, maka diperlukan nilai resolusi yang lebih besar (Meyer, 2004).
peak asymmetry factor (AF), yang diukur 10% dari tinggi puncak. Peak yang simetri mempunyai nilai AF sama dengan 1, tetapi peak dengan nilai AF pada rentang 0,95-1,1 masih dikatakan baik. Bila puncak berbentuk tailing, maka nilai AF lebih besar dari 1 dan sebaliknya bila puncak berbentuk fronting maka AF akan bernilai lebih kecil dari 1. Selain AF, parameter lain yang dapat digunakan yaitu peak tailing factor (Tf), yang diukur pada 5% tinggi puncak (Snyder et al, 1997).
Gambar 12. Penentuan peak asymmetry dan peak tailing factor (Meyer, 2004) Distribusi analit dalam fase gerak dan fase diam pada saat terjadi tailing dan fronting dapat dilihat dalam gambar 13.
Gambar 13. Distribusi analit dalam fase gerak dan fase diam (Rohman dan Gandjar, 2007)
yang tidak seragam, dan faktor yang terjadi di luar kolom seperti injektor (Noegrohati, 1994).
4. Analisis Kualitatif dan Analisis Kuantitatif
KCKT dapat digunakan untuk analisis kualitatif dan kuantitatif dari suatu sampel. Analisis kualitatif dilakukan dengan cara membandingkan waktu retensi senyawa murni (baku) dan waktu retensi yang dimaksud dalam sampel. Respon yang berupa tinggi peak maupun luas area peak dapat digunakan untuk analisis kuantitatif (Noegrohati, 1994).
Beberapa aspek yang perlu diperhatikan untuk memperoleh pemisahan yang baik tersaji pada tabel III berikut:
Tabel III. Pemisahan yang diinginkan dalam metode KCKT
Tujuan Keterangan
Resolusi Presisi dan ketahanan metode analisis kuantitatif memerlukan nilai Rs lebih besar dari 1,5
Waktu pemisahan < 5-10 menit merupakan waktu yang diinginkan untuk prosedur rutin
Kuantifikasi Nilai CV ≤ 2%
Tekanan kolom < 150 bar adalah yang diharapkan, namun biasanya < 200 bar masih diijinkan
Tinggi peak Bentuk peak yang sempit sangat diharapkan
Konsumsi fase gerak Jumlah fase gerak yang minimum setiap pengujian sangat diharapkan
(Snyder et al, 1997)
F. Landasan Teori
Obat Herbal Terstandar (OHT) Rheumakur® merupakan OHT yang
mengandung kurkumin yang memiliki aktivitas sebagai antireumatik. Produk OHT telah mengalami uji praklinis dan telah mengalami standarisasi bahan baku. Namun dalam produk OHT belum dilakukan penjaminan kualitas tentang kadar senyawa aktif di dalamnya.
Metode KCKT dapat digunakan untuk menetapkan kadar kurkumin dalam sediaan obat herbal terstandar (OHT) karena memiliki sensitifitas dan selektifitas yang tinggi. Pada penetapan kadar kurkumin dengan metode KCKT pada OHT Rheumakur® ini digunakan fase terbalik karena kurkumin cenderung bersifat
nonpolar sehingga kurkumin dapat berinteraksi dengan fase diam melalui ikatan Van der Waals. Optimasi pemisahan kurkumin ini dilakukan untuk mendapatkan kondisi yang optimum dalam menganalisis kurkumin. Dengan komposisi fase gerak dan kecepatan alir yang optimal akan dihasilkan pemisahan kurkumin yang baik yaitu bentuk peak simetris, nilai resolusi ≥ 1,5 terhadap peak terdekat, nilai HETP yang semakin kecil.
G. Hipotesis
26
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis penelitian yang berjudul “Optimasi Metode Kromatografi Cair Kinerja Tinggi (KCKT) Fase Terbalik pada Penetapan Kadar Kurkumin dalam Sediaan Kapsul Lunak Obat Herbal Terstandar (OHT) Rheumakur®” bersifat
eksperimental dengan rancangan penelitian deskriptif.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah perbandingan komposisi fase gerak metanol p.a:asam asetat glasial 2%, dan kecepatan alir yang digunakan. 2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah bentuk peak, waktu retensi (tR), nilai HETP, dan nilai resolusi yang dihasilkan.
3. Variabel pengacau terkendali
a. Kemurnian pelarut yang digunakan. Untuk mengatasinya digunakan pelarut yang pro analysis yang memiliki kemurnian tinggi.
b. pH pelarut yang mempengaruhi stabilitas kurkumin. Untuk mengatasinya digunakan metanol p.a pH 4.
C. Definisi Operasional
1. Kurkumin merupakan senyawa yang terdapat dalam sampel kapsul lunak OHT Rheumakur®.
2. Sistem KCKT yang digunakan adalah seperangkat alat KCKT fase terbalik dengan fase diam kolom reversed phase C18 dengan fase gerak campuran
metanol p.a dan asam asetat glasial 2%.
3. Optimasi dilakukan dengan mengubah-ubah komposisi fase gerak dan kecepatan alir.
4. Parameter pemisahan yang optimum dengan menggunakan KCKT dapat dilihat dari bentuk peak, waktu retensi, nilai HETP dan nilai resolusi yang dihasilkan.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian adalah baku kurkumin (hasil sintesis Pof. Dr. Sudibyo Martono M.S., Apt. yang telah dikonfirmasi strukturnya dengan metode spektroskopi 1H-NMR dan Mass Spectra, kurkumin
hasil sintesis tersebut memiliki titik lebur 181,2-182,4°C), metanol pro analysis 1.06009.2500 EMSURE® ACS, ISO, Reag., Ph Eur (E. Merck), asam asetat
glasial pro analysis 1.00063.2500 EMPARTA® ACS(E. Merck), aquabidestilata,
E. Alat Penelitian
Seperangkat alat spektrofotometri UV-Vis merk Milton Ray Spectronic 3000 Array dengan printer Epson LQ-1170, seperangkat alat KCKT fase terbalik dengan sistem gradien dengan detektor visibel, Shimadzu LC-2010C, kolom oktadesilsilan (C18) merk KNAUER C18 No. 25EE181KSJ (B115Y620) dengan
dimensi 250 x 4,6 mm, packing KROMASIL 100-5 C18, seperangkat komputer
merk Dell B6RDZ1S Connexant System RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet D2566 HP-024-000 625 730, ultrasonikator merk Retsch tipe T460 No V935922013 EY, syringe, neraca kasar, neraca analitik Ohaus Carat Series PAJ 1003 (max 60/120 g, min 0,001g, d = 0,01/0,1 mg), penyaring millipore, mikropipet Socorex, vakum, organic solvent membrane filter (Whatman) ukuran pori (0,45 µm; diameter 47 mm), seperangkat alat gelas (Pyrex).
F. Tata Cara Penelitian 1. Pembuatan asam asetat glasial 2%
Sebanyak 2,0 ml asam asetat glasial dimasukkan ke dalam labu ukur 100,0 ml, ditambahkan aquabidest hingga batas tanda.
2. Pembuatan pelarut
3. Pembuatan Fase Gerak
Fase gerak yang digunakan dalam penelitian ini yaitu campuran metanol dan asam asetat glasial 2% dengan komposisi pada tabel IV.
Tabel IV. Komposisi fase gerak metanol p.a : asam asetat glasial 2% No. Komposisi fase gerak
Metanol p.a Asam asetat glasial 2%
1 70 30
2 80 20
3 90 10
4 95 5
Masing-masing pelarut disaring menggunakan kertas Whatman yang dibantu dengan pompa vaccum dan di degassing dengan ultrasonikator selama 15 menit. Untuk mendapatkan komposisi fase gerak seperti dalam tabel di atas, pencampuran fase gerak dilakukan di dalam sistem KCKT.
4. Pembuatan Larutan Baku Kurkumin
a. Pembuatan Larutan Stok Kurkumin. Menimbang seksama lebih kurang 10,0 mg serbuk kurkumin dan dimasukkan dalam labu 10,0 ml dilarutkan dengan metanol p.a pH 4 hingga batas tanda.
b. Pembuatan Larutan Intermediet Kurkumin. Sebanyak 1,0 ml dari larutan stok kurkumin diencerkan dengan metanol p.a pH 4 dalam labu takar 10,0 ml hingga batas tanda.
5. Preparasi Sampel
Satu kapsul OHT dikeluarkan isinya dan ditimbang seksama lebih kurang 50 mg dan dilarutkan dengan 10 mL metanol p.a pH 4 kemudian diaduk dengan magnetic stirer selama 15 menit dengan kecepatan 70 rpm. Ambil sebanyak 0,5 mL dari larutan tersebut dan dimasukkan dalam labu 10,0 mL diencerkan dengan metanol p.a pH 4 sampai batas tanda. Larutan disaring dengan millipore dan didegassing dengan menggunakan ultrasonikator selama 15 menit (larutan A). Preparasi dilakukan di tempat yang terlindungi dari cahaya.
6. Penentuan Panjang Gelombang Maksimum Kurkumin
Penentuan panjang gelombang maksimum dilakukan dengan merekam spektra larutan baku kurkumin 1 ppm; 3,5 ppm; dan 6 ppm pada rentang panjang gelombang 400-500 nm dengan menggunakan spektrofotometer UV-Vis terhadap blanko metanol p.a pH 4. Dari spektra serapan dapat diketahui panjang gelombang yang dihasilkan dari tiap konsentrasi. Tentukan panjang gelombang yang akan digunakan pada sistem KCKT yaitu panjang gelombang dimana ketiga konsentrasi tersebut menghasilkan serapan yang maksimum. Pengerjaan larutan kurkumin dilakukan di tempat yang terlindungi dari cahaya.
7. Optimasi Metode KCKT Fase Terbalik
kecepatan alir 0,5; 1,0; 1,5 ml/menit dari masing-masing komposisi fase gerak metanol p.a dan asam asetat glasial 2%. Data kromatogram yang didapat pada baku maupun sampel diamati sehingga diperoleh sistem KCKT fase terbalik yang dapat memberikan pemisahan kurkumin yang paling baik dari masing-masing larutan yang dianalisis.
b. Reprodusibilitas resolusi sampel dari fase gerak hasil optimasi. Pembuatan larutan seri baku kurkumin (konsentrasi 1 ppm, 3,5 ppm, dan 6 ppm) seperti langkah F.3 dan pembuatan sampel kapsul lunak OHT seperti langkah F.4 dilakukan replikasi sebanyak 3 kali dan masing-masing dilakukan repetisi sebanyak 2 kali. Larutan baku dan sampel kemudian diinjeksikan ke dalam KCKT dengan menggunakan komposisi fase gerak dan kecepatan alir yang optimal.
G. Analisis Hasil
Hasil optimasi metode untuk menetapkan kadar kurkumin dalam kapsul lunak Rheumakur® dapat dilihat dari data kromatogram yang diperoleh baik pada
baku maupun sampel pada komposisi fase gerak dan kecepatan alir tertentu. Hasil yang optimal ditentukan dengan mengamati bentuk peak yang dihasilkan, waktu elusi yang dibutuhkan, menghitung nilai resolusi dan nilai HETP.
1. Bentuk peak pemisahan kurkumin
Nilai AF = 1 maka peak dikatakan simetri dan pada nilai AF = 0,95-1,1 maka peak dikatakan baik.
2. Waktu retensi (tR)
Amati waktu yang dibutuhkan untuk pemisahan senyawa. Apabila kurang dari 10 menit, maka pemisahan dikatakan efisien.
3. Nilai resolusi
Resolusi merupakan ukuran pemisahan dari dua puncak berdekatan yang
diukur dengan persamaan:
.
Pemisahan yang baik menghasilkan nilai Rs ≥ 1,5.
4. Nilai HETP
baik. Nilai HETP dihitung dengan rumus , dimana N merupakan jumlah
lempeng teoritik dengan persamaan
5. Reprodusibilitas resolusi
34
HASIL DAN PEMBAHASAN
A. Pembuatan Pelarut
Pada penelitian ini digunakan metanol p.a pH 4 sebagai pelarut kurkumin. Berdasarkan orientasi stabilitas pH kurkumin didapatkan bahwa kurkumin stabil pada pH 4. Pembuatan pelarut metanol p.a pH 4 dilakukan dengan menambahkan asam asetat glasial 2% ke dalam metanol p.a. Asam asetat glasial 2% digunakan sebagai pengatur pH untuk menjaga stabilitas dari kurkumin. Pengaturan pH dimaksudkan untuk menjaga stabilitas dari kurkumin. Menurut Tonnesen dan Karlsen (1985), kurkumin dapat terdegradasi menjadi asam ferulat dan vanilin pada pH basa.
B. Pembuatan Fase Gerak
yang hampir sama yaitu pada perbandingan komposisi 40:60 dengan indeks polaritas 8,11. Namun komposisi fase gerak metanol p.a:asam asetat glasial 2% (40:60) memiliki pH 3, bukan merupakan pH stabilitas kurkumin hasil orientasi. Selanjutnya komposisi fase gerak ditingkatkan menjadi metanol p.a:asam asetat glasial 2% dengan perbandingan 60:40 dengan indeks polaritas 7,108. Namun pada hasil orientasi, komposisi fase gerak tidak memberikan pemisahan yang optimum. Menurut Mulja dan Suharman (1995), dalam sistem KCKT fase terbalik, kemampuan elusi akan meningkat dengan menurunnya polaritas fase gerak. Maka diperkirakan dengan menurunkan indeks polaritas fase gerak dengan meningkatkan komposisi metanol p.a dan penurunan komposisi asam asetat glasial 2% dapat meningkatkan kemampuan elusi kurkumin dalam penelitian ini. Perbandingan komposisi fase gerak metanol p.a:asam asetat glasial 2% yang digunakan dalam penelitian ini adalah 70:30, 80:20, 90:10, dan 95:5. Nilai indeks polaritas dari masing-masing komposisi fase gerak dapat dilihat pada tabel V.
Tabel V. Nilai indeks polaritas dari masing-masing komposisi fase gerak metanol p.a:asam asetat glasial 2%
No. Komposisi fase gerak Indeks Polaritas metanol p.a asam asetat glasial 2%
1 70 30 6,606
2 80 20 6,104
3 90 10 5,602
4 95 5 5,351
komposisi fase gerak 95:5 bersifat paling nonpolar diantara komposisi fase gerak yang lain.
Metanol digunakan sebagai salah satu campuran fase gerak karena kurkumin larut baik dalam metanol, selain itu metanol mempunyai viskositas yang rendah yaitu 0,54 cP sehingga penggunaan metanol dapat mengurangi tekanan pada kolom dan meningkatkan efisiensi kolom dalam pemisahan kurkumin dalam sampel. Fase gerak metanol dengan asam asetat glasial 2% memiliki sifat lebih polar dibandingkan dengan fase diam oktadesilsilan (C18)
sehingga kromatografi yang digunakan termasuk kromatografi fase terbalik. Asam asetat glasial 2% digunakan sebagai salah satu campuran fase gerak, dimana dengan penambahan beberapa tetes saja tidak akan menyebabkan fase gerak terlalu asam. Apabila fase gerak yang digunakan terlalu asam (pH ≤ 2) dapat mempengaruhi kolom kromatografi. Pada pH ≤ 2, oktadesilsilan akan melepaskan oktadesilnya dan kembali ke bentuk silanol (gambar 14) sehingga akan mempengaruhi kepolaran dari kolom. Berubahnya kepolaran kolom akan mempengaruhi interaksi analit dengan fase diam sehingga berpengaruh pada elusi analit.
Si O Si (CH2)17CH3 Si OH + Cl Si (CH2)17CH3
silanol
H2O / H+
H+
Gambar 14. Reaksi hidrolisis kolom oktadesilsilan
C. Pembuatan Seri Larutan Baku Kurkumin
dikonfirmasi strukturnya dengan metode spektroskopi 1H-NMR dan Mass
Spectra, kurkumin hasil sintesis ini memiliki titik lebur 181,2-182,40C. Maka
baku kurkumin yang digunakan telah terjamin kepastian senyawa dan kemurniannya.
Optimasi metode KCKT ini menggunakan larutan baku kurkumin dengan konsentrasi tertentu sebagai pembanding untuk mengetahui hasil pemisahan kurkumin dalam sampel dan mendeteksi peak yang terdapat dalam sampel OHT Rheumakur® merupakan peak kurkumin. Larutan baku dibuat menggunakan
pelarut metanol p.a yang memiliki kemurnian tinggi (99,85%). Pembuatan konsentrasi baku berdasarkan hasil orientasi karena dalam kemasan produk OHT Rheumakur® tidak dicantumkan kadar dari kurkumin. Larutan seri baku kurkumin
yang digunakan dalam optimasi adalah konsentrasi rendah 1 ppm, konsentrasi tengah 3,5 ppm, dan konsentrasi tinggi 6 ppm. Penggunaan 3 level konsentrasi larutan baku kurkumin ini untuk memastikan respon yang muncul pada tiga level konsentrasi baku kurkumin.
D. Preparasi Sampel
Sampel yang digunakan dalam penelitian ini berupa sediaan semipadat OHT Rheumakur® yang mengandung kurkumin di dalamnya. Komposisi dari
OHT Rheumakur® adalah kurkuminoid dari Curcumae domesticae, minyak atsiri dari Curcumae domesticae, dan minyak atsiri dari Curcumae xanthorizza. Banyaknya campuran senyawa di dalam sampel OHT Rheumakur® maka ekstraksi
pH 4. Penggunaan metanol p.a pH 4 sebagai pelarut dan cairan pengekstraksi karena kurkumin larut dalam metanol dan kurkumin stabil pada pH 4.
Ekstraksi bertujuan untuk meminimalkan campuran senyawa yang terdapat dalam sampel, maka hanya senyawa-senyawa yang larut dalam metanol dan senyawa-senyawa yang memiliki kemiripan dengan metanol yang akan terekstraksi dengan prinsip like disolve like. Metode ekstraksi yang digunakan dalam penelitian ini yaitu maserasi mekanis dengan prinsip pengadukan dengan kecepatan tinggi. Untuk memaksimalkan ekstraksi kurkumin, larutan diekstraksi selama 15 menit.
E. Optimasi Penentuan Panjang Gelombang Maksimal Kurkumin dengan Spektrofotometri Visibel
Penentuan panjang gelombang maksimal bertujuan untuk mengetahui panjang gelombang dimana kurkumin memberikan serapan yang maksimal untuk dapat dibaca oleh sistem detektor KCKT. Analisis dengan KCKT yang dilakukan pada panjang gelombang maksimum akan meningkatkan sensitivitas alat dalam mendeteksi suatu analit. Dalam menentukan λmaks kurkumin, dilakukan scanning
λmaks dengan menggunakan spektrofotometer visibel.
Penentuan λmaks dilakukan dengan menggunakan 3 seri kadar dengan
berada pada rentang panjang gelombang tersebut. Hasil pengukuran panjang gelombang serapan maksimum tersaji gambar 15.
Gambar 15. Spektra serapan kurkumin dengan pelarut campuran metanol p.a dan asam asetat glasial 2% pada pH 4
Menurut Aggarwal (2006) panjang gelombang teoritis dari kurkumin dalam pelarut metanol sebesar 430 nm. Sementara itu, rentang pergeseran panjang gelombang maksimum yang diperbolehkan untuk daerah visibel yaitu 3 nm dari panjang gelombang yang ditentukan (Chan et al., 1995). Berdasarkan data hasil pengukuran panjang gelombang maksimum kurkumin diperoleh hasil panjang gelombang pengukuran yaitu 432 nm dan 433 nm. Dari hasil diketahui bahwa panjang gelombang hasil pengukuran menyimpang tidak lebih dari 3 nm dari panjang gelombang teoritis. Maka panjang gelombang hasil pengukuran dapat dikatakan sesuai dengan panjang gelombang teoritis kurkumin sehingga dapat dipastikan bahwa senyawa tersebut merupakan kurkumin.
Panjang gelombang 432 nm dipilih karena merupakan panjang gelombang maksimum yang paling sering muncul (dari ketiga level konsentrasi, pada konsentrasi rendah dan tinggi menghasilkan λmaks 432 nm).
Syarat suatu senyawa dapat ditetapkan kadarnya secara spektrofotometri visibel yaitu memiliki gugus kromofor, mempunyai auksokrom, dan merupakan senyawa berwarna. Kurkumin memiliki gugus kromofor yang bertanggung jawab dalam penyerapan radiasi sinar. Gugus auksokrom yang dimiliki oleh kurkumin terikat langsung pada gugus kromofor. Gugus auksokrom memiliki peran dalam pergeseran panjang gelombang dan intensitas serapan maksimum dari kurkumin. Gugus kromofor dan auksokrom dari kurkumin ditunjukkan pada gambar 16.
Gambar 16. Gugus kromofor dan auksokrom kurkumin. Keterangan = gugus kromofor, = gugus auksokrom
F. Optimasi Fase Gerak
Sistem kromatografi yang digunakan dalam penelitian ini merupakan kromatografi partisi fase terbalik dengan menggunakan fase gerak campuran metanol p.a dan asam asetat glasial 2% yang sifatnya lebih polar dari fase diam oktadesilsilan yang digunakan.
dalam alat KCKT untuk mendapatkan kepolaran yang diinginkan. Kepolaran fase gerak diatur dengan mengubah-ubah komposisi fase gerak.
Fase gerak yang dioptimasi yaitu metanol dan asam asetat glasial 2% dengan berbagai perbandingan komposisi yaitu 70 : 30; 80 : 20; 90 : 10; dan 95 : 5. Fase gerak terlebih dahulu disaring dengan penyaring Whatman uantuk menyaring partikel yang dapat menyumbat kolom. Fase gerak lalu dideggasing dengan menggunakan ultrasonikator untuk menghilangkan gelembung yang dapat mengganggu pemisahan sampel.
Pada proses optimasi fase gerak digunakan sampel yang telah dipreparasi dengan tujuan agar hasil optimasi ini dapat langsung diaplikasikan pada penetapan kadar sampel karena kandungan dalam sampel tidak hanya kurkumin saja tetapi terdapat senyawa lain seperti bahan pengisi dan lubrikan. Dalam proses ekstraksi sampel yang dilakukan, terdapat kemungkinan bahan-bahan lain tersebut ikut terekstraksi karena memiliki kelarutan yang hampir sama seperti kurkumin sehingga akan menyebabkan peak kurkumin mengalami overlapping (tidak terpisah). Oleh karena itu optimasi perlu dilakukannya dengan menghitung nilai resolusi dari kurkumin. Selain dari nilai resolusi, dilihat pula nilai HETP, waktu retensi, dan bentuk peak dari kromatogram yang dihasilkan.
kecepatan alir akan meningkatkan tekanan pompa, sehingga apabila tekanan pompa lebih dari 380 kPa dapat menyebabkan kerusakan kolom.
Tabel VI. Tekanan kolom (kgf/cm2=kPa)
Kecepatan alir Komp.
fase gerak * 0,5 ml/menit 1,0 ml/menit 1,5 ml/menit
70:30 85 137 233
80:20 74 157 199
90:10 62 80 166
95:5 49 87 120
* Komposisi fase gerak metanol p.a:asam asetat glasial 2%
Hasil pemisahan kurkumin dalam sampel OHT Rheumakur® dengan
Berdasarkan tabel VII dapat diketahui bahwa pada baku kurkumin hanya terdapat 1 peak, sedangkan dalam sampel terdapat 2–4 peak. Hal ini menunjukkan bahwa dalam baku hanya terdapat senyawa murni, sedangkan dalam sampel terdapat senyawa yang lain selain kurkumin. Untuk membuktikan bahwa peak yang terdapat sampel OHT Rheumakur® benar merupakan peak kurkumin maka dilakukan pengamatan waktu retensi sampel dibandingkan dengan waktu retensi baku kurkumin. Pada tabel VII dapat dilihat bahwa waktu retensi yang dimiliki oleh sampel OHT Rheumakur® mirip dengan waktu retensi pada baku kurkumin.
Dengan demikian peak tersebut benar merupakan peak kurkumin.
Untuk memperjelas penjelasan diatas, akan dibahas satu persatu komposisi fase gerak yang digunakan dalam penelitian ini.
1. Fase gerak metanol p.a: asam asetat glasial 2% dengan perbandingan 70 : 30
Gambar 17. A = baku kurkumin 3,5 ppm; B=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 70:30 kecepatan alir 0,5 ml/menit
Gambar 18. C = baku kurkumin 3,5 ppm; D=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 70:30 kecepatan alir 1,0 ml/menit
D
B
Gambar 19. E = baku kurkumin 3,5 ppm; F=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 70:30 kecepatan alir 1,5 ml/menit Pada gambar 17, 18, dan 19 dapat dilihat bahwa bentuk peak senyawa kurkumin dalam sampel OHT Rheumakur® memiliki profil yang sama dengan
peak baku kurkumin pada komposisi fase gerak metanol p.a:asam asetat glasial 2% (70:30) kecepatan alir 0,5; 1,0; dan 1,5 ml/menit. Profil yang sama ini menunjukkan bahwa peak yang terdapat dalam sampel OHT Rheumakur® benar merupakan peak kurkumin.
Penggunaan fase gerak metanol p.a:asam asetat glasial 2% 70:30 dengan kecepatan alir 0,5 ml/menit belum menghasilkan pemisahan yang optimal. Hal ini
dapat dilihat dari peak yang dihasilkan tidak simetri dengan nilai AF sebesar 1,833 (tabel VII). Selain itu, waktu yang dibutuhkan untuk elusi kurkumin tidak efisien, dimana dibutuhkan waktu mencapai 15,970 menit. Waktu retensi yang diharapkan dalam analisis dengan metode KCKT yaitu kurang dari 10 menit (Snyder et al., 1997).
Pada penggunaan fase gerak metanol p.a:asam asetat glasial 2% 70:30 dengan kecepatan alir 1,0 dan 1,5 ml/menit (gambar 18D dan 19F) diperoleh pemisahan kurkumin yang belum optimal pula. Walaupun waktu retensi peak kurkumin pada kecepatan alir 1,0 dan 1,5 ml/menit kurang dari 10 menit yaitu berturut-turut 7,960 menit dan 5,444 menit, tetapi peak yang dihasilkan asimetri dengan nilai AF sebesar 2,400 pada kecepatan alir 1,0 ml/menit dan 3,249 pada kecepatan alir 1,5 ml/menit.
terelusi sedikit demi sedikit sehingga peak yang dihasilkan landai dan mengalami tailing.
2. Fase gerak metanol p.a: asam asetat glasial 2% dengan perbandingan 80 : 20 Optimasi ini dilakukan dengan menggunakan fase gerak metanol p.a: asam asetat glasial 2% dengan perbandingan 80:20. Pada fase gerak ini jumlah metanol yang digunakan ditambah untuk meningkatkan eluent strength dari fase gerak. Peningkatan eluent strength diharapkan dapat meningkatkan kemampuan fase gerak untuk mengelusi dan memutus ikatan analit dengan fase diam sehingga diharapkan elusi dapat terjadi serempak dan peak yang dihasilkan simetris.
Gambar 20. A = baku kurkumin 3,5 ppm; B=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 0,5 ml/menit
Gambar 21. C = baku kurkumin 3,5 ppm; D=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 1,0 ml/menit
D
C
Gambar 22. E = baku kurkumin 3,5 ppm; F=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 80:20 kecepatan alir 1,5 ml/menit Pada gambar 20, 21, dan 22 dapat dilihat bahwa bentuk peak senyawa kurkumin dalam sampel OHT Rheumakur® memiliki profil yang sama dengan
peak baku kurkumin pada komposisi fase gerak metanol p.a:asam asetat glasial 2% (80:20) kecepatan alir 0,5; 1,0; dan 1,5 ml/menit. Profil yang sama ini menunjukkan bahwa peak yang terdapat dalam sampel OHT Rheumakur® benar merupakan peak kurkumin.
Pada gambar 20B dapat dilihat bahwa penggunaan fase gerak metanol p.a:asam asetat glasial 2% 80:20 dengan kecepatan alir 0,5 ml/menit belum menghasilkan pemisahan yang optimal dengan bentuk peak yang dihasilkan tidak ramping, lebar, dan asimetri dengan nilai AF sebesar 1,125 (tabel VII). Waktu elusi yang dibutuhkan sudah memenuhi syarat waktu retensi yang diharapkan kurang dari 10 menit yaitu 8,197 menit. Pada penggunaan fase gerak metanol p.a:asam asetat glasial 2% 80:20 dengan kecepatan alir 1,0 dan 1,5 ml/menit (gambar 21D dan 22F) diperoleh pemisahan kurkumin yang belum optimal pula. Waktu retensi peak kurkumin pada kecepatan alir 1,0 dan 1,5 ml/menit yaitu
berturut-turut 4,141 menit dan 2,844 menit, tetapi peak yang dihasilkan asimetri dengan nilai AF sebesar 1,636 pada kecepatan alir 1,0 ml/menit dan 1,500 pada kecepatan alir 1,5 ml/menit.
Dari hasil yang ditunjukkan pada tabel VIII dan gambar 20, 21, dan 22 dapat disimpulkan bahwa penggunaan fase gerak metanol p.a:asam asetat glasial 2% dengan perbandingan 80:20 belum dapat menghasilkan pemisahan yang optimal dengan bentuk peak kurkumin yang dihasilkan asimetri pada tiap kecepatan alir 0,5 hingga 1,5 ml/menit. Peak asimetri yang terjadi disebabkan oleh interaksi kurkumin yang terlalu kuat terhadap fase diam. Perbandingan komposisi fase gerak metanol p.a:asam asetat glasial 2% dengan perbandingan 80:20 yang digunakan tidak cukup kuat untuk mengelusi kurkumin keluar dari kolom secara serempak.
3. Fase gerak metanol p.a: asam asetat glasial 2% dengan perbandingan 90 : 10 Pada fase gerak ini jumlah metanol yang digunakan ditambah dari fase gerak yang telah dioptimasi sebelumnya, dengan demikian kemampuan mengelusi fase gerak ini lebih besar dari fase gerak sebelumnya.
Gambar 23. A = baku kurkumin 3,5 ppm; B=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 0,5 ml/menit
Gambar 24. C = baku kurkumin 3,5 ppm; D=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 1,0 ml/menit
D
B
Gambar 25. E = baku kurkumin 3,5 ppm; F=sampel OHT Rheumakur® pada fase
gerak metanol p.a : asam asetat glasial 2% 90:10 kecepatan alir 1,5 ml/menit Pada gambar 23, 24, dan 25 dapat dilihat bahwa bentuk peak senyawa kurkumin dalam sampel OHT Rheumakur® memiliki profil yang sama dengan
peak baku kurkumin pada komposisi fase gerak metanol p.a:asam asetat glasial 2% (90:10) kecepatan alir 0,5; 1,0; dan 1,5 ml/menit. Profil yang sama ini menunjukkan bahwa peak yang terdapat dalam sampel OHT Rheumakur® benar
merupakan peak kurkumin.
Pada gambar 23B dapat dilihat bahwa penggunaan fase gerak metanol p.a:asam asetat glasial 2% 90:10 dengan kecepatan alir 0,5 ml/menit belum menghasilkan pemisahan yang optimal dengan bentuk peak mengalami fronting,