BAB II
TINJAUAN PUSTAKA
2. 1 Minuman Berenergi
Minuman berenergi termasuk salah satu suplemen makanan yang terdiri dari komponen multivitamin, makronutrien (karbohidrat, protein), taurin dengan atau tanpa kafein dan biasanya ditambahkan herbal seperti ginseng, jahe dan sebagainya dengan bentuk sediaan COD(cairan obat dalam) dalam kemasan botol bervolume 150 mL, 250 mL atau serbuk dan tablet yang dilarutkan menjadi minuman, yang dalam setiap kemasannya mengandung energi minimal 100 Kkal, serta indikasinya adalah untuk menambah tenaga kesegaran, stimulasi metabolisme, memelihara kesehatan dan stamina tubuh, yang diminum pada saat bekerja keras atau setelah berolah raga (BPOM, 2006). Kandungan minuman berenergi dapat dilihat pada Tabel 1.1.
Tabel 1.1.Kandungan Minuman Berenergi
Zat Kandungan Efek terhadap Tubuh
Kafein
Stimulasi sistem saraf pusat sehingga memberi efek alert. Meningkatkan denyut jantung dan tekanan darah. Menyebabkan dehidrasi tubuh.
Taurin Meregulasi denyut jantung, kontraksi otot, dan tingkat energi. Merupakan inhibitor neurotransmitter yang ringan.
Vitamin B Membantu mengkonversikan makanan menjadi energi dalam tubuh.
Ginseng
Meningkatkan energi, mempunya komponen anti-lelah, melegakan stres, dan menguatkan ingatan. Menstimulasi hipotalamus dan hormon pitutari untuk mensekresi ACTH. Ginkgo Biloba Membantu daya ingat, konsentrasi, sirkulasi darah dan
Gula Sumber metabolisme karbohidrat untuk memberikan energi dalam tubuh.
Antioksidan Mengurangi adanya radikal bebas. Kreatin Menyipan energi dalam otot. (Babu, et. al., 2008)
Minuman berenergi dibuat untuk memberikan suatu hentakan energi yang diakibatkan oleh adanya kombinasi stimulan dan penambahan energi yang diberikan. Kafein diketahui sebagai senyawa utama yang bertanggung jawab terhadap efek ini. Begitupun, tubuh manusia tidak memiliki kebutuhan akan kafein, meskipun dosis rendah kafein dapat merubah penampilan kognitif dan mood (Malinauskas, et. al., 2007).
2. 2 Uraian Bahan 2. 2. 1 Natrium Benzoat
Asam benzoat adalah salah satu dari pengawet kimia tertua yang digunakan pada industri kosmetik, obat, dan makanan. Natrium benzoat adalah pengawet kimia pertama yang diperbolehkan penggunaannya dalam makanan oleh FDA (Food and Drug Administration) Amerika Serikat. Keuntungan penggunaan asam benzoat dan garamnya adalah harganya yang murah, mudah dibuat, tidak berwarna, dan toksisitasnya relatif rendah sehingga asam benzoat menjadi salah satu pengawet yang paling banyak digunakan secara luas di dunia (Davidson, et. al., 2005).
Menurut Ditjen POM (1995), rumus struktur dari natrium benzoatadalah :
Menurut Ditjen POM (1995), rumus molekul natrium benzoat adalah C6H5NaO2, dengan berat molekul 144,12. Kandungan dari natrium benzoat tidak kurang dari 99,5% dan tidak lebih dari100,5% C7H5NaO2
Pengawet adalah bahan tambahan makanan yang mencegah atau menghambat fermentasi, pengasaman atau peruraian lain terhadap makanan yang disebabkan oleh mikroorganisme (BSN, 1995). Zat pengawet organik lebih banyak digunakan daripada zat pengawet anorganik karena bahan ini lebih mudah larut. Bahan organik yang digunakan baik dalam bentuk asam maupun dalam bentuk garamnya (Cahyadi, 2008).
dihitung terhadap zatanhidrat. Pemeriannya yaitu granul atau serbuk hablur; putih; tidak berbauatau praktis tidak berbau; stabil di udara. Natrium benzoat mudah larut dalam air; agak sukar larut dalametanol, dan lebih mudah larut dalam etanol 96%.
Fungsi pengawet adalah untuk memperpanjang masa simpan suatu makanan. Sebagian besar kerusakan bahan makanan, khususnya hasil olahan, disebabkan oleh aktivitas mikroba yang memanfaatkan bahan makanan untuk metabolismenya. Bahan pengawet bersifat menghambat atau mematikan pertumbuhan mikroba penyebab kerusakan ini sehingga sering juga disebut dengan senyawa antimikroba. Namun demikian, penggunaan bahan pengawet tidak selalu menguntungkan, terutama apabila digunakan dalam jumlah yang berlebihan, karena bisa mengganggu kesehatan (Saparinto dan Diana, 2006).
memiliki sifat antimikroba, sedangkan sifat toksik dari natrium benzoat merupakan hasil dari molekul asam benzoat yang tidak terdisosiasi. Oleh karena jumlah dari asam yang tidak terdisosiasi berkurang seiring dengan meningkatnya pH, maka penggunaan asam benzoat atau natrium benzoat sebagai bahan pengawet makanan harus dibatasi untuk produk-produk yang memang sudah asam secara alami (Davidson, et. al., 2005).
Natrium benzoat merupakan hasil turunan asam benzoat penting yang diperoleh dari netralisasi asam benzoat dengan penambahan larutan natrium hidroksida atau natrium bikarbonat. Kalsium benzoat, kalsium benzoat, dan garam-garam benzoat lainnya juga diproduksi. Asam benzoat dan natrium benzoat (C6H5
Benzoat membutuhkan pH dibawah 4,5 supaya efektif dan bekerja lebih baik seiring dengan penurunan pH. Garam-garam benzoat juga terbentuk secara alami pada beberapa buah dan jusnya. Pada awal tahun 1990-an, FDA (Food and Drug Administration) menemukan bahwa benzoat dan asam askorbat dalam
minuman, dengan kondisi tertentu, dapat bereaksi dan menghasilkan benzen yang bersifat karsinogenik. Pada tahun 2005, FDA menemukan beberapa minuman mengalami kenaikan (> 5 parts per billion) kadar benzen (Myers, 2007).
COONa) digunakan sebagai bahan tambahan makanan dan ditambahkan ke dalam makanan, jus, dan minuman yang mengandung asam. Walaupun asam benzoat memiliki sifat antimikroba yang lebih baik daripada garamnya, natrium benzoat sekitar 200 kali lebih larut dalam air, sehingga natrium benzoat lebih sering dipilih untuk menjadi bahan pengawet(Myers, 2007).
Vitamin B6 merupakan vitamin larut air yang menembus melewati tubuh lebih cepat dari vitamin lipofil melalui sirkulasi aliran darah dan diekskresi dalm urin (Sather dan Teresa, 2011). Vitamin B6 berhubungan luas dengan metabolisme asam amino dan senyawa lain yang mengandung nitrogen, serta metabolisme lemak dan aktivitas hormon tertentu. Piridoksin, sebagaimana piridoksal fosfat, memiliki fungsi penting dalam perubahan triptofan menjadi asam nikotinat. Peningkatan konsumsi protein juga menyebabkan kenaikan kebutuhan piridoksin. Baik defisiensi ataupun kelebihan piridoksin dapat menyebabkan gangguan saraf (Hathcock, 2014).
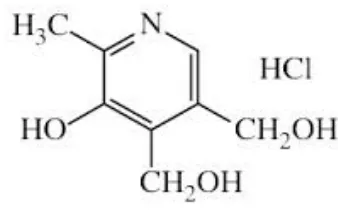
Menurut Ditjen POM (1995), rumus struktur vitamin B6 :
Gambar 2. Vitamin B6 (Piridoksin HCl)
Meurut Ditjen POM (1995), rumus molekul vitamin B6 adalah C8H11NO3.HCl dengan berat molekul 205,64. Kandungannya tidak kurang dari 98,0% dan tidak lebih dari 102,0% C8H11NO3
(piridoksal) dan PM (piridoksamin). Dan sebagai tambahan, terdapat juga tiga bentuk ester 5’-fosfat. Bentuk vitamin B6 yang paling stabil adalah piridoksal dan bentuk ini digunakan untuk fortifikasi vitamin pada makanan (Theobald dan Anklam, 1996).
Vitamin B6 yang terdapat dalam pil multivitamin dan minuman berenergi biasanya dalam bentuk piridoksin. Piridoksin merupakan kofaktor beberapa enzim sebagai katalis dekarboksilasi, transaminasi dan raseminasi dari asam amino dalam beberapa tubuh manusia. Manusia harus mendapatkan vitamin B6 dari konsumsi nutrien (Sather dan Teresa, 2011).
Sumber vitamin untuk piridoksin adalah dari daging, hati, ginjal, otak, telur, ragi, gandum dan sayuran. Pada daging dan ikan, ester fosfat dari PN (piridoksin) dan PL (piridoksal) merupakan vitamer yang mendominasi, sedangkan PN (piridoksin) sendiri adalah bentuk utama yang terdapat dalam sereal, buah, dan sayur-sayuran (Theobald dan Anklam, 1996).
2.3 Spektofotometri
Pada analisis spektrofotometri, sumber radiasi yang digunakan membentang menjadi spektrum daerah ultraviolet. Panjang gelombang radiasi tertentu dipilih yang memiliki lebar pita kurang dari 1 nm. Alat yang digunakan disebut spektrofotometer. Suatu spektrofotometer optik merupakan alat yang memiliki sistem optik yang dapat menghasilkan dispersi dari radiasi elektromagnetik yang diberikan, dan dimana pengukuran dapat dilakukan dari jumlah radiasi yang ditransmisi pada panjang gelombang tertentu di rentang spektrum. Ketika cahaya (monokromatik atau heterogen) mengenai medium homogen, suatu bagian dari cahaya yang ada dipantulkan, sebagian diserap medium, dan sisanya ditransmisikan atau diteruskan (Jeffery, et. al., 1989).
Radiasi pada rentang panjang gelombang (λ) 200 – 700 nm dilewatkan melalui suatu larutan senyawa. Elektron-elektron pada ikatan di dalam molekul menjadi terkesitasi sehingga menempati keadaan kuantum yang lebih tinggi dan dalam proses menyerap sejumlah energi yang melewati larutan tersebut. Semakin longgar elektron tersebut ditahan dalam ikatan molekul, semakin panjang gelombang (energi lebih rendah) radiasi yang diserap (Watson, 2010).
Radiasi di daerah UV/visibel diserap melalui eksitasi elektron-elektron yang terlibat dalam ikatan-ikatan antara atom-atom pembentuk molekul sehingga awan elektron menahan atom-atom bersama-sama mendistribusikan kembali atom-atom itu sendiri dan orbital yang ditempati oleh elektron-elektron pengikat tidak lagi bertumpang tindih (Watson, 2010).
Metode-metode ini biasanya berdasarkan pada penggunaan nilai A (1%, 1cm) standar untuk bahan aktif yang sedang diuji dan ini mengandalkan spektrofotometer UV yang dikalibrasi secara akurat. Metode tersebut juga diperkirakan bahwa tidak ada interfensi dari eksipien yang dapat menyebabkan penghamburan cahaya (Watson, 2010).
Menurut Jeffery, et. al. (1989), gelombang elektromagnetik biasanya dijelaskan dengan ( a ) panjang gelombang λ (jarak antara puncak gelombang dalam cm, kecuali dinyatakan lain), ( b ) nilai gelombang ῦ (nilai gelombang per cm), dan ( c ) frekuensi υ (nilai gelombang per detik). Jika ketiganya dikaitkan, maka akan menjadi seperti berikut:
1
������� ��������� = nilai gelombang =
��������� ��������� ��ℎ���
1
�
=
ῦ
=
� �2.3.1 Hukum Lambert-Beer
Hukum ini menyatakan bahwa ketika cahaya monokromatik menembus melewati medium, kecepatan penurunan intensitas terhadap ketebalan medium sebanding dengan intensitas cahaya. Hal ini setara dengan pernyataan bahwa intensitas pancaran cahaya berkurang secara eksponen, atau bahwa lapisan medium dengan ketebalan apapun menyerap fraksi yang sama dari cahaya yang mengenainya (Jeffery, et. al., 1989).
Pengukuran serapan cahaya oleh larutan molekul diatur dengan hukum Lambert-Beer ini, yang ditulis sebagai berikut :
Dengan I0 adalah intensitas radiasi yang masuk; It adalah intensitas radiasi yang ditransmisikan; A dikenal sebagai absorban dan merupakan ukuran jumlah cahaya
yang diserap oleh sampel; ε adalah tetapan yang dikenal sebagai koefisien
punahan molar dan merupakan absorban larutan 1 M analit tersebut; b adalah panjang jalur sel dalam cm, biasanya 1 cm; dan c adalah konsentrasi analit dalam mol per liter (Watson, 2010).
2.3.2 Kegunaan Spektofotometri
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk dilakukan (Satiadarma, dkk., 2004).
Metode spektrofotometri memiliki beberapa keuntungan antara lain kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1991). Akan tetapi, jika digabung dengan cara lain seperti spektroskopi inframerah, resonansi magnet inti dan spektroskopi massa, maka dapat digunakan untuk identifikasi atau analisis kualitatif senyawa tersebut (Gandjar dan Rohman, 2007).
sebanding dengan banyaknya molekul yang mengabsorpsi radiasi dan merupakan dasar analisis kuantiatif. Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet penggunaanya cukup luas (Satiadarma, dkk., 2004).
Menurut Dachriyanus (2004), pada umumnya spektrofotometri UV dalam analisis senyawa organik digunakan untuk:
1. Menentukan jenis kromofor, ikatan rangkap yang terkonjugasi dan auksokrom dari senyawa organik
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang maksimum suatu senyawa
3. Mampu menganalisis senyawa organik secara kuantitatif dengan menggunakan hukum Lambert-Beer
2.4 Spektrofotometri Derivatif
Spektrofotometri derivatif merupakan suatu metode analisis dengan kegunaan besar untuk mendapatkan informasi kualitatif dan kuantitatif dari spektrum yang diturunkankan dari spektrum orde nol (Rojas, et. al., 1988).
Sensitivitas dari metode spektrofotomeri UV/visibel dapat ditingkatkan jika teknik spektrofotometri derivatif digunakan (Jeffery, et. al., 1989). Peningkatan selektivitas ini merupakan hasil dari fakta bahwa diferensasi meemberikan informasi lebih banyak dari yang terdapat dalam spektrum serapan dasar (Kus, et. al., 1996). Spektrum derivatif dapat digunakan untuk menjelaskan pita-pita serapan dalam spektrum UV yang lebih kompleks. Efek utama derivatisasi adalah menghilangkan dasar pita-pita serapan luas yang hanya terdapat perubahan bertahap pada kemiringannya(Watson, 2010).
Derivatisasi spektrum orde nol dapat mengarahkan kepada pemisahan sinyal yang tumpang tindih dan pengeliminasian background pengganggu yang disebabkan adanya campuran senyawa lain dalam sampel. Ini menunjukan sifatnya yang dapat melakukan pengukuran atas satu atau lebih analit tanpa memerlukan pemisahan dan pemurnian terlebih dahulu (Patel, et. al., 2010).
Menurut Patel, et. al. (2010), Pengaplikasian spektrofotometri dapat dipisahkan menjadi tiga cara. Pertama adalah analisis multikomponen, dimana ini merupakanaplikasi spektrofotometri derivatif yang paling sering digunakan. Metode ini dapat menentukan satu atau lebih analit yang berada dalam matriks rumit. Cara kedua yaitu penentuan persamaan reaksi dan perhitungan konstanta fisikokimia, misalnya konstanta kompleksasi atau pengikatan. Dan terakhir adalah dengan penelusuran reaksi kinetik.
Menurut Owen (1995), spektrum derivatif dapat diperoleh dengan metode optik, elektronik, dan matematika.
dimodulasi menjadi panjang gelombang dengan rentang sempit dengan alat elektromekanik. Derivat pertama dan kedua dapat diperoleh menggunakan metode ini.
b. Metode matematika. Pertama, dilakukan digitalisasi terhadap spektrum dengan interval sampling Δλ. Ukuran Δλ tergantung pada lebar pita alami / natural bandwidth (NBW) dari pita yang sedang diproses dan dari lebar pita
yang digunakan alat untuk menghasilkan data. Untuk Spektrum UV/visibel, NBW biasanya sekitar 10 smpai 50 nm. Spektrum derivat pertama dapat dihitung dengan mengambil perbedaan absorbansi antara dua panjang gelombang yang jaraknya dekat untuk keseluruhan panjang gelombang:
�λ+∆λ/2 =
(�λ+∆λ− �λ) ∆λ
Dimana amplitudo derivatif, Dλ
�λ = (�λ −∆λ−2∆λ�λ2+�λ+∆λ)
, dihitung untuk panjang gelombang pertengahan antara dua absorbansi panjang gelombang.Untuk derivatif kedua ditentukan tiga absorbansi panjang gelombang yang jaraknya berdekatan dan menggunakan rumus ini :
Menurut Owen (1995), jika asumsinya adalah spektrum orde nol mematuhi hukum Lambert-Beer, maka adanya hubungan linear yang serupa antara konsentrasi dan amplitudo untuk semua orde derivatif:
Untuk komponen tunggal, pemilihan panjang gelombang tidak semudah pemilihan pada spektrum serapan karena akan ada dua puncak, positif dan negatif. Untuk derivatif orde genap terdapat satu puncak maksimum atau minimum yang
berada pada λmax yang sama dengan spektrum serapan, namun untuk spektrum derivat ganjil panjang gelombangnya adalah pada zero crossing (Owen, 1995).
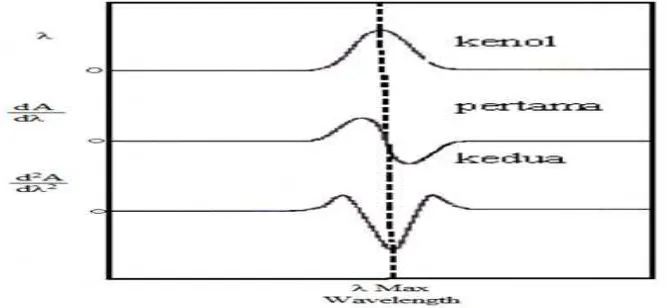
Menurut Owen (1995), spektrum derivat orde nol sampai derivat kedua dapat dilihat pada gambar 3.
Gambar 3. Spektrum derivat orde nol sampai derivat kedua
Spektrofotometri derivatif menemukan pengaplikasian yang luas dalam analisis sampel multikomponen. Teknik ini didasarkan pada penggunaan spektrum derivatif yang dihasilkan dari derivatisasian spektrum orde nol. Spektrum serivatif yang dihasilkan memberikan informasi yang lebih banyak daripada spektrum awalnya: puncak maksima dan minima baru muncul dan juga terdapat titik dimana spektrum melewati sumbu X-axis. Spektrofotometri derivatif tetap memakai semua hukum klasik seperti, keterikatan antara nilai derivatif dan konsentrasi analit juga dengan hukum adisi (Kus,et. al., 1996).
1. Graphic Measurement, 2. Numeric Measurement, 3. Zero Crossing,
4. Peak-to-peak, 5. Baseline-to-peak.
2. 4. 1 Teknik Zero Crossing
Zero crossing adalah prosedur yang paling umum untuk menentukan
campuran biner yang spektranya saling tumpang tindih secara simultan. Metode zero crossing dapat digunakan pada derivatif pertama dan kedua (Nurhidayati,
2007).Teknik zero crossing adalah cara pengukuan nilai derivatif pada panjang gelombang dimana derivatif dari komponen yang diukur berada pada nilai nol. Pada saat ini komponen lain tidak memberikan serapan yang mengganggu serapan senyawa pasangannya. Zero crossing bisa mengeliminasi pengaruh dari komponenlain yang mengganggu. Namun kekurangan metode ini adalah pengukurannya menjadi tidak terlalu cermat (Kus,et.al., 1996).
2. 4. 2 Keuntungan dan Kerugian Spektrofotometri Derivatif
Menurut Nurhidayati (2007), keuntungan penggunaan metode spektrofotometri derivatif antara lain :
1. Memberikan gambaran struktur yang terinci dari spektrum serapan dan semakin jelas seiring kenaikan orde,
2. Analisis komponen dalam campuran dengan bahan yang panjang gelombangnya berdekatan,
4. Biaya operasional lebih murah dan waktu analisisnya lebih cepat.
Adapun kerugian dalam penggunaan metode spektrofotometri derivatif yaitu adanya signal-to-noise ratio (S/N ratio) yang semakin rendah dengan meningkatnya orde. Terdeteksinya puncak serapan pada derivatif yang lebih tinggi ditentukan oleh S/N spektrum asal. Yang penting adalahmenghilangkan atau meminimalkan noise tanpa mengurangi sinyal penting. Perlu pendekatan matematika untuk memuluskan sebelum atau selama proses derivatisasi berlangsung (Nurhidayati, 2007).
2.5 Validasi Metode Analisis
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur analitik telah sesuai dengan penggunaan yang dikehendaki. Validasi merupakan persyaratan mendasar yang diperlukan untuk menjamin kualitas dan hasil dari semua aplikasi analitik (Ermer dan McB. Miller, 2005). Menurut USPNF (2007), karakteristik validasi metode yaitu meliput i akurasi/kecermatan, presisi/keseksamaan, spesifisitas, batas deteksi, batas kuantitasi, linieritas, rentang dan kekuatan/ketahanan.
2.5.1 Akurasi
Akurasi adalah kedekatan antara nilai hasil uji yang diperoleh melalui metode analitik dengan nilai sebenarnya. Akurasi dinyatakan dalam persen perolehan kembali (% recovery). Akurasi dapat ditentukan dengan dua metode, yakni spiked – placebo recovery dan standard addition method. Pada spiked – placebo recovery atau metode simulasi, analit murni ditambahkan (spiked) ke
dianalisis dan jumlah analit hasil analisis dibandingkan dengan jumlah analit teoritis yang diharapkan. Metode ini dinamakan standard addition method atau metode penambahan baku (Harmita, 2004).
2.5.2 Presisi
Berdasarkan rekomendasi International Conference on the Harmonisation (ICH), karakteristik presisi dilakukan pada tiga tingkatan, yakni keterulangan (repeatability), presisi antara (intermediate precision) dan reprodusibilitas (reproducibility). Keterulangan dilakukan dengan cara menganalisis sampel yang sama oleh analis yang sama menggunakan instrument yang sama dalam periode waktu singkat. Presisi antara dikerjakan oleh analis yang berbeda. Sedangkan reprodusibilitas dikerjakan oleh analis yang berbeda dan di laboratorium yang berbeda (Harmita, 2004).
2.5.3 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas kuantitasi adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan (Harmita, 2004).
2.5.4 Linearitas
tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya diproses untuk selanjutnya dapat ditentukan nilai kemiringan (slope), intersep dan koefisien korelasinya (Gandjar dan Rohman, 2007).
BAB III
METODOLOGI PENELITIAN
3. 1 Jenis Penelitian
Penelitian ini merupakan penelitian eksperimental, yaitu metode penelitian yang digunakan untuk mencari pengaruh perlakuan tertentu terhadap yang lain dalam kondisi yang terkendali. Ini merupakan jenis penelitian terbaik dalam pengujian hipotesis hubungan kausalitas.
3. 2 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian, Fakultas Farmasi, Universitas Sumatera Utara, Medan, mulai dari bulan Maret sampai Juni 2014.