LAPORAN RESMI PRAKTIKUM BIOKIMIA Isolasi DNA Ephitelial Mulut
Disusun Oleh:
Celyta Nirmala Putri Talia PKB 2022
22030194045
PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SURABAYA
2023
A. Judul Percobaan
Isolasi DNA Ephitelial Mulut B. Hari/Tanggal Percobaan
Kamis/23 November 2023 C. Selesai Percobaan
Pukul 13.00-15.30 D. Tujuan Percobaan
Mampu mengerjakan isolasi DNA sesuai prosedur, dengan sampel DNA diambil dari sel ephitelial mulut
E. Dasar Teori 1. DNA
Didalam inti sel suatu organisme, terdapat materi genetic. Materi genetic ini harus mempunyai kemampuan untuk mengkode suatu informasi secara spesifik dan menggandakan suatu informasi secara tepat. Contoh dari materi genetic adalah DNA/RNA, gen dan kromosom. Pada dasarnya sel mengandung dua asam nukleat, yaitu RNA dan DNA. Genom adalah keseluruhan materi genetik yang terdapat dalam suatu organisme. Genom pada semua sel adalah DNA, sedangkan pada virus genom dapat berupa DNA atau RNA. Umumnya istilah genom mengacu pada semua informasi genetic suatu organisme, termasuk semua DNA yang membentuk gen yang terkandung dalam kromosom. DNA yang dijumpai di nukleus disebut DNA kromosomal (DNA genom), DNA lain yang terdapat dalam sel di luar nukleus yaitu DNA mitokondria, DNA kloroplas, dan DNA plasmid, ketiganya disebut DNA ekstrakromosomal (ekstra genom). Fungsi dari genom adalah membawa materi hereditas yaitu materi yanga akan diwariskan generasi berikutnya dan mengatur metabolisme melalui proses sintesis protein. Komponen utama kromosom pada eukaryotik adalah molekul DNA dan protein histon. Protein histon ini bersifat basa, sehingga dapat menetralkan sifat asam dari DNA (Nurhayati, B, 2017).
Deoxyribonucleic acid (DNA) adalah polimer asam nukleat yang tersusun secara sistematis dan merupakan pembawa informasi genetik yang diturunkan kepada keturunannya. Informasi genetik disusun dalam bentuk
kodon yang berupa tiga pasang basa nukelotida. DNA pada makhluk hidup dapat ditemukan pada inti sel (nukleus), mitokondria, dan klorofil. Pada manusia, DNA ditemukan pada inti sel dan mitokondria. DNA pada nukleus berbentuk linear dan memiliki jumlah pasang basa sekitar tiga milyar, sedangkan DNA yang berada di mitokondria (mtDNA) berbentuk sirkuler dan memiliki jumlah pasang basa lebih sedikit yaitu sekitar 160.000.
Namun, apabila terjadi mutasi pada DNA mitokondria, dapat terjadi kerusakan pada sistem yang peka terhadap kebutuhan energi seperti sistem saraf dan otot. DNA diibaratkan sebagai otak yang dapat mengatur segala proses di dalam tubuh. Di samping itu, DNA juga mempunyai peran penting dalam pewarisan sifat. DNA merupakan suatu senyawa kimia yang penting pada makhluk hidup. Tugas utamanya membawa materi genetik dari suatu generasi ke generasi berikutnya. DNA juga merupakan senyawa polinukleotida yang membawa sifat-sifat keturunan yang khas pada kromosom. DNA penting dalam hal hereditas. Paket semua informasi genetik dan dibagikan pada generasi berikutnya. Dasar untuk ini terletak pada kenyataan bahwa DNA membuat gen dan gen membuat kromosom.
Manusia memiliki 23 pasang kromosom – total 46 kromosom. Dua puluh dua dari pasangan ini, yang disebut autosom, terlihat sama pada laki-laki dan perempuan. Ke 23 pasangan disebut kromosom seks dan berbeda antara pria dan wanita. Wanita memiliki dua salinan dari kromosom X atau XX, sedangkan pria memiliki satu X dan satu kromosom Y. Untai DNA tersusun dari rangkaian nukleotida yang terhubung melalui ikatan fosfodiester yang terbentuk diantara gula pentosa dan gugus fosfat. Sedangkan, untai ganda DNA terhubung melalui ikatan hidrogen yang terbentuk diantara pasangan basa nitrogen. Pasangan basa nitrogen pada DNA meliputi adenin dan timin (dua ikatan hidrogen) serta guanin dan sitosin (tiga ikatan hidrogen) (Wahyudiati, D, 2017).
2. Enzim Pada Isolasi DNA
Berikut ini merupakan beberapa enzim yang terdapat dan terlibat dalam DNA:
a. Enzim Nuklease
Asam nukleat baik DNA maupun RNA mampu dipotong dengan menggunakan suatu enzim yaitu nuklease. Enzim nuklease yang mampu memotong RNA disebut ribonuklease atau Rnase, sementara enzim yang mampu memotong DNA disebut deoksiribonuklease atau Dnase. Beberapa nuklease hanya memotong urutan asam nukleat yang single strand dan apa pula yang mampu memotong asam nukleat yang double strand. Nuklease ada dua macam yakni eksonuklease yang mampu memotong molekul asam nukleat single strand atau beberapa oligonukleotida pendek yang hanya mengenali salah satu ujung asam nukleat, yaitu ujung 5′ atau ujung 3′;
sementara endonuklease mampu memotong asam nukleat di dareah tengah daru sekuens asam nukleat yang mampu mengenali daerah spesifik pada urutan asam nukleat (Campbell, 2008).
b. Enzim Endonuklease
Enzim endonuklease adalah enzim yang memotong molekul DNA.
Enzim ini memotong DNA pada rangka gula-fosfat tanpa merusak basa.
Setiap enzim mempunyai sekuens pengenalan yang unik pada utas DNA, biasanya sepanjang 4-6 pasang basa. Enzi endonuklease merupakan enzim yang mengenali dan memotong kedua utas dari asam deoksiribonukleat (DNA) pada urutan pasang basa (sekuens) tertentu. Enzim ini mencari sekuens spesifiknya dengan cara menempel pada DNA baik secara spesifik maupun secara non-spesifik, kemudian berdifusi secara linear dengan kecepatan tertentu hingga ditemukannya sekuens spesifik yang dikenalinya.
Proses ini dipengaruhi oleh konsentrasi ion Mg. Setelah sekuens spesifik dikenali, akan terjadi perubahan konformasi enzim dan DNA (Pingoud dan Jelstch, 2001). Bagi enzim endonuklease restriksi, satu unit (U) aktivitas didefinisikan sebagai jumlah enzim yang dapat memotong 1 µg DNA dari fage λ selama 1 jam dalam kondisi buffer yang optimum pada suhu 37℃.
Seperti sifat enzim pada umumnya, enzim restriksi juga membutuhkan kondisi tertentu untuk menghasilkan aktivitas pemotongan yang optimum, seperti suhu, pH, kekuatan ionik, ion Mg2+ waktu reaksi, dan aditif penstabil Dalam reaksinya, enzim endonuklease. Restriksi membutuhkan ion.
Konsentrasi yang optimum berkisar antara 5-10 mM MgCl. Peranan Mg diduga untuk menyebabkan polarisasi ikatan fosfodiester yang akan dipotong atau untuk mengaktivasi molekul air untuk membentuk nukleofil yang dibutuhkan. Dengan demikian, adanya pengkelat ion seperti EDTA dapat mengganggu aktivitas pemotongan DNA. (Pingoud dan Jelstch, 2001).
c. Enzim DNase
Deoksiribonuklease atau DNase berasal dari pankreas Bovine.
Enzim ini mengkatalis endonukleolitik untai ganda maupun tunggal DNA dengan produk ujung 5′-fosfonukleotida dan 5′-fosfooligonukleotida dalam bentuk campuran yang komplekx. Adanya ion magnesium (mg), DNase bereaksi dengan masing-masing untai DNA secara terpisah pada lokasi yang acak. Selain itu, keberadaan manganese (II) menyebabkan DNase I bereaksi pada kedua untai hampir pada tempat yang sama. Kebanyakan protokol menggunakan ion magnesium dengan DNase, namun untuk tujuan tertentu, kebanyakan menggunakan manganese. Enzim ini memiliki berat molekul 30,072 yang dihitung dari sekuennya. Secara struktural, enzim ini berbentuk polipeptida tunggal yang tersusun atas dua jembatan disulfida dan satu karbohidrat dari monosakarida. pH optimum bagi aktivitas enzimatiknya berkisar 7-8, namun DNase yang bebas protease ini stabil pada kisaran pH 5-7 pada suhu 60 °C hingga 5 jam, lebih spesifik lagi pada suhu °C, 1 mg/mL larutan akan kehilangan aktivitasnya sebanyak 6% perjam baik pada buffer asetat (pH 5) atau pada buffer Tris pH 7.2. Aktivitas enzim akan rusak pada suhu 68 °C.
3. Isolasi DNA
Isolasi DNA merupakan salah satu tahap penting dalam kegiatan memperoleh informasi genetic dan analisis genetic. DNA dengan kualitas yang baik digunakan untuk kegiatan seperti pemanfaatan marka molekuler, pembuatan pustaka genom, hingga sekuensing. Prinsip isolasi DNA terdiri dari tiga tahapan, yaitu lisis dinding dan membrane sel, pemisahan atau purifikasi DNA dan presipitasi DNA (Triani, N, 2020). Struktur kimia DNA merupakan makromolekul kompleks yang terdiri dari 3 macam molekul,
yaitu gula pentosa (deoksiribosa), asam fosfat, dan basa nitrogen. Basa nitrogen DNA terdiri dari gugus purin yaitu gugus adenin, guanin dan pirimidin yaitu timin dan sitosin. DNA dapat bereplikasi membentuk salinan dirinya sendiri, karena setiap untai DNA mengandung urutan basa tertentu dan setiap basa menghubungkan molekul gula dan fosfat. Dalam sel tubuh manusia yang mengandung 46 kromosom, diperkirakan terdapat 26.000 hingga 40.000 gen dan gen tersebut menentukan warna rambut, jenis rambut, warna kulit, warna mata, dll. Misalnya seseorang memiliki rambut keriting hitam karena gen tersebut diturunkan dari keturunannya. Orang tua menginstruksikan sel folikel rambut untuk membentuk rambut hitam dan keriting (Hasibuan, S, I, 2022). DNA adalah molekul besar dan kompleks yang terdiri dari dua untai panjang yang saling memuntir untuk membentuk heliks ganda, dengan setiap untai termasuk polimer dari ratusan hingga ribuan nukleotida. Masing-masing nukleotida ini terdiri dari: Gula pentose deoksiribosa, yaitu gula pentosa (atom 5 C) telah kehilangan satu atom oksigen. Gugus fosfat melekat pada atom C nomor 5 dalam gula pentosa.
Basa nitrogen yang melekat pada atom C nomor 1 dalam gula pentose (Hasibuan, S, I, 2022).
Ekstraksi dan purifikasi DNA pada dasarnya merupakan serangkaian proses pemisahan DNA dari komponen-komponen sel lainnya. Ekstraksi DNA pada organisme eukaryot dilakukan melalui proses penghancuran dinding sel (lysis of cell wall), penghilangan protein dan RNA (cell digestion), dan pengendapan DNA (precipitation) dan pemanenan. Saat ini isolasi DNA secara teknis menjadi lebih mudah dengan munculnya berbagai teknik ekstraksi dan purifikasi dalam bentuk kit. (Nurhayati, B, 2017).
Isolasi DNA merupakan teknik ekstraksi dan atau purifikasi DNA dari suatu sel sebagai tahap awal suatu analisis genetik.
4. Peran Isolasi DNA
Isolasi DNA memainkan peranan penting dalam analisis molekuler sebagai Langkah utama untuk melakukan penelitian. DNA merupakan senyawa makromolekul yang terdiri dari polimer nukleotida. Setiap nukleotida memiliki tiga komponen utama, yaitu gugus phosphate, gula
deoksiribosa dan basa nitrogen. DNA memiliki fungsi sebagai wadah informasi genetik dan pewarisan sifat/karakteristik dari suatu organisme.
Pada tanaman, DNA terletak di dalam nukleus, kloroplas dan mitokondria.
Isolasi DNA (Deoxyribo Nucleic Acid) merupakan teknik yang penting dalam pengembangan ilmu ini. Derajat kemurnian dan konsentrasi dalam isolasi DNA sangat mempengaruhi hasil yang diperoleh. Analisis tingkat molekuler dengan DNA sebagai objeknya diawali dengan proses isolasi DNA, selanjutnya diikuti analisis molekuler, seperti PCR (Polymerase Chain Reaction), RLFP (Restricted Fragment Lenght Polymorphis), dan RAPD (Restricted Amplified Polymorphisms) (Hasibuan, S, I, 2022).
Isolasi DNA diperlukan untuk analisis genetic, yang digunakan untuk tujuan ilmiah, medis, atau forensik. Para ilmuwan menggunakan DNA yang sudah di isolasi di sejumlah aplikasi, seperti pengelanan DNA ke dalam sel dan binatang atau tanaman, atau untuk tujuan diagnostic. Dalam obat aplikasi yang terakhir adalah yang paling umum. Di sisi lain, ilmu forensic perlu memulihkan DNA untuk identifikasi individu.
5. Metode Isolasi DNA
Terdapat berbagai macam metode isolasi DNA. Metode isolasi DNA antara lain:
a) Teknik Random Amplified Polymorphic DNA (RAPD)
Teknik pengujian polimorfisme DNA merupakan teknik isolasi DNA berdasarkan pada amplifikasi dari segmen-segmen DNA acak yang menggunakan primer tunggal yang sekuen nukleotidanya ditentukan secara acak. Primer tunggal ini biasanya berukuran 10 basa.PCR dilakukan pada suhu anealing yang rendah yang memungkinkan primer menempel pada beberapa lokus pada DNA. Aturan sederhana untuk primer adalah terdiri atas 18- 28 susunan basa dengan persentase G+C 50-60% (Istanti, 1999).
b) Metode CTAB
Cetyl Trimethyl Ammonium Bromide (CTAB) merupakan metode yang umum digunakan dalam ekstraksi DNA genom tanaman yang banyak mengandung polisakarida dan senyawa polifenol (Ardiana, 2009). Metode ini menghasilkan pita DNA yang berukuran tebal dan dapat memisahkan
DNA dari polisakarida karena adanya perbedaan karakteristik kelarutan (differensial of solubility). Disamping deperoleh fragmen DNA, dengan metode CTAB juga akan diperoleh RNA dengan pita tipis yang terletak jauh berada di bawah pita DNA. Keberadaan pita RNA tergantung bahan yang diekstraksi (Prasetyo, 2008).
c) Phenol Chloroform
Pada metode ini mengunakan senyawa Phenol-choloroformisoamyl alcohol. Namun metode ini sekarang ditinggalkan, karena sifat toksik phenol (Barnum, 2005). Metode tertua pemurnian DNA di laboratorium, masih sering digunakan juga, mengandalkan campuran pelarut organik.
Sampel yang sudah lisis dicampur dengan fenol, kloroform, dan isoamylalcohol untuk pemisahan DNA dan protein. Protein didenaturasi dengan campuran organik. Ketika sampel disentrifugasi, DNA dipertahankan dalam air lapisan, fenol di bagian bawah tabung, dan protein didenaturasi membentuk antarmuka berawan. Metode ini sangat efisien, tetapi sayangnya hanya dapat digunakan jika jumlah bahan awal cukup melimpah. Selain itu, pelarut organik yang digunakan membawa masalah kesehatan dan keselamatan. Kualitas DNA dari prosedur ini biasanya tidak cukup untuk beberapa teknik analitis lebih sensitif (terutama sequencingdan kadang-kadang PCR).
d) Salting Out
Salting out merupakan metode isolasi DNA yang menggunakan garam konsentrasi tinggi (NaCl 6 M) untuk medenaturasi protein menggunakan Proteinase K untuk denaturasi protein (Barnum, 2005).
e) Guanidine Isothiocyanate
Metode ini lebih cepat dibandingakn dengan metode yang lain.
Namun senyawa thiosyanate yang digunakan untuk lisis dinding sel bersifat toksik serta memerlukan kloroform untuk denaturasi protein (Barnum, 2005).
f) Silica Gel
Pada metode ini, silica gel dapat mengikat DNA dengan perantaraan garam atau buffer tertentu misalnya NaI. Metode ini cepat tetapi untuk recovery DNA kurang (Barnum, 2005).
g) PCR (Polymerase Chain Reaction)
Metode ini merupakan suatu teknik perbanyakan (amplifikasi) potongan DNA secara in vitro pada daerah spesifik yang dibatasi oleh dua buah primer oligonukleotida.Primer yang digunakan sebagai pembatas daerah yang diperbanyak adalah DNA untai tunggal yang urutannya komplemen dengan DNA templatnya. Proses tersebut mirip dengan proses replikasi DNA secara in vivo yang bersifat semi konservatif.
6. Mekanisme Isolasi DNA
Secara umum, tahap isolasi DNA dimulai dari pengambilan sampel, pelisisan membran dan/atau dinding sel, ekstraksi DNA, presipitasi DNA, pemurnian DNA, dan pengawetan DNA. Isolasi DNA juga berfungsi sebagai media pembelajaran genetik, dapat mengetahui kelainan genetik yang diderita, dapat mengetahui agen penyebab penyakit infeksi, dan lain- lain. (Maftuchah, 2015). Secara kimiawi penghancuran sel dilakukan dengan memanfaatkan senyawa kimia seperti EDTA (Ethylen diamnine Tetra Acetic), SDS (Sodium Dodecyl Sulphat), Ammonium-Choride- Potassium (ACK). Kotoran akibat lisis sel dipisahkan dengan cara sentrifugasi. Kemudian molekul nukleotida (DNA dan RNA) yang telah dipisahkan dibersihkan dari protein yang masih ada dengan fenol. Dalam proses ini sebagian kecil RNA juga dapat dibersihkan. Sedangkan kloroform digunakan untuk membersihkan sisa- sisa protein dan polisakarida dari larutan. Enzim RNAase digunakan untuk menghancurkan RNA sehingga DNA dapat diisolasi secara utuh. Pemurnian atau purifikasi DNA dapat dilakukan dengan mencampur larutan DNA tersebut dengan NaCl yang berfungsi memekatkan, memisahkan DNA dari larutan, dan mengendapkan DNA pada saat dicampur dengan etanol. Proses sentrifugasi dengan kecepatan tinggi akan mengendapkan tepung berwarna putih (DNA) dan menempel di dasar microtube. Prinsip dasar isolasi DNA di atas
diaplikasikan dengan berbagai macam tahapan ekstraksi dan purifikasi DNA dengan berbagai modifikasi disesuaikan dengan kebutuhan atau jenis sampel yang diekstraksi. (Nurhayati, B, 2017).
Uji kualitas (kemurnian) dan kuantitas (konsentrasi) DNA dilakukan menggunakan spektrofotometer. Spektrofotometri adalah metode pengukuran kuantitatif yang didasarkan pada pengukuran absorbs (penyerapan) radiasi gelombang elektromagnetik. Spektrofotometri merupakan suatu metoda analisa yang didasarkan pada pengukuran serapan sinar monokromatis oleh suatu lajur larutan berwarna pada panjang gelombang spesifik dengan menggunakan monokromator prisma atau kisi difraksi dengan detektor fototube. Benda bercahaya seperti matahari atau bohlam listrik memancarkan spektrum yang lebar terdiri atas panjang gelombang. Panjang gelombang yang dikaitkan dengan cahaya tampak itu mampu mempengaruhi selaput pelangi mata manusia dan karenanya menimbulkan kesan subyektif akan ketampakan (vision). Spektrofotometer UV-VIS adalah salah satu metode instrument yang paling sering diterapkan dalam analisis kimia untuk mendeteksi senyawa (padat/cair) berdasarkan absorbansi foton. Agar sampel dapat menyerap foton pada daerah UV-VIS (panjang gelombang foton 200 nm – 700 nm), biasanya sampel harus diperlakukan atau derivatisasi, misalnya penambahan reagen dalam pembentukan garam kompleks dan lain sebagainya. Unsur diidentifikasi melalui senyawa kompleksnya. Prinsip kerja spektrofotometri UV-Vis adalah interaksi yang terjadi antara energy yang berupa sinar monokromatis dari sumber sinar dengan materi yang berupa molekul. Besar energy yang diserap tertentu dan menyebabkan electron tereksitasi dari ground state ke keadaan tereksitasi yang memiliki energy lebih tinggi. Serapan tidak terjadi seketika pada daerah ultraviolet-visible untuk semua struktur elektronik tetapi hanya pada system-sistem terkonjugasi, struktur elektronik dengan adanya ikatan p dan nonbonding electron. (Koentjoro, M, P, 2021).
7. Ephitelial Mulut
Ephitelium berasal dari kata epi yang berarti upon atau di atas dan thele yang berarti nipple atau punting. Penggunaan istilah epitel meluas
untuk semua bentuk lapisan yang terdiri atas lembaran sel-sel baik yang bersifat tembus cahaya ataupun tidak. Dengan berkembangnya pemakaian mikroskop, maka istilah epitel tidak terbatas pada kumpulan sel yang membentuk membrane yang menutupi, tetapi juga digunakan untuk kelenjar. Hal tersebut didukung dengan hasil penelitian embriologis yang menyimpulkan bahwa sel-sel epitel pada permukaan tumbuh ke dalam jaringan pengikat di bawahnya dan berkembang menjadi kelenjar (Campbell, 2008).
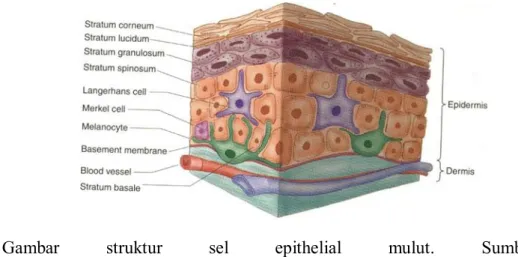
Gambar struktur sel epithelial mulut. Sumber:
https://sebuahopini2000.blogspot.com/2021/06/cocolan-histologi- kulit.html
Sel-sel epitel mukosa mulut terdiri dari empat lapisan berturut-turut dari yang paling dalam ke permukaan yaitu lapisan germinativum/basalis, lapisan spinosum, lapisan granulosum dan lapisan corneum. Stratum basalis terdiri dari selapis sel berbentuk kubus yang berbatasan dengan lamina propia dan mengandung sel-sel induk yang secara kontinyu bermitosis dan anak selnya dikirimkan ke lapisan yang lebih superfisial. Stratum spinosum terdiri dari beberapa lapis sel berbentuk bulat atau oval dan mempunyai karakteristik sel yang mulai matang. Stratum granulosum terdiri dari beberapa lapis sel yang lebih gepeng dan lebih matang dari stratum spinosum dan mengandung banyak granula keratohyalin yang merupakan bakal sel keratin. Stratum corneum terdiri dari selapis atau berlapis-lapis sel (tergantung regio) berbentuk pipih yang tidak berstruktur dan tidak mempunyai inti sel. Mukosa mulut dapat dikelompokkan menjadi tiga tipe yaitu mukosa pengunyahan, mukosa penutup dan mukosa khusus. Mukosa
pengunyahan terdapat di regio rongga mulut yang menerima tekanan kunyah seperti gusi dan palatum durum. Jaringan epitelnya para keratinised (mempunyai lapisan keratin tipis yang beberapa selnya ada yang masih memiliki inti sel yang tidak sempurna). Mukosa penutup terdapat pada dasar mulut, permukaan inferior lidah, permukaan dalam bibir dan pipi, palatum molle dan mukosa alveolaris kecuali gusi. Tipe epitelnya nonkeratinised (tidak memiliki lapisan keratin). Mukosa khusus terdapat pada dorsum lidah, tipe epitelnya ortokeratinised (memiliki lapisan keratin yang tebal yang terdiri dari sel-sel yang sudah tidak berinti). Perbandingan antara sel basal-parabasal, sel intermediet, dan sel superfisial disebut indeks maturasi.
Pada kondisi normal, jumlah sel pada lapisan superfisial sesuai dengan jumlah sel pada lapisan sel basal. Rongga mulut dibatasi oleh membrane mukosa yang berhubungan dengan kulit. Rongga mulut terdiri dari bibir yang disekitarnya mulut yang terbuka, pipi berada disepanjang rongga, lidah dan ototnya, hard dan soft palate. Mukosa mulut normalnya berwarna merah jambu terang (lightpink) dan lembab. Pada dasar mulut dan area bawah lidah kaya akan pembuluh darah. Tipe dari ulcer atau trauma dapat mengakibatkan perdarahan. Ada 3 kelenjar saliva yang mensekresikan 1 liter saliva per hari. Kelenjar buccal ditemukan pada mukosa yang membatasi pipi dan mulut yang mencegah hygiene dan kenyamanan pada jaringan oral (Dafrosa, L, 2014).
8. Isotonik
Minuman isotonik merupakan salah satu produk minuman ringan karbonasi atau nonkarbonasi untuk meningkatkan kebugaran, yang mengandung gula, asam sitrat, dan mineral. Minuman isotonik juga dikenal dengan sport drink yaitu minuman yang berfungsi untuk mempertahankan cairan dan garam tubuh serta memberikan energi karbohidrat ketika melakukan aktivitas. Minuman isotonik dibuat untuk menggantikan energi, cairan tubuh dan elektrolit yang hilang selama dan setelah kita melakukan aktivitas fisik, seperti bekerja dan olahraga. Komponen utama dari minuman isotonik ini adalah air sebagai pengganti cairan tubuh, karbohidrat sebagai penyuplai energi “siap saji” dan mineral sebagai pengganti elektrolit tubuh
yang hilang. Jumlah karbohidrat yang dikandung minuman isotonic 6-9%.
Air dalam tubuh diperlukan untuk mengatur panas dan menjaga keseimbangan cairan. Air adalah penyusun 45-70% dari masa tubuh yang setara dengan 33-53 liter untuk manusia dengan masa tubuh 75 kg. Rasa haus akan timbul jika tubuh kehilangan 25% air dari total massa tubuh.
Setiap harinya manusia membutuhkan asupan air minimal 2 liter per orang.
Khusus untuk orang yang sebagian besar aktivitas fisiknya berupa duduk, asupan air akan sesuai dengan jumlah air yang hilang dari tubuhnya (Koswara, 2009).
9. Aquades
Aquades merupakan air hasil penyulingan yang bebas dari zat-zat pengotor sehingga bersifat murni dalam laboratorium. Aquades berwarna bening, tidak berbau, dan tidak memiliki rasa. Aquades biasa digunakan untuk membersihkan alat-alat laboratorium dari zat pengotor. Aquades merupakan pelarut yang jauh lebih baik dibandingkan hampir semua cairan yang umum dijumpai. Senyawa yang segera melarut di dalam aquades mencakup berbagai senyawa organik netral yang mempunyai gugus fungsional polar seperti gula, alkohol, aldehida, dan keton. Kelarutannya disebabkan oleh kecenderungan molekul aquades untuk membentuk ikatan hidrogen dengan gugus hidroksil gula dan alkohol atau gugus karbonil aldehida dan keton (Lehninger, 1982). Maka, aquades juga dikenal sebagai pelarut universal. Aquades berada dalam kesetimbangan dinamis antara fase cair dan padat di bawah tekanan dan temperatur standar yaitu pada tekanan 100 kPa (1 bar) dan temperatur 273,15K (0°C). Dalam bentuk ion, aquades dapat dideskripsikan sebagai asosiasi (ikatan) antara sebuah ion hidrogen (H) dengan sebuah ion -hidroksida (OH+). Aquades merupakan air yang melalui proses pengolahan yang memenuhi standar medis dan kimiawi.
Aquades aman bagi kesehatan apabila telah memenuhi persyaratan fisika, mikrobiologis, kimiawi dan radioaktif. Dalam penelitian, diketahui bahwa aquades adalah air hasil penyulingan (diuapkan dan disejukkan kembali) memiliki kandungan murni H2O. Aquades juga memiliki rumus kimia yaitu
H2O yang berarti dalam 1 molekul terdapat 2 atom hidrogen kovalen dan atom oksigen tunggal.
F. Alat dan Bahan Alat:
Nama Alat Jumlah Alat
Tabung sentrifuge 2 buah
Tabung reaksi 3 buah
Gelas kimia 10 ml 3 buah
Blue tip dan mikropipet 10 buah dan 1 buah Gelas volume 10 ml 1 buah
Rak tabung reaksi 1 buah
Vortex 1 buah
Sentrifuge 1 buah
Spektrofotometri UV-VIS 1 buah
Bahan:
Nama Bahan Jumlah Bahan
Minuman isotonik 50 ml
Buffer Tris-EDTA 50 ml
Larutan NaCl 2,5 M 50 ml
Etanol dingin 60 ml
Aquades 100 ml
G. Alur Percobaan
1) Pengumpulan sel-sel
1. Diambil 10 ml
2. Digunakan untuk berkumur selama 1 menit
3. Hasil berkumur ditampung dalam gelas kimia yang digunakan sebagai sel epitel untuk isolasi DNA
2) Pemecahan sel (Lisis Sel)
1. Diambil 10 ml dimasukkan ke tabung sentrifuge
2. Disentrifuge dengan kecepatan 10.000 rpm selama 5 menit
3. Ditambahkan 1 ml buffer Tris-EDTA
4. Divortex selama 30 detik (sampai endapan hancur)
3) Pengendapan DNA
1. Dimasukkan ke tabung sentrifuge yang berisi larutan sampel
2. Dipindahkan semua isi tabung sentrifuge ke tabung reaksi yang bersih dan kering
3. Ditambahkan 1 ml etanol dingin secara perlahan 4. Dibiarkan 5 menit
Larutan isotonic dan aquades
Larutan sel epitel
Larutan sel ephitelial
Supernantant Endapan
Endapan hancur
1000 mikroliter NaCl 2,5 M
5. Diamati hasil DNA yang terbentuk (akan menggumpal diantara batas buffer dan etanol, terlihat ada yang melayang seperti benang putih)
6. Diukur absorbansi pada panjang gelombang 260 nm
Reaksi:
Benang-benang DNA
Nilai absorbansi
H. Hasil Pengamatan
No.
Perc
Prosedur Percobaan Hasil Pengamatan Dugaan/Reaksi Kesimpulan
Sebelum Sesudah
1. Pengumpulan sel-sel
1. Diambil 10 ml
2. Digunakan untuk berkumur selama 1 menit
3. Hasil berkumur ditampung dalam gelas kimia yang digunakan sebagai sel epitel untuk isolasi DNA
-Minuman isotonik: larutan bewarna keruh (+)
- Aquades: tidak bewarna
Setelah berkumur -Minuman
isotonik: larutan bewarna keruh (++)
- Aquades: larutan bewarna keruh (+)
Na+ dapat berikatan dengan gugus fosfat DNA. Sel-sel epitel mulut terkumpul pada larutan isotonik dan aquades. Setelah berkumur ditandaik dengan arutan yang bewarna keruh.
(Record, dkk,1998)
Berdasarkan hasil percobaan larutan isotonik,dan aquades dapat digunakan untuk mengumpulkan sel epitelial mulut Larutan isotonik dan aquades
Larutan sel epitel
2. Pemecahan sel (lisis sel)
1. Diambil 10 ml dimasukkan ke tabung sentrifuge
2. Disentrifuge dengan kecepatan 10.000 rpm selama 5 menit
3. Ditambahkan 1 ml buffer Tris- EDTA
4. Divortex selama 30 detik
-Larutan sel epitel isotonik:
keruh (++) -Larutan sel epitel aquades:
keruh (+)
-Buffer Tris EDTA: tidak bewarna
-Larutan sel epitel isotonik: keruh (++) dan terdapat endapan
-Larutan sel epitel aquades: keruh terdapat endapan (+)
Setelah ditambah buffer Tris-EDTA -Isotonik: larutan tidak bewarna endapan (++)
Pemecahan sel-sel pencernaan protein menjadi endapan DNA setelah di Vortex.
Sentrifuge akan memisahkan endapan dengan larutan (Champhbel, dkk.
2008)
Berdasarkan hasil percoban terdapat endapan setelah di sentrifuge selama 5 menit
Terjadi
pemecahan sel yang diandai dengan endapan hancur dan larut akibat proses vortex
Larutan sel ephitelial
Endapan Supernatant
Endapan hancur
-Aquades: larutan tidak bewarna endapan (+)
Setelah di vortex -Isotonik:
endapan hancur + larutan keruh(+) -Aquades:
endapan hancur + larutan keruh
3. Pengendapan DNA
1. Dimasukkan ke tabung sentrifuge yang berisi larutan sampel
2. Dipindahkan semua isi tabung sentrifuge ke tabung reaksi yang bersih dan kering
3. Ditambahkan 1 ml etanol dingin secara perlahan
4. Dibiarkan 5 menit
5. Diamati hasil DNA yang terbentuk
6. Diukur absorbansi pada panjang gelombang 260 nm
-Etanol dingin:
tidak bewarna -Larutan sampel isotonik: keruh (+)
-Larutan sampel aquades: keruh -NaCl: larutan tidak bewarna
Setelah ditambah NaCl
-Larutan sampel isotonik: keruh (+)
-Larutan sampel aquades: keruh
Setelah ditunggu 5 menit
-larutan sampel isotonik:larutan keruh dan benang putih melayang (++)
-Larutan sampel aquades: larutan keruh dan benang putih melayang (+)
Terdapat gumpalan DNA yang terbanyak pada laruan isotonik dibandingkan aquades (Forouzesh &
Nass,2023)
Berdasarkan Hasil Percobaan
DNA yang
terlepas dari sel akan
menggumpal dan membentuk serabut putih akibat
penambahan etanol dingin yang
menandakan
bahwa DNA
berhasil diisolasi Larutan yang paling banyak dalam
mengisolasi DNA adalah larutan 1000 mikroliter NaCl 2,5 M
Benang-benang DNA
Nilai absorbansi
Nilai absorbansi larutan isotonik:
4,0000
Larutan aquades:
3,3913
isotonik yang dibuktikan
dengan nilai absorbansi
larutan isotonik lebih besar dari aquades yakni:
larutan isotonik:
4,0000
Larutan aquades:
3,3913
I. Analisis dan Pembahasan
Pada percobaan yang berjudul Isolasi DNA Ephitelial Mulut memiliki tujuan yaitu mampu mengerjakan isolasi DNA sesuai prosedur, dengan sampel DNA diambil dari sel ephitelial mulut. DNA adalah molekul besar dan kompleks yang terdiri dari dua untai panjang yang saling memuntir untuk membentuk heliks ganda, dengan setiap untai termasuk polimer dari ratusan hingga ribuan nukleotida.
Masing-masing nukleotida ini terdiri dari: Gula pentose deoksiribosa, yaitu gula pentosa (atom 5 C) telah kehilangan satu atom oksigen. Gugus fosfat melekat pada atom C nomor 5 dalam gula pentosa. Basa nitrogen yang melekat pada atom C nomor 1 dalam gula pentose. Secara umum, tahap isolasi DNA dimulai dari pengambilan sampel, pelisisan membran dan/atau dinding sel, ekstraksi DNA, presipitasi DNA, pemurnian DNA, dan pengawetan DNA. Isolasi DNA juga berfungsi sebagai media pembelajaran genetik, dapat mengetahui kelainan genetik yang diderita, dapat mengetahui agen penyebab penyakit infeksi, dan lain-lain.
Epithelium berasal dari kata epi yang berarti upon atau di atas dan thele.
Penggunaan istilah epitel meluas untuk semua bentuk nipple lapisan yang terdiri atas lembaran sel-sel (cellular membrane) baik yang bersifat tembus cahaya ataupun yang tidak. Epitel dalam arti luas dikelompokan menjadi:
a) Jaringan yang sel-selnya tersusun dalam lapisan yang menutupi permukaan luar atau melapisi rongga di dalam tubuh yang dinamakan epitel permukaan, mereka dapat digolongkan sesuai jumlah lapisan sel dan morfologi sel pada lapisan permukaan.
b) Jaringan epitel yang tumbuh ke dalam jaringan pengikat menjadi epitel kelenjar, jaringan epitel kelenjar meliputi sel-sel dengan fungsi khusus menghasilkan cairan sekresi yang komposisinya berbeda dari darah atau cairan interseluler. Proses ini biasanya disertai proses makromolekul intraseluler. Persenyawaan ini biasanya ditampung di dalam sel dalam vesikel-vesikel kecil bermembran yang disebut granul sekresi.
Epitel dapat berkembang dari ketiga lapis embrional. Epitel yang melapisi kulit, mulut, hidung, dan anus berasal dari ektoderm. Pelapis sistem pernapasan, saluran cerna, dan kelenjar dari saluran cerna (misalnya, pancreas dan hati) berasal
dari endoderm. Epitel lainnya (misalnya, endotel pelapis pembuluh darah) berasal dari mesoderm. Dalam percobaan ini, menggunakan sel epithelial pada mulut.Sel epitel adalah jaringan yang sel-selnya tersusun dalam lapisan yang menutupi permukaan luar atau melapisi rongga di dalam tubuh. Jaringan ephitel mukosa mulut adalah ephitel berlapis gepeng. Sel-sel ephitel mukosa mulut terdiri dari empat lapisan berturut-turut dari yang paling dalam ke permukaan yaitu lapisan germinativum/basalis, lapisan spinosum, lapisan granulosum, dan lapisan corneum.
Struktur yang terdiri dari beberapa lapisan tersebut mencerminkan adanya proses pertumbuhan dan pematangan sel. Sel-sel di satu lapisan secara kontinyu digantikan oleh sel-sel dari lapisan di bawahnya.
Prinsip-prinsip dalam melakukan isolasi DNA ada 2, yaitu sentrifugasi dan presipitasi. Sentrifugasi merupakan teknik untuk memisahkan campuran berdasarkan berat molekul komponennya. Molekul yang mempunyai berat molekul besar akan berada pada bagian bawah tabung dan molekul ringan akan berada pada bagian atas tabung. Teknik sentrifugase dilakukan oleh mesin yaitu mesin sentrifugase dengan kecepatan yang bervariasi. Hasil sentrifugase akan menunjukkan dua macam fraksi yang terpisah, yaitu supernatant dibagian atas dan pellet dibagian bawah. Presipitasi merupakan langkah yang dilakukan untuk mengendapkan suatu komponen dari campuran (Tim Dosen Biokimia, 2021).
Tahapan dari isolasi DNA epithelial mulut antara lain sebagai berikut:
1. Pengumpulan sel-sel
Pada tahap pengumpulan sel-sel, larutan isotonik dan aquades diambil 10 ml lalu digunakan untuk berkumur selama 1 menit. Sel epithel yang digunakan merupakan sel epithel mulut karena proses pengambilannya lebih mudah dibandingkan dengan sel epitel pada organ yang lain seperti di hidung, kulit, atau anus.
Gambar struktur sel epithelial mulut. Sumber:
https://sebuahopini2000.blogspot.com/2021/06/cocolan-histologi-kulit.html
Epithel mulut merupakan golongan ektoderm yaitu jenis epithel yang melapisi bagian luar tubuh. Fungsi sel epithel pada mulut ialah sebagai pelindung permukaan mulut dalam atau yang biasa dikenal fungsi proteksi. Fungsi lainnya ialah sebagai kelenjar atau biasa dikenal sebagai fungsi sekresi. Minuman isotonik merupakan salah satu produk minuman ringan karbonasi atau nonkarbonasi untuk meningkatkan kebugaran, yang mengandung gula, asam sitrat, dan mineral serta elektrolit berupa Na+. Komponen utama dari minuman isotonik ini adalah air sebagai pengganti cairan tubuh, karbohidrat sebagai penyuplai energi “siap saji”
dan mineral sebagai pengganti elektrolit tubuh yang hilang. Fungsi larutan isotonic dan aquades adalah untuk mengambil sampel yang ada dimulut yaitu sebagai pelarut yang fungsinya untuk melarutkan DNA. Untuk proses berkumur hanya dilakukan oleh satu orang karena agar nilai absorbansi yang terukur dapat dibandingkan antara larutan isotonik dan aquades. Cara berkumur pada setiap orang juga berbeda dengan waktu yang sama yaitu 1 menit sehingga diketahui nilai absorbansi dan hasilnya tidak jauh berbeda. Kemudian, hasil berkumur ditampung dalam gelas kimia yang digunakan sebagai sel epitel untuk isolasi DNA. Hasil yang diperoleh adalah larutan sel epithel (larutan isotonik) berupa larutan keruh (++), larutan sel dan larutan sel epithel (aquades) berupa larutan keruh (+). Berdasarkan hasil tersebut dapat diketahui bahwa yang larutan sel epithel paling keruh adalah larutan isotonik. Hal ini dikarenakan pada larutan isotonik mengandung ion Na+. Ion Na+ akan berkatan dengan DNA khususnya pada gugus fosfat pada DNA.
2. Pemecahan sel (lisis sel)
Percobaan kedua merupakan lisis sel. Tujuan dari pemecahan sel (lisis) adalah memecah sel epithel dengan cara hidrolisis untuk mengeluarkan DNA dari sel epitthel serta untuk memisahkan sel-sel dari pengotornya. Langkah pertama pemecahan sel (lisis sel) adalah larutan sel epitel diambil 10 ml dan dimasukkan ke tabung sentrifuge. Kemudian disentrifuge dengan kecepatan 10.000 rpm selama 5 menit sehingga menghasilkan endapan dan supernatant. Tujuan dari sentrifuge ialah untuk membuat larutan sel epithel terpisah antara filtrat dan residunya. Sentrifuge merupakan suatu teknik untuk memisahkan campuran berdasarkan berat molekul komponennya. Molekul yang lebih besar beratnya akan berada dibagian bawah dan molekul yang lebih ringan berada di bagian atas tabung. Gaya yang terjadi pada sentrifuge adalah gaya sentrifugal. Gayasentrifugal merupakan efek semu yang dihasilkan ketika suatu benda melakukan gerak melingkar dan menjauhi arah putaran. Hal inimenyebabkan residu pada larutan akan mengendap sehingga akan terpisah antara filtrat dengan residunya. Kecepatan pada proses sentrifuge dilakukan pada kecepatan 10.000 rpm karena merupakan kecepatan optimum. jika kurang dari itu, sel yang terlarut dalam sampel tidak akan mengendap sempurna dan apabila lebih dari itu kemungkinan rusaknya sel menjadi bagian-bagian yang lebih kecil menjadi lebih besar Supernatantnya dibuang lalu endapan ditambahkan 1 ml buffer Tris-EDTA menggunakan mikropipet hal ini bertujuan agar volume hasil pengukuran bisa akurat. Fungsi penambahan buffer Tris-EDTA adalah untuk mempertahankan struktur DNA yang berkaitan dengan pH.
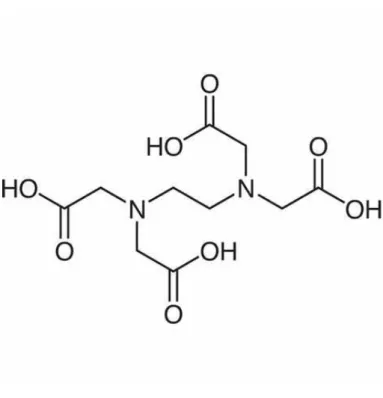
Gambar Struktur Buffer Tris-EDTA. Sumber:
https://cymitquimica.com/products/3B-E0084/60-00- 4/ethylenediaminetetraacetic-acid/
Buffer Tris-EDTA (TE) adalah salah satu jenis buffer yang digunakan dalam isolasi DNA. TE buffer terdiri dari Tris (Tris (hydroxymethyl) aminomethane) dan EDTA (Ethylenediaminetetraacetic acid). Larutan buffer Tris-EDTA yang digunakan dalam percobaan ini memiliki pH 8 karena struktur DNA akan stabil pada pH 8. Jika larutan buffer dengan pH rendah akan mengkibatkan depurifikasi dan mengakibatkan DNA terdistribusi ke fase fenol selama proses deproteinisasi.
Sedangkan pH larutan yang tinggi dan terlalu basa di atas 12 akan mengakibatkan degradasi DNA sehingga DNA tidak bisa terbaca pada spektrometri. Selain itu, fungsi larutan buffer Tris-EDTA untuk agen pengkhelat yang berfungsi menginaktivasi enzim DNAse yang dapat mendenaturasi DNA dan menginaktivasi enzim endonuklease dengan cara mengikat ion magnesium dan kalsium. Enzim endonukleoase berfungsi untuk memotong molekul DNA pada rangka gula fosfat tanpa merusak basa. Tris adalah penyangga biologis umum yang biasanya digunakan pada proses ekstraksi DNA. DNA sensitif terhadap perubahan pH, sehingga tris digunakan untuk menstabilkan pH. Tris akan berinteraksi dengan sel
dan lipopolysaccharides membrane sel dan membuatnya permeable sehingga akan membantu dalam proses lisis membran sel. Sedangkan EDTA sebagai agen pengkhelat yang dapat menghentikan aktifitas DNAse.
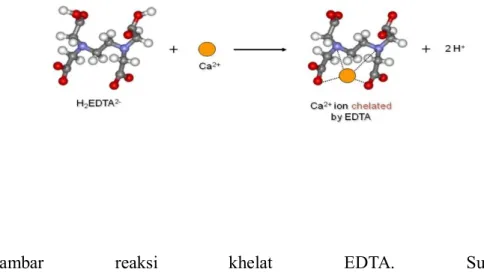
Gambar reaksi khelat EDTA. Sumber:
http://kumudtanwar.blogspot.com/2011/09/edta-reaction-with-metal-ions.html
EDTA (asam etilen diamina tetra asetat) adalah zat pembentuk kompleks khelat yang umum digunakan dalam titrasi kompleksometri untuk menentukan konsentrasi ion logam. EDTA membentuk kompleks dengan ion logam yang polivalent seperti Al, Bi, Ca, dan Cu, membentuk senyawa atau kompleks khelat yang stabil dan larut dalam air. DNAse sendiri merupakan enzim yang dapat melisiskan DNA. EDTA akan mengikat magnesium dan kalsium untuk membentuk khelat yang dapat inaktivasi enzim endonukleoase yang mana enzim ini akan memotong ikatan gugus phospat dan gula ribosa, sehingga harus dihentikan karena dapat menyebabkan DNA tidak dapat diamati. Langkah selanjutnya adalah divortex selama 30 detik sampai endapan hancur. Fungsi dari vortex ialah untuk membantu pemecahan sel dan untuk menghancurkan sel-sel yang ada di dalam endapan agar DNA bisa dikeluarkan dari dalam sel tersebut. Namun vortex yang berlebihan dapat menyebabkan pemisahan yang buruk antara komponen protein dan komponen asam nukleat dari isolasi. Hasil yang diperoleh setelah divortex ialah larutan menjadi tidak berwarna yang mana larutan isotonik menjadi tidak berwarna dan terbentuk endapan (+), aquades menjadi larutan tidak berwarna dan terbentuk endapan.
3. Pengendapan DNA
Percobaan ketiga merupakan pengendapan DNA. Tujuan dari pengendapan DNA adalah mengendapkan DNA pada larutan sel epithel. Pengendapan DNA bertujuan untuk memunculkan DNA yang menandakan DNA dapat berhasil diisolasi Pada pengendapan DNA, 1000 mikroliter NaCl 2,5 M dimasukkan ke tabung sentrifuge yang berisi larutan sampel. Fungsi penambahan NaCl sendiri adalah untuk mengikat dan melarutkan DNA yang bermuatan negatif yaitu gugus fosfat pada DNA karena NaCl mengandung ion Na akan mengikat gugus fosfat yang mana bermuatan negatif. Selain itu, fungsi penambahan NaCl ialah untuk membuang senyawa lain yang tidak diperlukan seperti karbohidrat, protein, dan polisakarida lainnya yang masih terkandung di dalam sampel. Hal ini dikarenakan NaCl dapat menyebabkan senyawa lain seperti karobohidrat, protein, dan polisakarida tersebut mengalami presipitasi. Selanjutnya, semua isi tabung sentrifuge dipindahkan ke dalam tabung reaksi yang bersih dan kering. Kemudian ditambahkan 1 ml etanol dingin secara perlahan dan dibiarkan selama 5 menit. Pada umumnya, penambahan etanol dingin pada isolasi DNA bertujuan untuk mengendapkan DNA dan memisahkannya dari komponen lain dalam sampel.
Penambahan etanol dingin dapat menurunkan konstanta dielektrik dalam larutan, sehingga memungkinkan DNA untuk mengendap lebih mudah. Sedangkan dielektrik konstan adalah ukuran kemampuan suatu zat untuk menahan medan listrik. Semakin tinggi konstanta dielektrik suatu zat, semakin sulit zat tersebut untuk mengendapkan DNA. Oleh karena itu, penambahan etanol dingin dapat membantu mempercepat proses pengendapan DNA dengan menurunkan konstanta dielektrik dalam larutan. Selanjutnya diamati hasil DNA yang terbentuk benang- benang DNA dan diukur nilai absorbansi pada panjang gelombang 260 nm. Prinsip spektrometri UV-Vis pada isolasi DNA adalah untuk mengukur absorbansi sampel DNA pada panjang gelombang tertentu. DNA memiliki kemampuan untuk menyerap sinar UV pada panjang gelombang 260 nm karena adanya ikatan hidrogen antara basa nitrogen dan basa nitrogen lainnya dalam molekul DNA. Oleh karena itu, pengukuran absorbansi pada panjang gelombang ini dapat digunakan untuk memperkirakan konsentrasi DNA dalam sampel. Rentang Panjang gelombang spektro UV-VIS dapat menukur antara 190-900 nm. Pada panjang
gelombang DNA 260 nm merupakan gelombang optimum dari dna bisa terbaca.
Hasil yang diperoleh pada tahap pengendapan DNA adalah larutan sampel isotonik berwarna keruh dan terbentuk benang putih melayang (++) sedangkan untuk larutan sampel aquades berwarna keruh dan terbentuk benang putih melayang (+).
J. Kesimpulan
Berdasarkan hasil percobaan DNA, larutan yang paling banyak dalam mengisolasi DNA adalah larutan isotonik yang dibuktikan dengan nilai absorbansi larutan isotonik lebih besar daripada larutan aquades yakni
Larutan isotonik: 4,000 Larutan aquades: 3,3913
K. Daftar Pustaka
Ardiana, 2009. Teknik Isolasi DNA Genom Tanaman Pepaya dengan Menggunakan Modifikasi Buffer CTAB. Buletin Teknik Pertanian. 14(1) : 12-15
Barnum., Susan, R, 2005. Biotechnology an Introduction, 2nd edition. USA:
Thomson Brooks/Cole
Campbell, Neil, A, 2008. Biologi Edisi Kelima Jilid 1 Alih Bahasa Rahyu Lestari. Jakarta: Penerbit Erlangga
Dafrosa, L, 2014. Laporan Praktikum Pembuatan Preparat Supravital Epitelium Mukosa Mulut. Semarang: Universitas Negeri Semarang.
Hasibuan, S, I, 2022. Isolasi DNA: Dengan Metode Sederhana, Konvensional, dan Modern. Medan: Universitas Muslim Nusantara Al -Washliyah
Istanti, Annie, 1999. Biologi Sel. Malang: jurusan biologi FMIPA Universitas Negeri Malang
Koentjoro, M, P, dkk, 2021. Modifikasi Metode Isolasi DNA Cetyl Trimethylammonium Bromide (CTAB) Untuk Sampek Epitel Pipi Manusia. Jurnal Laboratorium Kedokteran dan Sains Indonesia. 2(2).
Koswara, Sutrisno, 2009. Penuntun Praktikum Dasar-Dasar Biokimia Pangan. Bogor: IPB Press.
Lehninger AL, 1982. Dasar-Dasar Biokimia Jilid 3. Maggy Thenawijaya, penerjemah. Jakarta: Erlangga.
Maftuchah, dkk, 2015. Teknik Dasar Analisis Biologi Molekuler.
Yogyakarta: Deepublish
Nurhayati, B, dkk, 2017. Biologi Sel dan Molekuler. Bahan Ajar Teknologi Laboratorium Medis (TLM)
Pingoud,A., A, Jeltsch, 2001. Structure and Function Of Type II Restriction Endonucleases. Nucleic Acid Research.
Prasetyo, A, 2008. Karakterisasi Virus Pada Tanaman Jarak Pagar (Jatropha curcas L.) Fakultas Pertanian Uiversitas Gadjah Mada.
Tim Dosen Biokimia, 2021. Petunjuk Praktikum Biokimia. Surabaya:
Jurusan kimia FMIPA UNESA
Triani, N, 2020. Isolasi DNA Tanaman Jeruk dengan Mengunakan Metode CTAB. Malang: Universitas Islam Raden Rahmat
Wahyudiati, D, 2017. Buku Biokimia. Leppim Mataram. Mataram:
Universitas Islam Negeri Mataram.
L. Lampiran Foto
Dokumentasi Keterangan
Larutan isotonic dan aquades diambil 10 ml lalu digunakan untuk berkumur selama 1 menit
Larutan isotonic yang sudah dikumur dimasukkan ke dalam gelas kimia lalu dipindahkan ke dalam tabung sentrifuge
Larutan aquades yang sudah dikumur dimasukkan ke dalam gelas kimia lalu dipindahkan ke dalam tabung sentrifuge
Larutan isotonic dan
aquades sebelum
disentrifuge
Larutan isotonic dan aquades di sentrifuge dengan kecepatan 10.000 rpm selama 5 menit
Larutan isotonic dan aquades setelah disentrifuge
Ditambahkan 1 ml buffer Tris-EDTA pada larutan isotonic dan aquades
Larutan isotonik dan aquades divortex sampai endapan hancur
Larutan isotonik dan aquades setelah divortex
1000 mikroliter NaCl 2,5 M dimasukkan ke dalam tabung sentrifuge yang berisi larutan sampel (isotonic dan aquades)
Dipindahkan semua isi tabung sentrifuge ke dalam tabung reaksi yang bersih dan kering
Ditambahkan 1 ml etanol dingin pada larutan isotonic
Ditambahkan 1 ml etanol dingin pada larutan aquades
Larutan isotonic dan aquades dibiarkan selama 5 menit dan terbentuk benang-benang DNA
Terdapat benang-benang pada larutan isotonic
Terdapat benang-benang pada larutan aquades
Diukur nilai absorbansi dengan spektro UV-VIS pada panjang gelombang 260 nm
Nilai absorbansi larutan aquades: 3,3913
Nilai absorbansi larutan isotonic: 4,0000