PEMERIKSAAN CEMARAN LOGAM Pb, Cd DAN Cu PADA IKAN NILA (Oreochromis niloticus Linnaeus) SERTA AIR
SEKITAR KERAMBA DANAU MANINJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
YULIA ASMIRANTI NIM 151524052
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2017
PEMERIKSAAN CEMARAN LOGAM Pb, Cd DAN Cu PADA IKAN NILA (Oreochromis niloticus Linnaeus) SERTA AIR
SEKITAR KERAMBA DANAU MANINJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
YULIA ASMIRANTI NIM 151524052
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2017
PENGESAHAN SKRIPSI
PEMERIKSAAN CEMARAN LOGAM Pb, Cd DAN Cu PADA IKAN NILA (Oreochromis niloticus Linnaeus) SERTA AIR
SEKITAR KERAMBA DANAU MANINJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
YULIA ASMIRANTI NIM 151524052
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 3 Oktober 2017
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Prof. Dr. Masfria, M.S., Apt. Prof. Dr. rer. nat. Effendy De Lux Putra, S. U.,Apt.
NIP 195707231986012001 NIP 195306191983031001
Pembimbing II, Prof. Dr. Masfria, M.S., Apt.
NIP 195707231986012001
Sri Yuliasmi, S. Farm., M.Si., Apt. Dra. Suwarti Aris, M.Si., Apt.
NIP 198207032008122002 NIP 195107231982032001
Sri Yuliasmi, S. Farm., M.Si., Apt.
NIP 198207032008122002 Medan, Oktober 2017
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Masfria, M.S., Apt.
NIP 195707231986012001
KATA PENGANTAR Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan skripsi yang berjudul “Pemeriksaan Cemaran Logam Pb, Cd dan Cu Pada Ikan Nila (Oreochromis niloticus Linnaeus) Serta Air Sekitar Keramba Danau Maninjau Secara Spektrofotometri Serapan Atom”. Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis hendak menyampaikan rasa hormat dan terima kasih yang sebesar-besarnya kepada Ibu Prof. Dr. Masfria, M.S., Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas dan masukan selama masa pendidikan dan penelitian, kepada Ibu Prof. Dr. Masfria, M.S., Apt., dan Ibu Sri Yuliasmi, S.Farm., M.Si., Apt., selaku dosen pembimbing yang telah banyak memberikan bimbingan, arahan, dan bantuan selama masa penelitian dan penulisan skripsi ini berlangsung.
Penulis juga menyampaikan ucapan terima kasih kepada Bapak Prof. Dr. rer. nat.
Effendy De Lux Putra, S.U., Apt., dan ibu Dra. Suwarti Aris, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini dan Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama perkuliahan dan selaku penasehat akademik yang selalu memberikan bimbingan kepada penulis selama perkuliahan serta Bapak Drs. Nahitma Ginting, M.Si., Apt., selaku dosen pembimbing akademik yang selalu membimbing selama masa pendidikan.
Penulis juga ingin menyampaikan rasa terima kasih serta penghargaan yang tulus dan tak terhingga kepada suami tercinta Romadil Iswan, orang tua tersayang Ibunda Asma.B, Mertua Dasril Dt. Jangguk dan Faridah, Kakak Wandi Putra, adik Sri Ovanola dan anak-anak terkasih Ekwiyan Nevikh Rizano, Vasthi Zahra, serta Arisha Azzahra, atas doa dan dukungan baik moril maupun materil, juga sahabat-sahabat penulis serta teman-teman di Fakultas Farmasi Universitas Sumatera Utara semua yang telah membantu, memberikan dukungan dan menjadi penyemangat bagi penulis atas motivasi dan segala bantuan dalam penyelesaian skripsi ini yang tidak dapat disebutkan satu per satu.
Semoga Tuhan Yang Maha Kuasa memberikan balasan yang berlipat ganda kepada semua pihak yang telah membantu dalam penulisan skripsi ini.
Penulis menyadari bahwa skripsi ini masih banyak kekurangan. Oleh karena itu, sangat diharapkan kritik dan saran yang bersifat membangun dari semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, 06 Oktober 2017 Penulis,
Yulia Asmiranti NIM 151524052
SURAT PERNYATAAN TIDAK PLAGIAT
Saya yang bertanda tangan dibawah ini:
Nama : Yulia Asmiranti
Nomor Induk Mahasiswa : 151524052
Program Studi : Ekstensi Sarjana Farmasi
Judul Skripsi : Pemeriksaan Cemaran Logam Pb, Cd dan Cu pada Ikan Nila (Oreochromis niloticus Linnaeus) serta Air Sekitar Keramba Danau Maninjau Secara Spektrofotometri Serapan Atom
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri, dan belum pernah diajukan oleh orang lain untuk memperoleh gelar kesarjanaan di perguruan tinggi lain, dan bukan plagiat karena kutipan yag ditulis telah disebutkan sumbernya didalam daftar pustaka.
Apabila di kemudian hari ada pengaduan dari pihak lain karena didalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia mendapat sanksi apapun oleh Program Studi Fakultas Farmasi Universitas Sumatera Utara, dan bukan menjadi tanggung jawab pembimbing.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, 06 Oktober 2017 Yang membuat pernyataan
Yulia Asmiranti NIM 151524052
PEMERIKSAAN CEMARAN LOGAM Pb, Cd DAN Cu PADA IKAN NILA (Oreochromis niloticus Linnaeus) SERTA AIR SEKITAR KERAMBA
DANAU MANINJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Ikan nila merupakan salah satu ikan yang banyak dibudidayakan pada keramba di danau maninjau. Setiap tahun sering terjadi Tubo belerang yang menyebabkan kematian ikan secara masal dan menyebabkan penurunan kualitas air danau maninjau. Berbagai aktivitas di daerah sekitar danau dapat menghasilkan berbagai macam bahan pencemar, baik organik maupun anorganik yang secara langsung ataupun tidak langsung masuk ke perairan danau. Tujuan penelitian ini adalah untuk mengetahui kadar cemaran logam Pb, Cd dan Cu pada ikan nila (Oreochromis niloticus Linnaeus) serta air sekitar keramba danau Maninjau.
Sampel ikan nila dan air sekitar keramba diambil pada danau Maninjau Kabupaten Agam, Sumatera Barat dengan metode purposif. Preparasi sampel dilakukan dengan proses dekstruksi kering pada sampel ikan dan dekstruksi basah untuk sampel air. Pemeriksaan kadar cemaran logam Pb, Cd, dan Cu dilakukan dengan metode spektrofotometri serapan atom masing-masing pada panjang gelombang 283,3 nm, 228,8 nm dan 324,8 nm dengan nyala udara-asetilen.
Hasil penelitian menunjukkan bahwa kadar cemaran logam Pb, Cd dan Cu pada ikan (IK) sebesar (67±10,06)x10-3µg/g, (4,67±0,21)x10-3μg/g, 3,90940-3± 8,08x10-3 μg/g pada IK1, (97,42±6,08)x10-3μg/g, (3,54±0,24)x10-3μg/g, 2,71138±
1,13x10-3μg /g pada IK2 dan (61,81±6,06)x10-3μg /g, (3,47±0,25)x10-3μg /g, 4,55368±22,38x10-3μg /g pada IK3, serta air sekitar keramba (AK) sebesar (17,74±0,69)x10-3μg/ml, (0,66±16)x10-3μg/ml, (71,98±0,97)x10-3μg/ml pada AK1, (35,46±2,13)x10-3μg/ml, (0,85±0,05)x10-3μg/ml, (68,29±1,31)x10-3μg/ml pada AK2, (14,94±1,13)x10-3μg/ml, (1,02±0,28)x10-3μg/ml, (89,70±1,51)x 10-
3μg/ml pada AK3.
Kesimpulan penelitian ini adalah terdapat kandungan logam berat Pb, Cd dan Cu pada ikan nila (Orechromis niloticus Linnaeus) serta air sekitar keramba danau Maninjau yang masih berada di bawah batas maksimum yang ditetapkan.
Kata kunci: ikan nila, air sekitar keramba, Pb, Cd, Cu, destruksi kering, destruksi basah, spektrofotometri serapan atom.
EXAMINATION OF METAL CONTAMINATION SUCH Pb, Cd AND Cu ON NILE TILAPIA (Oreochromis niloticus Linnaeus) AND WATER
AROUND KERAMBA MANINJAU LAKE BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Nile tilapia is one of the many fish cultivated on the keramba in the maninjau lake. Every year there is often Tubo belerang that causing decline in lake water quality. The activies in the area around the lake can produce various kinds of pollutants, both organic and anorganic, that directly or indirectly into the lake water. The purposes of this research is to know the contamination value of metal such Pb, Cd and Cu on nile tilapia (Oreochromis niloticus Linnaeus) and water around keramba of Maninjau lake.
Sample of nile tilapia and water around keramba was taken on Maninjau lake of Agam district, West Sumatera Barat by purposive. Sample preparation was done by dry destruction process for fish and wet destruction for water water around keramba. Examination of metal contamination such Pb, Cd and Cu by atomic absorption spectrophotometry on wavelength 283.3 nm, 228.8 nm and 324.8 nm with flame air-asetilen.
The results showed that examination of metal contamination such Pb, Cd and Cu on nile tilapia (IK) is (67±10.06)x10-3µg /g, (4.67±0.21)x10-3μg /g, 3.90940-3±8.08x10-3 μg/g on IK1, (97.42±6.08)x10-3μg/g, (3.54±0.24)x10-3μg/g, 2.71138±1.13x10-3μg/g on IK2 and (61.81±6.06)x10-3μg/g, (3.47±0.25)x10-3μg/g, 4.55368± 22.38x10-3μg/g on IK3, The examination of metal contamination such Pb, Cd and Cu in water around keramba (AK) is (17.74±0.69)x10-3μg /ml, (0.66±16)x10-3μg/ml, (71.98±0.97)x10-3μg/ml on AK1, (35.46±2.13)x10-3μg/ml, (0.85±0.05)x10-3μg/ml, (68.29±1.31)x10-3μg/ml on AK2, (14.94±1.13)x10-3μg/ml, (1.02±0.28)x10-3μg/ml, (89.70±1.51)x10-3μg/ml on AK3.
The conclusion of research is found heavy metal content Pb, Cd on nile tilapia (Orechromis niloticus Linnaeus) and water around keramba of Maninjau lake still below the maximum threshold of heavy metal.
Kata kunci: nile tilapia, water around keramba, Pb, Cd, Cu, dry destruction, wet destruction, atomic absorption spectrophotometry
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN TIDAK PLAGIAT ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Ikan Nila ... 5
2.2 Air ... 6
2.3 Logam Berat ... 6
2.3.1 Logam Pb ... 7
2.3.2 Logam Cd... 8
2.3.3. Logam Cu ... 9
2.4 Destruksi ... 9
2.5 Spektrofotometri Serapan Atom ... 10
2.5.1 Instrumen Spektrofotometri Serapan Atom ... 10
2.5.2 Gangguan Spektrofotometri Serapan Atom ... 15
2.5.3 Validasi Metode ... 15
BAB III METODE PENELITIAN ... 18
3.1 Tempat dan Waktu Penelitian ... 18
3.2 Alat-alat ... 18
3.3 Bahan-bahan ... 18
3.3.1 Sampel ... 18
3.3.2 Pereaksi ... 19
3.3.3 Pembuatan Larutan HNO3 (1:1) ... 19
3.4 Identifikasi Sampel... 19
3.5 Prosedur Penelitian... 19
3.5.1 Pengambilan Sampel ... 19
3.5.2 Penyiapan Sampel... 19
3.5.2.1 Ikan Nila ... 19
3.5.2.2 Air ... ... 20
3.5.3 Proses Destruksi... ... 20
3.5.3.1 Proses Destruksi Kering Ikan Nila………… 20
3.5.3.1 Proses Destruksi Basah Air Sekitar Keramba. 21 3.5.4 Pemeriksaan Kuantitatif... 21
3.5.4.1Pembuatan Kurva Kalibrasi Pb ... 21
3.5.4.2 Pembuatan Kurva Kalibrasi Cd ... 22
3.5.4.3 Pembuatan Kurva Kalibrasi Cu Ikan nila ... 22
3.5.4.4 Pembuatan Kurva Kalibrasi Cu Air Sekitar Keramba Danau………...……….. 23
3.5.4.5 Penetapan Kadar Pb dalam Sampel ... 23
3.5.4.6 Penetapan Kadar Cd dalam Sampel ... 23
3.5.4.7 Penetapan Kadar Cu dalam Sampel Ikan Nila ... 24
3.5.4.8 Penetapan Kadar Cu dalam Sampel Air Sekitar Keramba Danau.. ... 24
3.5.5 Perhitungan Kadar Pb, Cd dan Cu dalam Sampel…. 24 3.5.6 Penolakan Hasil Pengamatan... 25
3.6 Validasi Metode ... 26
3.6.1 Uji Perolehan Kembali (recovery) ... 26
3.6.2 Uji Keseksamaan (presisi) ... 26
2.6.3 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation) ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Identifikasi Hewan ... 28
4.2 Analisis Kuantitatif ... 28
4.2.1 Kurva Kalibrasi Pb, Cd dan Cu dalam Sampel ... 28
4.2.2 Analisis Kadar Pb, Cd dan Cu dalam Sampel ... 30
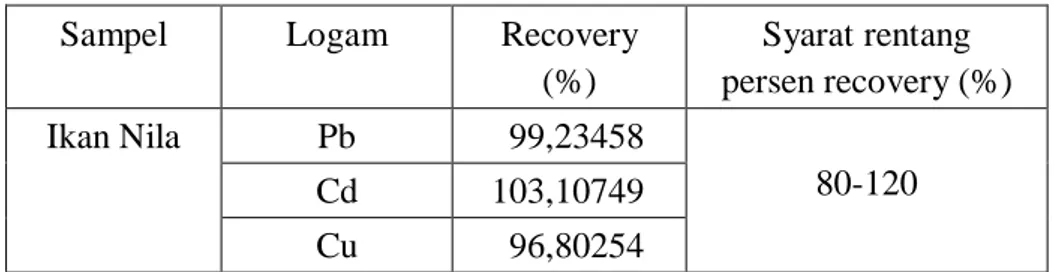
4.3 Uji Akurasi ... 33
4.4 Uji Presisi ... 34
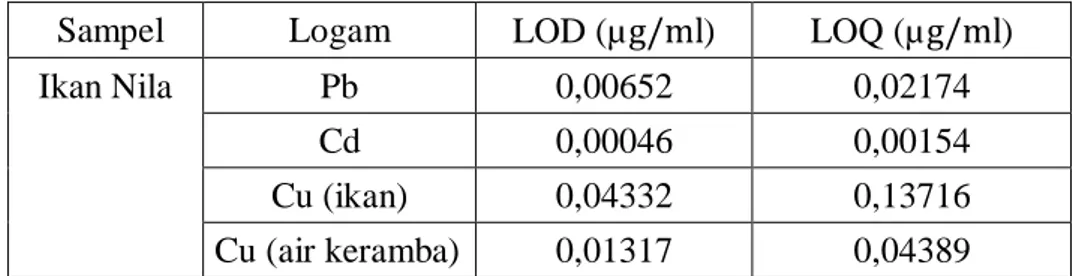
4.5 Batas Deteksi dan Batas Kuantitasi ... 35
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 39
LAMPIRAN ... 40
DAFTAR TABEL
Tabel Halaman
4.1 Hasil Analisis Kuantitatif Kadar Pb, Cd dan Cu dalam Sampel... 31
4.2 Batas Maksimum Cemaran Logam Pb, Cd dan Cu ... 32
4.3 Persen Uji Perolehan Kembali (Recovery) ... 34
4.4 Hasil Uji Presisi... ... 34
4.5 Batas Deteksi dan Batas Kuantitasi Pb, Cd dan Cu dalam Sampel .. 35
DAFTAR GAMBAR
Gambar Halaman
2.1 Komponen Spektrofotometri Serapan Atom ... 11
4.1 Gambar Kurva Kalibrasi Larutan Standar Pb… ... 28
4.2 Gambar Kurva Kalibrasi Larutan Standar Cd.. ... 29
4.3 Gambar Kurva Kalibrasi Larutan Standar Cu... 29
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil Identifikasi Ikan Nila ... 40
2 Gambar Sampel yang Digunakan ... 41
3 Gambar Alat-alat yang Digunakan ... 42
4 Bagan Alir Proses Destruksi Kering Ikan Nila ... 43
5 Bagan Alir Pembuatan Larutan Sampel ... 44
6 Bagan Alir Proses Destruksi Basah Air Sekitar Keramba ... 45
7 Data Hasil Pengukuran Absorbansi Larutan Standar Pb dan Perhitungan Persamaan Garis Regresi Pb ... 46
8 Data Hasil Pengukuran Absorbansi Larutan Standar Cd dan Perhitungan Persamaan Garis Regresi Cd ... 48
9 Data Hasil Pengukuran Absorbansi Larutan Standar Cu dan Perhitungan Persamaan Garis Regresi Cu pada Ikan Nila ... 50
10 Data Hasil Pengukuran Absorbansi Larutan Standar Cu dan Perhitungan Persamaan Garis Regresi Cu pada Air Sekitar Keramba Danau ... 52
11 Data Hasil Kadar Pb, Cd, dan Cu dalam Sampel Ikan Nila ... 54
12 Data Hasil Kadar Pb, Cd, dan Cu dalam Sampel Air Sekitar Keramba Danau ... 57
13 Contoh Perhitungan Kadar Pb, Cd dan Cu dalam Ikan Nila ... 60
14 Contoh Perhitungan Kadar Pb, Cd dan Cu dalam Air Sekitar Keramba Danau ... 62
15 Data Hasil Perhitungan Statistik Kadar Pb, Cd dan Cu ... 64
16 Contoh Perhitungan Statistik Kadar Pb, Cd dan Cu ... 73
17 Perhitungan Uji Akurasi Kadar Pb dalam Sampel Ikan Nila ... 88
18 Hasil Analisis Kadar Pb, Cd dan Cu Setelah Penambahan Masing-masing Larutan Standar pada Sampel ... 96
19 Perhitungan Uji Presisi Kadar Pb dalam Ikan Nila... 97 20 Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Pada Pb, Cd dan Cu ... 99 21 Tabel Distribusi t ... 103
BAB I PENDAHULUAN
1.1 Latar Belakang
Danau Maninjau merupakan danau vulkanik, yang secara administratif berada di kecamatan Tanjung Raya Kabupaten Agam dan terletak pada ketinggian 471 meter di atas permukaan laut. Secara keseluruhan luas Danau Maninjau mencapai 10,772 Ha atau sekitar 43,94 % dari luas kecamatan Tanjung Raya (4,8 % dari luas Kabupaten Agam), dengan kedalaman sekitar 157 meter dan keliling sekitar 66.000 meter (Anonim, 2000).
Pengembangan keramba yang sangat pesat dengan pemberian makanan berlebihan (±50-70 ton pakan/hari) menyebabkan banyak sisa makanan yang menumpuk di dasar danau, selain itu kotoran (feses) ikan juga menumpuk di dasar danau. Bahan-bahan organik ini kemudian diuraikan oleh mikroba yang memerlukaan banyak oksigen hingga mengakibatkan air di dasar danau kehabisan oksigen (anoksik) dan mengandung sulfur (belerang) yang beracun. Perubahan cuaca yang muncul bersamaan dengan bertiupnya angin barat menyebabkan berfluktuasinya air danau yang mengakibatkan lapisan dasar danau ini terangkat ke atas (overturn) maka ikan yang ada di permukaan akan mati secara masal karena kehabisan oksigen dan keracunan (Nontji, 2016). Kematian massal ikan ini dikenal oleh masyarakat sekitar dengan istilah Tubo Belerang. Kejadian ini diperkirakan akan menurunkan kualitas air. Penurunan kualitas air danau ini dapat memberikan dampak buruk bagi organisme yang hidup didalamnya.
Ikan nila (Oreochromis niloticus Linnaeus) merupakan salah satu hasil perikanan air tawar yang banyak dikonsumsi masyarakat. Keunggulan ikan ini
yaitu memiliki rasa yang spesifik, daging padat, tidak mempunyai banyak duri dan mudah dibudidayakan (Ardita, dkk., 2015). Ikan nila merupakan salah satu ikan yang banyak dibudidayakan pada keramba di Danau Maninjau. Menurut Hidayah, dkk. (2012) sebagai tempat pengembangan perikanan budidaya maka kualitas air sangat menentukan kelangsungan usaha dan hasil produksinya yang aman untuk dikonsumsi oleh manusia.
Keberagaman kegiatan pada Danau Maninjau telah menimbulkan resiko penurunan kualitas lingkungan perairan Danau Maninjau, diantaranya asap perahu motor yang digunakan masyarakat. Timbal merupakan salah satu zat yang ditambahkan ke dalam bahan bakar (premium) yaitu (C2H5)4Pb atau TEL (Tetra Ethyl Lead) yang berfungsi meningkatkan angka oktan sehingga mesin bisa bekerja dengan baik (Widowati, dkk., 2008). Secara alamiah, Pb dapat masuk ke badan perairan melalui pengkristalan Pb di udara dengan bantuan air hujan. Proses korosifikasi dari batuan mineral akibat hempasan gelombang dan angin, juga merupakan salah satu jalur sumber Pb yang akan masuk kedalam badan perairan (Palar, 2008).
Secara alamiah tembaga (Cu) masuk kedalam badan perairan akibat peristiwa erosi atau pengikisan batuan mineral dan melalui persenyawaan Cu di atmosfir yang dibawa turun oleh air hujan dan sebagai efek samping dari aktivitas yang dilakukan oleh manusia (Palar, 2008).
Menurut penelitian Yusuf, dkk. (2011) terdapat kandungan logam Fe, Cu, Pb dan Cd dalam sedimen sekitar keramba di perairan Danau Maninjau melebihi ambang batas yang berasal dari sedimen pakan ikan dan limbah vulkanik lainnya.
Tahun 2015 juga ditemukan adanya kandungan logam Cd, Cu, Fe, dan Zn pada
air, sedimen dan biota (Oxyeleotris marmorata dan Rasbora lateristriata) di Danau Maninjau (Syandri, dkk., 2015). Berbagai aktivitas di daerah sekitar danau dapat menghasilkan berbagai macam bahan pencemar, baik organik maupun anorganik yang secara langsung ataupun tidak langsung masuk ke perairan danau (Marganof, dkk., 2007). Sumber percemaran ini berasal dari limbah domestik, pertanian, serta budidaya ikan keramba.
Menurut Wardhana (2004), apabila bahan buangan anorganik masuk kedalam air maka akan terjadi peningkatan jumlah ion logam didalam air. Bahan buangan anorganik biasanya melibatkan unsur-unsur logam seperti Timbal (Pb), Arsen (As), Kadmium (Cd), Air Raksa (Hg), Krom (Cr), Nikel (Ni), Kalsium (Ca), Magnesium (Mg), Kobalt (Co) dan lain-lain.
Berdasarkan latar belakang tersebut, maka peneliti melakukan penelitian ini untuk mengetahui kadar Pb, Cd dan Cu pada ikan nila serta air sekitar keramba Danau Maninjau. Metode yang dipilih untuk penetapan kadar Pb, Cd dan Cu pada ikan nila serta air sekitar keramba danau Maninjau adalah menggunakan spektrofotometri serapan atom.
1.2 Perumusan Masalah
Berdasarkan latar belakang diatas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
a. Apakah ikan nila mengandung cemaran logam Pb, Cd, dan Cu?
b. Apakah air sekitar keramba Danau Maninjau mengandung cemaran logam Pb, Cd, dan Cu?
1.3 Hipotesis
Berdasarkan masalah yang dirumuskan diatas, maka hipotesis dalam penelitian ini adalah sebagai berikut:
a. Ikan nila mengandung cemaran logam Pb, Cd, dan Cu.
b. Air sekitar keramba Danau Maninjau mengandung cemaran logam Pb, Cd, dan Cu.
1.4 Tujuan Penelitian Penelitian ini bertujuan untuk:
a. Mengetahui kadar cemaran logam Pb, Cd, Cu pada ikan nila
b. Mengetahui kadar cemaran logam Pb, Cd, Cu pada air sekitar keramba Danau Maninjau
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat dan instansi terkait tentang adanya cemaran logam Pb, Cd, dan Cu pada ikan nila serta air sekitar keramba Danau Maninjau yang masih berada dibawah ambang batas yang disyaratkan sehingga ikan nila Danau Maninjau tersebut aman untuk dikonsumsi oleh masyarakat, namun perlu diperhatikan akumulasinya dalam tubuh untuk jangka waktu lama.
BAB II
TINJAUAN PUSTAKA
2.1. Ikan Nila (Oreochromis niloticus Linnaeus)
Ikan nila sangat dikenal oleh masyarakat penggemar air tawar. Ikan nila merupakan jenis ikan pendatang yang diintroduksi ke Indonesia. Ikan ini tergolong ikan pemakan segala atau omnivora (mengkonsumsi hewan dan tumbuhan), sehingga ikan ini mudah dibudidayakan. Makanan yang disukai ikan nila ketika masih benih adalah zooplankton, serta alga atau lumut yang menempel pada benda-benda dihabitatnya. Ikan nila juga memakan tanaman air yang tumbuh di kolam budidaya, jika sudah dewasa ikan ini diberi pelet sebagai makan tambahannya (Amri dan Khairuman, 2003).
Berdasarkan data FAO, kebutuhan ikan untuk pasar dunia sampai tahun 2010 masih kekurangan pasokan sebesar 2 juta ton/tahun, serta 0,5 ton pertahun untuk pasar domestik. Tingginya tingkat permintaan konsumen ikan sehingga ikan nila banyak dibudidayakan. Ikan nila memiliki toleransi hidup yang cukup tinggi sehingga habitat hidupnya beragam, seperti sungai, danau, waduk, sawah, rawa hingga tambak. Ikan ini dapat tumbuh normal pada habitatnya dengan suhu 14-380 C dan suhu optimum 25-300 C untuk pertumbuhan dan perkembangannya (Amri dan Khairuman, 2003).
Produksi ikan nila di Indonesia menduduki urutan ketiga untuk ikan kolam air tawar setelah ikan mas dan tawes (Amri dan Khairuman, 2003). Ikan nila sangat cocok dipelihara di perairan tenang, kolam, maupun reservoir. Ikan nila disukai masyarakat karena memiliki tekstur daging yang kesat dan rasa yang lezat serta harga yang terjangkau (Susanto, 2014).
2.2. Air
Air merupakan salah satu unsur yang sangat penting bagi hidup dan kehidupan manusia, flora, fauna dan makhluk hidup lainnya. Manusia memerlukan air tidak hanya sebagai zat makanan pendukung metabolisme tubuh, melainkan juga untuk kepentingan lainnya. Penyediaan air untuk kehidupan di bumi diatur atau mengikuti suatu siklus hidrologi, yaitu suatu siklus yang menggambarkan sirkulasi air secara terus-menerus melalui proses alami. Suplai air yang tersedia bagi manusia dan organisme lainnya dapat diperoleh dari dua sumber, yaitu air permukaan dan air tanah(Fauzi, dkk., 2011).
Air danau merupakan salah satu sumber air yang dimanfaatkan oleh manusia untuk menyokong berbagai aktivitas kehidupan. Pemanfaatan air dan lingkungan sekitar danau tanpa mempertimbangkan pelestarian lingkungan danau telah menyababkan berbagai kerusakan pada ekosistem danau termasuk kualitas dan kuantitas air danau. Penurunan kualitas air salah satunya terlihat pada Danau Maninjau yang tercemar akibat aktivitas kehidupan berlebihan disekitar danau sehingga Danau Maninjau masuk dalam 15 danau yang menjadi prioritas penyelamatan Pemerintah (Fauzi, dkk., 2014).
2.3. Logam Berat
Unsur logam secara luas ditemukan pada seluruh permukaan bumi. Unsur logam terkandung di tanah, batuan, badan air, bahkan pada lapisan atmosfir yang menyelimuti bumi. Logam-logam di alam umumnya ditemukan dalam bentuk persenyawaan dengan unsur lain, dan sangat jarang yang ditemukan dalam bentuk elemen tunggal (Palar, 2008).
Keberadaan logam-logam dalam badan perairan dapat berasal dari sumber- sumber alamiah dan berbagai aktivitas yang dilakukan oleh manusia. Sumber-
sumber logam yang masuk dalam perairan bisa berupa pengikisan dari bebatuan mineral yang banyak disekitar perairan, partikel-partikel yang ada diudara dan hujan. Logam yang berasal dari aktivitas manusia dapat berupa buangan sisa industri ataupun buangan rumah tangga (Palar, 2008).
Logam-logam berat memiliki daya racun yang mematikan terhadap organisme pada kondisi yang berbeda-beda. Logam-logam ini dapat mengakibatkan kematian biota perairan bila konsentrasi kelarutannya pada badan perairan melebihi nilai ambang batas. Logam berat dalam jumlah sedikit dan dalam waktu yang lama juga dapat mematikan, dimana terjadi akumulasi dalam organ target tubuh biota yang melebihi daya toleransi biota tersebut (Palar, 2008).
Daya racun dari logam berat yang terlarut dalam perairan dapat dipengaruhi oleh beberapa faktor, diantaranya bentuk logam dalam air, keberadaan logam-logam lain, fisiologis dari biota, dan kondisi biota (Palar, 2008).
2.3.1 Logam Pb
Timbal (Pb) secara alami terdapat di dalam kerak bumi. Keberadaan timbal dapat juga berasal dari kegiatan manusia yang mencapai 300 kali lebih banyak dibandingkan Pb alami. Pb adalah logam lunak berwarna abu-abu kebiruan, memiliki titik lebur rendah, mudah dibentuk, memiliki sifat kimia yang aktif, sehingga bisa digunakan untuk melapisi logam agar tidak timbul perkaratan (Widowati, dkk., 2008).
Keracunan Pb timbul akibat masuknya senyawa Pb ke dalam tubuh. Proses masuknya Pb ke dalam tubuh dapat melalui beberapa jalur, yaitu melalui makanan dan minuman, udara serta perembesan atau penetrasi pada selaput atau lapisan kulit. Sekitar 5-10% senyawa Pb masuk ke dalam tubuh melalui makanan, dan
30% terhirup pada saat bernafas akan diserap oleh tubuh, dimana hanya 15% yang mengendap pada jaringan tubuh dan sisanya akan terbuang bersama sisa metabolisme seperti urin dan feses (Palar, 2008).
Paparan Pb secara terus menerus bisa mengakibatkan kelelahan, gangguan gastrointestinal, infertilitas pada laki-laki, gangguan menstruasi pada wanita, depresi, sakit kepala, sulit berkonsentrasi, gangguan daya ingat dan sulit tidur (Widowati, dkk., 2008).
Toksisitas Pb secara akut dapat menyebabkan gangguang intestinal seperti kram perut, kolik, sembelit, mual,dan muntah, gangguan neurologi seperti sakit kepala, sering pingsan dan koma, serta gangguan fungsi ginjal (Widowati, dkk., 2008).
2.3.2 Logam Cd
Kadmuim (Cd) adalah logam berwarna putih perak, lunak, mengkilap, tidak larut dalam basa, mudah bereaksi dan mengasilkan kadmium oksida bila dipanaskan. Cd umumnya terdapat dalam kombinasi dengan klor atau belerang (Widowati, dkk., 2008). Logam Cd dapat ditemukan di daerah-daerah pembuangan sampah dan aliran air hujan serta air buangan. Logam Cd membawa sifat racun yang sangat merugikan bagi semua organisme hidup, dan sangat berbahaya untuk manusia. Dalam badan perairan, kelarutan Cd dalam kosentrasi tertentu dapat membunuh biota perairan (Palar, 2008).
Peristiwa keracunan Cd akut memiliki gejala timbulnya rasa sakit dan panas pada bagian dada yang muncul 4-10 jam setelah penderita terpapar oleh uap logam Cd ataupun CdO yang dapat menimbulkan penyakit paru-paru akut, sementara keracunan yang bersifat kronis disebabkan masuknya logam Cd ke dalam tubuh dalam jumlah kecil sehingga masih dapat ditolerir oleh tubuh, namun
jika terjadi secara terus-menerus maka tubuh tidak lagi mampu memberikan toleransi terhadap daya racun logam Cd tersebut (Palar, 2008).
2.3.3 Logam Cu
Tembaga atau cuprum merupakan unsur logam yang berbentuk Kristal dengan warna kemerahan. Unsur tembaga dapat ditemukan dalam bentuk logam bebas di alam, akan tetapi lebih banyak dalam bentuk persenyawaan sebagai senyawa padat dalam bentuk mineral. Cu merupakan logam berat yang berbeda dengan logam-logam lainnya seperti Hg, Cd, dan Cr. Logam berat Cu digolongkan ke dalam logam berat essensial: artinya, meskipun Cu merupakan logam berat beracun, unsur logam ini sangat dibutuhkan tubuh meski dalam jumlah yang sedikit. Toksisitas logam Cu akan terlihat bila logam ini masuk ke dalam tubuh organisme dalam jumlah besar atau melebihi nilai toleransi organisme tersebut (Palar, 2008). Kelebihan tembaga secara kronis menyebabkan penumpukan tembaga di dalam hati yang dapat menyebabkan nekrosis hati atau serosis hati (Almatsier, 2002).
2.4. Destruksi
Destruksi merupakan proses perusakan oksidatif dari bahan organik sebelum penetapan suatu analit anorganik atau untuk memecah ikatan dengan logam. Matriks atau ion-ion yang mengganggu dalam proses analisis dihilangkan dengan proses destruksi, dimana yang diharapkan tertinggal hanya logam logamnya saja. Dalam pendestruksian hendaknya memilih zat pengoksidasi yang cocok, baik untuk logam maupun jenis sampel-sampel yang akan dianalisis.
Secara umum, destruksi ada dua yaitu destruksi basah dan destruksi kering (Dewi, 2012).
Destruksi basah adalah perombakan sampel dengan asam-asam kuat seperti H2SO4, HNO3, H2O2, HClO4 baik tunggal maupun campuran, kemudian dioksidasi menggunakan zat pengoksidator. Keberhasilan destruksi ini ditandai dengan diperolehnya cairan jernih pada larutan destruksi dimana perombakan senyawa-senyawa organik telah berjalan dengan baik. Sementara destruksi kering merupakan perombakan logam organik menjadi logam anorganik dengan jalan pengabuan dengan suhu pemanasan tertentu pada sampel (Kristianingrum, 2012).
2.5. Spektrofotometri Serapan Atom
Prinsip dari spektrofotometri serapan atom adalah absorbsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu sesuai dengan sifat unsurnya (Gandjar dan Rohman, 2008), dimana atom-atom suatu logam diuapkan dalam suatu nyala dan radiasinya dilewatkan melalui nyala tersebut (Watson, 2009). Keberhasilan analisis spektrofotometri serapan atom tergantung pada proses eksitasi dan cara memperoleh garis resonansi yang tepat (Gandjar dan Rohman, 2008).
Spektrofotometri serapan atom memiliki beberapa keuntungan antara lain dapat digunakan untuk analisis logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), dan pelaksanaannya relatif sederhana (Gandjar dan Rohman, 2008), kecepatan analisis serta bahan yang digunakan sedikit dan spesifik untuk setiap logam tanpa dilakukan pemisahan terlebih dahulu (Khopkar, 1985).
2.5.1 Instrumen Spektrofotometri Serapan Atom
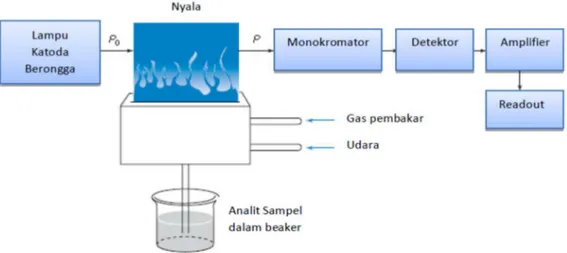
Menurut Harris (2007), sistem peralatan spektrofotometri serapan atom dapat dilihat pada Gambar berikut ini.
Gambar 2.1 Komponen Spektrofotometri Serapan Atom (Harris, 2007) a. Sumber Sinar
Sumber sinar yang sering dipakai adalah lampu katoda berongga (hollow cathoda lamp). Lampu terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari logam atau dilapisi oleh logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan yang tinggi (600 volt), maka katoda akan memancarkan berkas-berkas elektron yang bergerak menuju anoda dimana kecepatan dan energinya sangat tinggi. Elektron-elektron dengan energi tinggi ini dalam perjalanannya menuju anoda akan bertabrakkan dengan gas-gas mulia yang diisikan tadi. Akibat dari tabrakkan-tabrakkan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan menjadi bermuatan positif. Ion-ion gas mulia yang bermuatan positif ini selanjutnya akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi pula. Pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar dari permukaan katoda. Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat energi elektron yang lebih tinggi dan
akan memancarkan spektrum pencaran dari unsur yang sama dengan unsur yang akan dianalisis (Gandjar dan Rohman, 2008).
a. Tempat Sampel
Sampel yang akan dianalisis dengan spektrofotometri serapan atom harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala (flame) dan dengan tanpa nyala (flameless) (Gandjar dan Rohman, 2008).
1. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas-gas yang digunakan, misalkan untuk gas batu bara-udara, suhunya kira-kira sebesar 18000C, Asetilen-udara 22000C, dan gas asetilen-dinitrogen oksida (N2O) 30000C (Gandjar dan Rohman, 2008).
Pemilihan bahan bakar dan gas pengoksidasi serta komposisi perbandingannya sangat mempengaruhi suhu nyala. Sumber nyala yang paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi. Propana-udara dipilih untuk logam-logam alkali karena suhu nyala yang lebih rendah akan mengurangi banyaknya ionisasi (Gandjar dan Rohman, 2008).
Cara pengatoman pada nyala yaitu dengan memasukkan sampel ke dalam nyala dengan cara yang ajeg dan seragam membutuhkan suatu alat yang mampu mendispersikan sampel secara seragam di dalam nyala. Ada beberapa cara atomisasi dengan nyala ini, yaitu :
a. Cara langsung (Pembakaran konsumsi total atau total consumption burner) Pada cara ini, sampel diaspirasikan secara langsung ke dalam nyala, dan semua sampel akan dibakar oleh pembakar. Variasi ukuran kabut (droplet) sangat besar. Diameter partikel rata-rata sebesar 20 mikron, dan sejumlah partikel ada yang mempunyai diameter lebih besar 40 mikron. Semakin besar kabut yang melewati nyala (tanpa semuanya diuapkan), maka efisiensinya semakin rendah (Gandjar dan Rohman, 2008).
b. Cara tidak langsung
Pada model ini, larutan sampel dicampur terlebih dahulu dengan bahan pembakar dan bahan pengoksidasi dalam suatu kamar pencampuran sebelum dibakar. Tetesan-tetesan yang besar akan tertahan dan tidak masuk ke dalam nyala. Dengan cara ini, ukuran terbesar yang masuk ke dalam nyala ± 10 mikron sehingga nyala lebih stabil dibandingkan dengan cara langsung. Masalah yang terkait dengan penggunaan cara ini adalah adanya kemungkinan nyala membakar pencampuran dan terjadinya ledakan. Akan tetapi, hal ini dapat dihindari dengan menggunakan lubang sempit atau dengan cara mematuhi aturan yang benar terkait dengan cara menghidupkan gas (Gandjar dan Rohman, 2008).
2. Tanpa nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka karena atom gagal mencapai nyala, tetesan sampel yang masuk ke dalam nyala terlalu besar, dan proses atomisasi kurang sempurna. Oleh karena itu muncullah suatu teknik atomisasi baru yakni atomisasi tanpa nyala. Pengatoman dapat dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit (untuk sampel cair diambil hanya beberapa µL, sementara sampel padat diambil beberapa mg), lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan
sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadi proses penyerapan energi yang memenuhi kaidah analisa kuantitatif (Gandjar dan Rohman, 2008).
Sistem pemanasan tanpa nyala ini dapat melalui 3 tahap yaitu:
pengeringan (drying) yang membutuhkan suhu yang relatif rendah, pengabuan (ashing) yang membutuhkan suhu yang lebih tinggi karena untuk menghilangkan matriks kimia dengan mekanisme volatilasi atau pirolisis, dan pengatoman (atomising). Pada umumnya waktu dan suhu pemanasan tanpa nyala dilakukan dengan cara terprogram (Gandjar dan Rohman, 2008).
c. Monokromator
Monokromator digunakan untuk memisahkan dan memilih panjang gelombang yang digunakan dalam analisis. Alat untuk memisahkan radiasi resonansi dan kontinyu dikenal dengan chopper (Gandjar dan Rohman, 2008).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman. Biasanya digunakan tabung penggandaan foton. Ada 2 cara yang dapat digunakan dalam sistem deteksi yaitu: yang memberikan respon terhadap radiasi resonansi dan radiasi kontinyu dan yang hanya memberikan respon terhadap radiasi resonansi (Gandjar dan Rohman, 2008).
e. Sistem Pengolah (Amplifier)
Sistem pengolah atau Amplifier merupakan suatu alat untuk memperkuat signal yang diterima dari detektor sehingga dapat dibaca alat pencatat hasil atau Readout.
f. Pencatat hasil (Readout)
Pencatat hasil (Readout) merupakan suatu alat penunjuk hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2008).
2.5.2 Gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan pada spektrofotometri serapan atom adalah peristiwa- peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis lebih kecil atau bahkan lebih besar daripada konsentrasi yang terkandung dalam sampel. Gangguan-gangguan yang dapat terjadi adalah sebagai berikut:
a. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
b. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi dalam nyala
c. Gangguan oleh absorbansi yang disebabkan oleh bukan dari absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di dalam nyala.
d. Gangguan oleh penyerapan non-atomik yang disebabkan karena adanya penyerapan cahaya oleh partikel-partikel padat yang berada di dalam nyala (Gandjar dan Rohman, 2008).
2.5.3 Validasi Metode
Validasi metoda analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis menurut Harmita (2004) adalah sebagai berikut :
a. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara yaitu :
- Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
- Metode penambahan baku (standard addition method)
Dalam metode penambahan baku (standard addition method), sampel dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang diharapkan). Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
b. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan keseksamaan metode yang dilakukan (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel (Harmita, 2004).
d. Linearitas
Linearitas adalah kemampuan metode analisis yang memberikan respon yang secara langsung atau dengan bantuan transformasi matematik yang baik, proposional terhadap konsentrasi analit dalam sampel. Perlakuan matematik dalam pengujian linearitas adalah melalui persamaan garis lurus dengan metode kuadrat terkecil antara hasil analisis terhadap konsentrasi analit (Harmita, 2004).
e. Batas Deteksi dan Batas Kuantitasi
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang masih dapat dideteksi dan memberikan respon signifikan tetapi tidak dikuantitasi pada kondisi percobaan yang dilakukan. (Harmita, 2004).
Batas kuantitasi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi. Batas ini dinyatakan dalam konsentrasi analit (persen, bagian per seribu) dalam sampel (Harmita, 2004).
BAB III
METODE PENELITIAN
Metode yang digunakan dalam penelitian ini adalah metode deskriptif yang bertujuan menggambarkan sifat dari suatu keadaan secara sistematis yaitu untuk melihat kadar logam Pb, Cd, dan Cu pada Ikan Nila serta Air Sekitar Keramba Danau Maninjau, Kabupaten Agam, Sumatera Barat.
3.1. Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan Februari 2017 – Mei 2017.
3.2. Alat-alat
Alat yang digunakan pada penelitian ini adalah Spektrofotometer Serapan Atom (Hitachi Zeeman-2000) dengan nyala udara-asetilen lengkap dengan lampu katoda Pb, Cd, dan Cu, alat–alat gelas (Pyrex dan Oberol), blender, bola karet, erlenmeyer 250 ml, hot plate (BOECO Germany), krus porselin, kertas saring Whatman No.42, neraca analitik (BOECO Germany), penjepit tabung, pipet tetes, pipet volume, spatula, tanur (Nabertherm).
3.3. Bahan-Bahan 3.3.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah Ikan Nila (Orechromis niloticus Linnaeus) siap panen dengan berat 0,5 g/ekor dan Air dengan kedalaman
± 2 meter yang berada di sekitar keramba Danau Maninjau, diambil di tiga lokasi berbeda yaitu pada Pakan Rabaa, Koto Gadang dan Muko-Muko, Kabupaten Agam, Sumatera Barat.
3.3.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisa keluaran E. Merck kecuali disebutkan lain yaitu aquademineralisata, larutan standar Pb konsentrasi 1000 µg/ml, larutan standar Cd konsentrasi 1000 µg/ml, larutan standar Cu 1000 µg/ml, asam nitrat 65% b/v.
3.3.3 Pembuatan Larutan HNO3 (1:1)
Asam Nitrat 65% sebanyak 100 ml diencerkan dengan aquademineralisata 100 ml (Ditjen POM RI, 1979).
3.4. Identifikasi Sampel
Identifikasi sampel Ikan Nila dilakukan di Laboratorium Sistematika Hewan, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
3.5. Prosedur Penelitian 3.5.1 Pengambilan Sampel
Sampel yang digunakan adalah Ikan Nila (Oreochromis niloticus Linnaeus) serta Air sekitar keramba yang diambil secara purposif di Danau Maninjau, Kabupaten Agam, Sumatera Barat. Metode pengambilan sampel dilakukan dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan, dimana sampel ditentukan atas dasar pertimbangan bahwa semua sampel mempunyai karakteristik yang sama dengan yang diteliti (Sudjana, 2009).
3.5.2 Penyiapan Sampel 3.5.2.1 Ikan nila
Sampel ikan nila dicuci bersih dengan air mengalir, diambil bagian daging, ditiriskan, kemudian dihaluskan dengan menggunakan blender. Sampel yang telah
halus ditimbang masing-masing 25 g dalam krus porselin yang telah diberi kode IK1 (Pakan Rabaa), IK2 (Koto Gadang), IK3 (Muko-Muko) pada sampel.
Perlakuan penimbangan dan penetapan kadar Pb, Cd, dan Cu, dilakukan sebanyak 6 kali.
3.5.2.2 Air
Sampel air yang berada sekitar keramba Danau Maninjau diambil sebanyak 1,5 liter, dimasukkan kedalam wadah gelas, dan diasamkan dengan penambahan HNO3 sampai pH<2, diberi kode AK1 (Pakan Rabaa), AK2 (Koto Gadang), AK3 (Muko-Muko) pada sampel. untuk kemudian dilakukan pengujian pada Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.5.3 Proses Destruksi
3.5.3.1 Proses Destruksi Kering Ikan Nila
Sampel terlebih dahulu dihomogenkan, kemudian ditimbang sebanyak 25 g menggunakan krus porselin, diarangkan diatas hot plate, diabukan dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit, dilakukan selama 48 jam dan dibiarkan hingga dingin didalam tanur. Abu yang diperoleh ditambahkan 5 ml HNO3 (1:1), diuapkan pada hot plate sampai kering, dimasukkan kembali dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit, dilakukan selama 1 jam dan dibiarkan hingga dingin didalam desikator (suhu ± 27ºC) (Isaac, 1990).
Sampel hasil destruksi dilarutkan dalam 5 ml HNO3 (1:1), lalu dipindahkan ke dalam labu tentukur 25 ml, dibilas krus porselin dengan 5 ml aquademineralisata sebanyak tiga kali dan dicukupkan dengan aquademineralisata hingga garis tanda. Kemudian disaring dengan kertas saring Whatman No. 42
dimana 5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat selanjutnya ditampung ke dalam botol.
3.5.3.2 Proses Destruksi Basah Air Sekitar Keramba
Sebanyak 100 ml sampel air dimasukkan ke dalam Erlenmeyer 250 ml.
Ditambahkan 10 ml HNO3 (P) ke dalam erlenmeyer menggunakan corong.
Cuplikan didestruksi pada hot plate hingga volumenya menjadi ± 10 ml (hingga larutan berwarna jernih), lalu dipindahkan ke dalam labu ukur 25 ml, dan dibilas dengan aquademineralisata sebanyak 3 kali. Kemudian disaring larutan dengan kertas Whatman 42 dan masukkan ke dalam botol.
3.5.4 Pemeriksaan Kuantitatif
3.5.4.1 Pembuatan kurva Kalibrasi Pb
Larutan standar timbal nitrat (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml, diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku I (LIB I) konsentrasi 10 µg/ml.
Dari LIB I (10 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku II (LIB II) konsentrasi 500 ppb.
Dari LIB II (500 ppb) dipipet masing-masing sebanyak 2,5 ml; 5 ml;
7,5 ml; 10 ml; dan 12,5 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 25 ml yang berbeda kemudian diencerkan dengan akuademineralisata hingga garis tanda dan dikocok homogen sehingga diperoleh konsentrasi 50 ppb; 100 ppb; 150 ppb; 200 ppb; 250 ppb, dan diukur absorbansi pada panjang gelombang 283,3 nm, atomisasi dilakukan dengan nyala udara- asetilen dengan laju alir 2,0 L/menit, tinggi burner 7,5 cm, dan lebar celah 0,7 nm.
3.5.4.2 Pembuatan kurva Kalibrasi Cd
Larutan standar kadmium nitrat (1000 µg/ml) sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku I (LIB I) konsentrasi 10 µg/ml.
Dari LIB I (10 µg/ml) dipipet sebanyak 0,1 ml, dimasukkan ke dalam labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku II (LIB II) konsentrasi 100 ppb.
Dari LIB II (100 ppb) dipipet masing-masing sebanyak 0,5 ml; 1 ml;
1,5 ml; 2 ml; 2,5 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 25 ml kemudian diencerkan dengan akuademineralisata hingga garis tanda dan dikocok homogen sehingga diperoleh konsentrasi 2 ppb; 4 ppb; 6 ppb; 8 ppb;
10 ppb dan diukur absorbansi pada panjang gelombang 228,8 nm, atomisasi dilakukan dengan nyala udara-asetilen dengan laju alir 2,0 L/menit, tinggi burner 5 cm, dan lebar celah 0,7 nm.
3.5.4.3 Pembuatan kurva Kalibrasi Cu ikan nila
Larutan standar tembaga nitrat (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku I (LIB I) konsentrasi 10 µg/ml.
Dari LIB I (10 µg/ml) dipipet masing-masing sebanyak 1,25 ml; 2,5 ml;
3,75 ml; 5 ml; 6,25 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 25 ml yang berbeda kemudian diencerkan dengan akuademineralisata hingga garis tanda dan dikocok homogen sehingga diperoleh konsentrasi 0,5 µg/ml; 1 µg/ml; 1,5 µg/ml; 2 µg/ml; 2,5 µg/ml dan diukur absorbansi pada
panjang gelombang 324,8 nm, atomisasi dilakukan dengan nyala udara-asetilen dengan laju alir 2,0 L/menit, tinggi burner 7,5 cm, dan lebar celah 0,7 nm.
3.5.4.4 Pembuatan kurva Kalibrasi Cu air sekitar keramba danau
Larutan standar tembaga nitrat (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuademineralisata disebut Larutan Induk Baku I (LIB I) konsentrasi 10 µg/ml.
Dari LIB I (10 µg/ml) dipipet masing-masing sebanyak 0,25 ml; 0,5 ml;
0,75 ml; 1 ml; 1,25 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 25 ml yang berbeda kemudian diencerkan dengan akuademineralisata hingga garis tanda dan dikocok homogen sehingga diperoleh konsentrasi 0,1 µg/ml; 0,2 µg/ml; 0,3 µg/ml; 0,4 µg/ml; 0,5 µg/ml dan diukur absorbansi pada panjang gelombang 324,8 nm.
3.5.4.5 Penetapan Kadar Pb dalam Sampel
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 283,3 nm dengan menggunakan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan standar timbal. Kosentrasi timbal dalam sampel ditentukan berdasarkan persamaan garis regresi dan kurva kalibrasi.
3.5.4.6 Penetapan Kadar Cd dalam Sampel
Larutan sampel hasil destruksi diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 228,8 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh berada didalam rentang nilai kurva kalibrasi larutan baku standar kadmium. Kosentrasi kadmium dalam sampel ditentukan berdasarkan persamaan garis regresi dan kurva kalibrasi.
3.5.4.7 Penetapan Kadar Cu dalam Sampel Ikan Nila
Larutan sampel hasil destruksi dipipet 12,5 ml dimasukkan ke dalam labu tentukur 25 mL dan dicukupkan dengan aquademineralisata hingga garis tanda (faktor pengenceran = 25/12,5 = 2 kali). Lalu diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 324,8 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh berada didalam rentang nilai kurva kalibrasi larutan baku standar tembaga. Kosentrasi tembaga dalam sampel ditentukan berdasarkan persamaan garis regresi dan kurva kalibrasi.
3.5.4.8 Penetapan Kadar Cu dalam Sampel Air
Larutan sampel hasil destruksi dimasukkan ke dalam labu tentukur 25 mL dan dicukupkan dengan aquademineralisata hingga garis tanda. Lalu diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 324,8 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh berada didalam rentang nilai kurva kalibrasi larutan baku standar tembaga. Kosentrasi tembaga dalam sampel ditentukan berdasarkan persamaan garis regresi dan kurva kalibrasi.
3.5.5 Perhitungan Kadar Pb, Cd, dan Cu dalam Sampel
Kadar Pb, Cd, dan Cu dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar (μg/g) =C × V × Fp W
Keterangan: C = Konsentrasi logam dalam larutan sampel (µg/mL) V = Volume larutan sampel (mL)
Fp = Faktor pengenceran W = Berat sampel (g)
3.5.6 Penolakan Hasil Pengamatan
Menurut (Sudjana, 2009) Pb, Cd, dan Cu yang diperoleh dari hasil pengukuran masing-masing larutan sampel diuji secara statistik dengan cara menghitung standar deviasi menggunakan rumus sebagai berikut:
= ∑(Xi − X) n − 1 Keterangan: Xi = Kadar sampel
= Kadar rata-rata sampel n = Jumlah pengulangan
Kadar yang diperoleh dari hasil pengukuran masing-masing ke enam larutan sampel, diuji secara statistik dengan uji t.
Untuk mengetahui data ditolak atau diterima dilakukan dengan uji t yang dapat dihitung dengan rumus:
thitung =
n SD
X Xi
/
−
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t, apabila thitung < ttabel maka data tersebut diterima.
Untuk menentukan kadar suatu zat di dalam sampel dengan interval kepercayaan 95%, α = 0,05, dk = n-1, dapat digunakan rumus:
μ = ± (!",$%)SD √n⁄ Keterangan: µ = kadar logam
= kadar rata-rata sampel
t = harga t tabel sesuai dengan dk = n-1 α = tingkat kepercayaan
SD = standar deviasi n = jumlah pengulangan
3.6 Validasi Metode
3.6.1 Uji Perolehan Kembali (recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar logam dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar logam dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu (Ermer dan McB. Miller, 2005).
Sampel (ikan nila) yang telah dihaluskan ditimbang sebanyak 25 g dalam krus porselin, lalu ditambahkan 0,4 ml larutan standar Pb (konsentrasi 500 ppb), 0,2 ml larutan standar Cd (konsentrasi 100 ppb) dan 1 ml larutan standar Cu (konsentrasi 10 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya pada prosedur destruksi sampel dan pengukuran masing-masing logam pada panjang gelombang 283,3 nm, 228,8 nm dan 324,8 nm.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus berikut ini:
Persen Perolehan Kembali = *+, *-
*-∗
/
100%Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku CF = Kadar logam dalam sampel setelah penambahan baku C*A = Kadar larutan baku yang ditambahkan
3.6.2 Uji Keseksamaan (Presisi)
Uji keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode
dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah:
0 =
123̅/100%
Keterangan: /̅ : Kadar rata-rata sampel SD : Standard Deviation
RSD : Relative Standard Deviation 3.6.3 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi (Limit of Detection) merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan.
Sebaliknya, batas kuantitas (Limit Of Quantitation) merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku = 7∑(898:)<9 ; Batas Deteksi (LOD)
=
?@ABC=×1>Batas Kuantitasi (LOQ)
=
!D×1>?@ABCBAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Hewan
Identifikasi hewan dilakukan di Laboratorium Sistematika Hewan, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara, Medan. Hasil identifikasi menunjukkan bahwa ikan yang digunakan adalah ikan nila dengan jenis Oreochromis niloticus dari suku Cichlidae. Hasil identifikasi hewan dapat dilihat pada Lampiran 1, Halaman 40.
4.2 Analisis Kuantitatif
4.2.1 Kurva Kalibrasi Pb, Cd dan Cu
Kurva kalibrasi Pb, Cd dan Cu diperoleh dengan cara memplotkan absorbansi dengan konsentrasi larutan baku standar pada panjang gelombang 283,3 nm untuk Pb, 228,8 nm untuk Cd dan 324,8 nm untuk Cu. Pada logam Cu menggunakan dua kurva kalibrasi.
Kurva kalibrasi larutan standar Pb, Cd dan Cu dapat dilihat pada Gambar 4.1-4.3
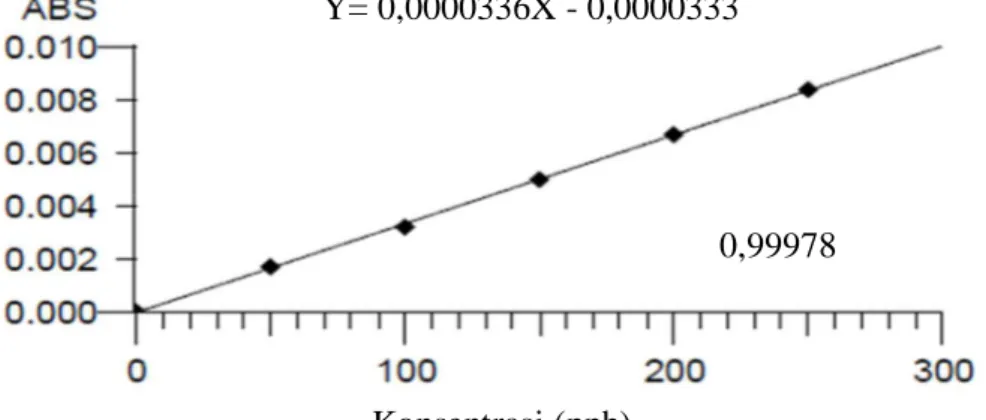
Gambar 4.1 Kurva Kalibrasi Larutan Standar Pb Y= 0,0000336X - 0,0000333
Konsentrasi(ppb)
0,99978
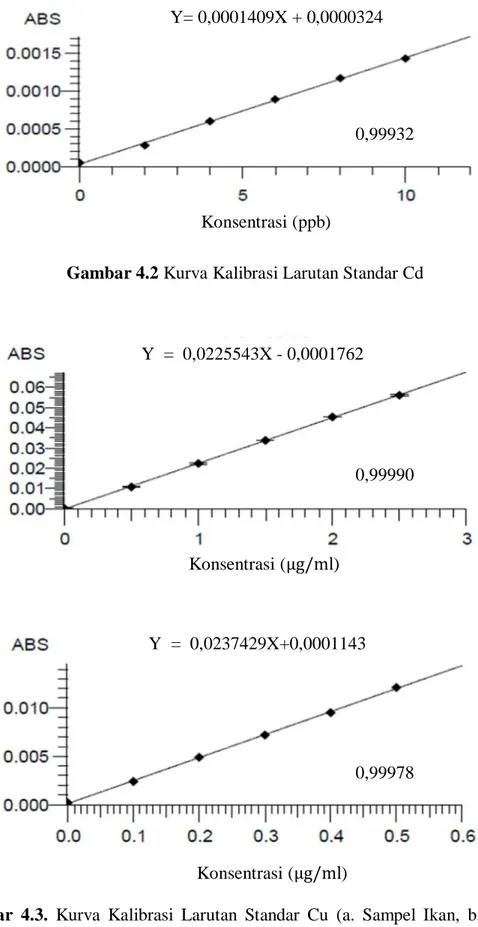
Gambar 4.2 Kurva Kalibrasi Larutan Standar Cd
Gambar 4.3. Kurva Kalibrasi Larutan Standar Cu (a. Sampel Ikan, b. Sampel Air)
Y= 0,0001409X + 0,0000324
Konsentrasi(ppb)
Konsentrasi(μg/ml) Y = 0,0225543X - 0,0001762
Y = 0,0237429X+0,0001143
Konsentrasi(μg/ml) a.
b.
0,99978 0,99990 0,99932
Dari pengukuran kurva kalibrasi diperoleh persamaan garis regresi yaitu Y= 0,0000336X-0,0000333 untuk Pb,Y= 0,0001409X+0,0000324 untuk Cd, dan dua kurva kalibrasi berbeda untuk Cu, dimana kurva kalibrasi Cu untuk sampel
ikan yaitu Y= 0,0225543X-0,0001762 dan untuk sampel air adalah Y= 0,0237429X+0,0001143.
Pada gambar 4.1-4.3 diperoleh hubungan yang linier antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) Pb sebesar 0,99978, Cd sebesar 0,99932, Cu sebesar 0,99990 dan 0,99978. Nilai r ≥ 0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi) (Ermer dan McB. Miller, 2005). Data hasil pengukuran absorbansi larutan standar Pb, Cd dan Cu dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 7-10, Halaman 46-53.
4.2.2 Analisis Kadar Pb, Cd dan Cu dalam Sampel
Penentuan kadar Pb, Cd dan Cu dilakukan secara Spektrofotometri Serapan Atom dengan nyala udara - asetilen (UA) dengan suhu nyala 2200°C.
Konsentrasi logam Pb, Cd dan Cu dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan standar masing-masing logam.
Hasil analisis kuantitatif kadar Pb, Cd dan Cu dapat dilihat pada Tabel 4.1 dibawah ini. Data dan contoh perhitungan dapat dilihat pada Lampiran 11-14, Halaman 54-63. Analisis dilanjutkan dengan perhitungan statistik, data dan contoh perhitungan dapat dilihat pada Lampiran 15-16, Halaman 64-87.
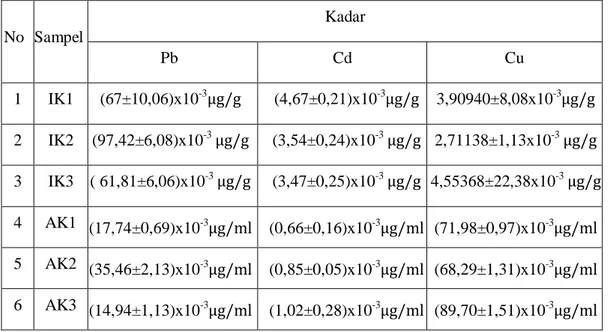
Tabel 4.1 Hasil Analisis Kuantitatif Kadar Pb, Cd dan Cu dalam Sampel
No Sampel
Kadar
Pb Cd Cu
1 IK1 (67±10,06)x10-3μg/g (4,67±0,21)x10-3μg/g 3,90940±8,08x10-3μg/g 2 IK2 (97,42±6,08)x10-3 μg/g (3,54±0,24)x10-3 μg/g 2,71138±1,13x10-3 μg/g 3 IK3 ( 61,81±6,06)x10-3 μg/g (3,47±0,25)x10-3 μg/g 4,55368±22,38x10-3 μg/g 4 AK1 (17,74±0,69)x10-3μg/ml (0,66±0,16)x10-3μg/ml (71,98±0,97)x10-3μg/ml 5 AK2 (35,46±2,13)x10-3μg/ml (0,85±0,05)x10-3μg/ml (68,29±1,31)x10-3μg/ml 6 AK3 (14,94±1,13)x10-3μg/ml (1,02±0,28)x10-3μg/ml (89,70±1,51)x10-3μg/ml
Keterangan :
IK1 : Ikan dari Pakan Rabaa, IK2 : Ikan dari Koto Gadang, IK3 : Ikan dari Muko-Muko AK1 : Air Sekitar Keramba dari Pakan Rabaa, AK2 : Air Sekitar Keramba dari Koto Gadang, AK3 : Air Sekitar Keramba dari Muko-Muko
Tabel 4.1 menunjukkan bahwa adanya kandungan cemaran logam Pb, Cd, dan Cu pada ikan nila serta air sekitar keramba danau Maninjau. Ikan sebagai salah satu biota air dapat dijadikan sebagai suatu indikator tingkat pencemaran yang terjadi di dalam perairan (Supriyanto, dkk., 2007). Berdasarkan hasil penelitian disimpulkan bahwa kandungan logam berat Pb, Cd dan Cu pada ikan nila lebih tinggi daripada kandungan logam Pb, Cd dan Cu pada air sekitar keramba, hal ini menjelaskan bahwa air bukanlah satu-satunya faktor penyebab terjadinya cemaran pada ikan nila. Sumber cemaran juga dapat disebabkan oleh pemberian pakan ikan yang berlebihan, penggunaan pestisida pada lahan pertanian di sekitar danau yang terbawa air hujan masuk ke danau, dan limbah domestik yang berasal dari limbah buangan rumah tangga dan limbah buangan perhotelan sekitar danau serta limbah vulkanik lainnya.
Tabel 4.2 Batas maksimum cemaran logam Pb, Cd dan Cu
Acuan Kategori Logam Batas
Maksimum SNI 7387 tahun 2009
tentang batas maksimum cemaran logam berat dalam pangan
Ikan dan hasil olahannya
Pb 0,3 mg/kg Cd 0,1 mg/kg SK Dirjen POM No.03725/B/SK/VII/89
tentang batas maksimum cemaran logam dalam makanan
Ikan dan hasil olahannya
Cu 20 mg/kg PP nomor 82 tahun 2001
tentang pengelolaan kualitas air dan pengendalian pencemaran air
Mutu air
Pb 0,03 mg/L Cd 0,01 mg/L Cu 0,02 mg/L Berdasarkan Tabel 4.1 dan Tabel 4.2 dapat disimpulkan bahwa kandungan cemaran logam Pb, Cd dan Cu pada ikan nila serta air sekitar keramba Danau Maninjau masih berada dibawah ambang batas yang ditetapkan.
Menurut Palar (2008), logam Cd membawa sifat racun yang sangat merugikan bagi semua organisme hidup, bahkan juga sangat berbahaya untuk manusia. Dalam badan perairan, kelarutan Cd dalam konsentrasi tertentu dapat membunuh biota perairan. Untuk biota air tawar, sebagai contoh ikan mas (cyprinus carpio) akan mengalami kematian dalam waktu 96 jam, bila dalam media hidupnya terkontaminasi oleh logam Cd dengan rentang konsentrasi 1,092- 1,104 µg/ml. (Sumber:Murphy P.M., Univ. of Wales Ins. Of Tech. and Sciences, 1974).
Tingkat dan lamanya paparan logam Cd akan mempengaruhi efek toksik dari Cd, semakin tinggi kadar dan semakin lama paparan, efek toksik yang diberikan semakin besar. Kadmium dalam dosis tunggal besar mampu menginduksi gangguan saluran pencernaan, sedangkan paparan Cd dalam dosis rendah tetapi berulang kali bisa mengakibatkan gangguan fungsi ginjal. Toksisitas kronis Cd bisa merusak sistem fisiologis tubuh, antara lain sistem urinaria, sistem