ISOLASI SENYAWA FLAVONOIDA DARI KULIT BAWANG
MERAH (
Allium cepa
L.)
SKRIPSI
CHRISTOU MAEDA RINGO
080802064
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ISOLASI SENYAWA FLAVONOIDA DARI KULIT BAWANG
MERAH (
Allium cepa
L.)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
CHRISTOU MAEDA RINGO
080802064
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ISOLASI SENYAWA FLAVONOIDA DARI KULIT
BAWANG MERAH (Allium cepa L.)
Kategori : SKRIPSI
Nama : CHRISTOU MAEDA RINGO
Nomor Induk mahasiswa : 080802064
Program studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Februari 2013
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dr. Sovia Lenny, M.Si Drs.Albert Pasaribu, M.Sc
NIP: 1975 1018 2000 032001 NIP: 1964 0810 1991 031002
Diketahui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ISOLASI SENYAWA FLAVONOIDA DARI DARI KULIT BAWANG
MERAH (
Allium cepa
L.)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Februari 2013
PENGHARGAAN
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Pemurah dan Maha Pengasih atas segala penyertaanNya sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi ini.
Ucapan terimakasih penulis sampaikan kepada Bapak Drs. Albert Pasaribu, M.Sc dan Ibu Dr. Sovia Lenny M.Si selaku dosen pembimbing yang telah banyak memberi bimbingan, arahan, ilmu dan waktu selama penulis melakukan penelitian dan penyusunan skripsi ini sampai selesai. Ucapan terima kasih juga ditujukan kepada Ketua dan Sekertaris Departemen Kimia FMIPA USU, Ibu Dr. Rumondang Bulan Nst MS dan Bapak Prof. Basuki Wirjosentono, M.Sc selaku dosen wali yang telah banyak memberi arahan dan masukan selama penulis kuliah, Bapak dan Ibu dosen bidang Kimia Bahan Alam serta seluruh dosen Departemen Kimia FMIPA USU. Terimakasih setulusnya penulis sampaikan kepada orang tua terkasih, ayahanda Mian Tua Parulian Siringo Ringo dan Ibunda Shearly Kaban yang selalu memberi kasih sayang dan dukungan dalam hal moral dan materi serta tak pernah lelah berdoa dan berjuang untuk selalu memberikan yang terbaik dalam kehidupan penulis. Penulis juga mengucapkan terimakasih kepada adik penulis, Ruth Gratia Ringo serta seluruh keluarga besar yang selalu memotivasi dan mendukung penulis. Terima kasih juga saya haturkan kepada teman dekat saya Laura yang selalu memberikan dukungan dan semangat dalam penelitian. Terimakasih juga penulis sampaikan kepada rekan-rekan asisten Kimia Bahan Alam FMIPA USU, teman-teman sesama penelitian dan teman-teman seperjuangan stambuk 2008 atas dukungan serta bantuan yang telah diberikan. Penulis juga mengucapkan terimakasih kepada seluruh teman, saudara dan kerabat yang telah banyak membantu dengan tulus namun namanya tak bisa dituliskan satu persatu.
ABSTRAK
Isolasi senyawa flavonoida yang terkandung di dalam kulit Bawang Merah (Allium cepa
L.) dilakukan dengan cara ekstraksi maserasi dengan menggunakan pelarut metanol. Ekstrak metanol dipekatkan lalu dilarutkan dengan etil asetat kemudian disaring dan diuapkan. Ektrak etil asetat yang diperoleh dilarutkan dengan metanol dan diekstraksi partisi dengan n-heksana. Lapisan metanol diuapkan hingga pekat lalu dipisahkan dengan kromatografi kolom dengan fasa diam silika gel dan fasa gerak n-heksana:etil asetat dengan perbandingan (90:10) v v⁄, (80:20) v⁄v, (70:30) v v⁄, (60:40) v v⁄, dan (50:50) v v⁄. Fraksi
dari perbandingan (50:50) v v⁄ selanjutnya dikristalisasi untuk mendapatkan senyawa murni.
ISOLATION OF FLAVONOID FROM THE CRUST OF ONION (Allium cepa L.)
ABTRACT
The isolation of flavonoid compound which contained in the crust of onion (Allium cepa
L.) was done by maseration tehnique with methanol solvent. The methanol extract evaporated, dissolved with ethyl acetate solvent, concentrated and evaporated. Ethyl acetate extract was dissolve with methanol and partitioned with n-hexana solvent. Methanol layer was separated using coloumn Chromatography with silica gel as the stationary phase and n-hexane:ethyl acetate (90:10) v v⁄, (80:20) v⁄v, (70:30) v v⁄ (60:40) v v⁄, and (50:50) v v⁄ as the mobile phase. The fraction from n-hexane:aethyl acetate (50:50) v v⁄
DAFTAR ISI
2.1.1 Morfologi Tumbuhan Bawang Merah 5
2.1.2 Sistematika Tumbuhan Bawang Merah 5
2.1.3 Manfaat Tumbuhan Bawang Merah 6
2.2Senyawa Flavonoida 6
2.2.1 Struktur Dasar Senyawa Flavonoida 8
2.2.2 Klasifikasi Senyawa Flavonoida 9
2.3.4 Kromatografi Kolom 17
2.4Teknik Spektroskopi 18
2.4.1 Spektrofotometer Ultra-Violet (UV-Vis) 18
2.4.2 Spektrofotometer Inframerah (FT-IR) 20
2.4.3 Spektrometer Resonansi Magnetik Inti Proton (1H-NMR) 21
Bab 3 Metodologi Penelitian 23
3.1Alat-alat 23
3.2Bahan-bahan 24
3.3Prosedur Penelitian 24
3.3.2.1 Skrining Fitokima 25 3.3.2.2. Analisis Kromatografi Lapis Tipis 25 3.3.3 Ekstraksi Maserasi Kulit bawang Merah 26 3.3.4 Isolasi Senyawa Flavonoida dengan Kromatografi Kolom 26
3.3.5 Kristalisasi 27
3.3.6 Uji Kemurnian Hasil Isolasi 27
3.3.6.1 Uji Kemurnian Hasil Isolasi dengan Kromatografi 27 Lapis Tipis
3.3.6.2 Uji Kemurnian Hasil Isolasi dengan Penentuan 28 Titik Lebur
3.3.7 Identifikasi Senyawa Hasil Isolasi 28
3.3.7.1 Identifikasi dengan Spektrometer 28 Ultraviolet-Visibel (UV-Vis)
3.3.7.2 Identifikasi dengan Spektrofotometer 28 Inframerah (FT-IR)
3.3.7.3 Identifikasi dengan Spektometer Resonansi 29 Magnetik Inti Proton (1
3.4Bagan Skrining Fitokimia 30
DAFTAR LAMPIRAN
Halaman
Lampiran A. Determinasi kulit Bawang Merah (Allium cepaL.) 42 Lampiran B. Gambar kulit Bawang Merah (Allium cepaL.) 43 Lampiran C. Kromatogram Lapis Tipis Ekstrak Pekat Metanol 44
kulit Bawang Merah (Allium cepaL.) sebelum Kromatografi Kolom Lampiran D. Kromatogram Lapis Tipis Senyawa Murni Hasil Isolasi 45 Lampiran E. Spektrum Ultraviolet-Visible Beberapa Senyawa Flavonoida 46 Lampiran F. Ekspansi Spektrum 1
Lampiran G.Spektrum
H-NMR Senyawa Hasil Isolasi 47 1
DAFTAR GAMBAR
Halaman
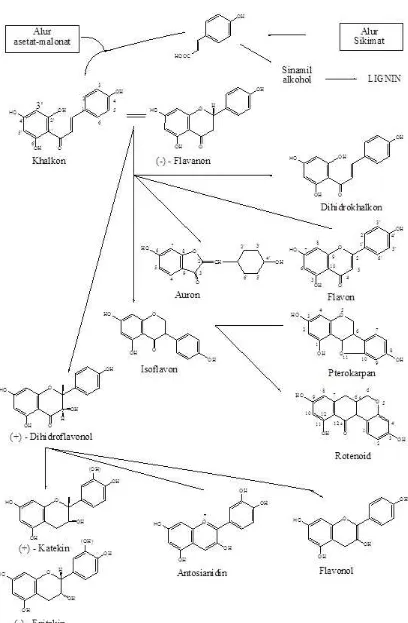
Gambar 2.1Biosintesa hubungan antara jenis monomer flavonoida 7 dari alur asetat-malonat dan alur sikimat
Gambar 2.2 Kerangka Dasar Flavonoida 8
Gambar 4.1 Spektrum UV-Vis Senyawa Hasil Isolasi 32 Gambar 4.2 Spektrum FT-IR Senyawa Hasil Isolasi 33 Gambar 4.3 Spektrum 1
Gambar 4.5 Struktur Flavonol 37
DAFTAR TABEL
Halaman
Tabel 2.1 Sifat golongan flavonoida 10
ABSTRAK
Isolasi senyawa flavonoida yang terkandung di dalam kulit Bawang Merah (Allium cepa
L.) dilakukan dengan cara ekstraksi maserasi dengan menggunakan pelarut metanol. Ekstrak metanol dipekatkan lalu dilarutkan dengan etil asetat kemudian disaring dan diuapkan. Ektrak etil asetat yang diperoleh dilarutkan dengan metanol dan diekstraksi partisi dengan n-heksana. Lapisan metanol diuapkan hingga pekat lalu dipisahkan dengan kromatografi kolom dengan fasa diam silika gel dan fasa gerak n-heksana:etil asetat dengan perbandingan (90:10) v v⁄, (80:20) v⁄v, (70:30) v v⁄, (60:40) v v⁄, dan (50:50) v v⁄. Fraksi
dari perbandingan (50:50) v v⁄ selanjutnya dikristalisasi untuk mendapatkan senyawa murni.
ISOLATION OF FLAVONOID FROM THE CRUST OF ONION (Allium cepa L.)
ABTRACT
The isolation of flavonoid compound which contained in the crust of onion (Allium cepa
L.) was done by maseration tehnique with methanol solvent. The methanol extract evaporated, dissolved with ethyl acetate solvent, concentrated and evaporated. Ethyl acetate extract was dissolve with methanol and partitioned with n-hexana solvent. Methanol layer was separated using coloumn Chromatography with silica gel as the stationary phase and n-hexane:ethyl acetate (90:10) v v⁄, (80:20) v⁄v, (70:30) v v⁄ (60:40) v v⁄, and (50:50) v v⁄ as the mobile phase. The fraction from n-hexane:aethyl acetate (50:50) v v⁄
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Flavonoida merupakan salah satu golongan fenol alam yang terbesar. Menurut
perkiraan, kira-kira 2% dari seluruh karbon yang difotosintesis oleh tumbuhan diubah
menjadi flavonoida atau senyawa yang berkaitan erat dengannya. (Markham, 1988).
Flavonoida adalah senyawa yang mengandung C15
Secara biologis, flavonoida memainkan peranan penting dalam penyerbukan pada
tanaman oleh serangga. Flavonoida memberikan kontribusi keindahan dan
kesemarakan pada bunga dan buah-buahan di alam. Sejumlah flavonoida mempunyai
rasa pahit hingga dapat bersifat menolak sejenis ulat tertentu (Sastrohamidjojo, 1996). terdiri atas dua inti fenolat yang
dihubungkan dengan tiga satuan karbon (Sastrohamidjojo, 1996). Flavonoida yang
terdapat di dalam tumbuhan dapat digunakan sebagai pelindung tubuh manusia dari
radikal bebas dan dapat mengurangi resiko penyakit kanker dan peradangan. (Nessa,
2003). Salah satu contoh flavonoida adalah antosianin yang berperan dalam pewarnaan
bunga-bunga (biru, ungu dan merah) (Manitto, 1992).
Salah satu tumbuhan yang terdapat di Indonesia dan dapat dijadikan obat adalah
tumbuhan Bawang Merah (Allium cepa L.). Kulit tumbuhan bawang merah banyak
digunakan sebagai obat untuk penyakit-penyakit seperti batuk, haid tidak teratur,
kencing manis, demam pada anak-anak (obat luar) dan perut kembung pada anak-anak
(obat luar) (Hapsoh dan Yaya Hasanah, 2011).
Allium cepa L. merupakan tanaman semusim yang berbentuk rumput, berbatang
pendek dan berakar serabut, tinggi dapat mencapai 15-20 cm dan membentuk rumpun.
merah seperti pipa, yakni bulat kecil memanjang antara 50-70 cm, berlubang, bagian
ujungnya meruncing, berwarna hijau muda sampai hijau tua dan letak daun melekat
pada tangkai yang ukurannya relatif pendek. Pangkal daunnya dapat berubah fungsi
seperti menjadi umbi lapis (Hapsoh dan Yaya Hasanah, 2011).
Beberapa penelitian tentang bawang merah antar lain Noviandiah Kurniawati tahun
2010 meneliti ekstrak etanol 70% bawang merah (Allium cepaL.) terhadap penurunan
kadar kolesterol pada tikus putih dan Boesro Soebagio tahun 2007 meneliti tentang
ekstrak umbi bawang merah sebagai antioksidan. Selanjutnya Kramer.et.al 2003 telah
mengisolasi 2 jenis senyawa flavonoida glucosyltransferase dari bawang merah
(Allium cepa L.). Studi literatur menunjukkan pemisahan senyawa flavonoida
Quercetin dari bawang merah (Allium cepa L.) dengan metode spektrofotometri dan
HPLC (Lombard, 2002).
Dari uji pendahuluan yang peneliti lakukan, yaitu dengan uji skrining fitokimia
dengan pereaksi FeCl3 5%, NaOH 10%, Mg-HCl dan H2SO4(p) menunjukkan bahwa
ekstrak metanol kulit bawang merah mengandung senyawa flvonoida.
Dari uraian diatas dan beberapa literatur penelitian yang telah dilakukan terhadap
tumbuhan bawang merah maka peneliti tertarik untuk meneliti kulit Allium cepa L.
yang merupakan salah satu spesies dari Genus Allium, khususnya mengenai senyawa
flavonoida yang terkandung dalam tumbuhan ini.
1.2 Permasalahan
Permasalahan dalam penelitian ini adalah bagaimana cara mengisolasi senyawa
flavonoida yang terdapat dalam kulit bawang merah (Allium cepaL.)
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengisolasi senyawa flavonoida yang terdapat
1.4 Manfaat Penelitian
Dari hasil penelitian diharapkan dapat memberikan sumber informasi ilmiah pada
bidang Kimia Bahan Alam khususnya tentang senyawa flavonoida yang terkandung
dalam kulit bawang merah (Allium cepaL.)
1.5 Lokasi Penelitian
1. Tempat pengambilan sampel
Sampel yang digunakan diperoleh dari areal sekitar Marendal Medan Amplas Sumatera
Utara.
2. Tempat melakukan penelitian
Penelitian dilakukan di laboratorium Kimia Bahan Alam FMIPA Universitas Sumatera
Utara.
3. Lokasi Identifikasi Kristal Hasil Isolasi
Analisis spektrofotometer Inframerah (FT-IR), spektrofotometer Ultaviolet-Visibel
(UV-Vis) dan Spektrometer Resonansi Magnetik Inti Proton (1H-NMR) dilakukan di
Pusat Penelitian Kimia – LIPI, kawasan PUSPITEK Serpong, Tangerang.
1.6 Metodologi Penelitian
Dalam penelitian ini, isolasi senyawa flavonoida dilakukan terhadap kulit bawang
merah (Allium cepa L.) berupa serbuk halus yang kering sebanyak 2000 gram. Tahap
awal dilakukan uji skrining fitokimia untuk senyawa flavonoida, yaitu dengan
menggunakan pereaksi FeCl35%, NaOH 10%, Mg-HCl dan H2SO4(p).
Tahap isolasi yang dilakukan:
1. Ekstraksi Maserasi
2. Ekstraksi Partisi
4. Analisis Kromatografi Kolom
5. Kristalisasi
6. Analisis Senyawa Hasil Isolasi
Tahap analisis senyawa hasil isolasi yang dilakukan adalah:
1. Analisis Kromatografi Lapis Tipis
2. Pengukuran Titik Lebur
3. Identifikasi dengan menggunakan spektofotometer Infra merah (FT–IR),
spektrofotometer Ultraviolet-Visible (UV–Vis) dan Spektrometer Resonansi
BAB 2
TINJAUAN PUSTAKA
2.1 Tumbuhan Bawang Merah
2.1.1 Morfologi Bawang Merah (Allium cepa L.)
Bawang merah (lihat lampiran B) merupakan tanaman semusim yang berbentuk
rumput, berbatang pendek dan berakar serabut, tinggi dapat mencapai 15-20 cm dan
membentuk rumpun. Akarnya berbentuk akar serabut yang tidak panjang. Bentuk daun
tanaman bawang merah seperti pipa, yakni bulat kecil memanjang antara 50-70 cm,
berlubang, bagian ujungnya meruncing, berwarna hijau muda sampai hijau tua dan
letak daun melekat pada tangkai yang ukurannya relatif pendek. Pangkal daunnya dapat
berubah fungsi seperti menjadi umbi lapis (Hapsoh dan Yaya Hasanah, 2011).
2.1.2 Sistematika Bawang Merah (Allium cepa L.)
Sistematika tumbuhan bawang merah adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Class : Dicotyledoneae
Ordo : Liliales
Family : Liliaceae
Genus : Allium
Spesies : Allium cepa L.
Tanaman ini ditanam secara besar-besaran di pegunungan Tengger, Padang dan
dataran tinggi Karo, terutama antara 1800 – 2200 m di atas permukaan laut. Bibitnya
ditebarkan dalam larikan, satu sama lain berjarak 20 cm dan kemudian dijarangkan
hingga kira-kira 15 cm. Selama pertumbuhannya haruslah disiangi dengan teratur dan
tanahnya digemburkan ( Heyne, 1981 ).
2.1.3 Manfaat Bawang Merah (Allium cepa L.)
Kulit tumbuhan bawang merah banyak digunakan sebagai obat untuk
penyakit-penyakit seperti batuk, haid tidak teratur, kencing manis, demam pada anak-anak (obat
luar) dan perut kembung pada anak-anak (obat luar) (Hapsoh dan Yaya Hasanah,
2011).
2.2 Senyawa Flavonoida
Senyawa flavonoida adalah senyawa-senyawa polifenol yang mempunyai 15 atom
karbon, terdiri dari dua cincin benzena yang dihubungkan menjadi satu oleh rantai
linear yang terdiri dari tiga atom karbon. Kerangka ini dapat ditullis sebagai C6-C3-C6.
Jadi senyawa flavonoida adalah senyawa 1,3 diarilpropana, senyawa isoflavonoida
adalah senyawa 1,2 biarilpropana, sedang senyawa-senyawa neoflavonoida adalah
senyawa 1,1 diarilpropana.
Istilah flavonoida dikenakan pada suatu golongan besar senyawa yang yang berasal
dari kelompok senyawa yang paling umum yaitu flavon. Suatu jembatan oksigen
terdapat diantara cincin A dalam kedudukan orto dan atom karbon benzil yang terletak
di sebelah cincin B membentuk cincin baari tipe 4-piron. Senyawa heterosiklik ini pada
tingkat oksidasi yang berbeda terdapat dalam kebanyakan tumbuhan. Flavon adalah
bentuk yang mempunyai cincin C dengan tingkat
oksidasi yang paling rendah dan dianggap sebagai struktur induk dalam nomenklatur
Gambar 2.1 Biosintesa hubungan antara jenis monomer flavonoida dari alur
Menurut perkiraan, kira-kira 2% dari seluruh karbon yang difotosintesis oleh
tumbuhan diubah menjadi flavonoida atau senyawa yang berkaitan erat dengannya.
Flavonoida terdapat dalam semua tumbuhan hijau. Flavonoida terdapat pada semua
bagian tumbuhan termasuk daun, akar, kayu, kulit, tepung sari, nektar, bunga, buah dan
biji.
Semua varian flavonoida saling berkaitan karena alur biosintesis yang sama, yang
memasukkan prazat dari alur sikimat dan asetat malonat. Flavonoida pertama
dihasilkan segera setelah kedua alur tersebut bertemu. Flavonoida yang dianggap
pertama kali terbentuk pada biosintesis adalah khalkkon dan semua bentuk lain
diturunkan darinya melalui berbagai alur (Markham, 1988).
Dalam tubuh manusia, flavonoida berfungsi sebagai antioksidan sehingga sangat
baik untuk pencegahan kanker. Manfaat lain lain flavonoida adalah melindungi struktur
sel, meningkatkan efektivitas vitamin C, antiinflamasi, mencegah keropos tulang dan
sebagai anti bioktik (Muhammad, 2011). Dalam dosis kecil flavon bekerja sebagai
stimulan pada jantung, hesperidin mempengaruhi pembuluh darah kapiler, flavon
terhidroksilasi bekerja sebagai diuretik dan antioksidan pada lemak. Kegunaan
flavonoida pada tumbuhan adalah untuk menarik serangga yang membantu proses
penyerbukan, membantu menarik perhatian binatang yang membantu penyebaran biji
(Sirait, 2007).
2.2.1 Struktur Dasar Senyawa Flavonoida
Senyawa flavonoida adalah senyawa yang mengandung C15 terdiri atas dua inti fenolat
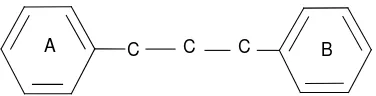
yang dihubungkan dengan tiga satuan karbon. Struktur dasar flavonoida dapat
digambarkan sebagai berikut:
C C C
A B
Gambar 2.2 Kerangka Dasar Flavonoida
2.2.2 Klasifikasi Senyawa Flavonoida
Flavonoida biasanya terdapat sebagai flavonoida O-glikosida. Pada senyawa tersebut
satu gugus hidroksil flavonoida atau lebih terikat pada satu gula atau lebih dengan
ikatan hemimasetal yang tak tahan asam. Pengaruh glikosilasi menyebabkan flavonoida
menjadi kurang reaktif dan lebih mudah larut dalam air. Glukosa merupakan gula yang
paling umum terlibat walaupun galaktosa, ramnosa, xilosa dan arabinosa juga sering
ditemukan.
Gula dapat juga terikat pada atom karbon flavonoida dan dalam hal ini gula
tersebut terikat langsung pada inti benzena dengan suatu ikatan karbon-karbon yang
tahan asam. Glikosida yang demikian disebut C-glikosida. Jenis gula yang terlibat lebih
sedikit dibandingkan dengan gula pada O-glikosida.
Flavonoida sulfat adalah golongan flavonoida lain yang mudah larut dalam air.
Senyawa ini mengandung satu ion sulfat atau lebih yang terikat pada hidroksi fenol
atau gula. Secara teknis senyawa ini sebenarnya bisulfat karena terdapat sebagai garam
yaitu flavon-O-SO3K. Banyak yang berupa glikosida bisulfat, bagian bisulfat terikat
pada hidroksil fenol yang mana saja yang masih bebas atau pada suatu gula.
Biflavonoida merupakan flavonoida dimer. Flavonoida yang biasanya terlibat
adalah flavon dan flavanon yang secara biosintesis mempunyai pola oksigenasi yang
sederhana dan ikatan antar flavonoida berupa ikatan karbon-karbon atau ikatan eter.
Monomer flavonoida yang digabungkan menjadi biflavonoida dapat berjenis sama atau
berbeda, dan letak ikatannya berbeda-beda. Banyak sifat fisika dan kimia biflavnoida
menyerupai sifat monoflavonoida pembentuknya dan akibatnya kadang-kadang
biflavonoida sukar dikenali. Biflavonoida jarang ditemukan sebagai glikosida.
Sejumlah aglikon flavonoida mempunyai atom karbon asimetrik dengan demikian
dapat menunjukkan keaktifan optik (yaitu memutar cahaya terpolarisasi-datar). Yang
termasuk dalam golongan flavonoida ini adalah flavanon, dihidroflavonol, katekin,
Menurut Harbone (1996), dikenal sekitar sepuluh kelas flavonoida, dimana semua
flavonoida menurut strukturnya merupakan turunan senyawa induk flavon dan
memiliki sifat tertentu yaitu:
Tabel 2.1 Sifat golongan flavonoida
Golongan flavonoida
Penyebaran Ciri khas
Antosianin
marak,dan biru juga dalam daun dan jaringan lain.
Terutama tanwarna, dalam daun tumbuhan berkayu.
Terutamako-pigmen tanwarna dalam bunga sianik dan asianik tersebar luas dalam daun.
Seperti flavonol
Seperti flavonol
Tanwarna; hampir seluruhnya terbatas pada gimnospermae
Pigmen bunga kuning, kadang-kadang terdapat juga dalam jaringan lain
Tanwarna; dalam daun dan buah (terutama dalam Citrus)
Tanwarna; sering kali dalam akar; hanya terdapat dalam satu suku, Leguminosae
Larut dalam air, λmaks 515-545 nm, bergerak dengan BAA pada kertas.
Menghasilkan antosianidin bila jaringan dipanaskan dalam HCl 2M selama setengah jam.
Setelah hidrolisis, berupa bercak kuning murup pada kromatogram Forestal bila disinari sinar UV; λmaks
spektrum pada 330 – 350 nm.
Setelah hidrolisis, berupa bercak coklat redup pada kromatogram Forestal; λmaks
spektrum pada 330-350 nm.
Mengandung gula yang terikat melalui ikatan C-C; bergerak dengan pengembang air, tidak seperti flavon biasa.
Pada kromatogram BAA beupa bercak redup dengan RF
Dengan amonia berwarna merah (perubahan warna dapat diamati in situ), maksimal spektrum 370-410 nm.
tinggi.
Berwarna merah kuat dengan Mg/HCl; kadang – kadang sangat pahit .
Menurut Robinson (1995), flavonoida dapat dikelompokkan berdasarkan
keragaman pada rantai C3
1. Flavonol
yaitu:
Flavonol sering terdapat sebagai glikosida, biasanya 3-glikosida dan aglikon
flavonol yang umum yaitu kamferol, kuarsetin dan miresetin yang berkhasiat sebagai
antioksidan dan antiinflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan
merupakan variasi struktur sederhana dari flavonol. Larutan flavonol dalam suasana
basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada
pengerjaannya masih dapat dilakukan.
O O
OH
2. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan
3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksi
warnanya. Flavon terdapat juga sebagai glikosidanya lebih sedikit daripada jenis
glikosida pada flavonol. Flavon yang paling umum dijumpai adalah apigenin dan
luteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang
paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula
melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap
sebagai induk dalam nomenklatur kelompok senyawa flavonoida.
O O
3. Isoflavon
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai
fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan sebagai
pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena reaksinya
memberikan warna biru muda cemerlang dengan sinar UV bila diuapi amonia, tetapi
kebanyakan yang lain tampak sebagai bercak lembayung yang pudar dengan amonia
berubah menjadi coklat.
O O
4. Flavanon
Flavanon terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan
bunga. Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan
buah jeruk, dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat
dalam buah anggur dan jeruk.
O O
5. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika
dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena
konsentrasinya rendah dan tidak berwarna.
O O
OH
6. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu.
dan daun teh kering yang mengandung kira-kira 30% senyawa ini. Katekin berkhasiat
Leukoantosianidin merupakan senyawa tanwarna, terutama terdapat pada tumbuhan
berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin,
apiferol.
O
OH
HO
OH
8. Antosianidin
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam
tumbuhan. pigmen yang berwarna kuat dan larut dalam air ini adalah penyebab hampir
semua warnamerah jambu, merah marak, ungu dan biru dalam daun, bunga dan buah
pada tumbuhan tinggi. Secara kimia semua antosianin merupakan struktur aromatik
tunggal yaitu sianidin dan semuanya terbentuk dari pigmen sianidin ini dengan
penambahan atau pengurangan gugus hidroksil atau dengan metilasi atau glikosilasi.
O
OH
9. Khalkon
Khalkon adalah pigmen fenol kuning yang berwarna coklat tua dengan sinar UV
bila dikromatografi kertas. Aglikon khalkon dapat dibedakan dari glikosidanya karena
hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas
O
10.Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita.
Dalam larutan basa senyawa ini berwarna ros dan tampak pada kromatografi kertas
berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah menjadi
merah jungga bila diberi uap amonia (Robinson, 1995).
HC
O
O
2.2.3 Sifat Kelarutan Senyawa Flavonoida
Aglikon flavonoida adalah polifenol dan karena itu mempunyai sifat kimia seperti
fenol yaitu bersifat agak asam sehingga dapat larut dalam basa. Tetapi bila didiamkan
dalam larutan basa dan disamping itu terdapat banyak oksigen maka akan banyak yang
terurai. Karena mempunyai sejumlah gugus hidroksil yang tak tersulih atau suatu gula,
flavonoida merupakan senyawa polar maka umumnya flavonoida larut dalam pelarut
polar seperti etanol, metanol, butanol, aseton, dimetilsulfoksida, dimetilformamida, air
dan lain-lain. Adanya gula yang terikat pada flavonoida cenderung menyebabkan
flavonoida lebih mudah larut dalam air. Dengan demikian campuran pelarut di atas
dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon
yang kurang polar seperti isoflavon, flavanon, flavon serta flavonol yang termetoksilasi
cenderung lebih mudah larut dalam pelarut seperti eter dan kloroform (Markham,
2.3 Teknik Pemisahan
2.3.1 Ekstraksi
Ekstraksi adalah suatu proses pemisahan substansi atau zat dari campurannya dengan
menggunakan pelarut yang sesuai. Ekstraksi dapat digolongkan berdasarkan bentuk
campuran yang diekstraksi dan proses pelaksanaannya. Berdasarkan bentuk campuran
yang diekstraksi, suatu ekstraksi dibedakan menjadi:
1. Ekstraksi padat-cair
Zat yang diekstrasi terdapat di dalam campuran yang berbentuk padatan. Ekstraksi
jenis ini banyak dilakukan di dalam usaha mengisolasi zat berkhasiat yang terkandung
di dalam bahan alam.
2. Ekstraksi cair-cair
Zat yang diekstraksi terdapat di dalam campuran yang berbentuk cair. Ekstraksi
cair-cair sering juga disebut ekstraksi pelarut untuk memisahkan logam-logam tertentu
didalam air.
Menurut proses pelaksanaannya ekstraksi dibedakan menjadi:
1. Ekstraksi berkesinambungan (kontinyu)
Pada ekstraksi kontinyu, pelarut yang sama digunakan secara berulang-ulang
sampai proses ekstraksi selesai. Tersedia berbagai alat untuk jenis ekstraksi ini, seperti
alat soklet.
2. Ekstraksi bertahap
Pada ekstraksi bertahap, setiap kali ekstraksi selalu digunakan pelarut yang baru
sampai proses ekstraksi selesai. Alat yang biasanyadigunakan adalah corong pisah.
2.3.2 Kromatografi
Kromatografi merupakan metode umum dalam pemisahan campuran berdasarkan fase
diam dan fase gerak. Fase gerak dapat berupa gas atau cairan dan fase diam berupa
melewati fase diam dan senyawa-senyawa dalam campuran akan bergerak secara
kontiniu diantara kedua fase sesuai dengan koefisien distribusi (Rodig, 1997).
Berdasarkan pada mekanisme pemisahannya, kromatografi dapat dibedakan
menjadi kromatografi adsorbsi, kromatografi partisi, kromatografi pasangan ion,
kromatografi penukar ion dan kromatografi ekslusi ukuran. Berdasarkan pada alat yang
diguanakan kromatografi dapat dibagi atas kromatografi kertas, kromatografi lapis
tipis, kromatografi cair kinerja tinggi, kromatografi gas dan kromaatografi kolom
(Ganjar,2007).
2.3.2.1 Kromatografi Lapis Tipis
Teknik kromatografi lapis tipis sering dilakukan dengan menggunakan lempeng atau
gelas plastik yang dilapisi fase diam dan fase geraknya merupakan pelarut. Campuaran
yang akan dianalisis diteteskan pada dasar lempeng dan perlarutnya akan bergerak naik
oleh gaya kapiler.
Pada umumnya fase diam bersifat polar dan senyawa polar akan melekat lebih kuat
pada lempeng daripada senyawa tak polar akibat interaksi tarik menarik dipole.
Senyawa tak polar kurang melekat erat pada fase diam polar sehingga bergerak naik
lebih jauh ke atas lempeng. Jarak tempuh ke atas lempeng merupakan cermin polaritas
senyawa. Peningkatan polaritas pelarut akan menurunkan interaksi senyawa dengan
fase diam sehingga senyawa dalam fase gerak bergerak lebih jauh pada lempeng
(Bresnick, 2005).
Fase diam yang digunakan pada kromatografi lapis tipis merupakan penyerap
berukuran kecil dengan diameter partikel 10-30 μm. Semakin kecil ukuran rata-rata partikel fase diam maka semakin baik kinerja kromatografi lapis tipis dalam hal
Nilai utama kromatografi lapis tipis pada penelitian flavonoida adalah sebagai cara
analisis cepat yang memerlukan bahan sangat sedikit. Menurut Markham,
Kromatografi Lapis Tipis terutama berguna untuk tujuan berikut:
1. Mencari pelarut untuk kromatografi kolom
2. Analisis fraksi yang diperoleh dari kromatografi kolom
3. Identifikasi flavonoida secara ko-kromatografi
4. Isolasi flavonoida murni skala kecil
5. Penyerap dan pengembang yang digunakan umumnya sama dengan penyerap dan
pengembang pada kromatografi kolom dan kromatografi kertas (Markham, 1988).
Faktor reterdasi merupakan parameter karakteristik kromatografi kertas dan
kromatografi lapis tipis. Harga Rf adalah ukuran kecepatan migrasi suatu komponen
pada kromatogram. Rf didefenisikan sebagai perrbandingan jarak yang ditempuh
komponen terhadap jarak yang ditempuh pelarut atau fase gerak.
(Sastrohamidjojo, 1996)
2.3.2.2 Kromatografi Kolom
Kolom kromatografi biasanya terbuat dari gelas. Panjang kolom disesuaikan dengan
jumlah komponen yang akan dianalisis dan lebar kolom disesuaikan dengan jumlah
senyawa yang akan akan dianalisis (Bintang, 2011). Pada kromatografi kolom fase
diam dan zat cair ditempatkan didalam tabung kaca berbentuk silinder, pada bagian
bawah tertutup dengan katup atau keran dan fase geraknya dibiarkan mengalir ke
bawah malalui gaya berat.
Kromatografi kolom biasanya dibuat dengan menuangkan suspensi fasa diam dan
pelarut yang sesuai kedalam kolom dan dibiarkan memadat. Selanjutnya pelarut
diturunkan sampai tepat pada bagian atas penyerap dan cuplikan yang akan dipisahkan
diletakkan pada bagian atas penyerap kemudian fase gerak dimasukkan dan dibiarkan
mengalir melewati kolom dan komponen campuran turun berupa pita dengan laju yang
R
f=
Jarak yang ditempuh nodaberlainan kemudian hasil pemisahan dari kolom dikumpulkan sebagai fraksi.
Kromatografi kolom merupakan bentuk kromatografi cair (Gritter, 1991).
2.4. Teknik Spektroskopi
Teknik spektroskopi adalah salah satu teknik analisis kimia-fisika yang mengamati
tentang interaksi atom atau molekul dengan radiasi elektromagnetik. Ada dua macam
instrumen pada teknik spektroskopik yaitu spektrometer dan spektrofotometer.
Instrumen yang memakai monokromator celah yang tetap pada bidang fokus disebut
spektrometer. Apabila spektrometer tersebut dilengkapi dengan detektor yang bersifat
fotoelektrik disebut sebagai spektrofotometer (Muldja, 1995).
Panjang gelombang pada suatu senyawa organik yang menyerap energi cahaya
bergantung pada struktur senyawa itu. Oleh karena itu teknik spektroskopi dapat
digunakan untuk menentukan struktur senyawaan yang tidak diketahui dan untuk
mempelajari karakteristik ikatan dari senyawaan yang diketahui (Fessenden, 1983).
Rumus molekul dapat ditentukan dari spektrum massa dan bentuk fragmentasinya.
Gugus fungsi alami ditentukan dari spektrum inframerah. Gugus fungsi terkonjugasi
dapat ditentukan dari spektrum elektronik. Struktur dapat ditentukan berdasarkan inti
proton dan karbon yang dihasilkan molekul dari spektrum 1H dan 13C NMR
(Brown,1937).
2.4.1 Spektrofotometer Ultraviolet-Visibel (UV-Vis)
Spektrofotometer ultraviolet-visible adalah anggota tenik analisis spektroskopik yang
memakai sumber radiasi elektromagnetik ultraviolet dekat dan sinar tampak dengan
memakai instrumen spektrofotometer. Spektrofotometer ultraviolet-visibel dapat
melakukan penentuan terhadap sampel yang berupa larutan, gas atau uap.
Spektofotometer ultraviolet-visibel melibatkan energi elektronik yang yang cukup
radiasi elektromagnetik akan mengabsopsi radiasi elektromagnetik yang energinya
sesuai. Interaksi tersebuat akan meningkatkan energi potensial elektron pada tingkat
keadaan eksitasi. Apabila pada molekul sederhana tersebut hanya terjadi transisi
elektronik pada satu macam gugus maka akan terjadi suatu absorpsi yang merupakan
garis spektrum (Muldja,1995).
Flavonoida mengandung sistem aromatik yang terkonjugasi karena itu memiliki
menunjukkan pita serapan kuat pada daerah spektrum ultraviolet dan spektrum tampak
(Harbone, 1987). Spektrum flavonoida biasanya ditentukan dalam larutan dengan
pelarut metanol atau etanol. Spektrum khas terdiri atas dua maksima pada rentang
240-285 nm (pita II) dan 300-550 nm (pita I). Kedudukan yang tepat dan kekuatan nisbi
maksima terssebut memberika informasi yang berharga mengenai sifat dan pola
oksigenasinya. Ciri khas spektrum adalah kekuatan nisbi yang rendah pada pita I dalam
dhidroflavon,dihidroflavonol dan isoflavon serta kedudukan pita I pada spektrum
khalkon, auron dan antosianin yang terdapat pada panjang gelombang yang tinggi.
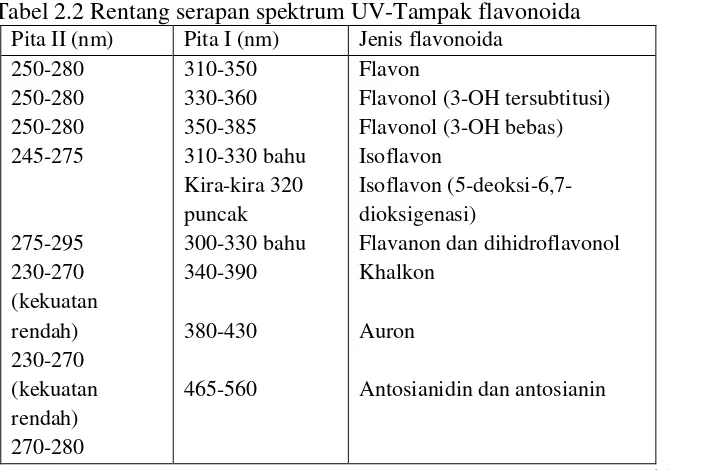
petunjuk mengenai rentang maksima utama yang diperkirakan untuk setiap jenis
flavonoida adalah sebagai berikut:
Tabel 2.2 Rentang serapan spektrum UV-Tampak flavonoida
2.4.2 Spektrofotometer Infra Merah (FT-IR)
Cahaya tampak terdiri dari beberapa range frekuensi elektomagnetik yang berbeda
dimana setiap frekuensi bisa dilihat sebagai warna yang berebeda. Radiasi inframerah
juga mengandung beberapa range frekuensi tetapi tidak dapat dilihat oleh mata.
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya inframerah
tengah yaitu pada panjang gelombang 2,5-50 μm atau bilangan gelombang 4000-200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran
pada molekul. Pita absorbsi inframerah sangat khas dan spesifik untuk setiap tipe
ikatan kimia atau gugus fungsi.
Jika suatu frekuensi tertentu dari radiasi inframerah dilewatkan pada suatu sampel
senyawa organik maka akan terjadi penyerapan frekunsi oleh senyawa tersebut.
Detektor akan mendeteksi frekuensi yang dilewatkan pada sampel yang tidak diserap
oleh senyawa. Banyaknya frekuensi yang melewati senyawa atau yang tidak diserap
akan diukur sebagai persen transmitan. Spektrum yang dihasilkan berupa grafik yang
akan menunjukkan persentase transmitan yang bervariasi pada setiap frekuensi radiasi
inframerah. Satuan frekunsi yang digunakan dinyatakan dalam bilangan gelombang
(Dachriyanus, 2004).
Terdapat dua macam getaran molekul, yaitu getaran ulur dan getaran tekuk.
Getaran ulur adalah suatu gerakan berirama di sepanjang sumbu ikatan sehingga jarak
antar atom bertambah atau berkurang. Getaran tekuk dapat terjadi karena perubahan
sudut-sudut ikatan antara ikatan-ikatan pada sebuah atom atau karena gerakan sebuah
gugusan atom terhadap sisa molekul tanpa gerakan nisbi atom-atom dalam gugusan
(Silverstein, 1986). Instrumen yang digunakan untuk mengukur resapan radiasi
inframerah pada berbagai macam panjang gelombang disebut spektrofotometer
inframerah (Fessenden, 1982). Spektrofotometer inframerah pada umumnya digunakan
untuk:
1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan
2.4.3 Spektrometer Resonansi Magnetik Inti proton (1H-NMR)
Spektrometer Resonansi Magnetik Inti (Nuclear Magnetic Resonance, NMR)
merupakan alat yang berguna pada penentuan struktur molekul organik. Teknik ini
memberikan informasi mengenai berbagai jenis atom hidrogen dalam molekul.
Spektrum Resonansi Magnetik Inti memberikan informasi mengenai lingkungan kimia
atom hidrogen, jumlah atom hidrogen dalam setiap lingkungan dan struktur gugusan
yang berdekatan dengan setiap atom hidrogen (Creswell, 1982).
Spektrum Resonansi Mangeti Inti pada umunya digunakan untuk:
1. Menentukan jumlah proton yang memiliki lingkungan kimia yang sama pada suatu
senyawa organik
2. Mengetahui informasi mengenai struktur suatu senyawa organik (Dachriyanus,
2004).
Terperisai dan tak terperisai merupakan istilah relatif. Untuk memperoleh
pengukuran yang kuantitatif diperlukan suatu titik rujukan. Senyawa yang dipilih untuk
rujukan adalah Tetrametilsilana (CH3)4
1. TMS mempunyai 12 atom hidrogen yang keseluruhannya mempunyai lingkungan
kimia yang sama, sehingga menghasilkan sinyal singlet yang kuat karena mengandung
banyak atom hidrogen
Si, yang proton-protonnya menyerap pada ujung
kanan spektrum NMR (Fessenden, 1982). Pada beberapa spektrum NMR akan terlihat
sinyal TMS pada angka nol sehingga sinyal ini tidak perlu dianalisa. TMS dipilih sebagai
standart karena:
2. Elektron-elektron pada ikatan C-H dalam senyawa ini berada dekat dengan hidrogen jia
dibanding dengan senyawa lain. Ini berarti inti hidrogen sangat terlindungi dari medan
magneteksternal sehingga dibutuhkan medan magnet yang besar untuk membawa atom
hidrogen ke kondisi resonansi (Dachriyanus, 2004).
Pada spektrometri NMR integrasi sangat penting. Harga integrasi menunjukkan
daerah atau luas puncak dari tiap – tiap proton . Sedangkan luas daerah atau luas puncak
tersebut sesuai dengan jumlah proton. Dengan demikian perbandingan tiap integrasi proton
Absorbsi kebanyakan proton lain dijumpai dibawah medan absorbsi TMS. Selisih
antara posisi absorbsi TMS dan posisi absorbsi suatu proton tertentu disebut pergeseran
kimia. Pergeseran kimia dinyatakan sebagai bagian tiap juta (ppm) dari radio frekuensi
BAB 3
6. Ekstraktor 5000 mL Schoot/ Duran
7. Tabung reaksi Pyrex
8. Pipet tetes
9. Pipa kapiler
10.Spatula
11.Rotarievaporator Bűchi R-114
12.Labu rotarievaporator 1000 mL
13.Labu didih 1000 mL Schoot/ Duran
14.Labu takar 250 mL Pyrex
15.Kolom kromatografi Pyrex
16.Botol vial
17.Neraca analitis Mettler AE 200
18.Lampu UV 254 nm/ 356 nm UVGL 58
19.Statif dan klem
20.Penangas air
21.Alat destilasi
22.Bunsen
23.Bejana Kromatografi Lapis Tipis
25.Spektrofotometer UV-Visible
26.Spektrometer 1H-NMR Jeol/Delta2NMR 500MHz
3.2 Bahan-bahan
1. Kulit Bawang Merah
2. Metanol Destilasi
Sampel yang diteliti adalah kulit bawang merah yang diperoleh dari areal sekitar
Marendal Medan Amplas, Sumatera Utara. Kulit bawang merah dikeringkan di udara
terbuka, lalu dihaluskan sampai diperoleh serbuk kulit bawang merah sebanyak 2000 g.
3.3.2 Uji Pendahuluan Terhadap Ekstrak Kulit Bawang Merah
Serbuk kulit bawang merah diidentifikasikan dengan menggunakan cara:
1. Skrining Fitokimia
3.3.2.1Skrining Fitokimia
Untuk mengetahui adanya senyawa flavonoida pada kulit bawang merah maka
dilakukan uji pendahuluan secara kualitatif sebagai berikut:
- Dimasukkan ± 10 gram serbuk kulit bawang merah yang telah dikeringkan dan
dipotong kecil-kecil ke dalam erlenmeyer
- Ditambahkan metanol ± 100 mL
- Didiamkan
- Disaring
- Dibagi ekstrak metanol kedalam 4 tabung reaksi
- Ditambahkan masing-masing pereaksi:
a. Tabung I : dengan FeCl3
b. Tabung II : dengan Mg-HCl menghasilkan larutan berwarna merah muda 5% menghasilkan larutan berwarna hitam
c. Tabung III : dengan NaOH 10% menghasilkan larutan biru violet
d. Tabung IV : dengan H2SO4(p) menghasilkan larutan orange kekuningan
3.3.2.2 Analisis Kromatografi Lapis Tipis
Analisis Kromatografi Lapis Tipis dilakukan terhadap ekstrak metanol dengan
menggunakan fasa diam silika gel 60 F254 Merck. Analisis ini dimaksudkan untuk
mencari pelarut yang sesuai didalam analisis kromatografi kolom. Pelarut yang
digunakan adalah campuran n-heksana:etilasetat. Fasa gerak yang digunakan adalah
campuran n-heksana:etilasetat dengan perbandingan (90:10) v v⁄ , (80:20) v v⁄ , (70:30) v v⁄
Dimasukkan 10 mL larutan fase gerak n-heksana:etilasetat (90:10) v v
⁄ kedalam
bejana kromatografi, kemudian dijenuhkan. Ditotolkan ekstrak pekat metanol pada
plat KLT yang telah diaktifkan. Dimasukkan plat kedalam bejana yang telah berisi
pelarut yang telah dijenuhkan, lalu ditutup dan dielusi. Plat yang telah dielusi
Diamati warna bercak yang timbul dan dihitung harga Rf yang diperoleh. Perlakuan
yang sama dilakukan untuk perbandingan pelarut n-heksana: etilasetat dengan
perbandingan (80:20) v v⁄ , (70:30) v v⁄, (60:40) v⁄v dan (50:50) v⁄v.
3.3.3 Ekstraksi Kulit Bawang Merah
Serbuk kulit bawang merah ditimbang sebanyak 2000 g, kemudian dimaserasi dengan
metanol sebanyak ± 12 L sampai semua sampel terendam dan dibiarkan selama ± 72
jam dan diulangi sebanyak 3 kali. Maserat ditampung dan dipekatkan dengan
menggunakan alat rotarievaporator sehingga diperoleh ekstrak pekat metanol.
Kemudian diuapkan hingga semua pelarut menguap. Lalu dilakukan pemblokan tanin
dengan cara melarutkan fraksi metanol dengan etilasetat dan disaring. Filtrat
kemuadian dirotarievaporator lalu diuapkan hingga semua pelarut etilasetat menguap.
Lalu fraksi etilasetat dilarutkan dengan metanol dan dipartisi berulang-ulang dengan
n-heksana. Lapisan metanol dipisahkan dari lapisan n-heksana lalu diuapkan hingga
pekat sehingga diperoleh ekstrak pekat metanol sebanyak 15 g.
3.3.4 Isolasi Senyawa Flavonoida dengan Kromatografi Kolom
Isolasi senyawa flavonoida secara kromatografi kolom dilakukan terhadap ekstrak
pekat metanol yang telah diperoleh. Fasa diam yang digunakan adalah silika gel dan
fasa gerak yaitu n-heksana 100%, campuran pelarut n-heksana:etilasetat dengan
perbandingan (90:10) v v⁄ , (80:20) v v⁄ , (70:30) v v⁄ , (60:40) v⁄v dan (50:50) v⁄v.
Dirangkai alat kolom kromatografi. Terlebih dahulu dibuburkan 175 g silika gel
dengan menggunakan n-heksana, diaduk hingga homogen lalu dimasukkan kedalam
kolom kromatografi. Kemudian dielusi dengan menggunakan n-heksana 100% hingga
silika gel padat dan homogen. Dimasukkan 15 g ekstrak pekat metanol kulit bawang
merah kedalam kolom kromatografi yang telah berisi bubur silika gel, lalu
ditambahkan fasa gerak n-heksana : etilasetat (90:10)v v
⁄ secara perlahan-lahan dan
diatur sehingga aliran fasa yang keluar dari kolom sama banyaknya dengan
gerak n-heksana : etilasetat dengan perbandingan (80:20) v
⁄. Hasil yang diperoleh ditampung dalam botol vial setiap 5 mL lalu di
KLT dan digabung fraksi dengan harga Rf yang sama.
3.3.5 Kristalisasi
Amorf yang diperoleh dari isolasi dengan Kromatografi Kolom dilarutkan kembali
dengan etilasetat. Kemudian ditambahkan metanol secara perlahan – lahan hingga
pembentukan kembali senyawa yang lebih murni dari sebelumnya dan jatuh di dasar
wadah. Didekantasi larutan bagian atas wadah. Lalu diuapkan sisa pelarut dari amorf
hingga diperoleh kristal yang benar – benar bebas dari pelarut (Jacobs, 1974).
3.3.6 Uji Kemurnian Hasil Isolasi
3.3.6.1. Uji Kemurnian Hasil Isolasi dengan Kromatografi Lapis Tipis
Uji kemurnian kristal dilakukan dengan kromatografi lapis tipis dengan menggunakan
fasa diam silika gel 60 F254
Dimasukkan fasa gerak n-heksana : etilasetat (50:50) v v
⁄ dalam bejana kromatografi
lalu dijenuhkan. Ditotolkan kristal yang sebelumnya dilarutkan dengan kloroform
pada plat KLT. Dimasukkan plat KLT tersebut kedalam bejana kromatografi yang
telah jenuh. Setelah pelarut fasa gerak merembes sampai batas atas plat KLT lalu plat
KLT dikeluarkan dari bejana kromatografi, dikeringkan dan difiksasi dengan
menggunakan pereaksi FeCl
dengan fasa gerak n-heksana : etilasetat (50:50) v v
⁄,
kloroform : metanol (80:20) v v
⁄ dan benzene : eter (80:20) v v
⁄.
3 5%. Diamati warna noda yang dihasilkan dan dihitung harga Rf yang diperoleh. Perlakuan yang sama dilakukan pada fasa gerak kloroform :
metanol (80:20) v v
⁄ dan benzene : eter (80:20) v v
3.3.6.2 Uji Kemurnian Hasil Isolasi dengan Penentuan Titik Lebur
Kristal hasil isolasi yang telah murni dimasukkan kedalam melting point apparatus
lalu diamati pada suhu berapa kristal melebur.
3.3.8 Identifikasi Senyawa Hasil Isolasi
3.3.8.1 Identifikasi dengan Spektrofotometer UV-Visible
Analisis dengan alat spektrofotometer UV-Visible diperoleh dari Laboratorium Pusat
Penelitian Kimia – LIPI, kawasan PUSPITEK Serpong Tangerang dengan
menggunakan metanol sebagai pelarut.
3.3.8.2 Identifikasi dengan Spektrofotometer Inframerah (FT-IR)
Analisis dengan alat spektrofotometer FT-IR diperoleh dari Laboratorium Pusat
Penelitian Kimia – LIPI, kawasan PUSPITEK Serpong Tangerang dengan
menggunakan KBr sebagai pelarut.
3.3.8.3 Identifikasi dengan Spektrometer Resonansi Magnetik Inti Proton (1
H-NMR)
Analisa dengan alat spektrometer 1H-NMR diperoleh dari Pusat Penelitian Kimia –
LIPI, kawasan PUSPITEK Serpong Tangerang dengan menggunakan Aseton sebagai
3.4 Bagan Skrining Fitokimia
10 g serbuk kulit bawang merah (Allium cepaL.)
diekstraksi maserasi dengan metanol disaring
dipekatkan
dibagi kedalam 4 tabung reaksi
3.5 Bagan Penelitian
2000 g serbuk kulit Bawang Merah
(Allium cepa L.)
Ekstrak metanol Residu
diskrining fitokimia (+)
dipekatkan dengan rotarievaporator Ekstrak pekat metanol
diuapkan hingga semua metanol menguap dilarutkan dengan etil asetat
disaring
Filtrat Residu
dipekatkan dengan rotarievaporator diuapkan hingga semua etil asetat menguap dilarutkan dengan metanol
diekstraksi partisi dengan n-heksana sampai bening
Lapisan metanol Lapisan n - heksana diskrining fitokimia (+)
dipekatkan dengan rotarievaporator
Ekstrak pekat metanol
di-KLT untuk mengetahui sistem eluen yang sesuai pada kromatografi kolom dipisahkan tiap fraksi melalui kromatografi kolom dengan fase gerak yaitu campuran pelarut n-heksana:etil asetat dengan
perbandingan 90:10 v/v; 80:20 v/v; 70:30 v/v; 60:40 v/v dan 50:50 v/v
ditampung tiap fraksi sebanyak 5 mL dalam botol vial di-KLT untuk mengetahui harga Rf
digabung fraksi dengan harga Rf yang sama
Fraksi 605 - 862 dan spektrometer 1H-NMR Hasil analisis
diskrining fitokimima
BAB 4
HASIL DAN PEMBAHASAN
4.1.Hasil Penelitian
Hasil skrining fitokimia terhadap ekstrak metanol dari kulit bawang merah (Allium
cepa L.) menunjukkan bahwa sampel positif terhadap pereaksi-pereaksi flavonoida.
Hasil isolasi senyawa flavonoida dari kulit bawang merah yaitu berupa kristal jarum,
berwarna putih kekuningan dengan massa= 10 mg, titik lebur 288- 290 OC dan harga
Rf= 0,25 diperoleh dengan fase gerak n-heksana : etilasetat (50:50) v v
⁄, positif terhadap
pereaksi flavonoida.
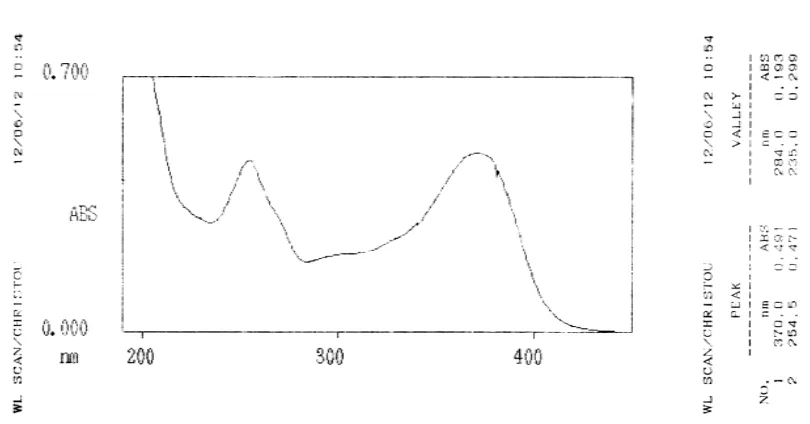
Spektrum UV-Visibel senyawa hasil isolasi ditunjukkan pada gambar 4.1 dibawah
ini:
Keterangan, x : Panjang gelombang (nm)
y : Absorbansi (abs)
600
Hasil analisis Spektrofotometer Ultraviolet-Visible (UV-Vis) dengan pelarut metanol memberikan panjang gelombang maksimum (λmaks) sebagai berikut:
1. Pada pita I memberikan panjang gelombang 370 nm
2. Pada pita II memberikan panjang gelombang 254,5 nm
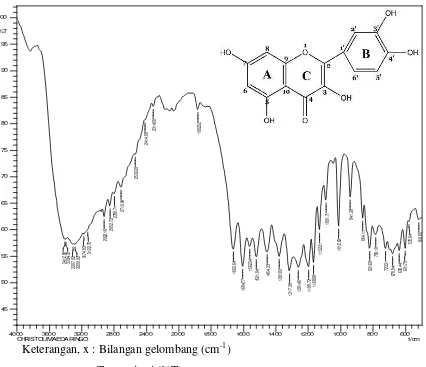
Spektrum FT-IR senyawa hasil isolaasi dapat dilihat pada gambar 4.2 dibawah ini:
Keterangan, x : Bilangan gelombang (cm-1
y : Transmitasi (%T)
)
Gambar 4.2 Spektrum FT-IR Senyawa Hasil Isolasi
Hasil analisis spektofotometer FT-IR pada senyawa hasil isolasi menghasilkan pita
serapan pada daerah gelombang sebagai berikut:
1. Pada bilangan gelombang 3412,08-3280,92 cm-1
2. Pada bilangan gelombang 2922,16-2713,84 cm
puncak melebar menunjukkan
adanya vibrasi ulur -OH.
-1
puncak sedang menunjukkan
3. Pada bilangan gelombang 1662,64 cm-1
4. Pada bilangan gelombang 1604,77-1454,33 cm
puncak tajam menunjukkan adanya vibrasi
ulur ikatan rangkap C=O dari keton.
-1
5. Pada bilangan gelombang 1261,45 cm
puncak tajam menunjukkan
adanya vibrasi ulur C=C dari sistem aromatik.
-1
6. Pada bilangan gelombang 1168,86 cm
puncak tajam menunjukkan adanya vibrasi
ulur C-O dari gugus alkohol.
-1
7. Pada bilangan gelombang 1012,63 cm
puncak tajam menunjukkan adanya vibrasi
ulur C-CO-C dari gugus keton.
-1
8. Pada bilangan gelombang 941,26 cm
menunjukkan adanya vibrasi ulur C-O-C
simetris.
-1
menunjukkan adanya vibrasi tekuk =C-H
aromatik (Silverstein,1986).
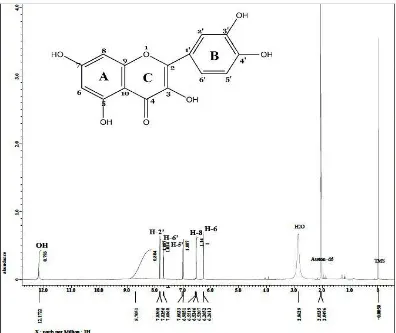
Spektrum Resonansi Magnetik inti proton (1
Gambar 4.3 Spektrum
H-NMR) senyawa hasil isolasi dapat
dilihat pada gambar 4.3 dibawah ini
1
Hasil analisa Spektrometer Resonansi Magnetik Inti Proton (1H-NMR) senyawa
hasil Isolasi dengan menggunakan pelarut Aseton-d6
1. Pergeseran kimia pada daerah δ= 6,2613-6,2652 ppm puncak doublet menunjukkan proton-proton H-6 pada cincin A struktur flavonoida.
memberikan pergeseran kimia
(ppm) sebagai berikut:
2. Pergeseran kimia pada daerah δ= 6,5207-6,5246 ppm puncak doublet menunjukkan proton-proton H-8 pada cincin A struktur flavonoida.
3. Pergeseran kimia pada daerah δ= 6,9851 - 7,0033 ppm puncak doublet menunjukkan proton-proton H-5’ pada cincin B struktur flavonoida.
4. Pergeseran kimia pada daerah δ= 7,6868-7,7089 puncak doublet-doublet menunjukkan proton-proton pada H-6’ pada cincin B struktur flavonoida.
5. Pergeseran kimia pada daerah δ= 7,8256-7,8308 puncak doublet menunjukkan proton-proton pada H-2’ pada cincin B struktur flavonoida.
6. Pergeseran kimia pada daerah δ = 12,1722 ppm puncak singlet menunjukkan proton dari OH pada C-5 dari cincin C struktur flavonoida.
4.2.Pembahasan
Dari hasil kromatografi lapis tipis, diketahui bahwa perbandingan pelarut yang baik
untuk mengisolasi senyawa flavonoida dari kulit bawang merah adalah
n-heksana:etilasetat (50:50) v v
⁄ yang menunjukkan pemisahan yang lebih baik dari noda
yang dihasilkan (Lampiran C).Selanjutnya dilakukan ekstraski maserasi terhadap kulit
bawang merah (Allium cepa L.) sehingga dihasilkan ekstrak pekat metanol kemudian
dipisahkan dengan kromatografi kolom. Fraksi dari kromatografi kolom kemudian di
uji KLT untuk mengetahui kemurnian dan harga Rf yang sama. Fraksi dari
kromatografi kolom kemudian digabungkan dan kemurniannya diuji KLT dengan
eluen n-heksana : etilasetat (50:50) v v⁄, benzena : eter (80:20) v v⁄ dan kloroform:metanol
(80:20) v v
⁄ yang menunjukkan hanya satu noda pada senyawa yang dihasilkan
(Lampiran F).
Dari hasil interpretasi spektrum UV-Vis memberikan serapan pada pita I dengan
panjang gelombang 370 nm dan pita II dengan panjang gelombang 254,5 nm yang
senyawa pembanding flavonoida yaitu Flavonol (dengan panjang gelombang pita I
berkisar 350-385 nm dan pita II 250-280 nm).
Hasil interpretasi Spektrum Inframerah (FT-IR) dan Spektrum Resonansi
Magnetik Inti Proton (1H-NMR) senyawa hasil isolasi dengan menggunakan pelarut
Aseton-d6
1. Pergeseran kimia pada daerah δ = 12,1722 ppm puncak singlet menunjukkan proton dari gugus OH dari C-5 pada cincin C struktur flavonoida. Hal ini
didukung oleh spektrum inframerah pada bilangan gelombang 3412,08 -
3280,92 cm
dalam standar TMS diperoleh:
-1
puncak melebar menunjukkan adanya vibrasi ulur -OH dan
spektrum pada bilangan gelombang 1261,45 cm-1
2. Pergeseran kimia pada daerah δ = 7,8256-7,8308 ppm puncak doublet menunjukkan proton-proton dari H-2’ pada cincin B struktur flavonoida
(Lampiran H). Hal ini didukung oleh spektrum inframerah pada bilangan
gelombang 2922,16-2713,84 cm
dengan puncak tajam
menunjukkan adanya vibrasi ulur C-O dari gugus alkohol.
-1
menunjukkan adanya vibrasi C-H aromatis
dan pada bilangan gelombang 1604,77-1454,33 cm-1 dengan puncak tajam
menunjukkan adanya vibrasi ulur C=C aromatis. Hal ini juga didukung dengan
bilangan gelombang 941,26 cm-1
3. Pergeseran kimia pada daerah δ = 7,6868-7,7089 ppm puncak doublet-doublet
menunjukkan proton-proton dari H-6’ pada cincin B struktur flavonoida
(Lampiran H). Hal ini didukung oleh spektrum inframerah pada bilangan
gelombang 2922,16-2713,84 cm
dengan puncak tajam menunjukkan adanya
vibrasi tekuk C-H aromatis.
-1
menunjukkan adanya vibrasi C-H aromatis
dan pada bilangan gelombang 1604,77-1454,33 cm-1 dengan puncak tajam
menunjukkan adanya vibrasi ulur C=C aromatis. Hal ini juga didukung dengan
bilangan gelombang 941,26 cm-1
4. Pergeseran kimia pada daerah δ = 6,9851 - 7,0033 ppm puncak doublet menunjukkan proton-proton dari H-5’ pada cincin B struktur flavonoida
(Lampiran H). Hal ini didukung oleh spektrum inframerah pada bilangan
gelombang 2922,16-2713,84 cm
dengan puncak tajam menunjukkan adanya
vibrasi tekuk C-H aromatis.
-1
menunjukkan adanya vibrasi C-H aromatis
menunjukkan adanya vibrasi ulur C=C aromatis. Hal ini juga didukung dengan
bilangan gelombang 941,26 cm-1
5. Pergeseran kimia pada daerah δ = 6,5207-6,5246 ppm puncak doublet menunjukkan proton dari H-8 pada cincin A struktur flavonoida (Lampiran H).
Hal ini didukung oleh spektrum inframerah pada bilangan gelombang
2922,16-2713,84 cm
dengan puncak tajam menunjukkan adanya
vibrasi tekuk C-H aromatis.
-1
menunjukkan adanya vibrasi C-H aromatis dan pada bilangan
gelombang 1604,77-1454,33 cm-1 dengan puncak tajam menunjukkan adanya
vibrasi ulur C=C aromatis. Hal ini juga didukung dengan bilangan gelombang
941,26 cm-1
6. Pergeseran kimia pada daerah δ = 6,2613-6,2652 ppm puncak doublet menunjukkan proton dari H-6 pada cincin A struktur flavonoida (Lampiran H).
Hal ini didukung oleh spektrum inframerah pada bilangan gelombang
2922,16-2713,84 cm
dengan puncak tajam menunjukkan adanya vibrasi tekuk C-H
aromatis.
-1
menunjukkan adanya vibrasi C-H aromatis dan pada bilangan
gelombang 1604,77-1454,33 cm-1 dengan puncak tajam menunjukkan adanya
vibrasi ulur C=C aromatis. Hal ini juga didukung dengan bilangan gelombang
941,26 cm-1 dengan puncak tajam menunjukkan adanya vibrasi tekuk C-H
aromatis.
Dari hasil pembahasan diatas, berdasarkan skrining fitokimia, data spektrum
UV-Vis, data spektrum inframerah dan 1
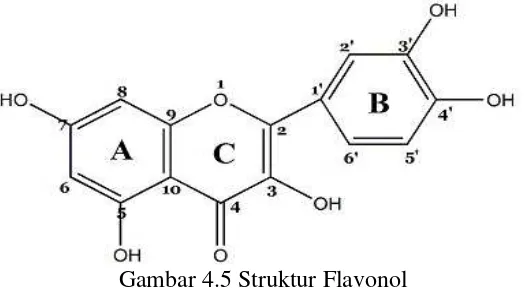
Gambar 4.5 Struktur Flavonol
H-NMR dapat diduga bahwa senyawa
yang diisolasi dari kulit bawang merah (Allium cepa L.) merupakan senyawa
BAB 5
KESIMPULAN DAN SARAN
5.1.Kesimpulan
1. Hasil uji skrining fitokimia dengan pereaksi flavonoida menunjukkan bahwa kulit
bawang merah mengandung senyawa flavonoida.
2. Hasil isolasi senyawa flavonoida dari kulit bawang merah yaitu berupa kristal
jarum, berwarna putih kekuningan dengan sebanyak 10 mg, titik lebur 288 -290 O
3. Hasil uji kemurnian Kromatografi Lapis Tipis terhadap kristal isolasi yang
diperoleh harga Rf=0,14 dengan fase gerak benzene:eter (80:20) v v
⁄ dan harga
Rf=0,88 dengan fase gerak cloroform:methanol (80:20), positif terhadap pereaksi
flavonoida
C
dan harga Rf= 0,25 dengan fase gerak n-heksana:etilasetat (50:50) v v
⁄, positif
terhadap pereaksi flavonoida.
4. Hasil analisis dengan spektrofotometer inframerah (FT-IR), spektrofotometer
Ultraviolet-Visible (UV-Vis) dan spektrometer Resonansi Magnetik Inti Proton
(1H-NMR) menunjukkan bahwa senyawa hasil isolasi dari kulit bawang merah
diduga adalah senyawa flavonoida golongan flavonol.
5.2.Saran
Untuk lebih mendukung struktur senyawa flavonoida dari kristal yang diperoleh
sebaiknya perlu dilakukan analisis Spektrometer 13C-NMR dan Spektrometer Massa
DAFTAR PUSTAKA
Bintang, M. 2011. Biokimia Teknik Penelitian. Bogor: Erlangga
Bresnick, S. 2003. Intisari Kimia Organik. Jakarta: Erlangga
Brown,D.W. 1988. Organic Spectroscopy. New Delhi: Thomson Press.
Cresswell, C.J, dkk. 1982. Analisis Spektrum Senyawa Organik. Edisi kedua. Bandung: Penerbit ITB
Dachriyanus. 2004. Analisis Struktur Senyawa Organik secara Spektroskopi. Padang: Andalas University Press
Fessenden, R.J. 1982. Kimia Organik. Jilid I. Cetakan Kedua. Terjemahan Aloysius Pudjaatmaka. Jakarta: Erlangga
Ganjar, J. 2007. Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Pelajar
Gritter, R. J. 1991. Pengantar Kromatografi. Terbitan ke-2. Terjemahan Kosasih Padmawinata. Bandung: Penerbit ITB
Hapsoh dan Hasanah, Y. 2011. Budidaya Tanaman Obat dan Rempah. Terbitan Pertama. USU Press. Medan
Harborne, J. B. 1987. Metoda Fitokimia Penuntun Cara Modern Menganalisa
Tumbuhan. Terbitan ke-2. Terjemahan Kosasih Padmawinata dan Iwang
Soediro. Bandung: Penerbit ITB
Heyne, K. 1981. Tumbuhan Berguna Indonesia. Jakarta:Badan Litbang Kehutanan
Kramer, Catherine.M. 2003. Phytochemistry : “Cloning and Regiospecificity Studies of
Two Flavonoid glucosyltransferases from Allium cepa L”. Brock University.
Canada
Lombard, Kevin.A. 2002. HortScience :”Flavonoid Quantification in Onion by
Spectrophotometric and High Performance Liquid Chromatography Analysis”.
Toronto. USA
Manitto, P. 1992. Biosintesis Produk Alami. Cetakan Pertama. Terjemahan Koensoemardiyah. Semarang: Penerbit IKIP Press
Markham, K. R. 1988. Cara Mengidentifikasi Flavonoida. Terjemahan Kosasih Padmawinata. Bandung: ITB Press
Muhammad,A. 2011. Sarang Semut dan Buah Merah Pembasmi Ragam Penyakit
Ganas. Cetakan Pertama. Jogjakarta: Laksana
Muldja, M.H. 1995. Analisis Instrumental. Cetakan Pertama. Surabaya: Universitas Airlangga Press
Nessa, F. 2003. Free Radical-Scavenging Activity of Organic Extracts and Pure
Flavonoids of Blumea balsamifera DC Leaves. Food Chemistry.88 (2004) hal
243-252
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. Terjemahan Padmawinata. Bandung: Penerbit ITB
Rodig,O.R. 1997. Organic Chemistry Laboratory: Standart and Microscale
Experiment. California: Saunders College Publishing
Sastrohamidjojo, H. 1996. Sintesis Bahan Alam. Yogyakarta: Penerbit Gadjah Mada University Press
Silverstein, R. M. 1986. Penyidikan Spektrometrik Senyawa Organik. Terjemahan A. J. Hatomo dan Anny Viktor Purba. Edisi ke-4. Jakarta: Penerbit Erlangga
Lampiran C. Komatogram Lapis Tipis Ekstrak Pekat Metanol kulit Bawang Merah
(Allium cepaL.) sebelum Kromatografi Kolom
Keterangan:
Fasa diam : Kieselgel 60 F
No
254
E : Ekstrak pekat metanol kulit Bawang Merah (Allium cepa L.)
Fasa gerak Jumlah noda Rf
I n-heksana:etilasetat (90:10) v v⁄ 1 0,025
II n-heksana:etilasetat (80:20) v v⁄ 3 0,065
0,045 0,025 III n-heksana:etilasetat (70:30) v v⁄ 3 0,125 0,065 0,025
IV n-heksana:etilasetat (60:40) v v⁄ 3 0,15
0,06 0,04
V n-heksana:etilasetat (50:50) v v⁄ 3 0,325
Lampiran D. Kromatogram Lapis Tipis Senyawa Murni Hasil Isolasi
Keterangan:
Fasa diam : Kieselgel 60 F
E : Ektrak Pekat Metanol kulit Bawang Merah (Allium cepa L.) 254
I : Fasa gerak benzene:eter (80:20) v v
⁄
II : Fasa gerak n-heksana:etilasetat (50:50) v v
⁄
III : Fasa gerak Kloroform:metanol (80:20) v v
⁄
No Fase Gerak Jumlah noda Rf
1 Benzene:eter (80:20) v v
⁄ 1 0,14
2 n-heksana:etilasetat (50:50) v v
⁄ 1 0,25
3 Kloroform:metanol (80:20) v v
Lampiran E. Spektrum Ultraviolet-Visible Beberapa Senyawa Flavonoida
Lampiran F. Ekspansi Spektrum 1
a. Ekspansi Spektrum
H-NMR Senyawa Hasil Isolasi 1
H-NMR Senyawa Hasil Isolasi (6,3 - 6,6 ppm)
Lampiran H. Spektrum 1H-NMR Senyawa Flavonoida Pembanding untuk